Лекция 6 Растворы электролитов.ppt
- Количество слайдов: 27

Теория электролитической диссоциации

Образование ионов 1. Растворение или плавление соединений с ионной связью: Na. Cl→Na++Cl 2. Химическая реакция соединений с ковалентной связью с растворителем: HCl + H 2 O → H 3 O+ + Cl-

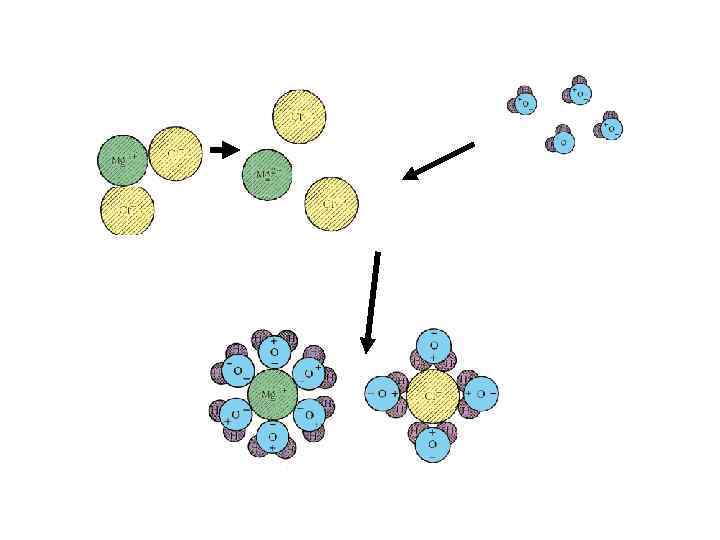
При электролитической диссоциации одновременно протекают: 1. ориентация молекул воды, 2. ионизация, 3. диссоциация электролита, 4. гидратация ионов

Сильные электролиты • Кислоты: HCl, HBr, HI, HNO 3, HCl. O 4, HCl. O 3, H 2 SO 4, H 2 Se. O 4, HBr. O 3, HBr. O 4, HIO 3, HIO 4, HSCN, HMn. O 4, H 2 Cr 2 O 7. • Основания: Li. OH, Na. OH, KOH, Rb. OH, Cs. OH, Ca(OH)2, Ba(OH)2, Sr(OH)2. • Растворимые соли

Степень электролитической диссоциации Nдисс. – число продиссоциированных молекул; N 0 – общее число молекул.

Изотонический коэффициент • N 0 – число молекул до диссоциации, N 0 – число диссоциированных молекул , (1 - N 0)- число недиссоциированных. ⇒К ионов→ NK ионов общее число частиц в растворе : (1 - )N + NK = [1 + (K – 1)]N.

Для растворов слабых электролитов
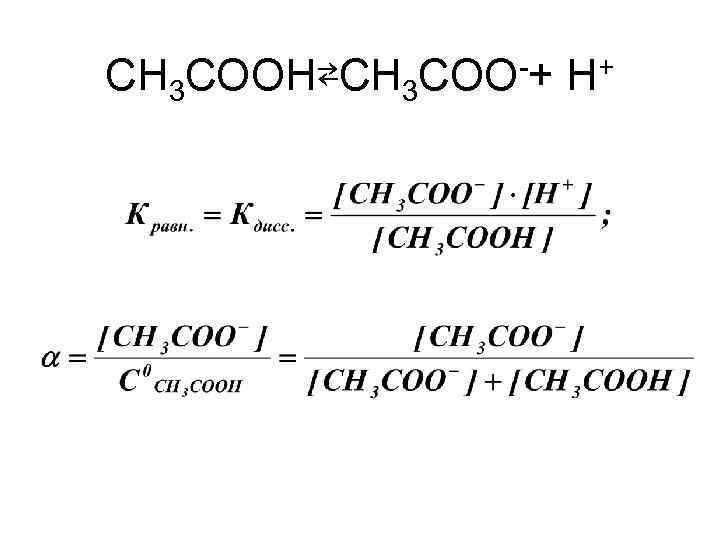
СH 3 COOH⇄CH 3 COO-+ H+
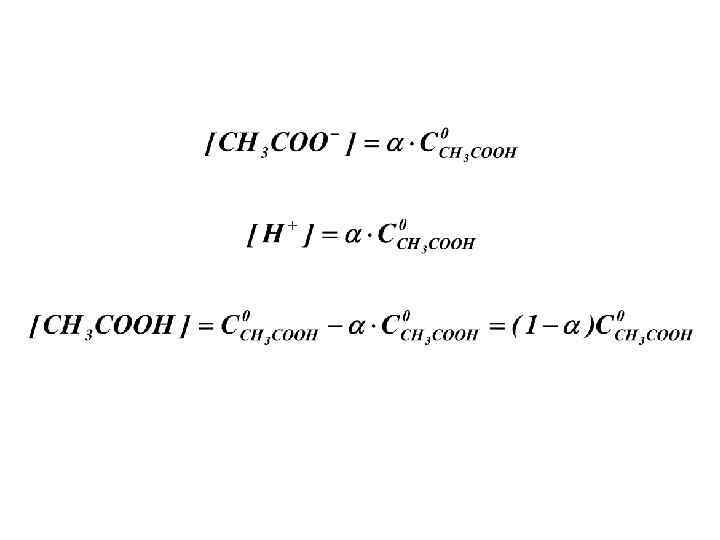
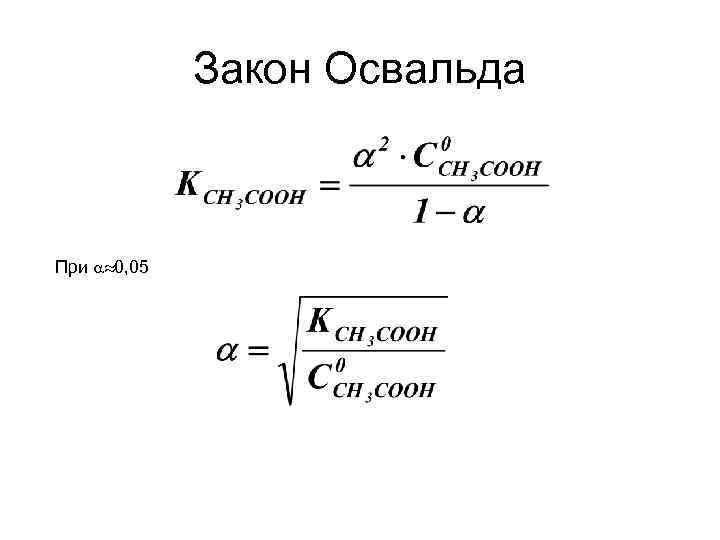
Закон Освальда При 0, 05

Теория сильных электролитов Na. Cl → Na++Cl- Ионная сила раствора — мера интенсивности электрического поля, создаваемого ионами в растворе.
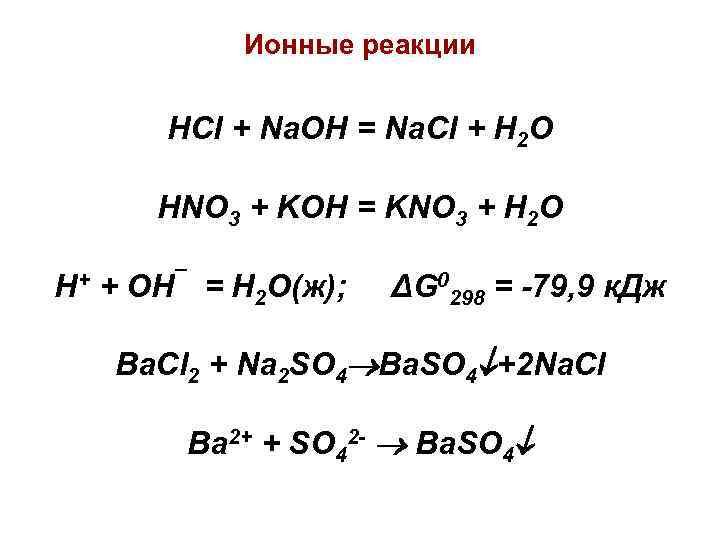
Ионные реакции HCl + Na. OH = Na. Cl + H 2 O HNO 3 + KOH = KNO 3 + H 2 O H+ + OH¯ = H 2 O(ж); ΔG 0298 = -79, 9 к. Дж Ba. Cl 2 + Na 2 SO 4 Ba. SO 4 +2 Na. Cl Ba 2+ + SO 42 - Ba. SO 4

Равновесие осадка Аn. Bm малорастворимого сильного электролита с раствором: Произведение растворимости ПР: Условие выпадения осадка: осадок выпадает. ⇄ n. A+ + m. B¯
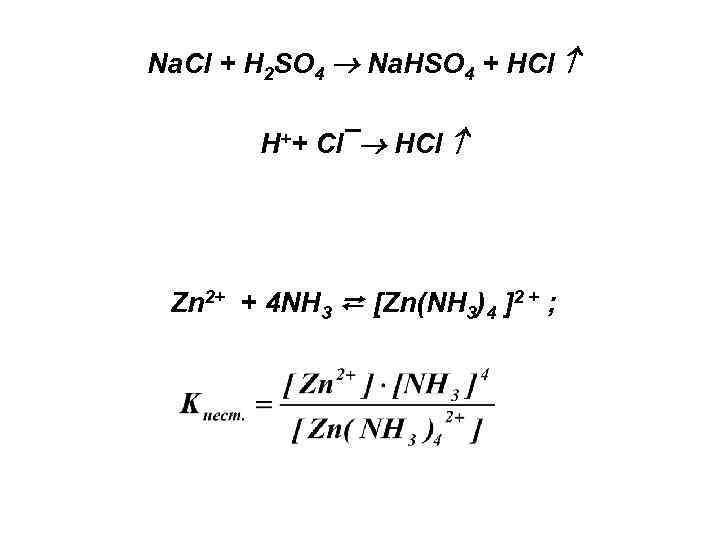
Na. Cl + H 2 SO 4 Na. HSO 4 + HCl H++ Cl¯ HCl Zn 2+ + 4 NH 3 ⇄ [Zn(NH 3)4 ]2 + ;
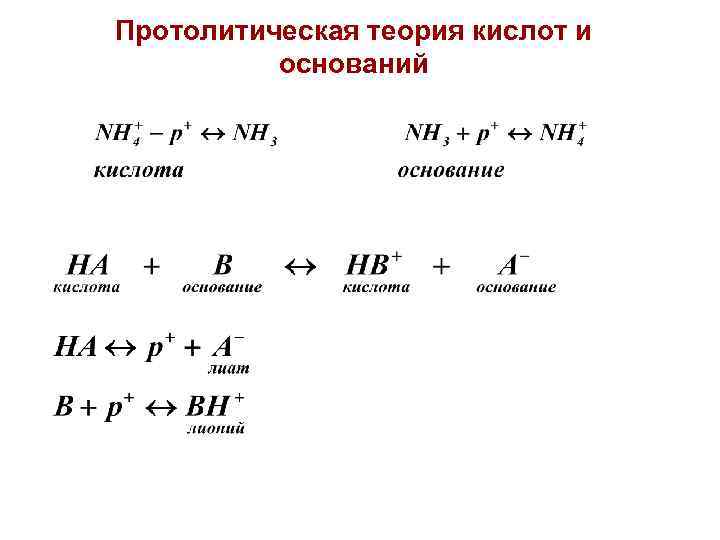
Протолитическая теория кислот и оснований
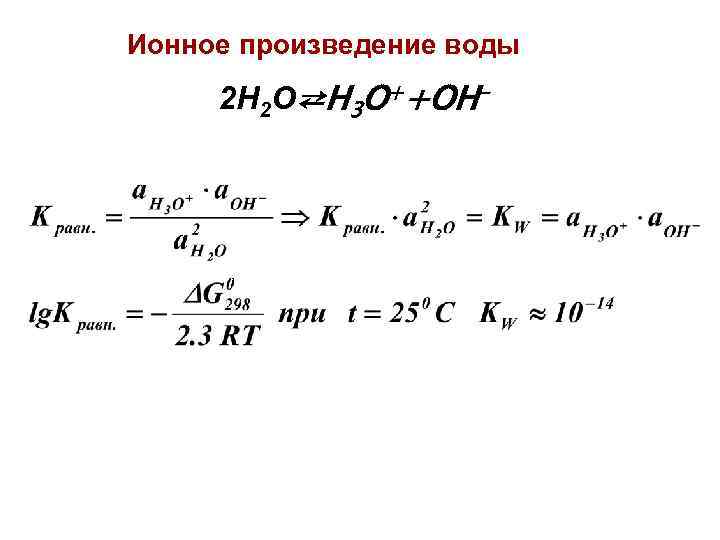
Ионное произведение воды 2 H 2 O⇄H 3 O++OH-

1. Раствор сильной кислоты или сильного основания При Ск или Cосн>10 -6 М автопротолиз воды подавлен

2. Раствор слабой кислоты или слабого основания Если α < 5%, Скислоты или Соснования > 10 -4, то автопротолизом можно пренебречь

Гидролиз • а) гидролиз солей, образованных сильным основанием и слабой кислотой; • б) гидролиз солей, образованных слабым основанием и сильной кислотой; • в) гидролиз солей, образованных слабым основанием и слабой кислотой.
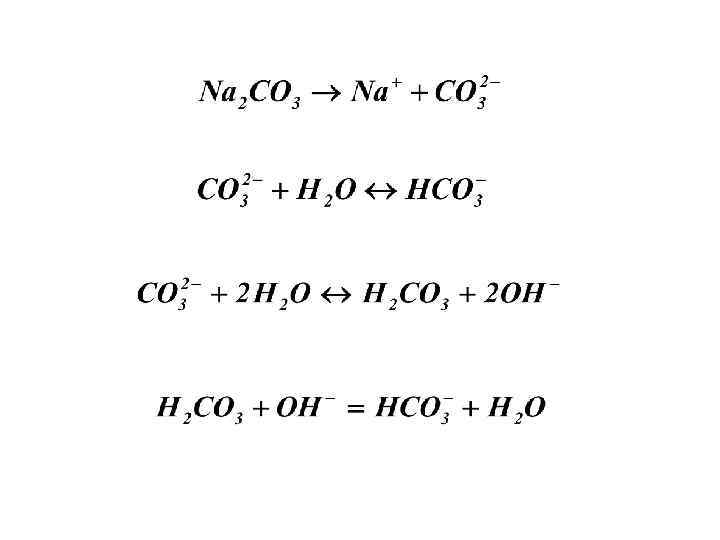

Константа гидролиза СН 3 СОО¯+ Н 2 О СН 3 СООН + ОН¯

Усиление гидролиза 1. Соль образована слабой кислотой и слабым основанием

2. Кислота и основание, образующие соль не только слабые электролиты, но и малорастворимы или неустойчивы.

Буферные растворы – это химическая система, сохраняющая постоянное р. Н при добавлении к ней кислот и оснований. оба равновесия сдвинуты влево.
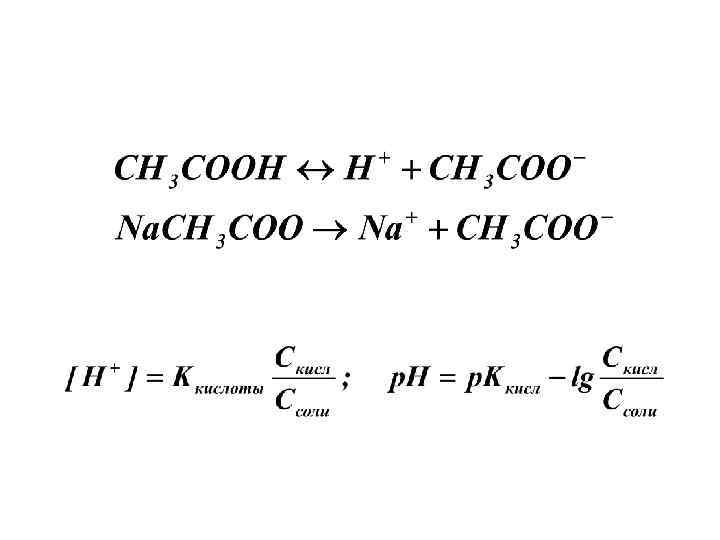

Свойства буферных растворов: - Сохранение р. Н при разбавлении - Сохранение р. Н при добавлении кислот или оснований.
Лекция 6 Растворы электролитов.ppt