Теория атома водорода по Бору Концепция атомизма Демокрит


Теория атома водорода по Бору

Концепция атомизма Демокрит Эпикур Лукреций Античные времена

Модель Томсона 1903 г. Вторая половина XIX века – эксперименты показали, что электрон является одной из основных составных вещества. электроны Положительное ядро 10-10 м

Опыты Резерфорда Прохождение α-частиц в веществе Большинство α-частиц рассеивалось на углы порядка 3° Отдельные α-частицы отклонялись на большие углы, до 180º (одна из 20 тысяч)
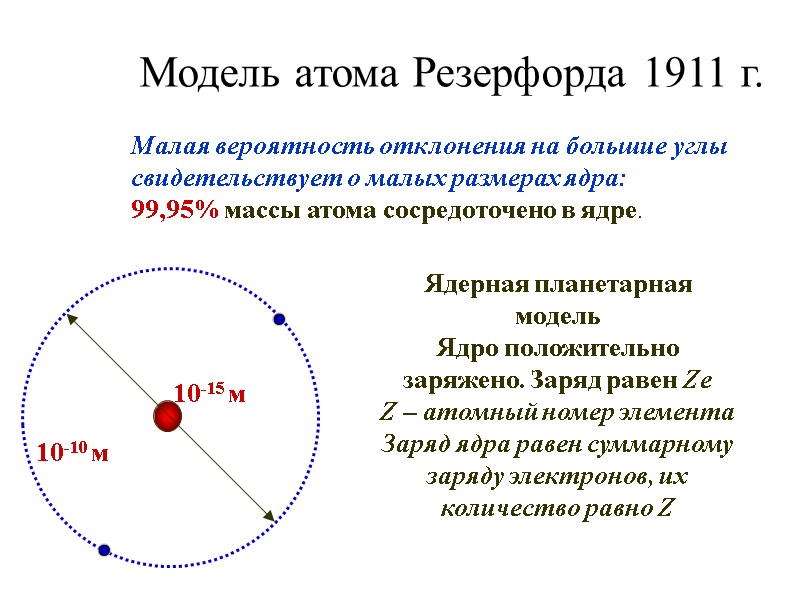
Модель атома Резерфорда 1911 г. Малая вероятность отклонения на большие углы свидетельствует о малых размерах ядра: 99,95% массы атома сосредоточено в ядре. Ядерная планетарная модель Ядро положительно заряжено. Заряд равен Ze Z – атомный номер элемента Заряд ядра равен суммарному заряду электронов, их количество равно Z

Движение электрона под действием кулоновской силы Противоречия: Энергия электрона может быть любой и спектры излучения должны быть сплошными. По теории Максвелла ускоренно движущиеся электроны должны излучать электромагнитные волны и терять энергию.

Атомный спектр испускания Еще в начале XIX столетия физики обнаружили, что при нагревании любое вещество излучает свет строго определенных длин волн. Систематическое изучение оптических спектров показало, что линии в оптическом спектре индивидуальны для каждого элемента.
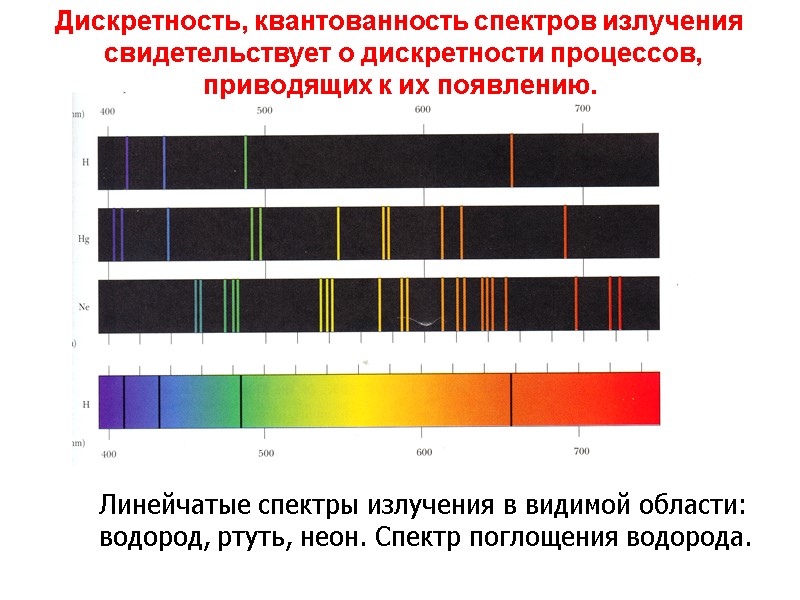
Линейчатые спектры излучения в видимой области: водород, ртуть, неон. Спектр поглощения водорода. Дискретность, квантованность спектров излучения свидетельствует о дискретности процессов, приводящих к их появлению.


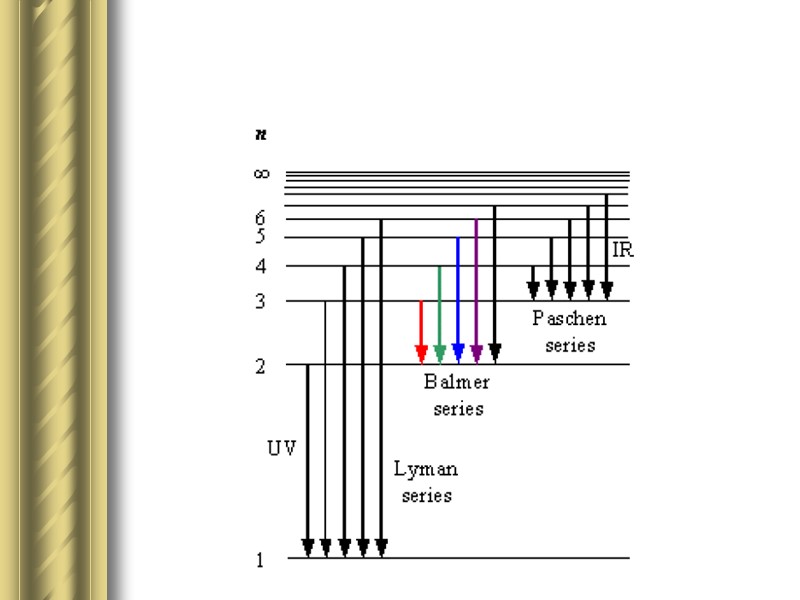
Дальнейшие исследования показали, что в спектре водорода имеется еще несколько серий:
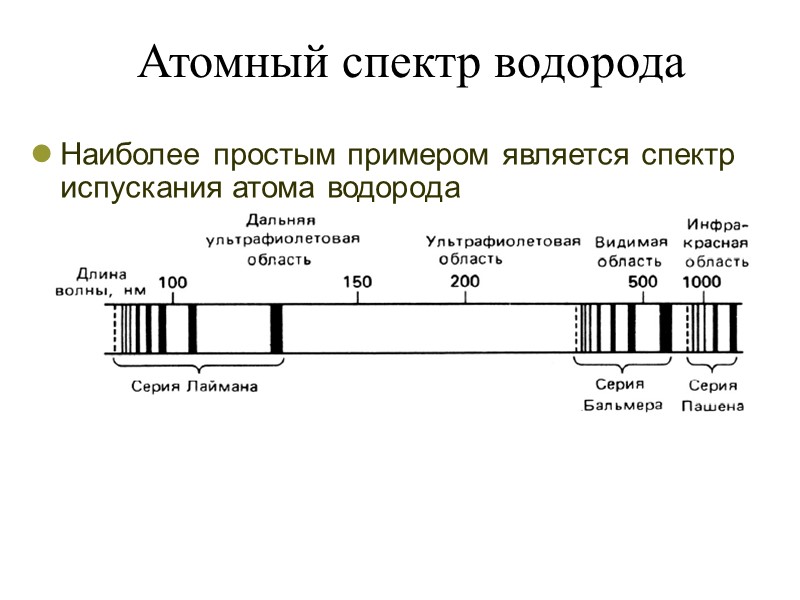
Атомный спектр водорода Наиболее простым примером является спектр испускания атома водорода


Теория Бора 1913 г. Создал первую квантовую модель атома, основанную на двух постулатах, которые прямо противоречили классическим представлениям и законам.

Постулаты Бора Первый постулат: В атоме существуют стационарные энергетические состояния. Пребывая в одном из стационарных состояний, атом не излучает энергию. Эти состояния характеризуются дискретными состояниями энергии. Стационарным состояниям соответствуют определенные (стационарные) орбиты электронов. При движении электронов по орбитам не происходит излучения энергии.

Условие для стационарных орбит: из всех орбит электрона возможны только те, для которых момент импульса электрона, равен целому кратному постоянной Планка: me vr = nħ n = 1, 2, 3,… главное квантовое число.

Второй постулат: Излучение или поглощение энергии в виде кванта энергии h происходит лишь при переходе электрона из одного стационарного состояния в другое. Световой квант равен разности энергий тех стационарных состояний, между которыми совершается переход электрона: - Правило частот Бора hv = Em – En m, n – номера состояний Набор возможных дискретных частот и Объясняет линейчатый спектр атома
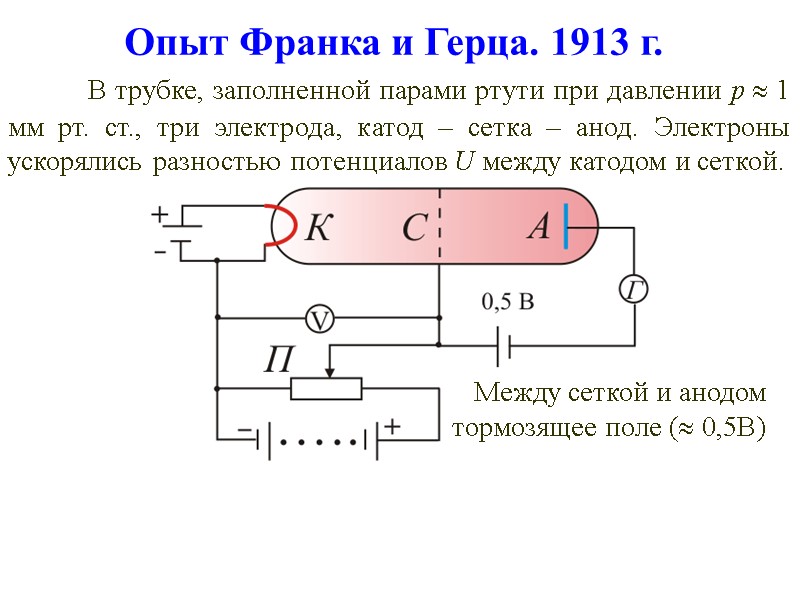
Опыт Франка и Герца. 1913 г. В трубке, заполненной парами ртути при давлении р 1 мм рт. ст., три электрода, катод – сетка – анод. Электроны ускорялись разностью потенциалов U между катодом и сеткой. Между сеткой и анодом тормозящее поле ( 0,5В)
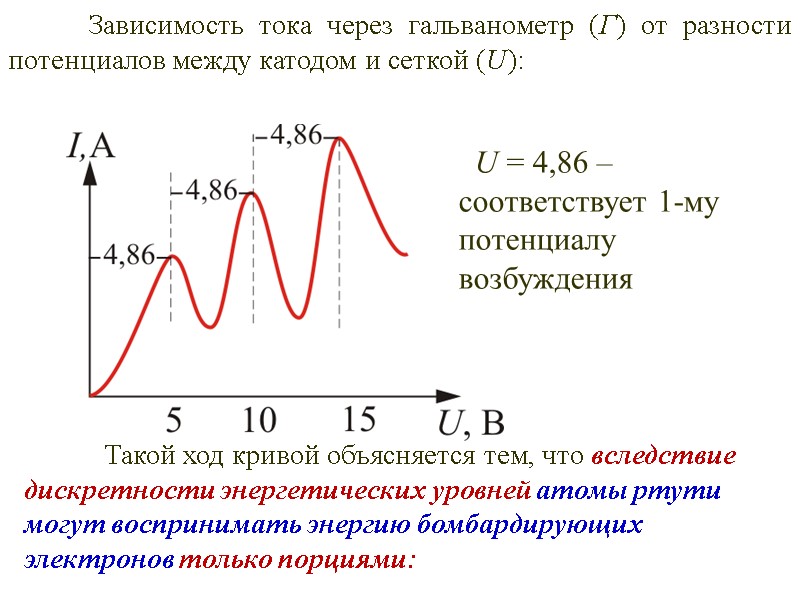
Зависимость тока через гальванометр (Г) от разности потенциалов между катодом и сеткой (U): U = 4,86 – соответствует 1-му потенциалу возбуждения Такой ход кривой объясняется тем, что вследствие дискретности энергетических уровней атомы ртути могут воспринимать энергию бомбардирующих электронов только порциями:

Спектр атома водорода по Бору me vr = nħ Уравнение движения электрона получим из равенства центробежной силе кулоновской силе: Отсюда найдем радиус стационарных орбит: Радиусы стационарных орбит растут пропорционально квадратам целых чисел.

Радиус первой орбиты водородного атома называют Боровским радиусом: При n =1, Z = 1 для водорода имеем: х = 0,529·10–10 м. Å=

Внутренняя энергия атома слагается из кинетической энергии электрона и потенциальной энергией электрона в электростатическом поле с ядра: Учитывая квантованные значения радиуса получим Отсюда видно, что: энергия электрона может принимать только дискретные значения, т.к. n = 1, 2, 3,…
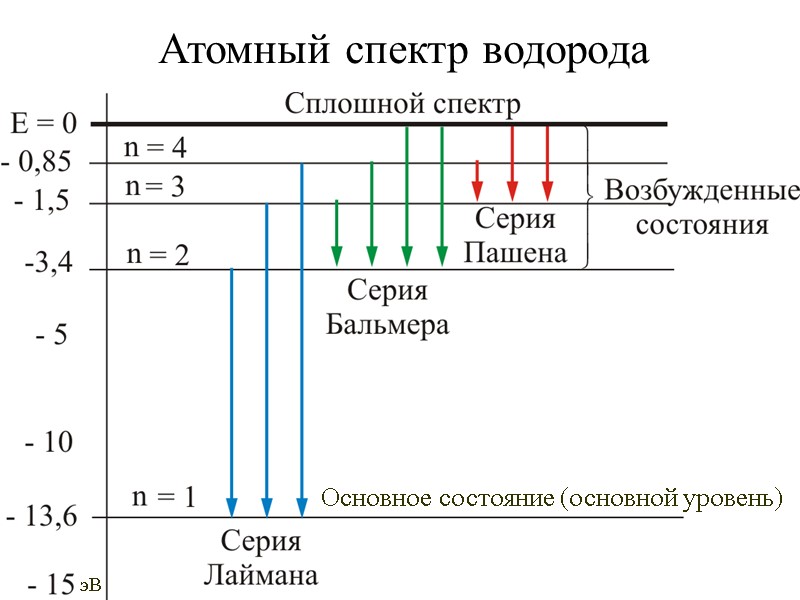
Атомный спектр водорода Основное состояние (основной уровень) эВ

При переходе электрона в атоме водорода из состояния n в состояние m излучается фотон с энергией : х и частота излучения, Это и есть обобщенная формула Бальмера, которая хорошо согласуется с экспериментом, где постоянная Ридберга
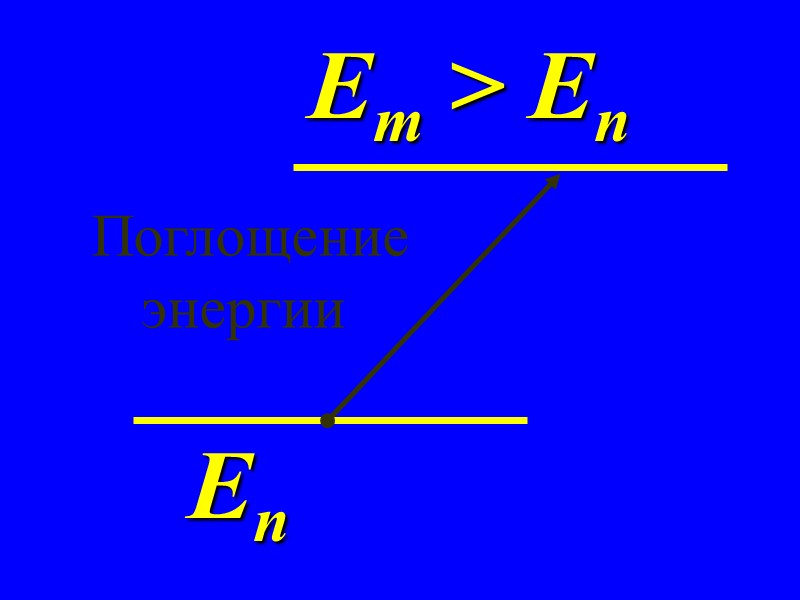
Еn Em > En Поглощение энергии
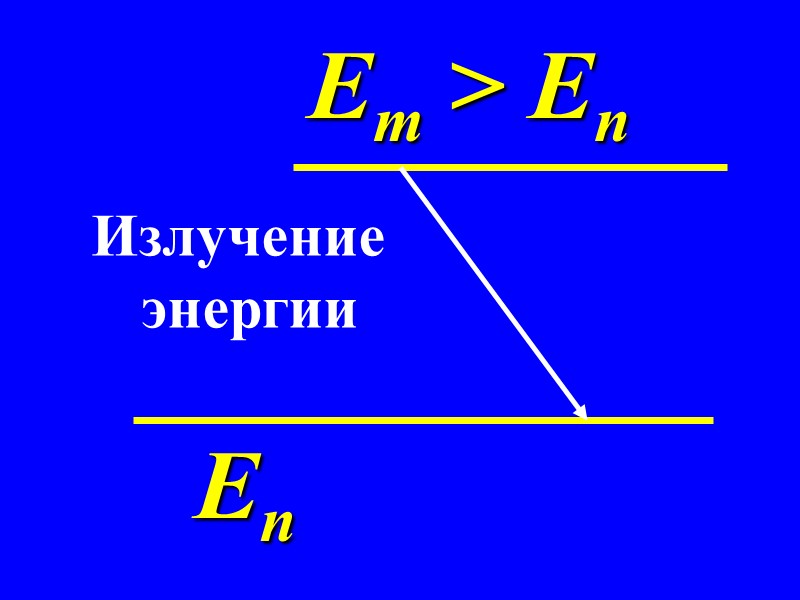
Еn Em > En Излучение энергии

Однако наряду с успехами в теории Бора с самого начала обнаружились существенные недостатки. Главнейшее – внутренняя противоречивость теории: механическое соединение классической физики с квантовыми постулатами. Теория не могла объяснить вопрос об интенсивностях спектральных линий. Серьезной неудачей являлась абсолютная невозможность применить теорию для объяснения спектров гелия (He) (два электрона на орбите, и уже теория Бора не справляется).



Экспериментальные исследования показали, что атом может не только излучать, но и поглощать видимый свет. Спектры постоянных звезд и туманностей в сравнении со спектрами Солнца и некоторых химических элементов: 1 - Солнце; 2 – желто-красная звезда; 3 – голубая звезда; 4 – Сириус; 5 - α - Геркулеса; 6 - Τ – Венца; 7 – туманность Дракона; 8 – водород; 9 – азот; 10 – светильный газ.


Спектры постоянных звезд и туманностей в сравнении со спектрами Солнца и некоторых химических элементов: 1 - Солнце; 2 – желто-красная звезда; 3 – голубая звезда; 4 – Сириус; 5 - α - Геркулеса; 6 - Τ – Венца; 7 – туманность Дракона; 8 – водород; 9 – азот; 10 – светильный газ.

37806-teoria_atoma_vodoroda_po_boru.ppt
- Количество слайдов: 34

