Teoria_aktivirovannogo_komplexa_perekhodnogo_s.ppt
- Количество слайдов: 29
 Теория активированного комплекса (переходного состояния) Лекция 8
Теория активированного комплекса (переходного состояния) Лекция 8
 История создания. • Развитие квантовой механики привело к созданию теории активированного комплекса (переходного состояния), предложенной в 1935 году одновременно Эйрингом, Эвансом и Поляни. • Но первые основные идеи теории были • сформулированы Р. Марселином в 1915 г. , Marcelin, Ann. Phys. , 3, 158 (1915), • погибшем в 1915 г. и не успевшем развить свои взгляды
История создания. • Развитие квантовой механики привело к созданию теории активированного комплекса (переходного состояния), предложенной в 1935 году одновременно Эйрингом, Эвансом и Поляни. • Но первые основные идеи теории были • сформулированы Р. Марселином в 1915 г. , Marcelin, Ann. Phys. , 3, 158 (1915), • погибшем в 1915 г. и не успевшем развить свои взгляды
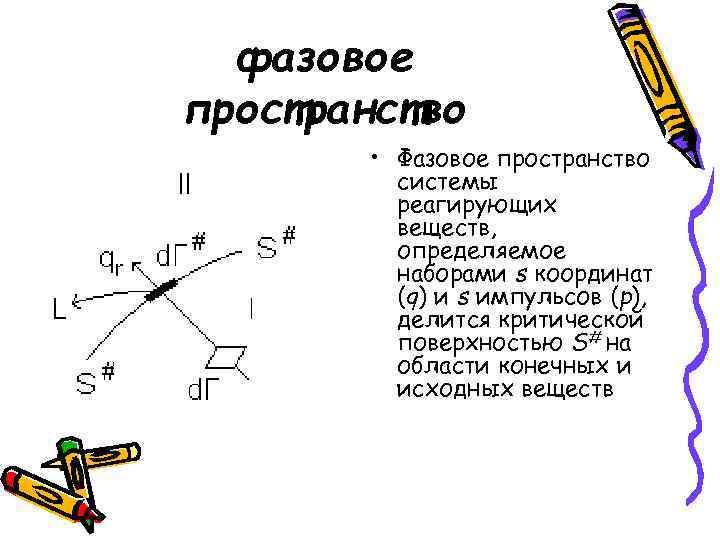 фазовое пространство • Фазовое пространство системы реагирующих веществ, определяемое наборами s координат (q) и s импульсов (р), делится критической поверхностью S# на области конечных и исходных веществ
фазовое пространство • Фазовое пространство системы реагирующих веществ, определяемое наборами s координат (q) и s импульсов (р), делится критической поверхностью S# на области конечных и исходных веществ
 Критическая поверхность (поверхность потенциальной энергии) • Вблизи критической поверхности предполагается выполнение • условий: • Существует некоторый потенциал (U), зависящий от координат ядер (qi) и отвечающий адиабатическому терму системы (основное электронное состояние). • Этот потенциал определяет движение вблизи критической поверхности S#. • Функция распределения состояний системы вблизи критической поверхности не зависит от времени, задана значением температуры и при пересечении. S# (термодинамическое равновесие не предполагается) равновесна.
Критическая поверхность (поверхность потенциальной энергии) • Вблизи критической поверхности предполагается выполнение • условий: • Существует некоторый потенциал (U), зависящий от координат ядер (qi) и отвечающий адиабатическому терму системы (основное электронное состояние). • Этот потенциал определяет движение вблизи критической поверхности S#. • Функция распределения состояний системы вблизи критической поверхности не зависит от времени, задана значением температуры и при пересечении. S# (термодинамическое равновесие не предполагается) равновесна.
 Адиабатическое приближение • метод приближённого решения задач квантовой механики, применяемый для описания квантовых систем, в которых можно выделить быструю и медленную подсистемы
Адиабатическое приближение • метод приближённого решения задач квантовой механики, применяемый для описания квантовых систем, в которых можно выделить быструю и медленную подсистемы
 Основные принципы адиабатического приближения • движение каждого из ядер происходит в потенциальном (электрическом) поле, создаваемом остальными ядрами, и в усредненном поле всех электронов молекул реагирующей системы в целом. • Усредненное поле электронов отвечает некоторому усредненному распределению их электрического заряда в пространстве. • потенциал (потенциальное поле) определяет для каждой ядерной конфигурации те силы, которые действуют на ядра. • потенциал зависит от того, как расположены ядра молекулы в каждый момент времени, и от того, каково состояние (основное или возбужденное) системы электронов в молекуле. • потенциальное поле для данной системы ядер зависит от расстояний между отдельными ядрами молекулярной системы и может быть представлено графически как некоторая функция межъядерных расстояний
Основные принципы адиабатического приближения • движение каждого из ядер происходит в потенциальном (электрическом) поле, создаваемом остальными ядрами, и в усредненном поле всех электронов молекул реагирующей системы в целом. • Усредненное поле электронов отвечает некоторому усредненному распределению их электрического заряда в пространстве. • потенциал (потенциальное поле) определяет для каждой ядерной конфигурации те силы, которые действуют на ядра. • потенциал зависит от того, как расположены ядра молекулы в каждый момент времени, и от того, каково состояние (основное или возбужденное) системы электронов в молекуле. • потенциальное поле для данной системы ядер зависит от расстояний между отдельными ядрами молекулярной системы и может быть представлено графически как некоторая функция межъядерных расстояний
 Координата реакции • величина, характеризующая изменение многоатомной системы в процессе ее химического превращения из реагентов в продукты реакции • Определение К. р. тесно связано с топографией поверхности потенциальной энергии (ППЭ) U (qi), которая является функциейц N внутренних координат системы qi (i=1, 2, . . . , N), определяющих взаимное расположение атомных ядер, т. е. ядерно-электронную конфигурацию системы
Координата реакции • величина, характеризующая изменение многоатомной системы в процессе ее химического превращения из реагентов в продукты реакции • Определение К. р. тесно связано с топографией поверхности потенциальной энергии (ППЭ) U (qi), которая является функциейц N внутренних координат системы qi (i=1, 2, . . . , N), определяющих взаимное расположение атомных ядер, т. е. ядерно-электронную конфигурацию системы
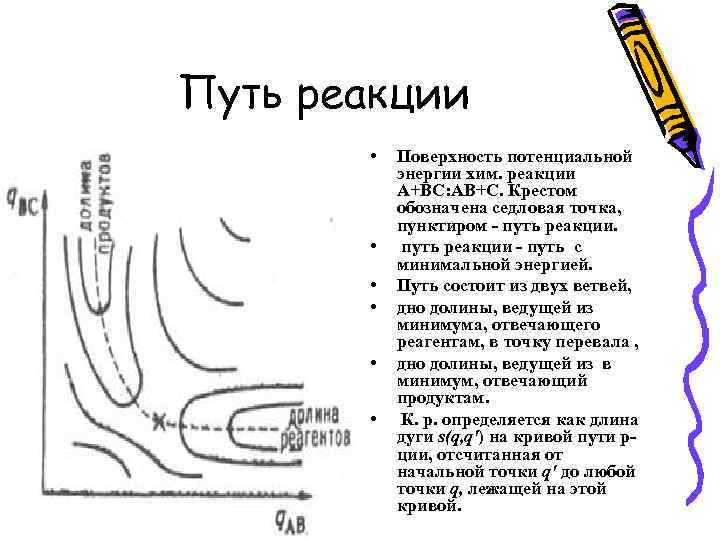 Путь реакции • • • Поверхность потенциальной энергии хим. реакции А+ВС: АВ+С. Крестом обозначена седловая точка, пунктиром - путь реакции - путь с минимальной энергией. Путь состоит из двух ветвей, дно долины, ведущей из минимума, отвечающего реагентам, в точку перевала , дно долины, ведущей из в минимум, отвечающий продуктам. К. р. определяется как длина дуги s(q, q') на кривой пути рции, отсчитанная от начальной точки q' до любой точки q, лежащей на этой кривой.
Путь реакции • • • Поверхность потенциальной энергии хим. реакции А+ВС: АВ+С. Крестом обозначена седловая точка, пунктиром - путь реакции - путь с минимальной энергией. Путь состоит из двух ветвей, дно долины, ведущей из минимума, отвечающего реагентам, в точку перевала , дно долины, ведущей из в минимум, отвечающий продуктам. К. р. определяется как длина дуги s(q, q') на кривой пути рции, отсчитанная от начальной точки q' до любой точки q, лежащей на этой кривой.
 Поверхность потенциальной энергии • Каждая точка на потенциальной поверхности есть не что иное, как энергия молекулярной системы в данном электронном состоянии при отсутствии движения ядер, то есть полная энергия за вычетом кинетической энергии ядер
Поверхность потенциальной энергии • Каждая точка на потенциальной поверхности есть не что иное, как энергия молекулярной системы в данном электронном состоянии при отсутствии движения ядер, то есть полная энергия за вычетом кинетической энергии ядер
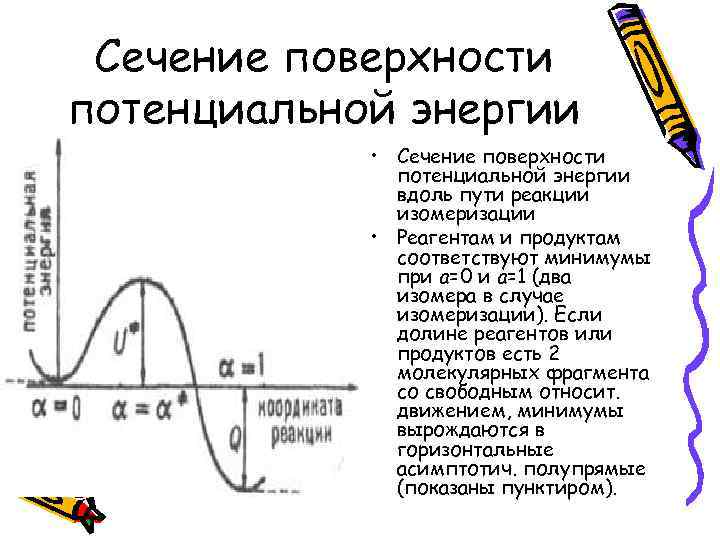 Сечение поверхности потенциальной энергии • Сечение поверхности потенциальной энергии вдоль пути реакции изомеризации • Реагентам и продуктам соответствуют минимумы при а=0 и а=1 (два изомера в случае изомеризации). Если долине реагентов или продуктов есть 2 молекулярных фрагмента со свободным относит. движением, минимумы вырождаются в горизонтальные асимптотич. полупрямые (показаны пунктиром).
Сечение поверхности потенциальной энергии • Сечение поверхности потенциальной энергии вдоль пути реакции изомеризации • Реагентам и продуктам соответствуют минимумы при а=0 и а=1 (два изомера в случае изомеризации). Если долине реагентов или продуктов есть 2 молекулярных фрагмента со свободным относит. движением, минимумы вырождаются в горизонтальные асимптотич. полупрямые (показаны пунктиром).
 Основные положения теории активированного комплекса • Всякая химическая реакция или любой другой молекулярный процесс, протекающий во времени (диффузия, вязкое течение), состоит в непрерывном изменении расстояний между ядрами атомов. • конфигурация ядер, отвечающая начальному состоянию, через некоторую промежуточную конфигурацию - активированный комплекс или переходное состояние - превращается в конечную конфигурацию. • исходные вещества находятся в равновесии с активированными комплексами, ( скорость образования последних намного больше скорости их распада), • распределение молекул реагирующих веществ по энергиям вследствие столкновений соответствует равновесному распределению Максвелла -
Основные положения теории активированного комплекса • Всякая химическая реакция или любой другой молекулярный процесс, протекающий во времени (диффузия, вязкое течение), состоит в непрерывном изменении расстояний между ядрами атомов. • конфигурация ядер, отвечающая начальному состоянию, через некоторую промежуточную конфигурацию - активированный комплекс или переходное состояние - превращается в конечную конфигурацию. • исходные вещества находятся в равновесии с активированными комплексами, ( скорость образования последних намного больше скорости их распада), • распределение молекул реагирующих веществ по энергиям вследствие столкновений соответствует равновесному распределению Максвелла -
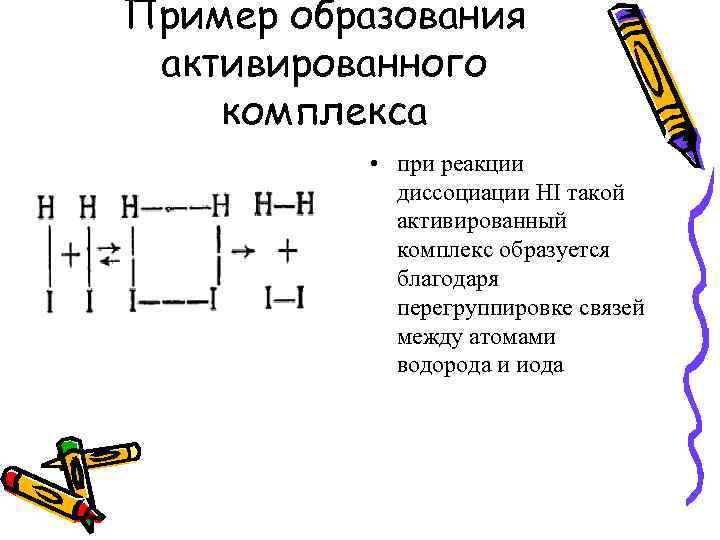 Пример образования активированного комплекса • при реакции диссоциации HI такой активированный комплекс образуется благодаря перегруппировке связей между атомами водорода и иода
Пример образования активированного комплекса • при реакции диссоциации HI такой активированный комплекс образуется благодаря перегруппировке связей между атомами водорода и иода
 Переходное состояние • Переходное состояние (активированный комплекс) можно рассматривать как обыкновенную молекулу, характеризующуюся определенными термодинамическими свойствами, за исключением того, что, кроме обычных трех степеней свободы поступательного движения центра тяжести, оно имеет четвертую степень свободы внутреннего поступательного движения, связанную с движением вдоль пути (координаты) реакции
Переходное состояние • Переходное состояние (активированный комплекс) можно рассматривать как обыкновенную молекулу, характеризующуюся определенными термодинамическими свойствами, за исключением того, что, кроме обычных трех степеней свободы поступательного движения центра тяжести, оно имеет четвертую степень свободы внутреннего поступательного движения, связанную с движением вдоль пути (координаты) реакции
 Особенности переходного состояния • переходное состояние не есть некоторое промежуточное соединение, так как ему соответствует максимальная энергия по пути реакции и, следовательно, оно неустойчиво и должно превращаться в продукты реакции • Молекулы, достигшие энергетического барьера, превращаются в продукты реакции
Особенности переходного состояния • переходное состояние не есть некоторое промежуточное соединение, так как ему соответствует максимальная энергия по пути реакции и, следовательно, оно неустойчиво и должно превращаться в продукты реакции • Молекулы, достигшие энергетического барьера, превращаются в продукты реакции
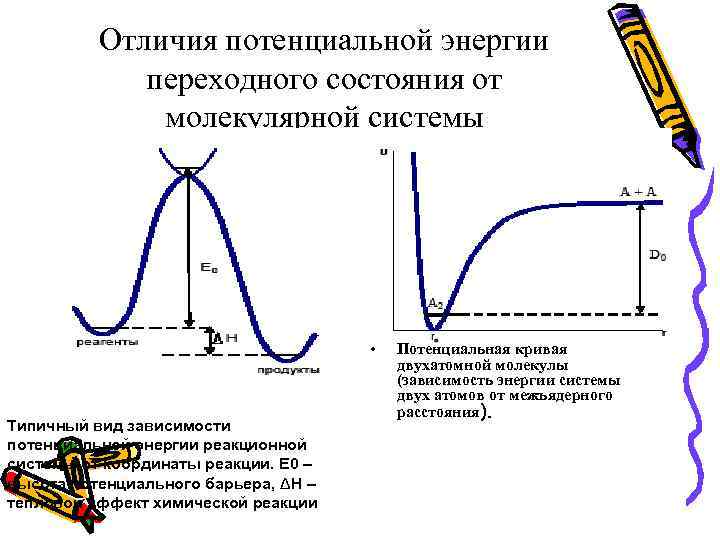 Отличия потенциальной энергии переходного состояния от молекулярной системы • Типичный вид зависимости потенциальной энергии реакционной системы от координаты реакции. Е 0 – высота потенциального барьера, ΔН – тепловой эффект химической реакции Потенциальная кривая двухатомной молекулы (зависимость энергии системы двух атомов от межъядерного расстояния).
Отличия потенциальной энергии переходного состояния от молекулярной системы • Типичный вид зависимости потенциальной энергии реакционной системы от координаты реакции. Е 0 – высота потенциального барьера, ΔН – тепловой эффект химической реакции Потенциальная кривая двухатомной молекулы (зависимость энергии системы двух атомов от межъядерного расстояния).
 Механизм образования активированного комплекса • Рассмотрим в общем виде реакцию А + В ←→ Х** → С + D, где А и В исходные вещества; X** - переходное состояние, или активированный комплекс; С и D - продукты реакции. • рассматриваемая реакция состоит из двух последовательных процессов. • Первый - это переход A и B в активированное состояние • Второй - распад образовавшегося комплекса на продукты С и D.
Механизм образования активированного комплекса • Рассмотрим в общем виде реакцию А + В ←→ Х** → С + D, где А и В исходные вещества; X** - переходное состояние, или активированный комплекс; С и D - продукты реакции. • рассматриваемая реакция состоит из двух последовательных процессов. • Первый - это переход A и B в активированное состояние • Второй - распад образовавшегося комплекса на продукты С и D.
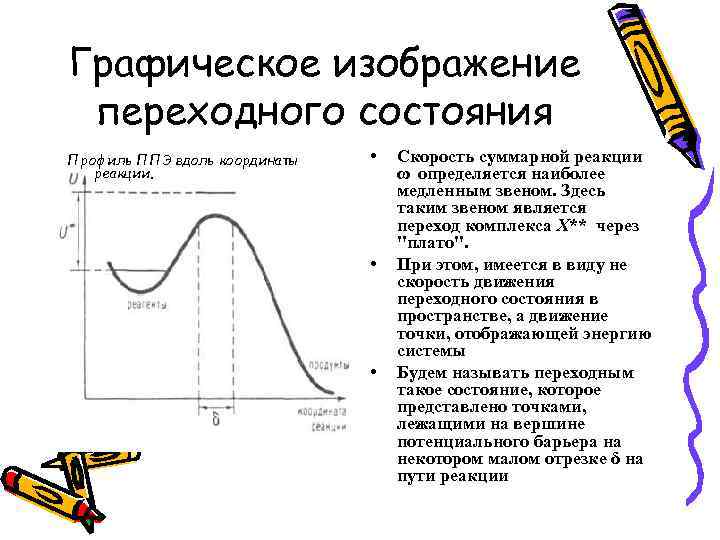 Графическое изображение переходного состояния Профиль ППЭ вдоль координаты реакции. • • • Скорость суммарной реакции ω определяется наиболее медленным звеном. Здесь таким звеном является переход комплекса Х** через "плато". При этом, имеется в виду не скорость движения переходного состояния в пространстве, а движение точки, отображающей энергию системы Будем называть переходным такое состояние, которое представлено точками, лежащими на вершине потенциального барьера на некотором малом отрезке δ на пути реакции
Графическое изображение переходного состояния Профиль ППЭ вдоль координаты реакции. • • • Скорость суммарной реакции ω определяется наиболее медленным звеном. Здесь таким звеном является переход комплекса Х** через "плато". При этом, имеется в виду не скорость движения переходного состояния в пространстве, а движение точки, отображающей энергию системы Будем называть переходным такое состояние, которое представлено точками, лежащими на вершине потенциального барьера на некотором малом отрезке δ на пути реакции
 Скорость реакции распада активированного комплекса • скорость реакции определяется числом распадов всех переходных состояний в единице объема в единицу времени: ω = c** /t. • Величина t может быть выражена через среднюю скорость движения переходного состояния и вдоль пути реакции на вершине барьера: • t = δ/u. (XVI. 28)
Скорость реакции распада активированного комплекса • скорость реакции определяется числом распадов всех переходных состояний в единице объема в единицу времени: ω = c** /t. • Величина t может быть выражена через среднюю скорость движения переходного состояния и вдоль пути реакции на вершине барьера: • t = δ/u. (XVI. 28)
 Время жизни АК • Неустойчивая конфигурация АК характеризуется временем жизни:
Время жизни АК • Неустойчивая конфигурация АК характеризуется временем жизни:
 Основное уравнение теории АК • теория постулирует термодинамическое равновесие между реагентами и АК, характеризуемое константой равновесия. На этом основании константа скорости химической реакции к выражается уравнениями:
Основное уравнение теории АК • теория постулирует термодинамическое равновесие между реагентами и АК, характеризуемое константой равновесия. На этом основании константа скорости химической реакции к выражается уравнениями:
 энтропия и энтальпия активации • энтропия и энтальпия активации, представляют собой изменения энтропии и энтальпии системы при переходе от реагентов к АК
энтропия и энтальпия активации • энтропия и энтальпия активации, представляют собой изменения энтропии и энтальпии системы при переходе от реагентов к АК
 Применение теории • Последовательный расчет абсолютных скорости реакции по уравнению (2) заключается в определении геометрических конфигураций реагентов и АК (на этом этапе также определяется высота потенциального барьера) и вычислении для этих конфигураций моментов инерции и колебательных частот, которые необходимы для расчета статистических сумм и окончательного определения энергии активации
Применение теории • Последовательный расчет абсолютных скорости реакции по уравнению (2) заключается в определении геометрических конфигураций реагентов и АК (на этом этапе также определяется высота потенциального барьера) и вычислении для этих конфигураций моментов инерции и колебательных частот, которые необходимы для расчета статистических сумм и окончательного определения энергии активации
 Ограниченность теории • Теория активированного комплекса теория основана на двух предположениях: • гипотеза о термодинамическом равновесии между реагентами и АК. • скорость реакции отождествляется со скоростью распада АК. • Оба предположения нельзя строго обосновать
Ограниченность теории • Теория активированного комплекса теория основана на двух предположениях: • гипотеза о термодинамическом равновесии между реагентами и АК. • скорость реакции отождествляется со скоростью распада АК. • Оба предположения нельзя строго обосновать
 Почему? • Координату реакции лишь в редких случаях правильно считать прямой линией, Обычно же она - кривая в многомерном пространстве внутренних переменных и является сложной комбинацией элементарных движений, которая неодинакова на различных своих участках.
Почему? • Координату реакции лишь в редких случаях правильно считать прямой линией, Обычно же она - кривая в многомерном пространстве внутренних переменных и является сложной комбинацией элементарных движений, которая неодинакова на различных своих участках.
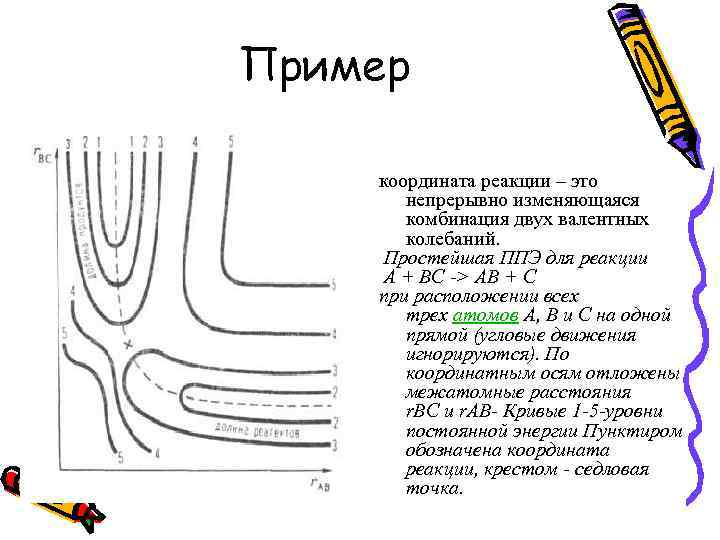 Пример координата реакции – это непрерывно изменяющаяся комбинация двух валентных колебаний. Простейшая ППЭ для реакции А + ВС -> АВ + С при расположении всех трех атомов А, В и С на одной прямой (угловые движения игнорируются). По координатным осям отложены межатомные расстояния r. BC и r. АВ- Кривые 1 -5 -уровни постоянной энергии Пунктиром обозначена координата реакции, крестом - седловая точка.
Пример координата реакции – это непрерывно изменяющаяся комбинация двух валентных колебаний. Простейшая ППЭ для реакции А + ВС -> АВ + С при расположении всех трех атомов А, В и С на одной прямой (угловые движения игнорируются). По координатным осям отложены межатомные расстояния r. BC и r. АВ- Кривые 1 -5 -уровни постоянной энергии Пунктиром обозначена координата реакции, крестом - седловая точка.
 электронно-неадиабатические процессы и трансмиссионный множитель • Из-за криволинейности координату реакции нельзя считать независимой степенью свободы. • Ее взаимод. с другими, поперечными движениями приводит к обмену энергией между ними. • В результате, может нарушиться первоначально равновесное распределение энергии по поперечным степеням свободы и система может вернуться в область реагентов даже после того, как она уже прошла через конфигурацию АК в направлении продуктов • Эти процессы учитывает трансмиссионный коэффициент • для реакций, в которых х значительно отличается от единицы, теория теряет смысл
электронно-неадиабатические процессы и трансмиссионный множитель • Из-за криволинейности координату реакции нельзя считать независимой степенью свободы. • Ее взаимод. с другими, поперечными движениями приводит к обмену энергией между ними. • В результате, может нарушиться первоначально равновесное распределение энергии по поперечным степеням свободы и система может вернуться в область реагентов даже после того, как она уже прошла через конфигурацию АК в направлении продуктов • Эти процессы учитывает трансмиссионный коэффициент • для реакций, в которых х значительно отличается от единицы, теория теряет смысл
 Туннельный эффект • оценка трансмиссионного множителя в рамках модельных динамических вычислений. • При этом предполагается, что с поступательным движением системы вдоль координаты реакции взаимодействуют не все, а лишь некоторые из поперечных степеней свободы. Они и учитываются в квантовом динамическом расчете; остальные степени свободы обрабатываются в рамках равновесной теории. При таких вычислениях автоматически определяются также и поправки на квантовое туннелирование. • Туннелирование – прохождение между поверхностями потенциальной энергии
Туннельный эффект • оценка трансмиссионного множителя в рамках модельных динамических вычислений. • При этом предполагается, что с поступательным движением системы вдоль координаты реакции взаимодействуют не все, а лишь некоторые из поперечных степеней свободы. Они и учитываются в квантовом динамическом расчете; остальные степени свободы обрабатываются в рамках равновесной теории. При таких вычислениях автоматически определяются также и поправки на квантовое туннелирование. • Туннелирование – прохождение между поверхностями потенциальной энергии
 Расчитанный кластер воды
Расчитанный кластер воды
 Взаимодействие воды с кислородом
Взаимодействие воды с кислородом


