ТЕОРИИ ХИМИЧЕСКОЙ КИНЕТИКИ.ppt
- Количество слайдов: 21
 ТЕОРИИ ХИМИЧЕСКОЙ КИНЕТИКИ
ТЕОРИИ ХИМИЧЕСКОЙ КИНЕТИКИ
 Зависимость скорости реакции от температуры Влияние температуры на скорость реакции оценивается величиной температурного коэффициента скорости γ, который показывает, во сколько раз увеличивается скорость реакции при повышении температуры на десять градусов (правило Вант-Гоффа) (4. 1) где k т +10, k т – константы скорости (сравнение скоростей производят при одинаковых концентрациях реагентов). Для любого интервала температур Т 1 -Т 2 справедливо соотношение: (4. 2) Правило Вант - Гоффа (4. 2) является приближенным и с повышением температуры величина уменьшается. Уравнение Аррениуса lnk = – B/T + C, (4. 3) в котором В, С – эмпирические постоянные, не зависящие от температуры и характеризующие данную реакцию; Т – абсолютная температура.
Зависимость скорости реакции от температуры Влияние температуры на скорость реакции оценивается величиной температурного коэффициента скорости γ, который показывает, во сколько раз увеличивается скорость реакции при повышении температуры на десять градусов (правило Вант-Гоффа) (4. 1) где k т +10, k т – константы скорости (сравнение скоростей производят при одинаковых концентрациях реагентов). Для любого интервала температур Т 1 -Т 2 справедливо соотношение: (4. 2) Правило Вант - Гоффа (4. 2) является приближенным и с повышением температуры величина уменьшается. Уравнение Аррениуса lnk = – B/T + C, (4. 3) в котором В, С – эмпирические постоянные, не зависящие от температуры и характеризующие данную реакцию; Т – абсолютная температура.
 (4. 4) (4. 4/) где Еа – энергия активации; R – универсальная газовая постоянная. Строгим путем уравнение Аррениуса (4. 4), (4. 4 ) для элементарных реакций получается из теории переходного состояния, согласно которой энергия активации – есть разность средней энергии активированного комплекса и энергии исходных веществ. Энергия активации Рассмотрим обратимую химическую реакцию, протекающую при постоянном объеме. Эн ерг Е 1 ия Е 2 Изменение энергии в ходе реакции. I II U 1 U 2 координата реакции
(4. 4) (4. 4/) где Еа – энергия активации; R – универсальная газовая постоянная. Строгим путем уравнение Аррениуса (4. 4), (4. 4 ) для элементарных реакций получается из теории переходного состояния, согласно которой энергия активации – есть разность средней энергии активированного комплекса и энергии исходных веществ. Энергия активации Рассмотрим обратимую химическую реакцию, протекающую при постоянном объеме. Эн ерг Е 1 ия Е 2 Изменение энергии в ходе реакции. I II U 1 U 2 координата реакции
 Уровень I соответствует исходным веществам, уровень 2 – продуктам реакции. В ходе реакции энергия сначала увеличивается, а затем уменьшается, т. е. преодолевается энергетический барьер. Высота этого барьера для прямой реакции характеризуется энергией Е 1. Величина Е 1 называется энергией активации. Т. е. Е 1 - минимальная дополнительная энергия, по сравнению со средней энергией теплового движения (U 1), которую нужно сообщить молекулам исходных веществ, чтобы произошла прямая реакция. При протекании реакции в обратном направлении энергия активации равна Е 2. Существование энергии активации можно обосновать с помощью общих положений термодинамики. Двусторонняя реакция, протекающая при постоянном объеме, характеризуется константой равновесия Кс = k 1/k 2 , (k 1, k 2 – константы скорости прямой и обратной реакции). Разность внутренних энергий системы U = U 2 – U 1 =E 1 – E 2 (рис. 4. 1) Подставим эти соотношения в уравнение изохоры Вант - Гоффа Экспериментально установлено, что слагаемые левой и правой частей попарно равны другу, т. е. И тогда для любой реакции можно записать уравнение Аррениуса в дифференциальной форме. 4. 5)
Уровень I соответствует исходным веществам, уровень 2 – продуктам реакции. В ходе реакции энергия сначала увеличивается, а затем уменьшается, т. е. преодолевается энергетический барьер. Высота этого барьера для прямой реакции характеризуется энергией Е 1. Величина Е 1 называется энергией активации. Т. е. Е 1 - минимальная дополнительная энергия, по сравнению со средней энергией теплового движения (U 1), которую нужно сообщить молекулам исходных веществ, чтобы произошла прямая реакция. При протекании реакции в обратном направлении энергия активации равна Е 2. Существование энергии активации можно обосновать с помощью общих положений термодинамики. Двусторонняя реакция, протекающая при постоянном объеме, характеризуется константой равновесия Кс = k 1/k 2 , (k 1, k 2 – константы скорости прямой и обратной реакции). Разность внутренних энергий системы U = U 2 – U 1 =E 1 – E 2 (рис. 4. 1) Подставим эти соотношения в уравнение изохоры Вант - Гоффа Экспериментально установлено, что слагаемые левой и правой частей попарно равны другу, т. е. И тогда для любой реакции можно записать уравнение Аррениуса в дифференциальной форме. 4. 5)
 Аналогично для реакции, протекающей при постоянном давлении, для которой -уравнение изобары разность энергий активации прямой и обратной реакции связана с тепловым эффектом Н. Энергия активации - это минимальная избыточная над средней энергия, рассчитанная на 1 моль вещества, которой должны обладать сталкивающиеся частицы, чтобы вступить в химическое взаимодействие и преодолеть энергетический барьер. Величина барьера зависит от природы реагирующих частиц (молекул, атомов, ионов, радикалов). Уравнение (4. 5) можно проинтегрировать, если принять, что Е от температуры не зависит. Для большинства реакций это действительно так. При этом получаются выражения (4. 4) и (4. 4 ) (4. 4 /) где ln. A – константа интегрирования. (4. 4) Постоянную интегрирования - А называют предэкспоненциальным множителем или фактором Аррениуса. Для одностадийных реакций этот множитель имеет простой физический смысл: фактор Аррениуса (А) – есть вероятность взаимодействия молекул, обладающих необходимой энергией, и выражается формулой A = A 0 * e S /R (4. 6)
Аналогично для реакции, протекающей при постоянном давлении, для которой -уравнение изобары разность энергий активации прямой и обратной реакции связана с тепловым эффектом Н. Энергия активации - это минимальная избыточная над средней энергия, рассчитанная на 1 моль вещества, которой должны обладать сталкивающиеся частицы, чтобы вступить в химическое взаимодействие и преодолеть энергетический барьер. Величина барьера зависит от природы реагирующих частиц (молекул, атомов, ионов, радикалов). Уравнение (4. 5) можно проинтегрировать, если принять, что Е от температуры не зависит. Для большинства реакций это действительно так. При этом получаются выражения (4. 4) и (4. 4 ) (4. 4 /) где ln. A – константа интегрирования. (4. 4) Постоянную интегрирования - А называют предэкспоненциальным множителем или фактором Аррениуса. Для одностадийных реакций этот множитель имеет простой физический смысл: фактор Аррениуса (А) – есть вероятность взаимодействия молекул, обладающих необходимой энергией, и выражается формулой A = A 0 * e S /R (4. 6)
 Объединяя уравнения (4. 4) и (4. 6), получаем k = A 0 e S /R*e–E/RT Если Е 0 (4. 7) kmax = A. Уравнения Аррениуса (4. 4) и (4. 4 ) содержат две постоянные для данной реакции величины. Их можно определить, если известны константы скорости при двух температурах Вычтем из одного уравнения другое и найдем: (4. 8) Энергию активации можно определить графически, если экспериментально найдены константы скорости при нескольких температурах. Как видно из уравнения (4. 4 ), в координатах lnk 1/T оно изображается прямой линией (рис. 4. 2), тангенс угла наклона которой tg = –Ea/R, отсюда Ea= – lnk Rtg. Графическое определение энергии активации. 1/T
Объединяя уравнения (4. 4) и (4. 6), получаем k = A 0 e S /R*e–E/RT Если Е 0 (4. 7) kmax = A. Уравнения Аррениуса (4. 4) и (4. 4 ) содержат две постоянные для данной реакции величины. Их можно определить, если известны константы скорости при двух температурах Вычтем из одного уравнения другое и найдем: (4. 8) Энергию активации можно определить графически, если экспериментально найдены константы скорости при нескольких температурах. Как видно из уравнения (4. 4 ), в координатах lnk 1/T оно изображается прямой линией (рис. 4. 2), тангенс угла наклона которой tg = –Ea/R, отсюда Ea= – lnk Rtg. Графическое определение энергии активации. 1/T
 x = (ED – E)/ED, где ЕD – сумма энергий диссоциации разрывающихся связей; Е – энергия активации. Для некаталитических реакций со стабильными молекулами х не превышает 0, 7. Для этого нужно построить график зависимости (ln k = f(T)). Тангенс угла н аклона касательной к кривой дает производную Теория активных соударений (столкновений) В соответствии с этой теорией: 1) Молекулы реагирующих веществ представляются маленькими твердыми шариками (т. е. бесструктурными частицами), находящимися в беспрерывном хаотическом движении. 2) Средняя кинетическая энергия молекул определяется температурой системы. 3) Скорости движения молекул различны. Число молекул, обладающих той или иной скоростью движения, определяется законом распределения Максвелла - Больцмана. . 4) Реакция осуществляется в момент соударения молекул реагирующих частиц и происходит мгновенно. 5) Реагируют лишь те молекулы, которые в момент столкновения обладают необходимым избытком энергии, т. е. активные молекулы. 6) Активные молекулы возникают в реакционной смеси в результате теплового движения, поглощения кванта света, действия электрических разрядов и т. д. Предполагается, что скорость активации молекул намного больше скорости превращения активных молекул в продукты реакции. Т. е. химическая реакция не нарушает равновесного Максвелл – Больцмановского распределения молекул по скоростям
x = (ED – E)/ED, где ЕD – сумма энергий диссоциации разрывающихся связей; Е – энергия активации. Для некаталитических реакций со стабильными молекулами х не превышает 0, 7. Для этого нужно построить график зависимости (ln k = f(T)). Тангенс угла н аклона касательной к кривой дает производную Теория активных соударений (столкновений) В соответствии с этой теорией: 1) Молекулы реагирующих веществ представляются маленькими твердыми шариками (т. е. бесструктурными частицами), находящимися в беспрерывном хаотическом движении. 2) Средняя кинетическая энергия молекул определяется температурой системы. 3) Скорости движения молекул различны. Число молекул, обладающих той или иной скоростью движения, определяется законом распределения Максвелла - Больцмана. . 4) Реакция осуществляется в момент соударения молекул реагирующих частиц и происходит мгновенно. 5) Реагируют лишь те молекулы, которые в момент столкновения обладают необходимым избытком энергии, т. е. активные молекулы. 6) Активные молекулы возникают в реакционной смеси в результате теплового движения, поглощения кванта света, действия электрических разрядов и т. д. Предполагается, что скорость активации молекул намного больше скорости превращения активных молекул в продукты реакции. Т. е. химическая реакция не нарушает равновесного Максвелл – Больцмановского распределения молекул по скоростям
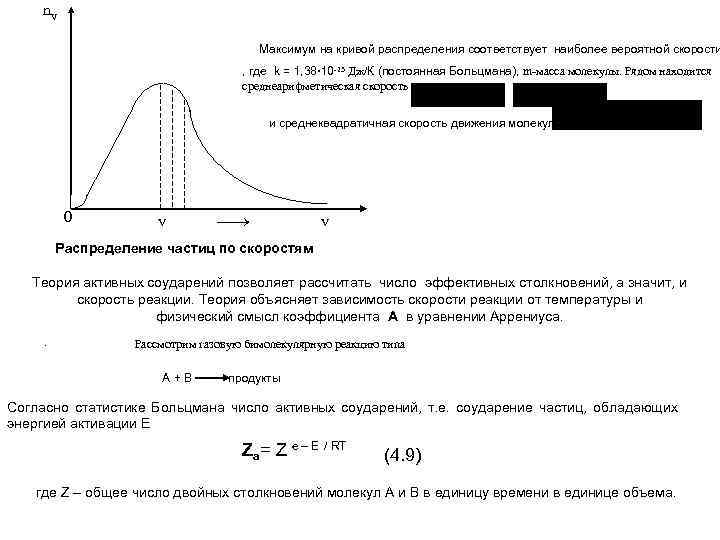 nv Максимум на кривой распределения соответствует наиболее вероятной скорости , где k = 1, 38 10 -23 Дж К (постоянная Больцмана), m-масса молекулы. Рядом находится среднеарифметическая скорость и среднеквадратичная скорость движения молекул 0 v v Распределение частиц по скоростям Теория активных соударений позволяет рассчитать число эффективных столкновений, а значит, и скорость реакции. Теория объясняет зависимость скорости реакции от температуры и физический смысл коэффициента А в уравнении Аррениуса. . Рассмотрим газовую бимолекулярную реакцию типа А+В продукты Согласно статистике Больцмана число активных соударений, т. е. соударение частиц, обладающих энергией активации Е Za= Z e – E RT (4. 9) где Z – общее число двойных столкновений молекул А и В в единицу времени в единице объема.
nv Максимум на кривой распределения соответствует наиболее вероятной скорости , где k = 1, 38 10 -23 Дж К (постоянная Больцмана), m-масса молекулы. Рядом находится среднеарифметическая скорость и среднеквадратичная скорость движения молекул 0 v v Распределение частиц по скоростям Теория активных соударений позволяет рассчитать число эффективных столкновений, а значит, и скорость реакции. Теория объясняет зависимость скорости реакции от температуры и физический смысл коэффициента А в уравнении Аррениуса. . Рассмотрим газовую бимолекулярную реакцию типа А+В продукты Согласно статистике Больцмана число активных соударений, т. е. соударение частиц, обладающих энергией активации Е Za= Z e – E RT (4. 9) где Z – общее число двойных столкновений молекул А и В в единицу времени в единице объема.
 Количество столкновений Z одной молекулы с остальными молекулами за 1 секунду равно количеству молекул в цилиндре с поперечным сечением d 2 и длиной, равной скорости молекулы, т. е. где d – диаметр молекулы, n – число молекул в единице объема , v - среднеарифметическая скорость движения м Полное число столкновений разных молекул в единице объема Z = n. А· n. В πd. АВ 2 * (4. 10) где m – приведенная масса молекул А и В т. е. за 1 сек. В выражении (4. 10) m= n. А, n. В – число молекул А и В в единице объема. Скорость бимолекулярной реакции, согласно закону действующих масс , , (4. 11) Количество активных столкновений равно числу реагирующих молекул, т. е. изменению числа молекул в единице объема за 1 с (4. 12) т. к. CА = n. A/Na, СВ = n. B/Na (Na = 6, 02· 1023 молекул – число Авогадро) Объединим уравнения (4. 9) и (4. 1 и выразим скорость реакции Ze–E/RT = – Na(d. CA/dt) (4. 13)
Количество столкновений Z одной молекулы с остальными молекулами за 1 секунду равно количеству молекул в цилиндре с поперечным сечением d 2 и длиной, равной скорости молекулы, т. е. где d – диаметр молекулы, n – число молекул в единице объема , v - среднеарифметическая скорость движения м Полное число столкновений разных молекул в единице объема Z = n. А· n. В πd. АВ 2 * (4. 10) где m – приведенная масса молекул А и В т. е. за 1 сек. В выражении (4. 10) m= n. А, n. В – число молекул А и В в единице объема. Скорость бимолекулярной реакции, согласно закону действующих масс , , (4. 11) Количество активных столкновений равно числу реагирующих молекул, т. е. изменению числа молекул в единице объема за 1 с (4. 12) т. к. CА = n. A/Na, СВ = n. B/Na (Na = 6, 02· 1023 молекул – число Авогадро) Объединим уравнения (4. 9) и (4. 1 и выразим скорость реакции Ze–E/RT = – Na(d. CA/dt) (4. 13)
 Сравнивая (4. 11) и (4. 13) с учетом (4. 10), получаем выражение для константы скорости (4. 14) Обозначим через Z 0 – фактор соударений, т. е. количество соударений в единице объема за 1 с при единичных концентрациях веществ, т. е. k = Z 0 * e–E/RT Величина Е, входящая в уравнения теории активных столкновений (4. 13)-(4. 15), называется истинной энергией активации, в отличие от опытной или эффективной - Еа, определяемой по уравнению Аррениуса. Установим связь между Е и Еа. Для этого перепишем уравнение (4. 15) в виде k = k/ T e–E/RT, (4. 15/ ) где k содержит все величины уравнения, не зависящие от Т. Прологарифмируем (4. 15/) и продифференцируем по Т.
Сравнивая (4. 11) и (4. 13) с учетом (4. 10), получаем выражение для константы скорости (4. 14) Обозначим через Z 0 – фактор соударений, т. е. количество соударений в единице объема за 1 с при единичных концентрациях веществ, т. е. k = Z 0 * e–E/RT Величина Е, входящая в уравнения теории активных столкновений (4. 13)-(4. 15), называется истинной энергией активации, в отличие от опытной или эффективной - Еа, определяемой по уравнению Аррениуса. Установим связь между Е и Еа. Для этого перепишем уравнение (4. 15) в виде k = k/ T e–E/RT, (4. 15/ ) где k содержит все величины уравнения, не зависящие от Т. Прологарифмируем (4. 15/) и продифференцируем по Т.
 lnk = lnk/ + 1/2 ln. T – E/RT (4. 16) Сравнивая полученное выражение (4. 16) с дифференциальным уравнением Аррениуса (4. 5), получаем Еа = Е + 1/2 RT Е 1/2 RT. Еа Е. Для объяснения расхождений теории с опытными данными было предложено ввести в формулу (4. 15) поправочный множитель р (стерический фактор), учитывающий ориентацию молекул друг относительно друга в момент столкновения k = p. Z 0 e–Е/R, (4. 18) т. е. предэкспоненциальный множитель в уравнении Аррениуса А = р. Z 0. Стерический фактор или фактор вероятности р зависит от природы реакции. Для реакций в газах он изменяется от 10 -8 до 1. Для сложных молекул р << 1, т. е. для протекания реакции между молекулами необходимо не только наличие избыточной энергии, молекулы должны быть определенным образом повернуты друг к другу. Когда столкновение происходит слишком быстро, молекулы не успевают прореагировать и р 1.
lnk = lnk/ + 1/2 ln. T – E/RT (4. 16) Сравнивая полученное выражение (4. 16) с дифференциальным уравнением Аррениуса (4. 5), получаем Еа = Е + 1/2 RT Е 1/2 RT. Еа Е. Для объяснения расхождений теории с опытными данными было предложено ввести в формулу (4. 15) поправочный множитель р (стерический фактор), учитывающий ориентацию молекул друг относительно друга в момент столкновения k = p. Z 0 e–Е/R, (4. 18) т. е. предэкспоненциальный множитель в уравнении Аррениуса А = р. Z 0. Стерический фактор или фактор вероятности р зависит от природы реакции. Для реакций в газах он изменяется от 10 -8 до 1. Для сложных молекул р << 1, т. е. для протекания реакции между молекулами необходимо не только наличие избыточной энергии, молекулы должны быть определенным образом повернуты друг к другу. Когда столкновение происходит слишком быстро, молекулы не успевают прореагировать и р 1.
 Теория активных соударений наряду со своими достоинствами (наглядность, простота математического аппарата) имеет целый ряд недостатков: – молекулы рассматриваются как жесткие сферы определенного диаметра; – не рассматривается протяженность химического взаимодействия во времени; – наблюдается расхождение рассчитанных и экспериментальных значений предэкспоненциального множителя; – не раскрывается природа активного состояния и нет возможности теоретического расчета энергии активации, стерического фактора. Теория переходного состояния (теория активного комплекса) Основное положение теории переходного состояния заключаются в том, что всякая химическая реакция протекает через образование некоторого активного комплекса, который затем распадается на продукты данной реакции. Например, реакцию взаимодействия двухатомных молекул АВ + СD = АС + BD (4. 19) можно представить следующим образом А | + B исходные вещества С | D А----С А–С B–D B----D малоустойчивый комплекс продукты реакции (4. 19 /)
Теория активных соударений наряду со своими достоинствами (наглядность, простота математического аппарата) имеет целый ряд недостатков: – молекулы рассматриваются как жесткие сферы определенного диаметра; – не рассматривается протяженность химического взаимодействия во времени; – наблюдается расхождение рассчитанных и экспериментальных значений предэкспоненциального множителя; – не раскрывается природа активного состояния и нет возможности теоретического расчета энергии активации, стерического фактора. Теория переходного состояния (теория активного комплекса) Основное положение теории переходного состояния заключаются в том, что всякая химическая реакция протекает через образование некоторого активного комплекса, который затем распадается на продукты данной реакции. Например, реакцию взаимодействия двухатомных молекул АВ + СD = АС + BD (4. 19) можно представить следующим образом А | + B исходные вещества С | D А----С А–С B–D B----D малоустойчивый комплекс продукты реакции (4. 19 /)
 В ходе реакции молекулы АВ и CD образуют некоторый малоустойчивый комплекс из четырех атомов. Этот комплекс, в котором “старые” связи между атомами еще не полностью разорвались, а новые еще не вполне образовались, называется активным комплексом или переходным состоянием. На образование активного комплекса расходуется энергия, равная энергии активации. Энергетическая диаграмма – это график зависимости реагирующих частиц от расстояния между ними. энергии системы Элементарный химический акт есть непрерывный процесс взаимного превращения кинетической энергии молекул во внутреннюю энергию движения ядер и электронов. В данной теории (переходного состояния) рассматривается лишь адиабатическое приближение (не путать с понятием адиабатического процесса в термодинамике). Адиабатическое приближение заключается в том, что движение ядер атомов при химическом взаимодействии не сопровождается электронными переходами, т. е. движение ядер не зависит от движения электронов. Рассмотрим простейший вариант – взаимодействие двухатомной молекулы АВ и атома D, когда все три атома располагаются на одной прямой. В этом случае потенциальная энергия системы зависит только от двух переменных r 1 (расстояние между А и В) и r 2 (расстояние между В и D). Согласно расчетам, потенциальная энергия является однозначной, непрерывной функцией U(r 1, r 2).
В ходе реакции молекулы АВ и CD образуют некоторый малоустойчивый комплекс из четырех атомов. Этот комплекс, в котором “старые” связи между атомами еще не полностью разорвались, а новые еще не вполне образовались, называется активным комплексом или переходным состоянием. На образование активного комплекса расходуется энергия, равная энергии активации. Энергетическая диаграмма – это график зависимости реагирующих частиц от расстояния между ними. энергии системы Элементарный химический акт есть непрерывный процесс взаимного превращения кинетической энергии молекул во внутреннюю энергию движения ядер и электронов. В данной теории (переходного состояния) рассматривается лишь адиабатическое приближение (не путать с понятием адиабатического процесса в термодинамике). Адиабатическое приближение заключается в том, что движение ядер атомов при химическом взаимодействии не сопровождается электронными переходами, т. е. движение ядер не зависит от движения электронов. Рассмотрим простейший вариант – взаимодействие двухатомной молекулы АВ и атома D, когда все три атома располагаются на одной прямой. В этом случае потенциальная энергия системы зависит только от двух переменных r 1 (расстояние между А и В) и r 2 (расстояние между В и D). Согласно расчетам, потенциальная энергия является однозначной, непрерывной функцией U(r 1, r 2).
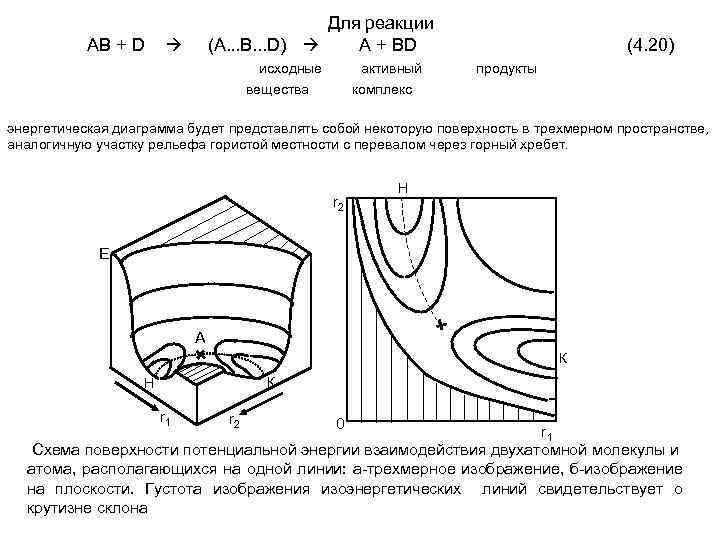 АВ + D Для реакции (A. . . B. . . D) A + BD исходные активный вещества (4. 20) продукты комплекс энергетическая диаграмма будет представлять собой некоторую поверхность в трехмерном пространстве, аналогичную участку рельефа гористой местности с перевалом через горный хребет. r 2 Н Е А К К Н r 1 r 2 0 r 1 Схема поверхности потенциальной энергии взаимодействия двухатомной молекулы и атома, располагающихся на одной линии: а-трехмерное изображение, б-изображение на плоскости. Густота изображения изоэнергетических линий свидетельствует о крутизне склона
АВ + D Для реакции (A. . . B. . . D) A + BD исходные активный вещества (4. 20) продукты комплекс энергетическая диаграмма будет представлять собой некоторую поверхность в трехмерном пространстве, аналогичную участку рельефа гористой местности с перевалом через горный хребет. r 2 Н Е А К К Н r 1 r 2 0 r 1 Схема поверхности потенциальной энергии взаимодействия двухатомной молекулы и атома, располагающихся на одной линии: а-трехмерное изображение, б-изображение на плоскости. Густота изображения изоэнергетических линий свидетельствует о крутизне склона
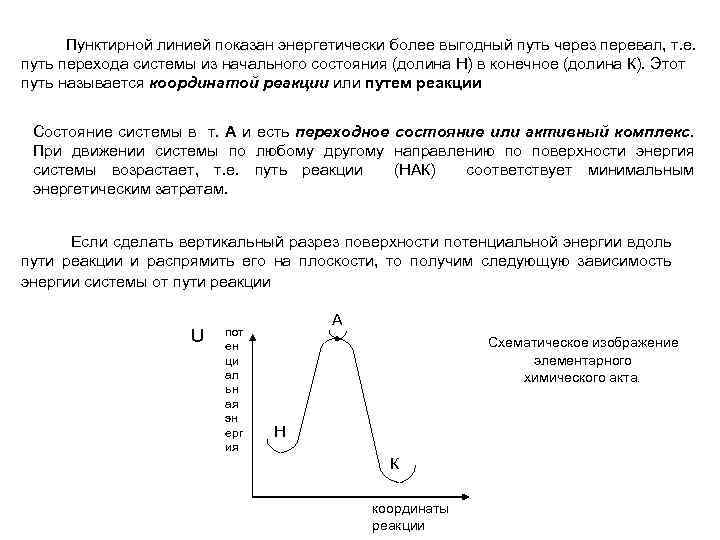 Пунктирной линией показан энергетически более выгодный путь через перевал, т. е. путь перехода системы из начального состояния (долина Н) в конечное (долина К). Этот путь называется координатой реакции или путем реакции Состояние системы в т. А и есть переходное состояние или активный комплекс. При движении системы по любому другому направлению по поверхности энергия системы возрастает, т. е. путь реакции (НАК) соответствует минимальным энергетическим затратам. Если сделать вертикальный разрез поверхности потенциальной энергии вдоль пути реакции и распрямить его на плоскости, то получим следующую зависимость энергии системы от пути реакции U пот ен ци ал ьн ая эн ерг ия А Схематическое изображение элементарного химического акта. Н К координаты реакции
Пунктирной линией показан энергетически более выгодный путь через перевал, т. е. путь перехода системы из начального состояния (долина Н) в конечное (долина К). Этот путь называется координатой реакции или путем реакции Состояние системы в т. А и есть переходное состояние или активный комплекс. При движении системы по любому другому направлению по поверхности энергия системы возрастает, т. е. путь реакции (НАК) соответствует минимальным энергетическим затратам. Если сделать вертикальный разрез поверхности потенциальной энергии вдоль пути реакции и распрямить его на плоскости, то получим следующую зависимость энергии системы от пути реакции U пот ен ци ал ьн ая эн ерг ия А Схематическое изображение элементарного химического акта. Н К координаты реакции
 Впервые приближенный расчет поверхности потенциальной энергии был сделан Эйрингом и Поляни для реакции обмена Н 2 + Н Н + Н 2 Рассчитанная энергия активации как разность энергии основного состояния активированного комплекса Е 0 и энергии исходных веществ (Е 0, АВ + Е 0, D) является истинной энергией активации Е. Еa = 35, 5 2, 1 Кдж/моль. Е = Е 0* – (Е 0, АВ + Е 0, D) (4. 21) Активированные комплексы во время реакции находятся с исходными веществами в состоянии, близком к равновесию (квазиравновесном).
Впервые приближенный расчет поверхности потенциальной энергии был сделан Эйрингом и Поляни для реакции обмена Н 2 + Н Н + Н 2 Рассчитанная энергия активации как разность энергии основного состояния активированного комплекса Е 0 и энергии исходных веществ (Е 0, АВ + Е 0, D) является истинной энергией активации Е. Еa = 35, 5 2, 1 Кдж/моль. Е = Е 0* – (Е 0, АВ + Е 0, D) (4. 21) Активированные комплексы во время реакции находятся с исходными веществами в состоянии, близком к равновесию (квазиравновесном).
 Расчет скорости реакции по методу переходного состояния В соответствии с положениями теории переходного состояния о протекании элементарной реакции через активированный комплекс, находящийся в квазиравновесном состоянии с исходными веществами, можно записать: АВ + D (АВD)* А + ВD (4. 22) I II Обозначим концентрацию активированных комплексов через С*, она равна числу возникающих активированных комплексов или числу элементарных актов реакции за время *. - среднее время жизни активированного комплекса, т. е. время, за которое происходит перестройка химических связей в реагирующей системе. Поскольку скорость элементарной реакции (4. 22) определяется скоростью образования молекул продуктов при распаде активированного комплекса, то она равна = C*/ * (4. 23) Методами статистической физики было определено, что * = h/к. БТ, где h – постоянная Планка, равная 6, 62. 10 -34 Дж. с; к. Б – постоянная Больцмана, равная 1, 38. 10 -23 Дж/град; Т – абсолютная температура системы.
Расчет скорости реакции по методу переходного состояния В соответствии с положениями теории переходного состояния о протекании элементарной реакции через активированный комплекс, находящийся в квазиравновесном состоянии с исходными веществами, можно записать: АВ + D (АВD)* А + ВD (4. 22) I II Обозначим концентрацию активированных комплексов через С*, она равна числу возникающих активированных комплексов или числу элементарных актов реакции за время *. - среднее время жизни активированного комплекса, т. е. время, за которое происходит перестройка химических связей в реагирующей системе. Поскольку скорость элементарной реакции (4. 22) определяется скоростью образования молекул продуктов при распаде активированного комплекса, то она равна = C*/ * (4. 23) Методами статистической физики было определено, что * = h/к. БТ, где h – постоянная Планка, равная 6, 62. 10 -34 Дж. с; к. Б – постоянная Больцмана, равная 1, 38. 10 -23 Дж/град; Т – абсолютная температура системы.
 Концентрацию активированных комплексов С* можно выразить через концентрации исходных веществ С 1 и С 2 из уравнения для константы равновесия Кс* стадии I реакции (4. 22) Кс* = С*/С 1 С 2 (4. 24) Подставляя в (4. 23) значение для *, а также выражение для С* из (4. 24), получаем W = к. Б Т КС С 1 С 2/h (4. 25) Скорость бимолекулярной реакции согласно закону действующих масс W = k С 1 * С 2. (4. 26) Сравнивая (4. 25) и (4. 26) получаем для константы скорости реакции (4. 22) (4. 27) Основное уравнение теории переходного состояния (4. 27) можно записать в виде (4. 28), учитывая соотношение к. Б= R/NА, где R – универсальная газовая постоянная (8, 31 Дж/моль град), NА – число Авогадро(6, 02 * 1023 моль-1), а также вводя поправочный коэффициент (4. 28)
Концентрацию активированных комплексов С* можно выразить через концентрации исходных веществ С 1 и С 2 из уравнения для константы равновесия Кс* стадии I реакции (4. 22) Кс* = С*/С 1 С 2 (4. 24) Подставляя в (4. 23) значение для *, а также выражение для С* из (4. 24), получаем W = к. Б Т КС С 1 С 2/h (4. 25) Скорость бимолекулярной реакции согласно закону действующих масс W = k С 1 * С 2. (4. 26) Сравнивая (4. 25) и (4. 26) получаем для константы скорости реакции (4. 22) (4. 27) Основное уравнение теории переходного состояния (4. 27) можно записать в виде (4. 28), учитывая соотношение к. Б= R/NА, где R – универсальная газовая постоянная (8, 31 Дж/моль град), NА – число Авогадро(6, 02 * 1023 моль-1), а также вводя поправочный коэффициент (4. 28)
 Поправочный множитель , входящий в основное уравнение теории (4. 28), называется коэффициентом прохождения или трансмиссионным коэффициентом. В теории переходного состояния константу равновесия Кс* выражают двумя способами: а) через статистические суммы по состояниям; б) через термодинамические характеристики реагирующих частиц. где QАВ, QD, Q - статистические суммы по состояниям исходных веществ, а также активированного комплекса, лишенного одной колебательной степени свободы, Н*00 – разность энтальпий активного комплекса и исходных молекул при температуре Т=0. (4. 29) (4. 29’) где изменение числа моль газообразных веществ. Учитывая это, можно рассчитать константу скорости по формуле. (4. 30)
Поправочный множитель , входящий в основное уравнение теории (4. 28), называется коэффициентом прохождения или трансмиссионным коэффициентом. В теории переходного состояния константу равновесия Кс* выражают двумя способами: а) через статистические суммы по состояниям; б) через термодинамические характеристики реагирующих частиц. где QАВ, QD, Q - статистические суммы по состояниям исходных веществ, а также активированного комплекса, лишенного одной колебательной степени свободы, Н*00 – разность энтальпий активного комплекса и исходных молекул при температуре Т=0. (4. 29) (4. 29’) где изменение числа моль газообразных веществ. Учитывая это, можно рассчитать константу скорости по формуле. (4. 30)
 Выразим константу скорости через изменение термодинамических функций при образовании активированного комплекса. Из уравнения изотермы химической реакции, протекающей при постоянном объеме: F 0* = RT ln. Kc*, где F* -изменение свободной энергии Гельмгольца при образовании активированного комплекса из исходных веществ в стандартном состоянии. F 0* = U 0* – T S 0* Кc * = е (4. 31) И учитывая выражения (4. 28), (4. 31) для константы скорости, можно записать: (4. 32) Для реакций, протекающих при постоянном давлении, используют уравнение (4. 32’) Т. е. скорость реакции определяется не энергией активации U 0* или Н 0* , а изменением энергии Гельмгольца F 0* или энергии Гиббса G 0* при образовании активированного комплекса.
Выразим константу скорости через изменение термодинамических функций при образовании активированного комплекса. Из уравнения изотермы химической реакции, протекающей при постоянном объеме: F 0* = RT ln. Kc*, где F* -изменение свободной энергии Гельмгольца при образовании активированного комплекса из исходных веществ в стандартном состоянии. F 0* = U 0* – T S 0* Кc * = е (4. 31) И учитывая выражения (4. 28), (4. 31) для константы скорости, можно записать: (4. 32) Для реакций, протекающих при постоянном давлении, используют уравнение (4. 32’) Т. е. скорость реакции определяется не энергией активации U 0* или Н 0* , а изменением энергии Гельмгольца F 0* или энергии Гиббса G 0* при образовании активированного комплекса.
 Чтобы выяснить физический смысл U 0*, прологарифмируем выражение (4. 28) и продифференцируем по температуре lnk = ln + ln. T + ln. Kc* (4. 33) Сравнивая (4. 33) с уравнением Аррениуса в дифференциальной форме (4. 5) и учитывая уравнение изохоры Вант - Гоффа получаем связь эффективной Еа и истинной U 0 энергий активации т. е. Еа = U 0 + RT = Eист + RT. Для многих реакций энергия активации намного больше RT, поэтому приближенно можно считать Еа = U 0.
Чтобы выяснить физический смысл U 0*, прологарифмируем выражение (4. 28) и продифференцируем по температуре lnk = ln + ln. T + ln. Kc* (4. 33) Сравнивая (4. 33) с уравнением Аррениуса в дифференциальной форме (4. 5) и учитывая уравнение изохоры Вант - Гоффа получаем связь эффективной Еа и истинной U 0 энергий активации т. е. Еа = U 0 + RT = Eист + RT. Для многих реакций энергия активации намного больше RT, поэтому приближенно можно считать Еа = U 0.


