Лекция 2. 2015.Теории.ppt
- Количество слайдов: 46

Теории газовой хроматографии Формы изотерм сорбции и соответствующие им контуры зон согласно различным теориям газовой хроматографии: а — линейная идеальная; б — нелинейная идеальная; в — линейная неидеальная: г — нелинейная неидеальная 1

Идеальная равновесная хроматография В простейшем случае можно допустить, что при переносе сорбата через хроматографическую колонку на каждом ее участке успевает установиться состояние равновесия. В этом случае для исследования работы колонки можно составить уравнение материального баланса для некоторого ее слоя толщиной dx. с=f(t, x). ω (мл/мин) - объемная скорость газа-носителя В слое толщиной dx происходит накопление компонента (положительное или отрицательное) в количестве: Скорость распределения сорбата между подвижной и неподвижной фазами в поперечном слое толщиной dx на расстоянии х от входа в колонку составляет: υa – объем адсорбционного слоя, υ – объем газовой фазы в расчете на единицу длины колонки 2 моль/мин (1) моль/мин (2)

По условию материального баланса скорость накопления и распределения сорбата между газом и НЖФ должны быть равны: или 3 (1) Т. к. детектор измеряет концентрацию сорбата в газовой фазе, то последнюю производную можно выразить через произведение двух частных производных: (2) характеризует изотерму адсорбции ca=f(c) и не зависит от x , поэтому будет справедливо уравнение (3)

4 Подставив выражение (3) в уравнение (1), получим (4) Т. к. с=f(x, t) функция двух переменных, то ее полный дифференциал При постоянной концентрации с (когда dc=0), разделив выражение (5) на dt, получим: (5) Т. к. (6) (7) (линейная скорость перемещения сорбата), то Вводя (7) в (4) и сокращая или , получим (8) основное уравнение теории равновесной газовой хроматографии

Если наблюдается линейная изотерма распределения Генри, то (9) а скорость перемещения данной концентрации компонента в газе вдоль колонки, согласно уравнения (8), составит (10) Такой случай называется линейной равновесной хроматографией Схема прохождения полос компонентов А и В через газохроматографическую колонку в условиях идеальной равновесной хроматографии. 5
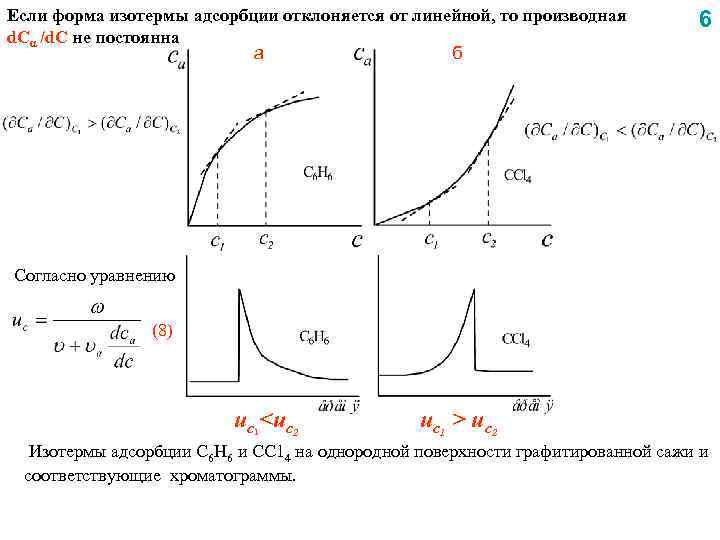
Если форма изотермы адсорбции отклоняется от линейной, то производная d. Cα /d. C не постоянна а б 6 Согласно уравнению (8) uc <uc 2 1 uc 1 > uc 2 Изотермы адсорбции С 6 Н 6 и СС 14 на однородной поверхности графитированной сажи и соответствующие хроматограммы.

7 Параметры удерживания Для газа-носителя константа Генри K 0=0, тогда в соответствии с уравнением (10) (11) линейная скорость газа-носителя: Линейные скорости передвижения компонента не измеряются, удобно пользоваться относительными скоростями передвижения компонента: (12) где σ = υa /υ – фазовое отношение. Так как обычно σ ≈ 1 и K>>1, то и σK>>1, поэтому RF<<1: (13) (14) Обычно непосредственно измеряемой величиной в газовой хроматографии является время удерживания данного компонента tc,
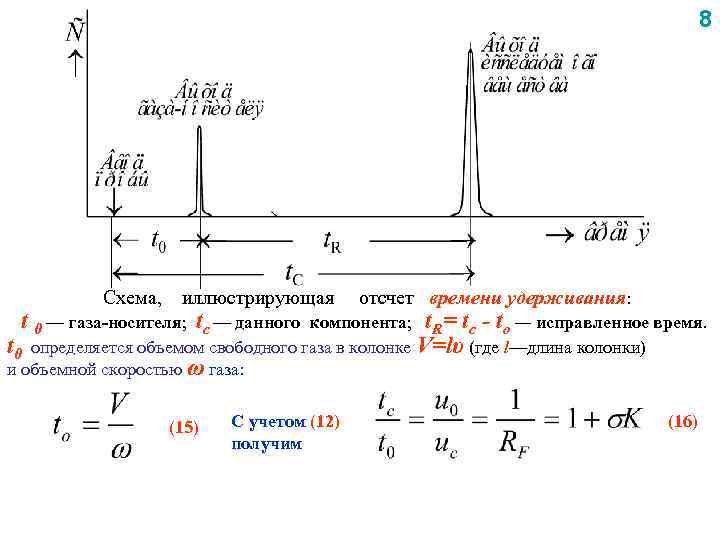
8 Схема, иллюстрирующая t 0 — газа-носителя; tc — данного отсчет времени удерживания: компонента; t. R= tc - to — исправленное время. t 0 определяется объемом свободного газа в колонке V=lυ (где l—длина колонки) и объемной скоростью ω газа: (15) С учетом (12) получим (16)

t. R=tc-t 0 = t 0σK, Учитывая (15) 9 (17) (18) получим Удерживаемый объем представляет объем газа-носителя, прошедший через колонку за исправленное время удерживания компонента t. R. . VR = t. Rω = VσK VR не зависит от ω VR = Va. K Т. к. В случае ГЖХ (19) Va=m/ρ , где (20) т—масса введенной в колонку НЖФ, а ρ – ее плотность. Поэтому (21)

10 Разделив обе части уравнения (21) на величину m (масса НЖФ), получим (22) ! удельный удерживаемый объем V R, m (газжидкость) обладает свойствами физикохимической константы В случае ГАХ (23) или (24) Связь между константами линейной изотермы адсорбции, выраженной в различных координатах К=са /с Va. K = m. KА, c=sm. K α, c = m. RTKА, p = sm. RTKα, p (25)

Подставляя выражения для Va. K в основную формулу (20) VR = Va. K и деля на т, получаем: V R , т (г–тв) =KА, c =RTKА, p (26) V R, m (г–тв) = s. Kα, c = s. RTK α, p 11 (27) Физико-химической константой, зависящей при данной температуре только от природы этой системы, будет абсолютная величина удерживаемого объема, т. е. отнесенная к единице поверхности твердого тела: (28) VR, s (г–тв) = VR, m (г–тв) /s= Kα, c = RTK α, p Определение удельной поверхности S Определение теплоты адсорбции: (30) (ГАХ) (29) (ГЖХ) (31) (33) (32) (34)

12 ТЕОРИИ НЕРАВНОВЕСНОЙ ХРОМАТОГРАФИИ Диффузионно-массообменная теория Ван-Деемтера Продольная диффузия в газе Δ 2 = 2 Dτ, DП = γD коэффициент «извилистости» γ >1 u (1) (2) зависит от размеров и формы зерен и их упаковки. Омывание зерен насадки ( «вихревая» диффузия) u отсюда (5) (8) Δ=dз (3) dз Массообмен с неподвижной фазой τ ~dз /u DB ~ d 3 u = λd 3 u (4) 1/k - время, в течение которого концентрация изменяется в е раз, а молекулы сорбата (не (7) участвующие в обмене с неподвижной фазой) переместятся в потоке газа на расстояние:

13 В соответствии с уравнением Эйнштейна (8) (9) учитывая выражение (8) , получим: или (10) Коэффициент общей эффективной диффузии равен (12) DЭ = γD + λdu +δu 2 Уравнение хроматографической кривой c=f(x, t), можно получить исходя из DЭ = DП+DB+DM (11) или уравнения 2 -го закона Фика для молекулярной диффузии: (13) интегрирование которого приводит к кривой Гаусса: Для реального процесса (14) заменяем D на D Э (15)
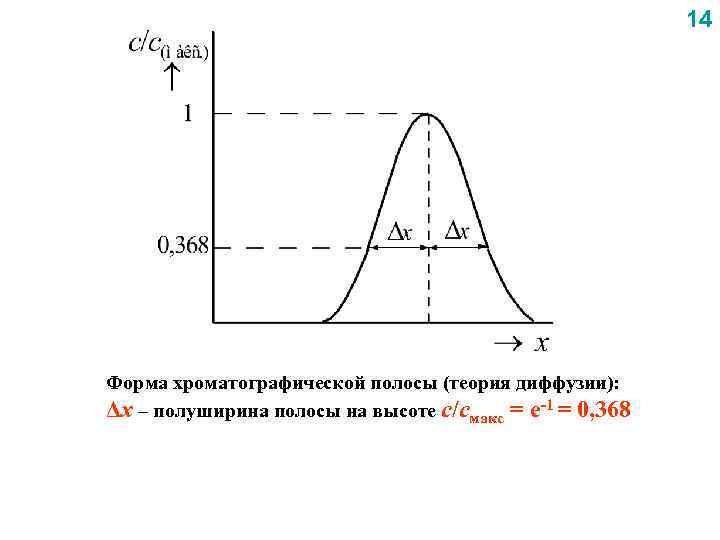
14 Форма хроматографической полосы (теория диффузии): Δх – полуширина полосы на высоте с/смакс = e-1 = 0, 368

15 ТЕОРИЯ ЭКВИВАЛЕНТНЫХ ТАРЕЛОК МАРТИНА (1) (2) (3) υэ — «эффективный объем тарелки» (4) Целесообразно ввести относительные единицы переменных
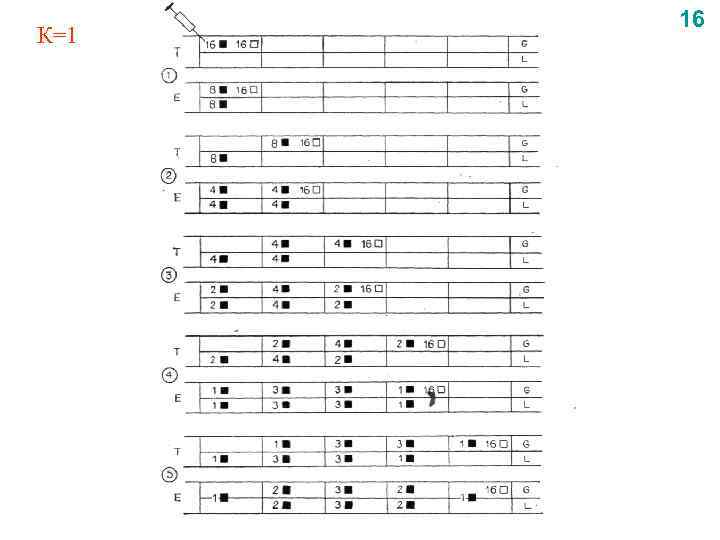
К=1 16

17 относительные единицы концентрации (5) с0 –концентрация газа на первой тарелке относительные единицы объема газа (6) где V—весь объем газа, прошедший (толчками) через колонку (7) Тогда ур-я (4) можно представить в виде Для решения системы из n дифференциальных уравнений надо принять начальные условия: при β=0 y 1=y 2=· · ·=yn=0 β 0<< β где причем V 0 — введенный в колонку объем газа, содержавший данный компонент (объем чистого газа-носителя, вошедшего после этого в колонку толчками, составляет V—V 0). Решением системы дифференциальных уравнений является уравнение (8) которое при β>100 с достаточной точностью (8) выражается уравнением Гаусса (9)

18 Уравнение (9) является уравнением хроматографической кривой. Максимуму этой кривой отвечает условие или (10) Следовательно (11) Удобнее использовать другую относительную концентрацию (12) тогда уравнение хроматографической кривой принимает вид (13) β=п (10 а)
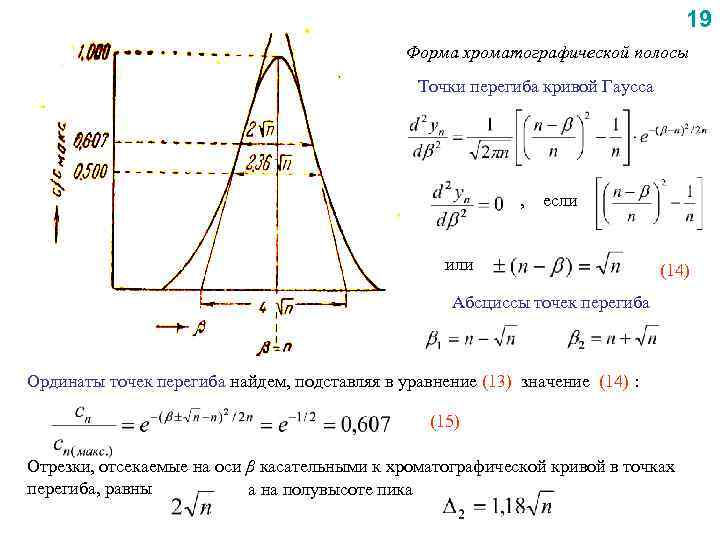
19 Форма хроматографической полосы Точки перегиба кривой Гаусса , если или (14) Абсциссы точек перегиба Ординаты точек перегиба найдем, подставляя в уравнение (13) значение (14) : (15) Отрезки, отсекаемые на оси β касательными к хроматографической кривой в точках перегиба, равны а на полувысоте пика
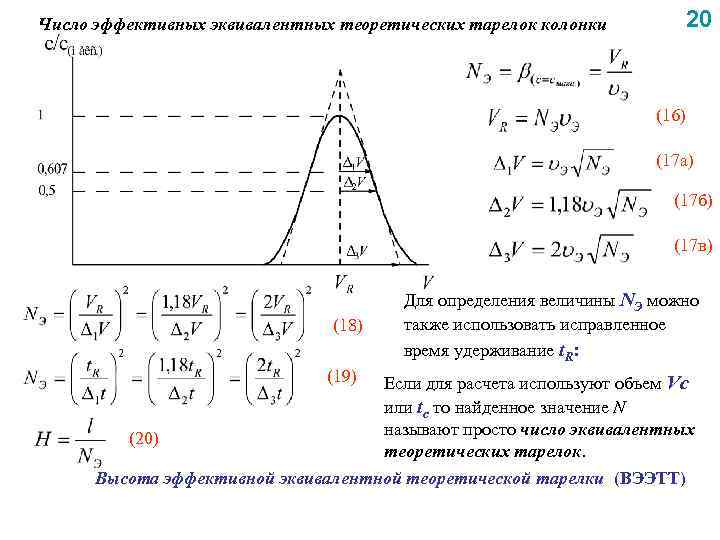
Число эффективных эквивалентных теоретических тарелок колонки 20 (16) (17 а) (17 б) (17 в) (18) (19) Для определения величины NЭ можно также использовать исправленное время удерживание t. R: Если для расчета используют объем Vc или tc то найденное значение N называют просто число эквивалентных (20) теоретических тарелок. Высота эффективной эквивалентной теоретической тарелки (ВЭЭТТ)
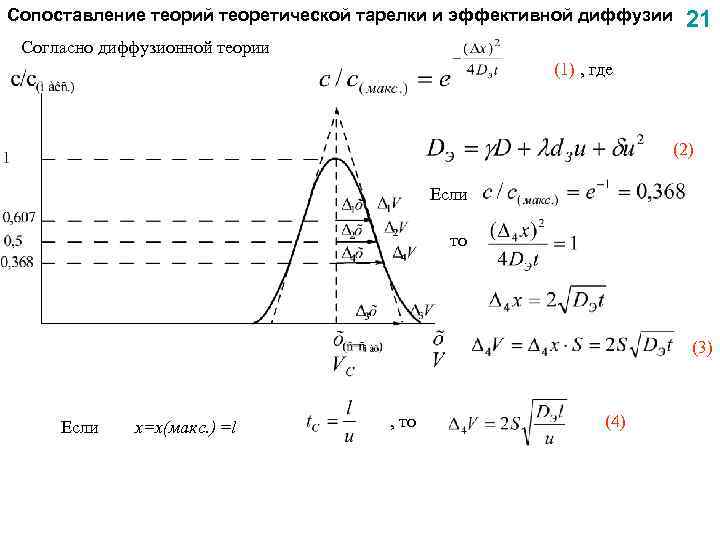
Сопоставление теорий теоретической тарелки и эффективной диффузии 21 Согласно диффузионной теории (1) , где (2) Если то (3) Если x=x(макс. ) =l , то (4)

22 Теория тарелок Мартина приводит к уравнению (5) Если с/с(макс. )=е-1=0, 368 и рассматривается распределение сорбата на выходе из колонки, то n=N (N – число тарелок, присущее данной колонке), а смещение (6) , из уравнений (4) и (6) следует, что (7) Если левую и правую часть уравнения (7) возвести в квадрат и умножить на N, тогда Умножим числитель и знаменатель правой части последнего уравнения на l , то Т. к. где , то (8) (9) Подставив в это уравнение значение DЭ = γD + λdu +δu 2 получим уравнение Ван-Деемтера: (10) (11)
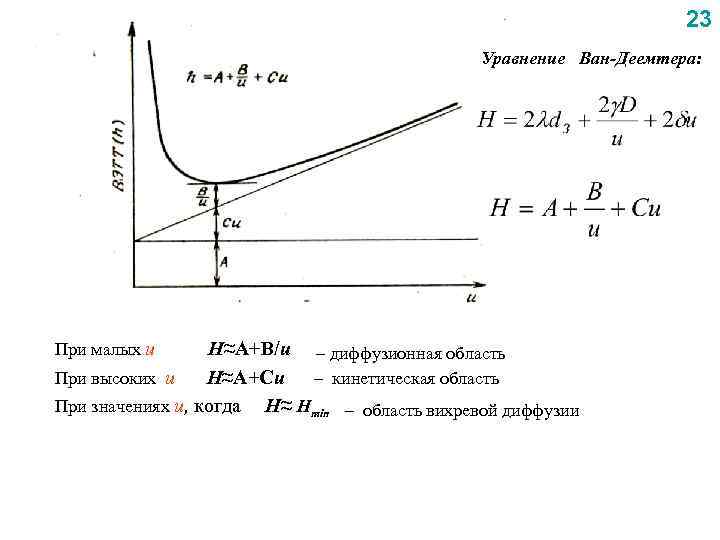
23 Уравнение Ван-Деемтера: При малых u H≈A+В/u – диффузионная область При высоких u Н≈А+Cu – кинетическая область При значениях u, когда H≈ Hmin – область вихревой диффузии
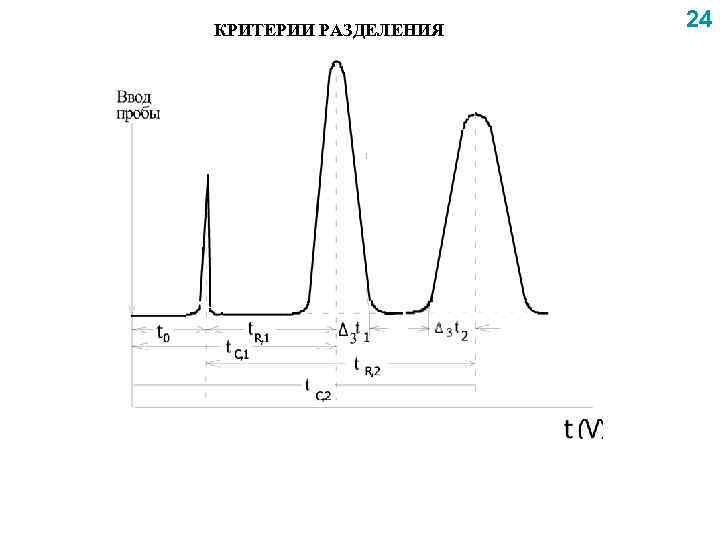
КРИТЕРИИ РАЗДЕЛЕНИЯ 24

Для оценки хроматографического разделения компонентов используют 25 три группы критериев Первая группа критериев разделения зависит от природы сорбента и сорбата, от температуры и характеризует качество разделения в зависимости от различия адсорбируемости или растворимости разделяемых веществ. К критериям этой группы относятся: Коэффициент селективности (1) (степень разделения) η критерий селективности Кс (2) Если обозначить (3) и разделить числитель и знаменатель на VС, 1 или t. С, 1 , то m 2, 1 тоже называется степенью разделения, но отличается от (4) η 2, 1 тем, что в ней не учтено удерживание несорбирующегося вещества. В случае высокой адсорбируемости Если η 2, 1= l, то вещества не разделяются или (5)

Вторая группа критериев N и H, а также отношение Dэфф /u. Высокая эффективность работы колонки при низкой селективности также не позволяет успешно проводить анализ сложных систем. 26 Третья группа критериев (обобщенные критерии) учитывает как различие в адсорбируемости или растворимости, так и размывание хроматографических полос. Коэффициент (или степень) разделения R, (6) Если R≥ 1, то достигается полное разделение компонентов. Т. к. υэфф=υ+υαК и обычно υαК >> υ, то υэфф ≈ υαК. VR, 1=υэфф, 1 N= υαК 1 N и ∆3 V 1= υэфф, 1 2√N= υαК 1 2√ N V R, 2 =υэфф, 2 N= υαК 2 N и ∆3 V 2= υэфф, 2 2√N= υαК 22√ N (7) (8)

Если подставить выражения (7) и (8) в уравнение (6), то получим выражения коэффициента разделения (9) 27 (10) Например, необходимо разделить сорбаты, коэффициент селективности для которых η=1, 1. Т. к. при полном разделении минимальное значение коэффициента разделения R=1, то отсюда N=1764. Для разделения такой смеси сорбатов требуется сравнительно высокоэффективная колонка. Если сорбаты существенно различаются по своим сорбционным свойствам, например η=2, то для их полного разделения достаточно колонки с N=36.
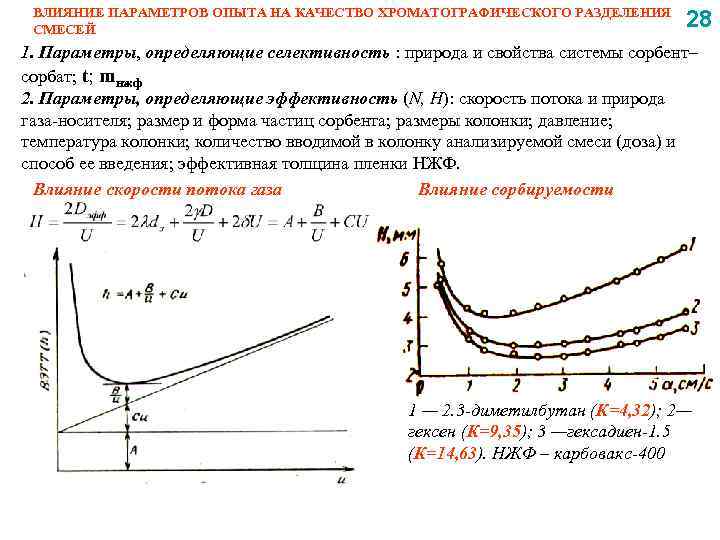
ВЛИЯНИЕ ПАРАМЕТРОВ ОПЫТА НА КАЧЕСТВО ХРОМАТОГРАФИЧЕСКОГО РАЗДЕЛЕНИЯ СМЕСЕЙ 28 1. Параметры, определяющие селективность : природа и свойства системы сорбент– сорбат; t; mнжф 2. Параметры, определяющие эффективность (N, H): скорость потока и природа газа-носителя; размер и форма частиц сорбента; размеры колонки; давление; температура колонки; количество вводимой в колонку анализируемой смеси (доза) и способ ее введения; эффективная толщина пленки НЖФ. Влияние скорости потока газа Влияние сорбируемости 1 — 2. 3 -диметилбутан (К=4, 32); 2— гексен (К=9, 35); 3 —гексадиен-1. 5 (К=14, 63). НЖФ – карбовакс-400
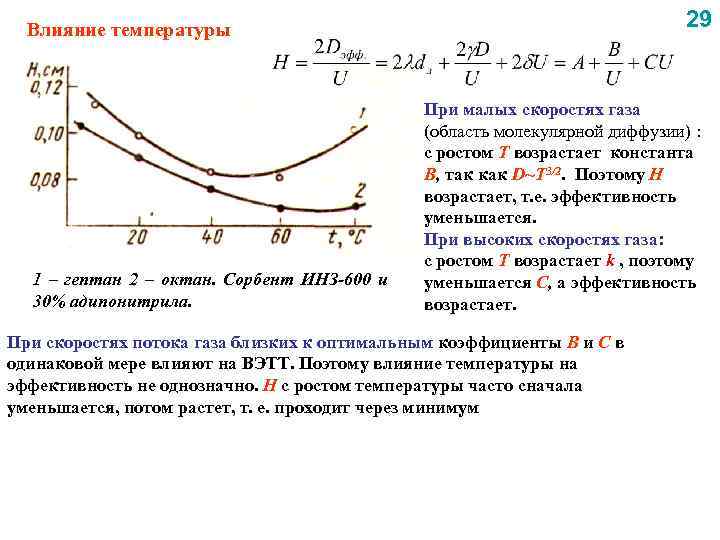
29 Влияние температуры 1 – гептан 2 – октан. Сорбент ИНЗ-600 и 30% адипонитрила. При малых скоростях газа (область молекулярной диффузии) : с ростом Т возрастает константа В, так как D~T 3/2. Поэтому H возрастает, т. е. эффективность уменьшается. При высоких скоростях газа: с ростом Т возрастает k , поэтому уменьшается С, а эффективность возрастает. При скоростях потока газа близких к оптимальным коэффициенты В и С в одинаковой мере влияют на ВЭТТ. Поэтому влияние температуры на эффективность не однозначно. H с ростом температуры часто сначала уменьшается, потом растет, т. е. проходит через минимум
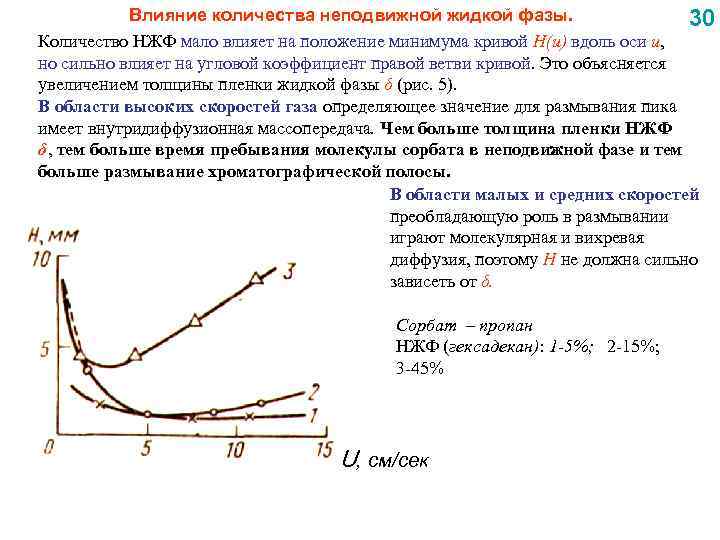
Влияние количества неподвижной жидкой фазы. 30 Количество НЖФ мало влияет на положение минимума кривой H(u) вдоль оси u, но сильно влияет на угловой коэффициент правой ветви кривой. Это объясняется увеличением толщины пленки жидкой фазы δ (рис. 5). В области высоких скоростей газа определяющее значение для размывания пика имеет внутридиффузионная массопередача. Чем больше толщина пленки НЖФ δ, тем больше время пребывания молекулы сорбата в неподвижной фазе и тем больше размывание хроматографической полосы. В области малых и средних скоростей преобладающую роль в размывании играют молекулярная и вихревая диффузия, поэтому H не должна сильно зависеть от δ. Сорбат – пропан НЖФ (гексадекан): 1 -5%; 2 -15%; 3 -45% U, см/сек
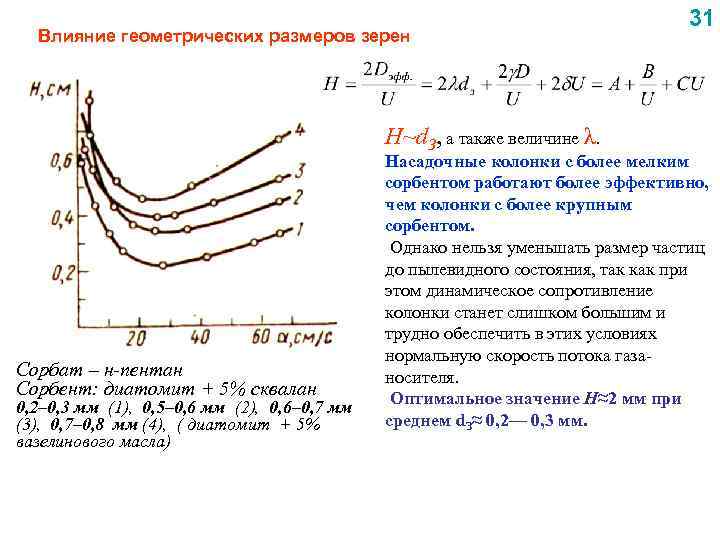
Влияние геометрических размеров зерен H~d. З, а также величине λ. Сорбат – н-пентан Сорбент: диатомит + 5% сквалан 0, 2– 0, 3 мм (1), 0, 5– 0, 6 мм (2), 0, 6– 0, 7 мм (3), 0, 7– 0, 8 мм (4), ( диатомит + 5% вазелинового масла) 31 Насадочные колонки с более мелким сорбентом работают более эффективно, чем колонки с более крупным сорбентом. Однако нельзя уменьшать размер частиц до пылевидного состояния, так как при этом динамическое сопротивление колонки станет слишком большим и трудно обеспечить в этих условиях нормальную скорость потока газаносителя. Оптимальное значение H≈2 мм при среднем d. З≈ 0, 2— 0, 3 мм.
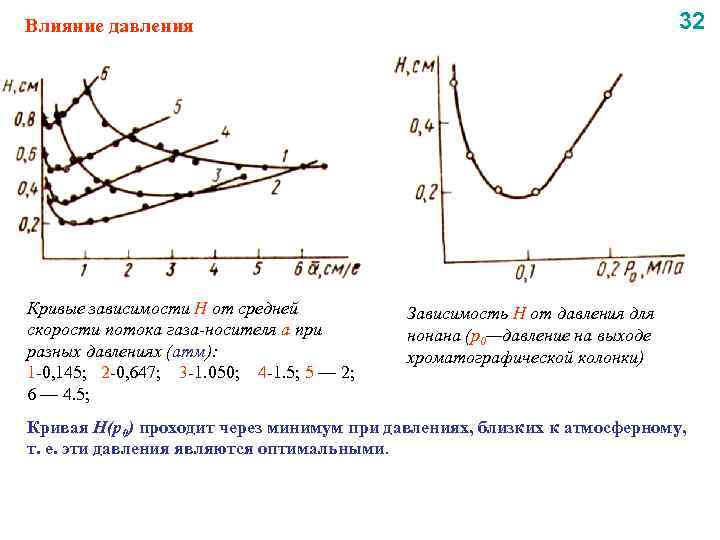
32 Влияние давления Кривые зависимости Н от средней скорости потока газа-носителя а при разных давлениях (атм): 1 -0, 145; 2 -0, 647; 3 -1. 050; 4 -1. 5; 5 — 2; 6 — 4. 5; Зависимость Н от давления для нонана (р0—давление на выходе хроматографической колонки) Кривая H(р0) проходит через минимум при давлениях, близких к атмосферному, т. е. эти давления являются оптимальными.

33 Изменение давления в колонке мало влияет на ее параметры. Более высокое давление улучшает разделение, однако усложняет конструкцию устройства ввода пробы. Обычно работают при атмосферном давлении на выходе колонки. Некоторую роль играет избыточное давление на входе колонки Р, связанное с газовым сопротивлением колонки. Как правило, давление на входе не превышает 0, 3 МПа.
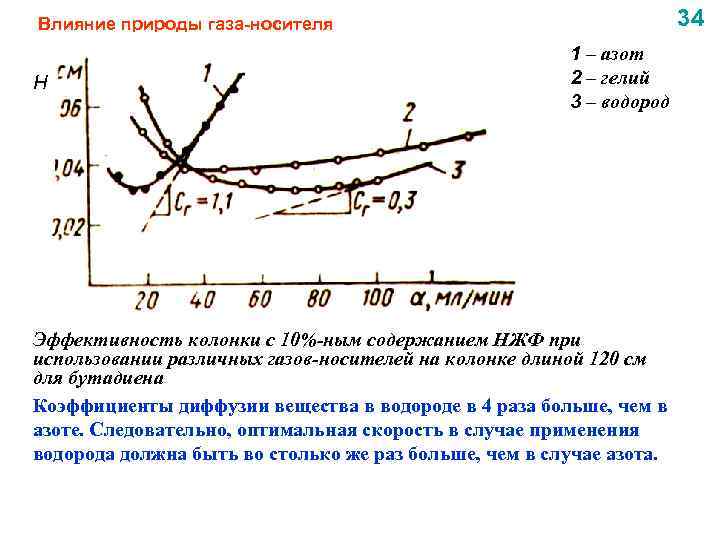
34 Влияние природы газа-носителя Н 1 – азот 2 – гелий 3 – водород Эффективность колонки с 10%-ным содержанием НЖФ при использовании различных газов-носителей на колонке длиной 120 см для бутадиена Коэффициенты диффузии вещества в водороде в 4 раза больше, чем в азоте. Следовательно, оптимальная скорость в случае применения водорода должна быть во столько же раз больше, чем в случае азота.

Влияние объема дозы q на ВЭТТ 35 Согласно теории теоретических тарелок следует, что проба не должна превышать емкости одной теоретической тарелки. Другими словами объем дозы в парообразном или газообразном состоянии не должен превышать ширину хроматографического пика, выраженную в миллилитрах, т. е. q ≤ ∆V. Обычные объемы смесей в газовой хроматографии составляют 0, 5— 0, 1 мкл жидкостей и 0, 5— 20 мл для газов. Влияние геометрических размеров колонки В лабораторной практике для аналитических целей применяются колонки с внутренним диаметром 2— 5 мм. Внутренний диаметр микронабивных колонок обычно 1 мм, капиллярных — 0, 2 − 0, 3 мм. Для препаративных целей применяют колонки диаметром от 1 до 100 см. С увеличением диаметра эффективность колонки падает (ВЭТТ растет). Величина поперечного сечения при малых значениях ее не влияет на ВЭТТ во всех областях скоростей потока газа-носителя. Однако с увеличением диаметра колонки свыше 1 см ВЭТТ интенсивно возрастает. С увеличением длины колонки пропорционально увеличивается число теоретических тарелок. Однако длина колонки очень мало влияет на ВЭТТ, но влияет на критерии разделения. С увеличением длины колонки растут время и объем удерживания, что приводит к увеличению размывания хроматографического пика, но в то же время увеличивается расстояние между вершинами пиков.

АДСОРБЕНТЫ ДЛЯ ГАХ. Классификация адсорбентов: 1) в соответствии с их химической природой (неорганические; неорганические, модифицированные монослоем органического соединения; органические пористые полимерные соединения). 2) по характеру и интенсивности межмолекулярного взаимодействия с адсорбатом (Киселев) 3) по геометрической структуре адсорбентов 36
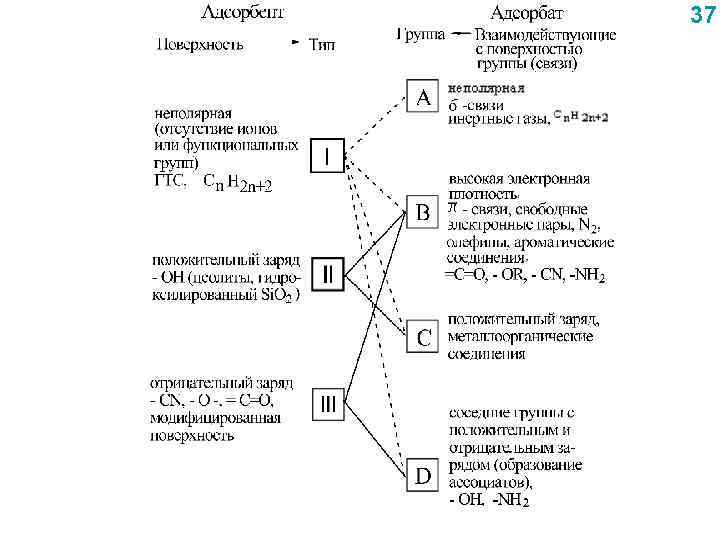
37
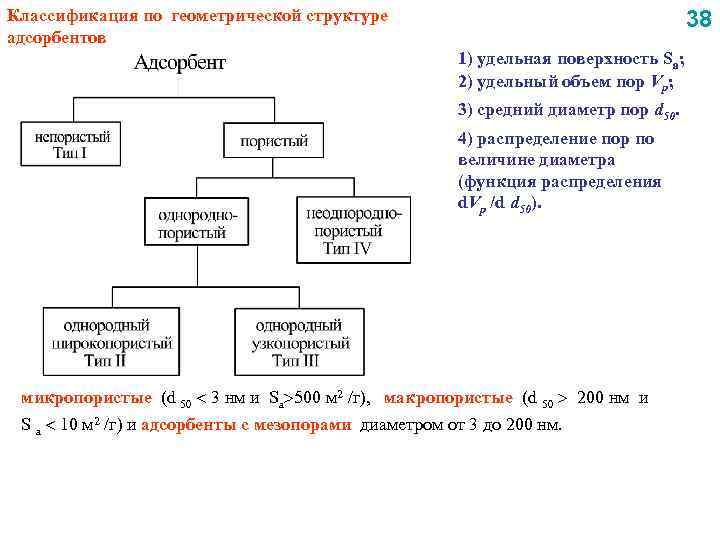
Классификация по геометрической структуре адсорбентов 38 1) удельная поверхность Sa; 2) удельный объем пор Vp; 3) средний диаметр пор d 50. 4) распределение пор по величине диаметра (функция распределения d. Vp /d d 50). микропористые (d 50 3 нм и Sa 500 м 2 /г), макропористые (d 50 200 нм и S a 10 м 2 /г) и адсорбенты с мезопорами диаметром от 3 до 200 нм.
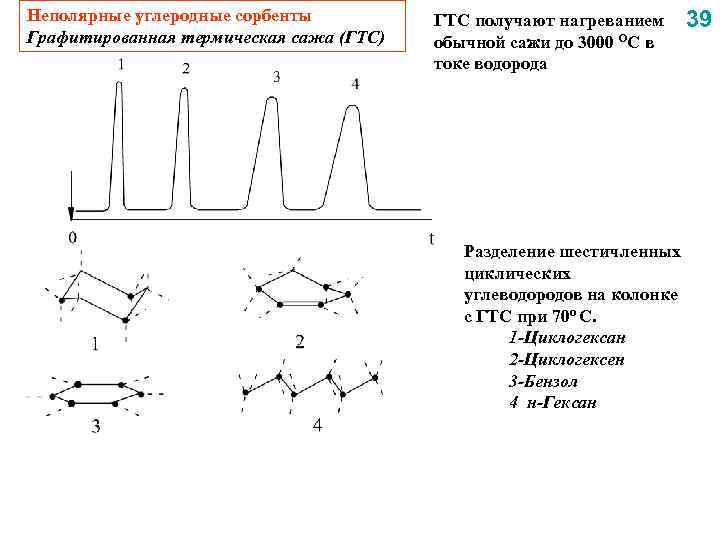
Неполярные углеродные сорбенты Графитированная термическая сажа (ГТС) ГТС получают нагреванием обычной сажи до 3000 ОС в токе водорода Разделение шестичленных циклических углеводородов на колонке с ГТС при 70 о С. 1 -Циклогексан 2 -Циклогексен 3 -Бензол 4 н-Гексан 39
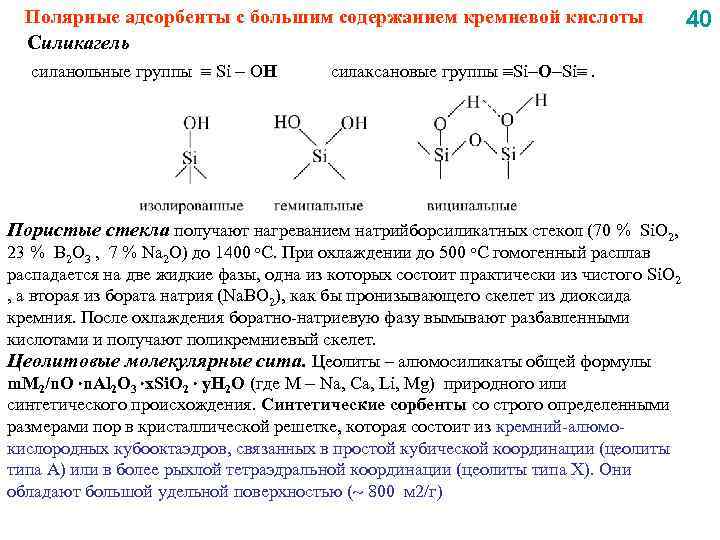
Полярные адсорбенты с большим содержанием кремневой кислоты Силикагель силанольные группы Si OH силаксановые группы Si O Si . Пористые стекла получают нагреванием натрийборсиликатных стекол (70 % Si. O 2, 23 % B 2 O 3 , 7 % Na 2 O) до 1400 о. С. При охлаждении до 500 о. С гомогенный расплав распадается на две жидкие фазы, одна из которых состоит практически из чистого Si. O 2 , а вторая из бората натрия (Na. BO 2), как бы пронизывающего скелет из диоксида кремния. После охлаждения боратно-натриевую фазу вымывают разбавленными кислотами и получают поликремниевый скелет. Цеолитовые молекулярные сита. Цеолиты – алюмосиликаты общей формулы m. M 2/n. O n. Al 2 O 3 x. Si. O 2 y. H 2 O (где М Na, Ca, Li, Mg) природного или синтетического происхождения. Синтетические сорбенты со строго определенными размерами пор в кристаллической решетке, которая состоит из кремний-алюмокислородных кубооктаэдров, связанных в простой кубической координации (цеолиты типа А) или в более рыхлой тетраэдральной координации (цеолиты типа Х). Они обладают большой удельной поверхностью ( 800 м 2/г) 40
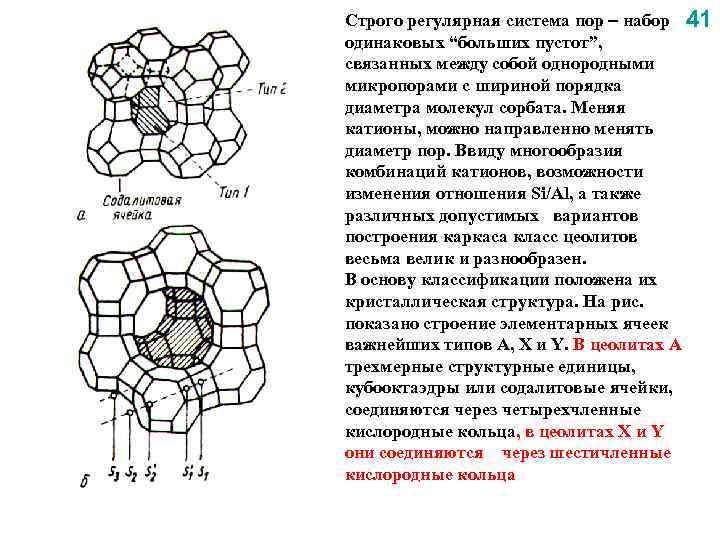
Строго регулярная система пор набор 41 одинаковых “больших пустот”, связанных между собой однородными микропорами с шириной порядка диаметра молекул сорбата. Меняя катионы, можно направленно менять диаметр пор. Ввиду многообразия комбинаций катионов, возможности изменения отношения Si/Al, а также различных допустимых вариантов построения каркаса класс цеолитов весьма велик и разнообразен. В основу классификации положена их кристаллическая структура. На рис. показано строение элементарных ячеек важнейших типов А, X и Y. В цеолитах А трехмерные структурные единицы, кубооктаэдры или содалитовые ячейки, соединяются через четырехчленные кислородные кольца, в цеолитах X и Y они соединяются через шестичленные кислородные кольца
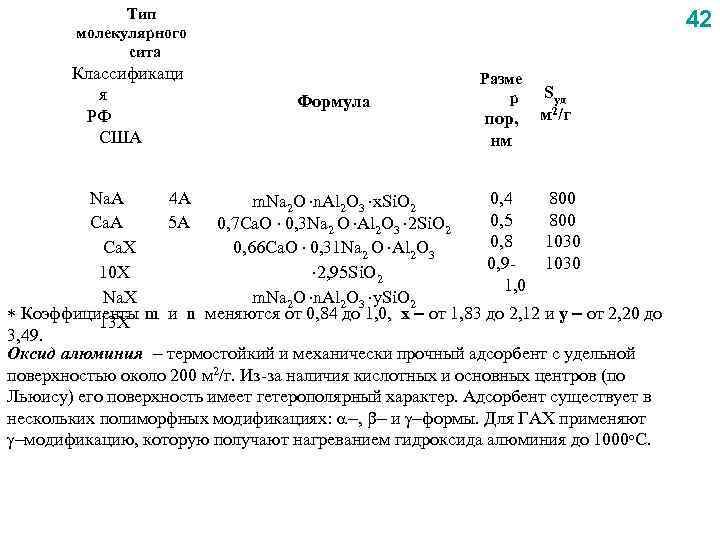
Тип молекулярного сита Классификаци я РФ США 42 Формула Разме р пор, нм Sуд м 2/г Na. A 4 A 0, 4 800 m. Na 2 O n. Al 2 O 3 x. Si. O 2 0, 5 800 Ca. A 5 A 0, 7 Ca. O 0, 3 Na 2 O Al 2 O 3 2 Si. O 2 0, 8 1030 Ca. X 0, 66 Ca. O 0, 31 Na 2 O Al 2 O 3 0, 91030 10 X 2, 95 Si. O 2 1, 0 Na. X m. Na 2 O n. Al 2 O 3 y. Si. O 2 Коэффициенты m и n меняются от 0, 84 до 1, 0, x от 1, 83 до 2, 12 и y от 2, 20 до 13 X 3, 49. Оксид алюминия термостойкий и механически прочный адсорбент с удельной поверхностью около 200 м 2/г. Из-за наличия кислотных и основных центров (по Льюису) его поверхность имеет гетерополярный характер. Адсорбент существует в нескольких полиморфных модификациях: , и формы. Для ГАХ применяют модификацию, которую получают нагреванием гидроксида алюминия до 1000 о. С.
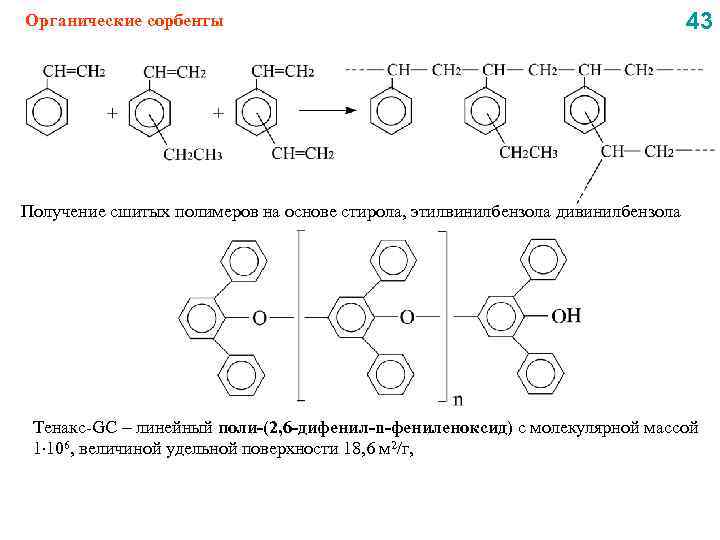
Органические сорбенты 43 Получение сшитых полимеров на основе стирола, этилвинилбензола дивинилбензола Тенакс-GC линейный поли-(2, 6 -дифенил-n-фениленоксид) с молекулярной массой 1 106, величиной удельной поверхности 18, 6 м 2/г,
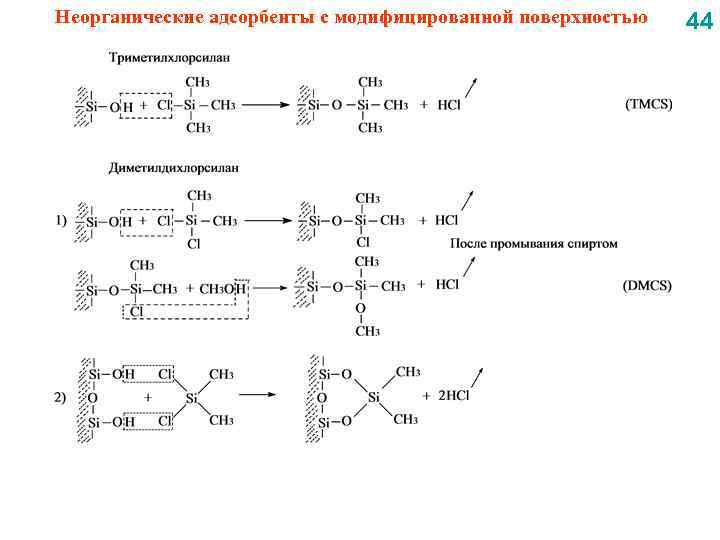
Неорганические адсорбенты с модифицированной поверхностью 44
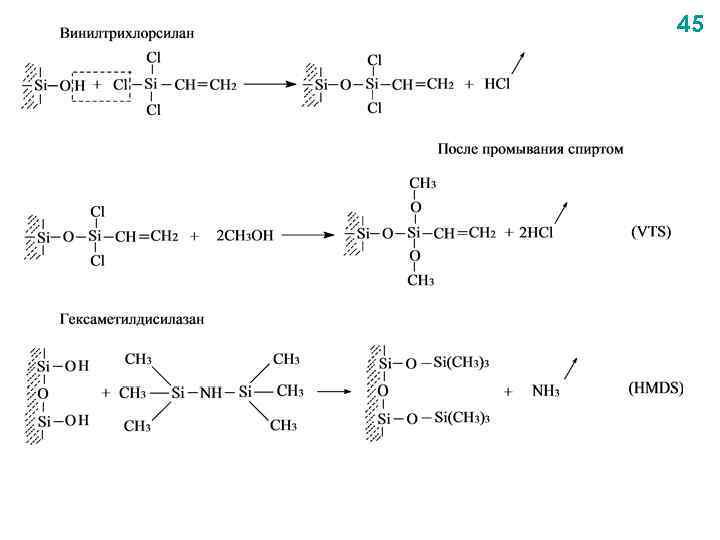
45
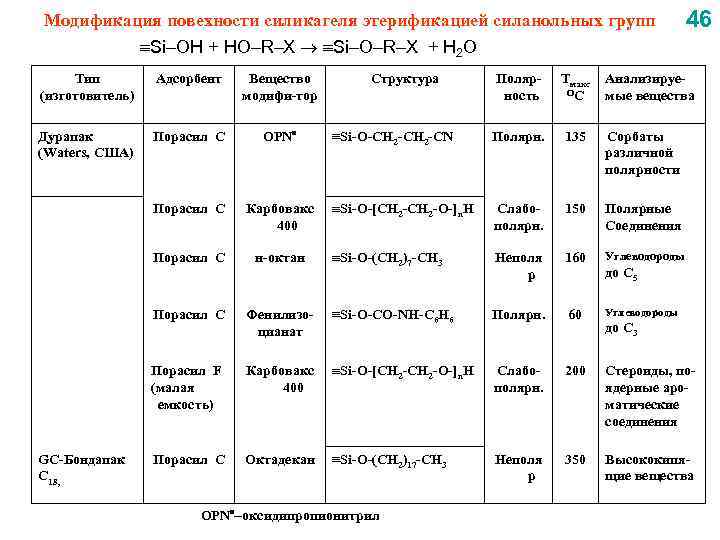
Модификация повехности силикагеля этерификацией силанольных групп Si OH + HO R X Si O R X + H 2 О Тип (изготовитель) Адсорбент Вещество модифи-тор Дурапак (Waters, США) Порасил С OPN Порасил С Карбовакс 400 Порасил С н-октан Порасил С Полярность Тмакс ОС Si-O-CH 2 -CN Полярн. 135 Сорбаты различной полярности Si-O-[CH 2 -O-]n. H Слабополярн. 150 Полярные Соединения Si-O-(CH 2)7 -CH 3 Неполя р 160 Углеводороды Фенилизоцианат Si-O-CO-NH-C 6 H 6 Полярн. 60 Углеводороды Порасил F (малая емкость) GC-Бондапак С 18, Структура 46 Карбовакс 400 Si-O-[CH 2 -O-]n. H Слабополярн. 200 Стероиды, поядерные ароматические соединения Порасил С Октадекан Si-O-(CH 2)17 -CH 3 Неполя р 350 Высококипящие вещества OPN оксидипропионитрил Анализируемые вещества до С 5 до С 3
Лекция 2. 2015.Теории.ppt