Teoreticheskie_osnovy_teplotekhniki_dlya_BVT.pptx
- Количество слайдов: 181

Теоретические основы теплотехники (техническая термодинамика и тепломассообмен)

Основная литература: Теплотехника : учебник для вузов / ред. А. П. Басков. 3 е изд. , перераб. и доп. М. : БАСТЕТ, 2010. 328 с. : ил. Библиогр. : с. 321. Дополнительная литература: Нащокин В. В. Техническая термодинамика и теплопередача: учеб. пособие для вузов; ред. В. С. Селецкий. М. : Высш. шк. , 1969. 560 с. Панкратов Г. П. Сборник задач по теплотехнике: Учеб. пособие для вузов. 3 е изд. , перераб. и доп. М. : Высш. шк. , 1995. 238 с.

1 ПРЕДМЕТ И МЕТОД ТЕРМОДИНАМИКИ

Термодинамика изучает законы превращения энергии в различных процессах, происходящих в макроскопических системах и сопровождающихся тепловыми эффектами. Макроскопической системой называется любой материальный объект, состоящий из большого числа частиц.

• Общая (физическая) термодинамика изучает превращение энергии в твердых, жидких и газовых телах, излучение различных тел, магнитные и электрические явления и т. д. • Кинетическая термодинамика изучает химические, тепловые процессы, равновесие и влияние на равновесие внешних условий. • Техническая термодинамика рассматривает закономерности взаимного превращения теплоты в работу (устанавливает взаимосвязь между тепловыми, механическими и химическими процессами, которые совершаются в тепловых и холодильных машинах, изучает процессы, происходящие в газах и парах, а также свойства этих тел при различных физических условиях)

1. 1 Основные определения термодинамики Термодинамической системой называется совокупность материальных тел, находящихся в тепловом, энергетическом и механическом взаимодействии. Выбор системы произволен и диктуется условиями решаемой задачи. Тела, не входящие в систему, называют окружающей средой. Систему отделяют от окружающей среды контрольной поверхностью (оболочкой). Для простейшей системы — газа, заключенного в цилиндре под поршнем, внешней средой является окружающий воздух, а контрольными повер хностями служат стенки цилиндра и поршень.

По способу передачи энергии и вещества между рассматриваемой системы и окружающей средой термодинамические системы классифицируются: открытая это система, которая обменивается и энергией, и веществом закрытая система в которой есть обмен только энергией изолированная это система в которой нет обмена с внешними телами ни энергией , ни веществом (в том числе и излучением )

Система, не имеющая теплообмена с окружающей средой, называется адиабатной. Система, имеющая во всех своих частях одинаковый состав и физические свойства, называется физически однородной. Однородная термодинамическая система, внутри которой отсутствуют поверхности раздела, называется гомогенной. Система, состоящая из нескольких макроскопических частей с различными физическими свойствами, отделённых одна от другой видимыми поверхностями раздела, называется гетерогенной.

Гомогенные части системы, отделенные от остальных частей видимыми поверхностями раздела, называются фазами. Компонентом термодинамической системы называют всякую химически однородную систему. Определенное сочетание свойств термодинамической системы называется состоянием системы. Параметр состояния системы это такой её показатель, изменение которого приводит к изменению состояния системы. Совокупность изменений состояния термодинамической системы при переходе из одного состояния в другое называется термодинамическим процессом.

Если все термодинамические параметры постоянны во времени и одинаковы во всех точках системы, то такое состояние системы называется равно весным. Если между различными точками в системе существуют разности темпера тур, давлений и других параметров, то она является неравновесной. Изолированная система с течением времени всегда приходит в состояние равновесия и никогда самопроизвольно выйти из него не может. В классической термодинамике рассматриваются только равновесные системы.
Газы очень далеки от начала конденсации размеры молекул исчезающе малы по сравнению с расстоянием между ними силы взаимного ничтожны притяжения Идеальные газы: силы молекулярного притяжения вообще отсутствуют, а сами молекулы представляют собой материальные точки, объем которых равен нулю.

Пары легко превращаются в жидкость учетом сил взаимного притяжения молекул конечность объема молекул Реальные газы В дальнейшем для простоты рабочее тело часто именуется газом. Если речь идет не о специфических особенностях идеальных газов, то под этим термином подразумеваются газы реальные.
1. 2 Основные параметры состояния рабочего тела В зависимости от внешних условий один и тот же газ может находиться в различных состояниях Каждое из таких состояний может быть охарактеризовано конкретными значениями ряда макроскопических (т. е. относящихся ко всему газу в целом) величин, называемых термодинамическими параметрами Это означает, что каждому состоянию газа соответствует одно и только одно значение каждого из термодинамических параметров. Совокупность трех параметров ( удельный объем, давление и температура) характеризует тепловое состояние тела, поэтому их называют термическими параметрами.

Удельным объемом газа, обозначаемым буквой υ, м³/кг, называется объем, занимаемый 1 кг данного газа. Так, если масса всего газа равна М кг, а полный объем V м³, то удельный объем его составляет: Величина, обратная удельному объему, т. е. масса газа, заключенная в 1 м³ его, называется плотностью и обозначается буквой ρ, кг/м³. Очевидно, что

Абсолютное давление газа является средним результатом ударов молекул о поверхность, ограничивающую объем, занимаемый газом. Оно представляет собой силу, отнесенную к единице площади этой поверхности и действующую со стороны газа в направлении, нормальном по отношению к ней. Поэтому в системе СИ основной единицей давления является 1 Н/м². Другие внесистемные единицы: 1 бар= Па (физ) 1 атм=760 мм рт. ст. =101325 Па (техн) 1 ат = 1 кг/см²=98066, 5 Па

Давление земной атмосферы зависит от высоты и метеорологических условий в данный момент. В среднем над уровнем моря оно равно 760 мм рт. ст. Эта величина называется нормальным давлением. Термодинамическим параметром состояния является только абсолютное давление. Если абсолютное давление газа в сосуде больше атмосферного, то разность между ними называется избыточным давлением. Если же абсолютное давление газа меньше атмосферного, то разность между ними называется разрежением или вакуумом.

Абсолютная температура газа интенсивности хаотического движения измеряется в градусах. является мерой его молекул и где k — постоянная Больцмана, равная 1, 380662∙ Дж/К, m – масса одной молекулы, ω – средняя квадратичная скорость поступательного движения молекул. Приведенное выражение показывает, что абсолютная температура всегда положительна, а нулевое значение ее соответствует состоянию полного покоя молекул.

Шкала, в которой температура отсчитывается от этого состояния, называется шкалой Кельвина Т, К. В технике же принята международная стоградусная шкала (шкала Цельсия), в которой отсчет ведется от состояния тающего льда при нормальном давлении (соответствующая абсолютной температуре Т=273, 15 К) t, °С. Величина градуса в обеих шкалах одинакова, поэтому пересчет с одной шкалы в другую производится по формуле:
Параметры состояния Интенсивные параметры состояния, не зависящие от массы системы (давление, температура и др. ) Экстенсивные (аддитивные) параметры, значения которых пропорциональны массе системы (объем, энергия)

1. 3 Термическое уравнение состояния рабочего тела Термические параметры p, v, T связаны между собой однозначной зависимостью, которая аналитически выражается в общем виде уравнением которое называется термическим уравнением состояния. Выражая каждый из термических параметров как явную функцию двух остальных, данное уравнение можно предоставить в одной из следующих формул: Термодинамическое состояние газа можно считать известным, если заданы значения двух его параметров, поскольку третий параметр может быть вычислен из уравнения состояния.
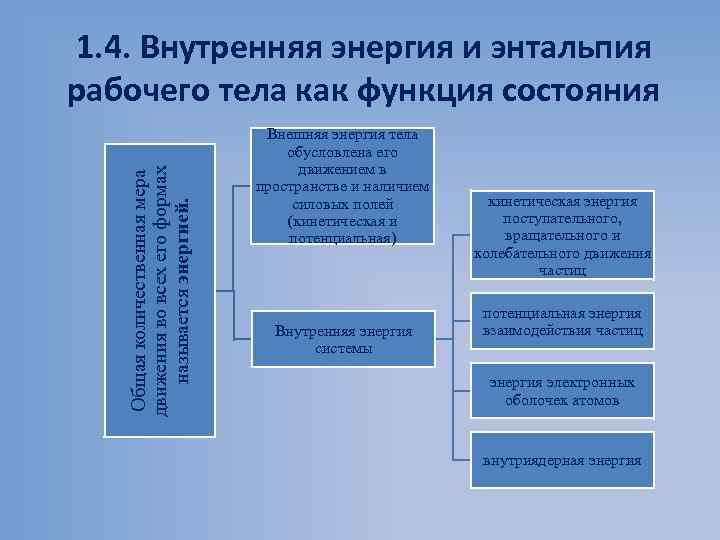
Общая количественная мера движения во всех его формах называется энергией. 1. 4. Внутренняя энергия и энтальпия рабочего тела как функция состояния Внешняя энергия тела обусловлена его движением в пространстве и наличием силовых полей (кинетическая и потенциальная) Внутренняя энергия системы кинетическая энергия поступательного, вращательного и колебательного движения частиц потенциальная энергия взаимодействия частиц энергия электронных оболочек атомов внутриядерная энергия

Внутренняя энергия U является свойством газа, т. е. зависит от его массы. экстенсивным Внутреннюю энергию газа обычно относят к единице массы (1 кг), Дж/кг. Таким образом, если масса рассматриваемого газа равна М кг, то Изменение внутренней энергии в каком либо процессе не зависит от характера процесса, а однозначно определяется заданными начальным и конечным состояниями газа.
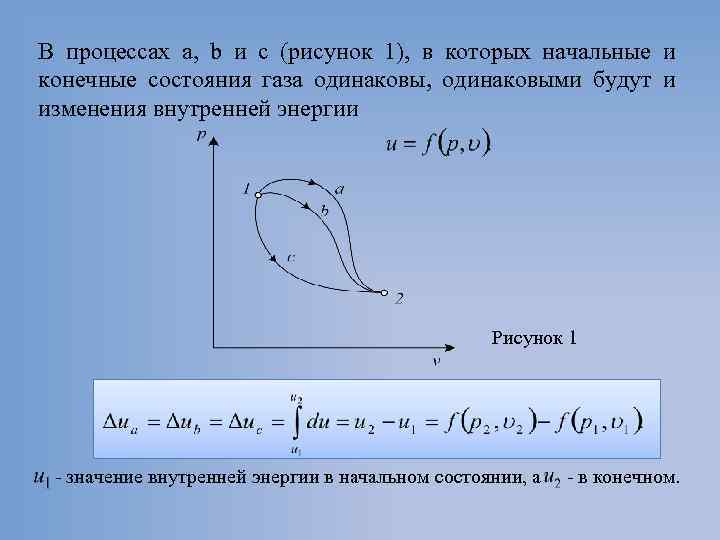
В процессах а, b и с (рисунок 1), в которых начальные и конечные состояния газа одинаковы, одинаковыми будут и изменения внутренней энергии Рисунок 1 значение внутренней энергии в начальном состоянии, а в конечном.

Бесконечно малое изменение внутренней энергии du есть полный дифференциал u; если выразить внутреннюю энергию в виде функции удельного объема и температуры, то Внутренняя энергия идеального газа, в котором отсутствуют силы взаимодействия между молекулами, не зависит от объема газа или давления , а определяется только его температурой, поэтому производная от внутренней энергии идеального газа по температуре есть полная производная: Для задач технической термодинамики важно не абсолютное значение внут ренней энергии, а ее изменение в различных термодинамических процессах.

Сумма внутренней энергии системы U и произведения давления системы р на ее объем V называется энтальпией обозначается Н: Так как входящие в нее величины являются функциями состояния, то и сама энтальпия является функцией состояния. Энтальпия обладает свойством аддитивности. Величина называемая удельной энтальпией (h = H/M), представляет собой энтальпию системы, содержащей 1 кг вещества. Поскольку энтальпия есть функция состояния, то она может быть представлена в виде функции двух любых параметров состояния: ; ; , а величина dh является полным дифференциалом. Изменение энтальпии в любом процессе определяется только начальным и конечным состояниями тела и не зависит от характера процесса.

Физический смысл энтальпии выясним на следующем примере: Рисунок 2 Энергия этой системы складывается из внутренней энергии газа и потенциальной энергии поршня с грузом в поле внешних сил: В условиях равновесия (G = p. F) эту функцию можно выразить через параметры газа: Получаем, что E=H, т. е. энтальпию можно трактовать как энергию расширенной системы.

Уравнение в случае, когда единственным видом работы является работа расширения, с учетом очевидного соотношения может быть записано в виде или Из этого соотношения следует, что если давление системы сохраняется неизменным, т. е. осуществляется изобарный процесс (dp=0), то и т. е. теплота, подведенная к системе при постоянном давлении, идет только на изменение энтальпии данной системы.

Для идеального газа получим Так как между энтальпией и внутренней энергией существует связь выбор начала отсчета одной из них не произволен: в точке, принятой за начало отсчета внутренней энергии, h = pv. При расчетах практический интерес представляет изменение энтальпии в конечном процессе:
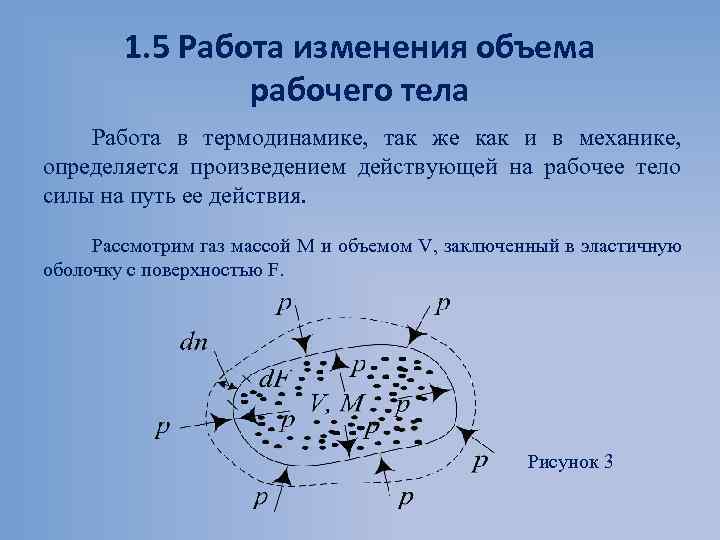
1. 5 Работа изменения объема рабочего тела Работа в термодинамике, так же как и в механике, определяется произведением действующей на рабочее тело силы на путь ее действия. Рассмотрим газ массой М и объемом V, заключенный в эластичную оболочку с поверхностью F. Рисунок 3

Общая работа, совершенная в течение бесконечно малого процесса: Из рисунка видно, что изменение объема d. V выражается в виде интеграла по поверхности: следовательно При конечном изменении объема работа против сил внешнего давления, называемая работой расширения, равна

Следует, что δL и d. V всегда имеют одинаковые знаки: • если d. V>0, то и δL>0, т. е. при расширении работа тела положительна, при этом тело само совершает работу; • если же d. V<0, то и δL<0, т. е. при сжатии работа тела отрицательна: это означает, что не тело совершает работу, а на его сжатие затрачивается работа извне. Отнеся работу расширения к 1 кг массы рабочего тела, получим l = L/M; Величина, представляющая собой удельную работу, совершаемую системой, содержащей 1 кг газа, равна Формулы справедливы только для равновесных процессов, при которых давление рабочего тела равно давлению окружающей среды.
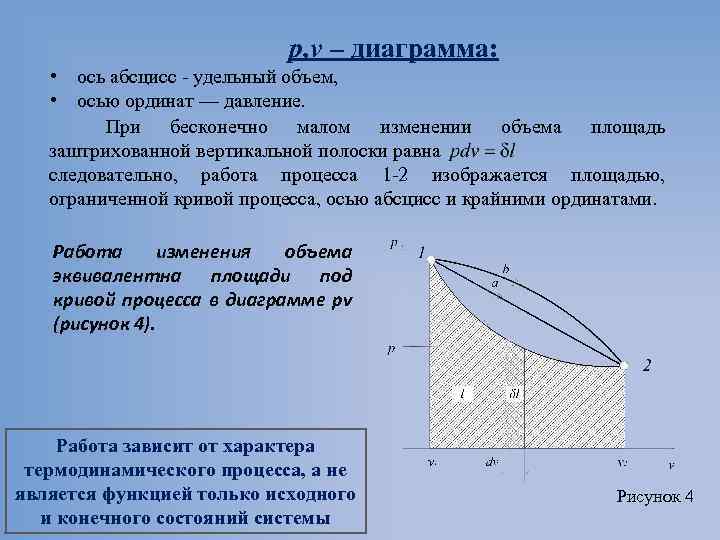
р, v – диаграмма: • ось абсцисс удельный объем, • осью ординат — давление. При бесконечно малом изменении объема площадь заштрихованной вертикальной полоски равна следовательно, работа процесса 1 2 изображается площадью, ограниченной кривой процесса, осью абсцисс и крайними ординатами. Работа изменения объема эквивалентна площади под кривой процесса в диаграмме рv (рисунок 4). Работа зависит от характера термодинамического процесса, а не является функцией только исходного и конечного состояний системы Рисунок 4

1. 6 Теплота Мерой количест ваэнергии, переданной микрофизиче ским путем, служит теплота. Теплота может передаваться либо при непосредственном контакте между телами (теплопроводностью, конвекцией), либо на расстоянии (излучением), причем во всех случаях этот процесс возможен только при наличии разности температур между телами.

ü Внутренняя энергия — это свойство самой системы, она характеризует состояние системы. ü Теплота и работа — это энергетические характеристики процессов механического и теплового взаимодействий системы с окружающей средой. Они характеризуют те количества энергии, которые переданы системе или отданы ею через ее границы в определенном процессе.

1. 7 Первый закон термодинамики Пусть некоторому рабочему телу с объемом V и массой М, имеющему температуру Т и давление р, сообщается извне бесконечно малое количество теплоты. В результате подвода теплоты тело нагревается на d. T и увеличивается в объеме на d. V. Рисунок 5

Ø Повышение температуры тела свидетельствует об увеличении кинетической энергии его частиц. Ø Увеличение объема тела приводит к изменению потенциальной энергии частиц. Ø В результате внутренняя энергия тела увеличивается на d. U. Ø Поскольку рабочее тело окружено средой, которая оказывает на него давление, то при расширении оно производит механическую работу против сил внешнего давления. Так как никаких других изменений в системе не происходит, то по закону сохранения энергии т. е. теплота, сообщаемая системе, идет на приращение ее внутренней энергии и на совершение внешней работы. Полученное уравнение является математическим выражением первого закона термодинамики.

Каждый из трех членов этого соотношения может быть положительным, отрицательным или равным нулю. Частные случаи: 1. теплообмен системы с окружающей средой отсутствует, т. е. теплота к системе не подводится и от нее не отводится. Процесс без теплообмена называется адиабатным. 2. при этом объем тела не изменяется, d. V=0. Такой процесс называется изохорным, для него 3. d. U=0 внутренняя энергия системы не изменяется

Для системы, содержащей 1 кг рабочего тела Выражение первого закона термодинамики в интегральной форме: Формулировки I закона термодинамики: 1. Энергия изолированной термодинамической системы остается неизменной, независимо от того, какие процессы в ней протекают. 2. Невозможно построить вечный двигатель I го рода, т. е. такую периодически действующую систему, которая совершала бы работу без затраты энергии.

2 ОСНОВНЫЕ ЗАКОНЫ ИДЕАЛЬНЫХ ГАЗОВ

2. 1 Уравнение состояния идеальных газов Идеальным называется газ, в котором собственный объем молекул принимается равным нулю, и отсутствуют силы межмолекулярного взаимодействия. Основное уравнение кинетической теории газов, или уравнение Клаузиуса: где р – давление газа; n – число молекул; m – масса молекул; ω – средняя скорость молекул.

Обозначив число молекул в одном килограмме газа через z, имеем и тогда Для двух произвольных состояний газа газовая постоянная Термическое уравнение состояния идеального газа или уравнение Клапейрона: Уравнение идеального газа: состояния произвольного количества

2. 2 Основные законы идеальных газов Закон Шарля: Процесс изохорный Закон Гей. Люссака: p 1 = p 2 Процесс изобарный Закон Бойля. Мариотта: T 1 = T 2 Процесс изотермический

n 1 = n 2 Разные газы, находящиеся при одинаковых давлениях и температурах и занимающие одинаковые объемы, содержат одинаковое число молекул. Это положение называется законом Авогадро. где μ – молекулярная масса газа. Объем киломоля такое количество газа, масса которого, выраженная в килограммах, численно равна его молекулярной массе. При нормальных условиях (р0 = 760 мм рт. ст =10133 Н/м 2 и t 0 = 0 0 C) объем киломоля любого газа равен 22, 4 м 3.

Масса одного киломоля газа равна μ кг. Поэтому удельный объем и плотность любого идеального газа при нормальных условиях: Естественно, что сказанное в полной мере относится лишь к идеальным газам.

Объем киломоля в произвольном состоянии газа – , масса его постоянна и в любом состоянии μ кг/кмоль, то уравнение состояния для одного киломоля идеального газа: Величина μR представляет собой газовую постоянную одного киломоля , Дж/(кмоль·K). Она не зависит от природы газа, т. е. для всех газов имеет одинаковое значение. Называется она универсальной газовой постоянной. Уравнение состояния для одного киломоля, написанного для нормальных условий: Газовая постоянная 1 кг любого газа

2. 3 Смеси идеальных газов Газовые смеси механическая смесь отдельных компонентов различных газов, химически не реагирующих между собой Закон Дальтона: полное давление смеси идеальных газов равно сумме парциальных давлений всех входящих в нее компонентов: Парциальное давление pi — давление, которое имел бы газ, если бы он один при той же температуре занимал весь объем смеси.

СПОСОБЫ ЗАДАНИЯ ГАЗОВЫХ СМЕСЕЙ Способы задания состава газовой смеси В абсолютных величинах В относительных величинах Массовые части Мi (кг) Массовые доли gi Объемные части Vi (м 3) Объемные доли ri Мольные части Ni (моль) Мольные доли ni

Массовой долей называется отношение массы отдельного компонента Мi, к массе смеси Мcм: Объемная доля представляет собой отношение приведенного объема газа Vi, к полному объему смеси Vсм: Приведенным называется объем, который занимал бы компонент газа, ес либы его давление и температура равня лисьдавлению и температуре смеси. Первое уравнение относится к состоянию компонента газа в смеси, когда он имеет парциальное давление pi и занимает полный объем смеси, а второе уравнение — к приведенному состоянию, когда давление и температура компонента равны, как и для смеси, р и Т

Мольной долей называется отношение количества молей Ni рассматриваемого компонента к общему количеству молей смеси Nсм Приве денный объем любого компонента может быть вычислен как произведение объема моля на число молей этого компо нента а объем смеси — тогда Задание смесильных газов мольными долями равно заданию ее объемными долями.

Газовая постоянная смеси газов

Кажущаяся молекулярная масса смеси

Соотношение между объемными и массовыми долями

3 ТЕПЛОЕМКОСТЬ ИДЕАЛЬНЫХ ГАЗОВ

3. 1 Основные определения Теплоемкостью тела в каком либо процессе изменения его состояния называется количество теплоты, потребное для повышения его температуры на один градус. Теплоемкость, отнесенная к единице количества вещества удельная теплоемкость (обычно ее называют просто теплоемкостью). Различают: ü массовую теплоемкость с, к. Дж/(кг·K), ü объемную теплоемкость с’, к. Дж/(м 3⋅K), ü мольную теплоемкость , к. Дж/(кмоль⋅K). где v 0 – удельный объем при нормальных условиях.

Однозначную связь между теплотой процесса и температурой газа, которую можно выразить уравнением q = f (T) , или представить графически в виде некоторой кривой. На различных участках такой кривой одному и тому же изменению температуры соответствуют различные количества подведенной теплоты, поэтому и значения теплоемкости на этих участках будут различными. Вводится понятие о теплоемкости, средней в заданном интервале температур от Т 1 до Т 2 (т. е. на участке 1 -2 кривой): Рисунок 6

Беспредельно уменьшая рассматриваемый температурный интервал, получаем истинную теплоемкость при заданной температуре: Характер процесса может быть задан постоянством какого либо из параметров газа в нем, x = const. В этом случае теплоемкость газа представляет собой частную производную:

3. 2 Теплоемкости сv и ср при постоянном объеме при постоянном давлении

Связь между ними устанавливается из первого закона термодинамики: Если теплота подводится при постоянном объеме, то dv = 0, Если теплота давлении, то подводится при постоянном

Для идеального газа pv = RT уравнение Майера

Умножая обе части уравнения Майера на молекулярную массу μ, получаем аналогичную зависимость для мольных теплоемкостей идеального газа

3. 3 Молекулярно-кинетическая теория теплоемкости Внутренняя энергия одного киломоля: Материальная точка имеет три степени свободы, следовательно, на каждую из них в одном киломоле газа приходится внутренняя энергия, равная

Если молекула состоит из двух или более атомов, то число степеней свободы ее составляют причем для двухатомных газов: для трехатомных газов: Внутренняя энергия одного киломоля газа:

Если газ нагревается при постоянном объеме, то он работы не совершает, а потому, согласно первому закону термодинамики, вся затраченная теплота расходуется на изменение внутренней энергии Формулы показывают, что согласно молекулярно кинетической теории газов теплоемкости их в процессах с постоянным объемом и с постоянным давлением являются величинами постоянными.

3. 4 Зависимость теплоемкости от температуры Колебательная составляющая теплоемкости может быть получена с помощью квантовой теории, формулы Эйнштейна: где vкол – число степеней свободы внутримолекулярных колебаний; θ – характеристическая температура внутримолекулярного колебательного движения, прямо пропорциональная частоте внутримолекулярных колебаний; е – основание натуральных логарифмов.

Рисунок 7 Зависимость теплоемкости от температуры у двух, трех и многоатомных газов Истинную теплоемкость можно считать производной теплоты по температуре

Рисунок 7 Зависимость теплоемкости от температуры у двух, трех и многоатомных газов Учитывая, что на оси ординат t = 0

3. 5 Теплоемкость газовых смесей Если смесь задана массовым составом, то ее массовая теплоемкость , к. Дж/(кг·K) В этом случае объемная теплоемкость , к. Дж/(м 3·K) Если же газовая смесь задана объемным составом, то проще сначала определить ее объемную теплоемкость к. Дж/(кг⋅K). В этом случае массовая теплоемкость Если смесь задана мольным составом, то принимаются те же формулы, что и при задании ее объемным составом, т. к. мольные доли компонентов смеси численно равны их объемным долям.

4 ТЕРМОДИНАМИЧЕСКИЕ ПРОЦЕССЫ ИДЕАЛЬНЫХ ГАЗОВ

Основные процессы: • изохорный, протекающий при постоянном объеме; • изобарный, протекающий при посто янном давлении; • изотермический, происходящий при постоянной темпера туре; • адиабатный — процесс, при ко тором отсутствует теплообмен с окружа ющей средой, • политропный, удов летворяющий уравне нию

Общий план изучения: 1. Выводится уравнение процесса 2. Устанавливается зависимость между основными параметрами рабочего тела в начале и конце процесса

3. Определяются изменения основных функций состояния в процессе:

4. Определяется работа изменения объема газа lрасш и располагаемая работа lрасп’:

1 Изохорный процесс При изохорном процессе dv = 0 или v = const. Из уравнения состояния идеального газа следует, что p/T=R/v=const, т. е. давление газа прямо пропорционально его абсолютной температуре: Рисунок 8 Изображение изохорного процесса в р, v- и T, s координатах

• Работа расширения в этом процессе равна нулю, так как dv= 0. • Количество теплоты, подведенной к рабочему телу в процессе 1 -2 при : При переменной теплоемкости

• Так как 1= 0, то в соответствии с первым законом термодинамики • Изменение энтропии в изохорном процессе определяется по формуле
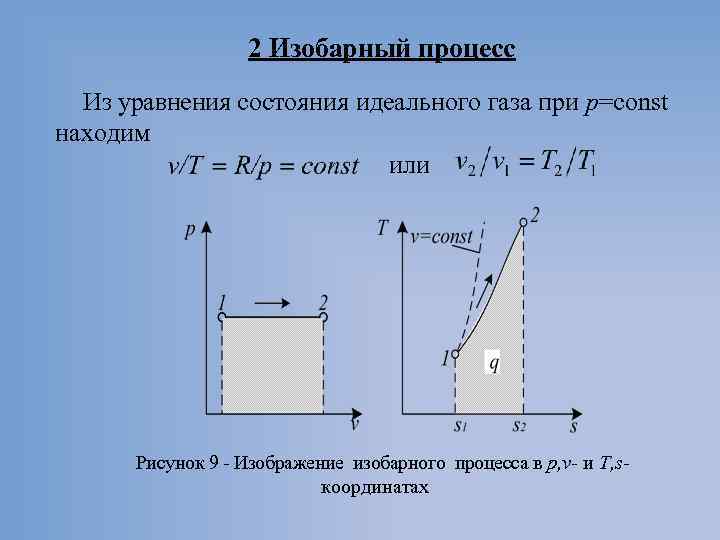
2 Изобарный процесс Из уравнения состояния идеального газа при р=const находим или Рисунок 9 Изображение изобарного процесса в p, v и T, s координатах

• Из выражения Так как следует, что и . , то одновременно • Количество теплоты, сообщаемое газу при нагревании (или отдаваемое им при охлаждении): при cp= const

• Изменение энтропии при ср = const согласно равно т. е. температурная зависимость энтро пии при изобарном процессе тоже имеет логарифмический характер, но поскольку ср>сv, то изобара в Т, s диаграмме идет более полого, чем изохора.
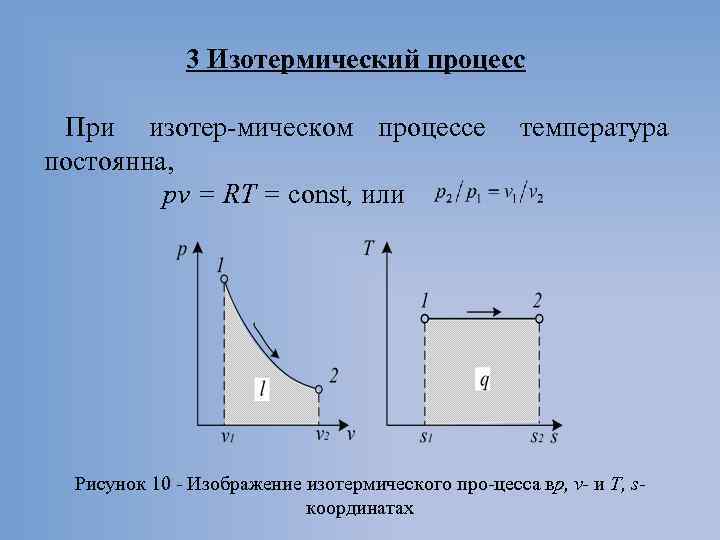
3 Изотермический процесс При изотер мическом процессе постоянна, pv = RT = const, или температура Рисунок 10 Изображение изотермического про цесса вр, v- и T, s координатах

• Работа процесса: • Так как температура не меняется, то внутренняя энергия идеального газа в данном процессе остается постоянной ( ) и вся подводимая к газу теплота полностью превра щается в работу расширения: • При изотермическом сжатии от газа отводится теплота в количестве, равном затраченной на сжатие работе. • Изменение энтропии:

4. Адиабатный процесс Процесс, происходящий без теплообмена с окружающей средой, называется адиабатным • Уравнения первого закона термодинамика для адиабатного процесса прини мают вид При условии, что k =cp/cv=const

После потенцирования имеем уравнение адиабаты идеального газа при постоянном отношении теплоемкостей показатель адиабаты Согласно классической кинетической теории теплоемкость газов не зависит от температуры, поэтому можно считать, что величина k также не зависит от температуры и определяется числом степеней свободы молекулы. Для одноатомного газа k=1, 66 для двухатомного k=1, 4, для трех и многоатомных газов k=l, 33.
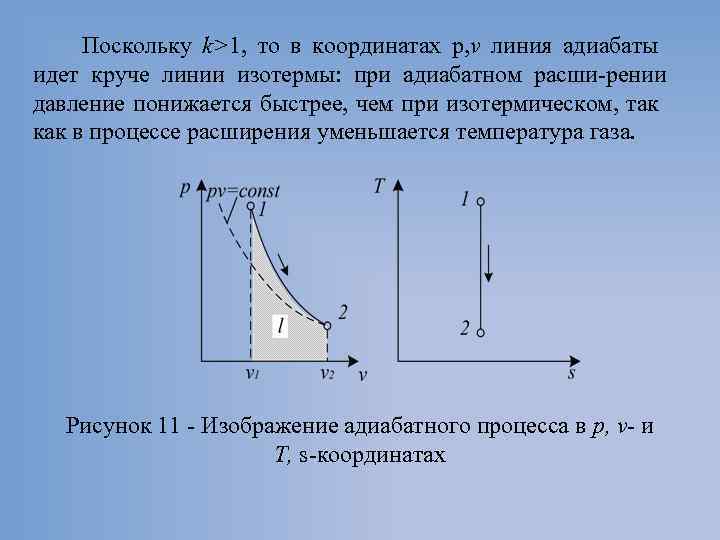
Поскольку k>1, то в координатах р, v линия адиабаты идет круче линии изотермы: при адиабатном расши рении давление понижается быстрее, чем при изотермическом, так как в процессе расширения уменьшается температура газа. Рисунок 11 Изображение адиабатного процесса в р, v- и Т, s координатах

Уравнение адиабатного процесса в форме, выражающей зависимость температуры от объема или давления: • Работа расширения при адиабатном процессе: Так как

• В данном процессе теплообмен газа с окружающей средой исключается, по этомуq=0. • Выражение показывает, что теплоемкость адиабатного процесса равна нулю. • Поскольку при адиабатном процессе энтропия рабочего тела не изме няется (ds=0 и s=const). Следовательно, на Т, s диаграмме адиабатный про цесс изображается вертикалью.

5. Политропный процесс и его обобщающее значение Любой произвольный процесс можно описать в р, v координатах (по крайней мере на небольшом участке) уравнением подбирая соответствующее значение п. Процесс, описываемый таким уравнением, называется политропным. Показатель политропы n может принимать любое численное значение в пределах от , но для данного процесса он является величиной постоянной.

Связь между р, v и Т в любых двух точках на политропе: • Работа расширения газа в политропном процессе имеет вид

• Количество подведенной (или отведенной) в процессе теплоты можно опре делить с помощью уравнения первого закона термодинамики:

представляет собой теплоемкость идеального газа в политропном процессе. При постоянных cv, k и п теплоемкость сn = const, поэтому политропный процесс иногда определяют как процесс с постоянной теплоемкостью. • Изменение энтропии
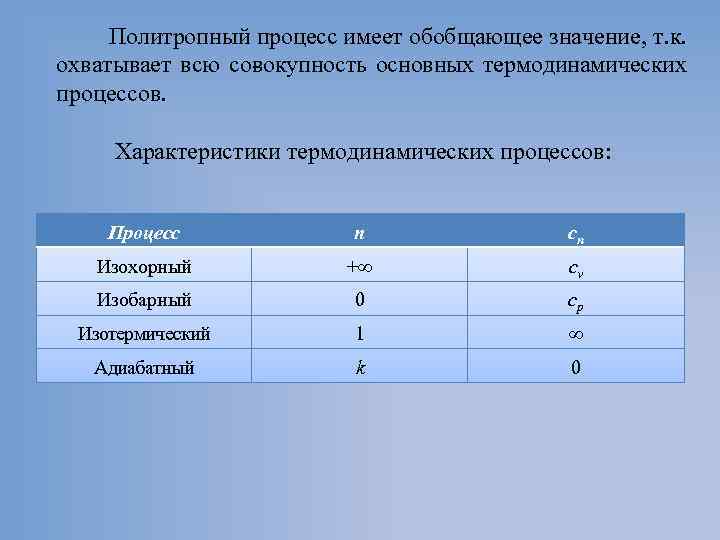
Политропный процесс имеет обобщающее значение, т. к. охватывает всю со окупность основных термодинамических в процессов. Характеристики термодинамических процессов: Процесс n cn Изохорный +∞ cv Изобарный 0 cp Изотермический 1 ∞ Адиабатный k 0
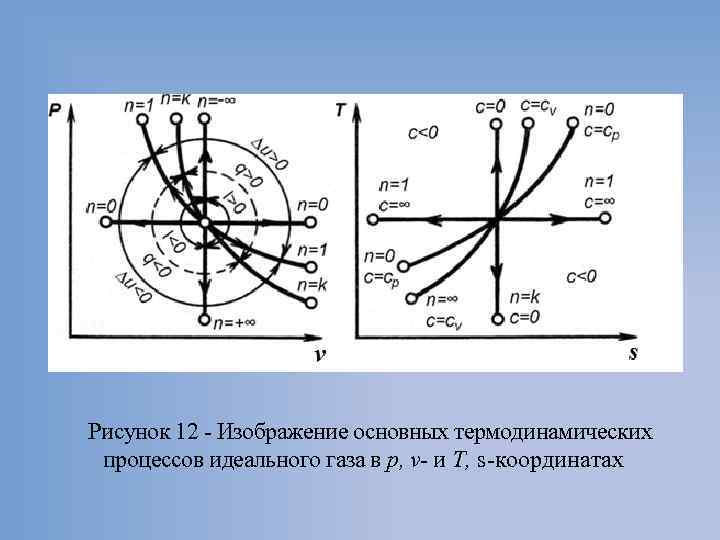
Рисунок 12 Изображение основных термодинамических процессов идеального газа в р, v- и Т, s координатах

5 ВТОРОЙ ЗАКОН ТЕРМОДИНАМИКИ

5. 1 Термодинамическая обратимость процессов Термодинамически обратимыми называются процессы изменения состояния рабочего тела, которые могут быть проведены в обратном направлении таким образом, что и само рабочее тело, и окружающая среда пройдут через те же промежуточные состояния, что и в прямом направлении, но лишь в обратной последовательности. В противном случае процессы термодинамически необратимыми. являются

Для того, чтобы процесс был обратимым, необходимо соблюсти два условия: • • процесс должен быть равновесным; разность температур при любом теплообмене между рабочим телом и внешним источником теплоты должна быть в каждый данный момент бесконечно малой. Если не соблюдено первое условие, то процесс является внутренне необратимым; если не соблюдено второе условие, то он является внешне необратимым.

5. 2 Обратимые циклы и оценка их эффективности В прямых циклах теплота превращается в работу, а в обратных – работа превращается в теплоту. Разность количеств тепла q 0 = q 1 – q 2 расходуется на совершение работы l 0 , равной площади, ограниченной линией цикла, по первому закону термодинамики q 0 = l 0. Рисунок 13 – Прямой цикл

Характеристикой эффективности прямых обратимых циклов является отношение, показывающее, какая доля всей затраченной на цикл теплоты превращается в работу: термический коэффициент полезного действия (КПД) данного цикла Превращение теплоты в работу не является процессом самопроизвольным и может быть осуществлено лишь при наличии компенсирующего процесса – передачи части затрачиваемого тепла из горячих в холодные теплоприемники без превращения в работу
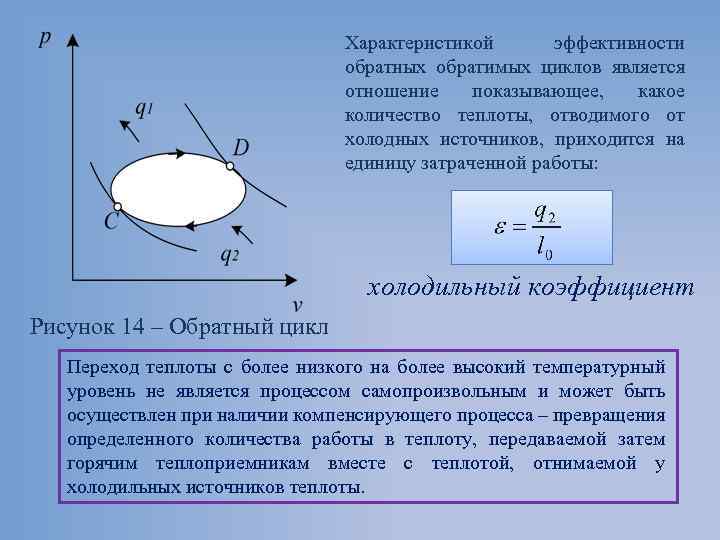
Характеристикой эффективности обратных обратимых циклов является отношение показывающее, какое количество теплоты, отводимого от холодных источников, приходится на единицу затраченной работы: холодильный коэффициент Рисунок 14 – Обратный цикл Переход теплоты с более низкого на более высокий температурный уровень не является процессом самопроизвольным и может быть осуществлен при наличии компенсирующего процесса – превращения определенного количества работы в теплоту, передаваемой затем горячим теплоприемникам вместе с теплотой, отнимаемой у холодильных источников теплоты.

5. 3 Основные формулировки второго закона термодинамики Р. Клаузиус в 1850 г. : Теплота не может переходить от холодного тела к более нагретому сама собой, даровым процессом (без компенсации). В. Томсон: Невозможно при помощи неодушевленного материального двигателя получить от какой либо массы вещества механическую работу путем охлаждения ее ниже самого холодного из окружающих предметов. М. Планк: невозможно построить периодически действующую машину, все действие которой сводилось бы к поднятию некоторого груза и охлаждению теплового источника. В. Ф. Оствальд дал наиболее лаконичную формулировку постулата Томсона: осуществление вечного двигателя второго рода невозможно.

Рисунок 15 Система, в которой теплота q 1, отнимаемая от верхнего источника c температурой Т 1, передается рабочему телу, совершающему обратимый цикл в двигателе А В результате этого производится полезная работа l 0 = q 1 – q 2, передаваемая машине В, а теплота q 2 сбрасывается в нижний источник. Обратный переход теплоты от холодного источника к горячему возможен лишь при наличии компенсирующего самопроизволь ного процесса превращения некоторого количества работы в теплоту.
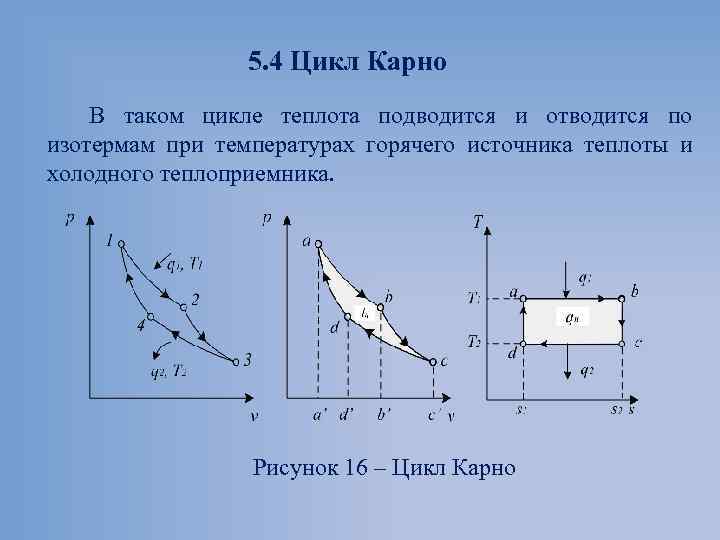
5. 4 Цикл Карно В таком цикле теплота подводится и отводится по изотермам при температурах горячего источника теплоты и холодного теплоприемника. Рисунок 16 – Цикл Карно

Считаем рабочее тело идеальным газом. или, учитывая, что под q 2 имеется в виду абсолютная величина отводимого тепла Для адиабаты 2 -3 Для адиабаты 1 -4
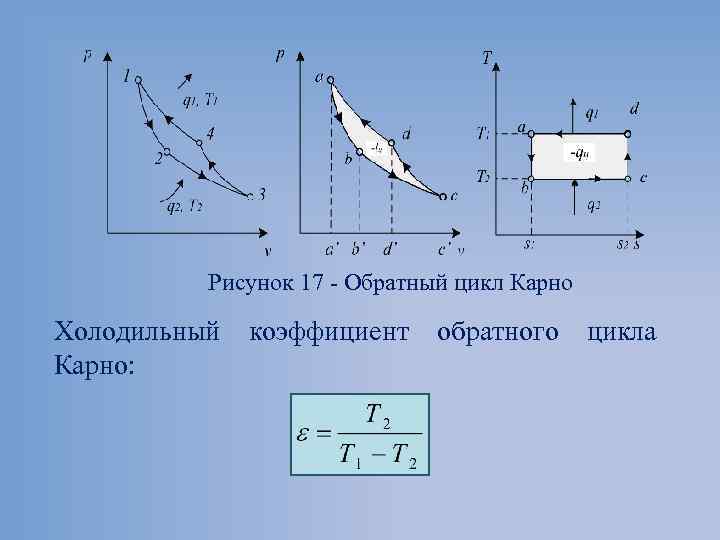
Рисунок 17 Обратный цикл Карно Холодильный Карно: коэффициент обратного цикла

5. 5 Теорема Карно Термический КПД обратимого цикла, осуществляемого между двумя источниками теплоты, не зависит от свойств рабочего тела, при помощи которого совершается этот цикл.

Рисунок 18– Система, в которой рабочее тело получает из холодного источника теплоту, отдает горячему источнику теплоту и совершает работу Термический КПД этого цикла будет равен:

Доказательство теоремы Карно получим «методом от противного» . Пусть обе машины работают одновременно, в машине А совершается обратный цикл, а в машине В – прямой. Подберем количество рабочих тел так, чтобы горячий источник отдавал рабочему телу машины В такое же количество теплоты, какое он получает от рабочего тела машины А, т. е. чтобы q 1′′ = q 1′ поскольку по предположению ηТ′′ > ηТ′.

В результате осуществления одновременно двух циклов совершается полезная работа Δl 0 = l 0′′ − l 0′. вытекает, что q 2′ > q 2′′ т. е. теплота, отнимаемая от холодного источника рабочим телом машины А, больше, чем теплота, отдаваемая ему рабочим телом машины В на величину Δq 2 = q 2′ − q 2′′. Единственным результатом одновременного осуществления двух циклов является совершение полезной работы Δl 0 за счет теплоты Δq 2 , отнимаемой у холодного источника. Предположение, что можно увеличить термический КПД обратного цикла, взяв другое рабочее тело, приводит к неправильным выводам. Это и является доказательством теоремы Карно.

5. 6 Энтропия Для прямого цикла Карно или q 2 абсолютная величина отводимого тепла. Алгебраически теплота q 2 отрицательна: или Отношение теплоты к температуре, при которой она подводится или отводится, называется приведенной теплотой. Для обратимого цикла Карно алгебраическая сумма теплот равна нулю.

Рисунок 19 Обратимый цикл интеграл Клаузиуса , 1854 г. где s – некоторая функция состояния, значение которой однозначно определяется состоянием тела и изменение которой зависит от начального и конечного состояний тела, но не от пути, по которому тело переходит от начального состояния к конечному.

Функция состояния S была названа Клаузиусом энтропией. Рисунок 20 – К определению энтропии В соответствии с равенством изменение ее в любом обратимом процессе является признаком наличия теплообмена между рабочим телом и окружающей средой.

Энтропию можно рассматривать как параметр состояния и изменение ее можно вычислить для любого процесса, если известно изменение двух других параметров состояния, например v и Т, р и Т или р и v. или уравнение состояния идеального газа в дифференциальной форме

В качестве независимых переменных заданы v и Т. На основании первого закона термодинамики

Если в качестве независимых переменных заданы р и Т

Если в качестве независимых переменных заданы v и р

При ро = 760 мм рт. ст и tо = 0 0 С энтропия S 0 = 0 Тогда при любых других условиях, параметрами р и Т, значение энтропии: заданных Энтропия имеет ту же размерность, что и массовая теплоемкость, т. е. к. Дж/(кг⋅K).

5. 7 TS диаграмма идеального газа Если изобразить процесс 1 2 в системе координат, в которой по оси абсцисс откладывается энтропия, а по оси ординат – абсолютная температура, то теплота всего процесса будет выражена в ней площадью, соответствующей данному интегралу TS диаграмма.
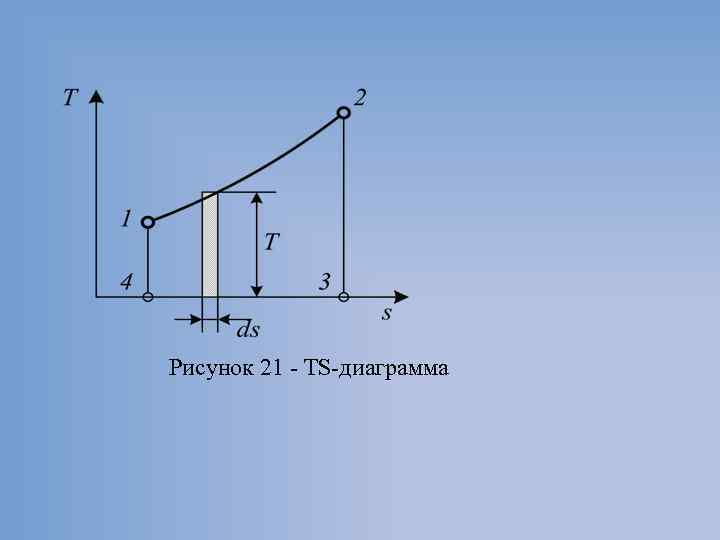
Рисунок 21 TS диаграмма

Процесс идет с подводом теплоты, то dq > 0 и ds > 0, (так как Т всегда положительна), т. е. энтропия рабочего тела возрастает, и линия процесса в TS диаграмме направлена слева направо. Процесс идет с отводом теплоты, то dq < 0 и ds < 0, т. е. энтропия рабочего тела уменьшается, и линия процесса направлена справа налево. Линии циклов на диаграмме образуют замкнутые контуры, причем линии прямых циклов направлены по часовой стрелке, а обратных – против часовой стрелки.
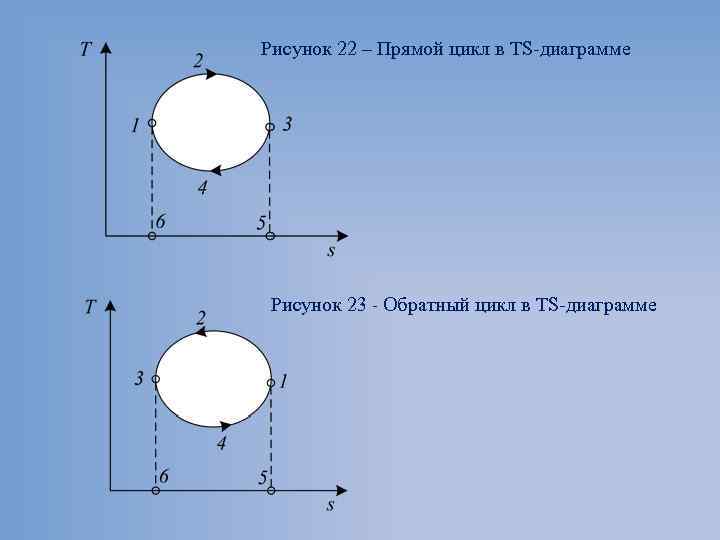
Рисунок 22 – Прямой цикл в TS диаграмме Рисунок 23 - Обратный цикл в TS диаграмме
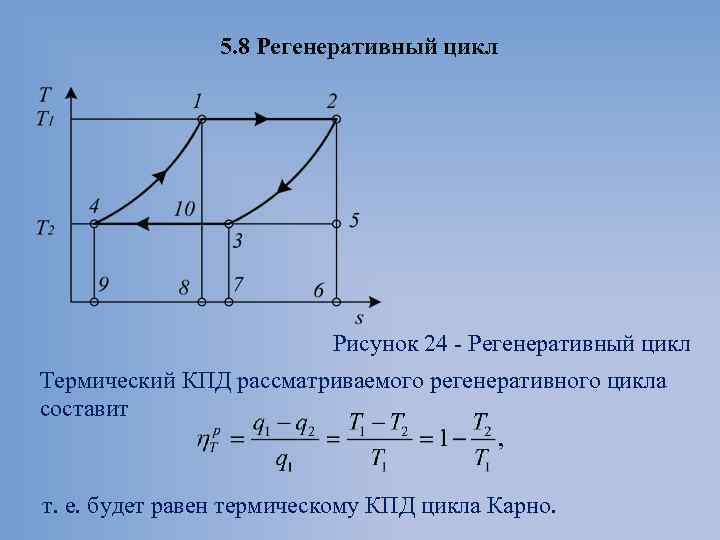
5. 8 Регенеративный цикл Рисунок 24 Регенеративный цикл Термический КПД рассматриваемого регенеративного цикла составит т. е. будет равен термическому КПД цикла Карно.

5. 9 Среднеинтегральная температура Среднеинтегральной температурой этого процесса называется отношение количества сообщаемой газу теплоты к приращению энтропии газа, т. е. Определение сохраняется и для процессов, происходящих с отводом теплоты, при которых как теплота, так и изменение энтропии отрицательны. В этом случае среднеинтегральная температура равна отношению количества отводимой от газа теплоты к уменьшению энтропии газа.
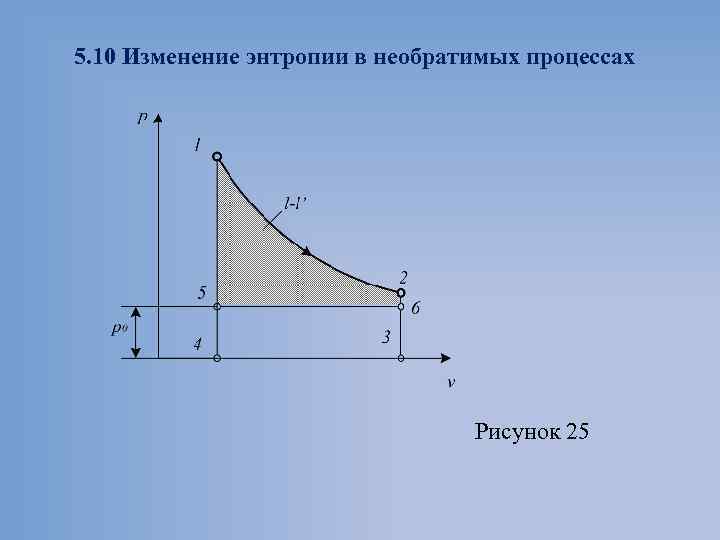
5. 10 Изменение энтропии в необратимых процессах Рисунок 25

Всякая необратимость процесса связана с потерей работы. Если процесс 1 2 обратим, то работа газа в нем Если этот процесс необратим из за того, что рокр = const и рокр = ро, а потому он протекает при конечной разности давлений, то работа его В данном случае величина представляет собой работу, необратимости процесса 1 2. потерянную вследствие

или Таким образом, в любом необратимом цикле интегральная сумма приведенных теплот, взятая по всему контуру цикла, отрицательна.
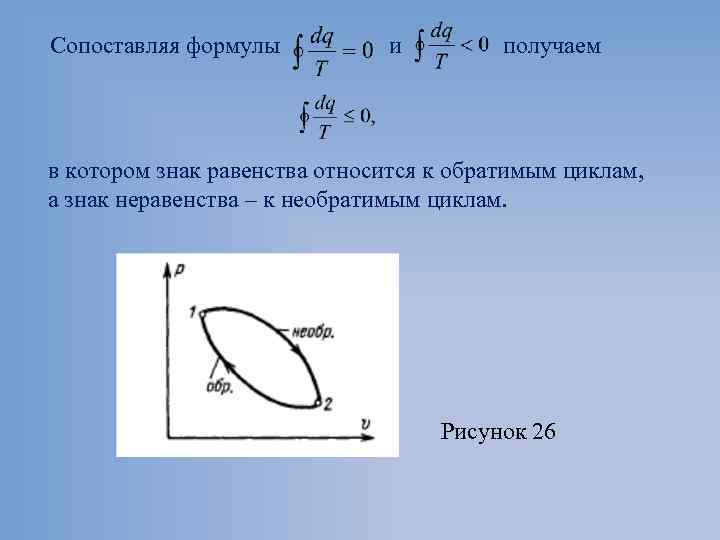
Сопоставляя формулы и получаем в котором знак равенства относится к обратимым циклам, а знак неравенства – к необратимым циклам. Рисунок 26

После осуществления необратимого процесса 1 2 рабочее тело возвращается в начальное состояние обратимым процессом 2 1. В результате будет осуществлен необратимый цикл, для которого , т. е.

Применительно к адиабатным необратимым процессам, для которых т. е. необратимые адиабатные процессы сопровождаются увеличением энтропии рабочего тела.
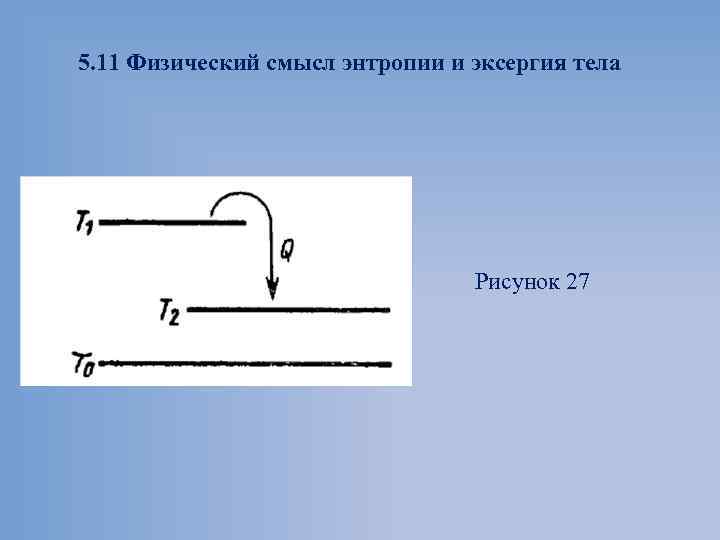
5. 11 Физический смысл энтропии и эксергия тела Рисунок 27

В результате процесса Знак минус нужен потому, что от первого тела отводится теплота, и его энтропия уменьшается, а под Q имеется в виду абсолютная величина передаваемой теплоты. Энтропия второго тела увеличивается Суммарное изменение энтропии системы, состоящей из двух тел, Энтропия системы увеличилась.

В интервале температур от Т 1 до Т 0 термический КПД цикла уравнение Гуи – Стодолы

Энтропия параметр состояния замкнутой системы, увеличение которого является количественной мерой потери работоспособности системы, имеющей место при протекании в ней необратимых процессов. Максимально возможная работа, которую можно получить за счет теплоты, если холодным приемником является окружающая среда, называется эксергией этой теплоты. Обозначается Е.

5. 12 Аналитическое выражение второго закона термодинамики Условия равновесия системы могут быть выражены аналитически условиями максимума ее энтропии Второй закон термодинамики устанавливает необратимость и одностороннюю направленность всех самопроизвольных процессов в неравновесных системах: энтропия неизолированной равновесной системы стремится к максимуму, достигая его, когда самопроизвольные процессы в ней прекращаются и система приходит в состояние равновесия.

Энтропия системы параметр, изменение которого отражает не только качественные, но и количественные ограничения, накладываемые на тепловые процессы вторым законом термодинамики. Аналитическое термодинамики: выражение второго закона знак равенства в системе необратимые процессы отсутствуют, знак неравенства наличие в ней необратимых процессов.

По первому закону термодинамики объединенное аналитическое выражение первого и второго закона термодинамики. Знак равенства относится к обратимым процессам, а знак неравенства – к необратимым.

5. 13 Статический характер второго закона термодинамики По Больцману самопроизвольные необратимые процессы являются проявлением того, что система стремится к переходу от менее вероятного неравновесного состояния к наиболее вероятному равновесному состоянию.

где Р – термодинамическая вероятность состояния системы, k – постоянная Больцмана, т. е. универсальная газовая постоянная, отнесенная к одной молекуле Установление связи между энтропией системы и вероятностью ее состояния позволило Больцману сформулировать второй закон термодинамики: природа стремится от состояний менее вероятных к состояниям более вероятным.

6 СВОЙСТВА РЕАЛЬНЫХ ГАЗОВ (самостоятельное изучение)

7 ПАРЫ И ВОДЯНОЙ ПАР

7. 1 Основные понятия Многие газообразные тела (с примесью одноименной жидкости в виде взвешенных мелкодисперсных частиц или без нее) принято называть парами. Все пары являются реальными газами и подчиняются всем присущим этим газам закономерностям, в частности закономерностям фазовых переходов. Образование пара из одноименной жидкости происходит посредством ее испарения или кипения. Испарение жидкости может происходить лишь с открытой поверхности. Наиболее подвижные молекулы жидкости, преодолевая действие сил молекулярного притяжения, отрываются от ее поверхности, переходят в свободное пространство и рассеиваются в нем Кипение жидкости может происходить и при отсутствии открытой поверхности. Т. к. генерация пара происходит в основном в объеме самой жидкости за счет испарения ее внутрь пузырьков пара.

Пар какого либо вещества, находящийся в динамическом равновесии с одноименной жидкостью, называется насыщенным паром. Рисунок 38 Жидкость в сосуде достаточно большого объема, верхняя часть которого первоначально заполнена сухим воздухом Температура, при которой давление насыщения становится равным внешнему давлению на жидкость, называется температурой кипения; она является функцией внешнего давления и с увеличением его возрастает.

ü Пар какого либо вещества, не содержащий в себе одноименной жидкости и имеющий температуру кипения при данном давлении, называется сухим насыщенным паром. ü Пар какого либо вещества, температура, которого превышает температуру кипения при данном давлении, называется перегретым паром.

Рисунок 39 Изобарный отвод теплоты от сухого насыщенного пара Насыщенный пар какого либо вещества, содержащий в себе одноименную жидкость в виде взвешенных в нем мелкодисперсных частиц, называется влажным паром.

Степень сухости влажного пара х массовая доля содержащегося в нем сухого насыщенного пара. Величина х может изменяться от единицы (что соответствует сухому насыщенному пару) до нуля (что соответствует кипящей воде), т. е. пределы возможных значений х выражаются формулой 0 ≤ х ≤ 1.

7. 2 Парообразование в pυ диаграмме Состояние влажного пара определяется значением независимых параметров: давление и степень сухости. Рисунок 40 двух Горизонтальная линия a-b-c-d процесс парообразования при постоянном давлении: • участок a-b соответствует подогреву жидкости от 0 °С до температуры кипения, • участок b-c – превращению кипящей воды в сухой насыщенный пар • участок с-d – перегреву пара до заданной температуры.
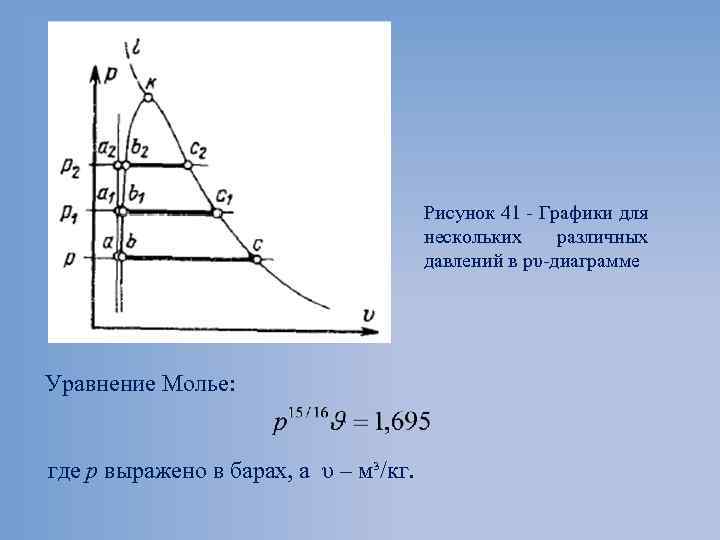
Рисунок 41 Графики для нескольких различных давлений в pυ диаграмме Уравнение Молье: где р выражено в барах, а υ – м³/кг.

• Линия b-b 1 -b 2, отделяющая область жидкости от области влажного пара и характеризуемая равенством х = 0, называется нижней пограничной кривой; • Линия c-c 1 -c 2, отделяющая область влажного пара от области перегретого пара и характеризуемая равенством х = 1, называется верхней пограничной кривой. Точка k соответствует некоторому предельному состоянию вещества, при котором исчезает видимое различие между жидкостью и паром. Критические параметры предельное состояние для воды, характеризующие

7. 3 Тройная точка. Правило фаз Отдельные части равновесной системы, находящиеся в различных агрегатных состояниях и отделенные друг от друга поверхностью раздела, называются фазами такой системы, а происходящий в ней переход из одного агрегатного состояния в другое называется фазовым превращением.

Рисунок 42 Фазовая диаграмма, в которой площадь, расположенная левее линии В А D соответствует твердой фазе, площадь, расположенная выше линии В А С, – жидкой фазе и площадь, расположенная правее линии С А D, – газовой фазе (перегретому пару). Точка А, соответствующая такому состоянию вещества, при котором оно может находиться во всех трех фазах, называется тройной точкой Для воды Тройная точка принята за начало отсчета внутренней энергии и энтропии воды и водяного пара

Равновесная система, в состав которой входят различные фазы одного и того же вещества, называется однокомпонентной (влажный пар при любых возможных параметрах, в том числе и при параметрах тройной точки) Если же в состав системы входят химически разнородные вещества, то она называется многокомпонентной (газовые смеси, водные растворы аммиака, различных солей, кислот и т. д. )

Число параметров, которые при переводе системы из одного состояния в другое можно изменять произвольно, называется числом степеней свободы этой системы. Однофазная однокомпонентная система обладает двумя степенями свободы, а двухфазная однокомпонентная система –одной. Правило фаз Гиббса: F=2+n−r, где F – число степеней свободы системы; n – число компонентов системы; r – число фаз в системе.

7. 4 Влажный пар и его параметры Рассматривая влажный пар как механическую смесь сухого насыщенного пара и жидкости той же температуры, т. е. температуры насыщения, его объем можно представить как сумму объемов указанных компонентов Здесь первое слагаемое представляет собой объем жидкости, содержащейся в 1 кг влажного пара, а второе – объем содержащегося в нем сухого насыщенного пара.

Для превращения 1 кг кипящей воды в сухой насыщенный пар при p = const ему необходимо сообщить определенное и различное для разных давлений количество теплоты, называемое теплотой парообразования Часть теплоты парообразования расходуется на увеличение внутренней энергии, связанное с совершением работы против сил взаимного притяжения молекул внутренняя теплота парообразования (ρ) Остальная часть теплоты парообразования расходует ся на работу расширения внешняя теплота парообразования
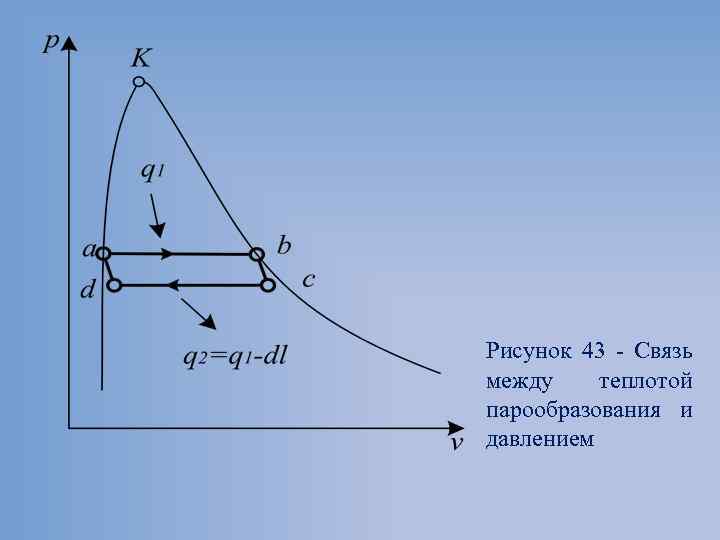
Рисунок 43 Связь между теплотой парообразования и давлением

Термический КПД цикла: уравнение Клапейрона – Клаузиуса
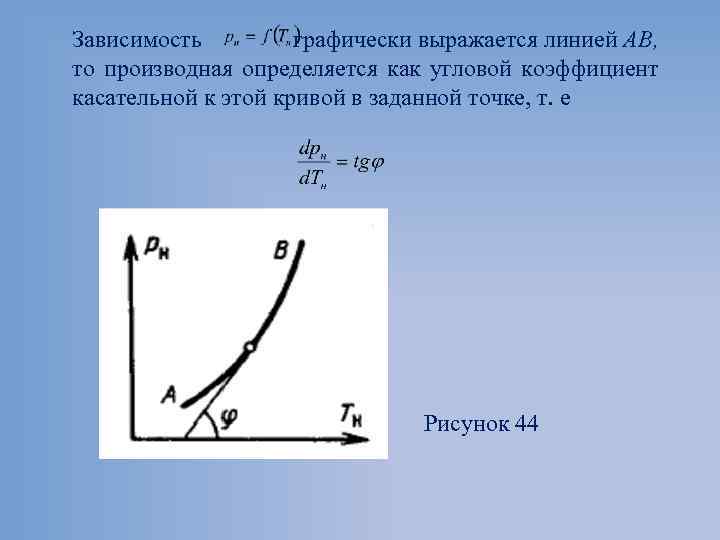
Зависимость графически выражается линией АВ, то производная определяется как угловой коэффициент касательной к этой кривой в заданной точке, т. е Рисунок 44

В процессе парообразования при p = const Энтропия влажного пара может быть определена по формуле где Тн – температура кипения при заданном постоянном давлении.

Для сухого насыщенного пара х = 1 Пользуясь приведенными формулами и зная степень сухости пара, можно определить все основные параметры и для влажного пара.

7. 5 TS диаграмма водяного пара Изменение энтропии воды в обратимом изобарном процессе Пусть изобары при любом давлении начинаются от температуры тройной точки ТА = Т 0, при которой энтропия равна s 0, уравнение изобары воды в TS диаграмме

Пусть для всех давлений sо = 0, В области жидкого состояния при невысоких давлениях можно считать cp = const
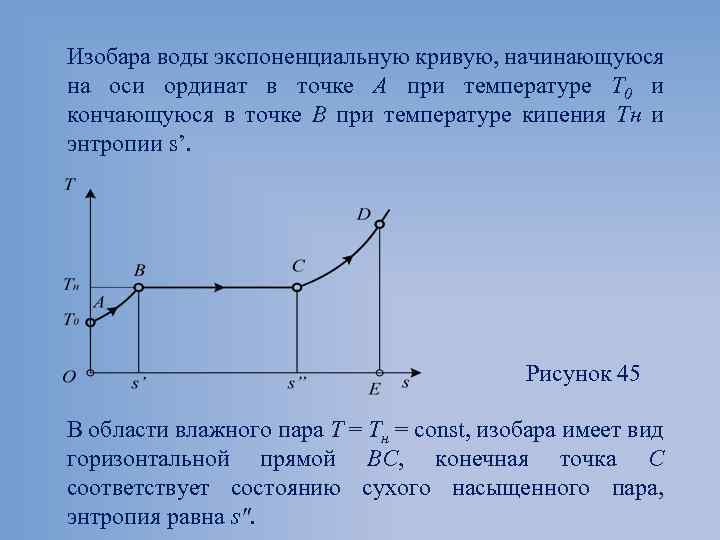
Изобара воды экспоненциальную кривую, начинающуюся на оси ординат в точке А при температуре Т 0 и кончающуюся в точке В при температуре кипения Тн и энтропии s’. Рисунок 45 В области влажного пара T = Тн = const, изобара имеет вид горизонтальной прямой ВС, конечная точка С соответствует состоянию сухого насыщенного пара, энтропия равна s".

В области перегретого пара где ср – истинная теплоемкость перегретого пара. В точке С изобара имеет излом (поскольку ср при переходе в область перегретого пара принимает конечное значение) и превращается в кривую СD. Крутизна этой кривой изменяется в зависимости от ср.

Из дифференциального соотношения следует, что угловой коэффициент касательной к изобаре перегретого пара
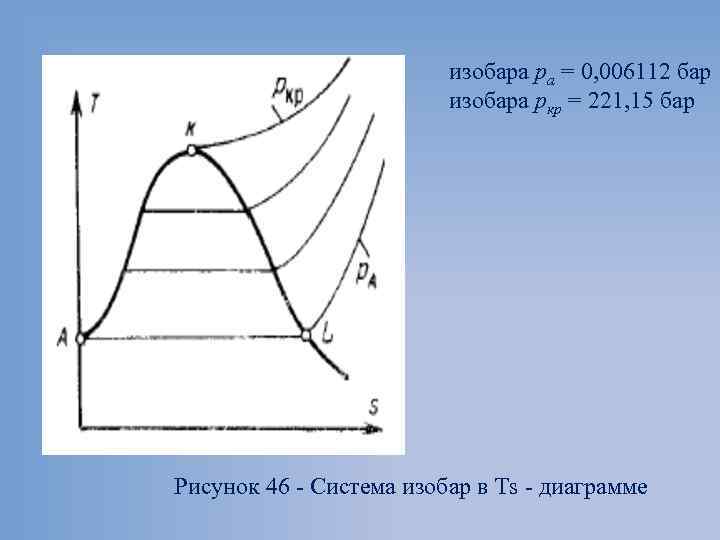
изобара ра = 0, 006112 бар изобара ркр = 221, 15 бар Рисунок 46 Система изобар в Ts диаграмме
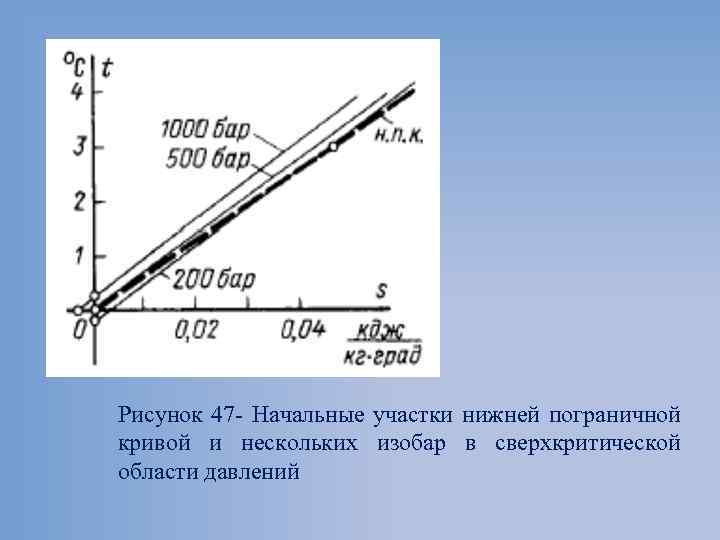
Рисунок 47 Начальные участки нижней пограничной кривой и нескольких изобар в сверхкритической области давлений
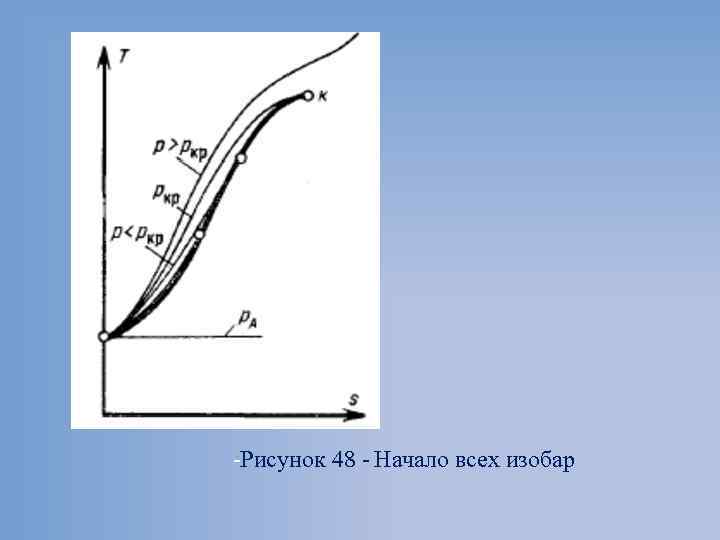
-Рисунок 48 - Начало всех изобар
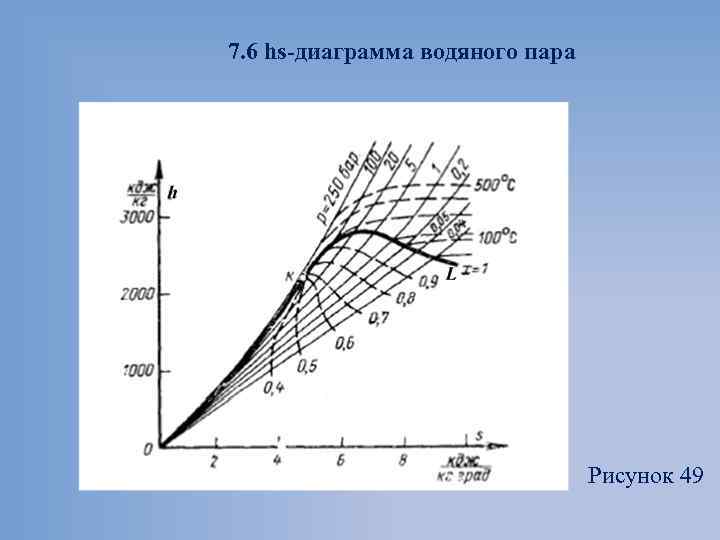
7. 6 hs диаграмма водяного пара Рисунок 49

Из уравнения при p = const В области влажного пара наносится система линий постоянной степени сухости (x = const). Каждая из этих линий делит все изобары влажного пара на пропорциональные отрезки

8 ВЛАЖНЫЙ ВОЗДУХ

8. 1 Основные определения ü Воздух, не содержащий водяного пара, называется сухим ü Если же в его состав входит водяной пар, то воздух называется влажным. Влажный воздух можно рассматривать как смесь сухого воздуха и водяного пара. Пар называется влажным, если он содержит мелкодисперсную жидкость, Влажный воздух содержит перегретый или в крайнем случае сухой насыщенный водяной пар.

Водяной пар, содержащийся во влажном воздухе, с достаточной точностью можно рассматривать как идеальный газ. Закон Дальтона, согласно которому давление влажного воздуха составляет где рв и рп – парциальные давления сухого воздуха и водяного пара в смеси. Содержание водяного пара во влажном воздухе может быть различным и характеризуется количеством пара в килограммах, приходящимся на 1 м 3 влажного воздуха. Эта величина называется абсолютной влажностью воздуха.
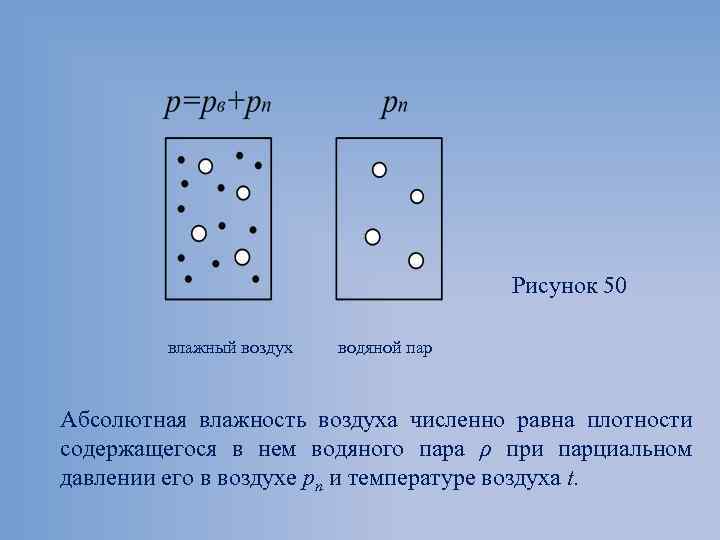
Рисунок 50 влажный воздух водяной пар Абсолютная влажность воздуха численно равна плотности содержащегося в нем водяного пара ρ при парциальном давлении его в воздухе рп и температуре воздуха t.
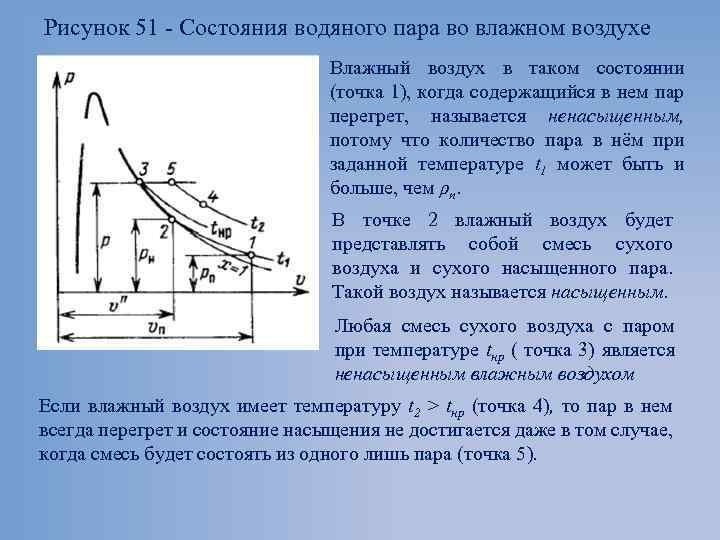
Рисунок 51 Состояния водяного пара во влажном воздухе Влажный воздух в таком состоянии (точка 1), когда содержащийся в нем пар перегрет, называется ненасыщенным, потому что количество пара в нём при заданной температуре t 1 может быть и больше, чем ρп. В точке 2 влажный воздух будет представлять собой смесь сухого воздуха и сухого насыщенного пара. Такой воздух называется насыщенным. Любая смесь сухого воздуха с паром при температуре tнр ( точка 3) является ненасыщенным влажным воздухом Если влажный воздух имеет температуру t 2 > tнр (точка 4), то пар в нем всегда перегрет и состояние насыщения не достигается даже в том случае, когда смесь будет состоять из одного лишь пара (точка 5).

Высшим пределом парциального давления пара во влажном воздухе при t < tнр является давление насыщения рн при данной температуре воздуха, а при t ≥ tнр этим пределом является само давление влажного воздуха р. Если воздух насыщен, то его абсолютная влажность зависит только от температуры и остается неизменной при любом давлении р > рн. Рисунок 52– Изотермически сжатый насыщенный влажный воздух

8. 2 Относительная влажность воздуха Отношение действительного содержания водяного пара во влажном воздухе к максимально возможному содержанию его в том же объеме влажного воздуха при данной температуре называется относительной влажностью При t ≤ tнр величина ρмакс представляет собой плотность сухого насыщенного пара при данной температуре, т. е. ρ ′′, а при t > tнр – плотность перегретого пара при данной температуре t и давлении смеси р.

Водяной пар во влажном воздухе подчиняется законам идеальных газов, и закону Бойля – Мариотта, согласно которым плотность газа изменяется прямо пропорционально его давлению. При t ≤ tнр а при t ≥ tнр где р – суммарное давление влажного воздуха.
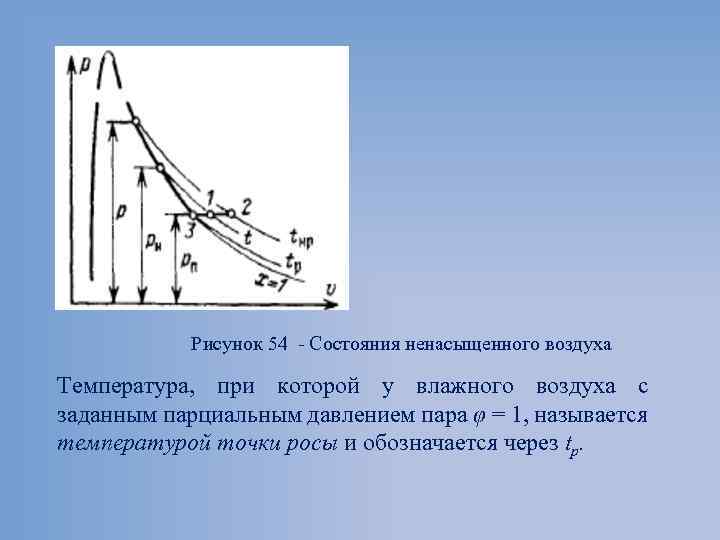
Рисунок 54 Состояния ненасыщенного воздуха Температура, при которой у влажного воздуха с заданным парциальным давлением пара φ = 1, называется температурой точки росы и обозначается через tр.

8. 3 Влагосодержание и энтальпия влажного воздуха Влагосодержание отношение массы водяного пара к массе сухого воздуха в смеси, или отношение плотностей пара и сухого воздуха, взятых при соответствующих парциальных давлениях (кг на 1 кг сухого воздуха)


Энтальпия влажного воздуха H, к. Дж на 1 кг сухого воздуха, суммируется из энтальпии 1 кг сухого воздуха и d кг водяного пара, т. е.
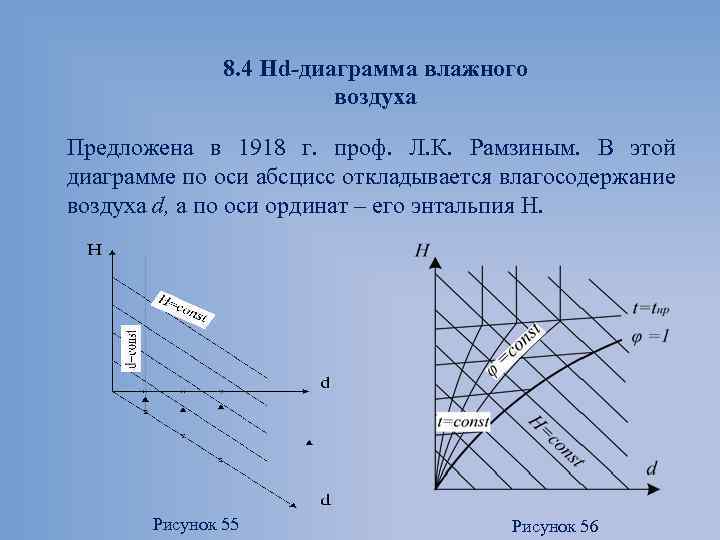
8. 4 Hd-диаграмма влажного воздуха Предложена в 1918 г. проф. Л. К. Рамзиным. В этой диаграмме по оси абсцисс откладывается влагосодержание воздуха d, а по оси ординат – его энтальпия H. Рисунок 55 Рисунок 56

где коэффициенты а и b при заданной температуре имеют постоянную величину. Эта формула представляет собой уравнение прямой линии. При t > tнр

8. 5 Температура мокрого термометра Когда вся убыль внутренней энергии воды, расходуемой на испарение, начнет восполняться теплотой, получаемой от воздуха, дальнейшее снижение температуры воды прекратится и она принимает постоянное значение tм, называемое температурой мокрого термометра
Teoreticheskie_osnovy_teplotekhniki_dlya_BVT.pptx