 ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ОРГАНИЧЕСКОЙ ХИМИИ ЛЕКЦИЯ 1
ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ОРГАНИЧЕСКОЙ ХИМИИ ЛЕКЦИЯ 1
 ОРГАНИЧЕСКАЯ ХИМИЯ • Это химия соединений углерода (И. Берцеллиус, 1806) • Это химия углеводородов и их производных
ОРГАНИЧЕСКАЯ ХИМИЯ • Это химия соединений углерода (И. Берцеллиус, 1806) • Это химия углеводородов и их производных
 СТРУКТУРНЫЕ ТЕОРИИ • Теория радикалов (Ж. Дюма и Ю. Либих, 1837 г. ) • Теория типов (Ш. Жерар, 1851 г. ) • Теория химического строения органических соединений (А. М. Бутлеров, 1861 г. ) • Стереохимическая теория (Вант–Гофф, 1874 г. ) • Электронная теория строения органических соединений • Метод валентных связей (В. Гайтлер, Ф. Лондон, 1924 г. ) • Метод молекулярных орбиталей (Ф. Хунд, Р. Малликен и др. , 1927 г. )
СТРУКТУРНЫЕ ТЕОРИИ • Теория радикалов (Ж. Дюма и Ю. Либих, 1837 г. ) • Теория типов (Ш. Жерар, 1851 г. ) • Теория химического строения органических соединений (А. М. Бутлеров, 1861 г. ) • Стереохимическая теория (Вант–Гофф, 1874 г. ) • Электронная теория строения органических соединений • Метод валентных связей (В. Гайтлер, Ф. Лондон, 1924 г. ) • Метод молекулярных орбиталей (Ф. Хунд, Р. Малликен и др. , 1927 г. )
 ТЕОРИЯ ХИМИЧЕСКОГО СТРОЕНИЯ • Свойства вещества определяются его структурой: природой, количеством и порядком соединения атомов • Вещества, имеющие одинаковые атомы, но различающиеся порядком их соединения и характером хими- ческой связи, обладают различными свойствами • Атомы, входящие в состав молекулы, оказывают взаимное влияние друг на друга (1828 -1886)
ТЕОРИЯ ХИМИЧЕСКОГО СТРОЕНИЯ • Свойства вещества определяются его структурой: природой, количеством и порядком соединения атомов • Вещества, имеющие одинаковые атомы, но различающиеся порядком их соединения и характером хими- ческой связи, обладают различными свойствами • Атомы, входящие в состав молекулы, оказывают взаимное влияние друг на друга (1828 -1886)
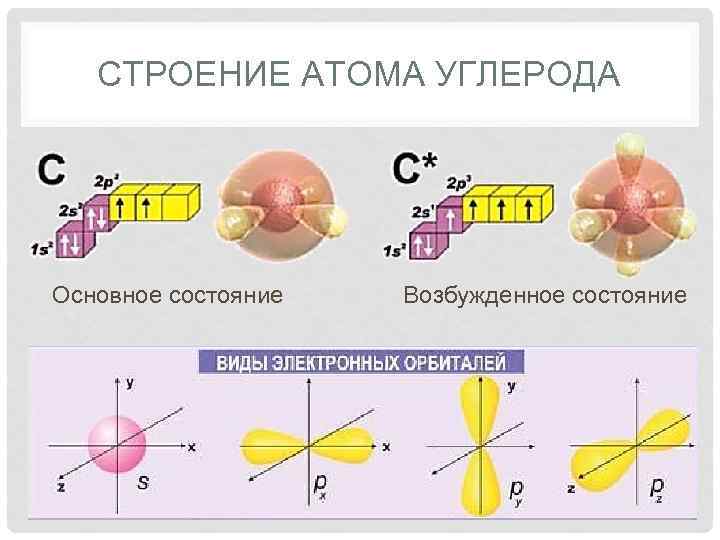 СТРОЕНИЕ АТОМА УГЛЕРОДА Основное состояние Возбужденное состояние
СТРОЕНИЕ АТОМА УГЛЕРОДА Основное состояние Возбужденное состояние
 ГИБРИДИЗАЦИЯ • Это квантово-механический прием смешения атомных орбиталей по форме и энергии с целью образования равноценных химических связей
ГИБРИДИЗАЦИЯ • Это квантово-механический прием смешения атомных орбиталей по форме и энергии с целью образования равноценных химических связей
 ВИДЫ ГИБРИДИЗАЦИИ
ВИДЫ ГИБРИДИЗАЦИИ
 ЭЛЕКТРОННЫЕ ЭФФЕКТЫ Большинство органических соединений состоит из атомов с различной электроотрицательностью Способность атомов вызывать поляризацию связей в молекуле за счет электроиндукции называют индуктивным эффектом. + I–эффект атома А или –I–эффект атома В Индуктивный эффект быстро уменьшается с увеличением числа связей между атомами.
ЭЛЕКТРОННЫЕ ЭФФЕКТЫ Большинство органических соединений состоит из атомов с различной электроотрицательностью Способность атомов вызывать поляризацию связей в молекуле за счет электроиндукции называют индуктивным эффектом. + I–эффект атома А или –I–эффект атома В Индуктивный эффект быстро уменьшается с увеличением числа связей между атомами.
 ЭЛЕКТРОННЫЕ ЭФФЕКТЫ Если в молекуле происходит поляризация сопряженных –связей со смещением электронных пар к соседним атомам, то такой эффект называется мезомерным Мезомерный эффект передаётся по цепи сопряжения без затухания.
ЭЛЕКТРОННЫЕ ЭФФЕКТЫ Если в молекуле происходит поляризация сопряженных –связей со смещением электронных пар к соседним атомам, то такой эффект называется мезомерным Мезомерный эффект передаётся по цепи сопряжения без затухания.
 РЕАГЕНТЫ Радикал - частица с неспаренным электроном. Атомы галогенов (Hal∙), радикалы из перекисных и других органических соединений (HO. , R. и другие). Электрофильные частицы - частицы с положительным зарядом или нейтральной молекулы, способной присоединять электронную пару. Катионы H+, +NO 2, +SO 3 H, R+; молекулы: BF 3, Zn. Cl 2, Al. Cl 3 Нуклеофильные частицы - частицы с отрицательным зарядом или нейтральной молекулы с неподеленной парой электронов, способной реагировать в виде электронодонора. Анионы : HO−, RCOO−, Hal −, H 2 N−; молекулы: H 2 O, NH 3, RNH 2 и другие.
РЕАГЕНТЫ Радикал - частица с неспаренным электроном. Атомы галогенов (Hal∙), радикалы из перекисных и других органических соединений (HO. , R. и другие). Электрофильные частицы - частицы с положительным зарядом или нейтральной молекулы, способной присоединять электронную пару. Катионы H+, +NO 2, +SO 3 H, R+; молекулы: BF 3, Zn. Cl 2, Al. Cl 3 Нуклеофильные частицы - частицы с отрицательным зарядом или нейтральной молекулы с неподеленной парой электронов, способной реагировать в виде электронодонора. Анионы : HO−, RCOO−, Hal −, H 2 N−; молекулы: H 2 O, NH 3, RNH 2 и другие.
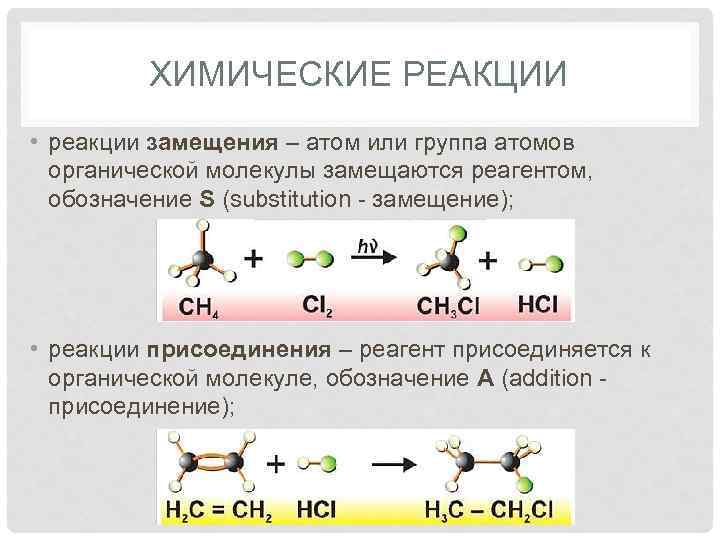 ХИМИЧЕСКИЕ РЕАКЦИИ • реакции замещения – атом или группа атомов органической молекулы замещаются реагентом, обозначение S (substitution - замещение); • реакции присоединения – реагент присоединяется к органической молекуле, обозначение A (addition - присоединение);
ХИМИЧЕСКИЕ РЕАКЦИИ • реакции замещения – атом или группа атомов органической молекулы замещаются реагентом, обозначение S (substitution - замещение); • реакции присоединения – реагент присоединяется к органической молекуле, обозначение A (addition - присоединение);
 ХИМИЧЕСКИЕ РЕАКЦИИ • реакции элиминирования – органическая молекула под действием реагента выделяет молекулу более простого строения, обозначение E (elimination - отщепление); • молекулярная перегруппировка – органическая молекула под действием реагента изменяет порядок соединения атомов.
ХИМИЧЕСКИЕ РЕАКЦИИ • реакции элиминирования – органическая молекула под действием реагента выделяет молекулу более простого строения, обозначение E (elimination - отщепление); • молекулярная перегруппировка – органическая молекула под действием реагента изменяет порядок соединения атомов.
 КЛАССИФИКАЦИЯ
КЛАССИФИКАЦИЯ