10 Температура и теплота.pptx
- Количество слайдов: 60
 ТЕМПЕРАТУРА И ТЕПЛОТА 1
ТЕМПЕРАТУРА И ТЕПЛОТА 1
 ТЕМПЕРАТУРА И ТЕПЛОТА Тепловое равновесие Про тело, у которого все свойства остаются неизменными, мы говорим: состояние тела не меняется. Напротив, при изменении какого либо свойства тела меняется его состояние. Состояние тела можно изменить, совершая над ним работу. Однако возможно дости гнуть таких же результатов и немеханическим путем. Вода нагреется как после интенсивного перемешивания, так и после поднесения к ней газовой горелки. 2
ТЕМПЕРАТУРА И ТЕПЛОТА Тепловое равновесие Про тело, у которого все свойства остаются неизменными, мы говорим: состояние тела не меняется. Напротив, при изменении какого либо свойства тела меняется его состояние. Состояние тела можно изменить, совершая над ним работу. Однако возможно дости гнуть таких же результатов и немеханическим путем. Вода нагреется как после интенсивного перемешивания, так и после поднесения к ней газовой горелки. 2
 ТЕМПЕРАТУРА И ТЕПЛОТА Тепловое равновесие Если внешняя среда или окружающие тела воздействуют на рассматриваемое тело или систему тел и меняют со стояние этого тела или системы тел немеханическим путем, то гово рят о теплообмене. Если теплообмен между телами отсутствует, то тела находятся в тепловом равновесии, имеют одинаковую температуру. Если тела соприкасаются друг с другом, то наличие теплового равновесия обнаруживается непосредственно: состояния тел 3 длительно оста ются теми же.
ТЕМПЕРАТУРА И ТЕПЛОТА Тепловое равновесие Если внешняя среда или окружающие тела воздействуют на рассматриваемое тело или систему тел и меняют со стояние этого тела или системы тел немеханическим путем, то гово рят о теплообмене. Если теплообмен между телами отсутствует, то тела находятся в тепловом равновесии, имеют одинаковую температуру. Если тела соприкасаются друг с другом, то наличие теплового равновесия обнаруживается непосредственно: состояния тел 3 длительно оста ются теми же.
 ТЕМПЕРАТУРА И ТЕПЛОТА Тепловое равновесие Теплообмен возможен и в случае далеких друг от друга тел. Обнаружить тепловое равновесие в этом случае можно при помощи третьего тела, которое играет роль термометра. Если термометр находится в равновесии с обоими телами, то температура этих тел одинакова. Это значит, что и при непосредственном сопри косновении они находились бы в состоянии теплового равновесия. 4
ТЕМПЕРАТУРА И ТЕПЛОТА Тепловое равновесие Теплообмен возможен и в случае далеких друг от друга тел. Обнаружить тепловое равновесие в этом случае можно при помощи третьего тела, которое играет роль термометра. Если термометр находится в равновесии с обоими телами, то температура этих тел одинакова. Это значит, что и при непосредственном сопри косновении они находились бы в состоянии теплового равновесия. 4
 ТЕМПЕРАТУРА И ТЕПЛОТА Тепловое равновесие При помощи «третьего тела» , термометра, всегда можно сказать, обладают ли тела разными или одинаковыми температурами. При помощи термометра можно не только устанавливать нали чие или отсутствие теплового равновесия, но можно и судить о сте пени отклонения от равновесия. 5
ТЕМПЕРАТУРА И ТЕПЛОТА Тепловое равновесие При помощи «третьего тела» , термометра, всегда можно сказать, обладают ли тела разными или одинаковыми температурами. При помощи термометра можно не только устанавливать нали чие или отсутствие теплового равновесия, но можно и судить о сте пени отклонения от равновесия. 5
 ТЕМПЕРАТУРА И ТЕПЛОТА Тепловое равновесие Чтобы термометр мог служить этой цели, нужно условиться о веществе термометра (ртуть, спирт, вода, газ) и о свойстве (признаке), по которому мы будем судить о достижении или отклонении от теплового равновесия предмета с термометром. Как и всегда в фи зике, важно условиться, какие приборы, в данном случае тер мометры, должны быть положе ны за основу. Далее всегда ожно м проградуировать любой тер мометр по эталонному. 6
ТЕМПЕРАТУРА И ТЕПЛОТА Тепловое равновесие Чтобы термометр мог служить этой цели, нужно условиться о веществе термометра (ртуть, спирт, вода, газ) и о свойстве (признаке), по которому мы будем судить о достижении или отклонении от теплового равновесия предмета с термометром. Как и всегда в фи зике, важно условиться, какие приборы, в данном случае тер мометры, должны быть положе ны за основу. Далее всегда ожно м проградуировать любой тер мометр по эталонному. 6
 ТЕМПЕРАТУРА И ТЕПЛОТА Тепловое равновесие Чтобы термометр мог служить этой цели, нужно условиться о веществе термометра (ртуть, спирт, вода, газ) и о свойстве (признаке), по которому мы будем судить о достижении или отклонении от теплового равновесия предмета с термометром. Как и всегда в фи зике, важно условиться, какие приборы, в данном случае тер мометры, должны быть положе ны за основу. Далее всегда ожно м проградуировать любой тер мометр по эталонному. 7
ТЕМПЕРАТУРА И ТЕПЛОТА Тепловое равновесие Чтобы термометр мог служить этой цели, нужно условиться о веществе термометра (ртуть, спирт, вода, газ) и о свойстве (признаке), по которому мы будем судить о достижении или отклонении от теплового равновесия предмета с термометром. Как и всегда в фи зике, важно условиться, какие приборы, в данном случае тер мометры, должны быть положе ны за основу. Далее всегда ожно м проградуировать любой тер мометр по эталонному. 7
 ТЕМПЕРАТУРА И ТЕПЛОТА Тепловое равновесие В качестве эталонного вещества для термометра берется газообраз ный водород. Признак, по которому судят о температуре, это давление газа р. Температура тела принимается пропорциональ ной давлению водорода в газовом термометре при постоянстве объема, занимаемого водородом. 8
ТЕМПЕРАТУРА И ТЕПЛОТА Тепловое равновесие В качестве эталонного вещества для термометра берется газообраз ный водород. Признак, по которому судят о температуре, это давление газа р. Температура тела принимается пропорциональ ной давлению водорода в газовом термометре при постоянстве объема, занимаемого водородом. 8
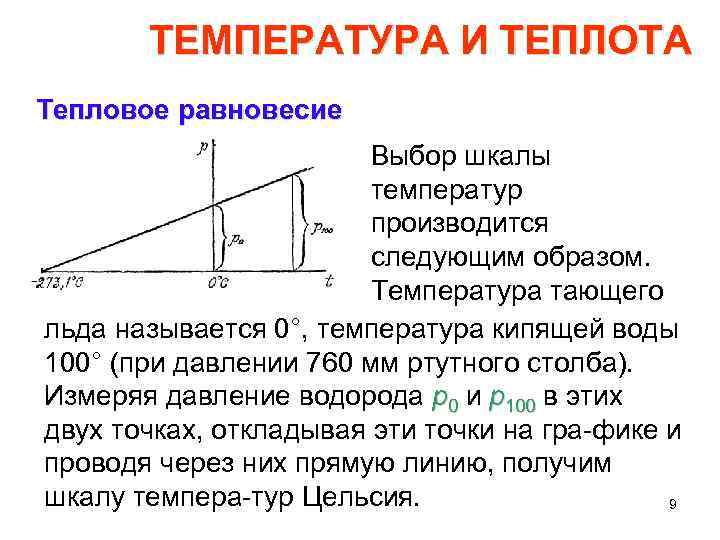 ТЕМПЕРАТУРА И ТЕПЛОТА Тепловое равновесие Выбор шкалы температур производится следующим образом. Температура тающего льда называется 0°, температура кипящей воды 100° (при давлении 760 мм ртутного столба). Измеряя давление водорода р0 и р100 в этих двух точках, откладывая эти точки на гра фике и проводя через них прямую линию, получим шкалу темпера тур Цельсия. 9
ТЕМПЕРАТУРА И ТЕПЛОТА Тепловое равновесие Выбор шкалы температур производится следующим образом. Температура тающего льда называется 0°, температура кипящей воды 100° (при давлении 760 мм ртутного столба). Измеряя давление водорода р0 и р100 в этих двух точках, откладывая эти точки на гра фике и проводя через них прямую линию, получим шкалу темпера тур Цельсия. 9
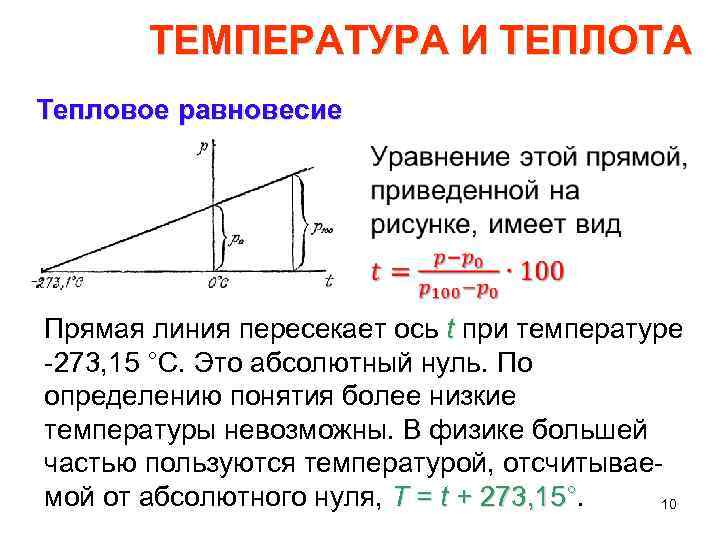 ТЕМПЕРАТУРА И ТЕПЛОТА Тепловое равновесие • Прямая линия пересекает ось t при температуре 273, 15 °С. Это абсолютный нуль. По определению понятия более низкие температуры невозможны. В физике большей частью пользуются температурой, отсчитывае мой от абсолютного нуля, Т = t + 273, 15° 10
ТЕМПЕРАТУРА И ТЕПЛОТА Тепловое равновесие • Прямая линия пересекает ось t при температуре 273, 15 °С. Это абсолютный нуль. По определению понятия более низкие температуры невозможны. В физике большей частью пользуются температурой, отсчитывае мой от абсолютного нуля, Т = t + 273, 15° 10
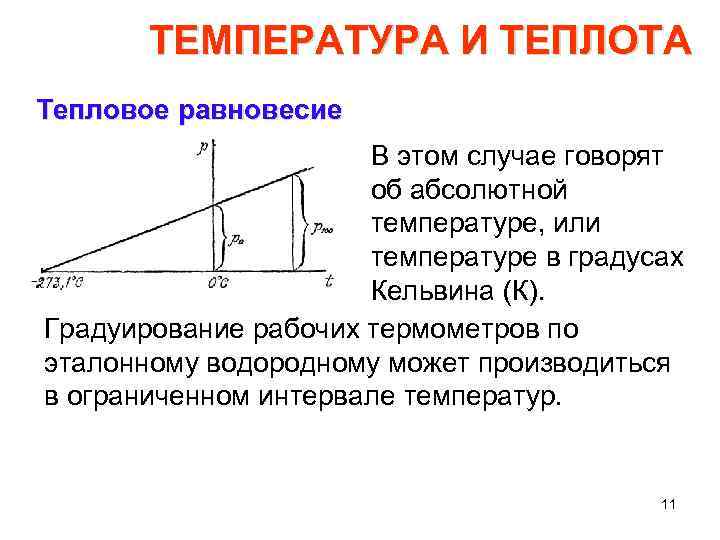 ТЕМПЕРАТУРА И ТЕПЛОТА Тепловое равновесие В этом случае говорят об абсолютной температуре, или температуре в градусах Кельвина (К). Градуирование рабочих термометров по эталонному водородному может производиться в ограниченном интервале температур. 11
ТЕМПЕРАТУРА И ТЕПЛОТА Тепловое равновесие В этом случае говорят об абсолютной температуре, или температуре в градусах Кельвина (К). Градуирование рабочих термометров по эталонному водородному может производиться в ограниченном интервале температур. 11
 ТЕМПЕРАТУРА И ТЕПЛОТА Тепловое равновесие При высоких температурах может начаться диффузия водорода через стенки сосуда. При низких температурах водород может превра титься в жидкость. Тем не менее принятое определение температуры имеет совершенно общий смысл. 12
ТЕМПЕРАТУРА И ТЕПЛОТА Тепловое равновесие При высоких температурах может начаться диффузия водорода через стенки сосуда. При низких температурах водород может превра титься в жидкость. Тем не менее принятое определение температуры имеет совершенно общий смысл. 12
 ТЕМПЕРАТУРА И ТЕПЛОТА Внутренняя энергия Основные черты поведения тел при механическом и тепловом взаимодействии превосходно отражает так называемая молекулярно кинетическая модель. Состоящее из молекул тело рассматривается как система движущихся и взаимодействующих частиц, подчиняющаяся законам механики. Такая система молекул должна обладать энергией, складывающейся из потенциальной энергии взаимодействия частиц и кинетической энергии их движения. 13
ТЕМПЕРАТУРА И ТЕПЛОТА Внутренняя энергия Основные черты поведения тел при механическом и тепловом взаимодействии превосходно отражает так называемая молекулярно кинетическая модель. Состоящее из молекул тело рассматривается как система движущихся и взаимодействующих частиц, подчиняющаяся законам механики. Такая система молекул должна обладать энергией, складывающейся из потенциальной энергии взаимодействия частиц и кинетической энергии их движения. 13
 ТЕМПЕРАТУРА И ТЕПЛОТА Внутренняя энергия Эту энергию и называют внутренней энергией тела. Определенному состоянию тела соответствует определенная внутренняя энергия. Изменения взаимного расположения или характера движения частиц связаны с изменением внутренней энер гии. Каким бы способом ни менялась внутренняя энергия тела, окружающие тела должны передать энергию молекулам рассматри ваемого тела. 14
ТЕМПЕРАТУРА И ТЕПЛОТА Внутренняя энергия Эту энергию и называют внутренней энергией тела. Определенному состоянию тела соответствует определенная внутренняя энергия. Изменения взаимного расположения или характера движения частиц связаны с изменением внутренней энер гии. Каким бы способом ни менялась внутренняя энергия тела, окружающие тела должны передать энергию молекулам рассматри ваемого тела. 14
 ТЕМПЕРАТУРА И ТЕПЛОТА Внутренняя энергия Если тело подвергается механическому воздействию, то передача энергии происходит упорядоченным образом; при теп ловом обмене энергия передается со стороны среды путем случайных импульсов, передаваемых то одной, то другой молекуле. Количество энергии, переданной телу механическим путем, из меряется величиной произведенной над телом работы. Количество энергии, переданной при теплообмене, 15 измеряется количеством тепла.
ТЕМПЕРАТУРА И ТЕПЛОТА Внутренняя энергия Если тело подвергается механическому воздействию, то передача энергии происходит упорядоченным образом; при теп ловом обмене энергия передается со стороны среды путем случайных импульсов, передаваемых то одной, то другой молекуле. Количество энергии, переданной телу механическим путем, из меряется величиной произведенной над телом работы. Количество энергии, переданной при теплообмене, 15 измеряется количеством тепла.
 ТЕМПЕРАТУРА И ТЕПЛОТА Внутренняя энергия Так как строгий подсчет внутренней энергии тела затруднителен, а большей частью и невозможен, и так как само представление о внутренней энергии как о чисто механической величине является лишь приближением, то надо ввести строгое определение этой величины. Это удается сделать, изучая процессы, происходящие без теплообмена с окружающей средой. Такие явления называются адиабатическими. 16
ТЕМПЕРАТУРА И ТЕПЛОТА Внутренняя энергия Так как строгий подсчет внутренней энергии тела затруднителен, а большей частью и невозможен, и так как само представление о внутренней энергии как о чисто механической величине является лишь приближением, то надо ввести строгое определение этой величины. Это удается сделать, изучая процессы, происходящие без теплообмена с окружающей средой. Такие явления называются адиабатическими. 16
 ТЕМПЕРАТУРА И ТЕПЛОТА Внутренняя энергия Производя опыт внутри теплоизолирующей оболочки и ограничивая измерения краткими сроками (пока тепло не успело «уйти» из изучаемого объема), удается вполне точно осуществить адиабатические условия. Многочисленные опыты, приведшие в свое время к установлению закона сохранения энергии, показывают; что каким бы путем ни изменялось в таком процессе состояние тела, на это потребуется одна и та же работа. 17
ТЕМПЕРАТУРА И ТЕПЛОТА Внутренняя энергия Производя опыт внутри теплоизолирующей оболочки и ограничивая измерения краткими сроками (пока тепло не успело «уйти» из изучаемого объема), удается вполне точно осуществить адиабатические условия. Многочисленные опыты, приведшие в свое время к установлению закона сохранения энергии, показывают; что каким бы путем ни изменялось в таком процессе состояние тела, на это потребуется одна и та же работа. 17
 ТЕМПЕРАТУРА И ТЕПЛОТА Внутренняя энергия Величина этой работы А равна по определению приросту внутренней энергии тела U: А = U 2 – U 1. Абсолютное значение внутренней энергии, разумеется, не может быть найдено из опыта. Если бы механическая модель тела была вполне точна, то утвер ждение, записанное выше, являлось бы простым следствием закона сохранения механической энергии. 18
ТЕМПЕРАТУРА И ТЕПЛОТА Внутренняя энергия Величина этой работы А равна по определению приросту внутренней энергии тела U: А = U 2 – U 1. Абсолютное значение внутренней энергии, разумеется, не может быть найдено из опыта. Если бы механическая модель тела была вполне точна, то утвер ждение, записанное выше, являлось бы простым следствием закона сохранения механической энергии. 18
 ТЕМПЕРАТУРА И ТЕПЛОТА Внутренняя энергия Однако молекулярно кинетическая модель есть только модель, и поэтому тот факт, что каждому состоянию тела можно сопоставить определенную энергию, так что разность энергий двух состояний равна адиабатической работе перехода, является важнейшим законом природы, приводящим к закону сохранения энергии. 19
ТЕМПЕРАТУРА И ТЕПЛОТА Внутренняя энергия Однако молекулярно кинетическая модель есть только модель, и поэтому тот факт, что каждому состоянию тела можно сопоставить определенную энергию, так что разность энергий двух состояний равна адиабатической работе перехода, является важнейшим законом природы, приводящим к закону сохранения энергии. 19
 ТЕМПЕРАТУРА И ТЕПЛОТА Внутренняя энергия Теплообмен и механическое воздействие могут приводить в ряде случаев к одинаковому изменению состояния, т. е. к одинаковым изменениям внутренней энергии тела. Это дает нам возможность сравнивать тепло и работу и измерять количество тепла в тех же единицах, что работу и энергию. Для представления о величинах внутренней энергии приведем следующие цифры. 20
ТЕМПЕРАТУРА И ТЕПЛОТА Внутренняя энергия Теплообмен и механическое воздействие могут приводить в ряде случаев к одинаковому изменению состояния, т. е. к одинаковым изменениям внутренней энергии тела. Это дает нам возможность сравнивать тепло и работу и измерять количество тепла в тех же единицах, что работу и энергию. Для представления о величинах внутренней энергии приведем следующие цифры. 20
 ТЕМПЕРАТУРА И ТЕПЛОТА Внутренняя энергия При нагревании воды на 1° энергия 1 г воды возрастает на 1 кал = 0, 427 кгс м = 4, 18 107 эрг = 4, 18 Дж = 2, 61 1019 э. В. При этом одна молекула воды увеличивает в среднем свою энергию на 3 10 23 кал = 1, 28 10 23 кгс м = 1, 25 10 15 эрг = 12, 5 10 23 Дж = 7, 8 10 4 э. В. 21
ТЕМПЕРАТУРА И ТЕПЛОТА Внутренняя энергия При нагревании воды на 1° энергия 1 г воды возрастает на 1 кал = 0, 427 кгс м = 4, 18 107 эрг = 4, 18 Дж = 2, 61 1019 э. В. При этом одна молекула воды увеличивает в среднем свою энергию на 3 10 23 кал = 1, 28 10 23 кгс м = 1, 25 10 15 эрг = 12, 5 10 23 Дж = 7, 8 10 4 э. В. 21
 ТЕМПЕРАТУРА И ТЕПЛОТА Внутренняя энергия При сгорании 1 г угля вещество отдает внутреннюю энергию в количестве 7000 кал = 2990 кгс м = 2, 93 1011 эрг = 2, 93 104 Дж = 18, 3 1022 э. В. В расчете на один атом углерода эти цифры примут вид 1, 4 10 19 кал = 5, 98 10 20 кгс м = 5, 86 10 12 эрг = 5, 86 10 19 Дж = 3, 66 э. В 22
ТЕМПЕРАТУРА И ТЕПЛОТА Внутренняя энергия При сгорании 1 г угля вещество отдает внутреннюю энергию в количестве 7000 кал = 2990 кгс м = 2, 93 1011 эрг = 2, 93 104 Дж = 18, 3 1022 э. В. В расчете на один атом углерода эти цифры примут вид 1, 4 10 19 кал = 5, 98 10 20 кгс м = 5, 86 10 12 эрг = 5, 86 10 19 Дж = 3, 66 э. В 22
 ТЕМПЕРАТУРА И ТЕПЛОТА Внутренняя энергия При ядерном делении 1 г урана 235 выделяется энергия 2, 03 1010 кал = 8, 65 109 кгс м = 8, 49 1017 эрг = 8, 49 1010 Дж = 5, 29 1029 э. В. Одно атомное ядро отдает при этом внутреннюю энергию в количестве 7, 9 10 12 кал=3, 38 10 12 кгс м=3, 3 10 4 эрг= = 3, 3 10 11 Дж = 206 106 э. В ≈ 200 Мэ. В, что более чем в 50 миллионов раз превышает энергию химических реакций (1 Мэ. В = 106 э. В). 23
ТЕМПЕРАТУРА И ТЕПЛОТА Внутренняя энергия При ядерном делении 1 г урана 235 выделяется энергия 2, 03 1010 кал = 8, 65 109 кгс м = 8, 49 1017 эрг = 8, 49 1010 Дж = 5, 29 1029 э. В. Одно атомное ядро отдает при этом внутреннюю энергию в количестве 7, 9 10 12 кал=3, 38 10 12 кгс м=3, 3 10 4 эрг= = 3, 3 10 11 Дж = 206 106 э. В ≈ 200 Мэ. В, что более чем в 50 миллионов раз превышает энергию химических реакций (1 Мэ. В = 106 э. В). 23
 ТЕМПЕРАТУРА И ТЕПЛОТА Первое начало термодинамики В самом общем случае, обмениваясь энергией со средой или ок ружающими телами, рассматриваемая система может получать или отдавать количество тепла Q, может производить работу или над ней может быть произведена работа. Тепло и работа это две формы, в которых энергия тела может передаваться среде или, на оборот, энергия среды может передаваться телу. Закон сохранения энергии исключает возможность каких либо потерь при энергетиче ском обмене. 24
ТЕМПЕРАТУРА И ТЕПЛОТА Первое начало термодинамики В самом общем случае, обмениваясь энергией со средой или ок ружающими телами, рассматриваемая система может получать или отдавать количество тепла Q, может производить работу или над ней может быть произведена работа. Тепло и работа это две формы, в которых энергия тела может передаваться среде или, на оборот, энергия среды может передаваться телу. Закон сохранения энергии исключает возможность каких либо потерь при энергетиче ском обмене. 24
 ТЕМПЕРАТУРА И ТЕПЛОТА Первое начало термодинамики Разность энергий системы в двух состояниях должна равняться сумме теплоты и работы, полученных системой от окру жающих тел. При этом прирост энергии при переходе системы от одного состояния к другому всегда один и тот же вне зависимости от характера или способа перехода от начального состояния к ко нечному. Принцип сохранения энергии заключен именно в последнем утверждении, и это утверждение вполне допускает экспериментальную проверку. 25
ТЕМПЕРАТУРА И ТЕПЛОТА Первое начало термодинамики Разность энергий системы в двух состояниях должна равняться сумме теплоты и работы, полученных системой от окру жающих тел. При этом прирост энергии при переходе системы от одного состояния к другому всегда один и тот же вне зависимости от характера или способа перехода от начального состояния к ко нечному. Принцип сохранения энергии заключен именно в последнем утверждении, и это утверждение вполне допускает экспериментальную проверку. 25
 ТЕМПЕРАТУРА И ТЕПЛОТА Первое начало термодинамики Измеряя сообщенные системе теплоту и работу в различных переходах от одного и того же начального к одному и тому же конечному состоянию, мы с неизбежностью убедимся, что прирост энергии во всех случаях один и тот же. Закон сохранения энергии, выраженный в такой форме, носит название первого начала термодинамики. Этот важнейший закон природы был установлен работами ряда ученых в середине XIX столетия, таких, как Юлиус Роберт фон Майер, Джеймс Прескотт Джоуль и прежде всего Герман Людвиг Фердинанд фон Гельмгольц. 26
ТЕМПЕРАТУРА И ТЕПЛОТА Первое начало термодинамики Измеряя сообщенные системе теплоту и работу в различных переходах от одного и того же начального к одному и тому же конечному состоянию, мы с неизбежностью убедимся, что прирост энергии во всех случаях один и тот же. Закон сохранения энергии, выраженный в такой форме, носит название первого начала термодинамики. Этот важнейший закон природы был установлен работами ряда ученых в середине XIX столетия, таких, как Юлиус Роберт фон Майер, Джеймс Прескотт Джоуль и прежде всего Герман Людвиг Фердинанд фон Гельмгольц. 26
 ТЕМПЕРАТУРА И ТЕПЛОТА Первое начало термодинамики Для записи первого начала термодинамики в виде формулы надо условиться о выборе знака для теплоты и работы. Мы примем, что теплота положительна тогда, когда она сообщается системе, а работу будем считать положительной тогда, когда тело совершает ее против действия внешних сил. Тогда первое начало термодинамики запи шется в виде ΔQ = d. U + ΔA. 27
ТЕМПЕРАТУРА И ТЕПЛОТА Первое начало термодинамики Для записи первого начала термодинамики в виде формулы надо условиться о выборе знака для теплоты и работы. Мы примем, что теплота положительна тогда, когда она сообщается системе, а работу будем считать положительной тогда, когда тело совершает ее против действия внешних сил. Тогда первое начало термодинамики запи шется в виде ΔQ = d. U + ΔA. 27
 ТЕМПЕРАТУРА И ТЕПЛОТА Первое начало термодинамики Иначе говоря, подведенное к телу тепло идет на изменение внутренней энергии и на произведенную телом работу. Разумеется, мыслимы любые пре вращения, при которых каждая из входящих в равенство величин может быть положительной и отрицательной. Не случайно в записи первого начала знак дифференциала ис пользован только для энергии. Работа и тепло не являются полными дифференциалами. 28
ТЕМПЕРАТУРА И ТЕПЛОТА Первое начало термодинамики Иначе говоря, подведенное к телу тепло идет на изменение внутренней энергии и на произведенную телом работу. Разумеется, мыслимы любые пре вращения, при которых каждая из входящих в равенство величин может быть положительной и отрицательной. Не случайно в записи первого начала знак дифференциала ис пользован только для энергии. Работа и тепло не являются полными дифференциалами. 28
 ТЕМПЕРАТУРА И ТЕПЛОТА Первое начало термодинамики • 29
ТЕМПЕРАТУРА И ТЕПЛОТА Первое начало термодинамики • 29
 ТЕМПЕРАТУРА И ТЕПЛОТА Первое начало термодинамики Применение закона сохранения энергии и, в частности, первого начала термодинамики охватывает все разделы физики. Ценность его для науки заключается в исключительной предсказательной силе. Не имея каких бы то ни было сведений о характере процесса, зная лишь начальное и конечное состояния системы, можно делать ряд ценных выводов. Пусть, например, в результате химической реакции присоединения молекулы А к В, образуется молекула АВ. 30
ТЕМПЕРАТУРА И ТЕПЛОТА Первое начало термодинамики Применение закона сохранения энергии и, в частности, первого начала термодинамики охватывает все разделы физики. Ценность его для науки заключается в исключительной предсказательной силе. Не имея каких бы то ни было сведений о характере процесса, зная лишь начальное и конечное состояния системы, можно делать ряд ценных выводов. Пусть, например, в результате химической реакции присоединения молекулы А к В, образуется молекула АВ. 30
 ТЕМПЕРАТУРА И ТЕПЛОТА Первое начало термодинамики Допустим, нам известны внутренние энергии молекул UA, UB и UAB. Если UAB больше, чем UA+UB, то мы можем предсказать, что реакция протекает с поглощением тепла, и притом в количестве, равном Q = UAB – UA – UB. Или, зная UA и UB и измеряя при помощи калориметра теплоту реакции, мы можем найти UAB и использовать эти данные для предсказания хода какой либо дру гой реакции, в которой участвует соединение АВ. 31
ТЕМПЕРАТУРА И ТЕПЛОТА Первое начало термодинамики Допустим, нам известны внутренние энергии молекул UA, UB и UAB. Если UAB больше, чем UA+UB, то мы можем предсказать, что реакция протекает с поглощением тепла, и притом в количестве, равном Q = UAB – UA – UB. Или, зная UA и UB и измеряя при помощи калориметра теплоту реакции, мы можем найти UAB и использовать эти данные для предсказания хода какой либо дру гой реакции, в которой участвует соединение АВ. 31
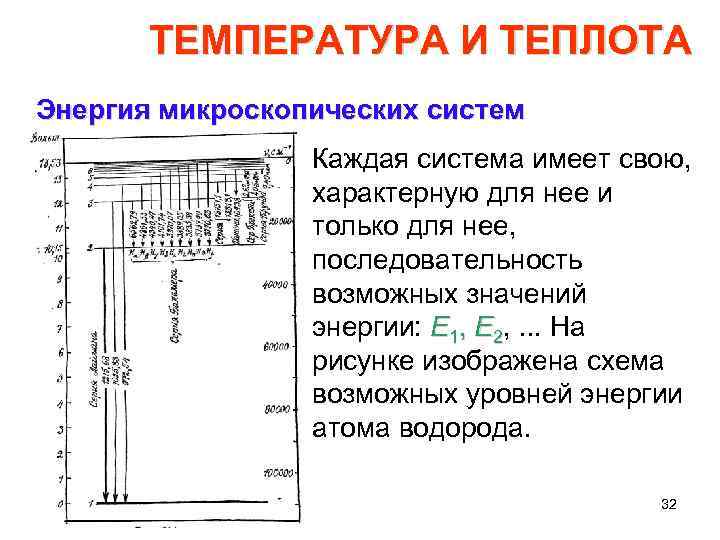 ТЕМПЕРАТУРА И ТЕПЛОТА Энергия микроскопических систем Каждая система имеет свою, характерную для нее и только для нее, последовательность возможных значений энергии: E 1, Е 2, . . . На рисунке изображена схема возможных уровней энергии атома водорода. 32
ТЕМПЕРАТУРА И ТЕПЛОТА Энергия микроскопических систем Каждая система имеет свою, характерную для нее и только для нее, последовательность возможных значений энергии: E 1, Е 2, . . . На рисунке изображена схема возможных уровней энергии атома водорода. 32
 ТЕМПЕРАТУРА И ТЕПЛОТА Энергия микроскопических систем Аналогично можно изобразить энергети ческие уровни и других атомных систем. При сообщении системе тепла или работы энергия атомов, молекул или иных микроскопи ческих систем может возрастать лишь скачкообразно, определенны ми порциями (квантами) энергии. Так же точно отдельными кван тами иотдается энергия окружающим телам. 33
ТЕМПЕРАТУРА И ТЕПЛОТА Энергия микроскопических систем Аналогично можно изобразить энергети ческие уровни и других атомных систем. При сообщении системе тепла или работы энергия атомов, молекул или иных микроскопи ческих систем может возрастать лишь скачкообразно, определенны ми порциями (квантами) энергии. Так же точно отдельными кван тами иотдается энергия окружающим телам. 33
 ТЕМПЕРАТУРА И ТЕПЛОТА Энергия микроскопических систем Строго говоря, закон о квантовом характере энергии, о наличии для каждой микроскопической системы «лестницы» возможных энер гетических уровней является вполне общим законом природы, спра ведливым и для больших тел. Однако у большого тела, состоящего из n атомов, число энергетических уровней, грубо гово ря, возрастает в n раз. По мере возрастания энергии, как это видно из рисунка для во дорода, уровни располагаются все 34 теснее.
ТЕМПЕРАТУРА И ТЕПЛОТА Энергия микроскопических систем Строго говоря, закон о квантовом характере энергии, о наличии для каждой микроскопической системы «лестницы» возможных энер гетических уровней является вполне общим законом природы, спра ведливым и для больших тел. Однако у большого тела, состоящего из n атомов, число энергетических уровней, грубо гово ря, возрастает в n раз. По мере возрастания энергии, как это видно из рисунка для во дорода, уровни располагаются все 34 теснее.
 ТЕМПЕРАТУРА И ТЕПЛОТА Энергия микроскопических систем Сближение этих уровней происходит у большого тела несравненно быстрее, чем у отдельного атома. Лишь самые низкие, бедные энергией уровни выглядят раз дельно. Более высокие уровни сливаются, и практически оказывает ся, что большое тело может изменять свою энергию непрерывно. Если от тела отнимать энергию, то оно «спускается» на более низкие уровни. Квантовый характер изменений энергии прояв ляется поэтому тем резче, чем ниже 35 температура тела, чем ближе она к абсолютному
ТЕМПЕРАТУРА И ТЕПЛОТА Энергия микроскопических систем Сближение этих уровней происходит у большого тела несравненно быстрее, чем у отдельного атома. Лишь самые низкие, бедные энергией уровни выглядят раз дельно. Более высокие уровни сливаются, и практически оказывает ся, что большое тело может изменять свою энергию непрерывно. Если от тела отнимать энергию, то оно «спускается» на более низкие уровни. Квантовый характер изменений энергии прояв ляется поэтому тем резче, чем ниже 35 температура тела, чем ближе она к абсолютному
 ТЕМПЕРАТУРА И ТЕПЛОТА Энергия микроскопических систем При механическом воздействии энергетические уровни тела или системы смещаются. В подавляющем большинстве случаев просле дить за этим смещением не удается. Для микроскопических систем – атомов и молекул – влияние давления очень мало. Тепловое взаимодействие состоит в переходах системы с одного уровня энергии на другой. Тепловое равновесие является подвижным равновесием. 36
ТЕМПЕРАТУРА И ТЕПЛОТА Энергия микроскопических систем При механическом воздействии энергетические уровни тела или системы смещаются. В подавляющем большинстве случаев просле дить за этим смещением не удается. Для микроскопических систем – атомов и молекул – влияние давления очень мало. Тепловое взаимодействие состоит в переходах системы с одного уровня энергии на другой. Тепловое равновесие является подвижным равновесием. 36
 ТЕМПЕРАТУРА И ТЕПЛОТА Энергия микроскопических систем Каждое тело не имеет все время какую то одну энергию, а непрерывно об ме ни ва ет ся энергией со средой так, что в среднем энергия остается неизменной. Обмен энергией происходит порциями – квантами. Если в какой то момент энергия равна E 1, то в следующий момент она изменится скачком до Е 2. Энергия отдается в виде излучения. Если Е 1 > Е 2, то Е 1 – Е 2 = h , где – частота излучения, a h – постоянная Планка, равная 6, 62 10 27 эрг с. 37
ТЕМПЕРАТУРА И ТЕПЛОТА Энергия микроскопических систем Каждое тело не имеет все время какую то одну энергию, а непрерывно об ме ни ва ет ся энергией со средой так, что в среднем энергия остается неизменной. Обмен энергией происходит порциями – квантами. Если в какой то момент энергия равна E 1, то в следующий момент она изменится скачком до Е 2. Энергия отдается в виде излучения. Если Е 1 > Е 2, то Е 1 – Е 2 = h , где – частота излучения, a h – постоянная Планка, равная 6, 62 10 27 эрг с. 37
 ТЕМПЕРАТУРА И ТЕПЛОТА Энергия микроскопических систем Приобретение энергии может произойти или в результате поглощения излучения или в результате механического толчка какой либо частицей. Если температура не остается постоянной, а падает, то число переходов на нижние уровни с верхних подавляет обратные пере ходы. Энергия снижается скачками, тело отдает один квант излу чения за другим. 38
ТЕМПЕРАТУРА И ТЕПЛОТА Энергия микроскопических систем Приобретение энергии может произойти или в результате поглощения излучения или в результате механического толчка какой либо частицей. Если температура не остается постоянной, а падает, то число переходов на нижние уровни с верхних подавляет обратные пере ходы. Энергия снижается скачками, тело отдает один квант излу чения за другим. 38
 ТЕМПЕРАТУРА И ТЕПЛОТА Энергия микроскопических систем Схематически описанные явления энергетического обмена были установлены вначале для атомов. Несколько позже стал очевидным вполне универсальный характер этой картины. 39
ТЕМПЕРАТУРА И ТЕПЛОТА Энергия микроскопических систем Схематически описанные явления энергетического обмена были установлены вначале для атомов. Несколько позже стал очевидным вполне универсальный характер этой картины. 39
 ТЕМПЕРАТУРА И ТЕПЛОТА Уравнение состояния Среди разнообразных свойств тела можно выделить три основных свойства, или параметра состояния. Это давление р, объем v и температура Т. Не всегда знания этих параметров достаточно для исчерпывающей характеристики тела. Если система состоит из мно гих веществ, то нужно знать их концентрации. Если тело находится в электрическом или магнитном полях, то нужно знать их напряженности. 40
ТЕМПЕРАТУРА И ТЕПЛОТА Уравнение состояния Среди разнообразных свойств тела можно выделить три основных свойства, или параметра состояния. Это давление р, объем v и температура Т. Не всегда знания этих параметров достаточно для исчерпывающей характеристики тела. Если система состоит из мно гих веществ, то нужно знать их концентрации. Если тело находится в электрическом или магнитном полях, то нужно знать их напряженности. 40
 ТЕМПЕРАТУРА И ТЕПЛОТА Уравнение состояния Всегда можно выбрать некоторую совокупность основных параме тров , которая будет однозначно определять состояние тела. Осталь ные характеристики тогда можно вычислить из основных пара метров. Если оставить без внимания электромагнитные поля и ограни читься рассмотрением простейших систем – газов, жидкостей и изо тропных твердых тел, то окажется, что всегда лишь два параметра определяют состояние тела. 41
ТЕМПЕРАТУРА И ТЕПЛОТА Уравнение состояния Всегда можно выбрать некоторую совокупность основных параме тров , которая будет однозначно определять состояние тела. Осталь ные характеристики тогда можно вычислить из основных пара метров. Если оставить без внимания электромагнитные поля и ограни читься рассмотрением простейших систем – газов, жидкостей и изо тропных твердых тел, то окажется, что всегда лишь два параметра определяют состояние тела. 41
 ТЕМПЕРАТУРА И ТЕПЛОТА Уравнение состояния В качестве этих двух параметров одина ково удобно выбрать любую пару из р, v, Т. Чаще всего выбор останавливают на v и Т. Тогда давление р будет функцией от v, Т. Уравнение p = f(v, Т) называют уравнением состояния Знание такого уравнения для како го либо тела, а в особенности для класса тел, имеет очень боль шое значение ля физики. Уравнения д состояния могут быть установлены опытным путем. 42
ТЕМПЕРАТУРА И ТЕПЛОТА Уравнение состояния В качестве этих двух параметров одина ково удобно выбрать любую пару из р, v, Т. Чаще всего выбор останавливают на v и Т. Тогда давление р будет функцией от v, Т. Уравнение p = f(v, Т) называют уравнением состояния Знание такого уравнения для како го либо тела, а в особенности для класса тел, имеет очень боль шое значение ля физики. Уравнения д состояния могут быть установлены опытным путем. 42
 ТЕМПЕРАТУРА И ТЕПЛОТА Уравнение состояния Характер зависимости давления от объема и темпе ратуры для жидких и твердых тел крайне индивидуален. Установив уравнение состояния для данного тела, мы получаем исчерпывающие сведения о его поведении в различных случаях, но не приобретаем каких либо знаний о поведении других тел. Исследуя поведение вещества, довольно часто характеризуют его не уравнением состояния, а производными одних параметров по другим. 43
ТЕМПЕРАТУРА И ТЕПЛОТА Уравнение состояния Характер зависимости давления от объема и темпе ратуры для жидких и твердых тел крайне индивидуален. Установив уравнение состояния для данного тела, мы получаем исчерпывающие сведения о его поведении в различных случаях, но не приобретаем каких либо знаний о поведении других тел. Исследуя поведение вещества, довольно часто характеризуют его не уравнением состояния, а производными одних параметров по другим. 43
 ТЕМПЕРАТУРА И ТЕПЛОТА Уравнение состояния • 44
ТЕМПЕРАТУРА И ТЕПЛОТА Уравнение состояния • 44
 ТЕМПЕРАТУРА И ТЕПЛОТА Уравнение состояния • 45
ТЕМПЕРАТУРА И ТЕПЛОТА Уравнение состояния • 45
 ТЕМПЕРАТУРА И ТЕПЛОТА Уравнение состояния • 46
ТЕМПЕРАТУРА И ТЕПЛОТА Уравнение состояния • 46
 ТЕМПЕРАТУРА И ТЕПЛОТА Уравнение состояния • 47
ТЕМПЕРАТУРА И ТЕПЛОТА Уравнение состояния • 47
 ТЕМПЕРАТУРА И ТЕПЛОТА Уравнение состояния • 48
ТЕМПЕРАТУРА И ТЕПЛОТА Уравнение состояния • 48
 ТЕМПЕРАТУРА И ТЕПЛОТА Уравнение состояния Поэтому, указывая значение какого нибудь коэффициента, надо сообщить, для каких значений давления и температуры приводится цифра. В неко торых случаях указываются средние значения коэффициентов в том или ином интервале температур или давлений. 49
ТЕМПЕРАТУРА И ТЕПЛОТА Уравнение состояния Поэтому, указывая значение какого нибудь коэффициента, надо сообщить, для каких значений давления и температуры приводится цифра. В неко торых случаях указываются средние значения коэффициентов в том или ином интервале температур или давлений. 49
 ТЕМПЕРАТУРА И ТЕПЛОТА Уравнение состояния газов • 50
ТЕМПЕРАТУРА И ТЕПЛОТА Уравнение состояния газов • 50
 ТЕМПЕРАТУРА И ТЕПЛОТА Уравнение состояния газов • 51
ТЕМПЕРАТУРА И ТЕПЛОТА Уравнение состояния газов • 51
 ТЕМПЕРАТУРА И ТЕПЛОТА Уравнение состояния газов • 52
ТЕМПЕРАТУРА И ТЕПЛОТА Уравнение состояния газов • 52
 ТЕМПЕРАТУРА И ТЕПЛОТА Уравнение состояния газов • 53
ТЕМПЕРАТУРА И ТЕПЛОТА Уравнение состояния газов • 53
 ТЕМПЕРАТУРА И ТЕПЛОТА Уравнение состояния газов • 54
ТЕМПЕРАТУРА И ТЕПЛОТА Уравнение состояния газов • 54
 ТЕМПЕРАТУРА И ТЕПЛОТА Уравнение состояния газов Реальные газы при нормальных условиях достаточно близки к идеальным. Так, водород, гелий, азот, воздух по рассматриваемым коэффициентам отличаются от идеального газа менее, чем на 0, 5 %. Газообразные вещества, находящиеся при давлениях, сущест венно превосходящих атмосферное, перестают подчиняться форму лам идеального газа. Вычисления могут привести к ошибкам в несколько процентов уже при 55 давлениях в несколько десятков атмосфер.
ТЕМПЕРАТУРА И ТЕПЛОТА Уравнение состояния газов Реальные газы при нормальных условиях достаточно близки к идеальным. Так, водород, гелий, азот, воздух по рассматриваемым коэффициентам отличаются от идеального газа менее, чем на 0, 5 %. Газообразные вещества, находящиеся при давлениях, сущест венно превосходящих атмосферное, перестают подчиняться форму лам идеального газа. Вычисления могут привести к ошибкам в несколько процентов уже при 55 давлениях в несколько десятков атмосфер.
 ТЕМПЕРАТУРА И ТЕПЛОТА Уравнение состояния газов Существенный вывод, к которому можно прийти, изучая поведе ние разреженных газов, заключается в том, что любой из них, во обще говоря, с тем же успехом, что и водород, мог быть положен в основу определения температуры. Водород ничем не выделяется среди разреженных газов. Можно поэтому сказать, что температур ная шкала, принятая в физике , – это не водородная шкала, а шкала давлений идеального газа. 56
ТЕМПЕРАТУРА И ТЕПЛОТА Уравнение состояния газов Существенный вывод, к которому можно прийти, изучая поведе ние разреженных газов, заключается в том, что любой из них, во обще говоря, с тем же успехом, что и водород, мог быть положен в основу определения температуры. Водород ничем не выделяется среди разреженных газов. Можно поэтому сказать, что температур ная шкала, принятая в физике , – это не водородная шкала, а шкала давлений идеального газа. 56
 ТЕМПЕРАТУРА И ТЕПЛОТА Уравнение состояния газов Именно это обстоятельство и оправдывает сде лан ный выбор способа определения тем пе ра ту ры : большой класс веществ приводит к тем пе ра тур ным шкалам , в точности совпадаю щим. 57
ТЕМПЕРАТУРА И ТЕПЛОТА Уравнение состояния газов Именно это обстоятельство и оправдывает сде лан ный выбор способа определения тем пе ра ту ры : большой класс веществ приводит к тем пе ра тур ным шкалам , в точности совпадаю щим. 57
 ТЕМПЕРАТУРА И ТЕПЛОТА Уравнения состояния реальных газов Для газов при больших давлениях, для паров, близких к насы щению, и в ряде других случаев уравнение газового состояния на чинает давать очень грубые ошибки. В этих случаях прибегают к другим уравнениям состояния. Часть из них найдена опытным путем, некоторые (как наиболее известное из них – уравнение Ван дер Ваальса) имеют качественное теоретическое обоснование. 58
ТЕМПЕРАТУРА И ТЕПЛОТА Уравнения состояния реальных газов Для газов при больших давлениях, для паров, близких к насы щению, и в ряде других случаев уравнение газового состояния на чинает давать очень грубые ошибки. В этих случаях прибегают к другим уравнениям состояния. Часть из них найдена опытным путем, некоторые (как наиболее известное из них – уравнение Ван дер Ваальса) имеют качественное теоретическое обоснование. 58
 ТЕМПЕРАТУРА И ТЕПЛОТА Уравнения состояния реальных газов Так или иначе, ценность того или иного уравнения может быть уста новлена лишь сравнением чисел, полученных из опыта и вычислен ных из уравнения. Приведем примеры уравнений состояния. Простейшая поправка, которая может быть введена в уравнение идеальных газов, — это, конечно, учет объема газовых молекул. Оче видно, даже бесконечно большим давлением нельзя сжать газ до нулевого объема. 59
ТЕМПЕРАТУРА И ТЕПЛОТА Уравнения состояния реальных газов Так или иначе, ценность того или иного уравнения может быть уста новлена лишь сравнением чисел, полученных из опыта и вычислен ных из уравнения. Приведем примеры уравнений состояния. Простейшая поправка, которая может быть введена в уравнение идеальных газов, — это, конечно, учет объема газовых молекул. Оче видно, даже бесконечно большим давлением нельзя сжать газ до нулевого объема. 59
 ТЕМПЕРАТУРА И ТЕПЛОТА Уравнения состояния реальных газов Это оправдывает уравнение состояния вида p(v—b) = RT, где b – константа, учитывающая конечный объем молекул. Чем больше число констант, которые будут введены в уравнение состояния, тем легче добиться хорошего совпадения опытных и рас считанных исел для конкретного газа в ч конкретных условиях. Однако тем меньше предсказательные возможности формул. 60
ТЕМПЕРАТУРА И ТЕПЛОТА Уравнения состояния реальных газов Это оправдывает уравнение состояния вида p(v—b) = RT, где b – константа, учитывающая конечный объем молекул. Чем больше число констант, которые будут введены в уравнение состояния, тем легче добиться хорошего совпадения опытных и рас считанных исел для конкретного газа в ч конкретных условиях. Однако тем меньше предсказательные возможности формул. 60


