Тема: Химическая связь и ее типы Задачи


















Хим. связь её типы.ppt
- Количество слайдов: 21
 Тема: Химическая связь и ее типы
Тема: Химическая связь и ее типы
 Задачи урока n Знать классификацию типов химической связи и характеристики каждого из них. n Уметь характеризовать свойства вещества, зная тип его кристаллической решетки; по формуле вещества предполагать тип связи, предсказывать тип кристаллической решетки
Задачи урока n Знать классификацию типов химической связи и характеристики каждого из них. n Уметь характеризовать свойства вещества, зная тип его кристаллической решетки; по формуле вещества предполагать тип связи, предсказывать тип кристаллической решетки
 Под химической связью понимают такое взаимодействие атомов, которое связывает их в молекулы, ионы, радикалы, кристаллы
Под химической связью понимают такое взаимодействие атомов, которое связывает их в молекулы, ионы, радикалы, кристаллы
 Ионная химическая связь n это связь, образовавшаяся за счет электростатического притяжения катионов к анионам Задание: Выпишите формулы веществ с ионной связью. РС 13; С 2 Н 2; Na 3 P; СС 14 Mg. Cl 2; СН 4; K 3 N; Na. Br.
Ионная химическая связь n это связь, образовавшаяся за счет электростатического притяжения катионов к анионам Задание: Выпишите формулы веществ с ионной связью. РС 13; С 2 Н 2; Na 3 P; СС 14 Mg. Cl 2; СН 4; K 3 N; Na. Br.
 Характеристика ионной связи n 1) ненаправленность - ион может притягиваться к противоположно заряженному иону по любому направлению; n 2) ненасыщаемостью - не теряется способность притягивать ионы по другим направлениям. n не бывает абсолютной, она остается частично ковалентной, характеризуется степенью ионности. n Одно из самых ионных соединений - фторид лития является ионным на 89%. В растворах и расплавах происходит диссоциация и вещества становятся ионными почти на 100%.
Характеристика ионной связи n 1) ненаправленность - ион может притягиваться к противоположно заряженному иону по любому направлению; n 2) ненасыщаемостью - не теряется способность притягивать ионы по другим направлениям. n не бывает абсолютной, она остается частично ковалентной, характеризуется степенью ионности. n Одно из самых ионных соединений - фторид лития является ионным на 89%. В растворах и расплавах происходит диссоциация и вещества становятся ионными почти на 100%.
 ИОННАЯ кристаллическая решетка Ионными называют кристаллические решетки, в узлах которых находятся ионы. Их образуют вещества с ионной связью. Ионные кристаллические решётки имеют соли, некоторые оксиды и гидроксиды металлов. Связи между ионами в кристалле очень прочные и устойчивые. Вещества с ионной решёткой обладают высокой твёрдостью и прочностью, тугоплавки и нелетучи.
ИОННАЯ кристаллическая решетка Ионными называют кристаллические решетки, в узлах которых находятся ионы. Их образуют вещества с ионной связью. Ионные кристаллические решётки имеют соли, некоторые оксиды и гидроксиды металлов. Связи между ионами в кристалле очень прочные и устойчивые. Вещества с ионной решёткой обладают высокой твёрдостью и прочностью, тугоплавки и нелетучи.
 Водородная связь n Химическая связь между положительно поляризованными атомами водорода одной молекулы (или ее части) и отрицательно поляризованными атомами сильно электроотрицательных элементов, имеющих неподеленные электронные пары (F, О, N и реже С 1 и S) другой молекулы (или ее части) O H…. . O H…. H H
Водородная связь n Химическая связь между положительно поляризованными атомами водорода одной молекулы (или ее части) и отрицательно поляризованными атомами сильно электроотрицательных элементов, имеющих неподеленные электронные пары (F, О, N и реже С 1 и S) другой молекулы (или ее части) O H…. . O H…. H H
 Водородная связь n Имеет частично электростатический, частично донорно-акцепторный характер. n Различают: межмолекулярную – этиловый спирт, карбоновые кислоты, вода, аммиак, фтороводород. n Внутримолекулярную: белки, ДНК- принцип комлиментарности.
Водородная связь n Имеет частично электростатический, частично донорно-акцепторный характер. n Различают: межмолекулярную – этиловый спирт, карбоновые кислоты, вода, аммиак, фтороводород. n Внутримолекулярную: белки, ДНК- принцип комлиментарности.
 Характеристика водородной связи n Водородная связь, обладает направленностью и насыщаемостью. Энергия водородной связи значительно ниже, чем ковалентной.
Характеристика водородной связи n Водородная связь, обладает направленностью и насыщаемостью. Энергия водородной связи значительно ниже, чем ковалентной.
 Молекулярные- кристаллические решетки МКР - в узлах располагаются молекулы. Химические связи в них водородные и ковалентные, как полярные, так и неполярные. Связи в молекулах прочные, но между молекулами связи не прочные. Вещества с МКР имеют малую твёрдость, плавятся при низкой температуре, летучие, при обычных условиях находятся в газообразном или жидком состоянии
Молекулярные- кристаллические решетки МКР - в узлах располагаются молекулы. Химические связи в них водородные и ковалентные, как полярные, так и неполярные. Связи в молекулах прочные, но между молекулами связи не прочные. Вещества с МКР имеют малую твёрдость, плавятся при низкой температуре, летучие, при обычных условиях находятся в газообразном или жидком состоянии
 Металлическая связь n связь в металлах и сплавах, которую выполняют относительно свободные электроны между ионами металлов в металлической кристаллической решетке Схема образования металлической связи: о п+ М — пе М Задание: Выпишите формулы веществ, в которых присутствует металлическая и водородная связи Na, KF, NH 3, C 2 H 2, CH 3 -COOH, H 2 S, AL, Na. CL.
Металлическая связь n связь в металлах и сплавах, которую выполняют относительно свободные электроны между ионами металлов в металлической кристаллической решетке Схема образования металлической связи: о п+ М — пе М Задание: Выпишите формулы веществ, в которых присутствует металлическая и водородная связи Na, KF, NH 3, C 2 H 2, CH 3 -COOH, H 2 S, AL, Na. CL.
 Домашнее задание n § 6 – ионная, водородная, металлическая связь – выучить з. в т. n Покажите механизм связи в молекулах : Ca. O, Ca. F 2, Na 2 O, Al. Cl 3, Ca
Домашнее задание n § 6 – ионная, водородная, металлическая связь – выучить з. в т. n Покажите механизм связи в молекулах : Ca. O, Ca. F 2, Na 2 O, Al. Cl 3, Ca
 Металлические – кристаллические решетки Металлическими называют решётки, в узлах которых находятся атомы и ионы металла. Для металлов характерны физические свойства: пластичность, ковкость, металлический блеск, высокая электро- и теплопроводность
Металлические – кристаллические решетки Металлическими называют решётки, в узлах которых находятся атомы и ионы металла. Для металлов характерны физические свойства: пластичность, ковкость, металлический блеск, высокая электро- и теплопроводность
 Ковалентная химическая связь n это связь, возникающая между атомами за счет образования общих электронных пар • Обменный Механизм образования связи: • Донорно-акцепторный
Ковалентная химическая связь n это связь, возникающая между атомами за счет образования общих электронных пар • Обменный Механизм образования связи: • Донорно-акцепторный
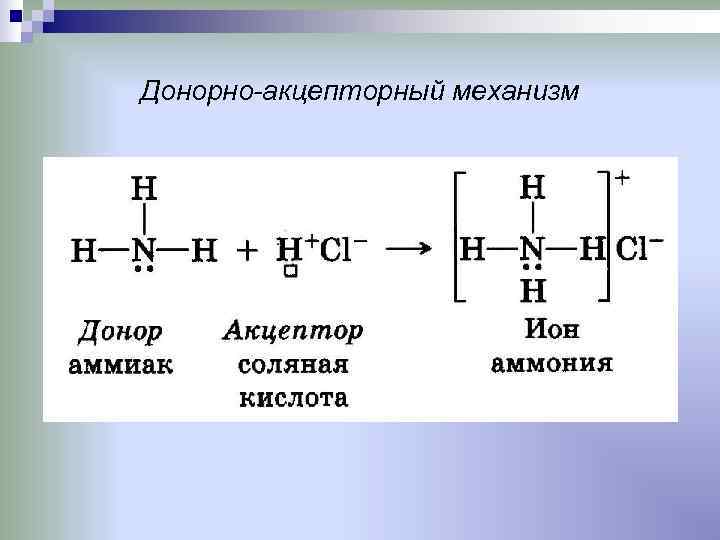
 Донорно-акцепторный механизм
Донорно-акцепторный механизм
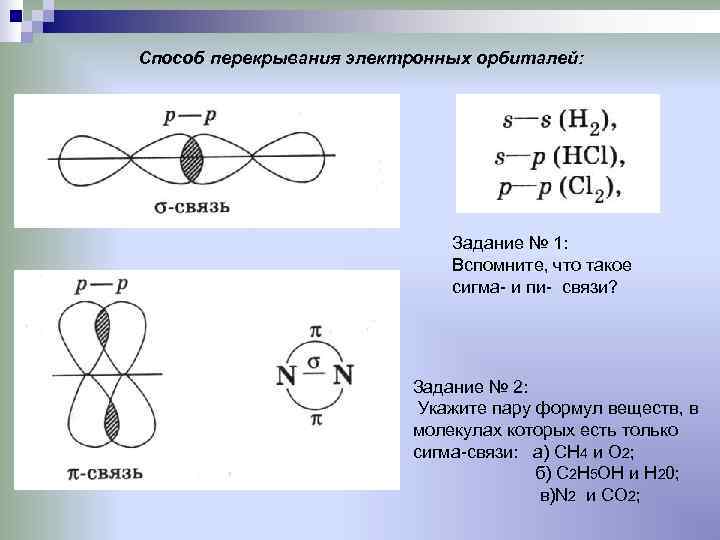
 Способ перекрывания электронных орбиталей: Задание № 1: Вспомните, что такое сигма- и пи- связи? Задание № 2: Укажите пару формул веществ, в молекулах которых есть только сигма-связи: а) СН 4 и О 2; б) С 2 Н 5 ОН и Н 20; в)N 2 и CO 2;
Способ перекрывания электронных орбиталей: Задание № 1: Вспомните, что такое сигма- и пи- связи? Задание № 2: Укажите пару формул веществ, в молекулах которых есть только сигма-связи: а) СН 4 и О 2; б) С 2 Н 5 ОН и Н 20; в)N 2 и CO 2;
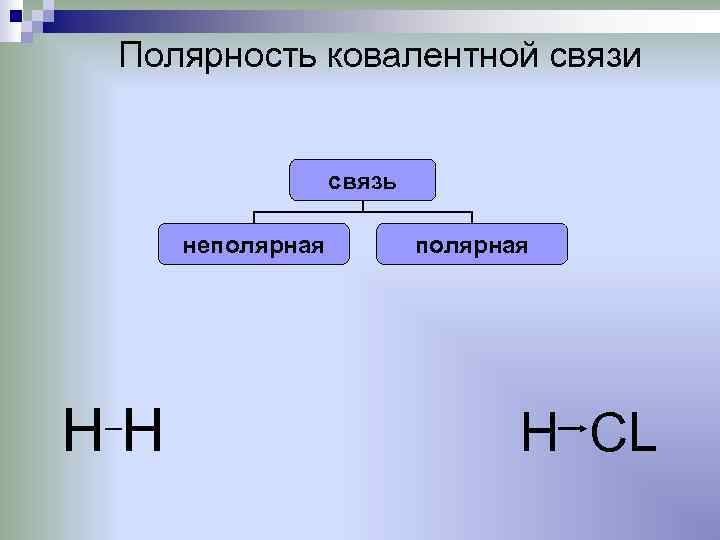
 Полярность ковалентной связи связь неполярная HH H СL
Полярность ковалентной связи связь неполярная HH H СL
 Ковалентную химическую связь, образующуюся между атомами с одинаковой электроотрицательностью, называют неполярной Ковалентную химическую связь, образующуюся между атомами с разной электроотрицательностью, называют полярной. Электроотрицательность (ЭО) — свойство оттягивать к себе валентные электроны от других атомов
Ковалентную химическую связь, образующуюся между атомами с одинаковой электроотрицательностью, называют неполярной Ковалентную химическую связь, образующуюся между атомами с разной электроотрицательностью, называют полярной. Электроотрицательность (ЭО) — свойство оттягивать к себе валентные электроны от других атомов
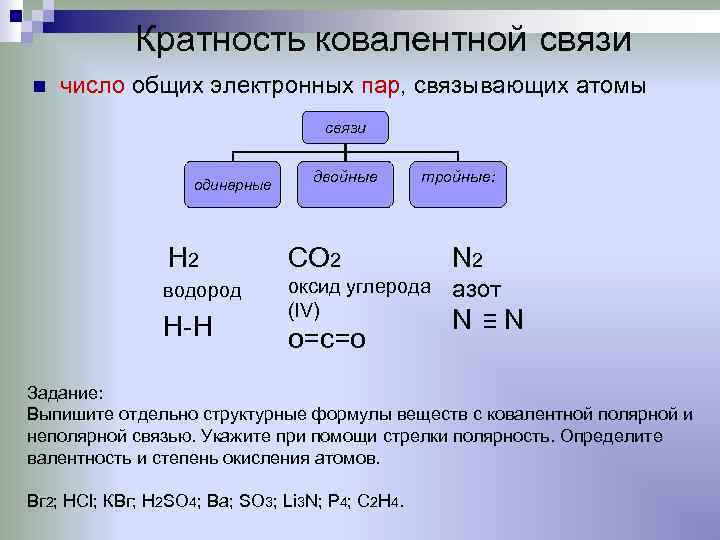
 Кратность ковалентной связи n число общих электронных пар, связывающих атомы связи двойные тройные: одинарные H 2 CO 2 N 2 водород оксид углерода азот (IV) H-H N N о=с=о Задание: Выпишите отдельно структурные формулы веществ с ковалентной полярной и неполярной связью. Укажите при помощи стрелки полярность. Определите валентность и степень окисления атомов. Вг 2; НСl; КВг; H 2 SO 4; Ba; SO 3; Li 3 N; P 4; C 2 H 4.
Кратность ковалентной связи n число общих электронных пар, связывающих атомы связи двойные тройные: одинарные H 2 CO 2 N 2 водород оксид углерода азот (IV) H-H N N о=с=о Задание: Выпишите отдельно структурные формулы веществ с ковалентной полярной и неполярной связью. Укажите при помощи стрелки полярность. Определите валентность и степень окисления атомов. Вг 2; НСl; КВг; H 2 SO 4; Ba; SO 3; Li 3 N; P 4; C 2 H 4.
 Атомные – кристаллические решетки АКР - в узлах находятся отдельные атомы, которые соединены очень прочными ковалентными связями. Вещества с АКР имеют высокие температуры плавления, обладают повышенной твёрдостью. Алмаз - самый твёрдый природный материал. бор, кремний, германий, кварц.
Атомные – кристаллические решетки АКР - в узлах находятся отдельные атомы, которые соединены очень прочными ковалентными связями. Вещества с АКР имеют высокие температуры плавления, обладают повышенной твёрдостью. Алмаз - самый твёрдый природный материал. бор, кремний, германий, кварц.
 Самостоятельная работа n Определите типы химических связей между атомами в веществах. Ca. Вг 2; НСl; К; H 2 SO 3; Ba. O; SO 2; Li. NО 3; S 2; C 2 H 2; Na; HCОOК.
Самостоятельная работа n Определите типы химических связей между атомами в веществах. Ca. Вг 2; НСl; К; H 2 SO 3; Ba. O; SO 2; Li. NО 3; S 2; C 2 H 2; Na; HCОOК.

