Тема уроку(химия).pptx
- Количество слайдов: 27
 Тема уроку: Валентність хімічних елементів. Визначення валентності
Тема уроку: Валентність хімічних елементів. Визначення валентності
 Очікувані результати: Вивчити поняття валентності; Навчитися визначати валентність; Складати формули сполук за валентністю.
Очікувані результати: Вивчити поняття валентності; Навчитися визначати валентність; Складати формули сполук за валентністю.
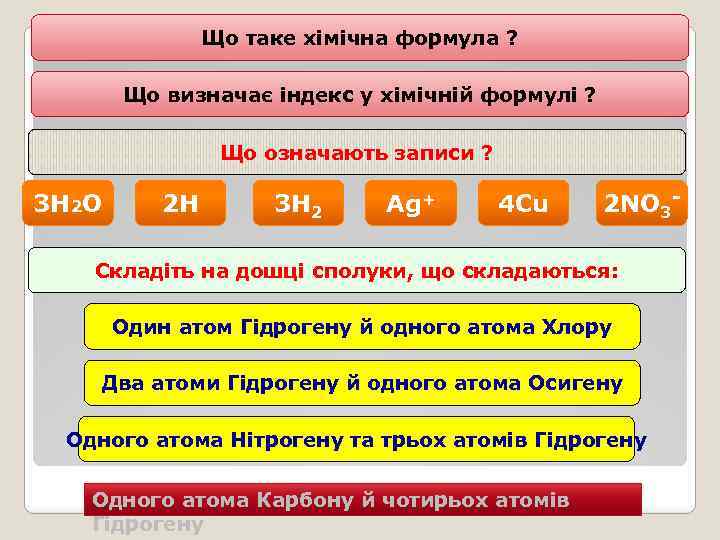 Що таке хімічна формула ? Що визначає індекс у хімічній формулі ? Що означають записи ? 3 H 2 O 2 H 3 H 2 Ag+ 4 Cu 2 NO 3 - Складіть на дошці сполуки, що складаються: Один атом Гідрогену й одного атома Хлору Два атоми Гідрогену й одного атома Осигену Одного атома Нітрогену та трьох атомів Гідрогену Одного атома Карбону й чотирьох атомів Гідрогену
Що таке хімічна формула ? Що визначає індекс у хімічній формулі ? Що означають записи ? 3 H 2 O 2 H 3 H 2 Ag+ 4 Cu 2 NO 3 - Складіть на дошці сполуки, що складаються: Один атом Гідрогену й одного атома Хлору Два атоми Гідрогену й одного атома Осигену Одного атома Нітрогену та трьох атомів Гідрогену Одного атома Карбону й чотирьох атомів Гідрогену
 Fe(OH) KHCO Ag. NO Na. OH Ba(NO ) Ca. CO HP CH PO SO 3 3 2 3 4 4 43 3 2 3 Прочитайте формули речовин
Fe(OH) KHCO Ag. NO Na. OH Ba(NO ) Ca. CO HP CH PO SO 3 3 2 3 4 4 43 3 2 3 Прочитайте формули речовин
 За хімічною формулою речовини ми отримуємо відомості про склад речовини, а за складом речовини можемо записати її хімічну формулу. Але ж речовин дуже багато. Чи можна запам‘ятати склад і формули всіх речовин? Чи потрібно це робити? Необхідно вивчити закономірності, за якими без проблем можна записувати безліч хімічних формул.
За хімічною формулою речовини ми отримуємо відомості про склад речовини, а за складом речовини можемо записати її хімічну формулу. Але ж речовин дуже багато. Чи можна запам‘ятати склад і формули всіх речовин? Чи потрібно це робити? Необхідно вивчити закономірності, за якими без проблем можна записувати безліч хімічних формул.
 Зверніть Ще три сотні років тому вчені встановили, що атоми з'єднуються в увагу молекули не безладно, а в певній послідовності за допомогою зв'язків, які називають хімічними. Тоді атоми уявляли у вигляді кульок, що мають “гачки”, за допомогою яких вони сполучались один з одним. Тільки багато років потому була встановлена істина природа хімічного зв‘язку.
Зверніть Ще три сотні років тому вчені встановили, що атоми з'єднуються в увагу молекули не безладно, а в певній послідовності за допомогою зв'язків, які називають хімічними. Тоді атоми уявляли у вигляді кульок, що мають “гачки”, за допомогою яких вони сполучались один з одним. Тільки багато років потому була встановлена істина природа хімічного зв‘язку.
 Як Ви вважаєте Атом може з'єднуватись з визначеною кількістю атомів, чи кількість таких зв'язків необмежена?
Як Ви вважаєте Атом може з'єднуватись з визначеною кількістю атомів, чи кількість таких зв'язків необмежена?
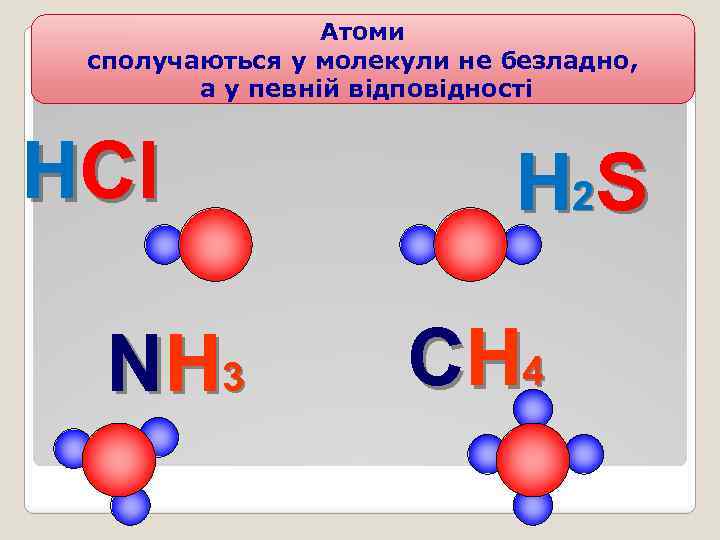 Атоми сполучаються у молекули не безладно, а у певній відповідності HCl NH 3 H 2 S CH 4
Атоми сполучаються у молекули не безладно, а у певній відповідності HCl NH 3 H 2 S CH 4
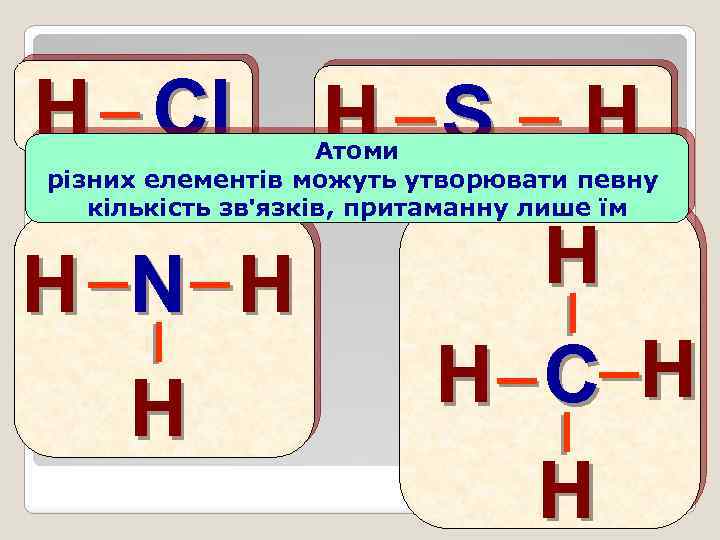 _ Cl H _S _ H H Атоми різних елементів можуть утворювати певну кількість зв'язків, притаманну лише їм _ _ _ _ H N H H _ C_H H H
_ Cl H _S _ H H Атоми різних елементів можуть утворювати певну кількість зв'язків, притаманну лише їм _ _ _ _ H N H H _ C_H H H
 Виходячи з кількості хімічних зв'язків, що утворює атом даного елементу, зробіть визначення “ВАЛЕНТНОСТІ”.
Виходячи з кількості хімічних зв'язків, що утворює атом даного елементу, зробіть визначення “ВАЛЕНТНОСТІ”.
 Властивість атомів приєднувати до себе певну кількість атомів того самого чи іншого хімічного елемент називається ВАЛЕНТНІСТЮ a Валентність кількість зв'язків, що утворює даний атом, поєднуючись з іншими атомами
Властивість атомів приєднувати до себе певну кількість атомів того самого чи іншого хімічного елемент називається ВАЛЕНТНІСТЮ a Валентність кількість зв'язків, що утворює даний атом, поєднуючись з іншими атомами
 Яким же чином ми можемо визначити валентність елемента і від чого вона залежить?
Яким же чином ми можемо визначити валентність елемента і від чого вона залежить?
 Валентність залежить від будови атома і визначається за положенням у періодичній системі. Валентність Стала Змінна Валентність (Н) = І Максимальна валентність = № групи. (виключення О = ІІ, Fe = ІІ, ІІІ) Валентність (О) = ІІ Валентність (F) = І Валентність елементів І, ІІІ груп = № групи (виключення Cu = I і ІІ) Мінімальна валентність ( неметалів у сполуках із металами і Н) = 8 – № групи. Проміжні валентності = максимальна валентність мінус числа кратні двом. У бінарних сполуках сумарна валентність усіх атомів одного елемента завжди дорівнює сумарній валентності усіх атомів другого елемента
Валентність залежить від будови атома і визначається за положенням у періодичній системі. Валентність Стала Змінна Валентність (Н) = І Максимальна валентність = № групи. (виключення О = ІІ, Fe = ІІ, ІІІ) Валентність (О) = ІІ Валентність (F) = І Валентність елементів І, ІІІ груп = № групи (виключення Cu = I і ІІ) Мінімальна валентність ( неметалів у сполуках із металами і Н) = 8 – № групи. Проміжні валентності = максимальна валентність мінус числа кратні двом. У бінарних сполуках сумарна валентність усіх атомів одного елемента завжди дорівнює сумарній валентності усіх атомів другого елемента
 Валентність атомів позначається римськими цифрами, які розташовуються над елементом IV II III С О 2 Al 2 О 3 II
Валентність атомів позначається римськими цифрами, які розташовуються над елементом IV II III С О 2 Al 2 О 3 II
 Н Окремі атоми Валентність характеризує тільки ті не мають валентності атоми, що поєдналися між собою Будова забезпечує їх потенційні можливості Валентність (О) - ІІ Валентність (Н) - І Н Чи мають валентність окремі Н атоми ? Н О І ІІ H 2 O 2 2× 1=2 Кількість валентностей Оксигену дорівнює сумарній валентності Гідрогену
Н Окремі атоми Валентність характеризує тільки ті не мають валентності атоми, що поєдналися між собою Будова забезпечує їх потенційні можливості Валентність (О) - ІІ Валентність (Н) - І Н Чи мають валентність окремі Н атоми ? Н О І ІІ H 2 O 2 2× 1=2 Кількість валентностей Оксигену дорівнює сумарній валентності Гідрогену
 O N O Валентність атомів елементів зі змінною валентністю N N O залежить від того, H H якими атомами і в якому кількісному співвідношенні вони поєдналися H N N O Розглянемо сполуки Сульфуру
O N O Валентність атомів елементів зі змінною валентністю N N O залежить від того, H H якими атомами і в якому кількісному співвідношенні вони поєдналися H N N O Розглянемо сполуки Сульфуру
 Виходячи із розташування у періодичній системі, атоми Сульфуру можуть виявляти валентність ІІ, ІV, VІ Н Валентністьть (S) = ІІ Валентність (Н) = І Н І S ІІ H 2 S 2 2× 1=2 Кількість валентностей Сульфуру дорівнює сумарній валентності Гідрогену
Виходячи із розташування у періодичній системі, атоми Сульфуру можуть виявляти валентність ІІ, ІV, VІ Н Валентністьть (S) = ІІ Валентність (Н) = І Н І S ІІ H 2 S 2 2× 1=2 Кількість валентностей Сульфуру дорівнює сумарній валентності Гідрогену
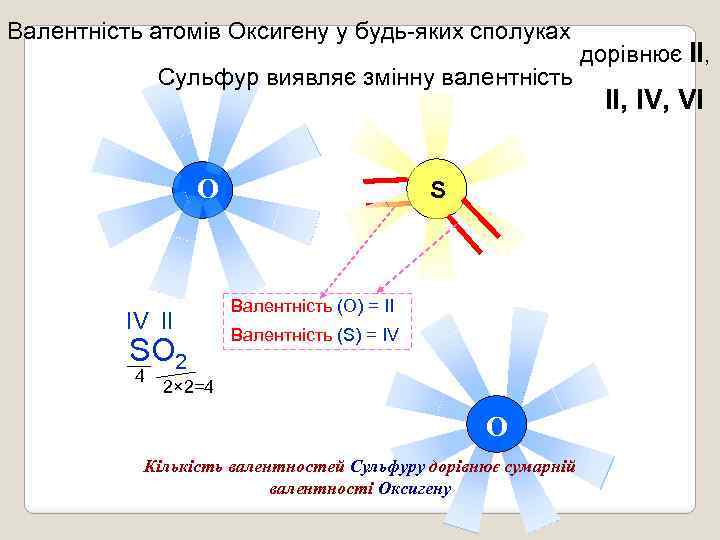 Валентність атомів Оксигену у будь-яких сполуках Сульфур виявляє змінну валентність O O S O ІV ІІ SO 2 4 Валентність (О) = IІ Валентність (S) = IV 2× 2=4 O Кількість валентностей Сульфуру дорівнює сумарній валентності Оксигену дорівнює ІІ, ІV, VI
Валентність атомів Оксигену у будь-яких сполуках Сульфур виявляє змінну валентність O O S O ІV ІІ SO 2 4 Валентність (О) = IІ Валентність (S) = IV 2× 2=4 O Кількість валентностей Сульфуру дорівнює сумарній валентності Оксигену дорівнює ІІ, ІV, VI
 Алгоритм складання хімічних формул за валентністю. Правило знаходження валентності: - У металів валентність визначається за номером групи. - У неметалу, що стоїть на першому місці в формулі, ставиться вища валентність. - У неметалу, що стоїть на другому місці в формулі, ставиться нижча валентність. Приклад: V I VI 1 10 2 6 0 II Na O P S Порядок дій: 1. Визначаємо хімічних елементівх хімічних елементів. 2. Знаходимо спільне кратне. валентність элементов. найменше 3. Находимо індекси. Знаходимо індекси. 2 : =2 =2 =1 1 : =1 5 3
Алгоритм складання хімічних формул за валентністю. Правило знаходження валентності: - У металів валентність визначається за номером групи. - У неметалу, що стоїть на першому місці в формулі, ставиться вища валентність. - У неметалу, що стоїть на другому місці в формулі, ставиться нижча валентність. Приклад: V I VI 1 10 2 6 0 II Na O P S Порядок дій: 1. Визначаємо хімічних елементівх хімічних елементів. 2. Знаходимо спільне кратне. валентність элементов. найменше 3. Находимо індекси. Знаходимо індекси. 2 : =2 =2 =1 1 : =1 5 3
 II III Al O 2 3
II III Al O 2 3
 II II Ca O __ __
II II Ca O __ __
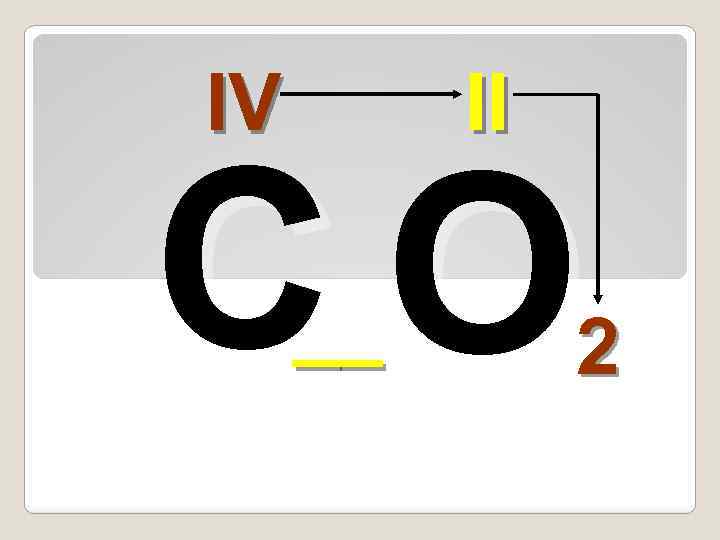 IV II СO __ 2
IV II СO __ 2
 Увага ! Складаючи хімічні формули бінарних сполук враховуйте порядок написання символів елементів у формулі. На першому місці записується символ того елемента, який у Періодичній системі розташований зліва або нижче порівняно з іншим. (виключення: метали з Гідрогеном – Na. H, Са. Н 2; NH 3, РН 3; Cl 2 O 7).
Увага ! Складаючи хімічні формули бінарних сполук враховуйте порядок написання символів елементів у формулі. На першому місці записується символ того елемента, який у Періодичній системі розташований зліва або нижче порівняно з іншим. (виключення: метали з Гідрогеном – Na. H, Са. Н 2; NH 3, РН 3; Cl 2 O 7).
 Застосуємо набуті знання на практиці Складіть формули сполук за їх валентністю: KO, Ca. Cl, Al. Cl, Na. S, Cu. O, Mg. S Складіть формули бінарних сполук з Оксигеном: Натрію; Карбону (ІІ); Феруму (ІІІ); Нітрогену (V).
Застосуємо набуті знання на практиці Складіть формули сполук за їх валентністю: KO, Ca. Cl, Al. Cl, Na. S, Cu. O, Mg. S Складіть формули бінарних сполук з Оксигеном: Натрію; Карбону (ІІ); Феруму (ІІІ); Нітрогену (V).
 Домашнє завдання: • Ознайомитись з матеріалом 10 параграфу підручника; • Виконати вправи 80, 83;
Домашнє завдання: • Ознайомитись з матеріалом 10 параграфу підручника; • Виконати вправи 80, 83;
 Підведемо підсумки уроку З якою метою ми вивчали валентність хімічних елементів? Чи досягли ми мети? Чи навчилися складати хімічні формули сполук? Що необхідно знати для складання формул? Оцініть результати своєї діяльності задовільно добре відмінно
Підведемо підсумки уроку З якою метою ми вивчали валентність хімічних елементів? Чи досягли ми мети? Чи навчилися складати хімічні формули сполук? Що необхідно знати для складання формул? Оцініть результати своєї діяльності задовільно добре відмінно
 Я дізнався… Я навчився… Вільний мікрофон
Я дізнався… Я навчився… Вільний мікрофон


