Неметаллы общие свойства.ppt
- Количество слайдов: 31
 Тема урока: «Простые вещества – неметаллы. Аллотропия»
Тема урока: «Простые вещества – неметаллы. Аллотропия»
 Цели урока: • Получить представление о простых веществах – неметаллах; • Познакомиться с общими физическими свойствами неметаллов и явлением аллотропии; • Научиться определять принадлежность веществ к неметаллам;
Цели урока: • Получить представление о простых веществах – неметаллах; • Познакомиться с общими физическими свойствами неметаллов и явлением аллотропии; • Научиться определять принадлежность веществ к неметаллам;
 Проверка домашнего задания. 1. Где в периодической системе находятся элементы, соответствующие простым веществам металлам?
Проверка домашнего задания. 1. Где в периодической системе находятся элементы, соответствующие простым веществам металлам?
 2. Каковы общие физические свойства металлов?
2. Каковы общие физические свойства металлов?
 3. По каким физическим свойствам различаются металлы?
3. По каким физическим свойствам различаются металлы?
 4. Какое из веществ названных в приведённом ниже стихотворении, не относится к металлам? Семь металлов создал Свет По числу семи планет: Медь, железо, серебро… Дал нам Космос на добро. Злато, олово, свинец… Сын мой, сера - их отец. А ещё ты должен знать: Всем им ртуть – родная мать.
4. Какое из веществ названных в приведённом ниже стихотворении, не относится к металлам? Семь металлов создал Свет По числу семи планет: Медь, железо, серебро… Дал нам Космос на добро. Злато, олово, свинец… Сын мой, сера - их отец. А ещё ты должен знать: Всем им ртуть – родная мать.
 Изучение новой темы. «Простые вещества – неметаллы. Аллотропия»
Изучение новой темы. «Простые вещества – неметаллы. Аллотропия»
 • Неметаллы - это химические элементы, которые образуют в свободном виде простые вещества, не обладающие физическими свойствами металлов.
• Неметаллы - это химические элементы, которые образуют в свободном виде простые вещества, не обладающие физическими свойствами металлов.
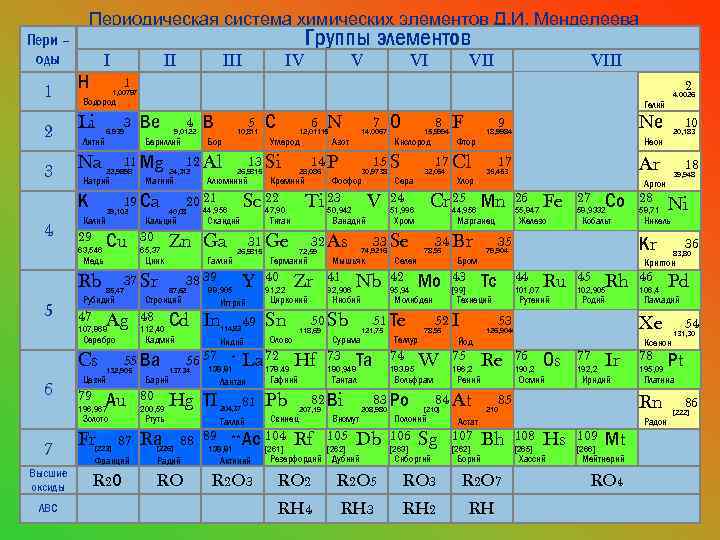 Периодическая система химических элементов Д. И. Менделеева Пери – оды 1 I Н Na Литий 3 6. 939 Калий 29 39, 102 Сu Медь Rb Бериллий Ag Серебро Cs Цезий 55 Ва 132, 905 196, 967 Золото Fr 112, 40 [223] Алюминий Иттрий Сd In 114, 82 80 200, 59 Rа Hg ТI [226] * 138, 81 VIII VII 204, 37 Таллий 32 As 72, 59 Zr Цирконий Sn Мышьяк 41 92, 906 Nb Сурьма 73 Свинец 121, 75 Та Rf [262] 51, 996 Селен 42 95, 94 Теллур 183. 85 34 Br Мо Db Дубний [263] Fe 27 Со 58, 9332 Кобальт 52 I 44 101, 07 Ru Рутений 45 Rh 102, 905 Родий 75 186, 2 Re Рений 84 At Sg Сиборгий 76 190, 2 Оs Осмий 77 192, 2 Ir Иридий [262] Bh Франций Радий Актиний Резерфордий Борий R 2 О RO R 2 O 3 RO 2 R 2 O 5 RO 3 R 2 O 7 RH 4 RH 3 RH 2 RH Ni Никель 46 106, 4 36 83, 80 Pd Палладий 78 195, 09 108 [265] Hs Хассий 109 [266] 54 Мt Мейтнерий RO 4 131, 30 Рt Платина Rn 85 Астат 107 58, 71 Ксенон 210 [210] 28 Xe 126, 9044 Йод W Аргон Криптон 53 78, 96 18 39, 948 Кr 35 Технеций Полоний 106 55, 847 Железо Тс [99] 26 79, 904 Бром 43 Ar 17 Хлор 10 20, 183 Неон 35, 453 Марганец Вольфрам 208, 980 Фтор 44, 956 78, 96 Nе 9 18, 9984 Cr 25 Мn 24 83 Ро Висмут 105 Сера 74 180, 948 F 17 Cl 32, 064 Молибден Тантал 207, 19 Кислород 51 Тe 82 Вi Pb 8 15, 9994 33 Se 74, 9216 50 Sb Гафний О Хром Ниобий 118, 69 Олово 88 89 ** Ас 104 138, 81 [261] V Ванадий 178. 49 81 Фосфор 2 4. 0026 Гелий 15 S 30, 9738 50, 942 Германий 91, 22 Азот Ti 23 La 72 Hf Лантан Ртуть 87 49 Индий Барий Кремний 40 7 14, 0067 14 P 28, 086 31 Ge Y N 12, 01115 Титан 26, 9815 88, 905 56 57 Углерод 47, 90 Скандий 38 39 137. 34 6 Sc 22 44, 956 Галлий 87, 62 С 13 Si 26, 9815 Zn Ga Стронций 48 Бор Кадмий Аu 79 65, 37 5 10, 811 20 21 40, 08 Кальций 30 В 12 Al 24, 312 Магний 37 Sr 85, 47 Рубидий 47 4 9, 0122 Цинк 107, 868 ЛВС Ве 19 Сa 63, 546 Высшие оксиды VI Не 11 Мg 22, 9898 Натрий К 7 V Водород 3 6 IV 1 Li 5 III 1, 00797 2 4 II Группы элементов Радон 86 [222]
Периодическая система химических элементов Д. И. Менделеева Пери – оды 1 I Н Na Литий 3 6. 939 Калий 29 39, 102 Сu Медь Rb Бериллий Ag Серебро Cs Цезий 55 Ва 132, 905 196, 967 Золото Fr 112, 40 [223] Алюминий Иттрий Сd In 114, 82 80 200, 59 Rа Hg ТI [226] * 138, 81 VIII VII 204, 37 Таллий 32 As 72, 59 Zr Цирконий Sn Мышьяк 41 92, 906 Nb Сурьма 73 Свинец 121, 75 Та Rf [262] 51, 996 Селен 42 95, 94 Теллур 183. 85 34 Br Мо Db Дубний [263] Fe 27 Со 58, 9332 Кобальт 52 I 44 101, 07 Ru Рутений 45 Rh 102, 905 Родий 75 186, 2 Re Рений 84 At Sg Сиборгий 76 190, 2 Оs Осмий 77 192, 2 Ir Иридий [262] Bh Франций Радий Актиний Резерфордий Борий R 2 О RO R 2 O 3 RO 2 R 2 O 5 RO 3 R 2 O 7 RH 4 RH 3 RH 2 RH Ni Никель 46 106, 4 36 83, 80 Pd Палладий 78 195, 09 108 [265] Hs Хассий 109 [266] 54 Мt Мейтнерий RO 4 131, 30 Рt Платина Rn 85 Астат 107 58, 71 Ксенон 210 [210] 28 Xe 126, 9044 Йод W Аргон Криптон 53 78, 96 18 39, 948 Кr 35 Технеций Полоний 106 55, 847 Железо Тс [99] 26 79, 904 Бром 43 Ar 17 Хлор 10 20, 183 Неон 35, 453 Марганец Вольфрам 208, 980 Фтор 44, 956 78, 96 Nе 9 18, 9984 Cr 25 Мn 24 83 Ро Висмут 105 Сера 74 180, 948 F 17 Cl 32, 064 Молибден Тантал 207, 19 Кислород 51 Тe 82 Вi Pb 8 15, 9994 33 Se 74, 9216 50 Sb Гафний О Хром Ниобий 118, 69 Олово 88 89 ** Ас 104 138, 81 [261] V Ванадий 178. 49 81 Фосфор 2 4. 0026 Гелий 15 S 30, 9738 50, 942 Германий 91, 22 Азот Ti 23 La 72 Hf Лантан Ртуть 87 49 Индий Барий Кремний 40 7 14, 0067 14 P 28, 086 31 Ge Y N 12, 01115 Титан 26, 9815 88, 905 56 57 Углерод 47, 90 Скандий 38 39 137. 34 6 Sc 22 44, 956 Галлий 87, 62 С 13 Si 26, 9815 Zn Ga Стронций 48 Бор Кадмий Аu 79 65, 37 5 10, 811 20 21 40, 08 Кальций 30 В 12 Al 24, 312 Магний 37 Sr 85, 47 Рубидий 47 4 9, 0122 Цинк 107, 868 ЛВС Ве 19 Сa 63, 546 Высшие оксиды VI Не 11 Мg 22, 9898 Натрий К 7 V Водород 3 6 IV 1 Li 5 III 1, 00797 2 4 II Группы элементов Радон 86 [222]
 Неметаллы Газообразные Жидкие Твёрдые
Неметаллы Газообразные Жидкие Твёрдые
 Газообразные вещества неметаллы: • • • О 2 N 2 H 2 Cl 2 F 2 -
Газообразные вещества неметаллы: • • • О 2 N 2 H 2 Cl 2 F 2 -
 N 2 Cl 2 F 2 В начало
N 2 Cl 2 F 2 В начало
 благородные газы: He Ne Ar Kr Xe Rn - • Инертные газы • Каждая молекула инертного газа состоит из одного атома. • Покажите как распределяются электроны в атомах гелия и неона.
благородные газы: He Ne Ar Kr Xe Rn - • Инертные газы • Каждая молекула инертного газа состоит из одного атома. • Покажите как распределяются электроны в атомах гелия и неона.
 Строение внешнего электронного слоя атомов гелия и неона He ) +10 Ne ) ) +2 2 2 8
Строение внешнего электронного слоя атомов гелия и неона He ) +10 Ne ) ) +2 2 2 8
 Применение гелия, неона и аргона.
Применение гелия, неона и аргона.
 Единственное жидкое вещество - Br 2.
Единственное жидкое вещество - Br 2.
 Твердые вещества: • • • S– P– I 2 – C– Si -
Твердые вещества: • • • S– P– I 2 – C– Si -
 Аллотропия – способность атомов одного химического элемента образовывать несколько простых веществ. Причины аллотропии: 1. Различное число атомов в молекуле; 2. Образование различных кристаллических форм.
Аллотропия – способность атомов одного химического элемента образовывать несколько простых веществ. Причины аллотропии: 1. Различное число атомов в молекуле; 2. Образование различных кристаллических форм.
 Аллотропия кислорода. Кислород и озон
Аллотропия кислорода. Кислород и озон
 Модификации кислорода. • • О 2 - кислород; бесцветный газ; не имеет запаха; плохо растворим в воде; • температура кипения-182, 9 С; • устойчивая молекула. • • О 3 – озон; газ голубого цвета; имеет резкий запах; растворяется в 10 раз лучше, чем кислород; • температура кипения -111, 9 С; • не устойчивая молекула.
Модификации кислорода. • • О 2 - кислород; бесцветный газ; не имеет запаха; плохо растворим в воде; • температура кипения-182, 9 С; • устойчивая молекула. • • О 3 – озон; газ голубого цвета; имеет резкий запах; растворяется в 10 раз лучше, чем кислород; • температура кипения -111, 9 С; • не устойчивая молекула.
 Аллотропия фосфора. Красный и белый фосфор • Р (красный фосфор) • Р 4 • (белый фосфор)
Аллотропия фосфора. Красный и белый фосфор • Р (красный фосфор) • Р 4 • (белый фосфор)
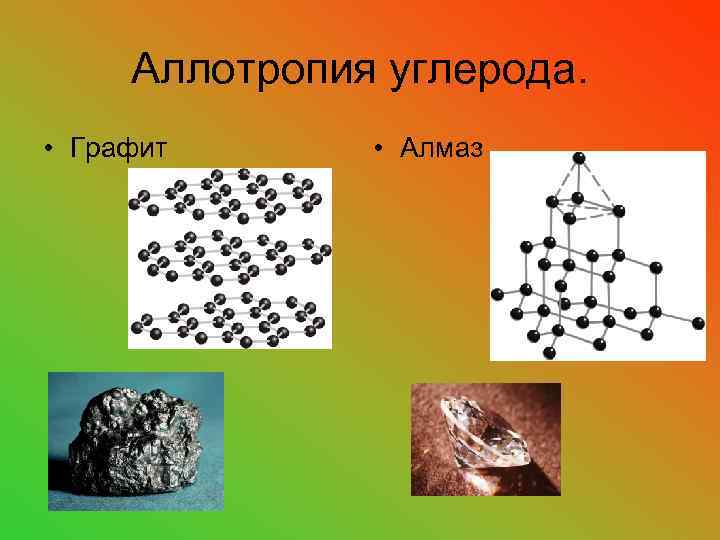 Аллотропия углерода. • Графит • Алмаз
Аллотропия углерода. • Графит • Алмаз
 Аллотропия серы. Кристаллическая, пластическая и моноклинная
Аллотропия серы. Кристаллическая, пластическая и моноклинная
 Пограничное положение между металлами и неметаллами. • Белое олово • металл • Серое олово • неметалл
Пограничное положение между металлами и неметаллами. • Белое олово • металл • Серое олово • неметалл
 Почему химически неверно поэтическое выражение: «В воздухе пахло грозой» ?
Почему химически неверно поэтическое выражение: «В воздухе пахло грозой» ?
 • Экспедиция полярного исследователя Р. Скотта к Южному полюсу в 1912 году погибла из-за того, что потеряла весь запас горючего: оно находилось в запаянных оловом баках. Какой химический процесс лежал в основе этого?
• Экспедиция полярного исследователя Р. Скотта к Южному полюсу в 1912 году погибла из-за того, что потеряла весь запас горючего: оно находилось в запаянных оловом баках. Какой химический процесс лежал в основе этого?
 • Какой тип химической связи должен быть в металлическом водороде?
• Какой тип химической связи должен быть в металлическом водороде?
 Выполните задание. • • • 1 вариант О 2 – кислород, газ; Р 4 – I 2 – Si – бетта Sn – He – H 2 – F 2 - • • • 2 вариант О 3 –озон, газ; P– C– альфа Sn – Ne – N 2 – Cl 2 – Br 2 –
Выполните задание. • • • 1 вариант О 2 – кислород, газ; Р 4 – I 2 – Si – бетта Sn – He – H 2 – F 2 - • • • 2 вариант О 3 –озон, газ; P– C– альфа Sn – Ne – N 2 – Cl 2 – Br 2 –
 Проверь ответы. • 1 вариант • О 2 – кислород, газ; • Р 4 – белый фосфор, твёрдый; • I 2 – йод, твердый • Si – кремний, твердый • бетта Sn – белое олово, металл, твёрдое; • He – гелий, благородный газ; • H 2 – водород, газ; • F 2 – фтор, газ. • 2 вариант • О 3 –озон, газ; • P – красный фосфор, твёрдый; • C – углерод, твёрдый; • альфа Sn – серое олово, неметалл, порошок; • Ne – неон, благородный газ; • N 2 – азот, газ; • Cl 2 – хлор, газ; • Br 2 – бром, жидкость.
Проверь ответы. • 1 вариант • О 2 – кислород, газ; • Р 4 – белый фосфор, твёрдый; • I 2 – йод, твердый • Si – кремний, твердый • бетта Sn – белое олово, металл, твёрдое; • He – гелий, благородный газ; • H 2 – водород, газ; • F 2 – фтор, газ. • 2 вариант • О 3 –озон, газ; • P – красный фосфор, твёрдый; • C – углерод, твёрдый; • альфа Sn – серое олово, неметалл, порошок; • Ne – неон, благородный газ; • N 2 – азот, газ; • Cl 2 – хлор, газ; • Br 2 – бром, жидкость.
 Критерии оценок • • 8 правильных ответов – « 5» ; 7, 6 првильных ответов – « 4» ; 5, 4 правильных ответов – « 3» ; Менее 4 правильных ответов – « 2» ;
Критерии оценок • • 8 правильных ответов – « 5» ; 7, 6 првильных ответов – « 4» ; 5, 4 правильных ответов – « 3» ; Менее 4 правильных ответов – « 2» ;
 Спасибо за внимание!
Спасибо за внимание!


