Предмет орг химии (для гимн).ppt
- Количество слайдов: 63

Тема урока: Понятие об органической химии.

Цель урока Выяснить: а) Что такое органическая химия? б) Как зарождалась органическая химия? в) Какова причина многообразия органических веществ?

Предмет органической химии Ú Органическая химия - это наука, изучающая соединения углерода. Однако имеется ряд соединений углерода, которые рассматриваются в неорганической химии. Это СО, СО 2, Na 2 CO 3, СS 2 и т. д. Поэтому более точное определение звучит так: Органическая химия - это химия углеводородов и их производных. Углеводороды (УВ)- это органические вещества, молекулы которых состоят из атомов двух элементов: углерода(С) и водорода (Н). Например, СН 4, С 2 Н 6.

Производные УВ – это продукты замещения атомов водорода в молекулах УВ на другие атомы или группы атомов. Например,
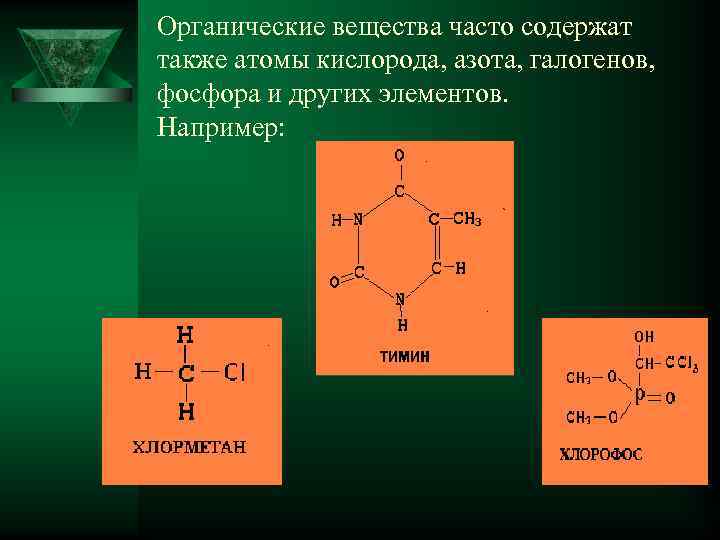
Органические вещества часто содержат также атомы кислорода, азота, галогенов, фосфора и других элементов. Например:

Ú В этом нет ничего удивительного, если подходить к этому вопросу диалектически. Природа - это единое целое, поэтому резкой границы между органическими и неорганическими веществами не существует.
Органические вещества Природные (Белки, жиры, углеводы) Искусственные (ацетатный шелк, целлулоид) Синтетические (полиэтилен, синтетические каучуки)

Когда зародилась органическая химия? Ú Органические вещества были знакомы человеку с самого начала его существования. Это пища, одежда, топливо. Затем люди научились готовить различные напитки, дубить кожу, красить предметы природными веществами. Они освоили способ варки мыла, стали использовать природные масла, сахар, крахмал, смолы.

Ú Органическая химия выделилась в самостоятельную науку в начале XIX в. , благодаря работам выдающегося шведского учёного Йенса Якоба Берцелиуса. (1779 -1848)

Состояние химической науки в первой половине XIX века Ú Органическая химия в эти годы представляла по выражению немецкого учёного Вёлера «девственный тропический лес, страшнее джунглей, в которые никто не решался проникнуть, так казалось, что из них нет выхода» .

Виталистическая теория Ú До 20 -х годов XIX в. многие учёные считали (в том числе и Й. Берцелиус), что органические вещества нельзя синтезировать в лаборатории из неорганических веществ, что они образуются только в живых организмах под действием особой «жизненной силы» . Это учение называлось витализмом ( от лат. Vita – жизнь).

Крах виталистической теории Виталистическое учение существовало недолго, потому что уже в начале и середине XIX в. были синтезированы из неорганических веществ многие органические вещества : Ú 1828 г - Вёлер синтезировал мочевину и щавелевую кислоту Ú 1842 г - Кольбе получил уксусную кислоту Ú 1850 г - Бертло синтезировал жиры Ú 1861 г - Бутлеров синтезировал углевод, похожий на глюкозу И в результате к середине XIX в. теория витализма была отвергнута большинством учёных.

Многообразие органических веществ Сейчас известно более 18 миллионов органических веществ (неорганических менее миллиона). Многие из органических веществ не существуют в природе, а получены в лаборатории химическим путём. Это каучуки, пластические массы, синтетические и искусственные волокна, лаки, красители, пестициды, лекарственные препараты – вот далеко неполный перечень органических веществ, без которых немыслимы технический и научный прогресс и благосостояние человека.

Примеры. Обои

Обувь

Парфюмерия

Бытовая и автохимия
Предметы быта

Причина многообразия органических веществ В чём же причина многообразия органических веществ? Надо полагать, что от числа химических элементов такое многообразие различных молекул веществ не зависит. Тогда от чего же?
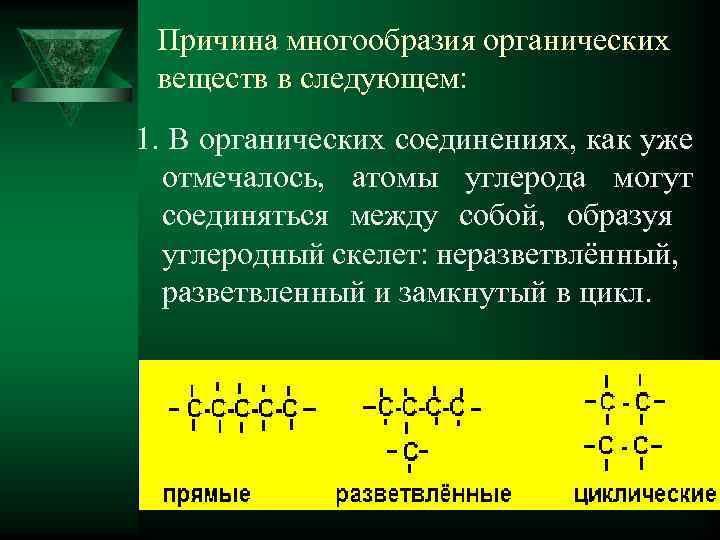
Причина многообразия органических веществ в следующем: 1. В органических соединениях, как уже отмечалось, атомы углерода могут соединяться между собой, образуя углеродный скелет: неразветвлённый, разветвленный и замкнутый в цикл.

2. Углерод может соединяться и с другими видами атомов. 3. Явление изомерии в органической химии.

Домашнее задание: § 1, Ú упр. 2, 4, 5 Ú

Предпосылки теории строения веществ: 1. Й. Берцелиус в 1830 г. открыл явление изомерии (наглядно можно посмотреть на веществе состава С 2 Н 6 О) С 2 Н 6 О СН 3 -СН 2 -О-Н Н 3 С-О-СН 3

Предпосылки теории строения веществ: 2. 3. 4. 5. 6. Ю. Либих в 1834 г. ввел теорию радикалов (частей молекул неизменных в ходе реакций). Ш. Жерар в 1848 г. ввел теорию типов (функциональных групп), т. е. установил, что свойства веществ предопределяются небольшой группой атомов. Э. Франкленд в 1853 г. ввёл понятие валентности. А. Кекуле в 1857 г. доказал, что углерод в органических соединениях 4 -х валентен и способен соединяться друг с другом, образуя прочные связи. А. Купер в 1858 г. предложил использование графических формул для изображения строения молекул органических веществ.

Ú Нужна была естественная, а не искусственные классификации веществ (теория типов, теория радикалов), так как они не опирались полностью на атомно - молекулярное учение.

Основные положения теории химического строения органических веществ А. М. Бутлерова. Ú Русский химик, академик Петербургской АН. Создатель теории химического строения органических веществ (1861). (1828 – 1886)

I положение теории химического строения Ú Атомы в молекулах органических веществ соединяются друг с другом в определённой последовательности согласно их валентности. Последовательность соединения атомов в молекуле называется химическим строением (структурой).

Химические формулы бывают: 1) эмпирические (простейшие) – показывают отношение атомов в молекуле (СН 3) 2) молекулярные - показывают только состав веществ (качественный и количественный): С 2 Н 4, С 2 Н 6 3) структурные показывают химическое строение веществ (с учётом валентности атомов в данной молекуле).

II положение теории химического строения Свойства веществ зависят не только от состава, но и от строения их молекул. Данное положение предполагает явление изомерии. Например, этанол и диэтиловый эфир имеют одну и ту же молекулярную формулу - С 2 Н 6 О, однако этанол взаимодействует с натрием, а диметиловый эфир не взаимодействует.
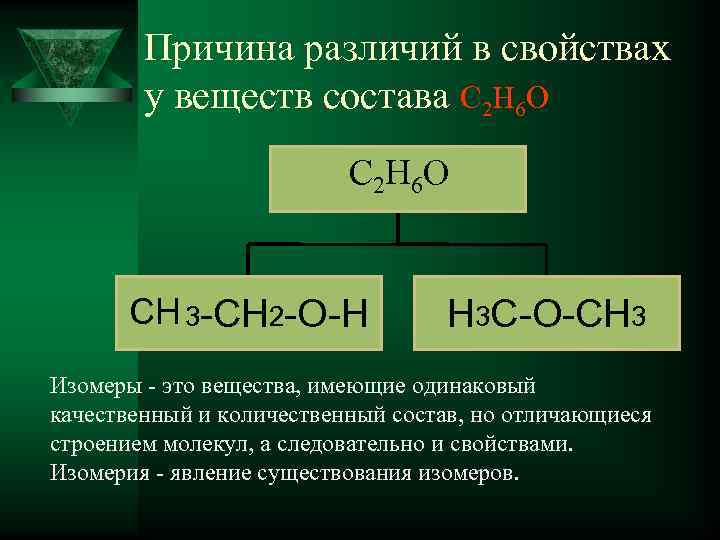
Причина различий в свойствах у веществ состава С 2 Н 6 О СН 3 -СН 2 -О-Н Н 3 С-О-СН 3 Изомеры - это вещества, имеющие одинаковый качественный и количественный состав, но отличающиеся строением молекул, а следовательно и свойствами. Изомерия - явление существования изомеров.

III положение теории химического строения В молекулах органических веществ атомы и группы атомов взаимно влияют друг на друга. Их взаимное влияние определяет свойства соединения. Это влияние передаётся через систему связей и проявляется в виде электронных эффектов (смещение электронной плотности под влиянием заместителей, радикалов и т. д. ). Рассмотрим на примере гидроксида натрия Na. OH и этанола С 2 H 5 OH.

Молекула гидроксида натрия и этанола содержат одинаковую группу –ОН. Однако первое вещество при диссоциации образует щелочную среду. Второе не диссоциирует в водном растворе и имеет нейтральную среду. Следовательно Na и С 2 Н 5 - по-разному влияют на подвижность атомов водорода в гидроксильной группе. Na – O-H С 2 Н 5 – О-Н

IV положение теории химического строения Ú По свойствам вещества можно определить строение его молекулы, а по строению - предвидеть свойства. Например, натрий из молекулы спирта этанола С 2 Н 5 ОН вытесняет только один атом водорода, хотя в молекуле спирта 6 атомов водорода. Почему?

Значение теории химического строения органических веществ Ú Эта теория существенно углубила наше представление о веществе. Ú Она не только смогла объяснить строение молекул всех известных веществ и их свойства, но и дала возможность теоретически предвидеть существование неизвестных веществ, найти пути их синтеза. Ú На сегодняшнем этапе теория А. М. Бутлерова дополнилась стереохимической теорией и электронным строением. Всё это вместе обеспечивает сегодня невиданные успехи в органическом синтезе.

Общие свойства органических веществ. Ú Во-первых, все органические вещества термически неустойчивы, т. е. при нагревании разлагаются: СН 4 → С + 2 Н 2 Ú Во-вторых, органические вещества горят: 2 С 2 Н 2 + 5 О 2 → 4 СО 2 + 2 Н 2 О

Домашнее задание: Ú§ 32 Ú№ 1, 3 стр. 151

Домашнее задание: Ú§ 1. 1, 1. 2, 1. 4 ÚУпр. № 1, 5, 7 стр. 151, 152

Тема урока: Изомерия, ее виды.

Цель урока: 1) Вспомнить что такое изомерия? Кто и когда открыл это явление? 2) На примерах рассмотреть различные виды изомерии. 3) Научиться графически строить изомеры различных видов.

Виды изомерии. Различают два основных типа изомерии: 1) структурную: а) углеродного скелета, б) положения кратных связей и функциональных групп, в) межклассовая. 2) пространственную: а) геометрическую (цис-транс) б) зеркальную (оптическая).

Структурная: Изомерия углеродного скелета на примере пентана - С 5 Н 12

Структурная: Изомерия положения двойной связи. Úа) CH 2 = CH – CH 2 – CH 3 бутен-1 Ú б) CH 3 – CH = CH – CH 3 бутен-2

Структурная: Изомерия положения функциональной группы а) CH 3 – CH 2 – OH пропанол-1 OH б) CH 3 – CH 3 пропанол-2
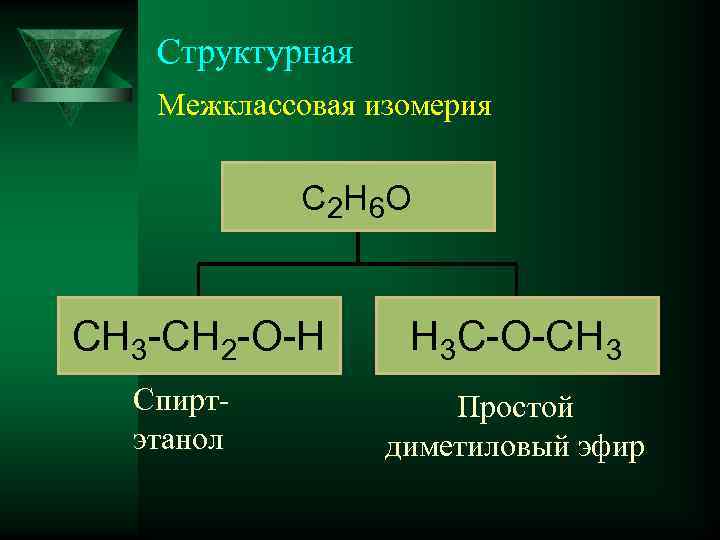
Структурная Межклассовая изомерия С 2 Н 6 О СН 3 -СН 2 -О-Н Спиртэтанол Н 3 С-О-СН 3 Простой диметиловый эфир

Пространственная : (бутен-2 H CH 3 – CH = CH – CH 3 ) H H С=С H 3 C CH 3 цис – изомер t° кип. =3, 7°С H 3 C H транс – изомер t° кип. =0, 9°С
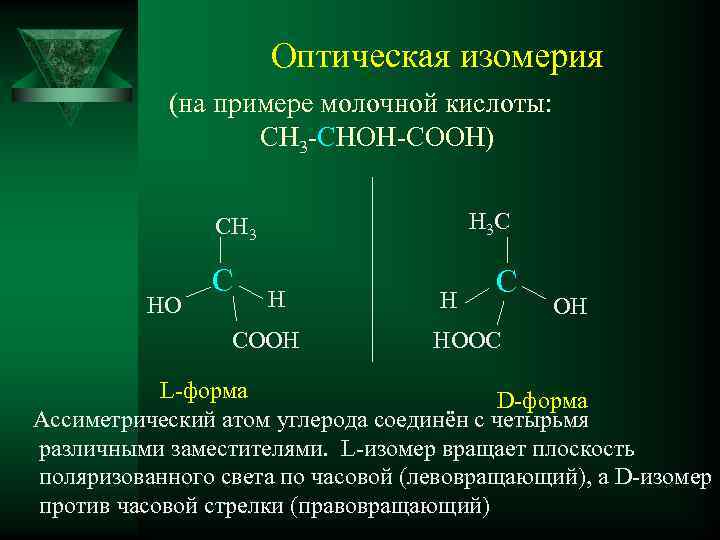
Оптическая изомерия (на примере молочной кислоты: СН 3 -СНОН-СООН) H 3 C CH 3 HO C H COOH H C OH HOOC L-форма D-форма Ассиметрический атом углерода соединён с четырьмя различными заместителями. L-изомер вращает плоскость поляризованного света по часовой (левовращающий), а D-изомер против часовой стрелки (правовращающий)

Домашнее задание: Ú § 1. 3 Ú № 2, 4 к гл. 1 (стр. 151, 152).


Вопросы для самоконтроля Ú В каком веке органическая химия выделилась в Ú Ú Ú Ú самостоятельную науку? Что изучает органическая химия? Каковы были взгляды виталистов на получение органических веществ? Какие учёные и как экспериментально доказали ошибочность взглядов виталистов? Каковы были предпосылки теории строения органических веществ? Что такое изомерия? Каково значение теории химического строения органических веществ А. М. Бутлерова для химической науки? Как можно объяснить многообразие органических веществ? В чем общность свойств органических веществ?



С 5 Н 12

Что мы должны понимать под свойствами вещества? Ú Свойства вещества - есть функция его химического, пространственного и электронного строения.

Виды изомерии. Ú Различают два основных типа изомерии: структурную (изомерия углеродного скелета, положения кратных связей, заместителей, межклассовая) и Ú пространственную: геометрическую (цис-транс) зеркальную (оптическая).

Структурная: Изомерия углеродного скелета на примере пентана - С 5 Н 12

Структурная: Изомерия положения двойной связи. Úа) CH 2 = CH – CH 2 – CH 3 бутен-1 Ú б) CH 3 – CH = CH – CH 3 бутен-2

Структурная: Изомерия положение заместителей а) CH 3 – CH 2 OH пропанол-1 OH б) CH 3 – CH 3 пропанол-2

Структурная Межклассовая изомерия С 2 Н 6 О СН 3 -СН 2 -О-Н Спиртэтанол Н 3 С-О-СН 3 Простой диметиловый эфир
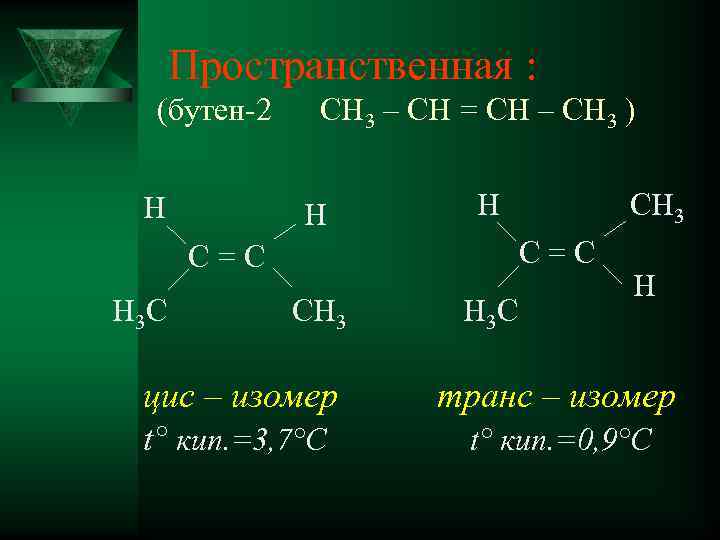
Пространственная : (бутен-2 H CH 3 – CH = CH – CH 3 ) H H С=С H 3 C CH 3 цис – изомер t° кип. =3, 7°С H 3 C H транс – изомер t° кип. =0, 9°С

Оптическая изомерия (на примере молочной кислоты: СН 3 -СНОН-СООН) H 3 C CH 3 HO C H COOH H C OH HOOC L-форма D-форма Ассиметрический атом углерода соединён с четырьмя различными заместителями. L-изомер вращает плоскость поляризованного света по часовой (левовращающий), а D-изомер против часовой стрелки (правовращающий)

Ú Каковы были предпосылки теории строения органических веществ? Ú Как можно объяснить многообразие органических веществ? Ú Что такое изомерия? Назовите типы изомерии. Ú Что такое химическое строение веществ? Объясните на примере. Ú Приведите примеры взаимного влияния атомов или групп атомов в молекулах органических веществ. Ú Каково значение теории химического строения органических веществ А. М. Бутлерова для химической науки?

Цель урока Выяснить: а) Как зарождалась органическая химия? б) Какова причина многообразия органических веществ? в) Познакомиться с основными положениями теории строения А. М. Бутлерова. г) Что такое изомерия? Научиться графически строить изомеры на конкретных примерах. д) Дать оценку значимости теории строения органических веществ.

Домашнее задание: Ú§ 1 ÚУпр. 3, 4
Предмет орг химии (для гимн).ppt