f147d72654252494b3aea94f320b2055.ppt
- Количество слайдов: 24
 Тема урока: Оксид водорода - вода «Вода… Ты не имеешь ни вкуса ни цвета ни запаха, тебя невозможно описать – тобой наслаждаешься. Ты не просто необходима для жизни, ты и есть сама жизнь. Ты божество, ты совершенство, ты самое большое богатство на свете » Антуан де Сент - Экзюпери
Тема урока: Оксид водорода - вода «Вода… Ты не имеешь ни вкуса ни цвета ни запаха, тебя невозможно описать – тобой наслаждаешься. Ты не просто необходима для жизни, ты и есть сама жизнь. Ты божество, ты совершенство, ты самое большое богатство на свете » Антуан де Сент - Экзюпери
 Цель урока: Изучить состав и строение молекулы воды, физические и химические свойства, рассмотреть экологические проблемы, связанные с загрязнением воды.
Цель урока: Изучить состав и строение молекулы воды, физические и химические свойства, рассмотреть экологические проблемы, связанные с загрязнением воды.

 97 % - морская вода 3% - пресная вода Ледники – 79% Подземные воды 20% Реки, озера, атмосферная влага - 1%
97 % - морская вода 3% - пресная вода Ледники – 79% Подземные воды 20% Реки, озера, атмосферная влага - 1%
 Запомните! • Вода – это жизнь ! Без воды живые организмы погибают.
Запомните! • Вода – это жизнь ! Без воды живые организмы погибают.
 Вода – единственное вещество, которое встречается на Земле во всех трех агрегатных состояниях Водяной пар входит в состав атмосферы Твердый лед можно увидеть и в виде снежинок, и в виде инея Жидкой водой наполнен Мировой океан, поверхностные воды суши и подземные воды
Вода – единственное вещество, которое встречается на Земле во всех трех агрегатных состояниях Водяной пар входит в состав атмосферы Твердый лед можно увидеть и в виде снежинок, и в виде инея Жидкой водой наполнен Мировой океан, поверхностные воды суши и подземные воды
 Н 2 О М=18 г/моль W (Н) = 11% W(О) = 89% Сложное вещество –оксид, молекулярного строения, связь ковалентная полярная.
Н 2 О М=18 г/моль W (Н) = 11% W(О) = 89% Сложное вещество –оксид, молекулярного строения, связь ковалентная полярная.
 Физические свойства воды Стр. 50 учебник
Физические свойства воды Стр. 50 учебник
 Структура молекулы воды. • Молекула воды является полярной, представляет собой диполь Н ОН +
Структура молекулы воды. • Молекула воды является полярной, представляет собой диполь Н ОН +
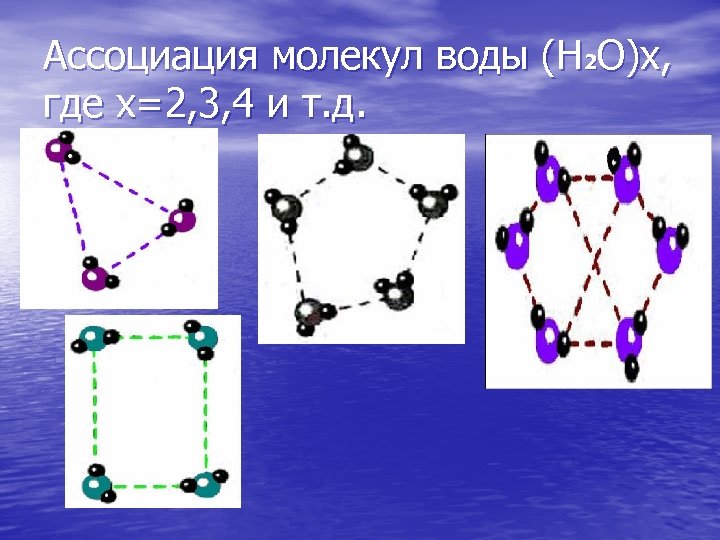 Ассоциация молекул воды (Н 2 О)x, где x=2, 3, 4 и т. д.
Ассоциация молекул воды (Н 2 О)x, где x=2, 3, 4 и т. д.
 Вода – универсальный растворитель она хорошо растворяет ионные соединения и вещества, состоящие из полярных молекул. Сульфат меди хорошо растворим в воде Борная кислота малорастворима в воде Песок не растворяется в воде
Вода – универсальный растворитель она хорошо растворяет ионные соединения и вещества, состоящие из полярных молекул. Сульфат меди хорошо растворим в воде Борная кислота малорастворима в воде Песок не растворяется в воде
 Химические свойства воды Вода – одно из наиболее реакционно – способных веществ. + кислотный оксид = кислота ВОДА + основный оксид = растворимое основание
Химические свойства воды Вода – одно из наиболее реакционно – способных веществ. + кислотный оксид = кислота ВОДА + основный оксид = растворимое основание
 Вода как окислитель взаимодействует с активными (щелочными и щелочноземельными металлами) • Na + Н 2 О = При нагревании возможно взаимодействие воды и с менее активными металлами, например с магнием. Mg+ Н 2 О t°C
Вода как окислитель взаимодействует с активными (щелочными и щелочноземельными металлами) • Na + Н 2 О = При нагревании возможно взаимодействие воды и с менее активными металлами, например с магнием. Mg+ Н 2 О t°C
 Вода как восстановитель • Взаимодействует с таким окислителем как фтор. (вода горит во фторе) 2 F 2 +2 H 2 O = 4 HF+ O 2
Вода как восстановитель • Взаимодействует с таким окислителем как фтор. (вода горит во фторе) 2 F 2 +2 H 2 O = 4 HF+ O 2
 Реакция разложения воды • При t= 2000°C или пропускании электрического тока вода разлагается на простые вещества – кислород и водород 2 Н 2 О 2 Н 2 + О 2
Реакция разложения воды • При t= 2000°C или пропускании электрического тока вода разлагается на простые вещества – кислород и водород 2 Н 2 О 2 Н 2 + О 2
 Выводы • Вода- универсальный растворитель • Вода - обладает окислительно – восстановительными свойствами. • Вода разлагается под действием электрического тока или при t= 2000°C • Связь между атомами в молекуле воды ковалентная полярная.
Выводы • Вода- универсальный растворитель • Вода - обладает окислительно – восстановительными свойствами. • Вода разлагается под действием электрического тока или при t= 2000°C • Связь между атомами в молекуле воды ковалентная полярная.
 Ответы теста • Вариант -1 2, 3, 2, 4 Вариант -2 2, 2, 4, 3
Ответы теста • Вариант -1 2, 3, 2, 4 Вариант -2 2, 2, 4, 3
 Трудно представить себе область человеческой деятельности, где не применялась бы вода Гидроэлектростанция Строительство Сельское хозяйство Машиностроение В быту
Трудно представить себе область человеческой деятельности, где не применялась бы вода Гидроэлектростанция Строительство Сельское хозяйство Машиностроение В быту
 Природная вода не бывает совершенно чистой, она содержит примеси: растворимые и нерастворимые вещества. Качество питьевой воды • Законодательно определено, что питьевая • вода, поступающая к потребителю, должна быть приятной в органолептическом отношении и безопасной для здоровья; Содержание примесей в воде не должно превышать предельно допустимых концентраций.
Природная вода не бывает совершенно чистой, она содержит примеси: растворимые и нерастворимые вещества. Качество питьевой воды • Законодательно определено, что питьевая • вода, поступающая к потребителю, должна быть приятной в органолептическом отношении и безопасной для здоровья; Содержание примесей в воде не должно превышать предельно допустимых концентраций.
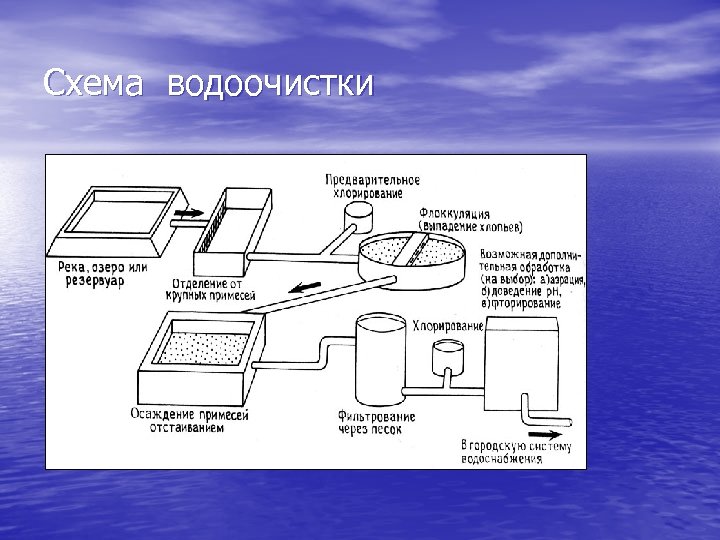 Схема водоочистки
Схема водоочистки
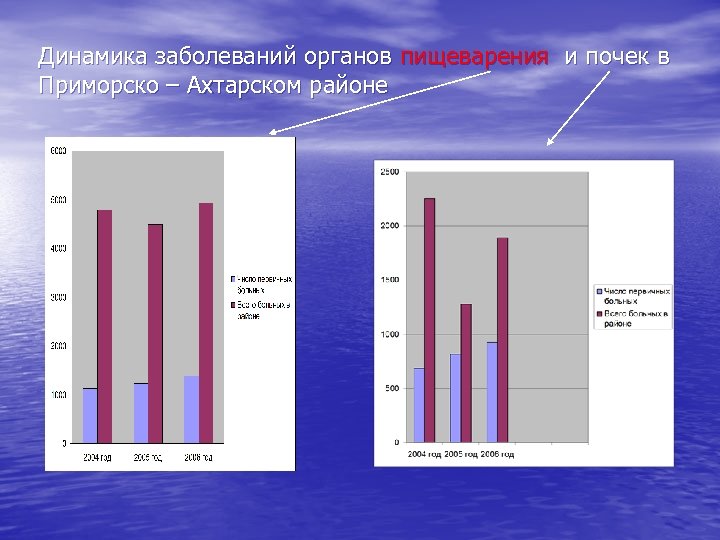 Динамика заболеваний органов пищеварения и почек в Приморско – Ахтарском районе
Динамика заболеваний органов пищеварения и почек в Приморско – Ахтарском районе
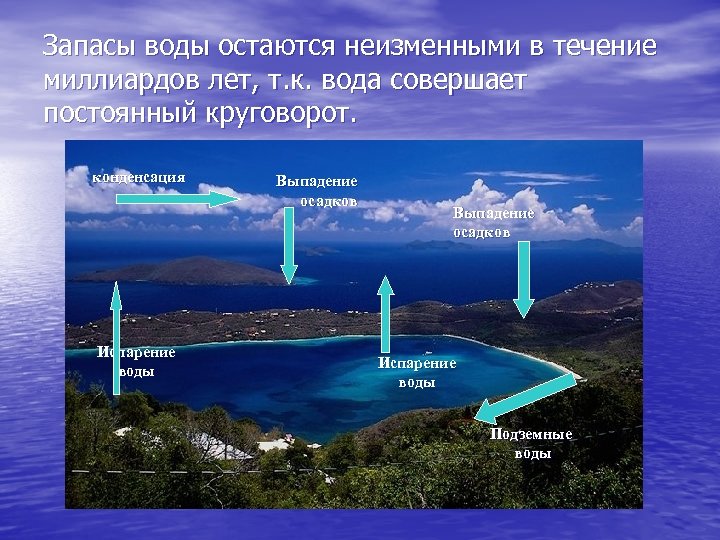 Запасы воды остаются неизменными в течение миллиардов лет, т. к. вода совершает постоянный круговорот. конденсация Испарение воды Выпадение осадков Испарение воды Подземные воды
Запасы воды остаются неизменными в течение миллиардов лет, т. к. вода совершает постоянный круговорот. конденсация Испарение воды Выпадение осадков Испарение воды Подземные воды
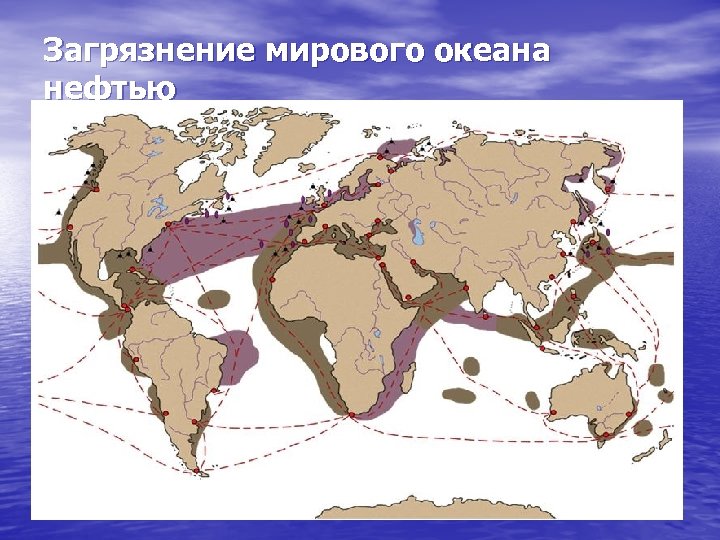 Загрязнение мирового океана нефтью
Загрязнение мирового океана нефтью
 Домашнее задание • § 11 стр. 55 – 56 упр. 1 -6 темы докладов и сообщений «Аномальные свойства воды» «Значение воды для живых организмов» «Экологические проблемы Азовского моря» « Всегда ли вода Н 2 О? Что такое тяжелая вода? »
Домашнее задание • § 11 стр. 55 – 56 упр. 1 -6 темы докладов и сообщений «Аномальные свойства воды» «Значение воды для живых организмов» «Экологические проблемы Азовского моря» « Всегда ли вода Н 2 О? Что такое тяжелая вода? »


