Аминокислоты .ppt
- Количество слайдов: 29
 Тема урока: «Аминокислоты»
Тема урока: «Аминокислоты»
 Микро-темы урока: 1. Последовательность изучения новой темы 2. Творческое задание № 1. 3. Творческое задание № 2. 4. Определение аминокислот как класса органических соединений. 5. Номенклатура АК: Международная номенклатура. АК. Номенклатура аминокислот с использованием букв греческого алфавита. Исторически сложившиеся названия аминокислот. 6. Изомерия АК: Изомерия углеродного скелета АК. Изомерия положения аминогруппы. 7. Творческое задание № 3. 8. Физические свойства АК. 9. Получение аминокислот. 10. Творческое задание № 4. 11. Творческое задание № 5. 12. Твоческое задание № 6. 13. Горение АК. 14. Реакция этерификации для АК. 15. Выводы по уроку. 16. Домашнее задание.
Микро-темы урока: 1. Последовательность изучения новой темы 2. Творческое задание № 1. 3. Творческое задание № 2. 4. Определение аминокислот как класса органических соединений. 5. Номенклатура АК: Международная номенклатура. АК. Номенклатура аминокислот с использованием букв греческого алфавита. Исторически сложившиеся названия аминокислот. 6. Изомерия АК: Изомерия углеродного скелета АК. Изомерия положения аминогруппы. 7. Творческое задание № 3. 8. Физические свойства АК. 9. Получение аминокислот. 10. Творческое задание № 4. 11. Творческое задание № 5. 12. Твоческое задание № 6. 13. Горение АК. 14. Реакция этерификации для АК. 15. Выводы по уроку. 16. Домашнее задание.
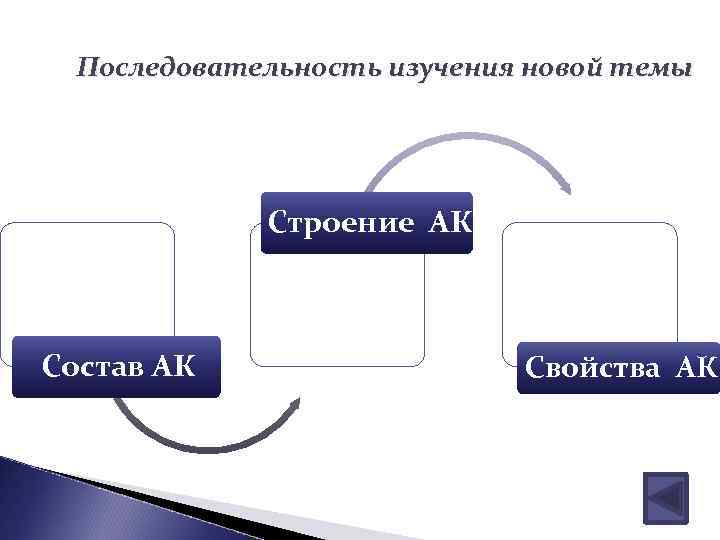 Последовательность изучения новой темы Строение АК Состав АК Свойства АК
Последовательность изучения новой темы Строение АК Состав АК Свойства АК
 Творческое задание № 1. Рассмотрите слово «Аминокислоты » с точки зрения словообразования.
Творческое задание № 1. Рассмотрите слово «Аминокислоты » с точки зрения словообразования.
 Ответ. «Аминокислоты »
Ответ. «Аминокислоты »
 Творческое задание № 2. Предложите общую формулу для аминокислот (АК) , исходя из морфемики этого слова.
Творческое задание № 2. Предложите общую формулу для аминокислот (АК) , исходя из морфемики этого слова.
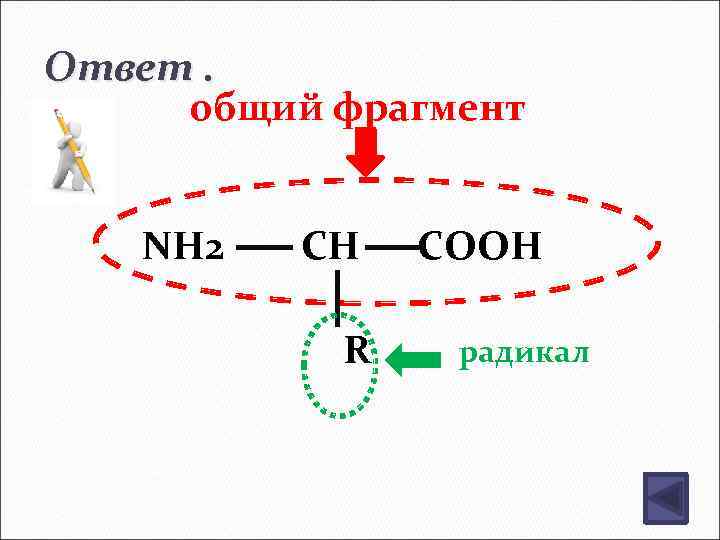 Ответ. общий фрагмент NH 2 CH R COOH радикал
Ответ. общий фрагмент NH 2 CH R COOH радикал
 Аминокислоты –гетерофункциональные соединения , которые обязательно содержат две функциональныегруппы: аминогруппу - NH 2 карбоксильную группу –СООН , связанные с углеводородным радикалом.
Аминокислоты –гетерофункциональные соединения , которые обязательно содержат две функциональныегруппы: аминогруппу - NH 2 карбоксильную группу –СООН , связанные с углеводородным радикалом.
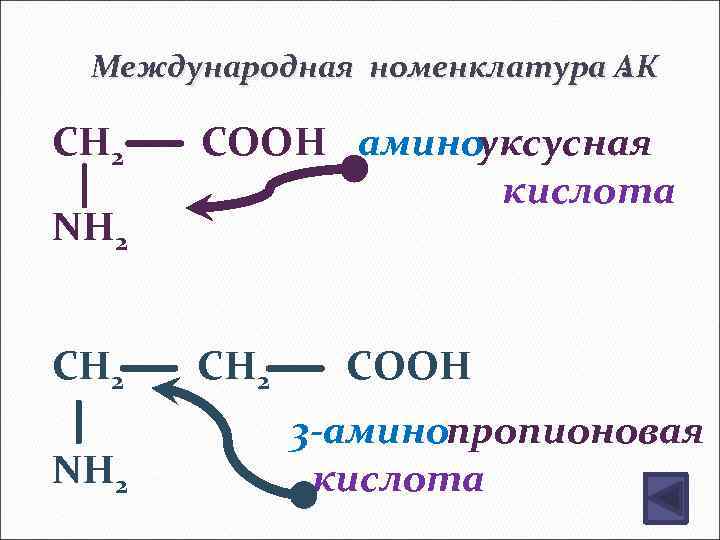 Международная номенклатура АК. CH 2 NH 2 COOH аминоуксусная кислота CH 2 COOH 3 -аминопропионовая кислота
Международная номенклатура АК. CH 2 NH 2 COOH аминоуксусная кислота CH 2 COOH 3 -аминопропионовая кислота
 Номенклатура аминокислот с использованием букв греческого алфавита. 3 β CH 2 2 α CH 2 1 COOH NH 2 β-аминопропионоваякислота
Номенклатура аминокислот с использованием букв греческого алфавита. 3 β CH 2 2 α CH 2 1 COOH NH 2 β-аминопропионоваякислота
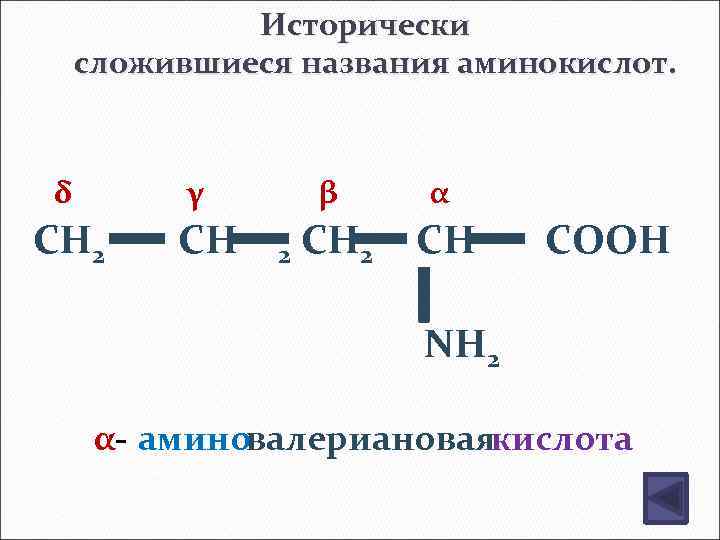 Исторически сложившиеся названия аминокислот. δ γ CH 2 CH β 2 α CH 2 CH COOH NH 2 α- аминовалериановаякислота
Исторически сложившиеся названия аминокислот. δ γ CH 2 CH β 2 α CH 2 CH COOH NH 2 α- аминовалериановаякислота
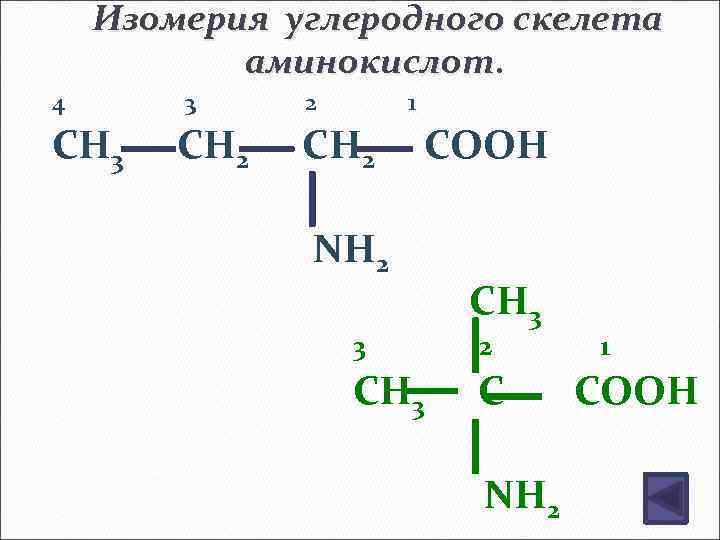 Изомерия углеродного скелета аминокислот. 4 CH 3 3 CH 2 2 1 CH 2 COOH NH 2 3 CH 3 2 C NH 2 1 COOH
Изомерия углеродного скелета аминокислот. 4 CH 3 3 CH 2 2 1 CH 2 COOH NH 2 3 CH 3 2 C NH 2 1 COOH
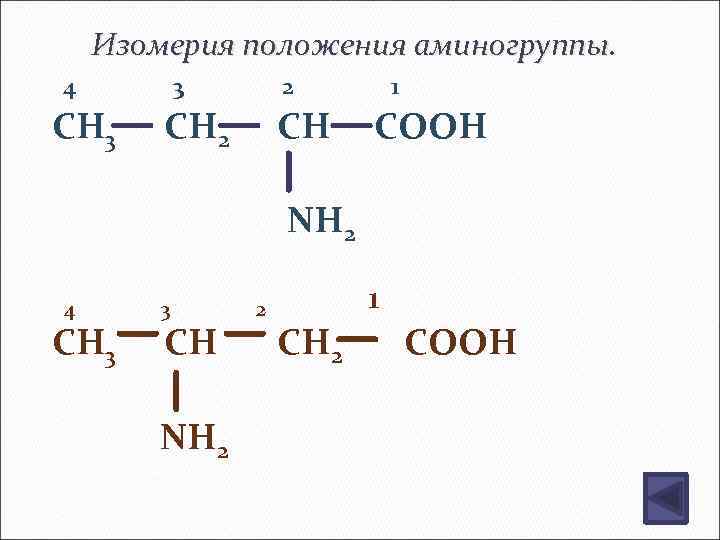 Изомерия положения аминогруппы. 4 CH 3 3 2 CH 1 COOH NH 2 4 CH 3 3 CH NH 2 2 1 CH 2 COOH
Изомерия положения аминогруппы. 4 CH 3 3 2 CH 1 COOH NH 2 4 CH 3 3 CH NH 2 2 1 CH 2 COOH
 Творческое задание № 3. Зная общую формулу аминокислот, составьте формулы аланина , фенилаланина , лейцина, изолейцина/
Творческое задание № 3. Зная общую формулу аминокислот, составьте формулы аланина , фенилаланина , лейцина, изолейцина/
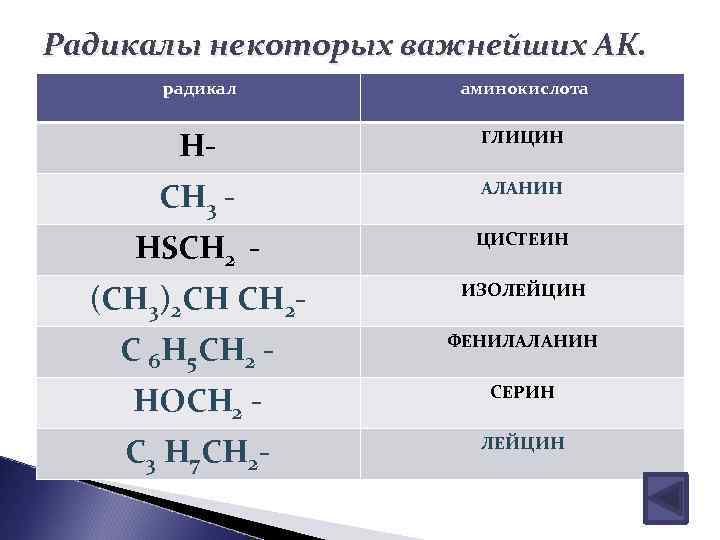 Радикалы некоторых важнейших АК. радикал аминокислота Н- ГЛИЦИН СН 3 - АЛАНИН НSCH 2 - ЦИСТЕИН (СН 3)2 СН СН 2 - ИЗОЛЕЙЦИН С 6 Н 5 СН 2 - ФЕНИЛАЛАНИН НОСН 2 - СЕРИН С 3 Н 7 СН 2 - ЛЕЙЦИН
Радикалы некоторых важнейших АК. радикал аминокислота Н- ГЛИЦИН СН 3 - АЛАНИН НSCH 2 - ЦИСТЕИН (СН 3)2 СН СН 2 - ИЗОЛЕЙЦИН С 6 Н 5 СН 2 - ФЕНИЛАЛАНИН НОСН 2 - СЕРИН С 3 Н 7 СН 2 - ЛЕЙЦИН
 Физические свойства АК. 1. Бесцветные кристаллические вещества ; 2. Хорошо растворимы в воде; 3. В зависимости от радикала могут иметь сладкий, горький или соленый вкус;
Физические свойства АК. 1. Бесцветные кристаллические вещества ; 2. Хорошо растворимы в воде; 3. В зависимости от радикала могут иметь сладкий, горький или соленый вкус;
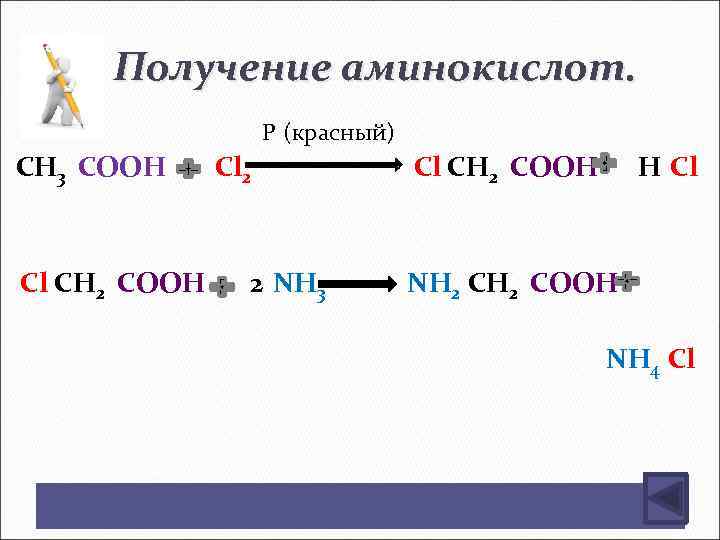 Получение аминокислот. P (красный) СН 3 СООН Сl СН 2 СООН Сl 2 2 NН 3 Сl СН 2 СООН Н Сl NН 2 СООН NН 4 Сl
Получение аминокислот. P (красный) СН 3 СООН Сl СН 2 СООН Сl 2 2 NН 3 Сl СН 2 СООН Н Сl NН 2 СООН NН 4 Сl
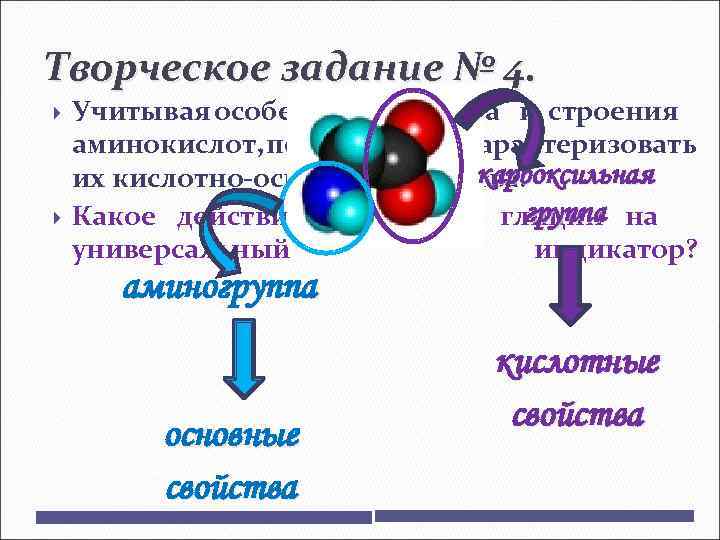 Творческое задание № 4. Учитывая особенности состава и строения аминокислот, попытайтесьохарактеризовать карбоксильная их кислотно-основные свойства. группа Какое действие окажет глицин на универсальный индикатор? аминогруппа основные свойства кислотные свойства
Творческое задание № 4. Учитывая особенности состава и строения аминокислот, попытайтесьохарактеризовать карбоксильная их кислотно-основные свойства. группа Какое действие окажет глицин на универсальный индикатор? аминогруппа основные свойства кислотные свойства
 Нейтральная реакция раствора глицина Универсальный индикатор
Нейтральная реакция раствора глицина Универсальный индикатор
 Творческое задание № 5. Щелочная среда (лизин) Кислая среда (глутаминовая кислота) Нейтральная среда (глицин)
Творческое задание № 5. Щелочная среда (лизин) Кислая среда (глутаминовая кислота) Нейтральная среда (глицин)
 Творческое задание № 6. Предложите химические реакции с помощью которых можно доказать : А) кислотный характер АК; Ответ. Б) основной характер АК; Ответ. проявляя основные А) кислотные свойства АК свойства реагируют с характеризуются неорганическими реакциями со кислотами с щелочами с образованием солей.
Творческое задание № 6. Предложите химические реакции с помощью которых можно доказать : А) кислотный характер АК; Ответ. Б) основной характер АК; Ответ. проявляя основные А) кислотные свойства АК свойства реагируют с характеризуются неорганическими реакциями со кислотами с щелочами с образованием солей.
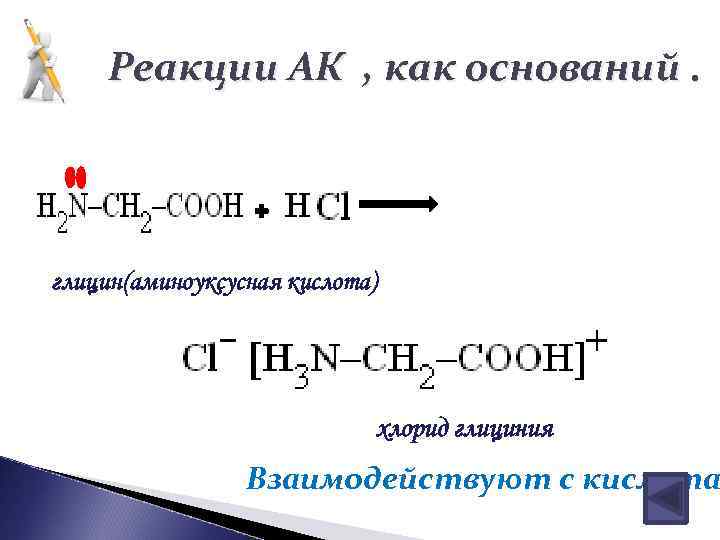 Реакции АК , как оснований. глицин(аминоуксусная кислота) хлорид глициния Взаимодействуют с кислота
Реакции АК , как оснований. глицин(аминоуксусная кислота) хлорид глициния Взаимодействуют с кислота
 Реакции АК, как кислот. аминоацетат натрия Взаимодействие с основаниями.
Реакции АК, как кислот. аминоацетат натрия Взаимодействие с основаниями.
 Реакции АК, как кислот. Взаимодействуют с основными оксидами, так при нагревании проходит реакция между оксидом меди (II) и глутаминовой кислотой с образованием соли ярко синего цвета – глутамата меди.
Реакции АК, как кислот. Взаимодействуют с основными оксидами, так при нагревании проходит реакция между оксидом меди (II) и глутаминовой кислотой с образованием соли ярко синего цвета – глутамата меди.
 Творческое задание № 6. Зная структурную формулу аминокислот , подумайте , могут ли они соединяться друг с другом ? Если да , то каким образом ?
Творческое задание № 6. Зная структурную формулу аминокислот , подумайте , могут ли они соединяться друг с другом ? Если да , то каким образом ?
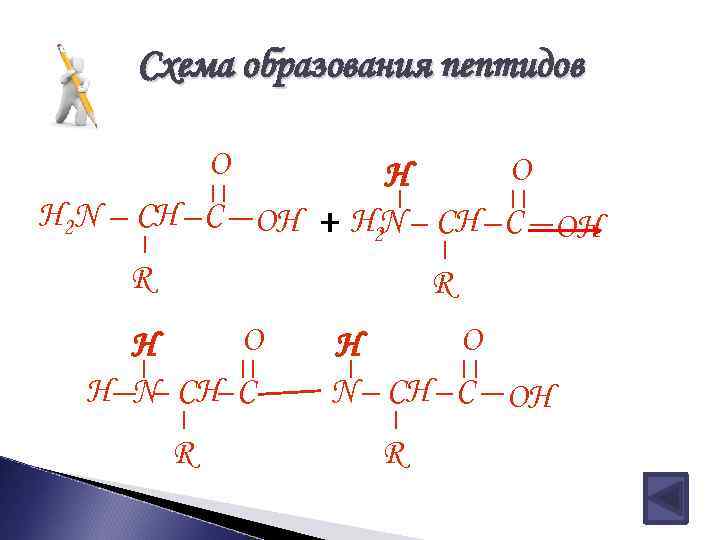 Схема образования пептидов O O H H 2 N CH C OH + H 2 N CH C OH R R O H H N CH C R O H N CH C OH R
Схема образования пептидов O O H H 2 N CH C OH + H 2 N CH C OH R R O H H N CH C R O H N CH C OH R
 Горение аминокислот. 4 NH 2 COOH + 13 O 2 8 CO 2 + 10 H 2 O + 2 N 2
Горение аминокислот. 4 NH 2 COOH + 13 O 2 8 CO 2 + 10 H 2 O + 2 N 2
 Этерификация H 2 SO 4 (к) NH 2 COOH + C 2 H 5 OH NH 2 COOC 2 H 5 + H 2 O
Этерификация H 2 SO 4 (к) NH 2 COOH + C 2 H 5 OH NH 2 COOC 2 H 5 + H 2 O
 Выводы по теме урока 1. 2. 3. 4. Аминокислоты – это бифункциональные органические соединения ; Для аминокислот возможны изомерия углеродного скелета и положения ; Аминокислоты – амфотерны; Аминокислоты –горят, вступают в реакции с неорганическими кислотами и основаниями, в реакцию этерификации и образуют пептиды ;
Выводы по теме урока 1. 2. 3. 4. Аминокислоты – это бифункциональные органические соединения ; Для аминокислот возможны изомерия углеродного скелета и положения ; Аминокислоты – амфотерны; Аминокислоты –горят, вступают в реакции с неорганическими кислотами и основаниями, в реакцию этерификации и образуют пептиды ;


