Л_17_Фтор_газы.ppt
- Количество слайдов: 74
 ТЕМА: СОЕДИНЕНИЯ ФТОРА, ЛЕТУЧИЕ ПАРЫ И ГАЗЫ ЛЕКЦИЯ № 17 ДЛЯ СТУДЕНТОВ 4 КУРСА, ОБУЧАЮЩИХСЯ ПО СПЕЦИАЛЬНОСТИ 060301 ФАРМАЦИЯ СТАРШИЙ ПРЕПОДАВАТЕЛЬ: КУТЯКОВ ВИКТОР АНДРЕЕВИЧ КРАСНОЯРСК, 2016
ТЕМА: СОЕДИНЕНИЯ ФТОРА, ЛЕТУЧИЕ ПАРЫ И ГАЗЫ ЛЕКЦИЯ № 17 ДЛЯ СТУДЕНТОВ 4 КУРСА, ОБУЧАЮЩИХСЯ ПО СПЕЦИАЛЬНОСТИ 060301 ФАРМАЦИЯ СТАРШИЙ ПРЕПОДАВАТЕЛЬ: КУТЯКОВ ВИКТОР АНДРЕЕВИЧ КРАСНОЯРСК, 2016
 Соединения фтора
Соединения фтора
 В течение последних десятилетий наблюдается стремительное развитие химии фтора, тесно связанное с потребностью практики, в первую очередь ядерной энергетики, химической промышленности, медицины, военных и космических исследований. За это время было синтезировано множество новых соединений, разработаны новые оригинальные методы синтеза.
В течение последних десятилетий наблюдается стремительное развитие химии фтора, тесно связанное с потребностью практики, в первую очередь ядерной энергетики, химической промышленности, медицины, военных и космических исследований. За это время было синтезировано множество новых соединений, разработаны новые оригинальные методы синтеза.
 Фтор - элемент, расположенный в правом верхнем углу периодической системы элементов, - привлек к себе усиленное внимание исследователей после того, как в 1928 г. Томас Миджли, которому человечество обязано появлением фреонов, получил указание разработать вместо использовавшихся в то время аммиака и сернистого ангидрида новые, более безопасные хладагенты.
Фтор - элемент, расположенный в правом верхнем углу периодической системы элементов, - привлек к себе усиленное внимание исследователей после того, как в 1928 г. Томас Миджли, которому человечество обязано появлением фреонов, получил указание разработать вместо использовавшихся в то время аммиака и сернистого ангидрида новые, более безопасные хладагенты.
 Фторхлоруглероды, отличающиеся крайней химической инертностью, негорючестью и нетоксичностью, быстро получили широкое распространение в качестве хладагентов. Фреоны
Фторхлоруглероды, отличающиеся крайней химической инертностью, негорючестью и нетоксичностью, быстро получили широкое распространение в качестве хладагентов. Фреоны
 Биологически активные вещества При замещении атома водорода в органической молекуле, участвующей в метаболизме животных или растений, на атом фтора, организм часто не способен обнаружить эту подмену и включает такую молекулу в процессы метаболизма. Этот эффект, называемый "эффектом маскировки" (mimic effect), отчетливо проявляется, например, в случае монофторуксусной кислоты.
Биологически активные вещества При замещении атома водорода в органической молекуле, участвующей в метаболизме животных или растений, на атом фтора, организм часто не способен обнаружить эту подмену и включает такую молекулу в процессы метаболизма. Этот эффект, называемый "эффектом маскировки" (mimic effect), отчетливо проявляется, например, в случае монофторуксусной кислоты.
 При увеличении числа атомов фтора в молекуле организм уже не обманывается: если производные монофторуксусной кислоты являются сильно токсичными веществами, то ди- и трифторуксусная кислота и их производные обладают лишь слабой токсичностью.
При увеличении числа атомов фтора в молекуле организм уже не обманывается: если производные монофторуксусной кислоты являются сильно токсичными веществами, то ди- и трифторуксусная кислота и их производные обладают лишь слабой токсичностью.
 Фторсодержащие вещества, ошибочно включенные организмом в обменные процессы в результате эффекта маскировки, во многих случаях проявляют биологическую активность, заключающуюся в торможении различных стадий метаболизма ("блокировочный эффект"). Например, упомянутая выше монофторуксусная кислота включается в цикл трикарбоновых кислот (цикл Кребса) и превращается во фторлимонную кислоту.
Фторсодержащие вещества, ошибочно включенные организмом в обменные процессы в результате эффекта маскировки, во многих случаях проявляют биологическую активность, заключающуюся в торможении различных стадий метаболизма ("блокировочный эффект"). Например, упомянутая выше монофторуксусная кислота включается в цикл трикарбоновых кислот (цикл Кребса) и превращается во фторлимонную кислоту.
 Введение фтора наряду с токсичностью может приводить к появлению фармакологической активности, примером чего является возникновение противовоспалительного действия у фторсодержащих стероидов или канцеролитического действия у 5 фторурацила. В этом случае причиной появления такой активности можно считать совместное действие эффекта маскировки и блокировочного эффекта.
Введение фтора наряду с токсичностью может приводить к появлению фармакологической активности, примером чего является возникновение противовоспалительного действия у фторсодержащих стероидов или канцеролитического действия у 5 фторурацила. В этом случае причиной появления такой активности можно считать совместное действие эффекта маскировки и блокировочного эффекта.
 Основные направления использования соединений фтора Фреоны (галогенфторуглероды) Использование хлорфторуглеродов в качестве хладагентов и пропеллентов для аэрозольных упаковок в определенной степени связано с трудностью полного фторирования хлоруглеводородов, вследствие чего в их молекулах сохраняются атомы хлора. Остающиеся в молекуле фторированного соединения связи С - С 1 помогают получить вещества с оптимальными температурами кипения: СС 14 CF 3 C 1 CF 2 C 12 CFCI 3 фреон-13 фреон-12 фреон-11
Основные направления использования соединений фтора Фреоны (галогенфторуглероды) Использование хлорфторуглеродов в качестве хладагентов и пропеллентов для аэрозольных упаковок в определенной степени связано с трудностью полного фторирования хлоруглеводородов, вследствие чего в их молекулах сохраняются атомы хлора. Остающиеся в молекуле фторированного соединения связи С - С 1 помогают получить вещества с оптимальными температурами кипения: СС 14 CF 3 C 1 CF 2 C 12 CFCI 3 фреон-13 фреон-12 фреон-11
 Эмульсии ПФС как искусственная кровь О возможности применения ПФС в качестве искусственной крови, т. е. в качестве вещества, обладающего способностью транспортировать кислород, сообщили впервые Кларк и др. в 1966 г. Они обратили внимание на высокую растворимость кислорода в ПФС и обнаружили, что при погружении мыши в перфторбутилтетрагидро-фуран, в котором в достаточном количестве растворен кислород, ее состояние не меняется в течение нескольких часов. Затем в экспериментах с сердцем крысы они подтвердили возможность применения ПФС в качестве среды, снабжающей организм кислородом
Эмульсии ПФС как искусственная кровь О возможности применения ПФС в качестве искусственной крови, т. е. в качестве вещества, обладающего способностью транспортировать кислород, сообщили впервые Кларк и др. в 1966 г. Они обратили внимание на высокую растворимость кислорода в ПФС и обнаружили, что при погружении мыши в перфторбутилтетрагидро-фуран, в котором в достаточном количестве растворен кислород, ее состояние не меняется в течение нескольких часов. Затем в экспериментах с сердцем крысы они подтвердили возможность применения ПФС в качестве среды, снабжающей организм кислородом
 ФТОРСОДЕРЖАЩИЕ ЛЕКАРСТВЕННЫЕ ПРЕПАРАТЫ
ФТОРСОДЕРЖАЩИЕ ЛЕКАРСТВЕННЫЕ ПРЕПАРАТЫ
 Средства для ингаляционного наркоза Галогенфторуглероды типа CF 3 CHC 1 Вr (галотан) являются негорючими жидкостями с высокой летучестью (т. кип. 50°С), в связи с чем находят применение в качестве средств для наркоза.
Средства для ингаляционного наркоза Галогенфторуглероды типа CF 3 CHC 1 Вr (галотан) являются негорючими жидкостями с высокой летучестью (т. кип. 50°С), в связи с чем находят применение в качестве средств для наркоза.
 Средства для ингаляционного наркоза Фпуроксен Фпуоромар Галотан Фпуотан Метоксифлуран Галопропан Энфлуран Изофлуран Поскольку препараты обладают рядом других достоинств, они находят широкое применение в медицинской практике.
Средства для ингаляционного наркоза Фпуроксен Фпуоромар Галотан Фпуотан Метоксифлуран Галопропан Энфлуран Изофлуран Поскольку препараты обладают рядом других достоинств, они находят широкое применение в медицинской практике.
 Открытое Фридом и др. в 1953 г. резкое усиление активности стероидных гормонов при введении в молекулу фтора привлекло внимание фармацевтической промышленности к соединениям фтора, ранее совершенно не применявшимся в этой области, что в свою очередь привело к открытию многих новых фторсодержащих лекарственных препаратов, в том числе нестероидного типа.
Открытое Фридом и др. в 1953 г. резкое усиление активности стероидных гормонов при введении в молекулу фтора привлекло внимание фармацевтической промышленности к соединениям фтора, ранее совершенно не применявшимся в этой области, что в свою очередь привело к открытию многих новых фторсодержащих лекарственных препаратов, в том числе нестероидного типа.
 - Канцеролитический препарат 5 - фторурацил; - Фторсодержащие стероидные лекарственные препараты; - Фторсодержащие производные витамина D 3. Ранее о витамине D 3 было известно лишь то, что он лечит рахит, вызываемый аномалиями в кальциевом обмене в организме.
- Канцеролитический препарат 5 - фторурацил; - Фторсодержащие стероидные лекарственные препараты; - Фторсодержащие производные витамина D 3. Ранее о витамине D 3 было известно лишь то, что он лечит рахит, вызываемый аномалиями в кальциевом обмене в организме.
 Психотропные препараты Препараты для лечения нервных болезней и транквилизаторы Трифлуперидол, имеющий скелет п-фторбутирофенона, эффективен при лечении шизофрении
Психотропные препараты Препараты для лечения нервных болезней и транквилизаторы Трифлуперидол, имеющий скелет п-фторбутирофенона, эффективен при лечении шизофрении
 Снотворные препараты, антидепрессанты Флуразепам Препараты, снижающие аппетит Фенфлурамин Препараты, поднимающие кровяное давление, и мочегонные средства Политиазид
Снотворные препараты, антидепрессанты Флуразепам Препараты, снижающие аппетит Фенфлурамин Препараты, поднимающие кровяное давление, и мочегонные средства Политиазид
 Фторсодержащие антибиотики Противоамебные препараты Флубендазал ФТОРСОДЕРЖАЩИЕ ПЕСТИЦИДЫ
Фторсодержащие антибиотики Противоамебные препараты Флубендазал ФТОРСОДЕРЖАЩИЕ ПЕСТИЦИДЫ
 Фтористые соли (фториды) l l Источники фторидов Фтор присутствует в переменных количествах в почве и естественных водных запасах. В тех случаях, когда "естественное" содержание фтора в воде низкое, используют добавки фторидов как средство профилактики кариеса. Фториды - эффективные ингибиторы фермента и в связи с этим нашли значительное использование в сохранении биологических образцов. Смеси фторидов доступны в форме таблеток для предотвращения кариеса. Они также предписаны при лечении остеопороза и других заболеваний костей.
Фтористые соли (фториды) l l Источники фторидов Фтор присутствует в переменных количествах в почве и естественных водных запасах. В тех случаях, когда "естественное" содержание фтора в воде низкое, используют добавки фторидов как средство профилактики кариеса. Фториды - эффективные ингибиторы фермента и в связи с этим нашли значительное использование в сохранении биологических образцов. Смеси фторидов доступны в форме таблеток для предотвращения кариеса. Они также предписаны при лечении остеопороза и других заболеваний костей.
 Фтористые соли (фториды) l l Отравление фтористыми солями Известны острые и хронические отравления, вызванные приемом пищи, содержащей фториды. Симптомы и признаки острого отравления фторидами включают тошноту, рвоту, диарею, боль в животе и парестезию. Объектами исследования на фториды являются главным образом кровь, моча, пищевые продукты и при смертельном исходе – внутренние органы трупа.
Фтористые соли (фториды) l l Отравление фтористыми солями Известны острые и хронические отравления, вызванные приемом пищи, содержащей фториды. Симптомы и признаки острого отравления фторидами включают тошноту, рвоту, диарею, боль в животе и парестезию. Объектами исследования на фториды являются главным образом кровь, моча, пищевые продукты и при смертельном исходе – внутренние органы трупа.
 Фтористые соли (фториды) l l l Изолирование. Тщательно измельченные объекты в количестве 25 г подщелачивают избытком гидроксида кальция, смачивают раствором нитрата аммония или концентрированной азотной кислоты, высушивают и прокаливают при температуре не выше 500°С до полного сжигания. При отсутствии химически чистой извести объект подщелачивают гидроксидом натрия и сжигают. Полученную золу смешивают с раствором хлорида кальция, кипятят, охлаждают. Отфильтрованный осадок промывают дистиллированной водой до нейтральной реакции, сжигают осадок вместе с фильтром и золу исследуют на наличие фторидов. Необходима постановка слепого опыта. Все реактивы в тех же количествах обрабатывают в той же чашке, в которой будет производиться выпаривание. По высушивании остаток прокаливают и исследуют на фториды.
Фтористые соли (фториды) l l l Изолирование. Тщательно измельченные объекты в количестве 25 г подщелачивают избытком гидроксида кальция, смачивают раствором нитрата аммония или концентрированной азотной кислоты, высушивают и прокаливают при температуре не выше 500°С до полного сжигания. При отсутствии химически чистой извести объект подщелачивают гидроксидом натрия и сжигают. Полученную золу смешивают с раствором хлорида кальция, кипятят, охлаждают. Отфильтрованный осадок промывают дистиллированной водой до нейтральной реакции, сжигают осадок вместе с фильтром и золу исследуют на наличие фторидов. Необходима постановка слепого опыта. Все реактивы в тех же количествах обрабатывают в той же чашке, в которой будет производиться выпаривание. По высушивании остаток прокаливают и исследуют на фториды.
 Фтористые соли (фториды) l 2. Метод дистилляции с водяным паром (метод С. А. Лаврешина): фториды из биоматериала отгоняют с водяным паром в виде плавиковой кислоты (HF) из смеси азотной и серной кислот при температуре 200 о. С. При необходимости проводят очистку путем осаждения в виде фторида кальция: l 2 HF + Ca 2+ Ca. F 2 + 2 H+ l Осадок фторида кальция фильтрованием и исследуют. отделяют
Фтористые соли (фториды) l 2. Метод дистилляции с водяным паром (метод С. А. Лаврешина): фториды из биоматериала отгоняют с водяным паром в виде плавиковой кислоты (HF) из смеси азотной и серной кислот при температуре 200 о. С. При необходимости проводят очистку путем осаждения в виде фторида кальция: l 2 HF + Ca 2+ Ca. F 2 + 2 H+ l Осадок фторида кальция фильтрованием и исследуют. отделяют
 Качественное обнаружение l l l 1. Часть остатка в платиновом (или свинцовом) тигле смачивают несколькими каплями воды и обливают небольшим количеством концентрированной серной кислоты, тигель быстро закрывают часовым стеклом, нижняя поверхность которого покрыта воском или парафином. Часть слоя воска или парафина предварительно удаляют, делая условную надпись при помощи острия иглы. Тигель оставляют на сутки, защитный слой воска или парафина удаляют и наблюдают травление стекла. Ca. F 2 + H 2 SO 4 2 HF +Ca. SO 4 3 Si. O 2 + 6 HF 2 H 2 Si. O 3 + H 2 Si. F 6 Стекло Si. O 2 растворяется под воздействием HF с образованием кремниевой и кремнефтористой кислот. Приготовление лака. К раствору в 15— 20 мл эфира растертой в тонкий порошок 8 г канифоли медленно приливают около 80 мл коллодия. Покрытые лаком кусочки стекла сушат на воздухе, а затем в шкафу при температуре 1200 С.
Качественное обнаружение l l l 1. Часть остатка в платиновом (или свинцовом) тигле смачивают несколькими каплями воды и обливают небольшим количеством концентрированной серной кислоты, тигель быстро закрывают часовым стеклом, нижняя поверхность которого покрыта воском или парафином. Часть слоя воска или парафина предварительно удаляют, делая условную надпись при помощи острия иглы. Тигель оставляют на сутки, защитный слой воска или парафина удаляют и наблюдают травление стекла. Ca. F 2 + H 2 SO 4 2 HF +Ca. SO 4 3 Si. O 2 + 6 HF 2 H 2 Si. O 3 + H 2 Si. F 6 Стекло Si. O 2 растворяется под воздействием HF с образованием кремниевой и кремнефтористой кислот. Приготовление лака. К раствору в 15— 20 мл эфира растертой в тонкий порошок 8 г канифоли медленно приливают около 80 мл коллодия. Покрытые лаком кусочки стекла сушат на воздухе, а затем в шкафу при температуре 1200 С.
 Качественное обнаружение l l l 2. Часть золы смешивают с Si. O 2 (песком), помещают в пробирку и приливают концентрированную серную кислоту. В отверстии пробирки держат стеклянную палочку с каплей воды. В случае наличия фтористого водорода капля мутнеет вследствие выделения кремневой кислоты из образующегося летучего фторида кремния (кремний из силиката стекла). Пары фторида кремния можно при помощи стеклянной трубки пропустить в другую влажную пробирку, при этом стенки пробирки покрывают кремневой кислотой: Са. F 2 + Н 2 SО 4 → Са. SО 4 + 2 НF 4 НF + Si. O 2 → Si. F 4 + 2 Н 20 3 Si. F 4 + 3 Н 20 → Н 2 Si. O 3 + 2 Н 2 Si. F 6 Естественносодержащиеся в организме фториды и кремнефториды по описанной методике анализа не могут дать реакций «травления» стекла или помутнения капли воды от Si. F 4.
Качественное обнаружение l l l 2. Часть золы смешивают с Si. O 2 (песком), помещают в пробирку и приливают концентрированную серную кислоту. В отверстии пробирки держат стеклянную палочку с каплей воды. В случае наличия фтористого водорода капля мутнеет вследствие выделения кремневой кислоты из образующегося летучего фторида кремния (кремний из силиката стекла). Пары фторида кремния можно при помощи стеклянной трубки пропустить в другую влажную пробирку, при этом стенки пробирки покрывают кремневой кислотой: Са. F 2 + Н 2 SО 4 → Са. SО 4 + 2 НF 4 НF + Si. O 2 → Si. F 4 + 2 Н 20 3 Si. F 4 + 3 Н 20 → Н 2 Si. O 3 + 2 Н 2 Si. F 6 Естественносодержащиеся в организме фториды и кремнефториды по описанной методике анализа не могут дать реакций «травления» стекла или помутнения капли воды от Si. F 4.
 Качественное обнаружение l 3. Небольшое количество золы вносят в короткое колено реактивной трубки, заполненной 2% раствором К 2 Сг 2 О 7 в концентрированной серной кислоте, перемешивают и наблюдают за появлением несмачиваемости стенок трубки в коротком колене – реакция основана на способности НF разрушать стекло и делать его гидрофобным (несмачиваемым). Реакция чувствительна (2 – 5 мкг F– в пробе) и специфична, но ей мешают жиры, кремнийорганические соединения и другие гидрофобные вещества.
Качественное обнаружение l 3. Небольшое количество золы вносят в короткое колено реактивной трубки, заполненной 2% раствором К 2 Сг 2 О 7 в концентрированной серной кислоте, перемешивают и наблюдают за появлением несмачиваемости стенок трубки в коротком колене – реакция основана на способности НF разрушать стекло и делать его гидрофобным (несмачиваемым). Реакция чувствительна (2 – 5 мкг F– в пробе) и специфична, но ей мешают жиры, кремнийорганические соединения и другие гидрофобные вещества.
 Качественное обнаружение l 4. Капельная реакция: при нанесении водного раствора, содержащего фтор, на фильтровальную бумагу, пропитанную цирконализариновым лаком, красная окраска бумаги исчезает (красное окрашивание переходит в светло-желтое). Реактив: А 0, 05 г нитрата циркония растворяют в 20 мл воды; Б 0, 05 г. ализаринового красного растворяют в 20 мл воды. Перед употреблением равные объемы растворов смешивают.
Качественное обнаружение l 4. Капельная реакция: при нанесении водного раствора, содержащего фтор, на фильтровальную бумагу, пропитанную цирконализариновым лаком, красная окраска бумаги исчезает (красное окрашивание переходит в светло-желтое). Реактив: А 0, 05 г нитрата циркония растворяют в 20 мл воды; Б 0, 05 г. ализаринового красного растворяют в 20 мл воды. Перед употреблением равные объемы растворов смешивают.
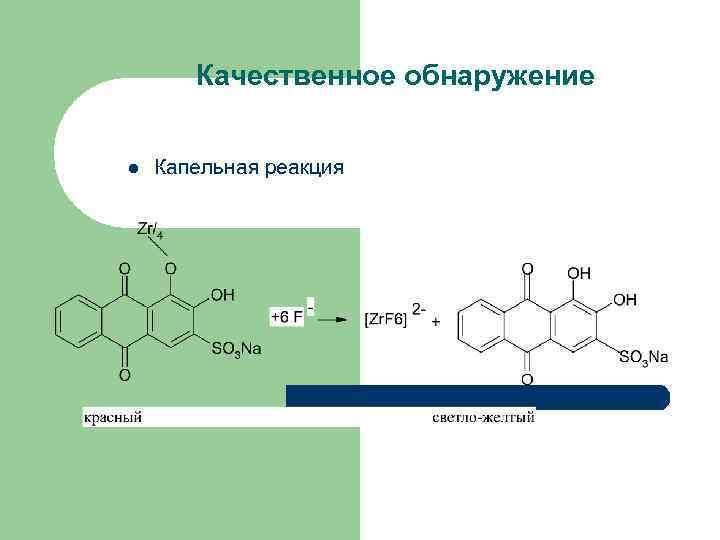 Качественное обнаружение l Капельная реакция
Качественное обнаружение l Капельная реакция
![Качественное обнаружение l l 5. Реакция обесцвечивания тиоцианатного комплекса железа (III): [Fe(SCN)]3 - + Качественное обнаружение l l 5. Реакция обесцвечивания тиоцианатного комплекса железа (III): [Fe(SCN)]3 - +](https://present5.com/presentation/3/-64547806_437587111.pdf-img/-64547806_437587111.pdf-29.jpg) Качественное обнаружение l l 5. Реакция обесцвечивания тиоцианатного комплекса железа (III): [Fe(SCN)]3 - + 6 F- [Fe. F 6]3 - + 6 SCNНаблюдается обесцвечивание кроваво-красного окрашивания комплекса 6. К части образца крови добавляют 25%-ый раствор хлорида кальция. Фториды дают белый желатиновый осадок, который нерастворим в 30% растворе уксусной кислоты, и слабо растворим в разведенной хлористоводородной кислоте.
Качественное обнаружение l l 5. Реакция обесцвечивания тиоцианатного комплекса железа (III): [Fe(SCN)]3 - + 6 F- [Fe. F 6]3 - + 6 SCNНаблюдается обесцвечивание кроваво-красного окрашивания комплекса 6. К части образца крови добавляют 25%-ый раствор хлорида кальция. Фториды дают белый желатиновый осадок, который нерастворим в 30% растворе уксусной кислоты, и слабо растворим в разведенной хлористоводородной кислоте.
 Кремнефтористые соли (фторосиликаты)
Кремнефтористые соли (фторосиликаты)
 Кремнефтористые соли (фторосиликаты) l l l Кремнефторид натрия (Nа 2 Si. F 6). Кремнефторид бария Ва. Si. F 6 Кремнефторид калия. К 2 Si. F 6
Кремнефтористые соли (фторосиликаты) l l l Кремнефторид натрия (Nа 2 Si. F 6). Кремнефторид бария Ва. Si. F 6 Кремнефторид калия. К 2 Si. F 6
 Кремнефтористые соли (фторосиликаты) l l l Сухие кремнефтористые соли разлагаются при нагревании в кислой среде на фтористую соль и фтористый кремний: Nа 2 Si. F 6 + 2 Н+→ 2 HF + Si. F 4 + 2 Na+ Трудно растворимы Ва. Si. F 6 (1: 3731 при 17°С) и К 2 Si. F 6 (1: 833 при 17°С).
Кремнефтористые соли (фторосиликаты) l l l Сухие кремнефтористые соли разлагаются при нагревании в кислой среде на фтористую соль и фтористый кремний: Nа 2 Si. F 6 + 2 Н+→ 2 HF + Si. F 4 + 2 Na+ Трудно растворимы Ва. Si. F 6 (1: 3731 при 17°С) и К 2 Si. F 6 (1: 833 при 17°С).
 Качественное обнаружение l l l К раствору кремнефторида прибавляют раствор хлорида бария. Кристаллический осадок отфильтровывают и высушивают на воздухе. Сухую соль (кремнефторид бария) помещают в платиновый тигель и обливают концентрированной серной кислотой: Ва. Si. F 6 + Н 2 SО 4 → Ва. SО 4 + Н 2 Si. F 6; Н 2 Si. F 6 → 2 HF + Si. F 4 Травление стекла указывает на наличие фтористого водорода, а помутнение поднесенной на палочке капли воды — на фторид кремния:
Качественное обнаружение l l l К раствору кремнефторида прибавляют раствор хлорида бария. Кристаллический осадок отфильтровывают и высушивают на воздухе. Сухую соль (кремнефторид бария) помещают в платиновый тигель и обливают концентрированной серной кислотой: Ва. Si. F 6 + Н 2 SО 4 → Ва. SО 4 + Н 2 Si. F 6; Н 2 Si. F 6 → 2 HF + Si. F 4 Травление стекла указывает на наличие фтористого водорода, а помутнение поднесенной на палочке капли воды — на фторид кремния:
 Качественное обнаружение l l l l 3 Si. F 4 + 3 Н 20 → Н 2 Si. O 3 + 2 Н 2 Si. F 6 Реакцию проводят в платиновом тигле, так как в стеклянной пробирке, образование фторида кремния может иметь место при наличии фторидов. 4. Добавление к раствору соли раствора едкого натра вызывает выпадение осадка кремневой кислоты: Na. HF ↔ Na. F + HF 4 Na. F + Si. O 2 + H 2 O → Si. F 4 + 4 Na. OH 3 Si. F 4 + 3 H 2 O → Н 2 Si. F 6 + Н 2 Si. O 3 (следы в растворе) Н 2 Si. F 6 + 2 Na. OH → Nа 2 Si. F 6 + H 2 O
Качественное обнаружение l l l l 3 Si. F 4 + 3 Н 20 → Н 2 Si. O 3 + 2 Н 2 Si. F 6 Реакцию проводят в платиновом тигле, так как в стеклянной пробирке, образование фторида кремния может иметь место при наличии фторидов. 4. Добавление к раствору соли раствора едкого натра вызывает выпадение осадка кремневой кислоты: Na. HF ↔ Na. F + HF 4 Na. F + Si. O 2 + H 2 O → Si. F 4 + 4 Na. OH 3 Si. F 4 + 3 H 2 O → Н 2 Si. F 6 + Н 2 Si. O 3 (следы в растворе) Н 2 Si. F 6 + 2 Na. OH → Nа 2 Si. F 6 + H 2 O
 Количественное определение l l Количественное определение фторидов в биологических жидкостях проводят колориметрическим и спектрофотометрическим методами по реакции обесцвечивания ализаринциркониевого лака. Чем выше концентрация фторидов, тем в большей степени разрушается комплекс (при увеличении концентрации фторидов оптическая плотность раствора уменьшается).
Количественное определение l l Количественное определение фторидов в биологических жидкостях проводят колориметрическим и спектрофотометрическим методами по реакции обесцвечивания ализаринциркониевого лака. Чем выше концентрация фторидов, тем в большей степени разрушается комплекс (при увеличении концентрации фторидов оптическая плотность раствора уменьшается).
 Токсикологическое значение l l l Токсикологическое значение имеет, главным образом, натриевая соль фтористоводородной кислоты (Na. F) и натриевая соль кремнефтористой кислоты (Nа 2 Si. F 6). Отравления производными фтористоводородной кислоты в большинстве случаев обусловлены ошибочным применением их в быту вместо других солей. Нередко наблюдались отравления животных. Токсическая доза для человека 0, 012 г, смертельная— 10 г (О. И. Глазова). Диагностика отравлений фторидами трудна, так клиника и патологоанатомическая картина нехарактерны.
Токсикологическое значение l l l Токсикологическое значение имеет, главным образом, натриевая соль фтористоводородной кислоты (Na. F) и натриевая соль кремнефтористой кислоты (Nа 2 Si. F 6). Отравления производными фтористоводородной кислоты в большинстве случаев обусловлены ошибочным применением их в быту вместо других солей. Нередко наблюдались отравления животных. Токсическая доза для человека 0, 012 г, смертельная— 10 г (О. И. Глазова). Диагностика отравлений фторидами трудна, так клиника и патологоанатомическая картина нехарактерны.
 ЯДОВИТЫЕ ГАЗООБРАЗНЫЕ ВЕЩЕСТВА
ЯДОВИТЫЕ ГАЗООБРАЗНЫЕ ВЕЩЕСТВА
 Область применения соединений Газы, применяемые в медицине и фармацевтике Токсичные и имеющие побочные эффекты Сжиженные, применяемые в качестве пропеллента в аэрозолях Представители Кислород, окись углерода, гелий, азот Моноксид углерода, сероводород Азот, окись азота, окись углерода, пропан, бутаны, фторированные и хлорированные углеводороды
Область применения соединений Газы, применяемые в медицине и фармацевтике Токсичные и имеющие побочные эффекты Сжиженные, применяемые в качестве пропеллента в аэрозолях Представители Кислород, окись углерода, гелий, азот Моноксид углерода, сероводород Азот, окись азота, окись углерода, пропан, бутаны, фторированные и хлорированные углеводороды
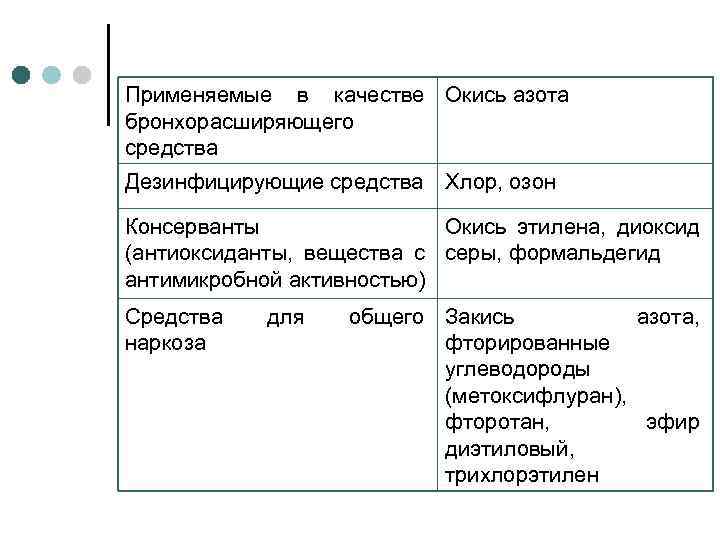 Применяемые в качестве Окись азота бронхорасширяющего средства Дезинфицирующие средства Хлор, озон Консерванты Окись этилена, диоксид (антиоксиданты, вещества с серы, формальдегид антимикробной активностью) Средства наркоза для общего Закись азота, фторированные углеводороды (метоксифлуран), фторотан, эфир диэтиловый, трихлорэтилен
Применяемые в качестве Окись азота бронхорасширяющего средства Дезинфицирующие средства Хлор, озон Консерванты Окись этилена, диоксид (антиоксиданты, вещества с серы, формальдегид антимикробной активностью) Средства наркоза для общего Закись азота, фторированные углеводороды (метоксифлуран), фторотан, эфир диэтиловый, трихлорэтилен
 NB! Пропелленты могут употребляться в качестве средств для злоупотребления. Вдыхание высоких доз галогеноуглеводородов с целью получения состояния эйфории может привести к угнетению ЦНС, дыхания, аритмии, возможно наступление смерти. Пропан и бутаны могут вызывать асфиксию. Примеси хлороводорода и фосгена в пропеллентах (образующиеся при неправильном хранении или истечения срока хранения) могут вызывать повышение температуры тела. ¢ ¢ ¢
NB! Пропелленты могут употребляться в качестве средств для злоупотребления. Вдыхание высоких доз галогеноуглеводородов с целью получения состояния эйфории может привести к угнетению ЦНС, дыхания, аритмии, возможно наступление смерти. Пропан и бутаны могут вызывать асфиксию. Примеси хлороводорода и фосгена в пропеллентах (образующиеся при неправильном хранении или истечения срока хранения) могут вызывать повышение температуры тела. ¢ ¢ ¢
 Оксид углерода (II) l l l Из ядовитых газообразных веществ особый токсикологический и судебно-медицинский интерес представляет окcид углерода (II). Оксид углерода (СО) – бесцветный газ без запаха и вкуса. Молекулярная масса 28, 01. В воде почти не растворяется, горит синеватым пламенем до образования окcида углерода (IV) с выделением тепла. Острые отравления окисью углерода занимают ведущее место среди ингаляционных отравлений, летальные исходы составляют 12, 5% от общего числа всех смертельных отравлений.
Оксид углерода (II) l l l Из ядовитых газообразных веществ особый токсикологический и судебно-медицинский интерес представляет окcид углерода (II). Оксид углерода (СО) – бесцветный газ без запаха и вкуса. Молекулярная масса 28, 01. В воде почти не растворяется, горит синеватым пламенем до образования окcида углерода (IV) с выделением тепла. Острые отравления окисью углерода занимают ведущее место среди ингаляционных отравлений, летальные исходы составляют 12, 5% от общего числа всех смертельных отравлений.
 Оксид углерода (II) l l Источники СО Оксид углерода встречается везде, где существуют условия для неполного сгорания веществ, содержащих углерод, входит в состав многих промышленных газов (доменный, генераторный, коксовый); широко применяется в современном органическом синтезе. Важными источниками СО являются выхлопные газы автомобилей (содержание оксида углерода от 1 до 13%. ), дым от пожара и неверно эксплуатируемые и вентилируемые нагревательные системы. Реже - воздействие солнечных лучей на пары дихлорметана (от типографных линий, детергентов и аэрозолей) может приводить к отравлению оксидом углерода, потому как данный растворитель может быть метаболизирован неспецифическими оксидазами до угарного и углекислого газов.
Оксид углерода (II) l l Источники СО Оксид углерода встречается везде, где существуют условия для неполного сгорания веществ, содержащих углерод, входит в состав многих промышленных газов (доменный, генераторный, коксовый); широко применяется в современном органическом синтезе. Важными источниками СО являются выхлопные газы автомобилей (содержание оксида углерода от 1 до 13%. ), дым от пожара и неверно эксплуатируемые и вентилируемые нагревательные системы. Реже - воздействие солнечных лучей на пары дихлорметана (от типографных линий, детергентов и аэрозолей) может приводить к отравлению оксидом углерода, потому как данный растворитель может быть метаболизирован неспецифическими оксидазами до угарного и углекислого газов.
 Оксид углерода (II) l Превращение и распределение в организме Единственным путем попадания оксида углерода являются дыхательные пути. Токсический эффект для человека наблюдается при вдыхании воздуха с концентрацией СО 3*10 -3 г/л в течение 1 часа. l Основным в механизме токсического действия оксида углерода является образование карбоксигемоглобина (Нb. CO), по реакции: l Нb. O 2+CO Hb. CO+O 2 l Реакция идет с вытеснением О 2, т. к. сродство СО к двухвалентному атому железа порфириновых колец гемоглобина в 204 -209 раз выше сродства к нему кислорода.
Оксид углерода (II) l Превращение и распределение в организме Единственным путем попадания оксида углерода являются дыхательные пути. Токсический эффект для человека наблюдается при вдыхании воздуха с концентрацией СО 3*10 -3 г/л в течение 1 часа. l Основным в механизме токсического действия оксида углерода является образование карбоксигемоглобина (Нb. CO), по реакции: l Нb. O 2+CO Hb. CO+O 2 l Реакция идет с вытеснением О 2, т. к. сродство СО к двухвалентному атому железа порфириновых колец гемоглобина в 204 -209 раз выше сродства к нему кислорода.
 Оксид углерода (II) l l l Диссоциация Hb. CO в 3600 раз медленнее Hb. O, что приводит к нарушению транспорта кислорода и развитию кислородной недостаточности, гемической гипоксии. Mолекулы Hb. CO, т. е. гемоглобина, в которой он связан с оксидом углерода, удерживают кислород более прочно, чем гемоглобин, связанный с 4 -мя молекулами О 2, поэтому отравления СО оказываются более тяжелыми, чем можно было ожидать, исходя из предположения о том, что действие СО ограничиваются только блокированием части молекул Hb. Оксид углерода - не только кровяной, но и клеточный яд, оказывающий прямое токсическое действие на тканевые биохимические системы, содержащие железо: миоглобин, цитохромы, цитохромоксидазу, каталазу, пероксидазу. В незначительной степени оксид углерода окисляется в диоксид углерода. У человека за 1 час образуется 0, 1% СО 2 от общего количества СО.
Оксид углерода (II) l l l Диссоциация Hb. CO в 3600 раз медленнее Hb. O, что приводит к нарушению транспорта кислорода и развитию кислородной недостаточности, гемической гипоксии. Mолекулы Hb. CO, т. е. гемоглобина, в которой он связан с оксидом углерода, удерживают кислород более прочно, чем гемоглобин, связанный с 4 -мя молекулами О 2, поэтому отравления СО оказываются более тяжелыми, чем можно было ожидать, исходя из предположения о том, что действие СО ограничиваются только блокированием части молекул Hb. Оксид углерода - не только кровяной, но и клеточный яд, оказывающий прямое токсическое действие на тканевые биохимические системы, содержащие железо: миоглобин, цитохромы, цитохромоксидазу, каталазу, пероксидазу. В незначительной степени оксид углерода окисляется в диоксид углерода. У человека за 1 час образуется 0, 1% СО 2 от общего количества СО.
 Оксид углерода (II) Распределение в организме При острых отравлениях оксид углерода связывается преимущественно железом гемоглобина эритроцитов. При хронических отравлениях в плазме обнаруживается 25 -30% общего количества окиси углерода, связанной кровью. В значительном количестве СО переходит из крови в ткани. При остром отравлении в скелетных мышцах и миокарде обнаруживается до 14% от общего количества адсорбированной окиси углерода, где она связана с миоглобином. Между содержанием карбоксигемоглобина в крови и карбоксимиоглобина в мышцах существует определенная зависимость. Концентрация карбоксимиоглобина в мышцах всегда примерно в два раза ниже концентрации карбоксигемоглобина в крови. На распределение СО между кровью и мышцами влияют концентрация яда во вдыхаемом воздухе и продолжительность контакта. l l l
Оксид углерода (II) Распределение в организме При острых отравлениях оксид углерода связывается преимущественно железом гемоглобина эритроцитов. При хронических отравлениях в плазме обнаруживается 25 -30% общего количества окиси углерода, связанной кровью. В значительном количестве СО переходит из крови в ткани. При остром отравлении в скелетных мышцах и миокарде обнаруживается до 14% от общего количества адсорбированной окиси углерода, где она связана с миоглобином. Между содержанием карбоксигемоглобина в крови и карбоксимиоглобина в мышцах существует определенная зависимость. Концентрация карбоксимиоглобина в мышцах всегда примерно в два раза ниже концентрации карбоксигемоглобина в крови. На распределение СО между кровью и мышцами влияют концентрация яда во вдыхаемом воздухе и продолжительность контакта. l l l
 Оксид углерода (II) Выделение из организма Оксид углерода выводится из организма в основном через дыхательные пути в течение нескольких часов. После прекращения вдыхания СО 60 -70% токсиканта выделяется у человека в течение первого часа, за четыре часа выделения составляет 96% от абсорбированной организмом дозы. В ничтожном количестве оксид углерода выделяется через кожу: около 0, 007 мл/ч, несколько больше - через желудочно-кишечный тракт и почки. Выделение СО с мочой происходит в виде комплексного соединения с железом. l l l
Оксид углерода (II) Выделение из организма Оксид углерода выводится из организма в основном через дыхательные пути в течение нескольких часов. После прекращения вдыхания СО 60 -70% токсиканта выделяется у человека в течение первого часа, за четыре часа выделения составляет 96% от абсорбированной организмом дозы. В ничтожном количестве оксид углерода выделяется через кожу: около 0, 007 мл/ч, несколько больше - через желудочно-кишечный тракт и почки. Выделение СО с мочой происходит в виде комплексного соединения с железом. l l l
 Оксид углерода (II) l l Диагностическое значение определение оксида углерода в крови Существует определенная связь между тяжестью острого отравления и содержанием карбоксигемоглобина в крови. В случае острого отравления концентрация карбоксигемоглобина составляет около 40%, а при смертельных исходах в крови обнаруживается 60% и более (см. таблицу 1).
Оксид углерода (II) l l Диагностическое значение определение оксида углерода в крови Существует определенная связь между тяжестью острого отравления и содержанием карбоксигемоглобина в крови. В случае острого отравления концентрация карбоксигемоглобина составляет около 40%, а при смертельных исходах в крови обнаруживается 60% и более (см. таблицу 1).
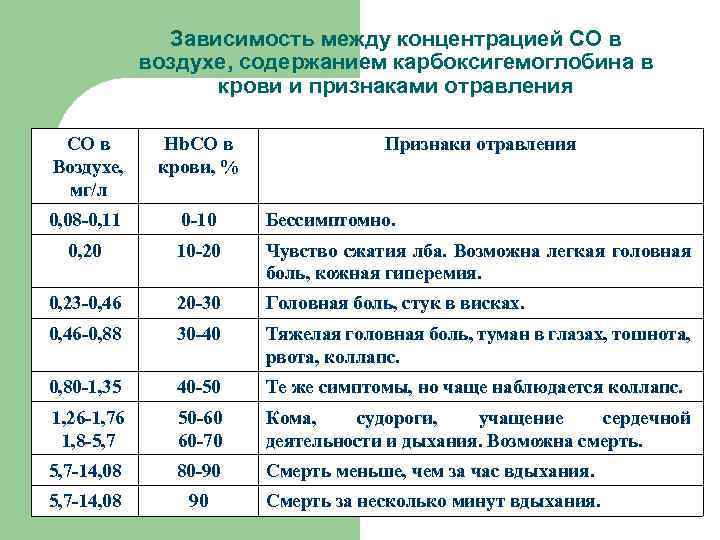 Зависимость между концентрацией СО в воздухе, содержанием карбоксигемоглобина в крови и признаками отравления СО в Воздухе, мг/л Нb. СО в крови, % Признаки отравления 0, 08 -0, 11 0 -10 Бессимптомно. 0, 20 10 -20 Чувство сжатия лба. Возможна легкая головная боль, кожная гиперемия. 0, 23 -0, 46 20 -30 Головная боль, стук в висках. 0, 46 -0, 88 30 -40 Тяжелая головная боль, туман в глазах, тошнота, рвота, коллапс. 0, 80 -1, 35 40 -50 Те же симптомы, но чаще наблюдается коллапс. 1, 26 -1, 76 1, 8 -5, 7 50 -60 60 -70 Кома, судороги, учащение сердечной деятельности и дыхания. Возможна смерть. 5, 7 -14, 08 80 -90 Смерть меньше, чем за час вдыхания. 5, 7 -14, 08 90 Смерть за несколько минут вдыхания.
Зависимость между концентрацией СО в воздухе, содержанием карбоксигемоглобина в крови и признаками отравления СО в Воздухе, мг/л Нb. СО в крови, % Признаки отравления 0, 08 -0, 11 0 -10 Бессимптомно. 0, 20 10 -20 Чувство сжатия лба. Возможна легкая головная боль, кожная гиперемия. 0, 23 -0, 46 20 -30 Головная боль, стук в висках. 0, 46 -0, 88 30 -40 Тяжелая головная боль, туман в глазах, тошнота, рвота, коллапс. 0, 80 -1, 35 40 -50 Те же симптомы, но чаще наблюдается коллапс. 1, 26 -1, 76 1, 8 -5, 7 50 -60 60 -70 Кома, судороги, учащение сердечной деятельности и дыхания. Возможна смерть. 5, 7 -14, 08 80 -90 Смерть меньше, чем за час вдыхания. 5, 7 -14, 08 90 Смерть за несколько минут вдыхания.
 Оксид углерода (II) l l l Скорость образования СО в организме человека составляет 0, 42 – 0, 07 мг/ч и его содержание в литре крови соответственно равно 1 -3 мл. За счет эндогенного оксида углерода физиологический уровень карбоксигемоглобина колеблется от 1, 5 до 3, 4%. Однако эта физиологическая норма бывает значительно повышена в результате вдыхания оксида углерода, загрязняющего воздух городов. У городского населения содержание карбоксигемоглобина составляет в среднем 8, 8%, в то время, как у жителей сельского района оно не превышает в среднем 5, 3%.
Оксид углерода (II) l l l Скорость образования СО в организме человека составляет 0, 42 – 0, 07 мг/ч и его содержание в литре крови соответственно равно 1 -3 мл. За счет эндогенного оксида углерода физиологический уровень карбоксигемоглобина колеблется от 1, 5 до 3, 4%. Однако эта физиологическая норма бывает значительно повышена в результате вдыхания оксида углерода, загрязняющего воздух городов. У городского населения содержание карбоксигемоглобина составляет в среднем 8, 8%, в то время, как у жителей сельского района оно не превышает в среднем 5, 3%.
 Оксид углерода (II) l Значительное влияние на величину карбоксигемоглобина в крови оказывает курение табака. Разница между содержанием карбоксигемоглобина в крови населения России в среднем составляет 5 -6% и наблюдается чаще всего от 1, 5 до 9%.
Оксид углерода (II) l Значительное влияние на величину карбоксигемоглобина в крови оказывает курение табака. Разница между содержанием карбоксигемоглобина в крови населения России в среднем составляет 5 -6% и наблюдается чаще всего от 1, 5 до 9%.
 Классификация отравлений оксидом углерода l l Легкое отравление соответствует удовлетворительному состоянию пострадавших, не терявших сознания в зоне с повышенной концентрацией окиси углерода. Преобладают общемозговые расстройства, незначительно учащены пульс и дыхание. Среднетяжелое отравление обусловливает состояние средней тяжести, даже кратковременная потеря сознания свидетельствует о тяжелой гипоксии. Нарастают общемозговые и психические расстройства, появляются стволово-мозжечковые, пирамидальные и экстрапирамидальные симптомы.
Классификация отравлений оксидом углерода l l Легкое отравление соответствует удовлетворительному состоянию пострадавших, не терявших сознания в зоне с повышенной концентрацией окиси углерода. Преобладают общемозговые расстройства, незначительно учащены пульс и дыхание. Среднетяжелое отравление обусловливает состояние средней тяжести, даже кратковременная потеря сознания свидетельствует о тяжелой гипоксии. Нарастают общемозговые и психические расстройства, появляются стволово-мозжечковые, пирамидальные и экстрапирамидальные симптомы.
 Классификация отравлений оксидом углерода l l Тяжелое отравление отмечается у больных в коматозном состоянии, с выраженными расстройствами дыхания и функции сердечнососудистой системы. Возможно развитие кожнотрофических расстройств и нарушение почечной функции. Тяжесть состояния пострадавших коррелирует с содержанием карбоксигемоглобина в крови. Интенсивное курение сигарет может поднять содержание карбоксигемоглобина до 16%. При концентрации карбокcигемоглобина более 20% появляется общемозговая симптоматика, около 50% – выраженная картина отравления окисью углерода, а при концентрации 60– 70% – потеря сознания, судороги, выраженные расстройства дыхания и функций сердечно-сосудистой системы с возможным летальным исходом.
Классификация отравлений оксидом углерода l l Тяжелое отравление отмечается у больных в коматозном состоянии, с выраженными расстройствами дыхания и функции сердечнососудистой системы. Возможно развитие кожнотрофических расстройств и нарушение почечной функции. Тяжесть состояния пострадавших коррелирует с содержанием карбоксигемоглобина в крови. Интенсивное курение сигарет может поднять содержание карбоксигемоглобина до 16%. При концентрации карбокcигемоглобина более 20% появляется общемозговая симптоматика, около 50% – выраженная картина отравления окисью углерода, а при концентрации 60– 70% – потеря сознания, судороги, выраженные расстройства дыхания и функций сердечно-сосудистой системы с возможным летальным исходом.
 Детоксикация отравлений оксидом углерода l l Лечение надо начинать безотлагательно! Если пострадавший продолжает оставаться в коматозном состоянии более 7 -8 часов, прогноз неблагоприятный. Вот почему, как только пострадавшего вынесли из помещения, где произошло отравление, ему сначала дают 100% кислород через маску до тех пор, пока содержание карбоксигемоглобина не понизится до безопасного уровня (10%). Наиболее эффективным методом лечения является гипербарическая оксигенация, которая показана в тех случаях, когда содержание карбоксигемоглобина превышает 15%. Уже после одного сеанса лечения содержание карбоксигемоглобина снижается с 50 до 5 -10%. При остановке дыхания показана интубация и аппаратное дыхание, которое также проводится под давлением. В наиболее тяжелых случаях отравления может оказаться жизнеспасительным частичное обменное переливание крови. Показано симптоматическое лечение.
Детоксикация отравлений оксидом углерода l l Лечение надо начинать безотлагательно! Если пострадавший продолжает оставаться в коматозном состоянии более 7 -8 часов, прогноз неблагоприятный. Вот почему, как только пострадавшего вынесли из помещения, где произошло отравление, ему сначала дают 100% кислород через маску до тех пор, пока содержание карбоксигемоглобина не понизится до безопасного уровня (10%). Наиболее эффективным методом лечения является гипербарическая оксигенация, которая показана в тех случаях, когда содержание карбоксигемоглобина превышает 15%. Уже после одного сеанса лечения содержание карбоксигемоглобина снижается с 50 до 5 -10%. При остановке дыхания показана интубация и аппаратное дыхание, которое также проводится под давлением. В наиболее тяжелых случаях отравления может оказаться жизнеспасительным частичное обменное переливание крови. Показано симптоматическое лечение.
 Определение оксида углерода в крови l l Для определения оксида углерода в крови можно использовать различные методы, включая предварительные пробы, спектрофотометрию, газовую хроматографию и специальные методы. Методы анализа оксида углерода в крови дают возможность определять либо основную часть СО, связанную с гемоглобином, либо общее количество его, т. е. СО карбоксигемоглобина и плазмы. В первом случае проводят определение оксида углерода по карбоксигемоглобину, во втором – выделяют из пробы крови газообразную смесь СО, СО 2, N 2, замеряют количество газа и тем или иным способом устанавливают содержание в нем оксида углерода.
Определение оксида углерода в крови l l Для определения оксида углерода в крови можно использовать различные методы, включая предварительные пробы, спектрофотометрию, газовую хроматографию и специальные методы. Методы анализа оксида углерода в крови дают возможность определять либо основную часть СО, связанную с гемоглобином, либо общее количество его, т. е. СО карбоксигемоглобина и плазмы. В первом случае проводят определение оксида углерода по карбоксигемоглобину, во втором – выделяют из пробы крови газообразную смесь СО, СО 2, N 2, замеряют количество газа и тем или иным способом устанавливают содержание в нем оксида углерода.
 Определение оксида углерода в крови l l l l Предварительные пробы (экспресс – тесты) Экспресс-тесты или пробы проводятся непосредственно на месте происшествия или сразу после поступления пострадавшего в больницу или клинику. Цель – быстро установить наличие карбоксигемоглобина (Нb. СО). Проба 1. К 15 мл воды добавляют 1 -2 капли исследуемой крови и отдельно донорскую кровь, пробирки встряхивают. Норма – светло-розовый цвет. Нb. СО – вишнево-красный цвет. Затем добавляют 5 капель 20% раствора едкого натра. После энергичного встряхивания при наличии Нb. СО в течение нескольких секунд сохраняется светло-розовый цвет (концентрация Нb. СО не менее 20%). Если светло-розовый цвет перейдет в соломенно-желтый – в крови нет Нb. СО или его содержится менее 20%. Целесообразно провести контрольную пробу с донорской кровью.
Определение оксида углерода в крови l l l l Предварительные пробы (экспресс – тесты) Экспресс-тесты или пробы проводятся непосредственно на месте происшествия или сразу после поступления пострадавшего в больницу или клинику. Цель – быстро установить наличие карбоксигемоглобина (Нb. СО). Проба 1. К 15 мл воды добавляют 1 -2 капли исследуемой крови и отдельно донорскую кровь, пробирки встряхивают. Норма – светло-розовый цвет. Нb. СО – вишнево-красный цвет. Затем добавляют 5 капель 20% раствора едкого натра. После энергичного встряхивания при наличии Нb. СО в течение нескольких секунд сохраняется светло-розовый цвет (концентрация Нb. СО не менее 20%). Если светло-розовый цвет перейдет в соломенно-желтый – в крови нет Нb. СО или его содержится менее 20%. Целесообразно провести контрольную пробу с донорской кровью.
 Определение оксида углерода в крови l l l Проба 2. В две пробирки вносят по 10 мл воды, затем: в первую – 5 капель анализируемой пробы (кровь) и 5 капель свежеприготовленного раствора сульфида аммония; во вторую – 5 капель донорской крови и 5 капель свежеприготовленного раствора сульфида аммония. Осторожно перемешать и добавить в обе пробирки по 2 -3 капли 30% раствора уксусной кислоты. Анализируемая проба при наличии карбоксигемоглобина окрашивается в красный цвет, контрольная проба (донорская) – в грязно-зеленый.
Определение оксида углерода в крови l l l Проба 2. В две пробирки вносят по 10 мл воды, затем: в первую – 5 капель анализируемой пробы (кровь) и 5 капель свежеприготовленного раствора сульфида аммония; во вторую – 5 капель донорской крови и 5 капель свежеприготовленного раствора сульфида аммония. Осторожно перемешать и добавить в обе пробирки по 2 -3 капли 30% раствора уксусной кислоты. Анализируемая проба при наличии карбоксигемоглобина окрашивается в красный цвет, контрольная проба (донорская) – в грязно-зеленый.
 Определение оксида углерода в крови l l l Проба 3. К 5 мл крови, разбавленной в 100 раз, добавляют 5 капель концентрированного раствора сульфида меди. Длительно и энергично встряхивают. Кровь, содержащая карбоксигемоглобин – красного цвета, не содержащая – зеленого. Проба 4. К одной капле крови добавляют 40 капель воды и 5 капель 40% раствора фенилгидразина. При содержании карбоксигемоглобина окраска крови остается светло-красной, при отсутствии – темно- или черно-красной. Проба 5. К 5 мл крови, разведенной в 100 раз, добавляют 5 капель 1% раствора К 4 (Fе(СN)6). Кровь, содержащая карбоксигемоглобин, вишневого цвета, не содержащая – светло-коричневого (железо гемоглобина окисляется до Fе - геминовая формула – метгемоглобин).
Определение оксида углерода в крови l l l Проба 3. К 5 мл крови, разбавленной в 100 раз, добавляют 5 капель концентрированного раствора сульфида меди. Длительно и энергично встряхивают. Кровь, содержащая карбоксигемоглобин – красного цвета, не содержащая – зеленого. Проба 4. К одной капле крови добавляют 40 капель воды и 5 капель 40% раствора фенилгидразина. При содержании карбоксигемоглобина окраска крови остается светло-красной, при отсутствии – темно- или черно-красной. Проба 5. К 5 мл крови, разведенной в 100 раз, добавляют 5 капель 1% раствора К 4 (Fе(СN)6). Кровь, содержащая карбоксигемоглобин, вишневого цвета, не содержащая – светло-коричневого (железо гемоглобина окисляется до Fе - геминовая формула – метгемоглобин).
 Определение оксида углерода в крови Газовая хроматография Метод газовой хроматографии является достаточно простым и прямым методом определения общего количества оксида углерода в крови. Высвобождение СО из карбоксигемоглобина в крови достигается обычно добавлением к крови растворов карбоната натрия, натрия бикарбоната, ферроцианида калия и т. п. Оксид углерода переходит в газовую фазу. Газовая фаза вводится в хроматограф, снабженный детектором по теплопроводности. Концентрация СО определяется по калибровочному графику после измерения площади пика. Данный метод дает достаточные результаты при концентрациях карбоксигемоглобина от 30% до 100%. l l l
Определение оксида углерода в крови Газовая хроматография Метод газовой хроматографии является достаточно простым и прямым методом определения общего количества оксида углерода в крови. Высвобождение СО из карбоксигемоглобина в крови достигается обычно добавлением к крови растворов карбоната натрия, натрия бикарбоната, ферроцианида калия и т. п. Оксид углерода переходит в газовую фазу. Газовая фаза вводится в хроматограф, снабженный детектором по теплопроводности. Концентрация СО определяется по калибровочному графику после измерения площади пика. Данный метод дает достаточные результаты при концентрациях карбоксигемоглобина от 30% до 100%. l l l
 Определение оксида углерода в крови Спектрофотометрические методы Объектами исследования на СО являются главным образом кровь и воздух, содержащий окись углерода, в частности, воздух производственных предприятий. Большое диагностическое значение имеет определение карбокcигемоглобина в крови, взятой непосредственно на месте происшествия, так как при оказании пострадавшему первой помощи происходит частичная элиминация угарного газа и снижается содержание Hb. CO в крови. Карбокcигемоглобин в крови трупа можно определять спустя очень длительный (до 2 лет) срок после смерти (спектрофотометрический метод). Спектрофотометрические методы привлекательны по той причине, что все гемоглобиновые структуры имеют абсорбцию в определенной части спектра. Из большого числа вариантов спектрофотометрического метода рассмотрим только некоторые l l
Определение оксида углерода в крови Спектрофотометрические методы Объектами исследования на СО являются главным образом кровь и воздух, содержащий окись углерода, в частности, воздух производственных предприятий. Большое диагностическое значение имеет определение карбокcигемоглобина в крови, взятой непосредственно на месте происшествия, так как при оказании пострадавшему первой помощи происходит частичная элиминация угарного газа и снижается содержание Hb. CO в крови. Карбокcигемоглобин в крови трупа можно определять спустя очень длительный (до 2 лет) срок после смерти (спектрофотометрический метод). Спектрофотометрические методы привлекательны по той причине, что все гемоглобиновые структуры имеют абсорбцию в определенной части спектра. Из большого числа вариантов спектрофотометрического метода рассмотрим только некоторые l l
 Определение оксида углерода в крови Спектроскопический метод В основу спектроскопического (и микроспектрального) анализа положено свойство гемоглобина и его производных поглощать волны света определенной длины, поэтому при прохождении луча света через растворы, содержащие гемоглобин или его производные, в спектре появляются темные полосы поглощения, расположенные в определенной части спектра для каждого производного гемоглобина. l l
Определение оксида углерода в крови Спектроскопический метод В основу спектроскопического (и микроспектрального) анализа положено свойство гемоглобина и его производных поглощать волны света определенной длины, поэтому при прохождении луча света через растворы, содержащие гемоглобин или его производные, в спектре появляются темные полосы поглощения, расположенные в определенной части спектра для каждого производного гемоглобина. l l
 Определение оксида углерода в крови l l Количественное определение карбоксигемоглобина в крови колориметрически (Модифицированный метод Вольфа) Этот метод основан на том, что при р. Н = 4, 95, температуре 55– 60 ОС, за время 10 -15 минут оксигемоглобин выпадает в осадок быстрее, чем карбоксигемоглобин. Таким образом, эти два вещества отделяют и Нb. СО определяют колориметрически. Прежде всего строят калибровочную кривую, используя растворы разной степени разведения из образца крови с известным содержанием гемоглобина и исследуют на фотоколориметре. Исследуемый образец крови разбавляют в 50 -100 раз, измеряют светопоглощение и по калибровочной кривой находят концентрацию гемоглобина.
Определение оксида углерода в крови l l Количественное определение карбоксигемоглобина в крови колориметрически (Модифицированный метод Вольфа) Этот метод основан на том, что при р. Н = 4, 95, температуре 55– 60 ОС, за время 10 -15 минут оксигемоглобин выпадает в осадок быстрее, чем карбоксигемоглобин. Таким образом, эти два вещества отделяют и Нb. СО определяют колориметрически. Прежде всего строят калибровочную кривую, используя растворы разной степени разведения из образца крови с известным содержанием гемоглобина и исследуют на фотоколориметре. Исследуемый образец крови разбавляют в 50 -100 раз, измеряют светопоглощение и по калибровочной кривой находят концентрацию гемоглобина.
 Определение оксида углерода в крови Спектрофотометрический метод Фрейтвурста и Майнеке Метод основан на определении поглощения света при λ=575 или 578 нм раствором гемолизированной крови до и после восстановления оксигемоглобина гидросульфитом натрия. В случае 100% насыщения крови угарным газом величина поглощения света после добавки гидросульфита не меняется. При неполном насыщении или при отсутствии СО она уменьшается. По степени этого уменьшения определяют процент Нb. СО в исследуемом образце. Метод можно использовать при длительном посмертном сроке (до 2 лет). l l
Определение оксида углерода в крови Спектрофотометрический метод Фрейтвурста и Майнеке Метод основан на определении поглощения света при λ=575 или 578 нм раствором гемолизированной крови до и после восстановления оксигемоглобина гидросульфитом натрия. В случае 100% насыщения крови угарным газом величина поглощения света после добавки гидросульфита не меняется. При неполном насыщении или при отсутствии СО она уменьшается. По степени этого уменьшения определяют процент Нb. СО в исследуемом образце. Метод можно использовать при длительном посмертном сроке (до 2 лет). l l
 Определение оксида углерода в крови Количественное определение карбоксигемоглобина в крови методом спектрофотометрии При добавлении восстановителя (натрия тиосульфата) к исследуемой крови окси- и метгемоглобин количественно разлагаются с образованием восстановленной формы гемоглобина. Последняя имеет спектр поглощения, представленный на рис. 1 линией В. l l
Определение оксида углерода в крови Количественное определение карбоксигемоглобина в крови методом спектрофотометрии При добавлении восстановителя (натрия тиосульфата) к исследуемой крови окси- и метгемоглобин количественно разлагаются с образованием восстановленной формы гемоглобина. Последняя имеет спектр поглощения, представленный на рис. 1 линией В. l l
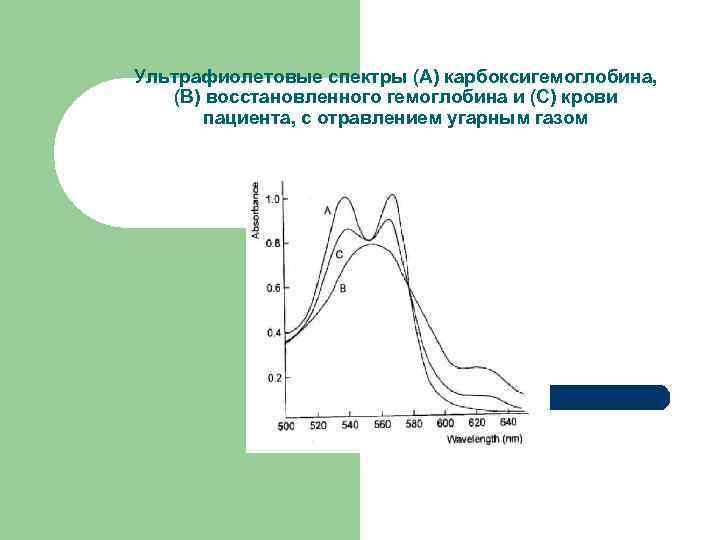 Ультрафиолетовые спектры (А) карбоксигемоглобина, (В) восстановленного гемоглобина и (С) крови пациента, с отравлением угарным газом
Ультрафиолетовые спектры (А) карбоксигемоглобина, (В) восстановленного гемоглобина и (С) крови пациента, с отравлением угарным газом
 Определение оксида углерода в крови l Оксид углерода (II) имеет большее сродство к гемоглобину, чем кислород, и поэтому комплекс Нb. СО не может быть разрушен тиосульфатом натрия. Таким образом, после обработки тиосульфатом натрия комплекс Нb. СО проявляется характерным спектром с двумя максимумами поглощения, представленным на рис. 1 линией А. Максимальная разница оптической плотности между спектрами А и В отмечается при длине волны 540 нм, тогда как при длине волны 579 нм оптическая плотность практически одинакова. Процентное содержание СО в крови (линия А) может быть вычислено, исходя из значения оптической плотности «здоровой» , не содержащей Нb. СО, крови (линия В) и исследуемого образца (линия С), после восстановления каждого из них тиосульфатом натрия.
Определение оксида углерода в крови l Оксид углерода (II) имеет большее сродство к гемоглобину, чем кислород, и поэтому комплекс Нb. СО не может быть разрушен тиосульфатом натрия. Таким образом, после обработки тиосульфатом натрия комплекс Нb. СО проявляется характерным спектром с двумя максимумами поглощения, представленным на рис. 1 линией А. Максимальная разница оптической плотности между спектрами А и В отмечается при длине волны 540 нм, тогда как при длине волны 579 нм оптическая плотность практически одинакова. Процентное содержание СО в крови (линия А) может быть вычислено, исходя из значения оптической плотности «здоровой» , не содержащей Нb. СО, крови (линия В) и исследуемого образца (линия С), после восстановления каждого из них тиосульфатом натрия.
 Определение оксида углерода в крови Интерпретация результатов норма <5%; для курильщиков характерно <10%; появление симптоматической головной боли характерно при концентрациях от 10 до 20%; токсическая концентрация от 20 до 30%; потенциально смертельная концентрация >45%. l l
Определение оксида углерода в крови Интерпретация результатов норма <5%; для курильщиков характерно <10%; появление симптоматической головной боли характерно при концентрациях от 10 до 20%; токсическая концентрация от 20 до 30%; потенциально смертельная концентрация >45%. l l
 Определение оксида углерода в крови Химические методы (дополнительно к экспресс-тестам) Суть методов состоит в том, что при добавлении соответствующих реактивов окраска нормальной крови изменяется, а кровь, содержащая карбоксигемоглобин, окраску не изменяет или изменяет незначительно. Поэтому всегда проводят два параллельных опыта. 1. Проба Гоппе-Зейлера. К пробам испытуемой и нормальной крови прибавляют равные объемы 30% раствора едкого натра: кровь, содержащая окись углерода, сохраняет розовую окраску, а контрольная принимает зеленовато-черную окраску. l l 2. Проба Кункеля-Ветцеля. К разбавленным в соотношении 1: 4 пробам исследуемой и контрольной крови прибавляют приблизительно по три объема 1% раствора танина и взбалтывают: кровь, содержащая окись углерода, сохраняет розовый цвет; контрольная кровь принимает серую окраску. l 3. Проба Сидорова. К 2 мл разбавленных проб контрольной и испытуемой крови прибавляют по 3 -5 капель 30% раствора гексацианоферрата калия и 0, 01% раствора бихромата калия: кровь, содержащая окись углерода, окрашивается в карминово-красный цвет, контрольная кровь буреет.
Определение оксида углерода в крови Химические методы (дополнительно к экспресс-тестам) Суть методов состоит в том, что при добавлении соответствующих реактивов окраска нормальной крови изменяется, а кровь, содержащая карбоксигемоглобин, окраску не изменяет или изменяет незначительно. Поэтому всегда проводят два параллельных опыта. 1. Проба Гоппе-Зейлера. К пробам испытуемой и нормальной крови прибавляют равные объемы 30% раствора едкого натра: кровь, содержащая окись углерода, сохраняет розовую окраску, а контрольная принимает зеленовато-черную окраску. l l 2. Проба Кункеля-Ветцеля. К разбавленным в соотношении 1: 4 пробам исследуемой и контрольной крови прибавляют приблизительно по три объема 1% раствора танина и взбалтывают: кровь, содержащая окись углерода, сохраняет розовый цвет; контрольная кровь принимает серую окраску. l 3. Проба Сидорова. К 2 мл разбавленных проб контрольной и испытуемой крови прибавляют по 3 -5 капель 30% раствора гексацианоферрата калия и 0, 01% раствора бихромата калия: кровь, содержащая окись углерода, окрашивается в карминово-красный цвет, контрольная кровь буреет.
 Определение оксида углерода в крови l 4. Проба Либмана. К 5 мл крови добавляют 5 мл формалина и сильно взбалтывают. Кровь, содержащая карбоксигемоглобин, сохраняет алую окраску, а кровь, не содержащая карбоксигемоглобина, через несколько минут становится коричнево-черной. l 5. Проба Бюркера. К 5 мл крови добавляют 500 мл воды и сильно взбалтывают. К 5 мл полученного раствора добавляют 5 капель 1% раствора гексацианоферрата калия. Кровь, содержащая карбоксигемоглобин, сохраняет алую окраску, а кровь, не содержащая карбоксигемоглобина, становится желтоватой. l 6. Проба Рубнера. Контрольная кровь, смешанная с 5 частями раствора основного ацетата свинца, принимает грязно-зеленое окрашивание. Кровь с окисью углерода сохраняет свой цвет. l 7. Проба Хорошкевича-Маркса. К 2 мл крови добавляют 4 мл 8% раствора хинина гидрохлорида, доводяи до кипения. После охлаждения добавляют 2 -3 капли сульфида аммония: нормальная кровь – грязно-бурого цвета, содержащая карбоксигемоглобин, - красная.
Определение оксида углерода в крови l 4. Проба Либмана. К 5 мл крови добавляют 5 мл формалина и сильно взбалтывают. Кровь, содержащая карбоксигемоглобин, сохраняет алую окраску, а кровь, не содержащая карбоксигемоглобина, через несколько минут становится коричнево-черной. l 5. Проба Бюркера. К 5 мл крови добавляют 500 мл воды и сильно взбалтывают. К 5 мл полученного раствора добавляют 5 капель 1% раствора гексацианоферрата калия. Кровь, содержащая карбоксигемоглобин, сохраняет алую окраску, а кровь, не содержащая карбоксигемоглобина, становится желтоватой. l 6. Проба Рубнера. Контрольная кровь, смешанная с 5 частями раствора основного ацетата свинца, принимает грязно-зеленое окрашивание. Кровь с окисью углерода сохраняет свой цвет. l 7. Проба Хорошкевича-Маркса. К 2 мл крови добавляют 4 мл 8% раствора хинина гидрохлорида, доводяи до кипения. После охлаждения добавляют 2 -3 капли сульфида аммония: нормальная кровь – грязно-бурого цвета, содержащая карбоксигемоглобин, - красная.
 Определение оксида углерода в крови l 8. Проба Сальковского-Катаяма. К 10 мл дистиллированной воды добавляют по 5 капель крови и сульфида аммония, осторожно взбалтывают, добавляют 30% раствор уксусной кислоты до слабокислой реакции: нормальная кровь – серозелёная, содержащая карбоксигемоглобин, - малиновокрасная. l 9. Проба Ветцеля. К 10 мл разбавленной крови добавляют 5 мл 20% раствора гексацианоферрата калия и 1 мл ледяной уксусной кислоты. Нормальная кровь образует сероватокоричневый осадок, а исследуемая – вишнево-красный осадок. l 10. Проба Залесского. К 5 мл разбавленной крови добавляют 5 капель 10% раствора сульфата меди. Нормальная кровь – зеленоватая, содержащая карбоксигемоглобин, - красная.
Определение оксида углерода в крови l 8. Проба Сальковского-Катаяма. К 10 мл дистиллированной воды добавляют по 5 капель крови и сульфида аммония, осторожно взбалтывают, добавляют 30% раствор уксусной кислоты до слабокислой реакции: нормальная кровь – серозелёная, содержащая карбоксигемоглобин, - малиновокрасная. l 9. Проба Ветцеля. К 10 мл разбавленной крови добавляют 5 мл 20% раствора гексацианоферрата калия и 1 мл ледяной уксусной кислоты. Нормальная кровь образует сероватокоричневый осадок, а исследуемая – вишнево-красный осадок. l 10. Проба Залесского. К 5 мл разбавленной крови добавляют 5 капель 10% раствора сульфата меди. Нормальная кровь – зеленоватая, содержащая карбоксигемоглобин, - красная.
 Определение оксида углерода в крови l l Реакции можно также производить, смочив разведенной кровью белую фильтровальную бумагу, а затем нанося на нее реактивы. Заключение о наличии карбоксигемоглобина можно сделать на основании большинства этих реакций. Если в крови мало карбоксигемоглобина, то окраска может измениться, поэтому все реакции непригодны для малых концентраций карбоксигемоглобина.
Определение оксида углерода в крови l l Реакции можно также производить, смочив разведенной кровью белую фильтровальную бумагу, а затем нанося на нее реактивы. Заключение о наличии карбоксигемоглобина можно сделать на основании большинства этих реакций. Если в крови мало карбоксигемоглобина, то окраска может измениться, поэтому все реакции непригодны для малых концентраций карбоксигемоглобина.
 Обнаружение окиси углерода в воздухе l l l Количественное определение окиси углерода в воздухе. Метод основан на окислении окиси углерода йодноватым ангидридом и определении образовавшегося угольного ангидрида. Реакция протекает по уравнению: l I 2 O 5 + 5 CO = 5 CO 2 + I 2 Угольный ангидрид поглощается раствором гидроксида бария: l Ва(ОН)2 + СО 2 = Ва. СО 3 + Н 2 О Избыток гидроксида бария оттитровывают (микротитрование) хлористоводородной кислотой: l Ва(ОН)2 + 2 НСl = Ва. Сl 2 + 2 Н 2 О
Обнаружение окиси углерода в воздухе l l l Количественное определение окиси углерода в воздухе. Метод основан на окислении окиси углерода йодноватым ангидридом и определении образовавшегося угольного ангидрида. Реакция протекает по уравнению: l I 2 O 5 + 5 CO = 5 CO 2 + I 2 Угольный ангидрид поглощается раствором гидроксида бария: l Ва(ОН)2 + СО 2 = Ва. СО 3 + Н 2 О Избыток гидроксида бария оттитровывают (микротитрование) хлористоводородной кислотой: l Ва(ОН)2 + 2 НСl = Ва. Сl 2 + 2 Н 2 О
 Токсикологическое значение l l Отравления окисью углерода встречаются часто. Преждевременное закрытие печей, чугунные печи, пропускающие в накаленном состоянии окись углерода, камины, снабженные вьюшками, жаровни - обыкновенные источники отравлений окисью углерода и быту. Окись углерода, вызывающая профессиональные отравления, может получиться путем восстановления угольного ангидрида при прохождении его через раскаленный уголь, что имеет место в доменных печах, литейных мастерских и других производствах: l СО 2 + С = 2 CO
Токсикологическое значение l l Отравления окисью углерода встречаются часто. Преждевременное закрытие печей, чугунные печи, пропускающие в накаленном состоянии окись углерода, камины, снабженные вьюшками, жаровни - обыкновенные источники отравлений окисью углерода и быту. Окись углерода, вызывающая профессиональные отравления, может получиться путем восстановления угольного ангидрида при прохождении его через раскаленный уголь, что имеет место в доменных печах, литейных мастерских и других производствах: l СО 2 + С = 2 CO
 Токсикологическое значение l l Содержание СО в водяном газе может доходить до 50%. При разложении пироксилина, что имеет место при взрыве артиллерийских снарядов, мин, образуются газы, содержащие до 30% окиси углерода, что может повлечь массовые отравления. В связи с развитием автомобильного транспорта необходимо учитывать поступление в воздух городов больших количеств окиси углерода. В табачном дыме находятся значительные количества окиси углерода.
Токсикологическое значение l l Содержание СО в водяном газе может доходить до 50%. При разложении пироксилина, что имеет место при взрыве артиллерийских снарядов, мин, образуются газы, содержащие до 30% окиси углерода, что может повлечь массовые отравления. В связи с развитием автомобильного транспорта необходимо учитывать поступление в воздух городов больших количеств окиси углерода. В табачном дыме находятся значительные количества окиси углерода.
 Благодарю за внимание!
Благодарю за внимание!


