aminokisloty_2.ppt
- Количество слайдов: 62

Тема следующей лекции «Микробиологический синтез аминокислот» 1

Микробиологический метод получения аминокислот, наиболее распро- страненный в настоящее время, основан на способности микроорганизмов синтезировать все Lаминокислоты, а в определенных условиях – обеспечивать их сверхсинтез. 2

Биосинтез аминокислот в микробных клетках протекает в виде так называемых свободных аминокислот или «пула аминокислот» , из которого в процессах конструктивного метаболизма синтезируются клеточные макромолекулы. 3

Пути синтеза большинства аминокислот взаимосвязаны. При этом одни аминокислоты являются предшественниками для биосинтеза других. 4

Предшественники: u Пируват лейцина; аланина, валина, u 3 -фосфоглицерат глицина, цистеина; – серина, u щавелево-уксусная кислота – аспартата, аспарагина, метионина, лизина, треонина, изолейцина; 5

u α-кетоглутаровая кислота – глутамата, глутамина, аргинина, пролина; u фосфоенолпируват+эритро зо-4 - фосфат – фенилаланина, тирозина, триптофана; u 5 -фосфорибозил-1 - пирофосфат + АТФ – 6

Контроль осуществляется по принципу обратной связи u на уровне генов, ответственных за синтез соответствующих ферментов (репрессия), u на уровне самих ферментов, которые в результате избытка образующихся аминокислот могут изменять свою активность (ретроингибирование). 7

Данный механизм контроля исключает перепроизводство аминокислот и также препятствует их выделению из клеток в окружающую среду. 8

Чтобы добиться сверхсинтеза отдельных аминокислот, нужно обойти или изменить данный контрольный механизм их синтеза. 9

два варианта u. Состав и условия среды – влияние на ферменты u. Генетические блоки 10

Ауксотрофные мутанты – это организмы, утратившие способность к синтезу одной или нескольких аминокислот. 11

Среди продуцентов аминокислот – различные микроорганизмы, представители родов: u Corynebacterium, Brevibacterium, u Bacillus, u Aerobacter, u Microbacterium, u Eschirichia. u 12

Синтез L- глутамата можно переключить на образование L-глутамина или L- пролина, изменяя условия ферментации. 13

Например: u При повышении концентрации ионов аммония и биотина в среде стимулируется образование Lпролина; u слабо кислая среда и ионы цинка при избытке аммония усиливают синтез L-глутамина. 14

Ауксотрофные мутанты используют в тех случаях, когда необходимо синтезировать аминокислоты, являющиеся конечными продуктами разветвленных цепей метаболических реакций аминокислот. 15

Например, для получения: u L-лизина, L-треонина, L-метионина или L-изолейцина, для которых общим предшественником является L-аспартат, применяют мутанты, ауксотрофные по гомосерину или треонину и гомосерину. 16

Ауксотрофные мутанты не способны образовывать ингибиторы соответствующего метаболического пути, работающие по принципу отрицательной обратной связи из-за отсутствия определенной ключевой ферментативной реакции. Поэтому при выращивании такого штамма в среде с минималь- ной концентрацией необходимого ингредиента (аминокислоты) они способны на суперпродукцию аминокислотыпредшественника. 17

Ауксотрофные мутанты, способные накапливать конечные продукты неразветвленных цепей биосинтеза, например Lаргинина, невозможны. 18

В данной ситуации приходится получать мутанты с частично нарушенной регуляцией биосинтеза, так как это позволяет повысить выход целевого продукта. Такие организмы являются регуляторными мутантами. 19

Максимальная продукция аминокислоты наступает, как правило, когда прирост биомассы практически прекращается. Поэтому питательная среда: u на первом этапе ферментации должна обеспечивать сбалансированный рост клеток; u а на втором – условия для сверхсинтеза целевой аминокислоты. 20

L-глутаминовая кислота (αаминоглутаровая) – первая аминокислота, полученная на основе промышленного микробиологического синтеза: НООС – СН 2 – NH 2 СН – СООН Глутаминовая кислота является важнейшей аминокислотой растительных и животных белков, не будучи незаменимой. 21

Синтез глутаминовой кислоты происходит в цикле трикарбоновых кислот в результате ферментативного восстановительного аминирования 2 -кетоглутаровой кислоты НАДФзависимой глутаматдегидрогеназой: НООС – СН 2 – СООН + НАД(Ф)Н 2 + NН 3 → НООС – СН 2 – NН 2 СН – СООН + НАД(Ф). 22

Продуцировать глутаминовую кислоту способны дрожжи, микроскопические грибы, бактерии. Бактерии обеспечивают наибольший выход по отношению к использованному углеродному субстрату (не менее 40– 50 %). 23

Промышленные продуценты u Micrococcus, u Brevibacterium, u Microbacterium, u Corynebacterium 24

Сверхсинтез кислоты у диких штаммов возможен в специальных физиологических условиях при торможении скорости роста и увеличении проницаемости клеточной мембраны для глутаминовой кислоты. Такие условия обеспечивает определенная концентрация биотина в среде (1– 5 мкг/л), а также присутствие некоторых антибиотиков. 25

Сверхпродукция глутаминовой кислоты связана также с высокой концентрацией аммония в среде, высокой активностью НАД(Ф)Н-зависимой глутаматдегидрогеназы и отсутствием или дефектом α-кетоглутаратдегидрогеназы, катализирующей превращение 2 - кетоглутарата в янтарную кислоту. 26

Получение глутаминовой кислоты и глутамата натрия u Микроорганизмы - продуценты глутаминовой кислоты. Факторы, регулирующие накопление глутаминовой кислоты. Технология производства глутаминовой кислоты. Характеристика готового продукта. Получение глутамата натрия. 27
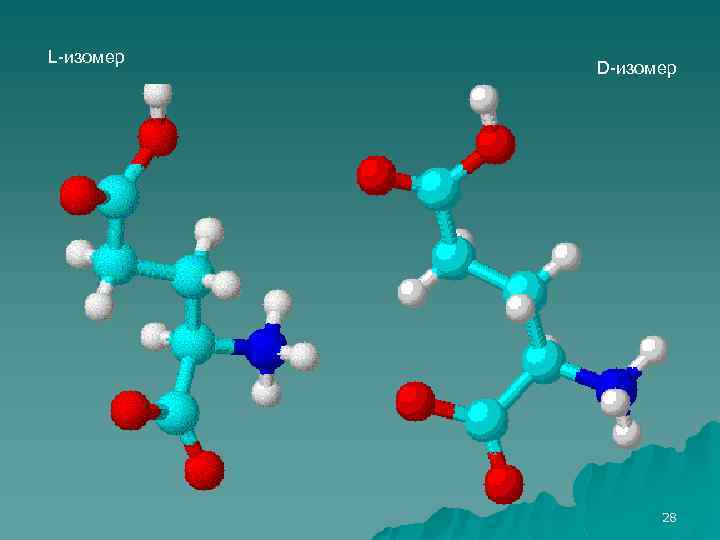
L-изомер D-изомер 28
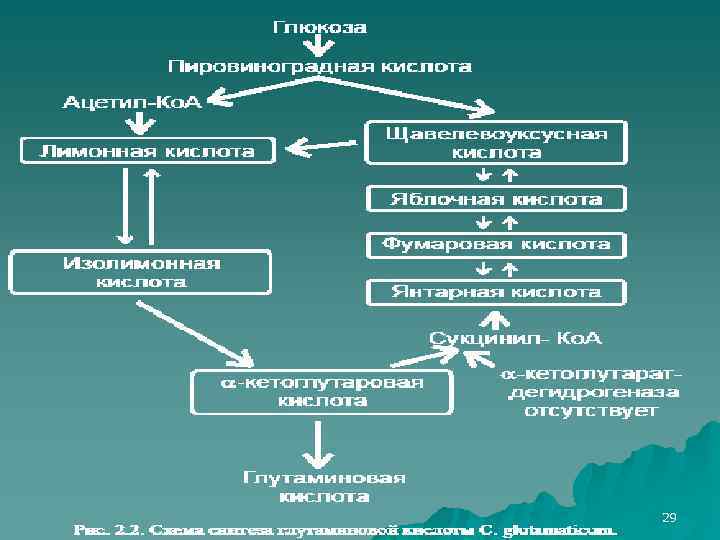
29

Получение кристаллической глутаминовой кислоты u u u u на первом этапе обработки в культуральную жидкости в нее добавляют негашеную известь или известковое молоко. После этого избыток ионов осаждают кислотой, осадок удаляют центрифугированием. Фильтрат после осветления активированным углем и сорбции на ионообменных смолах концентрируют вакуум-выпариванием при 40– 60°С. Осаждение кристаллов глутаминовой кислоты проводят в изоэлектрической точке (р. Н 3. 2 при 4– 15°С). Перекристаллизация - чистота продукта достигает 99. 6 %. Кристаллы кислоты отделяют от маточника 30 центрифугированием, промывают и

глутамат натрия влажные кристаллы растворяют в воде, нейтрализуют 50 % раствором едкого натра. u Полученный раствор фильтруют, u упаривают под вакуумом до содержания сухих веществ 60 % u направляют на перекристаллизацию. u кристаллы глутамата натрия выделяют из маточного раствора центрифугированием u высушивают током горячего воздуха. u 31

Глутамат натрия усиливает вкус многих пищевых продуктов, способ- ствует длительному сохранению вкусовых качеств консервированных продуктов (овощей, рыбы, мясных продуктов). 32

Мировое производство 400 000 т/г 33

Страны - лидеры u. Япония u. США 34

Получение лизина u Характеристика микроорганизмов продуцентов лизина. Влияние компонентов питательной среды и условий культивирования на процесс биосинтеза лизина. Технологическая схема получения лизина. Товарные формы препаратов лизина и их характеристика. 35

L-Лизин (α, εаминокапроновая кислота): СН 2 NH 2 – (СН 2)3 – NH 2 СН – СООН 36
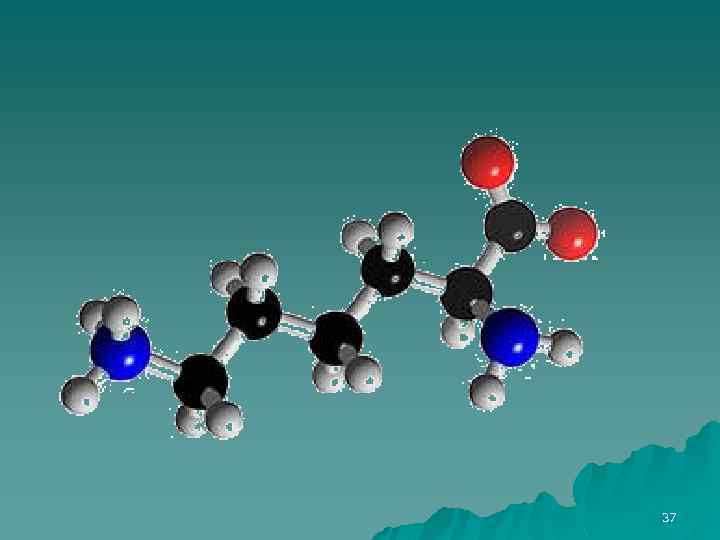
37

u Среди ведущих компаний на мировом рынке l-лизина лидируют японская Ajinomoto Co и американская Archer Daniels & Midlands (ADM), которые контролируют по 33% мирового производства каждая. Другими крупными игроками на рынке являются Degussa-Huels (Германия), BASF (Германия), Kyowa Hokko (Япония) и Cheil Jedang Corporation (Южная Корея). Большинство этих компаний не считают производство лизина своим приоритетным бизнесом. В основном, это диверсифицированные пищевые или химические концерны, в обороте которых на лизин приходится максимум 38

Производственные штаммыпродуценты лизина – это ауксотрофные штаммы глутаматпродуцирующих коринебактерий: u Corynebacterium u glutamaticum, Brevibacterium flavum 39

Применяют три типа ауксотрофных мутантов: ауксотрофы по гомосерину или треонину с подавленной гомосеринкиназой; u метионин- и треонинчувствительные штаммы с существенно сниженной активностью гомосериндегидрогеназы; u аналогорезистетные прототрофные продуценты лизина, устойчивые к треонину и аминоэтицилцистеину, с аспартаткиназой, нечувствительной к согласованному ин- гибированию лизином и треонином. u 40
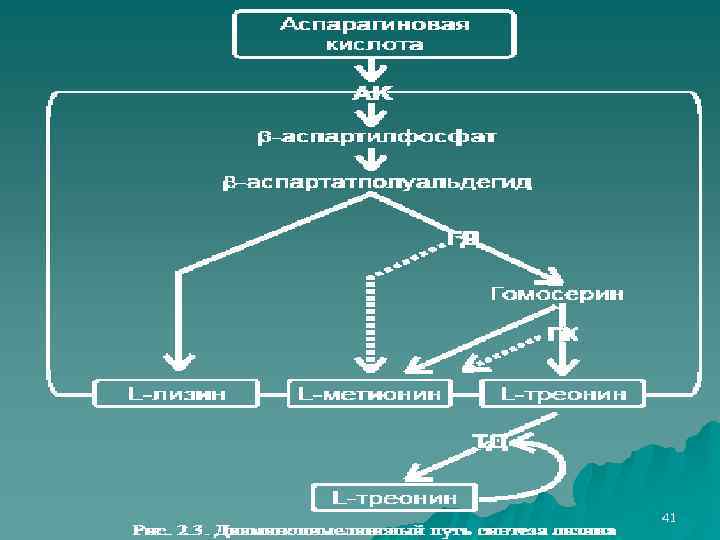
41

Получены штаммы, обеспечивающие 40% конверсию углеродного субстрата в аминокислоту и выходы лизина на сахарах до 40, уксусной кислоте – до 70 г/л. 42

Основные сырьевые компоненты для производства лизина: u меласса, кукурузный экстракт, соляная кислота, аммиачная вода, витамины, отруби, подсолнечный шрот, рыбная мука, мясокостная мука и рапс. 43

Помимо сахаров (7– 12 % по объему), сульфата ам- мония и фосфатов калия, в среду вносят кукурузный экстракт в качестве источника биологически активных веществ (1. 2– 1. 5 % по содержанию сухих веществ), а также мел и синтетический пеногаситель. 44

Среда должна содержать (в л): 200 мг метионина, 800 мг треонина, 15– 20 мкг биотина (при меньших концентрациях биотина синтезируется глутаминовая кислота, при 2. 5 мг – молочная кислота, как механизм обратного действия). 45

Соотношение углерода и азота в среде оптимально как 11: 1 (при его увеличении выход лизина падает, при уменьшении – накапливается аланин). 46

Культивирование осуществляется в строго стерильной глубинной аэроб- ной периодической культуре в аппаратах объемом 50 и 100 м 3 при коэффи- циенте заполнения 0. 75. Процесс длится 48– 72 ч при 29– 30°С, контроли- руемом р. Н 7. 0– 7. 5, непрерывном перемешивании и избыточном давлении 20– 30 к. Па. Уровень аэрации составляет 1 м 3 воздуха/м 3 среды в минуту. При ухудшении условий аэрации происходит образование молочной кислоты. 47

Конечная концентрация продукта достигает 40 г/л при остаточной концентрации сахаров около 0. 5– 1. 0 г/л. 48

Эффективный процесс получения лизина реализован на более доступном субстрате – уксусной кислоте. Экономический коэффициент по потреб- ляемому ацетату при этом составляет 27 %. Конечная концентрация лизина в среде достигает 40– 50 г/л. В последние годы получены мутантные штаммы B. flavum, обеспечивающие на ацетатной среде выход лизина до 73 г/л. 49

Токсичность данного субстрата делает необходимой дробную подачу ацетата; его концентрация в среде не должна превышать 2 %. Небольшие добавки сахара в среду (около 1 %) повышают выход лизина на 30– 50 %. 50

Практически весь производимый микробиологическим способом Lлизин используется в кормопроизводстве для повышения усвояемости и питательности кормов. Поэтому выпускается лизин, главным образом, в виде кормовых препаратов – жидкого концентрата лизина (ЖКЛ) и кормового концентрата лизина (ККЛ). 51

При производстве ЖКЛ культуральную жидкость, предварительно стабилизированную 25 % раствором гидросульфита натрия, подкисляют соляной кислотой до р. Н 4. 5– 5. 0. Образующийся при этом термостабильный монохлорид лизина упаривают в вакуумновыпарных аппаратах до 40 % содержания сухих веществ. Готовый препарат ЖКЛ не замерзает при температуре до – 18°C и сохраняет свои свойства в течение 3 месяцев. 52

ККЛ получают на основе ЖКЛ, высушивая жидкий концентрат в распылительных сушилках при температуре не более 90°С до остаточной влажности 4– 8 %. Сухой препарат лизина гигроскопичен и в процессе хранения подвержен порче. 53

Для устранения данного нежелательного явления в концентрат перед высушиванием вводят наполнители в виде костной муки, негашеной извести, пшеничных отрубей. Высушивание полученной пасты проводят конвективным способом на вальцево-ленточных сушилках. 54

Препарат по составу близок к жидкому концентрату лизина и содержит (в %): 7– 10 лизина, 15– 17 белка, до 14 других аминокислот, 10– 13 бетаина и 20 – 25 зольных веществ. Препарат сыпуч и негигроскопичен. Срок его хранения возрастает до 1 года. 55

Получение триптофана u Технология производства триптофана трансформацией антраниловой кислоты и индола. Микробный синтез триптофана. Микроорганизмы - продуценты триптофана. Основные закономерности биосинтеза триптофана. Принципиальная технологическая схема получения. 56
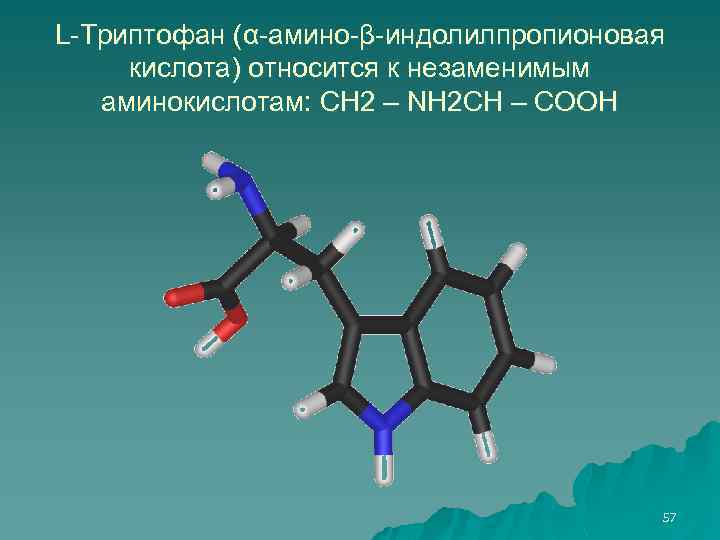
L-Триптофан (α-амино-β-индолилпропионовая кислота) относится к незаменимым аминокислотам: СН 2 – NН 2 СН – СООН 57

Отсутствие или дефицит триптофана в организме приводит к ряду тяжелых заболеваний (диабет, туберкулез, пеллагра). 58

Микробиологический синтез Lтриптофана осуществляют на основе мутантных штаммов дрожжей (Candida) и бактерий (E. coli, Bacillus subtilis), дефицитных по тирозину и фенилаланину. Промышленный синтез L- триптофана осуществляется на основе сахаров. 59

Исходная питательная среда для стерильного периодического выращивания дрожжей содержит (в %): сахароза 10, мочевина 0. 5, кукурузный экстракт 2. 0, а также хлорид кальция, калий фосфорнокислый и сульфат магния. Продолжительность периодической ферментации при 37°С не превышает 48 ч. 60

Триптофан выделяют из культуры по обычным схемам. Для получения очищенного кристаллического препарата работают с культуральной жидкостью. Для получения кормового концентрата используют и биомассу клеток. 61

62
aminokisloty_2.ppt