Применение и получение водорода.ppt
- Количество слайдов: 13

ТЕМА: Получение и применение водорода

Промышленные способы получения водорода 1. Разложение воды под действием электрического тока: 2 H 2 O = 2 H 2 + О 2 2. Разложением некоторых гидридов металлов при нагревании ТіH 2 Ті + H 2

Промышленные способы получения водорода 3. В основном получают из природного газа путем конверсии (превращения) под действием водяных паров и катализатора: СН 4 + 2 Н 2 О = 4 Н 2↑+СО 2 4. Разложение метана при нагревание: CH 4 =2 H 2↑ +C 5. Пропуская водяные пары над раскаленным углем: С + Н 20 = СО + Н 2.

Ответьте на вопросы: • Каким методом можно собрать водород? • Почему нужно собирать водород в перевернутый вверх дном сосуд? • Как можно обнаружить, что продуктом реакции является водород? • Почему нужно проверять водород на чистоту?
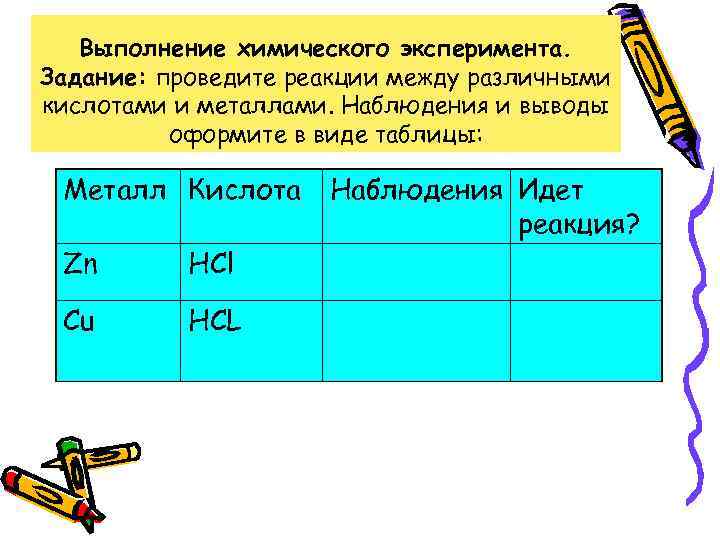
Выполнение химического эксперимента. Задание: проведите реакции между различными кислотами и металлами. Наблюдения и выводы оформите в виде таблицы: Металл Кислота Zn HCl Cu HCL Наблюдения Идет реакция?
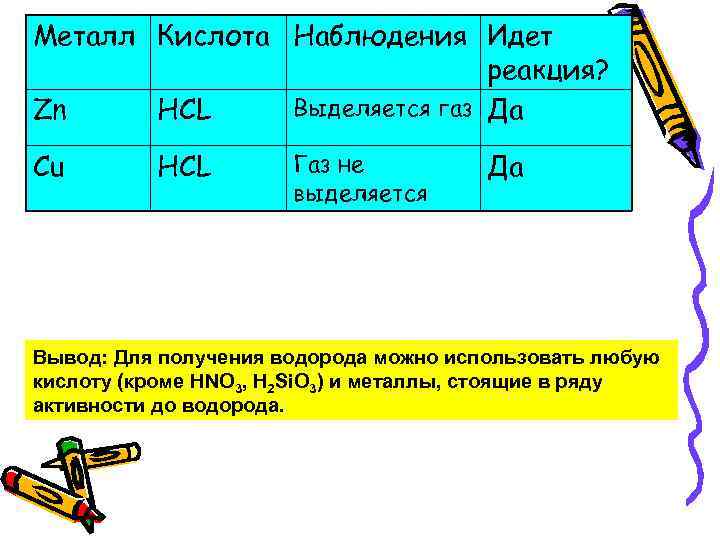
Металл Кислота Наблюдения Идет реакция? Выделяется газ Да Zn HCL Cu HCL Газ не выделяется Да Вывод: Для получения водорода можно использовать любую кислоту (кроме HNO 3, H 2 Si. O 3) и металлы, стоящие в ряду активности до водорода.

Лабораторный способ получения водорода II I Zn + 2 HCl = Zn Cl 2 + Н 2
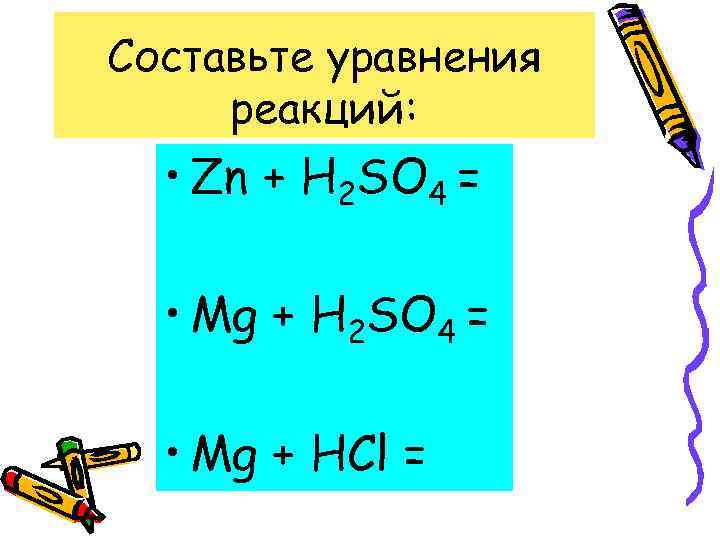
Составьте уравнения реакций: • Zn + H 2 SO 4 = • Mg + HCl =
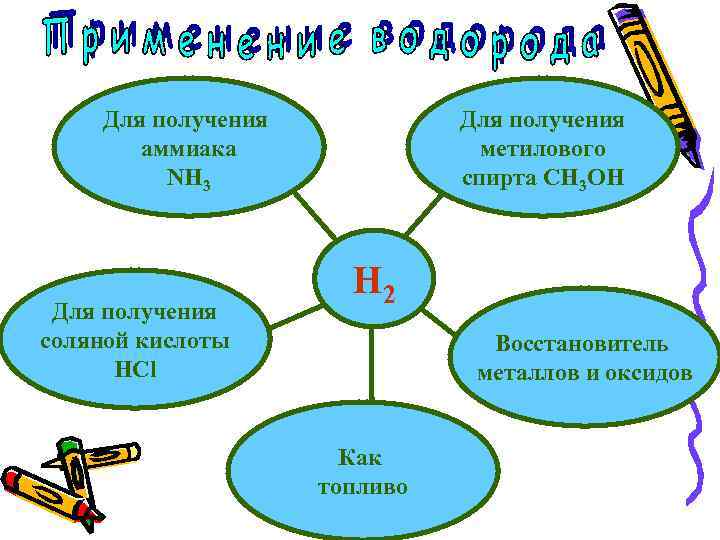
Для получения аммиака NH 3 Для получения соляной кислоты HCl Для получения метилового спирта СH 3 OH H 2 Восстановитель металлов и оксидов Как топливо
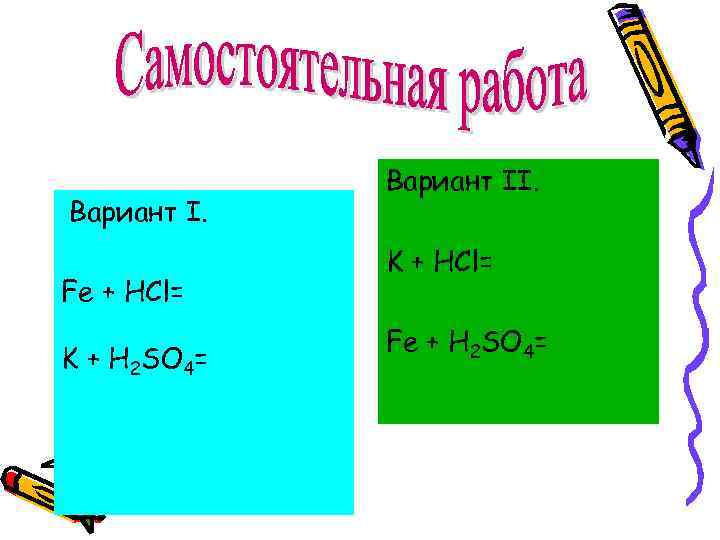
Вариант I. Fe + HCl= K + H 2 SO 4= Вариант II. K + HCl= Fe + H 2 SO 4=

Вариант I. Fe+2 HCl=Fe. Cl 2+H 2 2 K+H 2 SO 4=K 2 SO 4+H 2 Вариант II. 2 K+2 HCl=2 KCl + H 2 Fe+H 2 SO 4=Fe. SO 4+H 2

Выводы: • B промышленности для получения водорода используют доступное и дешевое сырье — природный газ, каменный уголь и воду. • В лаборатории водород можно получить при взаимодействии металлов с кислотами. • Водород — это перспективный источник энергии XXI в.

Домашнее задание: • Найти еще примеры применение водорода • Творческое задание «Почему водород называют топливом будущего? »
Применение и получение водорода.ppt