
Тема: Плазматична мембрана. Іонні канали.

План 1. Електричні властивості мембран. Поверхневий заряд мембрани. Потенціал спокою та потенціал дії. 2. Класифікація транспортних процесів: проста дифузія, полегшена дифузія, активний транспорт. 3. Характеристика транспортних процесів. Транспорт низькомолекулярних речовин. 4. Іонні канали: керовані напрогую К+ -канали, керовані напрогую Na+ -канали, структурна та функціональна характеристика Са 2+ -каналів. 5. Антибіотики як переносники іонів. Самостійна робота: 6. Водні канали.

Рекомендована література: Основна: 1. Болдырев А. А. , Кяйвяряйнен Е. И. , Илюха В. А. Биомембранология: Учебное пособие. Петрозаводск: Изд-во Кар. НЦ РАН, 2006: – 226 с. 2. Геннис Р. Биомембраны. Молекулярная структура и функции. – М. : Мир, 1997. – 624 с. 3. Курський М. Д. , Кучеренко С. М. Біомемембранологія. - К. : Вища школа, 1992. – 260 с. 4. Мушкамбаров Н. Н. , Кузнєцов С. Л. Молекулярная биология. -М. : ООО «Медицинское информационное агентство» , 2003. – 287 с. 5. Остапченко Л. І. , Михайлик І. В. Біологічні мембрани: методи дослідження структури та функцій: Навчальний посібник. – К. : Видавничо-поліграфічний центр «Київський університет» , 2006. – 215 с. 6. Фізіологія людини і тварин: підручник [для студ. вищ. навч. закл. ] / М. Ю. Клевець, В. В. Манько, М. О. Гільків, та ін. – Львів: ЛНУ імені Івана Франка, 2011. – 304 с. Додаткова: 7. Alberts B. , Johnson A. , Lewis J. , Raff M. , Roberts K. , Walter P. Molecular biology of the Cell, 5 th edition. Garland Science, 2008. 8. Аквапорины: строение, систематика и особенности регуляции. 2004 г. А. Ю. Шапигузов.

1. Електричні властивості мембран. Поверхневий заряд мембрани. Потенціал спокою та потенціал дії. Біоелектричні потенціали - це електричні потенціали, що генеруються живими системами і відіграють важливу роль у процесах життєдіяльності. У ході генерування біоелектричних потенціалів хімічна енергія переходить в електричну, оскільки значна частина енергії обміну речовин витрачається живими клітинами на створення нерівномірного розподілу іонів і генерування біоелектричних потенціалів. Біоелектричні потенціали забезпечують одну з основних властивостей живого - його збудливість, тобто здатність переходити в активний стан під дією зовнішніх чинників.
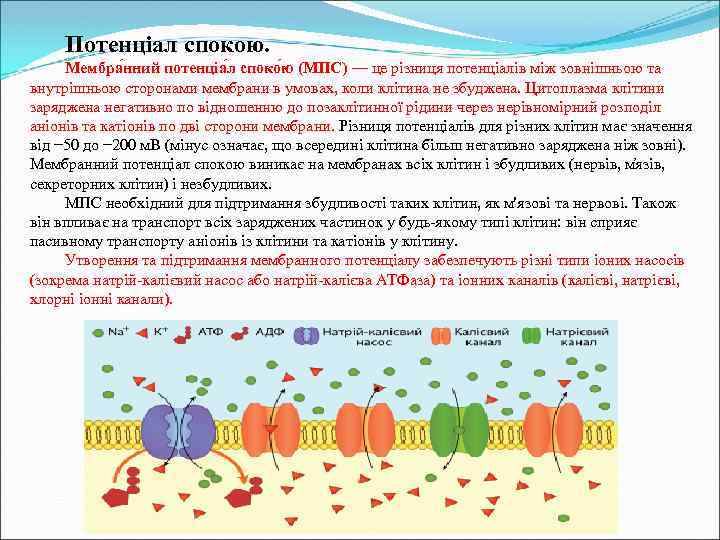
Потенціал спокою. Мембра нний потенціа л споко ю (МПС) — це різниця потенціалів між зовнішньою та внутрішньою сторонами мембрани в умовах, коли клітина не збуджена. Цитоплазма клітини заряджена негативно по відношенню до позаклітинної рідини через нерівномірний розподіл аніонів та катіонів по дві сторони мембрани. Різниця потенціалів для різних клітин має значення від − 50 до − 200 м. В (мінус означає, що всередині клітина більш негативно заряджена ніж зовні). Мембранний потенціал спокою виникає на мембранах всіх клітин і збудливих (нервів, м язів, секреторних клітин) і незбудливих. МПС необхідний для підтримання збудливості таких клітин, як м'язові та нервові. Також він впливає на транспорт всіх заряджених частинок у будь-якому типі клітин: він сприяє пасивному транспорту аніонів із клітини та катіонів у клітину. Утворення та підтримання мембранного потенціалу забезпечують різні типи іоних насосів (зокрема натрій-калієвий насос або натрій-калієва АТФаза) та іонних каналів (калієві, натрієві, хлорні іонні канали).

Формування потенціалу спокою Рис. Концентрації іонів K+, Na+, Cl- та органічних аніонів всередині та зовні клітини. До виникнення мембранного потенціалу спокою призводять два фактори: по-перше, концентрації різних іонів відрізняються зовні та в середині клітини, по-друге мембрана є напівпроникною: одні іони можуть через неї проникати, інші — ні. Обидва ці явища залежать від наявності у мембрані спеціальних білків: концентраційні градієнти створюють іонні насоси, а проникність мембрани для іонів забезпечують іонні канали. Найважливішу роль у формуванні мембранного потенціалу відіграють іони калію, натрію та хлору. Концентрації цих іонів відрізняюються по дві сторони мембрани. Для нейрона ссавців концентрація K+ становить 140 м. М всередині клітини і тільки 5 м. М ззовні, градієнт концентрації Na+ майже протилежний — 150 м. М зовні та 15 м. М всередині. Такий розподіл іонів підтримується натрій-калієвим насосом у плазматичній мембрані — білком що використовує енергію АТФ для закачування K+ у клітину і викачування Na+ із неї. Також існує концентраційний градієнт і для інших іонів, наприклад, хлорид аніону Cl-.
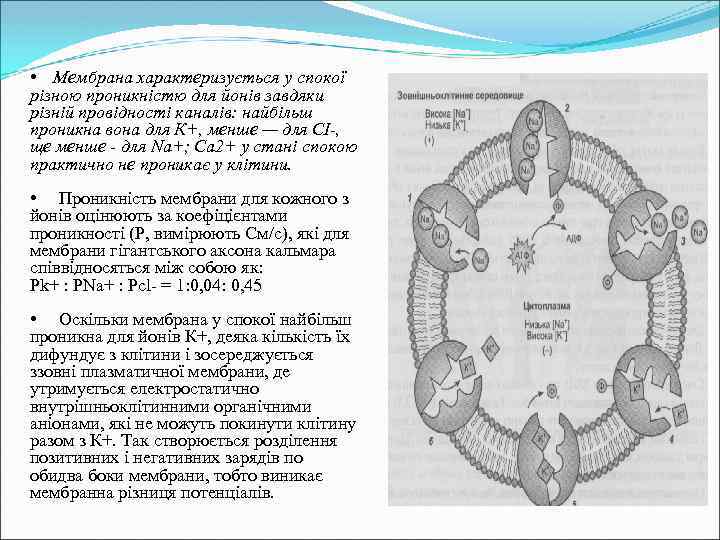
• Мембрана характеризується у спокої різною проникністю для йонів завдяки різній провідності каналів: найбільш проникна вона для К+, менше — для СІ-, ще менше - для Na+; Са 2+ у стані спокою практично не проникає у клітини. • Проникність мембрани для кожного з йонів оцінюють за коефіцієнтами проникності (Р, вимірюють См/с), які для мембрани гігантського аксона кальмара співвідносяться між собою як: Pk+ : PNa+ : Pcl- = 1: 0, 04: 0, 45 • Оскільки мембрана у спокої найбільш проникна для йонів К+, деяка кількість їх дифундує з клітини і зосереджується ззовні плазматичної мембрани, де утримується електростатично внутрішньоклітинними органічними аніонами, які не можуть покинути клітину разом з К+. Так створюється розділення позитивних і негативних зарядів по обидва боки мембрани, тобто виникає мембранна різниця потенціалів.
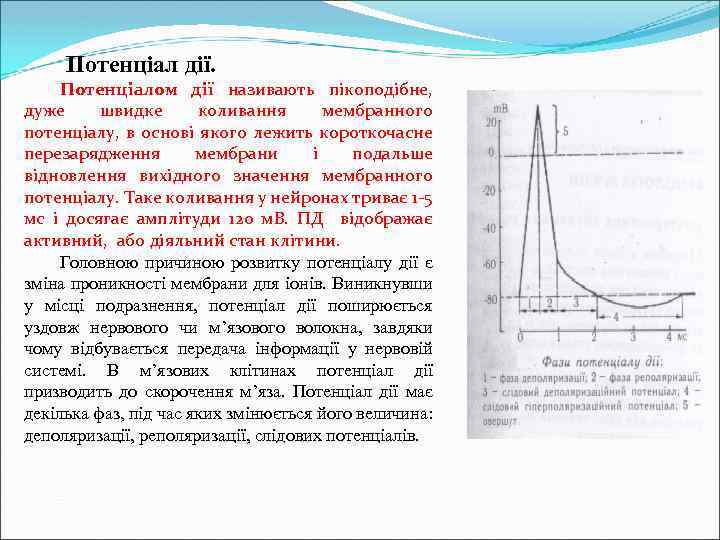
Потенціал дії. Потенціалом дії називають пікоподібне, дуже швидке коливання мембранного потенціалу, в основі якого лежить короткочасне перезарядження мембрани і подальше відновлення вихідного значення мембранного потенціалу. Таке коливання у нейронах триває 1 -5 мс і досягає амплітуди 120 м. В. ПД відображає активний, або діяльний стан клітини. Головною причиною розвитку потенціалу дії є зміна проникності мембрани для іонів. Виникнувши у місці подразнення, потенціал дії поширюється уздовж нервового чи м’язового волокна, завдяки чому відбувається передача інформації у нервовій системі. В м’язових клітинах потенціал дії призводить до скорочення м’яза. Потенціал дії має декілька фаз, під час яких змінюється його величина: деполяризації, реполяризації, слідових потенціалів.
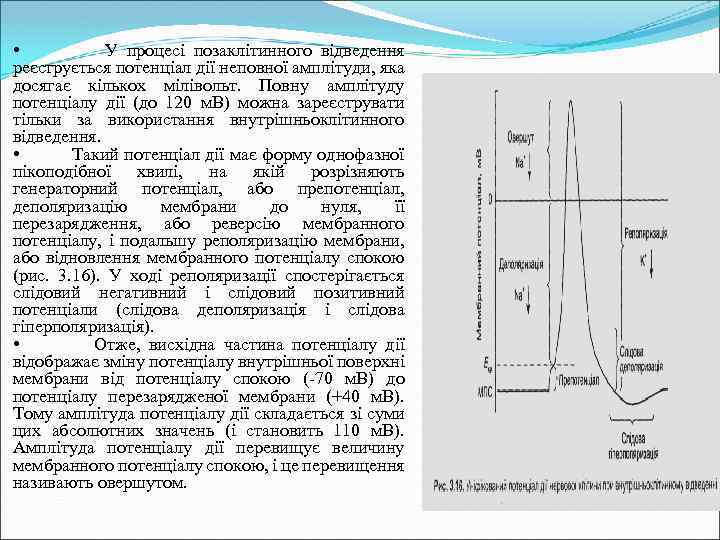
• У процесі позаклітинного відведення реєструється потенціал дії неповної амплітуди, яка досягає кількох мілівольт. Повну амплітуду потенціалу дії (до 120 м. В) можна зареєструвати тільки за використання внутрішньоклітинного відведення. • Такий потенціал дії має форму однофазної пікоподібної хвилі, на якій розрізняють генераторний потенціал, або препотенціал, деполяризацію мембрани до нуля, її перезарядження, або реверсію мембранного потенціалу, і подальшу реполяризацію мембрани, або відновлення мембранного потенціалу спокою (рис. 3. 16). У ході реполяризації спостерігається слідовий негативний і слідовий позитивний потенціали (слідова деполяризація і слідова гіперполяризація). • Отже, висхідна частина потенціалу дії відображає зміну потенціалу внутрішньої поверхні мембрани від потенціалу спокою (-70 м. В) до потенціалу перезарядженої мембрани (+40 м. В). Тому амплітуда потенціалу дії складається зі суми цих абсолютних значень (і становить 110 м. В). Амплітуда потенціалу дії перевищує величину мембранного потенціалу спокою, і це перевищення називають овершутом.

2. Класифікація транспортних процесів: проста дифузія, полегшена дифузія, активний транспорт. МЕМБРÁННИЙ ТРÁНСПОРТ — перенесення різноманітних речовин через плазматичну мембрану. Механізм транспорту речовин до клітини та з неї залежить від розмірів частинок, що транспортуються. Малі молекули та іони проходять крізь мембрани шляхом пасивного чи активного транспорту. Перенесення макромолекул та великих частинок здійснюється за рахунок ендоцитозу та екзоцитозу. Пасивний транспорт відбувається мимовільно без затрати енергії шляхом дифузії, осмосу та полегшеної дифузії. Дифузія — це транспорт молекул та іонів через мембрану з ділянки з високою концентрацією до ділянки з низькою концентрацією, тобто речовини надходять за градієнтом концентрації. Дифузія може бути простою та полегшеною. Якщо речовини добре розчинні в ліпідах, то вони проникають до клітини шляхом простої дифузії. Напр. оксиген, потрібний клітині при диханні, та вуглекислий газ у розчині швидко дифундують крізь мембрани. Таким способом проникають до клітини також деякі фармацевтичні препарати, які є ліпідорозчинними. Вода також здатна проходити крізь мембранні пори, що утворені білками, і переносити молекули та іони речовин, які в ній розчинені. Речовини, які не є розчинними у ліпідах, транспортуються крізь іоні канали, утворенні в мембрані білками, чи за допомогою білків-переносників – це полегшена дифузія. Активний транспорт речовин крізь мембрану здійснюється проти градієнта їхньої концентрації із затратою енергії АТФ та за участю спеціальних мембранних білків — транспортних АТФаз, які також називаються іонними насосами. Найбільш поширеними в клітині тварин є Н+-АТФаза, Na+, K+-АТФаза і Са 2+-АТФаза, що являють собою цілі мембранні комплекси із складною структурою. Функціональне значення біологічних насосів полягає у підтримці всередині клітини постійного іонного складу.

Існує кілька підходів щодо класифікації мембранних транспортних процесів. Згідно з традиційною класифікацією, розрізняють такі види мембранного транспорту: • пасивний (за градієнтом концентрації, без витрат енергії); • активний (проти градієнта концентрації з енергетичними витратами); • транспорт, пов'язаний зі змінами конфігурації мембрани (екзоцитоз, ендоцитоз). За типом субстрату виділяють: • йонний; • водний; • низькомолекулярний; • транспорт макромолекул та їх комплексів.

За механізмом транспорту : • безпосередній (без носія) транспорт речовин здійснюється через пори мембран або через їх ліпідну фазу й завжди відбувається за градієнтом концентрації (проста дифузія); • опосередкований (з носієм) транспорт здійснюється з допомогою специфічних транспортних систем: • полегшена дифузія – дифузія з допомогою переносника, що дозволяє інтенсифікувати транспортні процеси; • активний транспорт – транспорт проти градієнта концентрації. За величиною субстрату: • транспорт малих молекул (дифузія, осмос, активний транспорт); • транспорт великих молекул (ендоцитоз, екзоцитоз).

3. Характеристика транспортних процесів. Для всіх заряджених молекул (іонів), незалежно від їх розмірів, ліпідний бішар є практично непроникним: високий ступінь гідратації таких молекул попереджає їх проходження через вуглеводневу ділянку бішару.

Транспортні білки - це специфічні трансмембранні білки, призначені для перенесення через мембрану речовин, для яких біліпідний шар є непроникним. Виділяють такі види транспортних білків: 1. Переносники (транспортери, транслокази). Під час зв'язування із субстратом змінюють свою конформацію, у результаті чого речовина переноситься на інший бік мембрани. Можуть забезпечувати полегшену дифузію та активний транспорт. Одні транспортери переносять розчинену речовину з одного боку мембрани на другий (уніпорт). Інщі функціонують як котранспортні системи, в яких перенесення однієї речовини залежить від одночасного або послідовного перенесення іншої речовини в тому ж (симпорт) або в протилежному (антипорт) напрямку. 2. Канали (тунельні білки). Формують у бішарі заповнені водою пори, під час відкривання яких відбувається просування певних іонів.
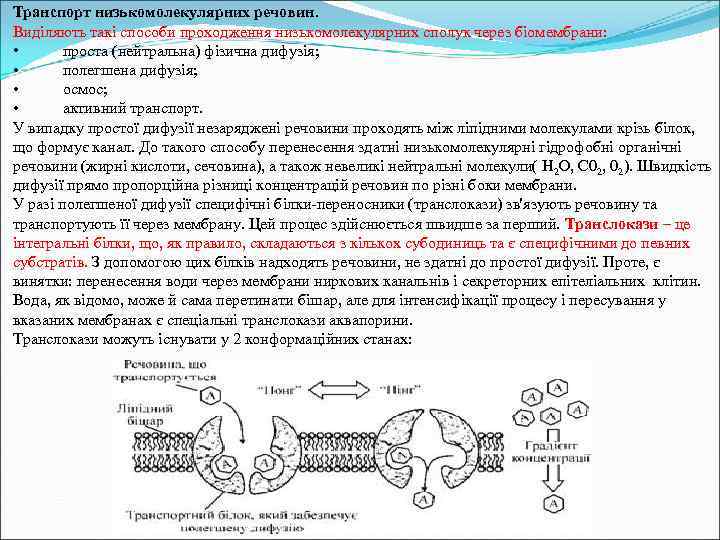
Транспорт низькомолекулярних речовин. Виділяють такі способи проходження низькомолекулярних сполук через біомембрани: • проста (нейтральна) фізична дифузія; • полегшена дифузія; • осмос; • активний транспорт. У випадку простої дифузії незаряджені речовини проходять між ліпідними молекулами крізь білок, що формує канал. До такого способу перенесення здатні низькомолекулярні гідрофобні органічні речовини (жирні кислоти, сечовина), а також невеликі нейтральні молекули( Н 2 О, С 02, 02). Швидкість дифузії прямо пропорційна різниці концентрацій речовин по різні боки мембрани. У разі полегшеної дифузії специфічні білки-переносники (транслокази) зв'язують речовину та транспортують її через мембрану. Цей процес здійснюється швидше за перший. Транслокази – це інтегральні білки, що, як правило, складаються з кількох субодиниць та є специфічними до певних субстратів. З допомогою цих білків надходять речовини, не здатні до простої дифузії. Проте, є винятки: перенесення води через мембрани ниркових канальнів і секреторних епітеліальних клітин. Вода, як відомо, може й сама перетинати бішар, але для інтенсифікації процесу і пересування у вказаних мембранах є спеціальні транслокази аквапорини. Транслокази можуть існувати у 2 конформаційних станах:

4. Іонні канали: керовані напрогую Na+ -канали, керовані напрогую К+ -канали, структурна та функціональна характеристика Са 2+ -каналів. • Потенціалкеровані іонні канали реагують на зміни напруженості електричного поля в мембрані конформаційними змінами білків, що утворюють іонний канал. • Концепція їх існування зародилась ще на початку 50 – х років минулого століття з розшифровкою іонних механізмів генерації потенціалу дії. Це значною мірою зумовило той факт, що історично класичні потенціалзалежні іонні канали названо по типу основного іона який вони переносять – Na+, K+, Ca 2+. • Головною особливістю потенціалзалежних натрієвих, калієвих та кальцієвих каналів є те, що їх функціональний стан визначається величиною мембранного потенціалу.
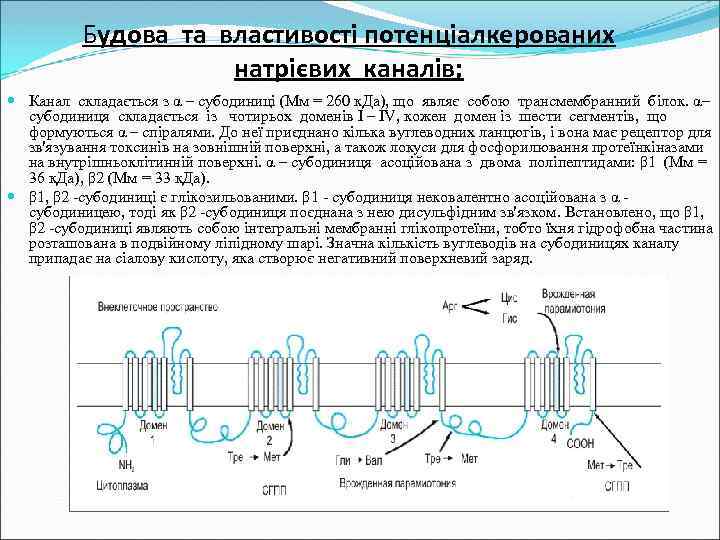
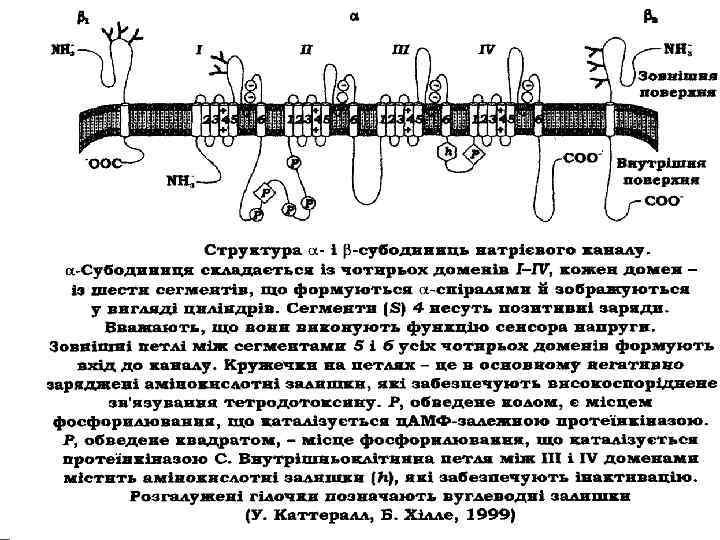
Будова та властивості потенціалкерованих натрієвих каналів; Канал складається з α – субодиниці (Мм = 260 к. Да), що являє собою трансмембранний білок. α– субодиниця складається із чотирьох доменів I – IV, кожен домен із шести сегментів, що формуються α – спіралями. До неї приєднано кілька вуглеводних ланцюгів, і вона має рецептор для зв'язування токсинів на зовнішній поверхні, а також локуси для фосфорилювання протеїнкіназами на внутрішньоклітинній поверхні. α – субодиниця асоційована з двома поліпептидами: β 1 (Мм = 36 к. Да), β 2 (Мм = 33 к. Да). β 1, β 2 -субодиниці є глікозильованими. β 1 - субодиниця нековалентно асоційована з α субодиницею, тоді як β 2 -субодиниця поєднана з нею дисульфідним зв'язком. Встановлено, що β 1, β 2 -субодиниці являють собою інтегральні мембранні глікопротеїни, тобто їхня гідрофобна частина розташована в подвійному ліпідному шарі. Значна кількість вуглеводів на субодиницях каналу припадає на сіалову кислоту, яка створює негативний поверхневий заряд.

Модулятори натрієвих каналів: Існують два класи токсинів, які або спонтанно відкривають натрієві канали, або запобігають їх нормальному закриттю після того, як їх було відкрито. Це розчинні в ліпідах стероїди, такі як рослинні алкалоїди: вератридин, аконітин, батрахотоксин та пептидні токсини отрути скорпіонів і анемон, які діють на рецептор на зовнішній поверхні мембрани. Серед блокаторів натрієвих каналів особливе місце посідають тетродотоксин сакситоксин, які зв'язуються з рецепторним локусом, розташованим у зовнішньому вході натрієвого каналу, і блокують провідність унаслідок оклюзії пори. Лідокаїн і прокаїн (новокаїн) є широко відомими місцевими анестетиками, що застосовують у клініці. Потенціалзалежними блокаторами натрієвих каналів є також низка фармакологічних препаратів, які застосовують у клініці як антиаритміки й протисудомні засоби.

2. Калієві канали загальна характеристика: К+ - канали - це велика група макромолекул, що формують пори, які переважно є проникними для К+. Вони відіграють значну роль у різних функціях клітини. К+ - канали беруть участь у регуляції мембранного потенціалу і, таким чином, модулюють електричну збудливість клітин й електрохімічну рушійну силу для різноманітних транспортних механізмів. Роль потенціалкерованих К+ - каналів є важливою у формуванні змін мембранного потенціалу під час потенціалу дії в усіх збудливих клітинах. Вони функціонують у клітинних механізмах навчання та пам'яті. У регуляції К+ - каналів беруть участь ковалентна модифікація, зумовлена фосфорилюванням, а також нековалентні взаємодії з іонами, нуклеотидами, киснем, ліпідами, такими зарядженими сполуками, як спермін, який належить до поліамінів. За останні 10 років було клоновано десятки різновидів К+ - каналів.
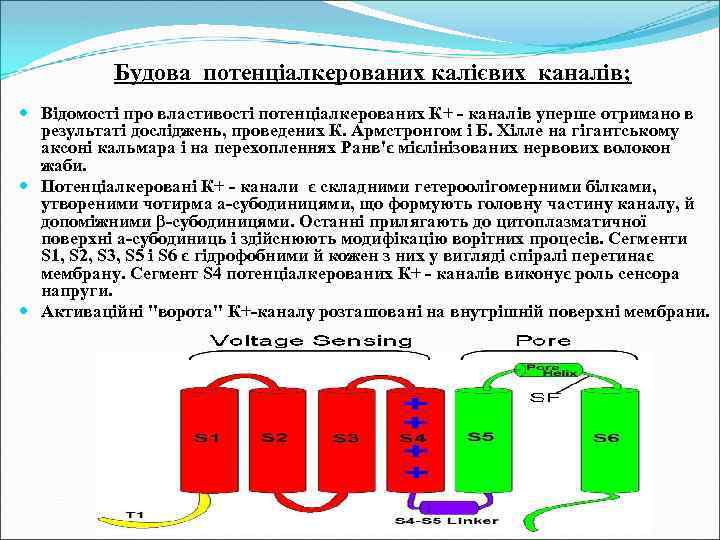
Будова потенціалкерованих калієвих каналів; Відомості про властивості потенціалкерованих К+ - каналів уперше отримано в результаті досліджень, проведених К. Армстронгом і Б. Хілле на гігантському аксоні кальмара і на перехопленнях Ранв'є мієлінізованих нервових волокон жаби. Потенціалкеровані К+ - канали є складними гетероолігомерними білками, утвореними чотирма а-субодиницями, що формують головну частину каналу, й допоміжними β-субодиницями. Останні прилягають до цитоплазматичної поверхні а-субодиниць і здійснюють модифікацію ворітних процесів. Сегменти S 1, S 2, S 3, S 5 і S 6 є гідрофобними й кожен з них у вигляді спіралі перетинає мембрану. Сегмент S 4 потенціалкерованих К+ - каналів виконує роль сенсора напруги. Активаційні "ворота" К+-каналу розташовані на внутрішній поверхні мембрани.
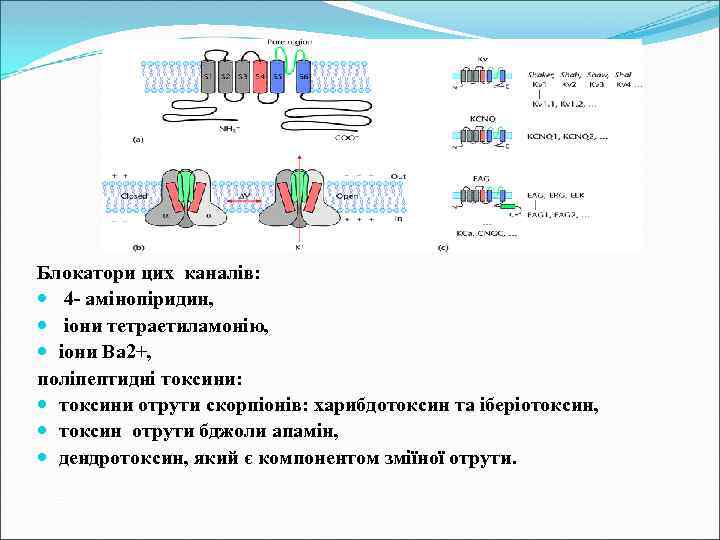
Блокатори цих каналів: 4 - амінопіридин, іони тетраетиламонію, іони Ва 2+, поліпептидні токсини: токсини отрути скорпіонів: харибдотоксин та іберіотоксин, токсин отрути бджоли апамін, дендротоксин, який є компонентом зміїної отрути.
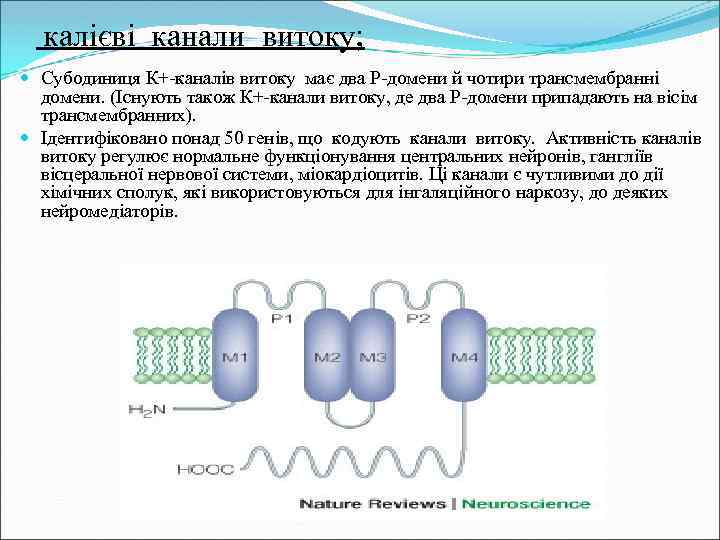
калієві канали витоку; Субодиниця К+-каналів витоку має два Р-домени й чотири трансмембранні домени. (Існують також К+-канали витоку, де два Р-домени припадають на вісім трансмембранних). Ідентифіковано понад 50 генів, що кодують канали витоку. Активність каналів витоку регулює нормальне функціонування центральних нейронів, гангліїв вісцеральної нервової системи, міокардіоцитів. Ці канали є чутливими до дії хімічних сполук, які використовуються для інгаляційного наркозу, до деяких нейромедіаторів.
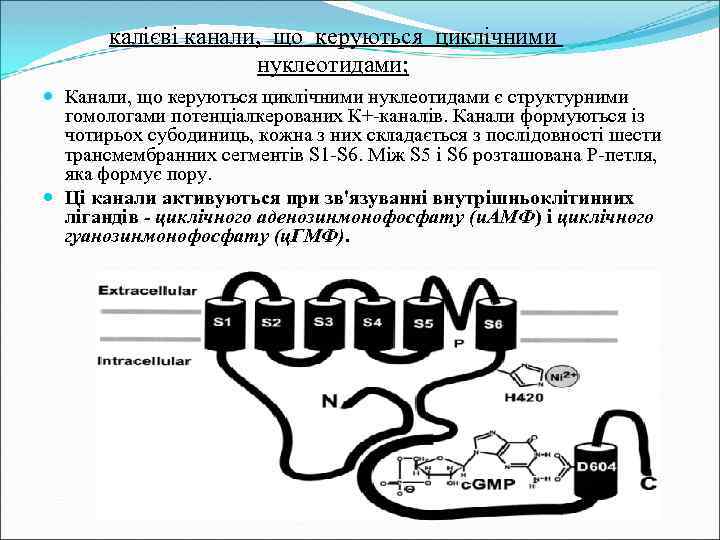
калієві канали, що керуються циклічними нуклеотидами; Канали, що керуються циклічними нуклеотидами є структурними гомологами потенціалкерованих К+-каналів. Канали формуються із чотирьох субодиниць, кожна з них складається з послідовності шести трансмембранних сегментів S 1 -S 6. Між S 5 і S 6 розташована Р-петля, яка формує пору. Ці канали активуються при зв'язуванні внутрішньоклітинних лігандів - циклічного аденозинмонофосфату (и. АМФ) і циклічного гуанозинмонофосфату (ц. ГМФ).
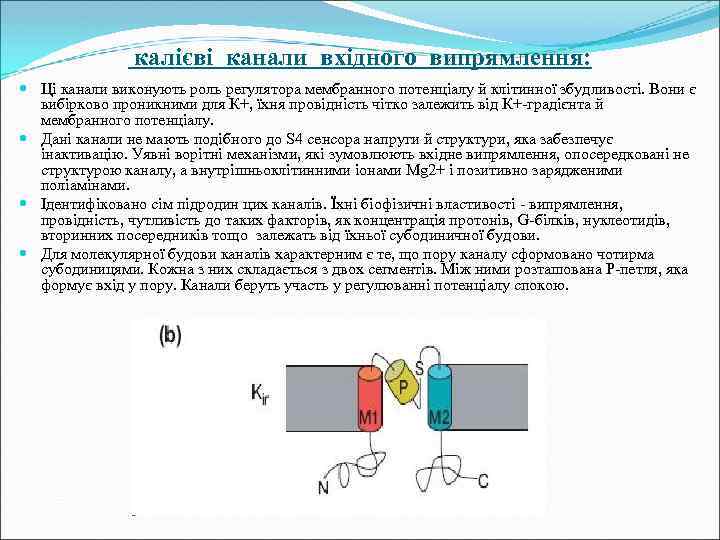
калієві канали вхідного випрямлення: Ці канали виконують роль регулятора мембранного потенціалу й клітинної збудливості. Вони є вибірково проникними для К+, їхня провідність чітко залежить від К+-градієнта й мембранного потенціалу. Дані канали не мають подібного до S 4 сенсора напруги й структури, яка забезпечує інактивацію. Уявні ворітні механізми, які зумовлюють вхідне випрямлення, опосередковані не структурою каналу, а внутрішньоклітинними іонами Мg 2+ і позитивно зарядженими поліамінами. Ідентифіковано сім підродин цих каналів. Їхні біофізичні властивості - випрямлення, провідність, чутливість до таких факторів, як концентрація протонів, G-білків, нуклеотидів, вторинних посередників тощо залежать від їхньої субодиничної будови. Для молекулярної будови каналів характерним є те, що пору каналу сформовано чотирма субодиницями. Кожна з них складається з двох сегментів. Між ними розташована Р-петля, яка формує вхід у пору. Канали беруть участь у регулюванні потенціалу спокою.

Потенціалкеровані кальцієві канали. Надходження іонів кальцію у клітину відбувається в основному через Са 2+ - канали. Як незначні, так і істотні зміни внутрішньоклітинної концентрації іонів кальцію впливають на велику кількість клітинних процесів. Кальцієвий сигнал викликає скорочення м’язів та секрецію. Іони кальцію беруть участь також у більш тривалих процесах – мітозі та апоптпозі. Зміна концентрації Са 2+ в мітохондріях є важливою в регуляції таких функцій, як дихання, розвиток апоптозу. Кальцій відіграє значну роль в регулювання функції комплексу Гольджі. Цитоплазматична концентрація Са 2+ приблизно у 10000 разів є меншою за позаклітинну. Високі концентрації кальцію притаманні внутрішньоклітинним органелам (депо), таким як сарко- і ендоплазматичний ретикулум. Транзиторне збільшення проникності для Са 2+ плазматичної мембрани, або мембрани внутрішньоклітинних кальцієвих депо, викликає значне локальне підвищення його концентрації в цитозолі. Вхід Са 2+ в електрично збудливі клітини відбувається під час активації потенціал керованих кільцієвик каналів зумовлених потенціалом дії. Вхід кальцію забезпечує подальше Са 2+ - індуковане вивільнення кільцію з депо внаслідок активації ріанодинових рецепторів. Загалом, розрізняють 2 класи кальцієвих каналів: потенціалкеровані та рецепторкеровані. Рецепторкеровані Са 2+ - канали пов’язані з мембранними рецепторами, що взаємодіють в основному з нейромедіаторами і гормонами. Потенціалкеровані Са 2+ - канали виявлено у ПМ практично всіх елекрично збудливих клітин - клітин серцевого м’яза, клітин гладеньких м’язів, ендокринних клітин, м’язових волокон членистоногих, нервових клітин, клітин електрорецепторів ската.

класифікація потенціалкерованих кальцієвих каналів С. Хагівара зі співробітниками в 1975 р. зареєстрували високопорогові й низькопорогові кальцієві струми на яйцеклітинах морської зірки. На підставі фармакологічних і біофізичних характеристик розрізняють L-, N-, P-, Q-, R-, T-типи Са 2+- каналів. До низькопорогових належить лише T-тип каналів. До високопорогових L-, N-, P-, Q-, R-типи. Низькопорогові Са 2+-канали виділяють як досить різноманітну підродину каналів. Її члени відрізняються фармакологічними властивостями, іонною вибірковістю, кінетикою активації та інактивації. L-, N-, P-, Q-, R-типи каналів активуються значно швидше, й між ними існує помітна різниця в розмірах і швидкості інактивації. Блокатори високопорогових каналів: L-тип блокує зміїна отрута кальциклюдин, кальцисептин, таїтоксин; N, P, Q-типи блокуються токсином молюска Conus Geographus; R-тип блокується пептидом отрути тарантула SNX-482; Низькопорогові Т канал блокуються пептидом отрути скорпіона куртоксином. и Неспецифічними блокаторами різних типів кальцієвих каналів є іони Ni 2+, Cd 2+, Mn 2+, верапаміл.
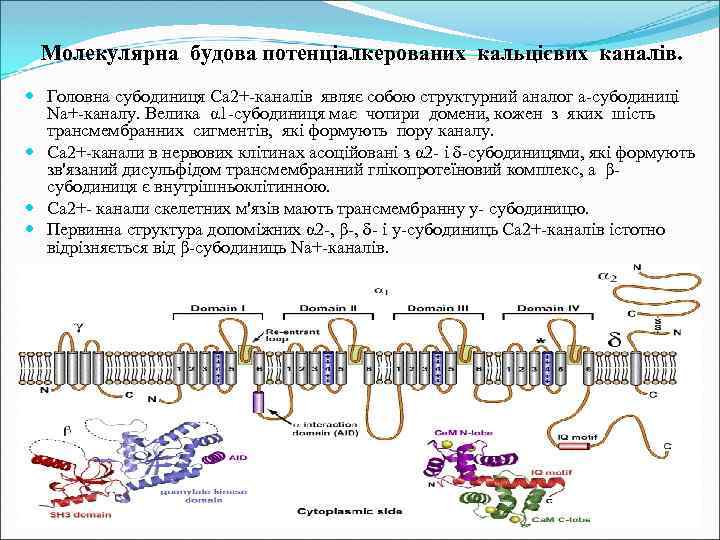
Молекулярна будова потенціалкерованих кальцієвих каналів. Головна субодиниця Са 2+-каналів являє собою структурний аналог а-субодиниці Nа+-каналу. Велика α 1 -субодиниця має чотири домени, кожен з яких шість трансмембранних сигментів, які формують пору каналу. Са 2+-канали в нервових клітинах асоційовані з α 2 - і δ-субодиницями, які формують зв'язаний дисульфідом трансмембранний глікопротеїновий комплекс, а βсубодиниця є внутрішньоклітинною. Са 2+- канали скелетних м'язів мають трансмембранну у- субодиницю. Первинна структура допоміжних α 2 -, β-, δ- і у-субодиниць Са 2+-каналів істотно відрізняється від β-субодиниць Nа+-каналів.

5. Антибіотики як переносники іонів Антибіотики-іонофори останнім часом міцно увійшли в арсенал біохімії і біофізики як ефективні інструменти для дослідження процесів, пов'язаних з транспортом іонів через біологічні мембрани. Іонофори мають різноманітну будова і принцип дії. Одні з них є самими справжніми переносниками: чіпляючи до себе іон, вони буквально протягують його через мембрану. Інші іонофори утворюють в біомембранами проникні для іонів пори, або канали. Цікаво, що валіноміцин, що відноситься до іонофорів-переносників, має макроциклічну структуру, іншими словами кільце. Інший антибіотик - граміцидин А (що є продуктом життєдіяльності цвілевих грибків), що відноситься до «канальним» іонофоров, має лінійну структуру. На рисунку зображена схема будови граміцидинового каналу в мембрані та валіноміцин.

Валіноміцин утворює жиророзчинний комплекс з іонами К+, який легко проходить через внутрішню мембрану мітохондрій, тоді як за відсутності валіноміцину іони К+ проникають крізь неї з великими труднощами. Антибіотикиіонофори вирівнюють іонні градієнти на будь-якій, а не лише на мітохондріальній мембрані. Іонофор граміцидин є антибіотиком з бактеріостатичною й бактерицидною дією. Він полегшує проникнення крізь мембрану К+ і Nа+, причому діє на клітини як мікроорганізмів, так і хворого, тому його необхідно застосовувати тільки у вигляді мазей і паст для лікування гнійних ран.
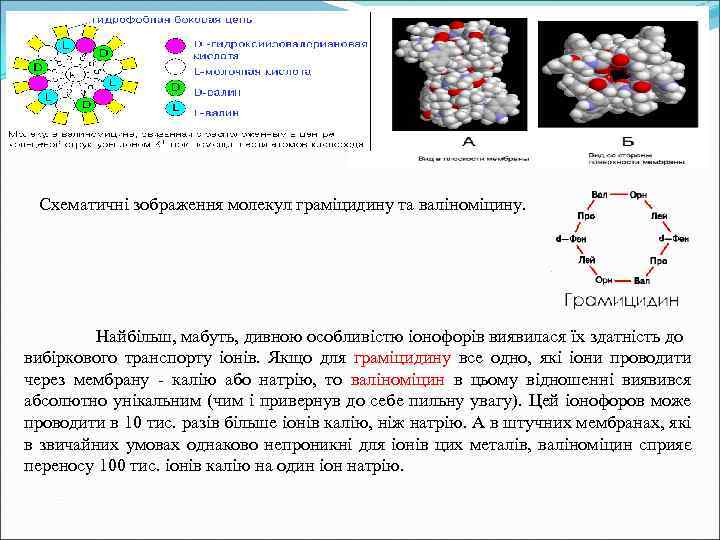
Схематичні зображення молекул граміцидину та валіноміцину. Найбільш, мабуть, дивною особливістю іонофорів виявилася їх здатність до вибіркового транспорту іонів. Якщо для граміцидину все одно, які іони проводити через мембрану - калію або натрію, то валіноміцин в цьому відношенні виявився абсолютно унікальним (чим і привернув до себе пильну увагу). Цей іонофоров може проводити в 10 тис. разів більше іонів калію, ніж натрію. А в штучних мембранах, які в звичайних умовах однаково непроникні для іонів цих металів, валіноміцин сприяє переносу 100 тис. іонів калію на один іон натрію.

ВИСНОВКИ Мембрана клітини в стані спокою поляризована: зовнішня поверхня заряджена електропозитивно, а внутрішня – електронегативно. 2 види транспорту – пасивний та активний. Пасивний транспорт не пов’язаний прямо з витратою хімічної енергії; він здійснюється в результаті дифузії речовин у бік меншого електрохімічного потенціалу. Активний транспорт відбувається при витраті хімічної енергії АТФ. Ознайомилися з транспортом низькомолекулярних речовин. Розглянули такі іонні канали, як: керовані напрогую К+ -канали, керовані напрогую Na+ -канали, структурна та функціональна характеристика Са 2+ каналів. Антибіотики як переносники іонів, на прикладі валіноміцину, який утворює жиророзчинний комплекс з іонами К+ та граміцидину він полегшує проникнення крізь мембрану К+ і Nа+.