органические реакции.ppt
- Количество слайдов: 43

Тема: «Основные принципы реакционной способности органических соединений»

РЕАКЦИОННАЯ СПОСОБНОСТЬ – способность вещества вступать в ту или иную химическую реакцию и реагировать с меньшей или большей скоростью. ¡ ! Чем меньше энергия активации реакции, тем выше ее скорость. Органические реакции, как правило, протекают в несколько стадий, каждая из которых характеризуется определенной скоростью. Скорость реакции в целом определяется скоростью самой медленной.

Реакционную способность соединения всегда должна рассматриваться только по отношению к партнеру. ¡ В этой связи, принято выделять 2 -а типа реагирующих частиц: СУБСТРАТ — вещество, в котором происходит разрыв старых и образование новых связей с участием атома углерода, и атакующий РЕАГЕНТ — вещество, под действием которого происходят изменения в субстрате.

¡ В ходе химической реакции обычно затрагивается не вся молекула, а только ее реакционный центр. РЕАКЦИОННЫЙ ЦЕНТР– это атом или группа атомов, участвующих в разрыве или образовании связей.

¡ Появление реакционных центров обусловлено неравномерным распределением электронной плотности в молекуле.

ТИПЫ РЕАГЕНТОВ ¡ ¡ Органические реагенты подразделяют на: радикальные, электрофильные, нуклеофильные. Радикалы (R) или радикальные реагенты— незаряженные частицы, имеющие неспаренный электрон, вследствие чего являющиеся чрезвычайно реакционноспособными, например:
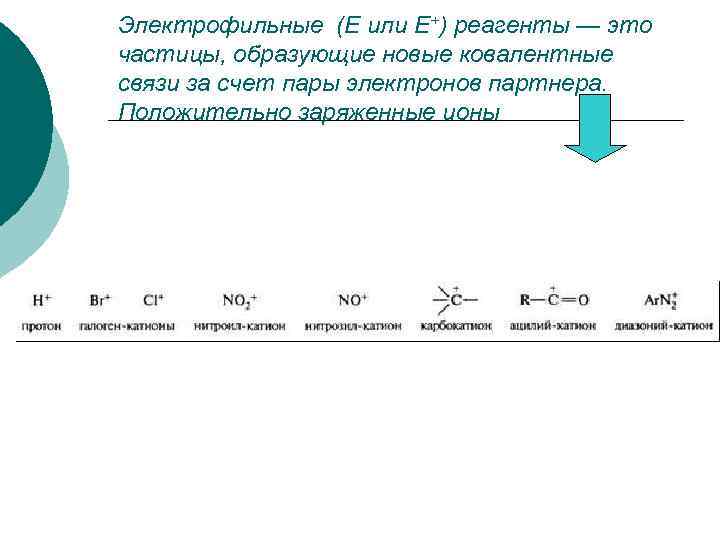
Электрофильные (Е или Е+) реагенты — это частицы, образующие новые ковалентные связи за счет пары электронов партнера. Положительно заряженные ионы

Нейтральные молекулы, имеющие электронодефицитный центр:

¡ Нуклеофильные реагенты (Nu или Nu–) — это частицы, образующие новые ковалентные связи со своим партнером, предоставляя для этого пару электронов. Отрицательно заряженные ион:
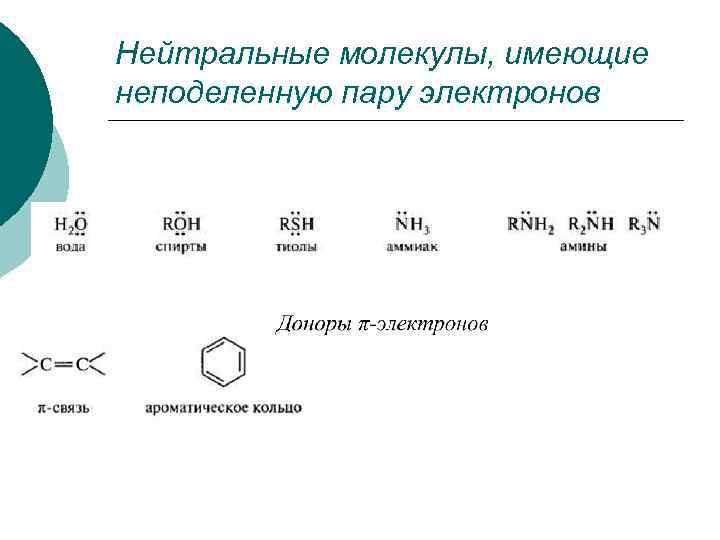
Нейтральные молекулы, имеющие неподеленную пару электронов

ТИПЫ РЕАКЦИИ В основе классификации реакций в органической химии лежат различные признаки: ¡ 1. Характер изменения связей в субстрате и реагенте. По этому признаку реакции подразделяют на: радикальные, ионные и согласованные (синхронные). ¡

1. 1. Радикальные реакции протекают преимущественно в случае неполярных или малополярных связей и сопровождаются расщеплением по обменному механизму (гомолизом):

1. 2. Ионные или гетеролитические реакции – разрыв ковалентной связи происходит неравномерно (т. е. по донорно-акцепторному механизму) и электронная пара остается у более электроотрицательного элемента, при этом образуются заряженные частицы

¡ Частицы, обладающие избытком электронной плотности (Nu– или δ– ), частицы с недостатком электронной плотности (Е+ или δ+):
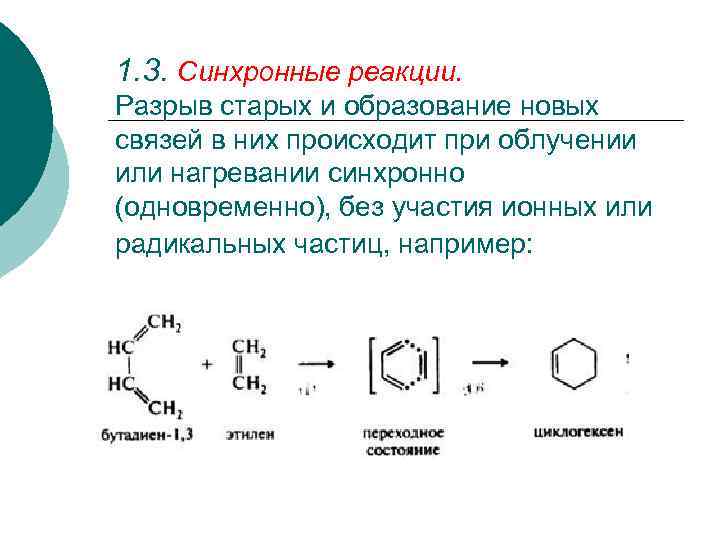
1. 3. Синхронные реакции. Разрыв старых и образование новых связей в них происходит при облучении или нагревании синхронно (одновременно), без участия ионных или радикальных частиц, например:

II. Направление реакции: ¡ По направлению процесса органические реакции делят на: замещения (символ S), присоединения (А), отщепления (элиминирования Е) и перегруппирровки.

Каждая из органических реакций замещения (S), присоединения (А) или элиминирования (Е) может быть: ¡ электрофильной (Е), нуклеофильной (N) или радикальной (R). Таким образом, в органической химии выделяют 9 типовых реакций, обозначаемых символами S, А или Е с индексами R, N или Е:

Реакции замещения (S): ¡ ¡ для насыщенных углеводородов характерны SR (радикального замещения); для ароматических соединений – SE (электрофильного замещения), для карбоновых кислот, галогенпроизводных и спиртов – SN (нуклеофильного замещения).

Механизм хлорирования SR на примере метана ¡ Реакции протекает несколько стадий:

Стадия 2 Рост цепи. ¡ Радикал хлора атакует связь С—Н в молекуле метана, вырывает радикал водорода и образует нейтральную молекулу хлороводорода HCI.
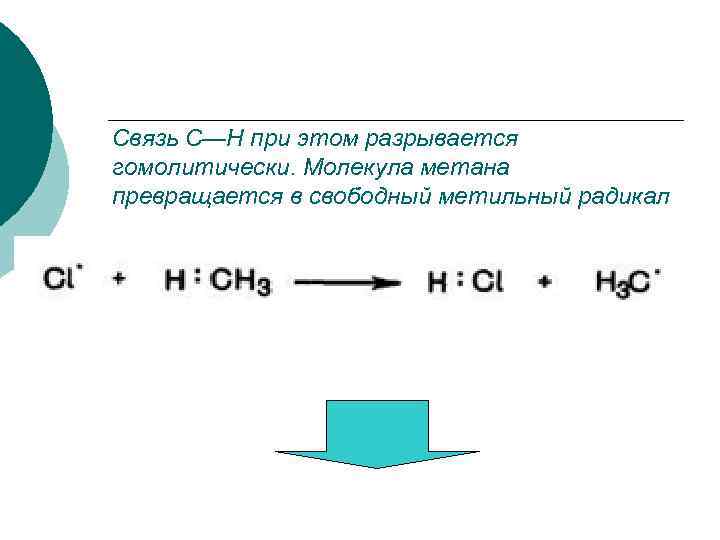
Связь С—Н при этом разрывается гомолитически. Молекула метана превращается в свободный метильный радикал

¡ В метильном радикале атом углерода находится в состоянии sp 2 -гибридизации, т. е. имеет плоское строение. На негибридизованной рорбитали находится один неспаренный электрон. Высокая реакционная способность СН 3 радикала объясняется стремлением к образованию ковалентной связи с участием этого электрона и доступностью для взаимодействия р-орбитали.
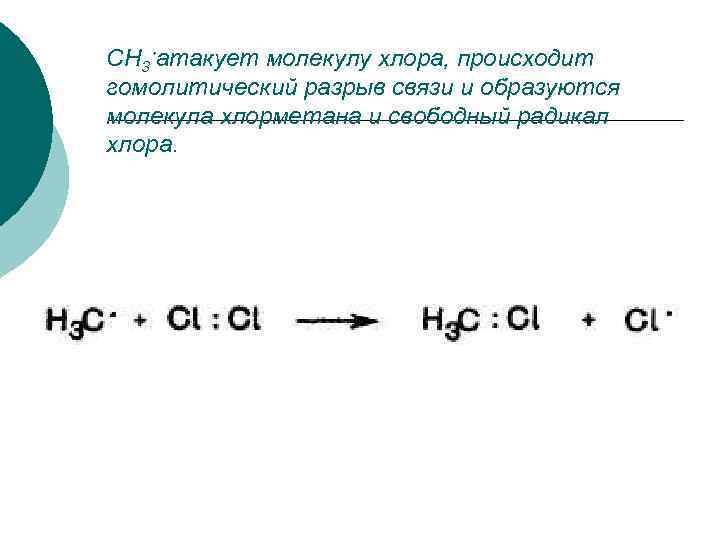
СН 3 атакует молекулу хлора, происходит гомолитический разрыв связи и образуются молекула хлорметана и свободный радикал хлора.

Радикал хлора снова атакует молекулу метана и далее повторяются описанные выше реакции: ¡ В результате получается смесь продуктов различной степени хлорирования СН 3 С 1, СН 2 С 12, СНС 13 и СС 14. Процессы такого типа называют цепными, так как один свободный радикал хлора мог бы инициировать хлорирование всех молекул метана, имеющихся в реакционной среде.

Стадия 3. Обрыв цепи ¡ Последовательно идущие реакции роста цепи могут прерваться, если произойдет исчезновение свободного радикала.

Чаще всего обрыв цепи происходит за счет взаимодействия радикалов хлора между собой.

У высших алканов свободный атом галогена атакует, ¡ прежде всего, атом водорода у 3 -ого атома углерода, затем у 2 -ого и в последнюю очередь у первичного, т. е. проявляется избирательность в атаке галогена. Это объясняется тем, что легче всего гомолитически разрывается связь третичного атома углерода с водородом — энергия связи 376 к. Дж/моль; затем вторичного — 390 к. Дж/моль и, наконец, первичного — 415 к. Дж/моль.

Поэтому и устойчивость образующихся при этом радикалов будет увеличиваться в ряду:

Реакции электрофилъного замещения (SE). ¡ Для ароматических соединений бензольного ряда, конденсированных и гетероциклических ароматических соединений характерны реакции SE –типа. Особенностью реакций SE является то, что атакующий реагент — электрофил — образуется на первой стадии реакции в присутствии кислот Льюиса – AICI 3, Fe. Br 3 (реакции галогенирования, алкилирования по Фриделю -Крафтсу. ) либо в условиях кислотного катализа (алкилирование алкенами и спиртами, нитрование),


Образовавшаяся электрофильная частица Е+ атакует нуклеофильный центр — бензольное ядро. ¡ В результате атаки образуется неустойчивая структура (σ-комплекс) с нарушенной системой кругового сопряжения. Эта стадия является лимитирующей (стадия I). Стабилизация структуры происходит путем отщепления протона от σ комплекса с образованием конечного продукта.
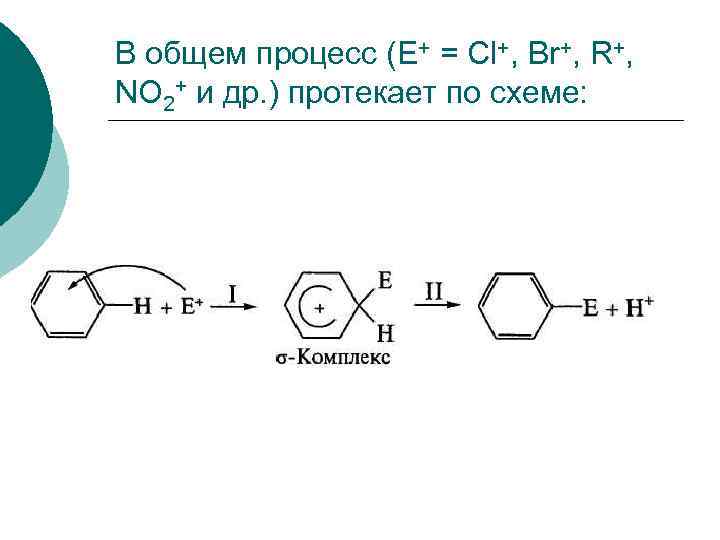
В общем процесс (Е+ = Cl+, Br+, R+, NO 2+ и др. ) протекает по схеме:

На реакционную способность и скорость реакции SE оказывает влияние структура субстрата, т. е. окружение реакционного центра. ¡ Так, электронодонорные заместители (+I, +М-эффект) увеличивают электронную плотность в бензольном ядре, что приводит к росту реакционной способности субстрата; такие заместители ориентируют электрофил в реакциях SE в орто-, и пара-положение, (ортои пара -ориентанты, или ориентанты I рода).

Электроноакцепторные заместители (-М-эффект), ¡ напротив, снижают электронную плотность в бензольном кольце, что приводит к снижению реакционной способности реакционного центра субстрата; такие заместители ориентируют электрофил в мета-положение (мета-ориентанты, или ориентанты II рода).
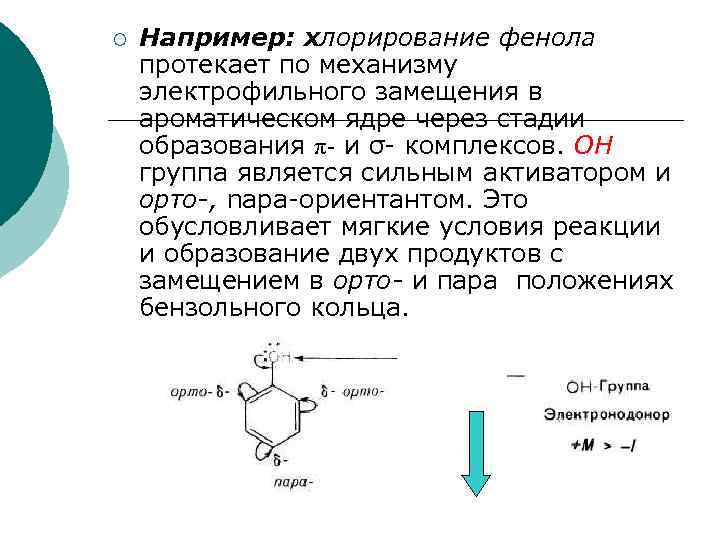
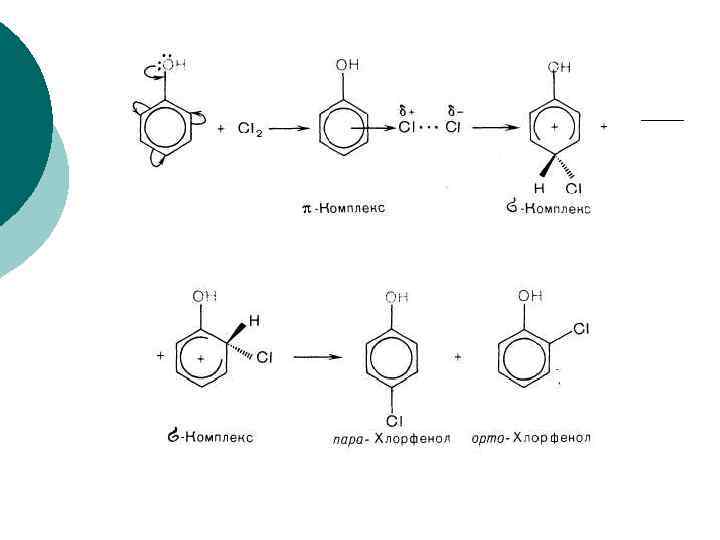
¡ Например: хлорирование фенола протекает по механизму электрофильного замещения в ароматическом ядре через стадии образования π- и σ- комплексов. ОН группа является сильным активатором и орто-, napa-ориентантом. Это обусловливает мягкие условия реакции и образование двух продуктов с замещением в орто- и пара положениях бензольного кольца.

¡ Реакции присоединения (А). Для ненасыщенных углеводородов характерны АЕ, для альдегидов и кетонов – АN типа.

Реакции отщепления, или элиминирования (символ Е). ¡ Эти реакции по направлению обратны реакциям присоединения. Примером может служить дегидрохлорирование третбутилхлорида.

¡ Как правило, реакции отщепления осуществляются как β-элиминирование, т. е. когда отщепляющиеся группы, как в приведенном выше примере, уходят от соседних атомов углерода.
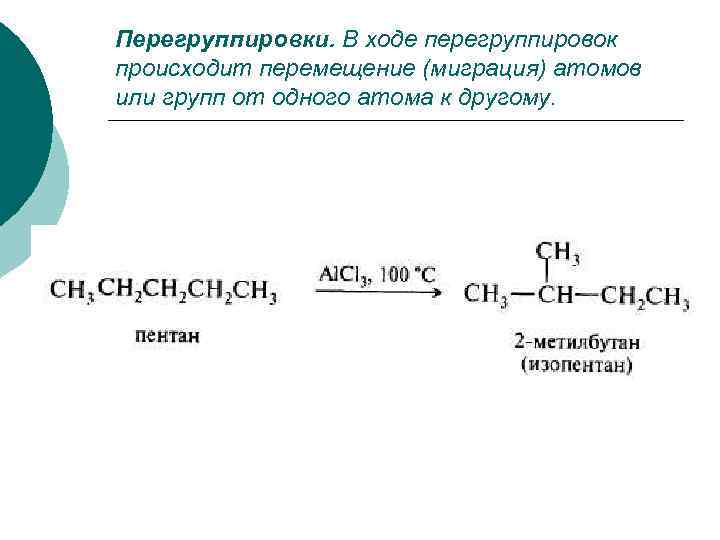
Перегруппировки. В ходе перегруппировок происходит перемещение (миграция) атомов или групп от одного атома к другому.

Окислительновосстановительный характер ¡ органических реакций выявляется не так наглядно, как в случае неорганических. Под окислением в органической химии понимают введение атома кислорода в молекулу субстрата или удаление двух атомов водорода. Восстановление представляет собой обратный процесс, т. е. удаление атома кислорода или введение двух атомов водорода.

¡ В классификации таких реакций учитывается изменение степени окисления атома углерода, являющегося реакционным центром.
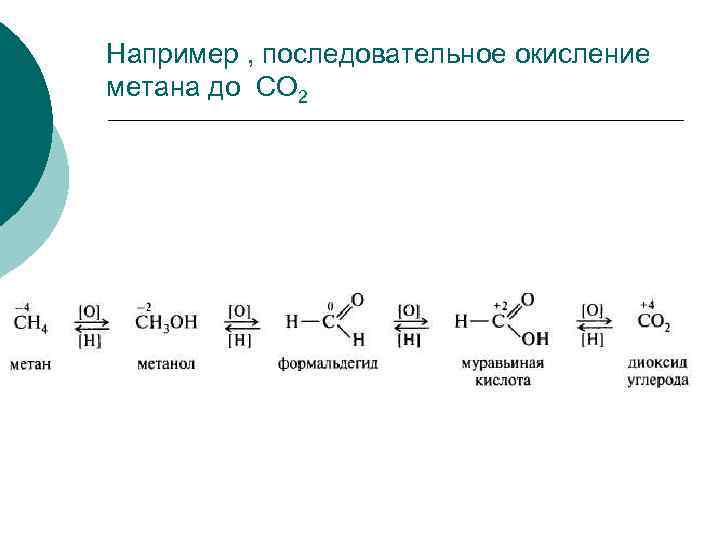
Например , последовательное окисление метана до СО 2
органические реакции.ppt