Тема: «Неметаллы» План урок:













 Тема: «Неметаллы»
Тема: «Неметаллы»
 План урок: -Дать понятие неметаллы - Физические свойства неметаллов - Строение неметаллов - Химические свойства неметаллов - Аллотропия неметаллов - Использование неметаллов
План урок: -Дать понятие неметаллы - Физические свойства неметаллов - Строение неметаллов - Химические свойства неметаллов - Аллотропия неметаллов - Использование неметаллов
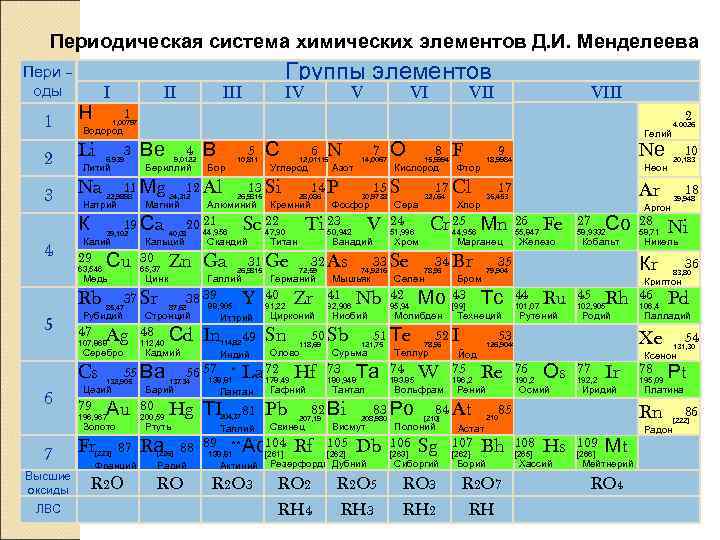
 Периодическая система химических элементов Д. И. Менделеева Пери – Группы элементов оды I III IV VII VIII 1 Н 1, 00797 Не 2 4. 0026 Водород Гелий 2 Li 6. 939 3 Ве 4 9, 0122 В 5 10, 811 С 6 12, 01115 N 7 14, 0067 О 8 15, 9994 F 9 18, 9984 Nе 10 20, 183 Литий Бериллий Бор Углерод Азот Кислород Фтор Неон Na 11 Мg 24, 312 Al 12 13 Si 14 P 15 S 17 Cl 17 Ar 18 3 Натрий 22, 9898 Магний Алюминий 26, 9815 Кремний 28, 086 Фосфор 30, 9738 Сера 32, 064 Хлор 35, 453 39, 948 Аргон К 39, 102 19 Сa 40, 08 20 21 44, 956 Sc 22 47, 90 Ti 2350, 942 V 24 51, 996 Cr 25 Мn 44, 956 26 55, 847 Fe 27 58, 9332 Со 28 58, 71 Ni Калий Кальций Скандий Титан Ванадий Хром Марганец Железо Кобальт Никель 4 29 63, 546 Сu 30 65, 37 Zn Ga 31 Ge 26, 9815 32 As 72, 59 33 Se 74, 9216 34 Br 78, 96 35 79, 904 Кr 36 83, 80 Медь Цинк Галлий Германий Мышьяк Селен Бром Криптон Rb 85, 47 37 Sr 87, 62 38 39 88, 905 Y 40 91, 22 Zr 41 92, 906 Nb 42 95, 94 Мо 43 [99] Тс 44 101, 07 Ru 45 102, 905 Rh 46 106, 4 Pd Рубидий Стронций Иттрий Цирконий Ниобий Молибден Технеций Рутений Родий Палладий 5 47 107, 868 Ag 48 112, 40 Сd In 114, 82 49 Sn 50 Sb 118, 69 51 Тe 121, 75 52 I 78, 96 53 126, 9044 Xe 54 131, 30 Серебро Кадмий Индий Олово Сурьма Теллур Йод Ксенон Cs 132, 905 55 Ва 137. 34 57 * 56 138, 81 La 72 Hf 178. 49 73 180, 948 Та 74 183. 85 W 75 186, 2 Re 76 190, 2 Оs 77 192, 2 Ir 78 195, 09 Рt Цезий Барий Лантан Гафний Тантал Вольфрам Рений Осмий Иридий Платина 6 79 196, 967 Аu 80 200, 59 Hg ТI 204, 37 81 Pb 82 Вi 207, 19 83 Ро 208, 980 84 At [210] 210 85 Rn 86 [222] Золото Ртуть Таллий Свинец Висмут Полоний Астат Радон Fr 87 Rа 88 89 ** Ас104 Rf 105 Db 106 Sg 107 Bh 108 Hs 109 Мt 7 [223] [226] 138, 81 [261] Резерфордий. Дубний [262] [263] Сиборгий [262] Борий [265] Хассий [266] Мейтнерий Франций Радий Актиний Высшие оксиды R 2 О RO R 2 O 3 RO 2 R 2 O 5 RO 3 R 2 O 7 RO 4 ЛВС RH 4 RH 3 RH 2 RH
Периодическая система химических элементов Д. И. Менделеева Пери – Группы элементов оды I III IV VII VIII 1 Н 1, 00797 Не 2 4. 0026 Водород Гелий 2 Li 6. 939 3 Ве 4 9, 0122 В 5 10, 811 С 6 12, 01115 N 7 14, 0067 О 8 15, 9994 F 9 18, 9984 Nе 10 20, 183 Литий Бериллий Бор Углерод Азот Кислород Фтор Неон Na 11 Мg 24, 312 Al 12 13 Si 14 P 15 S 17 Cl 17 Ar 18 3 Натрий 22, 9898 Магний Алюминий 26, 9815 Кремний 28, 086 Фосфор 30, 9738 Сера 32, 064 Хлор 35, 453 39, 948 Аргон К 39, 102 19 Сa 40, 08 20 21 44, 956 Sc 22 47, 90 Ti 2350, 942 V 24 51, 996 Cr 25 Мn 44, 956 26 55, 847 Fe 27 58, 9332 Со 28 58, 71 Ni Калий Кальций Скандий Титан Ванадий Хром Марганец Железо Кобальт Никель 4 29 63, 546 Сu 30 65, 37 Zn Ga 31 Ge 26, 9815 32 As 72, 59 33 Se 74, 9216 34 Br 78, 96 35 79, 904 Кr 36 83, 80 Медь Цинк Галлий Германий Мышьяк Селен Бром Криптон Rb 85, 47 37 Sr 87, 62 38 39 88, 905 Y 40 91, 22 Zr 41 92, 906 Nb 42 95, 94 Мо 43 [99] Тс 44 101, 07 Ru 45 102, 905 Rh 46 106, 4 Pd Рубидий Стронций Иттрий Цирконий Ниобий Молибден Технеций Рутений Родий Палладий 5 47 107, 868 Ag 48 112, 40 Сd In 114, 82 49 Sn 50 Sb 118, 69 51 Тe 121, 75 52 I 78, 96 53 126, 9044 Xe 54 131, 30 Серебро Кадмий Индий Олово Сурьма Теллур Йод Ксенон Cs 132, 905 55 Ва 137. 34 57 * 56 138, 81 La 72 Hf 178. 49 73 180, 948 Та 74 183. 85 W 75 186, 2 Re 76 190, 2 Оs 77 192, 2 Ir 78 195, 09 Рt Цезий Барий Лантан Гафний Тантал Вольфрам Рений Осмий Иридий Платина 6 79 196, 967 Аu 80 200, 59 Hg ТI 204, 37 81 Pb 82 Вi 207, 19 83 Ро 208, 980 84 At [210] 210 85 Rn 86 [222] Золото Ртуть Таллий Свинец Висмут Полоний Астат Радон Fr 87 Rа 88 89 ** Ас104 Rf 105 Db 106 Sg 107 Bh 108 Hs 109 Мt 7 [223] [226] 138, 81 [261] Резерфордий. Дубний [262] [263] Сиборгий [262] Борий [265] Хассий [266] Мейтнерий Франций Радий Актиний Высшие оксиды R 2 О RO R 2 O 3 RO 2 R 2 O 5 RO 3 R 2 O 7 RO 4 ЛВС RH 4 RH 3 RH 2 RH
 Определение понятия неметаллы Неметаллы – химические элементы, которые образуют в свободном виде простые вещества, не обладающие физическими свойствами металлов.
Определение понятия неметаллы Неметаллы – химические элементы, которые образуют в свободном виде простые вещества, не обладающие физическими свойствами металлов.
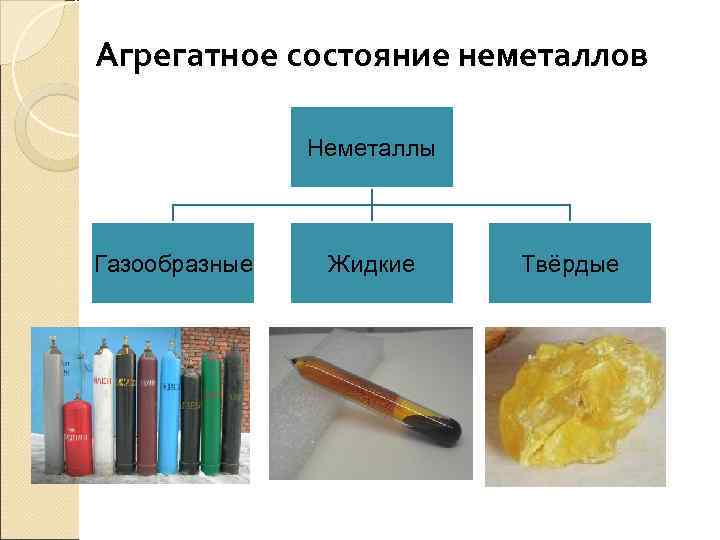
 Агрегатное состояние неметаллов Неметаллы Газообразные Жидкие Твёрдые
Агрегатное состояние неметаллов Неметаллы Газообразные Жидкие Твёрдые
 Свойства неметаллов: 1. Отсутствие металлического блеска (исключение – кремний) I - йод C - углерод S - сера Si - кремний
Свойства неметаллов: 1. Отсутствие металлического блеска (исключение – кремний) I - йод C - углерод S - сера Si - кремний
 Свойства неметаллов: 2. Низкая теплопроводность (газовая прослойка –наилучший теплоизолятор) 3. Низкая электрическая проводимость (исключение – графит)
Свойства неметаллов: 2. Низкая теплопроводность (газовая прослойка –наилучший теплоизолятор) 3. Низкая электрическая проводимость (исключение – графит)
 Свойства неметаллов: 5. Хрупкость
Свойства неметаллов: 5. Хрупкость
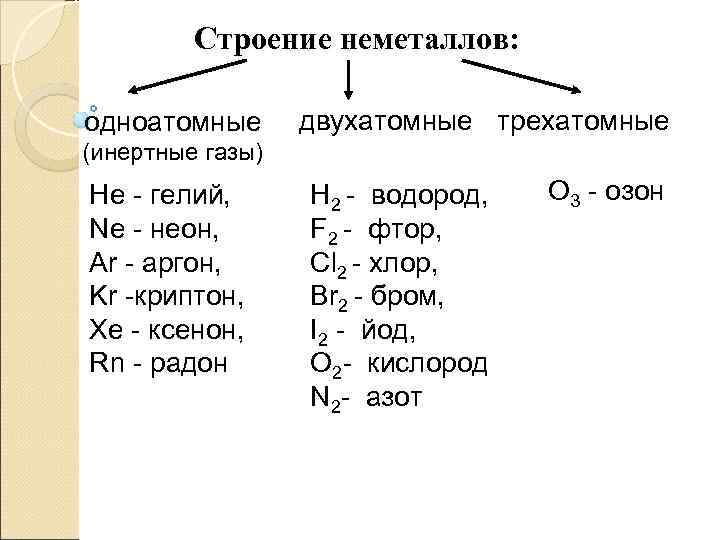
 Строение неметаллов: одноатомные двухатомные трехатомные (инертные газы) He - гелий, H 2 - водород, O 3 - озон Ne - неон, F 2 - фтор, Ar - аргон, Cl 2 - хлор, Kr -криптон, Br 2 - бром, Xe - ксенон, I 2 - йод, Rn - радон O 2 - кислород N 2 - азот
Строение неметаллов: одноатомные двухатомные трехатомные (инертные газы) He - гелий, H 2 - водород, O 3 - озон Ne - неон, F 2 - фтор, Ar - аргон, Cl 2 - хлор, Kr -криптон, Br 2 - бром, Xe - ксенон, I 2 - йод, Rn - радон O 2 - кислород N 2 - азот
 Электроотрицательность-способность атомов химического элемента смещать к себе общие электронные пары Ряд электроотрицательности неметаллов H, As, I, Si, P, Se, C, S, Br, Cl, N, O, F Усиление электроотрицательности
Электроотрицательность-способность атомов химического элемента смещать к себе общие электронные пары Ряд электроотрицательности неметаллов H, As, I, Si, P, Se, C, S, Br, Cl, N, O, F Усиление электроотрицательности
 Химические свойства неметаллов: Характерными для большинства неметаллов являются окислительные свойства: - с металлами: Ca + Cl 2 = Ca. Cl 2 - с менее электротрицательными неметаллами: H 2 + S = H 2 S - со сложными веществами: 2 Fe. Cl 2 + Cl 2 = 2 Fe. Cl 3
Химические свойства неметаллов: Характерными для большинства неметаллов являются окислительные свойства: - с металлами: Ca + Cl 2 = Ca. Cl 2 - с менее электротрицательными неметаллами: H 2 + S = H 2 S - со сложными веществами: 2 Fe. Cl 2 + Cl 2 = 2 Fe. Cl 3
 Химические свойства неметаллов: Менее характерны для неметаллов восстановительные свойства: -с более электротрицательными неметаллами: Si + 2 F 2 = Si. F 4 C + O 2 = CO 2 - со сложными веществами: H 2 + HCHO = CH 3 OH
Химические свойства неметаллов: Менее характерны для неметаллов восстановительные свойства: -с более электротрицательными неметаллами: Si + 2 F 2 = Si. F 4 C + O 2 = CO 2 - со сложными веществами: H 2 + HCHO = CH 3 OH
 Аллотропия- это способность химического элемента образовывать несколько простых веществ Химический элемент углерод С Алмаз Графит
Аллотропия- это способность химического элемента образовывать несколько простых веществ Химический элемент углерод С Алмаз Графит
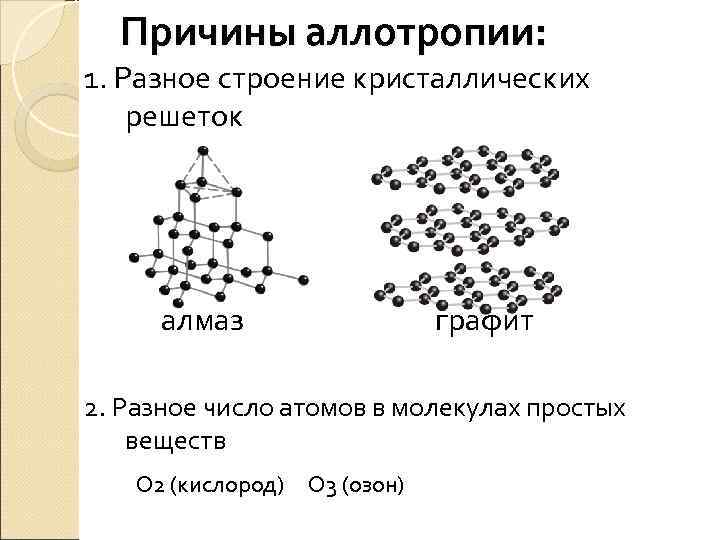
 Причины аллотропии: 1. Разное строение кристаллических решеток алмаз графит 2. Разное число атомов в молекулах простых веществ О 2 (кислород) О 3 (озон)
Причины аллотропии: 1. Разное строение кристаллических решеток алмаз графит 2. Разное число атомов в молекулах простых веществ О 2 (кислород) О 3 (озон)
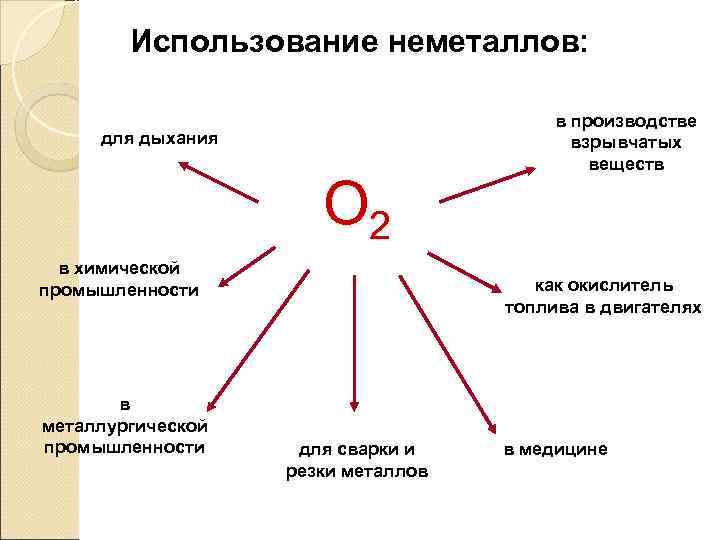
 Использование неметаллов: в производстве для дыхания взрывчатых веществ О 2 в химической промышленности как окислитель топлива в двигателях в металлургической промышленности для сварки и в медицине резки металлов
Использование неметаллов: в производстве для дыхания взрывчатых веществ О 2 в химической промышленности как окислитель топлива в двигателях в металлургической промышленности для сварки и в медицине резки металлов
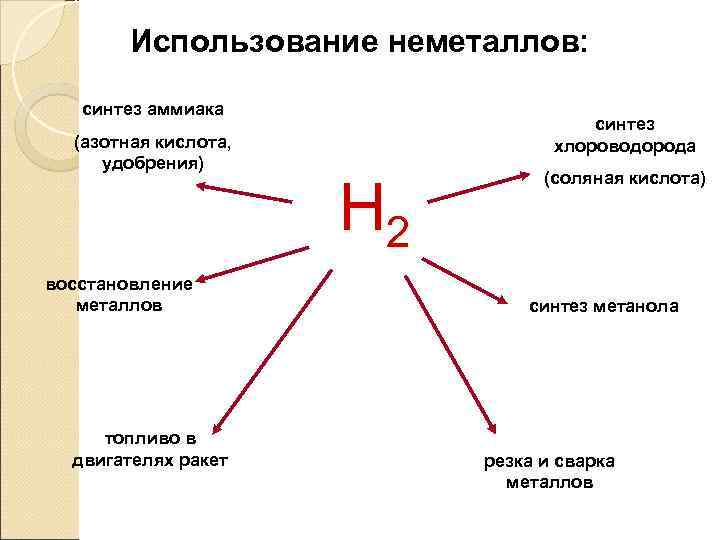
 Использование неметаллов: синтез аммиака синтез (азотная кислота, хлороводорода удобрения) (соляная кислота) Н 2 восстановление металлов синтез метанола топливо в двигателях ракет резка и сварка металлов
Использование неметаллов: синтез аммиака синтез (азотная кислота, хлороводорода удобрения) (соляная кислота) Н 2 восстановление металлов синтез метанола топливо в двигателях ракет резка и сварка металлов
 Использование неметаллов: Вода применяется для: • в жизни растений, животных и человека; • в быту; • в различных отраслях промышленности и сельского хозяйства; • для получения щелочей; • для получения кислот; • для получения водорода.
Использование неметаллов: Вода применяется для: • в жизни растений, животных и человека; • в быту; • в различных отраслях промышленности и сельского хозяйства; • для получения щелочей; • для получения кислот; • для получения водорода.
 Закрепление знаний: 1. Дайте определение неметаллы? 2. Выберите из перечисленных веществ неметаллы: O 2, Zn, Cl, Br 2, Ne, O 3, Al, I 2 3. Какой самый сильный неметалл? Какой самый слабый неметалл? 4. Назовите одноатомные, двухатомные и трехатомные неметаллы? 5. Перечислите использование неметаллов O 2 и H 2.
Закрепление знаний: 1. Дайте определение неметаллы? 2. Выберите из перечисленных веществ неметаллы: O 2, Zn, Cl, Br 2, Ne, O 3, Al, I 2 3. Какой самый сильный неметалл? Какой самый слабый неметалл? 4. Назовите одноатомные, двухатомные и трехатомные неметаллы? 5. Перечислите использование неметаллов O 2 и H 2.

