 ТЕМА: «Многоатомные спирты» Многоатомные спирты – спирты, содержащие две и более гидроксогрупп.
ТЕМА: «Многоатомные спирты» Многоатомные спирты – спирты, содержащие две и более гидроксогрупп.
 Представители многоатомных спиртов Этиленгликоль (двухатомный спирт) СН 2 – СН 2 ОН ОН ЭТАНДИОЛ – 1, 2 Глицерин (трёхатомный спирт) СН 2 – ОН ПРОПАНТРИОЛ – 1, 2, 3
Представители многоатомных спиртов Этиленгликоль (двухатомный спирт) СН 2 – СН 2 ОН ОН ЭТАНДИОЛ – 1, 2 Глицерин (трёхатомный спирт) СН 2 – ОН ПРОПАНТРИОЛ – 1, 2, 3
 Глицерин и его соединения Глицерин открыт в 1779 году химиком и фармацевтом Шееле при изготовлении пластыря, т. е. при нагревании жира с оксидом свинца.
Глицерин и его соединения Глицерин открыт в 1779 году химиком и фармацевтом Шееле при изготовлении пластыря, т. е. при нагревании жира с оксидом свинца.
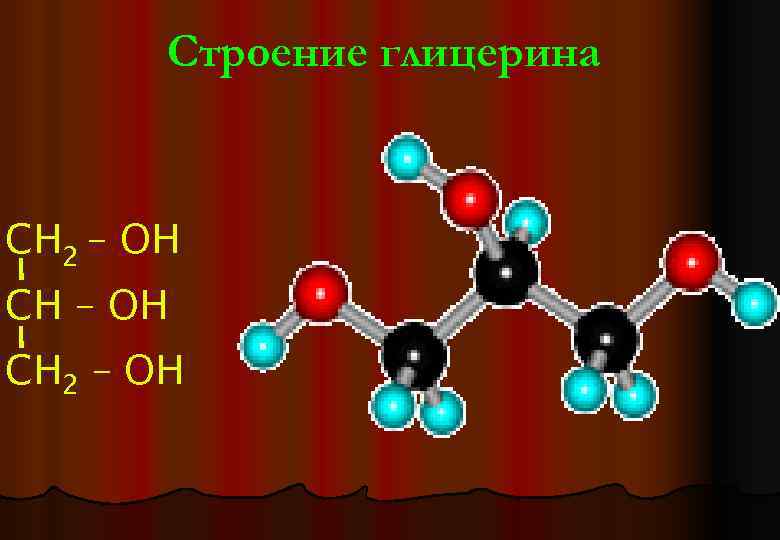 Строение глицерина СН 2 – ОН
Строение глицерина СН 2 – ОН
 Физические свойства глицерина Бесцветная, сиропообразная жидкость, сладкая на вкус, тяжелее воды, хорошо растворяется в воде. Имеет высокую температуру кипения – 900 С. Совершенно чистый и безводный глицерин – твёрдое вещество с t пл. 180 С, обладает большой гигроскопичностью, вызывает ожоги. Не ядовит.
Физические свойства глицерина Бесцветная, сиропообразная жидкость, сладкая на вкус, тяжелее воды, хорошо растворяется в воде. Имеет высокую температуру кипения – 900 С. Совершенно чистый и безводный глицерин – твёрдое вещество с t пл. 180 С, обладает большой гигроскопичностью, вызывает ожоги. Не ядовит.
 Химические свойства Для двух – и трёхатомных спиртов характерны все реакции одноатомных спиртов. Кислотность многоатомных спиртов выше, чем одноатомных, что объясняется наличием в молекуле дополнительных гидроксильных групп.
Химические свойства Для двух – и трёхатомных спиртов характерны все реакции одноатомных спиртов. Кислотность многоатомных спиртов выше, чем одноатомных, что объясняется наличием в молекуле дополнительных гидроксильных групп.
 1. Взаимодействие со щелочными металлами: СН 2 – ОН СН 2 – О – Na 2 СН – ОН + 6 Na → 2 СН – О – Na СН 2 – ОН +3 Н 2↑ СН 2 – О – Na Можно заместить один, два или три атома водорода на металл. Соли трёхатомных спиртов – глицераты. Соли двухатомных спиртов – гликоляты.
1. Взаимодействие со щелочными металлами: СН 2 – ОН СН 2 – О – Na 2 СН – ОН + 6 Na → 2 СН – О – Na СН 2 – ОН +3 Н 2↑ СН 2 – О – Na Можно заместить один, два или три атома водорода на металл. Соли трёхатомных спиртов – глицераты. Соли двухатомных спиртов – гликоляты.
 2. Образование сложных эфиров: а) Реакция с азотной кислотой: CH 2—O—NO 2 │ │ СН—ОН + 3 НNO 3 → CH—O—NO 2 + 3 Н 2 О │ │ 3(HO–NO 2) СН 2—ОН CH 2 —O—NO 2 СН 2—ОН глицерин тринитрат глицерина (нитроглицерин)
2. Образование сложных эфиров: а) Реакция с азотной кислотой: CH 2—O—NO 2 │ │ СН—ОН + 3 НNO 3 → CH—O—NO 2 + 3 Н 2 О │ │ 3(HO–NO 2) СН 2—ОН CH 2 —O—NO 2 СН 2—ОН глицерин тринитрат глицерина (нитроглицерин)
 Разложение нитроглицерина: Н 2 С—О—NO 2 │ 4 HC—O—NO 2 → 6 N 2↑+12 CO 2↑+10 H 2 O │ H 2 C—O—NO 2 Нитроглицерин - жидкость, взрывается даже от слабой встряски. Используется в производстве динамита.
Разложение нитроглицерина: Н 2 С—О—NO 2 │ 4 HC—O—NO 2 → 6 N 2↑+12 CO 2↑+10 H 2 O │ H 2 C—O—NO 2 Нитроглицерин - жидкость, взрывается даже от слабой встряски. Используется в производстве динамита.
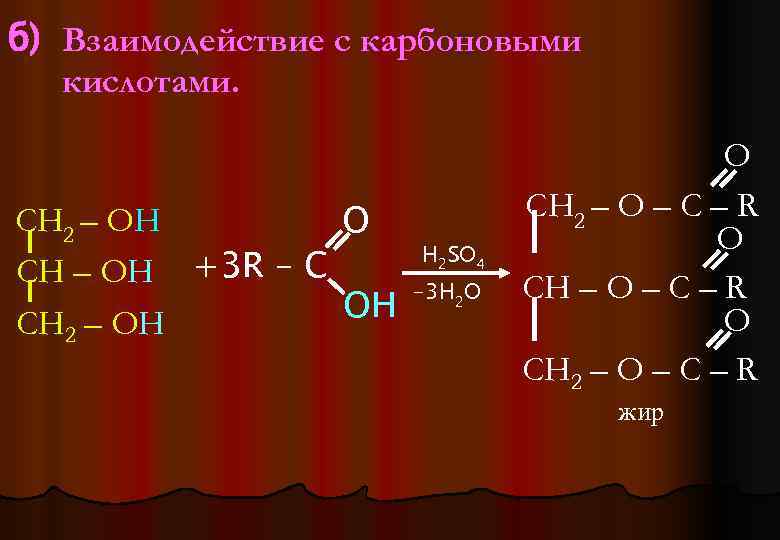 б) Взаимодействие с карбоновыми кислотами. СН 2 – ОН O СН – ОН +3 R – C OH СН 2 – ОН H 2 SO 4 -3 H 2 O O СН 2 – О – C – R жир
б) Взаимодействие с карбоновыми кислотами. СН 2 – ОН O СН – ОН +3 R – C OH СН 2 – ОН H 2 SO 4 -3 H 2 O O СН 2 – О – C – R жир
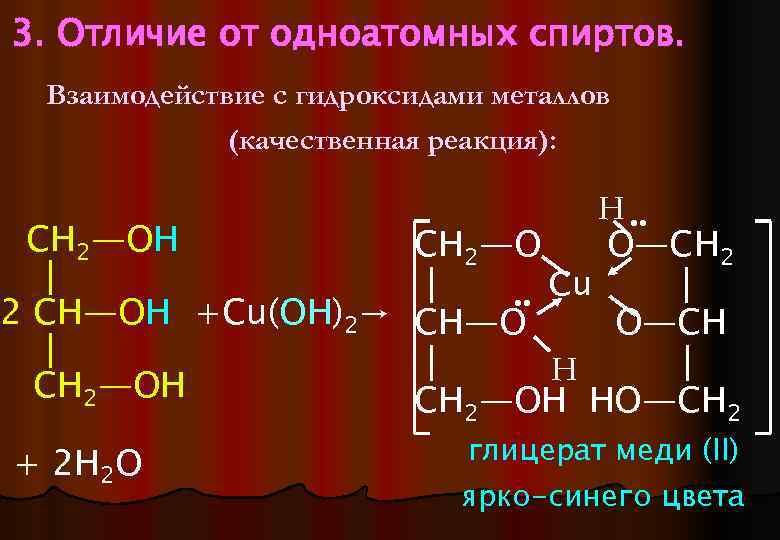 3. Отличие от одноатомных спиртов. Взаимодействие с гидроксидами металлов (качественная реакция): Н • • CH 2—OH СН 2—О O—CH 2 │ │ Сu │ • • 2 CH—OH +Cu(OH)2→ CH—O O—CH │ │ │ Н CH 2—OH СН 2—ОН НO―CH 2 + 2 H 2 O глицерат меди (II) ярко-синего цвета
3. Отличие от одноатомных спиртов. Взаимодействие с гидроксидами металлов (качественная реакция): Н • • CH 2—OH СН 2—О O—CH 2 │ │ Сu │ • • 2 CH—OH +Cu(OH)2→ CH—O O—CH │ │ │ Н CH 2—OH СН 2—ОН НO―CH 2 + 2 H 2 O глицерат меди (II) ярко-синего цвета
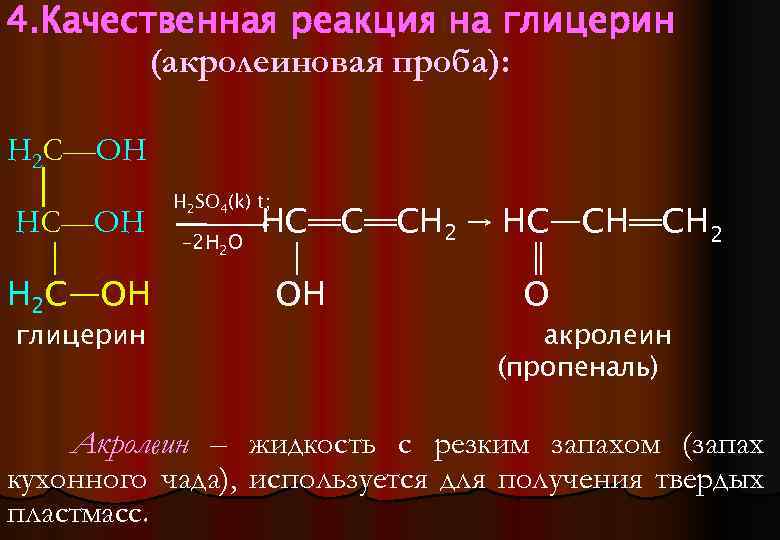 4. Качественная реакция на глицерин (акролеиновая проба): Н 2 С—ОН │ Н 2 С—ОН глицерин Н 2 SO 4(k) t; – 2 H 2 O HC═C═CH 2 → HC—CH═CH 2 │ ║ OH O акролеин (пропеналь) Акролеин – жидкость с резким запахом (запах кухонного чада), используется для получения твердых пластмасс.
4. Качественная реакция на глицерин (акролеиновая проба): Н 2 С—ОН │ Н 2 С—ОН глицерин Н 2 SO 4(k) t; – 2 H 2 O HC═C═CH 2 → HC—CH═CH 2 │ ║ OH O акролеин (пропеналь) Акролеин – жидкость с резким запахом (запах кухонного чада), используется для получения твердых пластмасс.
 Получение многоатомных спиртов 1. Из алкенов (реакция Вагнера): СН 2═ СН 2 + Н 2 О + [ О ] этилен t, K, P CH 2—CH 2 KMn. O 4 │ │ OH OH этиленгликоль 2. Из дигалогенопроизводных: СН 2 — СН 2 + 2 Na. OH → CH 2 — CH 2 водн. р-р │ │ OH OH Сl Cl 1, 2 -дихлорэтан этиленгликоль + 2 Na. Cl
Получение многоатомных спиртов 1. Из алкенов (реакция Вагнера): СН 2═ СН 2 + Н 2 О + [ О ] этилен t, K, P CH 2—CH 2 KMn. O 4 │ │ OH OH этиленгликоль 2. Из дигалогенопроизводных: СН 2 — СН 2 + 2 Na. OH → CH 2 — CH 2 водн. р-р │ │ OH OH Сl Cl 1, 2 -дихлорэтан этиленгликоль + 2 Na. Cl
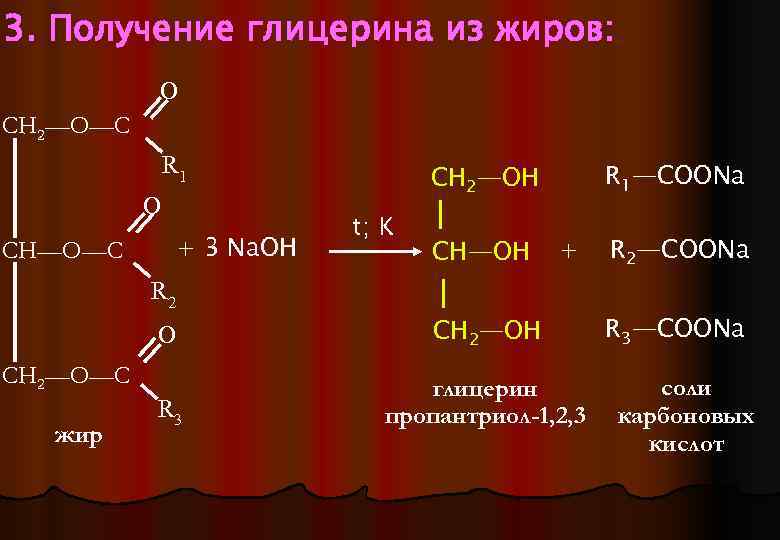 3. Получение глицерина из жиров: О СН 2—О—С R 1 О + 3 Na. OH СН—О—С R 2 R 1—COONa CH 2—OH t; K CH—OH + О CH 2—OH R 3 глицерин пропантриол-1, 2, 3 СН 2—О—С жир R 2—COONa R 3—COONa соли карбоновых кислот
3. Получение глицерина из жиров: О СН 2—О—С R 1 О + 3 Na. OH СН—О—С R 2 R 1—COONa CH 2—OH t; K CH—OH + О CH 2—OH R 3 глицерин пропантриол-1, 2, 3 СН 2—О—С жир R 2—COONa R 3—COONa соли карбоновых кислот