Растворы электролитов - копия.ppt
- Количество слайдов: 27

ТЕМА ЛЕКЦИИ Растворы электролитов. Сильные и слабые электролиты. Водородный показатель. Буферные растворы.

Электролиты Электролиты - это вещества, расплавы или растворы которых проводят электрический ток вследствие диссоциации на ионы. Электролиты также называют проводниками второго рода. Положительно заряженные ионы – катионы (+). Отрицательно заряженные ионы – анионы (-). Электролитами являются соли, кислоты и основания.

Электролитическая диссоциация вызывается взаимодействием полярных молекул растворителя с частицами растворяемого вещества. Например, для водных растворов: HCl (газ) + n. H 2 O = H+ n. H 2 O + Cl , Na. Cl (крист) + (p+q)H 2 O = Na+ p. H 2 O + Cl q. H 2 O.

Диссоциация электролитов Диссоциация веществ с ионной связью Диссоциация веществ с полярной связью
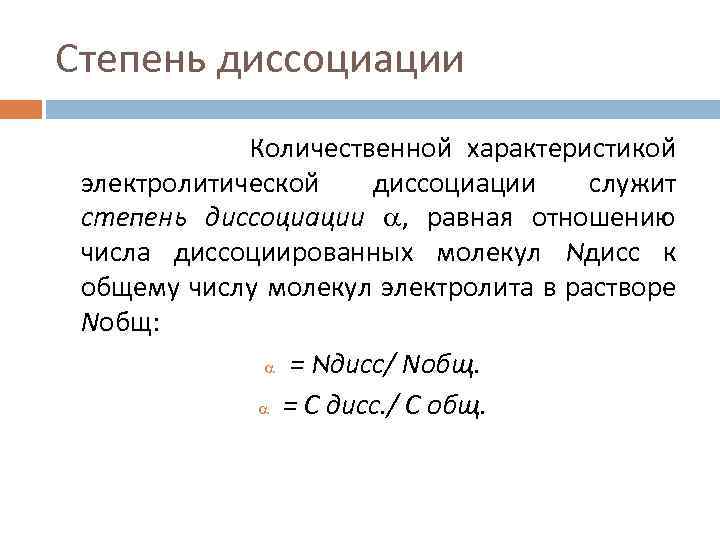
Степень диссоциации Количественной характеристикой электролитической диссоциации служит степень диссоциации , равная отношению числа диссоциированных молекул Nдисс к общему числу молекул электролита в растворе Nобщ: = Nдисс/ Nобщ. = С дисс. / С общ.

Сильные и слабые электролиты В зависимости от величины степени диссоциации электролита , различают сильные электролиты ( > 0, 3), электролиты средней силы (0, 03< < 0, 3) слабые ( < 0, 03) электролиты

Сильные электролиты (Егидр. > Еассоц. ) В водных растворах сильными электролитами являются: большинство солей, такие кислоты, как HCl. O 4, HMn. O 4, H 2 SO 4, HNO 3, HCl, HBr, HI гидроксиды щелочных и щелочно-земельных металлов: Li. OH, Na. OH, KOH, Rb. OH, Cs. OH, Ca(OH)2, Sr(OH)2, Ba(OH)2

Диссоциация сильных электролитов Кислоты: HNO 3 = H+ + NO 3 Основания: КОН = К+ + ОН- Соли: - средние соли диссоциируют в одну ступень Al 2(SO 4)3 = 2 Al 3+ + 3 SO 42 -; - кислые соли диссоциируют ступенчато: Na. HCO 3 = Na+ + НСО 3ˉ = Н+ + СО 3ˉ - основные соли диссоциируют ступенчато: Mg. OHCl = Mg. OH+ + Сlˉ Mg. OH+= Mg 2+ + ОНˉ

Сильные электролиты Для оценки состояния ионов в растворе пользуются величиной, называемой активностью (активной концентрацией). Под активностью иона понимают ту эффективную концентрацию его, соответственно которой он проявляет себя в физико-химических процессах. а = fа·Сэл-та, где fа – коэффициент активности
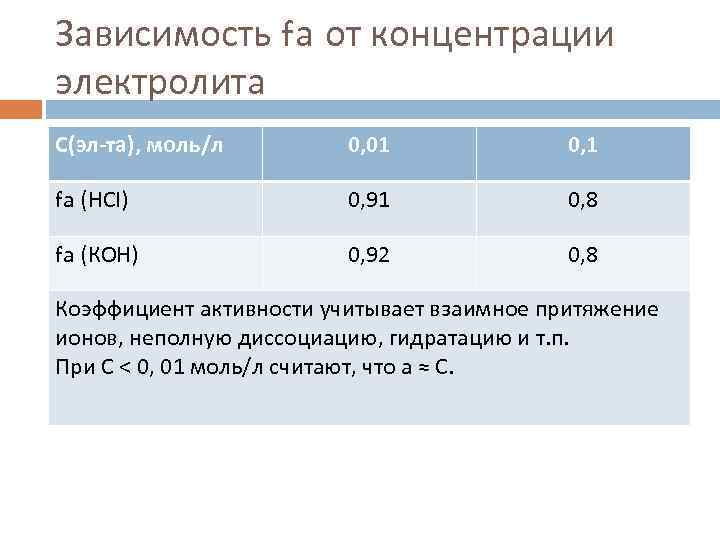
Зависимость fа от концентрации электролита С(эл-та), моль/л 0, 01 0, 1 fа (НСl) 0, 91 0, 8 fа (КОН) 0, 92 0, 8 Коэффициент активности учитывает взаимное притяжение ионов, неполную диссоциацию, гидратацию и т. п. При С ˂ 0, 01 моль/л считают, что а ≈ С.
![Расчет концентрации ионов в растворах сильных электролитов В сильных кислотах [H+] = a. H+ Расчет концентрации ионов в растворах сильных электролитов В сильных кислотах [H+] = a. H+](https://present5.com/presentation/-57947336_240889538/image-11.jpg)
Расчет концентрации ионов в растворах сильных электролитов В сильных кислотах [H+] = a. H+ = а к-ты. При концентрациях менее 0, 01 моль/л [H+] = Сн(к-ты). В сильных основаниях [ОН-] = a. ОН- = а осн При концентрациях менее 0, 01 моль/л [ОН-] = Сн(осн).

Слабые электролиты Для диссоциации уксусной кислоты СН 3 СООН ↔ Н+ + СН 3 СООˉ константа равновесия имеет вид: К = ([Н+]·[СНз. СООˉ])/[СНз. СООН] Константа равновесия, отвечающая диссоциации слабого электролита, называется константой диссоциации. Величина Кд зависит: 1. от природы электролита и растворителя, 2. от температуры. !!! Кд не зависит от концентрации раствора.

Константа диссоциации слабых электролитов Константа диссоциации характеризует способность данного вещества распадаться на ионы: чем больше Кд, тем легче электролит диссоциирует. Кд(СН 3 СООН) = 2· 10 -5 Кд(НСN) =8· 10 -10 Следовательно, уксусная кислота является более сильным электролитом, чем циановодородная.

Диссоциация многоосновных кислот и оснований Многоосновные кислоты, а также основания двух- и более валентных металлов диссоциируют ступенчато. 1. Н 2 СО 3 ↔ Н + + НСО 3ˉ К 1 = 5· 10 -7 2. НСО 3ˉ ↔ Н+ + СО 32ˉ К 2 = 5· 10 -11 Как видно, К 1 ˂˂ К 2, то есть диссоциация идет преимущественно по первой ступени.
![Закон разбавления Оствальда МА М+ + А– [M+] [A–] KD = ––––– [MA] [M+] Закон разбавления Оствальда МА М+ + А– [M+] [A–] KD = ––––– [MA] [M+]](https://present5.com/presentation/-57947336_240889538/image-15.jpg)
Закон разбавления Оствальда МА М+ + А– [M+] [A–] KD = ––––– [MA] [M+] = [A–] = c 0 [MA] = (1 – ) c 0 KD = 2 c 0 / (1 – ) если << 1 ( < 0, 05) KD = 2 c 0

Степень диссоциации слабого электролита зависит от: 1. Концентрации электролита. Степень диссоциации тем больше, чем ниже концентрация, то есть чем больше разбавлен раствор. 2. Температуры. При нагревании раствора увеличивается. 3. Природы растворителя. Чем полярнее растворитель, тем в большей степени он изолирует ионы друг от друга, тем больше . 4. Наличия одноименных ионов в растворе.

Диссоциация воды Вода не только самый распространенный растворитель, она также является слабым электролитом. 2 Н 2 О Н 3 О + + ОН- где Н 3 О+ (Н+·Н 2 О)- катион гидроксония (гидратированный катион водорода) По упрощенной схеме диссоциацию воды можно выразить следующим уравнением: Н 2 О Н+ + ОН
![Ионное произведение воды Константа диссоциации воды Kд = [H+] [OH ]/ [H 2 O] Ионное произведение воды Константа диссоциации воды Kд = [H+] [OH ]/ [H 2 O]](https://present5.com/presentation/-57947336_240889538/image-18.jpg)
Ионное произведение воды Константа диссоциации воды Kд = [H+] [OH ]/ [H 2 O] Поскольку степень диссоциации воды очень мала, то концентрацию недиссоциированных молекул можно принять равной молярной концентрации жидкой воды. Поэтому при Т=const [H+] [OH ] = Kд· [H 2 O] = const. Произведение концентраций ионов [H+] и [ОН ] носит название ионного произведения воды и является постоянной величиной при неизменной температуре. При 298 К (25 о. С): [H+] [ОН ] = K(H 2 O) = KВ = 10 -14 Ионное произведение воды Kв увеличивается с ростом температуры, т. к. диссоциация воды –эндотермический процесс. Например: Kв(50 о. С)= 5, 5· 10 -14 , Kв(100 о. С) = 55· 10 -14

Водородный показатель Для указания концентрации ионов водорода в растворе используют так называемый водородный показатель – отрицательный десятичный логарифм от концентрации катионов водорода: p. H = –lg[Н+], а для обозначения концентрации гидроксид-ионов гидроксидный показатель: p. OH = –lg[ОН ]. При температуре 298 К р. Н + р. ОН = 14, поэтому в чистой воде [Н+] = [ОН ] = 1 10 -7 моль/л, следовательно, в нейтральной среде р. Н = р. ОН = 7; в кислотной среде [H+] > [ОН ], р. Н < 7; в щелочных растворах [H+] < [ОН ], поэтому р. Н > 7.

Способы измерения р. Н Индикаторный способ Индикаторы – это вещества, изменяющие свою окраску в зависимости от р. Н раствора. Интервал перехода окраски индикатора – это интервал значений р. Н, в котором индикатор изменяет свой цвет. Метиловый оранжевый: 3, 1 – 4, 5 Лакмус: 5, 0 – 8, 0 Фенолфталеин: 8, 0 – 9, 8
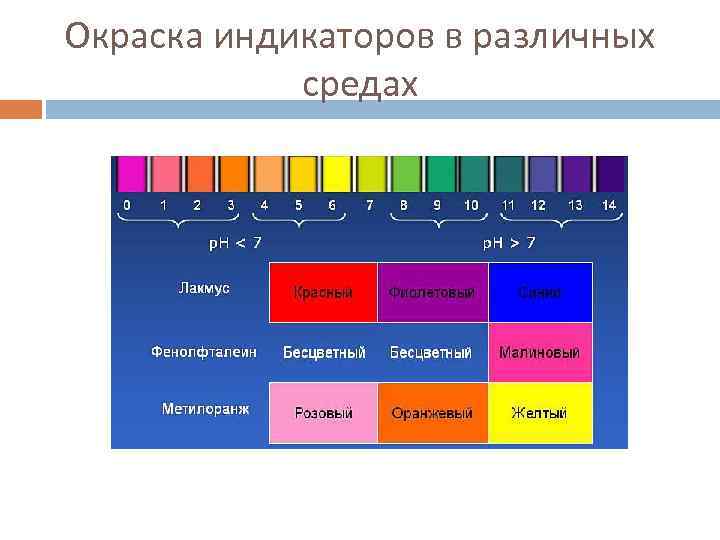
Окраска индикаторов в различных средах

р. Н - метрия

р. Н физиологических жидкостей Желудочный сок Слюна Кровь Слезы 1, 60 – 1, 80 6, 35 – 6, 85 7, 35 – 7, 45 7, 30 – 7, 40

Буферные растворы — растворы, обладающие способностью поддерживать р. Н (водородный показатель) на одном уровне при их разбавлении, концентрировании и при добавлении к ним небольших количеств сильных кислот или щелочей. Карбонатный буфер: Na. HCO 3 +Na 2 CO 3 Ацетатный буфер: СН 3 СООН + СН 3 СООNa Аммиачный буфер: NH 3 + NH 4 Cl

Буферные растворы Буферная система представляет собой смесь слабой кислоты и ее соли, образованной сильным основанием (например, уксусной кислоты СН 3 СООН и ацетата натрия CH 3 COONa), или смесь слабого основания и его соли, образованной сильной кислотой (например, смесь раствора аммиака NH 3 и хлористого аммония NH 4 Cl). Величина р. Н буферного раствора зависит от величины константы диссоциации слабой кислоты или слабого основания и от соотношения концентраций компонентов, образующих буферную систему.

Буферные растворы 1. 2. Буферная емкость – число эквивалентов сильного электролита, которое необходимо добавить для изменения р. Н одного литра буферного раствора на одну единицу. Буферная емкость зависит: от концентрации компонентов: чем больше С, тем больше буферная емкость; от соотношения концентраций. Оптимально равенство С компонентов буферного раствора.

Оптимальные р. Н для овощных культур - растения, растущие на нейтральных почвах (р. Н 6, 6 -7, 0): капуста белокочанная и почти все разновидности капусты, лук, пастернак, перец, свекла столовая - растения, требующие слабокислой реакции (р. Н 6, 3 -6, 7): баклажаны, бобы, горох, дыня, кабачки, картофель, огурец, салат кочанный, фасоль, шпинат - растения, хорошо переносящие умеренную кислотность почвы (р. Н 5, 0 -5, 5): морковь, помидоры, редька, репа, тыква.
Растворы электролитов - копия.ppt