Лек. Растворы.ppt
- Количество слайдов: 10
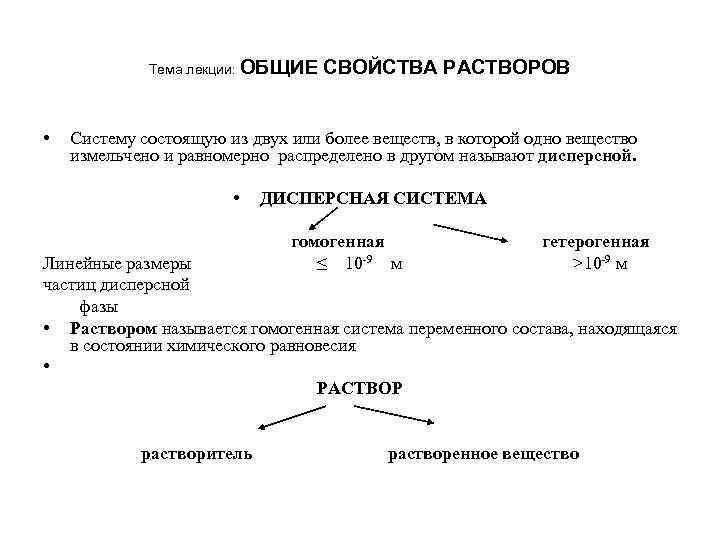
Тема лекции: ОБЩИЕ • СВОЙСТВА РАСТВОРОВ Систему состоящую из двух или более веществ, в которой одно вещество измельчено и равномерно распределено в другом называют дисперсной. • ДИСПЕРСНАЯ СИСТЕМА гомогенная ≤ 10 -9 м гетерогенная >10 -9 м Линейные размеры частиц дисперсной фазы • Раствором называется гомогенная система переменного состава, находящаяся в состоянии химического равновесия • РАСТВОР растворитель растворенное вещество

Термодинамика процесса растворения Процесс растворения – сложный физико-химический процесс: 1. Разрушение химических и межмолекулярных связей в растворяющихся веществах. ΔН 1 > 0; 2. Химическое взаимодействие растворителя с растворенным веществом с образованием сольватов, гидратов. ΔН 2 < 0; 3. Самопроизвольное перемешивание раствора. ΔН 3 > 0. ΔН процесса растворения = ΔН 1 + ΔН 2 + ΔН 3. ΔН процесса растворения < 0 или ΔН процесса растворения >0 Δ Gпроцесса растворения < 0, процесс протекает самопроизвольно; Δ S процесса растворения > 0 (при растворении твердого вещества в воде); Δ S процесса растворения < 0 (при растворении газов в воде).
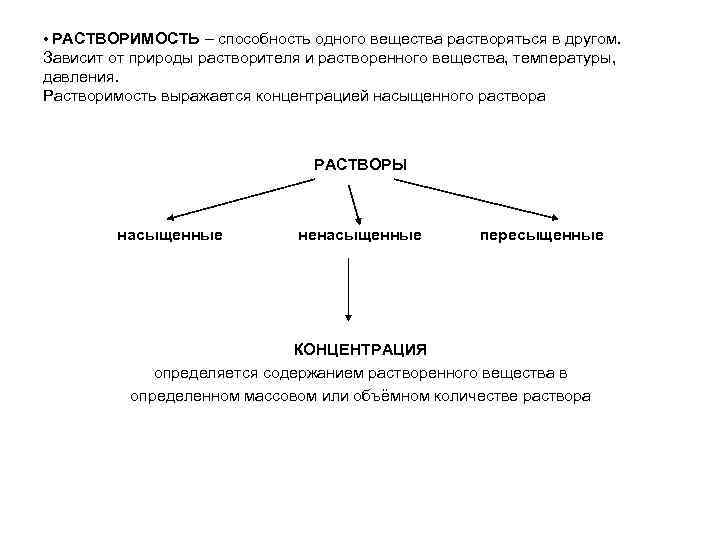
• РАСТВОРИМОСТЬ – способность одного вещества растворяться в другом. Зависит от природы растворителя и растворенного вещества, температуры, давления. Растворимость выражается концентрацией насыщенного раствора РАСТВОРЫ насыщенные ненасыщенные пересыщенные КОНЦЕНТРАЦИЯ определяется содержанием растворенного вещества в определенном массовом или объёмном количестве раствора

СПОСОБЫ ВЫРАЖЕНИЯ КОНЦЕНТРАЦИИ РАСТВОРОВ Концентрация Размерность Расчетная формула Массовая доля % Молярная моль/л Моляльная моль/ кг растворителя Мольная доля безразмерная

Общие свойства растворов с нелетучим растворенным веществом Общими ( коллигативными или коллективными) являются свойства растворов, которые не зависят от концентрации и практически не зависят от природы растворенных веществ свойства. • понижение температуры замерзания и повышение температуры кипения; • осмотическое давление. • понижение насыщенного пара растворителя над раствором; Идеальные растворы – не происходит химического взаимодействия между компонентами, силы межмолекулярного взаимодействия между компонентами одинаковы (ΔH = 0, ΔV = 0)

ДАВЛЕНИЕ ПАРА НАД РАСТВОРОМ Давление насыщенного пара над чистым растворителем Р 0 есть величина постоянная при данной температуре. Закон РАУЛЯ (1887 г ) Давление насыщенного пара Р растворителя над растворос нелетучим растворенным веществом пропорционально мольной доле растворителя Nрастворителя Р = Р 0 ·Nрастворителя. Относительное понижение давления насыщенного пара над раствором с нелетучим растворенным веществом пропорционально мольной доли растворенного вещества Nраств. в-ва
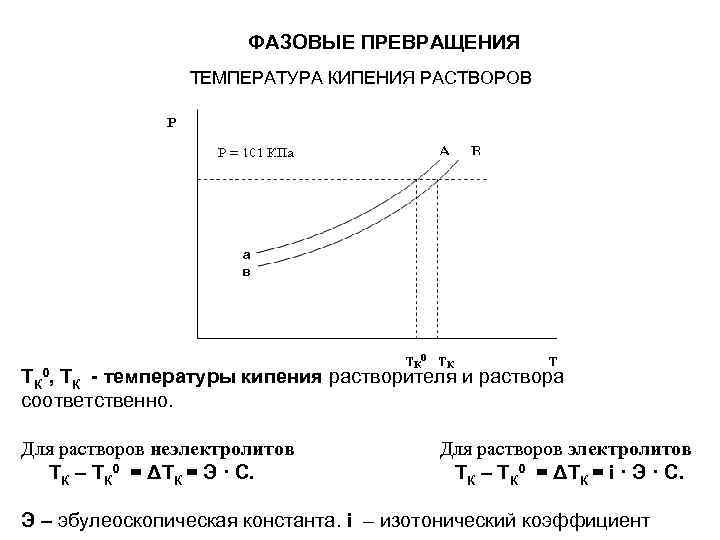
ФАЗОВЫЕ ПРЕВРАЩЕНИЯ ТЕМПЕРАТУРА КИПЕНИЯ РАСТВОРОВ а в ТК 0, ТК - температуры кипения растворителя и раствора соответственно. Для растворов неэлектролитов ТК – ТК 0 = ΔТК = Э · С. Для растворов электролитов ТК – ТК 0 = ΔТК = i · Э · С. Э – эбулеоскопическая константа. i – изотонический коэффициент
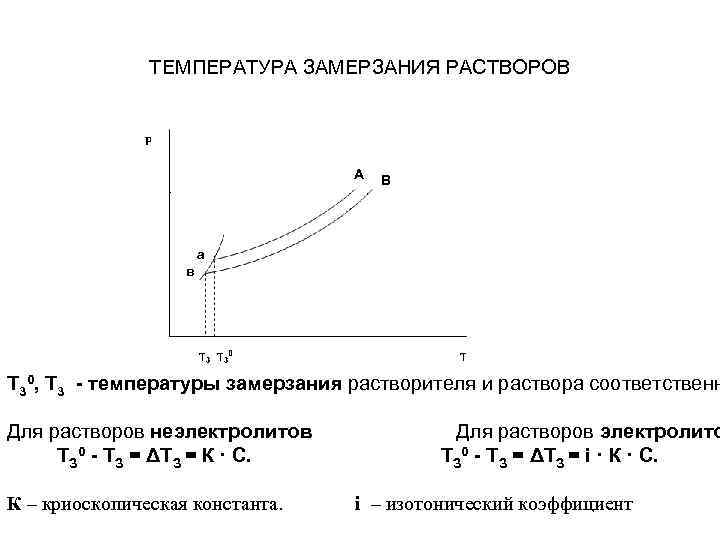
ТЕМПЕРАТУРА ЗАМЕРЗАНИЯ РАСТВОРОВ А В а в Т 30, Т 3 - температуры замерзания растворителя и раствора соответственн Для растворов неэлектролитов ТЗ 0 - ТЗ = ΔТЗ = К · С. К – криоскопическая константа. Для растворов электролито ТЗ 0 - ТЗ = ΔТЗ = i · К · С. i – изотонический коэффициент

Криоскопия • Понижение температуры замерзания раствора по сравнению с чистым растворителем ΔТЗ пропорционально моляльной концентрации раствора Данная закономерность позволяет: • Определять молярную концентрацию растворенного вещества. • Готовить атифризы, не замерзающие до необходимой температура. • Использовать химические вещества для борьбы с гололедом и наледями на дорогах, взлетных полосах аэродромов.

ОСМОТИЧЕСКОЕ ДАВЛЕНИЕ • Осмос – самопроизвольный переход растворителя через полупроницаемую мембрану, разделяющую раствор и растворитель, или два раствора с различной концентрацией растворенного вещества. • Количественно осмос характеризуется осмотическим давлением (π). • Осмотическое давление – это сила препятствующая выравниванию концентраций дальнейшему Растворы h Неэлектролитов 1 2 π = c∙R∙T Электролитов π = i∙c∙R∙T 3 Cхема осмометра: 1 – вода; 2 – раствор; 3 – полупроницаемая мембрана Осмотическое давление зависит от концентрации раствора и температуры и не зависит от природы растворенного вещества и растворителя
Лек. Растворы.ppt