Выделение и фракционирование биомолекул.ppt
- Количество слайдов: 35

Тема лекции: МЕТОДИЧЕСКИЕ ПОДХОДЫ ВЫДЕЛЕНИЯ И ФРАКЦИОНИРОВАНИЯ СУБКЛЕТОЧНЫХ СТРУКТУР И БИОМОЛЕКУЛ

Буферы, применяемые для биологических исследований, должны удовлетворять ряду требований: • • Обладать достаточной буферной емкостью в требуемом диапазоне значений р. Н Обладать высокой степенью чистоты Хорошо растворяться в воде и не проникать через биологические мембраны Обладать устойчивостью к действию ферментов и гидролизу р. Н буферных растворов должен как можно меньше зависеть от их концентрации, температуры и ионного или солевого состава среды Не оказывать токсического или ингибирующего действия Не поглощать свет в видимой и ультрафиолетовой области спектра

• Гипертонические растворы, осмотическое давление которых выше осмотического давления в растительных или животных клетках и тканях. В зависимости от функциональной, видовой и экологической специфики клеток осмотическое давление в них различно, и раствор, гипертоничный для одних клеток, может оказаться изотоничным или даже гипотоничным для других. При погружении растительных клеток в гипертонический раствор он отсасывает воду из клеток, которые уменьшаются в объёме, а затем дальнейшее сжатие прекращается и протоплазма отстаёт от клеточных стенок.

• Изотонические растворы (от изо. . . и греч. tónos — напряжение), растворы с одинаковым осмотическим давлением; в биологии и медицине — природные или искусственно приготовленные растворы с таким же осмотическим давлением, как и в содержимом животных и растительных клеток, в крови и тканевых жидкостях. В нормально функционирующих животных клетках внутриклеточное содержимое обычно изотонично внеклеточной жидкости. При сильном нарушении изотоничности растворов в растительной клетке и окружающей среде вода и растворимые вещества свободно перемещаются в клетку или обратно, что может привести к расстройству нормальных функций клетки (см. Плазмолиз, Тургор).

ФРАКЦИОНИРОВАНИЕ КЛЕТОК • Фракционирование клеток состоит из двух последовательных стадий — гомогенизации и разделения. На стадии гомогенизации структура ткани разрушается и ткань превращается в так называемый гомогенат. На второй стадии — разделении — происходит группирование отдельных компонентов гомогената по принципу общности их физических свойств, таких, как размер и плотность.

ГОМОГЕНИЗАЦИЯ Гомогениза ция (от греч. ὁμογενής — однородный) — создание устойчивой во времени однородной (гомогенной) структуры в двух- или многофазной системе путём ликвидации концентрационных микронеоднородностей, образующихся при смешивании взаимно-нерастворимых веществ (водамасло, этиловый спирт-ртуть).

СПОСОБЫ РАЗРУШЕНИЯ ТКАНЕЙ И КЛЕТОК Для разрушения клеток чаще всего применяют физические методы. Большинство животных клеток разрушается сравнительно легко, однако при разрушении растительных и бактериальных клеток зачастую приходится сталкиваться со значительными трудностями, связанными с наличием клеточных стенок. Физические методы разрушения клеток подразделяются в зависимости от того, происходит ли оно под действием сил трения между клетками и твердыми веществами (растирание клеток с твердыми материалами) или гидродинамически (разрушение клеток в жидких средах).

СПОСОБЫ РАЗРУШЕНИЯ ТКАНЕЙ И КЛЕТОК 1. Растирание клеток с твердыми материалами. В современной модификации этот метод состоит в растирании клеток с песком или абразивным порошком в ступке при помощи пестика. Этот метод применяется для разрушения животных клеток довольно редко, однако им по-прежнему пользуются для разрушения растительных и бактериальных клеток. Желательно, чтобы абразивные частицы были как можно более острыми и имели такой же размер, что и разрушаемые клетки.

СПОСОБЫ РАЗРУШЕНИЯ ТКАНЕЙ И КЛЕТОК 2. Разрушение клеток в жидких средах. Разрушение клеток, находящихся в суспензии, происходит либо при вращении лопастей или поршня (блендеры), либо при поступательном движении вверх и вниз поршня или шаров (гомогенизаторы).

Блендеры, как правило, имеют режущие лопасти, вращающиеся с большой скоростью. Количество и конструкция этих лопастей бывают разными, но все они обычно заострены под прямым углом друг к другу, а форма их обеспечивает хорошее перемешивание содержимого сосуда.

Гомогенизаторы предназначены для перемешивания, гомогенизации и диспергирования и решения научноисследовательских задач, применяемых в биохимии, микробиологии, молекулярной биологии, химии, токсикологии. Гомогенизаторы имеют следующие функциональные возможности: • гомогенизация клеток и клеточных культур, • гомогенизация макромолекул (ДНК, РНК, белки), • измельчение вещества, • гомогенизация вещества (получение однородной смеси), • получение эмульсий и суспензий, • подготовка образцов для анализа, • ультразвуковая очистка.

Sartorius Potter S Благодаря точному контролю функций, гомогенизатор может использоваться даже для изоляции клеточных ядер. В биологии клетки, биохимии и физиологии растений, прибор служит для быстрого разрушения клеток с целью последующего выделения ДНК, РНК и белков, или для приготовления препаратов клеточных органелл. Встроенная колба охлаждения, заполненная ледяной водой или подключенная к внешнему источнику охлаждения, позволяет контролировать температуру образца во время гомогенизации и замедлить разрушение термолабильных компонентов.

СПОСОБЫ РАЗРУШЕНИЯ ТКАНЕЙ И КЛЕТОК 3. Разрушение с помощью ультразвука. Ультразвуковой гомогенизатор использует плотность ультразвука высокой мощности на поверхности зондов, чтобы воздействовать на небольшие количества жидкостей ультразвуком. ВЧ-генератор преобразует сетевое напряжение частотой 50 или 60 Гц в напряжение высокой частоты 20 к. Гц. Переменное напряжение настраивается и сглаживается. Напряжение постоянного тока затем преобразуется в высокочастотное напряжение, следствием чего является постоянно высокая частота и, следовательно, также ультразвуковая мощность «прямой звук» .

УЛЬТРАЗВУКОВЫЕ ГОМОГЕНИЗАТОРЫ LABSONIC — ультразвуковые гомогенизаторы для гомогенизации клеток, тканей, макромолекул и получения дисперсных систем • разрушение клеток, бактерий, вирусов • гомогенизация образцов • эмульгирование материалов • диспергирование и перемешивание образцов • ускорение химических и биологических реакций • дегазирование образцов

СПОСОБЫ РАЗРУШЕНИЯ ТКАНЕЙ И КЛЕТОК 4. Разрушение клеток с помощью высокого давления. Этот метод применяется основном для разрушения микробных клеток. Для цели пользуются специальными прессами, например френч- прессом (French Pressure), в котором создается давление до 10, 4·107 Па.

СПОСОБЫ РАЗРУШЕНИЯ ТКАНЕЙ И КЛЕТОК 4. Прочие методы. К ним относятся: разрушение клеток методом осмотического шока, переваривание клеточных стенок ферментами, на пример лизоцимом, и сложными ферментными препаратами, вы деленными из улиток и содержащими целлюлазу, хитиназу и липазу. Для разрушения клеток некоторых видов успешно применяют замораживание и оттаивание, автолиз и обработку органическими растворителями, такими, как этилацетат и толуол.

Mikro-Dismembrator – шаровая мельница для твердых и замороженных образцов: семена растений, пигменты, волосы, ногти, кости, хрящи, замороженные ткани и клетки, минералы. Mikro-Dismembrator U – для гомогенизации различных образцов. Mikro-Dismembrator S – для максимально быстрой гомогенизации образцов, например, замороженных в жидком азоте, для диагностики раковых клеток. Преимущества: • Высокая эффективность и быстрая гомогенизация ломких, замороженных и твердых материалов; • Возможность изменения частоты перемешивания; • Возможность предварительной установки времени гомогенизации; • Повышенная безопасность – встроенный защитный кожух; • Адаптируется к конкретным задачам благодаря большому выбору емкостей из тефлона и стали от 3 до 20 мл и шариков из стекла, агата, карбида вольфрама или стали
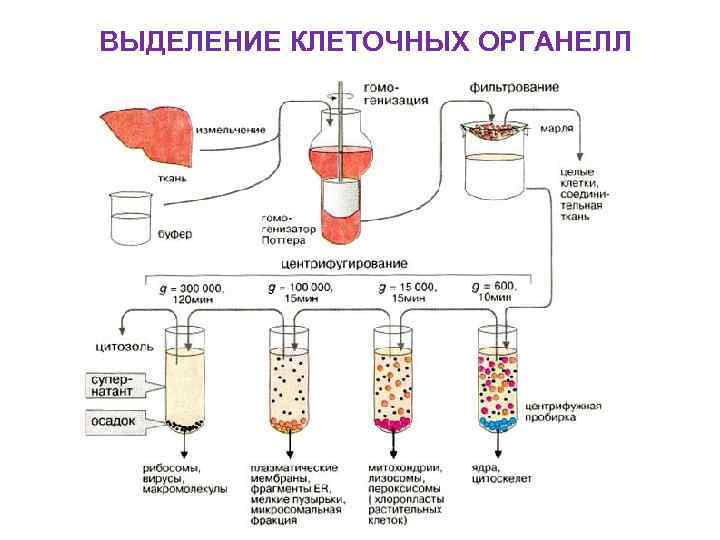
ВЫДЕЛЕНИЕ КЛЕТОЧНЫХ ОРГАНЕЛЛ
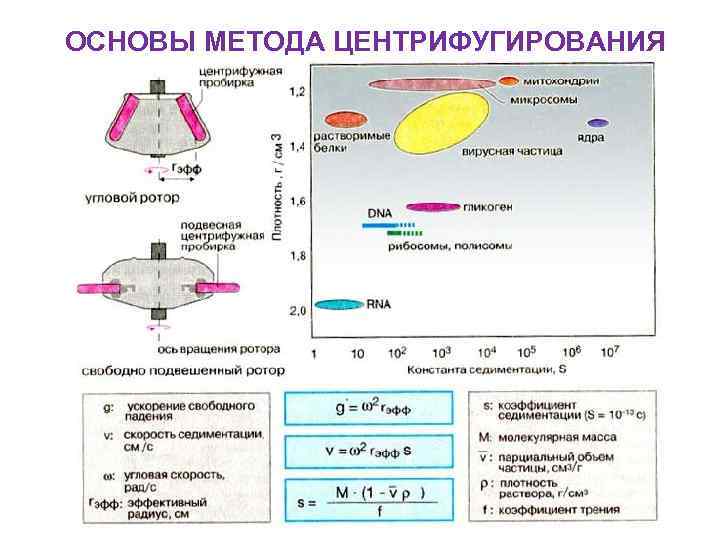
ОСНОВЫ МЕТОДА ЦЕНТРИФУГИРОВАНИЯ

СВЕДБЕРГ (Svedberg), Теодор 30 августа 1884 г. – 25 февраля 1971 г. В 1926 году присуждена Нобелевская премия по химии «за работы в области дисперсных систем» . Основные труды посвящены коллоидной химии, определению размеров и формы молекул, электрофорезу. Экспериментально подтвердил (1906) разработанную А. Эйнштейном и М. Смолуховским теорию броуновского движения. Создал метод ультрацентрифугирования для выделения коллоидных частиц из раствора, построил первые ультрацентрифуги. Внёс большой вклад в развитие физико-химии белков. В честь него названа применяемая при седиментационном анализе единица измерения отношения скорости седиментации к центробежному ускорению — сведберг. 1 сведберг = 10− 13 сек. Обозначается большой латинской буквой S (пример: белок 7 S)

ПРЕПАРАТИВНОЕ ЦЕНТРИФУГИРОВАНИЕ 1. Дифференциальное центрифугирование Этот метод основан на различиях в скоростях седиментации частиц, отличающихся друг от друга размерами и плотностью. Например, гомогенат ткани, центрифугируют при ступенчатом увеличении центробежного ускорения, которое выбирается так, чтобы на каждом этапе на дно пробирки осаждалась определенная фракция.
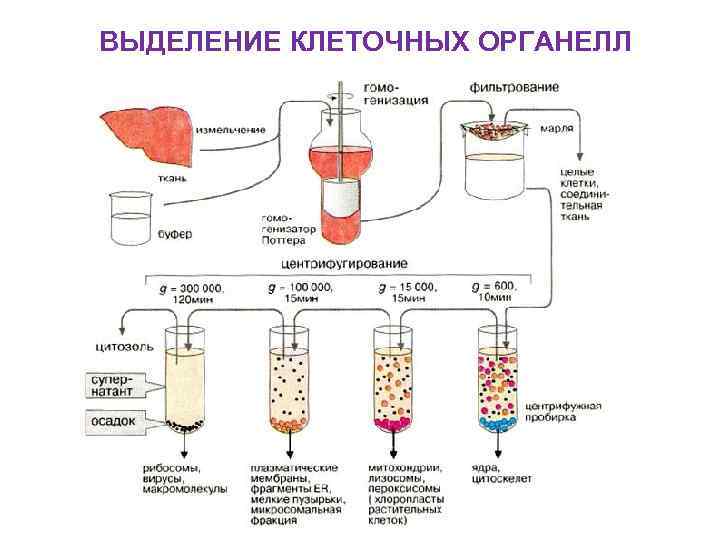
ВЫДЕЛЕНИЕ КЛЕТОЧНЫХ ОРГАНЕЛЛ

ПРЕПАРАТИВНОЕ ЦЕНТРИФУГИРОВАНИЕ 2. Зонально-скоростное центрифугирование Метод заключается в наслаивании исследуемого образца на поверхность раствора с непрерывным градиентом плотности. Образец центрифугируют до тех пор, пока частицы не распределятся вдоль градиента в виде дискретных зон или полос. Метод применяется для разделения гибридов РНК-ДНК, субъединиц рибосом и других клеточных компонентов.

ПРЕПАРАТИВНОЕ ЦЕНТРИФУГИРОВАНИЕ 3. Изопикническое центрифугирование Пробу (например ДНК, РНК или вирусы) равномерно распределяют во всем объеме раствора (обычно Cs. CI). В этом случае разделение продолжается значительно дольше, чем при зональном центрифугировании. Градиент плотности создается в процессе центрифугирования за счет седиментации и диффузии. Со временем каждая частица попадает в область, соответствующую ее собственной плавучей плотности. Центрифугирование прекращают, когда устанавливается равновесие.
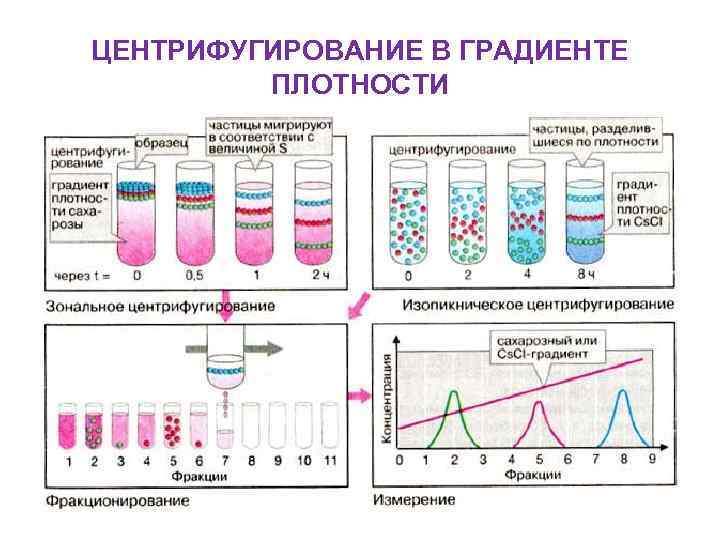
ЦЕНТРИФУГИРОВАНИЕ В ГРАДИЕНТЕ ПЛОТНОСТИ

АНАЛИТИЧЕСКОЕ ЦЕНТРИФУГИРОВАНИЕ • В биологии аналитическое центрифугирование применяется для определения молекулярных весов макромолекул, проверки чистоты получаемых образцов, а также для исследования конформационных изменений в макромолекулах. • Существует три основных метода определения молекулярных весов при помощи аналитического центрифугирования: определение скорости седиментации, метод седиментационного равновесия и метод приближения к седиментационному равновесию.
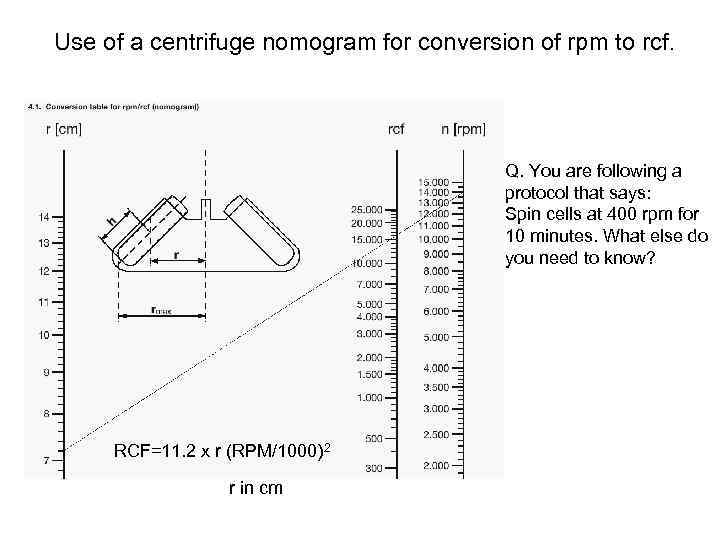
Use of a centrifuge nomogram for conversion of rpm to rcf. Q. You are following a protocol that says: Spin cells at 400 rpm for 10 minutes. What else do you need to know? RCF=11. 2 x r (RPM/1000)2 r in cm


ЦЕНТРИФУГИ Microfuge® 16 Microfuge® - серия микроцентрифуг, предназначенных для осаждения субклеточных структур, вирусов и бактерий, а также выделения нуклеиновых кислот и белков. Наличие адаптеров позволяет работать с пробирками различного объема. Использование микроцентрифуг максимально упрощает работу на этапе пробоподготовки. Максимальная скорость/ускорение: Microfuge® 16 - 14 000 об/мин; 16 163 x g Microfuge® 18 - 14 800 об/мин; 18 000 x g Максимальный объем: Microfuge® 16 - 24 x 2, 2 мл Microfuge® 18 - 24 x 1, 5/2, 0 мл Microfuge® 18 Диапазон устанавливаемый температуры: отсутствует

ЦЕНТРИФУГИ Allegra® - серия настольных центрифуг, предназначенных для осаждения субклеточных структур, разделения в градиенте плотности, дифференциального разделения нуклеиновых кислот, белков и вирусов. Максимальная скорость/ускорение: Allegra® X-12/X-12 R - 10 200 об/мин; 11 400 xg Allegra® X-22/X-22 R - 14 000 об/мин; 22 065 xg Allegra® 64 R - 30 000 об/мин; 64 400 xg Настольная многофункциональная центрифуга Allegra® X-22 Максимальный объем: Allegra® X-12/X-12 R – 4 x 750 мл Allegra® X-22/X-22 R – 4 х250 мл Allegra® 64 R – 6 х85 мл Диапазон устанавливаемый температуры: от -20 о С до +40 о С Комплектация угловыми и бакетными роторами

ЦЕНТРИФУГИ Avanti® J-30 i – центрифуга идеально подходит для субклеточного фракционирования, осаждения РНК/ДНК, выделения живых микроорганизмов. Комплектация угловыми, бакетными, проточными и зональными роторами. Наличие адаптеров позволяет работать с пробирками различного объема. Многофункциональная высокоскоростная центрифуга Avanti® J-30 i Ротор JA-30. 50 Ti Основные параметры: Максимальная скорость: от 100 до 30 000 об/мин; Максимальное ускорение: 110 500 x g; Максимальный объем: 4 000 мл; Объем образца в одном гнезде: от 1, 8 до 1000 мл Диапазон устанавливаемый температуры: от -20 о С до +40 о С Ротор JS-24. 15 Ротор JS-7. 5

ЦЕНТРИФУГИ Ультрацентрифуги серии Optima™ LP способны создавать ускорение 802 400 x g при скорости 100 000 об/мин. Ультрацентрифуги данной серии идеально подходят для научных исследований в области протеомики, геномики и клеточного анализа. Встроенный компьютер, усовершенствованное программное обеспечение и сенсорный экран позволяет проводить исследования на высоком уровне. Напольная ультрацентрифуга Optima™ L-100 ХР Ротор Type 90 Ti ПО позволяет моделировать и создавать протоколы центрифугирования, оптимизировать режимы центрифугирования, производить необходимые условия, автоматически записывать предыдущие режимы центрифугирования.
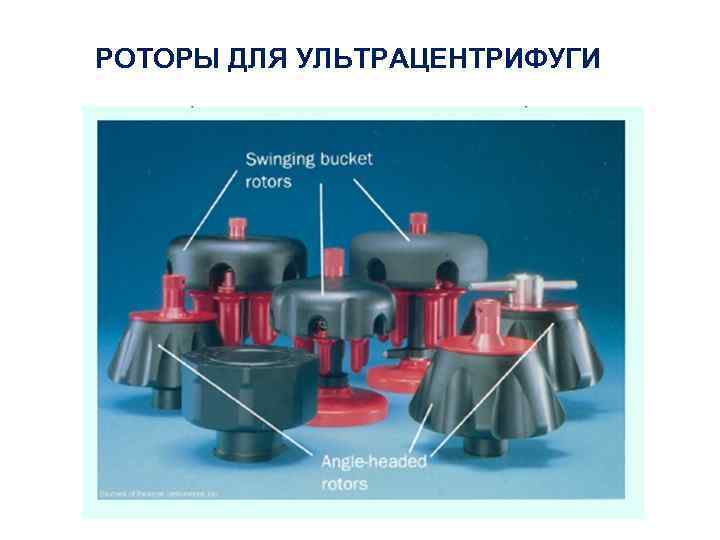
РОТОРЫ ДЛЯ УЛЬТРАЦЕНТРИФУГИ

Примеры фракционирования клеток и клеточных структур, очистки плазмидной ДНК на ультрацентрифуге

МЕТОДЫ ОЧИСТКИ И РАЗДЕЛЕНИЯ БЕЛКОВ • • Избирательной денатурацией Высаливанием Гель – фильтрацией Ультрацентрифугированием Электрофорезом Ионообменной хроматографией Аффинной хроматографией
Выделение и фракционирование биомолекул.ppt