Лекция 11 Кинетика ЗО.ppt
- Количество слайдов: 22
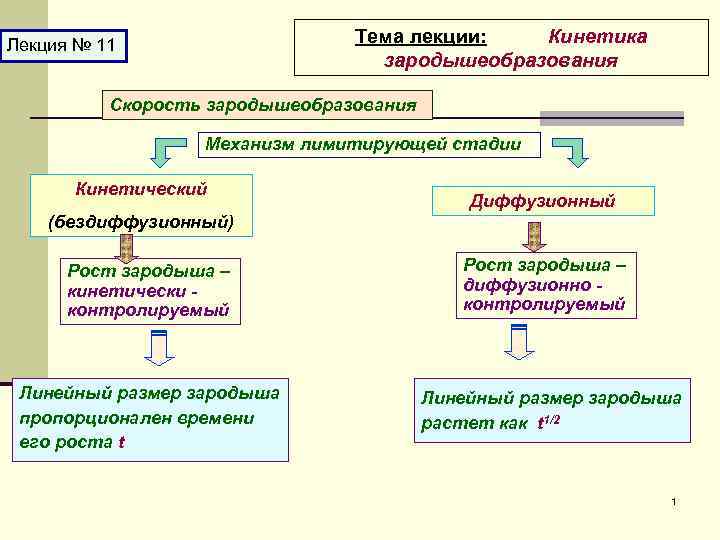
Тема лекции: Кинетика зародышеобразования Лекция № 11 Скорость зародышеобразования Механизм лимитирующей стадии Кинетический Диффузионный (бездиффузионный) Рост зародыша – кинетически контролируемый Линейный размер зародыша пропорционален времени его роста t Рост зародыша – диффузионно контролируемый Линейный размер зародыша растет как t 1/2 1
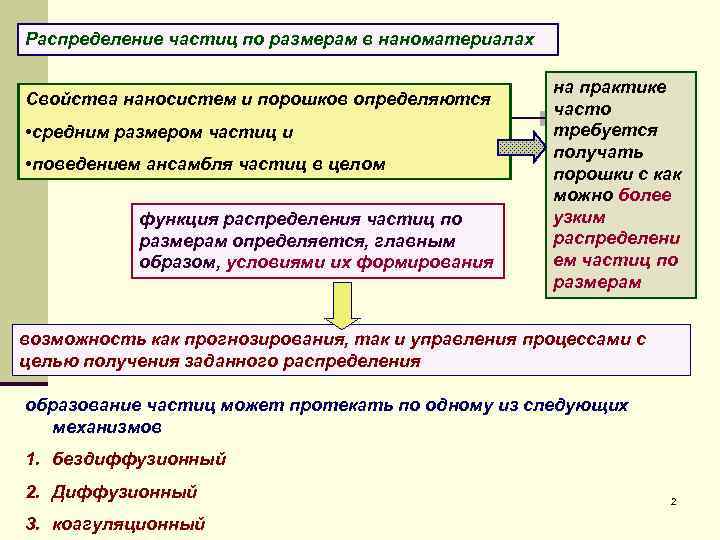
Распределение частиц по размерам в наноматериалах Свойства наносистем и порошков определяются • средним размером частиц и • поведением ансамбля частиц в целом функция распределения частиц по размерам определяется, главным образом, условиями их формирования на практике часто требуется получать порошки с как можно более узким распределени ем частиц по размерам возможность как прогнозирования, так и управления процессами с целью получения заданного распределения образование частиц может протекать по одному из следующих механизмов 1. бездиффузионный 2. Диффузионный 3. коагуляционный 2

- реализуется в том случае, когда скорость роста частицы определяется процессами на границе раздела фаз (адсорбцией, гетерогенной химической реакцией, растворением и т. д. ) линейные размеры образующейся фазы пропорциональны продолжительности ее роста для поддержания роста частиц требуется перенос на значительные расстояния атомов различных компонентов Рост частицы пропорционален скорости диффузии атомов к поверхности формирующегося материала. Радиус частицы пропорционален корню квадратному из времени роста - связан со столкновениями друг с другом частиц различных размеров, сопровождающимися их слипанием может сопровождаться быстрой рекристаллизацией или слиянием по 3 механизму вязкого течения (подобно жидким каплям) - коалесценцией
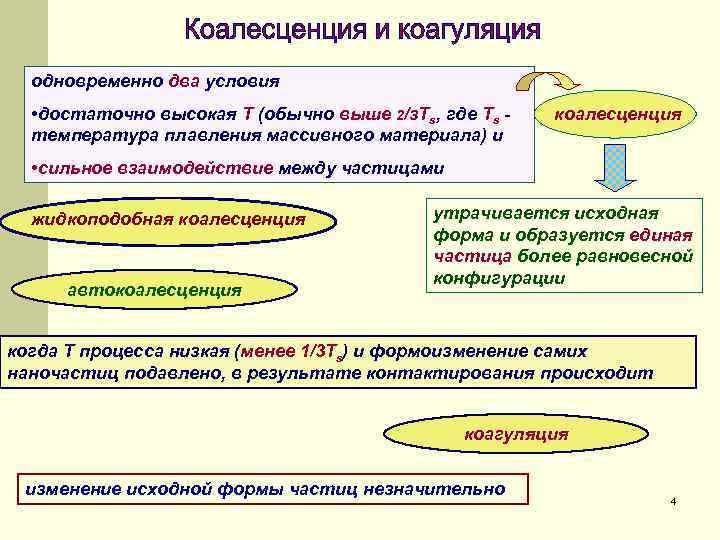
одновременно два условия • достаточно высокая Т (обычно выше 2/з. Тs, где Ts температура плавления массивного материала) и коалесценция • сильное взаимодействие между частицами жидкоподобная коалесценция автокоалесценция утрачивается исходная форма и образуется единая частица более равновесной конфигурации когда Т процесса низкая (менее 1/3 Тs) и формоизменение самих наночастиц подавлено, в результате контактирования происходит коагуляция изменение исходной формы частиц незначительно 4
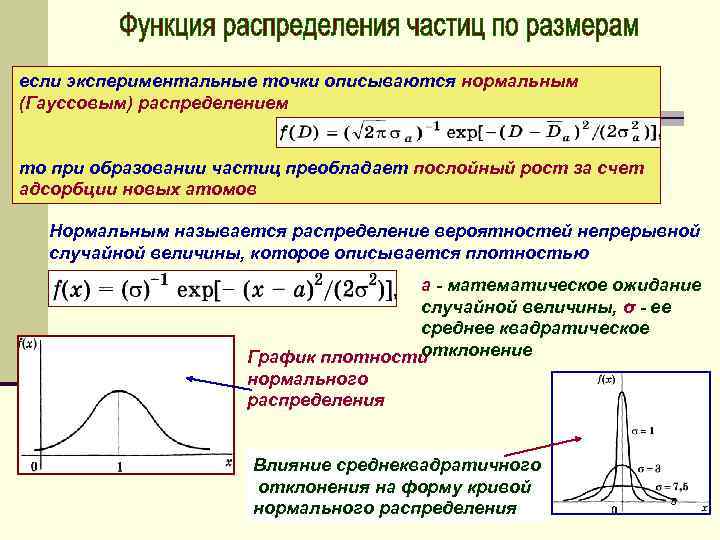
если экспериментальные точки описываются нормальным (Гауссовым) распределением то при образовании частиц преобладает послойный рост за счет адсорбции новых атомов Нормальным называется распределение вероятностей непрерывной случайной величины, которое описывается плотностью а - математическое ожидание случайной величины, σ - ее среднее квадратическое отклонение График плотности нормального распределения Влияние среднеквадратичного отклонения на форму кривой нормального распределения 5

Если при образовании частиц преобладает процесс коагуляции на всех стадиях роста, то на экспериментальной кривой будет длинный «хвост» в сторону больших размеров Подобная зависимость описывается логарифмическинормальным законом где D – среднеарифметический диаметр текущий диаметр среднегеометрический диаметр стандартное арифметическое отклонение σg - стандартное геометрическое отклонение На практике чаще всего распределение по размерам есть нечто среднее между этими двумя законами 6

нормальное распределение характерно для частиц с размером < 10 нм вероятность логарифмически-нормального распределения выше для частиц с большим и средним размером распределение промежуточной формы наиболее вероятно для всех частиц, кроме мелких хорошо описываются нормальным распределением по размерам гистограммы, полученные для металлических наночастиц, выращенных химическим методом Наночастицы, полученные в плазмохимических процессах, могут иметь логарифмическинормальное распределение Коагуляция как механизм роста играет большую роль для образцов с большим и средним размером частиц 7
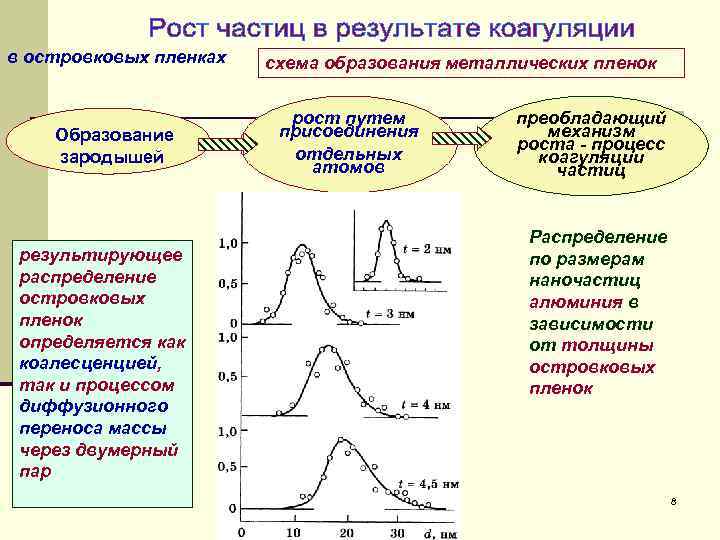
в островковых пленках Образование зародышей результирующее распределение островковых пленок определяется как коалесценцией, так и процессом диффузионного переноса массы через двумерный пар схема образования металлических пленок рост путем присоединения отдельных атомов преобладающий механизм роста - процесс коагуляции частиц Распределение по размерам наночастиц алюминия в зависимости от толщины островковых пленок 8
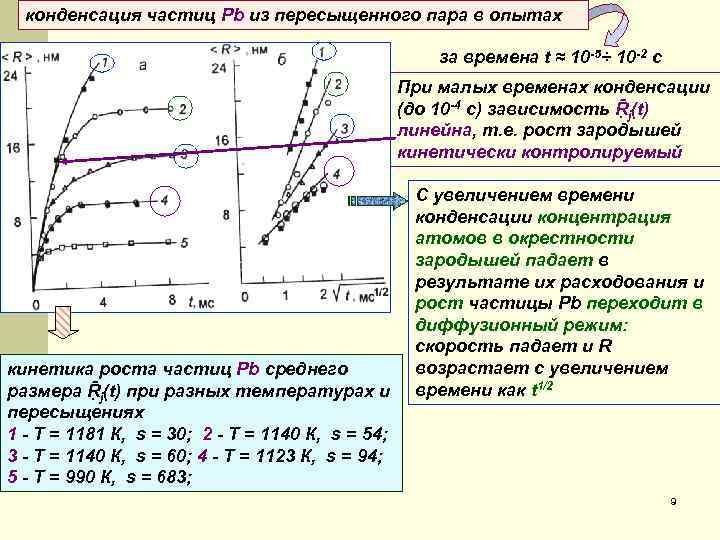
конденсация частиц Pb из пересыщенного пара в опытах за времена t ≈ 10 -5÷ 10 -2 c При малых временах конденсации (до 10 -4 с) зависимость Ṝj(t) линейна, т. е. рост зародышей кинетически контролируемый кинетика роста частиц Pb среднего размера Ṝj(t) при разных температурах и пересыщениях 1 - Т = 1181 К, s = 30; 2 - Т = 1140 К, s = 54; 3 - Т = 1140 К, s = 60; 4 - Т = 1123 К, s = 94; 5 - Т = 990 К, s = 683; С увеличением времени конденсации концентрация атомов в окрестности зародышей падает в результате их расходования и рост частицы Pb переходит в диффузионный режим: скорость падает и R возрастает с увеличением времени как t 1/2 9

Диффузионный режим Для того, чтобы атомы могли адсорбироваться и присоединиться к зародышу, они из объема жидкой или газовой фазы должны продиффундировать к его поверхности внешняя диффузия Согласно закону Фика скорость диффузии пропорциональна градиенту концентрации и величине поверхности: где D – коэффициент диффузии, м 2/с; S – поверхность, через (на) которую осуществляется диффузия; x – координата, м; c – концентрация, моль/м 3; dc/dx – градиент концентрации в направлении диффузии вследствие того с ростом зародыша увеличивается его поверхность, и, следовательно, пропорционально ей увеличивается протяженность диффузионного поля, линейный размер формирующегося ансамбля атомов возрастает как t 1/2 Возможны • промежуточные кинетические режимы образования и роста зародышей новой фазы, а также 10 • смена одного режима другим в ходе конденсации

О предэкспонециальном множителе в уравнении скорости реакции Вид предэкспоненциального множителя В в уравнении зависит от характера модели формирования новой фазы Поверхность сферического зародыша с радиусом Rj, кр. , будет 4π Rj, кр. 2. Вероятность конденсации молекул пара принимается одинаковой для всех кластеров и равной Не все атомы, поступившие на поверхность зародыша, на ней остаются, ε где число соударений молекул (атомов) массой m с единичной площадью поверхности в единицу времени при давлении пара р и температуре Т; k. В - постоянная Больцмана; ε – эффективный «коэффициент конденсации» Итак, 11

О предэкспонециальном множителе в уравнении скорости реакции Принимая, что для идеального газа Р = ni k. БТ, и выражая Δμ через пересыщение (Δμ = k. БТ lns), где s = P/Po – пересыщение, Ро – давление насыщенных паров), получаем : Множитель В пропорционален квадрату плотности пара ni (число атомов в 1 см 3) и обратно пропорционален (ln s)2 Для описания образования кристаллических насыщенного пара в результате предэкспоненциальный множитель В преобразуем зародышей из переохлаждения 12

О предэкспонециальном множителе в уравнении скорости роста З Кристаллизация из пара Полагаем, что кристаллический зародыш, состоящий из j атомов и имеющий кубическую решетку с параметрами а и γ ≈ ΔН/6 а 2, где ΔН – теплота испарения, находится в равновесии с собственными насыщенными парами с давлением Ро: Член в левой части уравнения представляет собой скорость адсорбции атомов из гомогенной газовой фазы на поверхность зародыша, а в правой части - скорость десорбции с поверхности в расчете на один атом (ν – частота колебания адсорбированного атома нормально к поверхности) и Р ≈Ро Запишем Δμ через переохлаждение пара (Δμ = ΔНΔТ/Т) и получим следующее выражение для В: Можно показать, что скорость образования зародышей в случае кристаллизации из насыщенного пара в режиме переохлаждения существенно выше, чем при конденсации из пересыщенного пара 13

Скорость ЗО в конденсированных жидких средах пропорциональна квадрату плотности растворенных атомов и их потоку на поверхность формирующегося зародыша В конденсированной фазе направленное перемещение атомов является активируемым процессом Т. к. требуется преодоление потенциальных барьеров, связанных с разрывом или изменением характера связей ближнего порядка со средой при переходе в зародыш 2 1 В случае растворов – это диффузия атомов к поверхности зародыша и их последующее встраивание в зародыш Для расплава – это перестройка ближнего порядка при переходе атома в зародыш, энергия активации которой есть энергия активации вязкого течения, при котором относительное смещение атомов вид предэкспоненциального множителя В в выражении для скорости образования зародышей одинаков Для сферического зародыша энергия Гиббса активации переноса между двумя равновесными положениями, отстоящими друг от друга 14 на расстоянии а

Скорость ЗО в конденсированных жидких средах В случае растворов ΔGтр включает в себя энергии активации диффузии и перестройки, связанной с переходом атома из среды (раствора) в зародыш процесс малоизучен, можно оценить лишь энергию активации для встраивания атомов в решетку макроскопического кристалла Значение ΔGтр лежит в интервале ΔНпл - ΔНисп вещества и может составлять от десятков до сотен к. Дж/моль для оценки величины предэкспоненциального множителя В применительно к скорости формирования зародышей из раствора, преобразуем выражение Для кристаллизации Fe из раствора (например, при восстановлении водных растворов солей, T ≈ 300 К ) В ≈ 1021 см-3. с-1. При T≈373 К В ≈ 2. 1024 см-3. с-1 Таким образом, скорости кристаллизации из раствора сравнимы со скоростями конденсации из насыщенного пара в режиме 15 переохлаждения

Зародышеобразование из расплава Выражение для В в случае зародышеобразования из расплава в результате переохлаждения можно записать в виде где ΔT- переохлаждение, ΔНпл /Т 0 - энтропия плавления Значения ΔGтр в расплавах значительно ниже, чем в растворах, и по оценкам ΔGтр ≈ (0, 33 0, 5) ΔНпл. Так, для кристаллизации Fe из расплава при Тпл = 1810 К , ΔT = 295 К; получаем В ≈ 1, 7/1039 см-3 -с-1 Отсюда следует, что т. е. скорости формирования зародышей из расплава в режиме переохлаждения значительно выше, чем из раствора, что обусловлено как • более высокой концентрацией атомов в расплаве, так и • более низкими значениями ΔGтр 16

Скорость гетерогенного зародышеобразования Зарождение новой фазы на регулярной поверхности возможно вокруг любого из адсорбированных статистически атомов с удельной плотностью n. S (атом/см 2) При этом выражение для удельной скорости зародышеобразования Is аналогично уравнению В случае, когда новые атомы поступают к зародышу за счет потока из объема среды , выражение для Bs [атом/(см 2 с)] приобретает вид где - площадь шарового сегмента 17

Если зарождение новой фазы происходит в конденсированной среде (раствор, расплав), то, очевидно, поток следует заменить на : Когда зародыш формируется из потока адсорбированных атомов В реальных ситуациях зарождение новой фазы происходит на поверхностных дефектах - трещинах, сколах, ступенях роста, областях выхода дислокаций и т. п. , которые являются центрами зарождения При этом энергия образования зародышей на этих центрах ΔGтр* может существенно понижаться по сравнению с регулярными областями поверхности Тогда в выражении следует заменить n на n* - удельную плотность потенциальных центров зарождения, а ΔGтр на ΔGтр*. 18

Для гетерогенного зарождения произведение BSSΣ, где SΣ -суммарная площадь поверхностей (стенок сосуда, посторонних частиц, подложек, площадь поверхности пор), может быть меньше произведения BSVΣ в случае гомогенного зародышеобразования, где VΣ - суммарный объем системы В то же время уменьшение входящей в экспоненциальный множитель энергии образования зародышей на достаточно сильно адсорбционноактивных поверхностях приводит к повышению вероятности зарождения, и поэтому скорость зарождения на поверхности будет выше, чем в гомогенном случае, из-за значительно более сильного влияния на скорость ЗО экспоненциального члена, чем предэкспоненциального множителя Рассмотренные особенности скорости образования новой фазы на нерегулярной поверхности в равной мере относятся и к ЗО в реальной твердой фазе, где также могут присутствовать как n макродефекты, например трещины, так и nмикродефекты, связанные с нарушением трансляционной симметрии кристаллической решетки (вакансии, дислокации, инородные примеси), 19 способствующие понижению энергии образования зародышей.

Скорость зародышеобразования при электрокристаллизации металлов В отличие от кристаллизации из газовой фазы частота присоединения и отрыва атомов от кластера определяется энергией активации электрохимических реакций разряда - ионизации и зависит от кривизны поверхности кластера При стадийности разряда многовалентных ионов скорость ЗО может изменяться в зависимости от соотношения скоростей отдельных стадий электрохимических реакций и массопереноса Доставка «строительных элементов» при росте, а в некоторых случаях и при зарождении должна играть более существенную роль поскольку Скорость доставки ионов к поверхности основы в условиях электрокристаллизации меньше, чем при росте из пара 20

Скорость ЗО в процессе электрокристаллизации В рамках классических представлений вид зависимости скорости образования зародышей критического размера в процессе электрокристаллизации аналогичен выражению где ; ; qо - плотность потока атомов; Sкр - поверхность критического зародыша; jкp - число атомов в критическом зародыше; η - перенапряжение; Таким образом, в условиях электроосаждения металлов изменение электрохимического потенциала системы и пересыщение связаны непосредственно с измеряемым перенапряжением Зависимость скорости ЗО кристаллов от перенапряжения при электрокристаллизации многократно экспериментально проверялась на ряде модельных систем (осаждение Ag, Hg, Cd, Pb на Pt). 21

Эксперименты Получено хорошее согласие опытных данных с предсказаниями по уравнению 1 зарождение кристаллов Pb протекает с большей скоростью, чем Ag, Т. к. для металла с большей степенью окисления работа образования критического зародыша должна быть меньше Уменьшению величины также способствует то обстоятельство, что γРЬ < γAg. Полулогарифмическая анаморфоза зависимости (1) 1 - Ag из I н. раствора Ag. NO 3; 2 - Pb из 2 н. раствора Pb(N 03)2 Линейность зависимости [ ln. Wкр, η-2 ] выполняется в узком интервале изменения потенциалов, т. к. в условиях электрокристаллизации поток вещества qо зависит от кинетики электрохимической реакции и 22 перенапряжения катода
Лекция 11 Кинетика ЗО.ppt