 Тема лекции № 1: Термодинамика химического равновесия и растворов.
Тема лекции № 1: Термодинамика химического равновесия и растворов.
 Химическая термодинамика Изолированная система m=0 Е = 0 Закрытая система m=0 Е ≠ 0 Открытая система m≠ 0 Е ≠ 0
Химическая термодинамика Изолированная система m=0 Е = 0 Закрытая система m=0 Е ≠ 0 Открытая система m≠ 0 Е ≠ 0
 Химическая термодинамика l l l l Функциями состояния являются следующие величины: Температура (Т) Объем (V) Давление (P) Внутренняя энергия (U) Энтальпия (H) Энтропия (S) Свободная энергия Гиббса (G)
Химическая термодинамика l l l l Функциями состояния являются следующие величины: Температура (Т) Объем (V) Давление (P) Внутренняя энергия (U) Энтальпия (H) Энтропия (S) Свободная энергия Гиббса (G)
 Химическая термодинамика Математическое выражение первого начала термодинамики Q = U + W
Химическая термодинамика Математическое выражение первого начала термодинамики Q = U + W
 Химическая термодинамика При изохорном процессе V = const, тогда V = 0, W = Р×∆V, то W = 0 Уравнение I начала термодинамики принимает вид: QV = UV
Химическая термодинамика При изохорном процессе V = const, тогда V = 0, W = Р×∆V, то W = 0 Уравнение I начала термодинамики принимает вид: QV = UV
 Химическая термодинамика При изобарном процессе P = const Н = U + PV Qp = H 2 – H 1 Qp = H
Химическая термодинамика При изобарном процессе P = const Н = U + PV Qp = H 2 – H 1 Qp = H
 Химическая термодинамика I закон термодинамики для изобарных процессов ∆Нр = ∆U + P∆V
Химическая термодинамика I закон термодинамики для изобарных процессов ∆Нр = ∆U + P∆V
 Химическая термодинамика ЗАКОН ГЕССА Тепловой эффект реакции при постоянном объеме или давлении не зависит от пути процесса, а зависит от начального и конечного состояния системы
Химическая термодинамика ЗАКОН ГЕССА Тепловой эффект реакции при постоянном объеме или давлении не зависит от пути процесса, а зависит от начального и конечного состояния системы
 Химическая термодинамика Стандартные условия Т = 298 К Р = 1, 013× 105 Н/м 2
Химическая термодинамика Стандартные условия Т = 298 К Р = 1, 013× 105 Н/м 2
 Химическая термодинамика Первое следствие из закона Гесса: H 0 = n H 0298 обр. пр. р. - n H 0298 обр. исх. в-в.
Химическая термодинамика Первое следствие из закона Гесса: H 0 = n H 0298 обр. пр. р. - n H 0298 обр. исх. в-в.
 Химическая термодинамика Второе следствие из закона Гесса H 0 сгор = n H 0 298 сгор. исх. в-в. - n H 0298 сгор. пр. р.
Химическая термодинамика Второе следствие из закона Гесса H 0 сгор = n H 0 298 сгор. исх. в-в. - n H 0298 сгор. пр. р.
 Химическая термодинамика Интегральная форма закона Кирхгофа ∆НТ 2= ∆НТ 1+ ∆Ср(Т 2 -Т 1) ∆UТ 2= ∆UТ 1+ ∆Сv(Т 2 -Т 1) Cр0=а. Т+в. Т 2+с. Т 3
Химическая термодинамика Интегральная форма закона Кирхгофа ∆НТ 2= ∆НТ 1+ ∆Ср(Т 2 -Т 1) ∆UТ 2= ∆UТ 1+ ∆Сv(Т 2 -Т 1) Cр0=а. Т+в. Т 2+с. Т 3
 ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ. АНАЛИТИЧЕСКОЕ ВЫРАЖЕНИЕ 2 -го НАЧАЛА ТЕРМОДИНАМИКИ
ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ. АНАЛИТИЧЕСКОЕ ВЫРАЖЕНИЕ 2 -го НАЧАЛА ТЕРМОДИНАМИКИ
![[S] = Дж/К, [ΔS] = Дж/моль×К [S] = Дж/К, [ΔS] = Дж/моль×К](https://present5.com/presentation/33901673_128684221/image-14.jpg) [S] = Дж/К, [ΔS] = Дж/моль×К
[S] = Дж/К, [ΔS] = Дж/моль×К
 Условие самопроизвольного протекания процессов в изолированной системе ΔS > 0
Условие самопроизвольного протекания процессов в изолированной системе ΔS > 0
 МАТЕМАТИЧЕСКОЕ ВЫРАЖЕНИЕ 2 -ГО ЗАКОНА ТЕРМОДИНАМИКИ ΔS ≥ 0
МАТЕМАТИЧЕСКОЕ ВЫРАЖЕНИЕ 2 -ГО ЗАКОНА ТЕРМОДИНАМИКИ ΔS ≥ 0
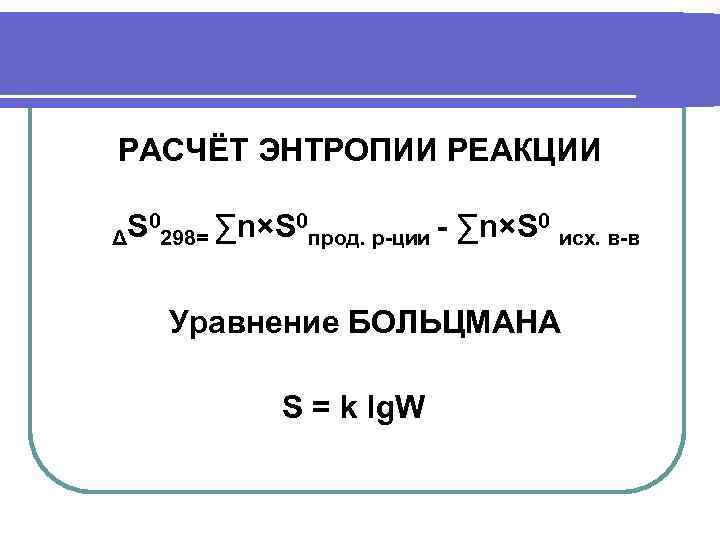 РАСЧЁТ ЭНТРОПИИ РЕАКЦИИ S 0298= ∑n×S 0 прод. р-ции - ∑n×S 0 исх. в-в Δ Уравнение БОЛЬЦМАНА S = k lg. W
РАСЧЁТ ЭНТРОПИИ РЕАКЦИИ S 0298= ∑n×S 0 прод. р-ции - ∑n×S 0 исх. в-в Δ Уравнение БОЛЬЦМАНА S = k lg. W
 Свободная энергия Гельмгольца F = U –TS
Свободная энергия Гельмгольца F = U –TS
 l УРАВНЕНИЕ ГИББСА ΔG 0 = ΔH 0 – TΔS 0
l УРАВНЕНИЕ ГИББСА ΔG 0 = ΔH 0 – TΔS 0
 -∆F = Амах -∆G 0 = Амах - Р∆V = Амах
-∆F = Амах -∆G 0 = Амах - Р∆V = Амах
 Энергия Гиббса Условие возможности протекания реакции в прямом направлении без затраты энергии ΔG < 0 ΔG< 0, то реакция неосуществима в прямом направлении ΔG = 0, то система находится в состоянии равновесия
Энергия Гиббса Условие возможности протекания реакции в прямом направлении без затраты энергии ΔG < 0 ΔG< 0, то реакция неосуществима в прямом направлении ΔG = 0, то система находится в состоянии равновесия
 Расчёт изменения свободной энергии Гиббса G 0 = n G 0 298 обр. пр. р. - n G 0 298 обр. исх. в-в.
Расчёт изменения свободной энергии Гиббса G 0 = n G 0 298 обр. пр. р. - n G 0 298 обр. исх. в-в.
 АНАЛИЗ УРАВНЕНИЯ ГИББСА 1) ΔG 0 < 0, если ΔН 0 < 0, ΔS 0 > 0 2) ΔG 0 < 0, если ΔН 0<0, ΔS<0 при низких температурах и ΔS – очень мало |ΔH|>|ТΔS| 3)ΔG 0 < 0, если ΔН 0 > 0, ΔS 0 > 0 - при высоких температурах, |ТΔS |>|ΔH|
АНАЛИЗ УРАВНЕНИЯ ГИББСА 1) ΔG 0 < 0, если ΔН 0 < 0, ΔS 0 > 0 2) ΔG 0 < 0, если ΔН 0<0, ΔS<0 при низких температурах и ΔS – очень мало |ΔH|>|ТΔS| 3)ΔG 0 < 0, если ΔН 0 > 0, ΔS 0 > 0 - при высоких температурах, |ТΔS |>|ΔH|
![ХИМИЧЕСКОЕ РАВНОВЕСИЕ а. А + в. В ↔ с. С + d. D [C], ХИМИЧЕСКОЕ РАВНОВЕСИЕ а. А + в. В ↔ с. С + d. D [C],](https://present5.com/presentation/33901673_128684221/image-24.jpg) ХИМИЧЕСКОЕ РАВНОВЕСИЕ а. А + в. В ↔ с. С + d. D [C], [D], [A], [B] – равновесные концентрации веществ, моль/л c, d, a, b – стехиометрические коэффициенты реакции
ХИМИЧЕСКОЕ РАВНОВЕСИЕ а. А + в. В ↔ с. С + d. D [C], [D], [A], [B] – равновесные концентрации веществ, моль/л c, d, a, b – стехиометрические коэффициенты реакции
 Выражение константы равновесия через парциальное давление
Выражение константы равновесия через парциальное давление
 Изобара химической реакции Уравнение изобары химической реакции после интегрирования
Изобара химической реакции Уравнение изобары химической реакции после интегрирования
 Изохора химической реакции
Изохора химической реакции