антитела.ppt
- Количество слайдов: 22

Тема лекції: Будова і властивості антитіл Лич Інна Валентинівна

МЕТА ЛЕКЦІЇ: Ознайомитися з будовою молекул імуноглобулінів і вивчити їх основні властивості та функціональні особливості ПЛАН ЛЕКЦІЇ: 1. Загальна структура антитіл. 2. Фрагменти імуноглобулінів. 3. Будова різних класів імуноглобулінів та їх функції.

Антитіла (АТ) – це особливі розчинні білки з певною біологічною структурою (імуноглобуліни), які присутні в сироватці крові і інших біологічних рідинах, які організм виробляє для зв'язування різноманітних антигенів. Всі без виключення АТ належать до одного типу білкових молекул, які мають глобулярну вторинну структуру, тому цей тип молекул називається імуноглобулін. Тобто всі АТ – імуноглобуліни. Міжнародна абрівіатура імуноглобулінів – Ig. Заглавна літера поряд з Ig означає один із п'яти класів імуноглобулінів, які існують у ссавців – M, G, A, E, D. Наступна арабська цифра означає підклас. Підкласи існують тільки у імуноглобулінів класів G (Ig. G 1, Ig. G 2, Ig. G 3, Ig. G 4, Ig. G 5) та А (Ig. А 1, Ig. А 2). Класи і підкласи називаються ізотипами імуноглобулінів. Таким чином, ізотипів 9.
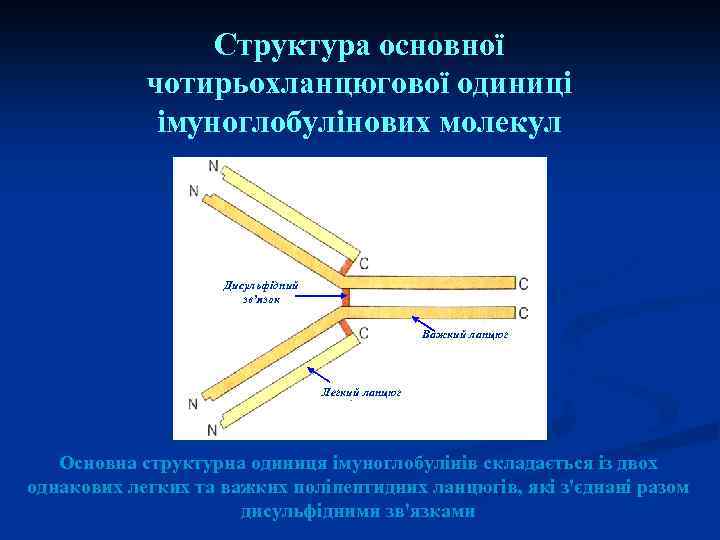
Структура основної чотирьохланцюгової одиниці імуноглобулінових молекул Дисульфідний зв’язок Важкий ланцюг Легкий ланцюг Основна структурна одиниця імуноглобулінів складається із двох однакових легких та важких поліпептидних ланцюгів, які з'єднані разом дисульфідними зв'язками

Молекула антитіла складається з двох типів поліпептидних ланцюгів: важких (Н – hight) та легких (L – light). Важкі ланцюги поділяються на класи: α (альфа), μ (мю), γ (гамма), δ (дельта), ε (епсілон) і відповідно розрізняють п'ять класів Ig. M, Ig. G, Ig. A, Ig. E, Ig. D. Для легких ланцюгів виділяють типи k – каппа і λ – лямбда. Легкий та важкий ланцюг має G-кінець та N-кінець (С- СОО- - залишок карбоксильної групи АК, N-кінець залишок аміногрупи NН 3+). Легкі ланцюги приєднані до N-кінця важких ланцюгів, С-кінець важких ланцюгів формує Fcфрагмент молекули Ig.
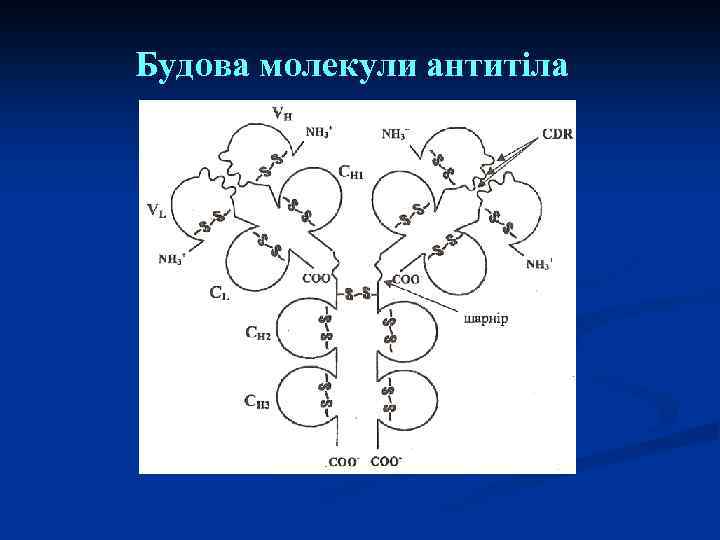
Будова молекули антитіла

Різноманітність будови гіперваріабельних ділянок молекули імуноглобуліну
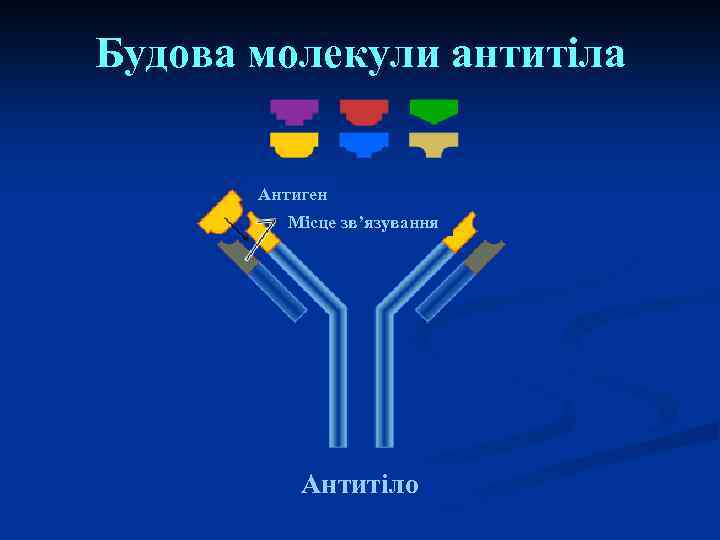
Будова молекули антитіла Антиген Місце зв’язування Антитіло

Протеолітичні фрагменти молекули антитіла
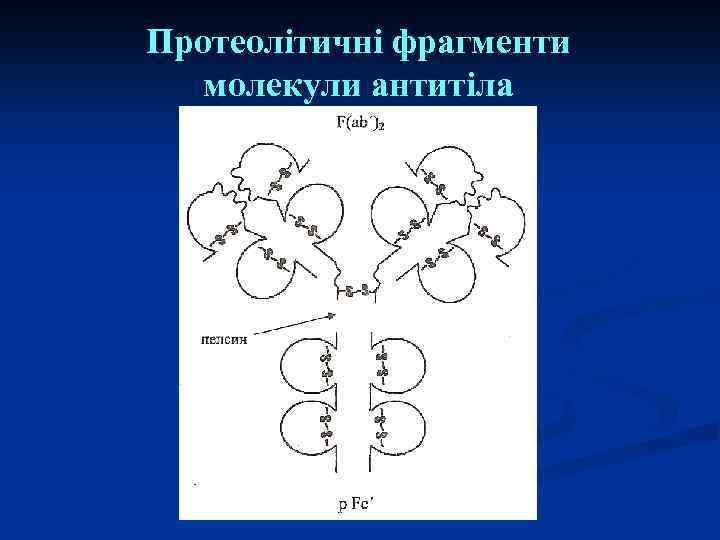
Протеолітичні фрагменти молекули антитіла
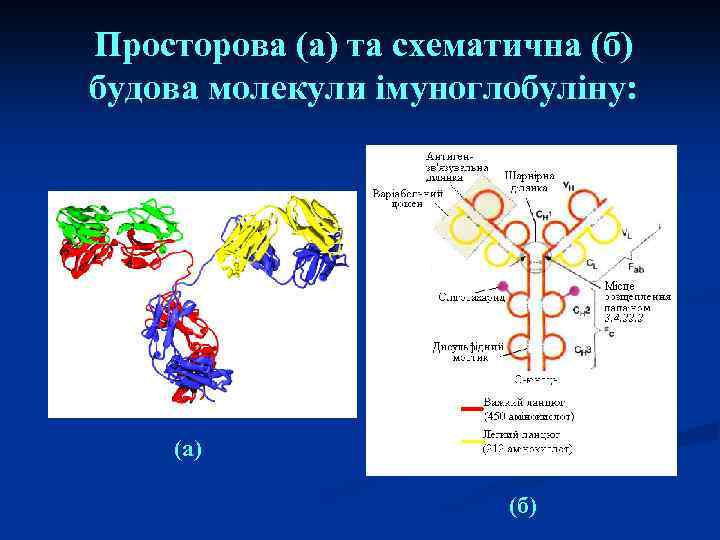
Просторова (а) та схематична (б) будова молекули імуноглобуліну: (а) (б)

Будова різних класів імуноглобулінів та їх функції - Ig M Активовані В-Лф в першу чергу секретують Ig M складають приблизно 7% сироваткових Ig. Це досить крупні молекули, які склдаються з 5 звичайних мономерних одиниць, зв’язаних jланцюгом. Завдяки такій конструкції Ig M – пентамер має 10 активних центрів і міцно зв'язується з АГ, які несуть епітопні повтори. Такі АГ є на поверхні більшості бактерій і вірусів, тому Ig M є першим бар'єром на шліху інфекції. Хоча Ig M має невисоку спорідненість до АГ, завдяки олігомерності легко викликає аглютинацію мікробних клітин, що сприяє їх знищенню макрофагами. Так звані “нормальні антитіла”, присутні в крові здорових індивидів, теж є здебільшого Ig M. Це антитіла екстремального імунного захисту. Важливо! Якщо в сироватці крові ідентифікують велику кількість Ig M проти того чи іншого захворювання – це гостра фаза інфекційного процесу.

Структура Ig. М людини J-ланцюг Важкі ланцюги Ig. М просторово звертаються з утворенням п’яти доменів

Будова різних класів імуноглобулінів та їх функції - Ig G – це головний імуноглобулін сироватки крові і тканинних рідин. Приблизно 75% сироваткових імуноглобулінів - Ig G. Більшість антитіл при вторинній імунній відповіді – це Ig G. Вони володіють різними ефекторними функціями: підсилення фагоцитарних реакцій, активація комплементу, активний транспорт через плаценту, нейтралізація мікроорганізмів та їх токсинів. Цьому сприяє тривалий (близько 20 діб) період напіврозпаду (для імуноглобілінів інших класів – 2 -10 діб). Підкласи Ig G відрізняються за своїми властивостями (Ig G 1, Ig G 2, Ig G 3, Ig G 4, Ig G 5). Класичним носієм властивостей антитіл є Ig G 1, на долю якого припадає 50 – 70% від всієї кількості сироваткових Ig. Важливо! Якщо в сироватці крові ідентифікують велику кількість Ig G проти того чи іншого захворювання – це хронічна фаза інфекційного процесу.
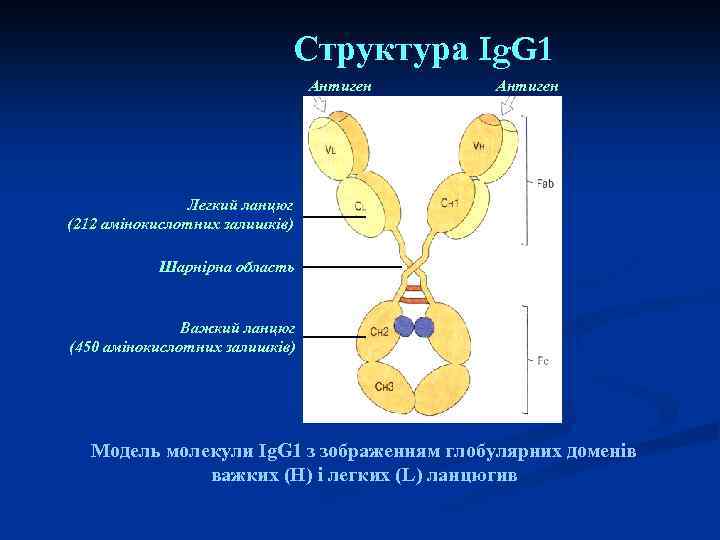
Структура Ig. G 1 Антиген Легкий ланцюг (212 амінокислотних залишків) Шарнірна область Важкий ланцюг (450 амінокислотних залишків) Модель молекули Ig. G 1 з зображенням глобулярних доменів важких (Н) і легких (L) ланцюгив

Будова різних класів імуноглобулінів та їх функції - Ig А За вмістом в сироватці та тканинних рідинах Ig А посідає 2 місце після Ig G. ≈ 15 – 20% всіх Ig сироватки, але лідирує в зовнішніх секретах (слина, сльози, травні соки, молозиво, молоко) та в секретах слизових оболонок (мигдалики). Більшість молекул сироваткового Ig А представлені мономерною (звичайною) формою. Секреторний Ig А (s. Ig. A) – димер, який складається з двох молекул Ig А, що з'єднані j-ланцюгом. Крім того, він містить додатковий пептид, який називається секреторним компонентом (S-компонент). Секреторні Ig А слугують важливим фактором захисту слизових оболонок від бактерій та вірусних інфекцій. Ig А людини поділяється на 2 підкласи: Ig А 1 та Ig А 2. Вони розрізняються за чутливістю до протеолітичних ферментів і розподіленню в організмі. Деякі бактерії, які паразитують на слизових оболонках, утворюють протеази, які руйнують Ig А 1, але не Ig А 2.
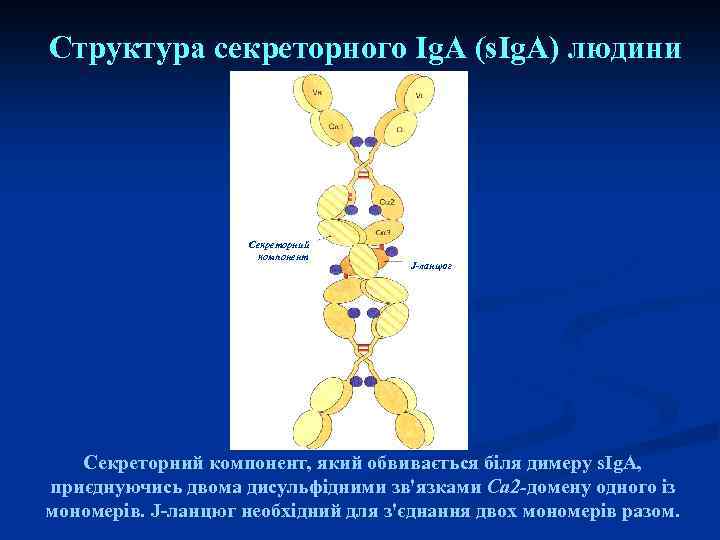
Структура секреторного Ig. А (s. Ig. A) людини Секреторний компонент J-ланцюг Секреторний компонент, який обвивається біля димеру s. Ig. A, приєднуючись двома дисульфідними зв'язками Са 2 -домену одного із мономерів. J-ланцюг необхідний для з'єднання двох мономерів разом.

Будова різних класів імуноглобулінів та їх функції - Ig D Вміст Ig D в сироватці складає 0, 03 мг/л. Функції цих Ig не зовсім вивчені. Вони складають основну частину мембранних Ig, разом з Ig М.
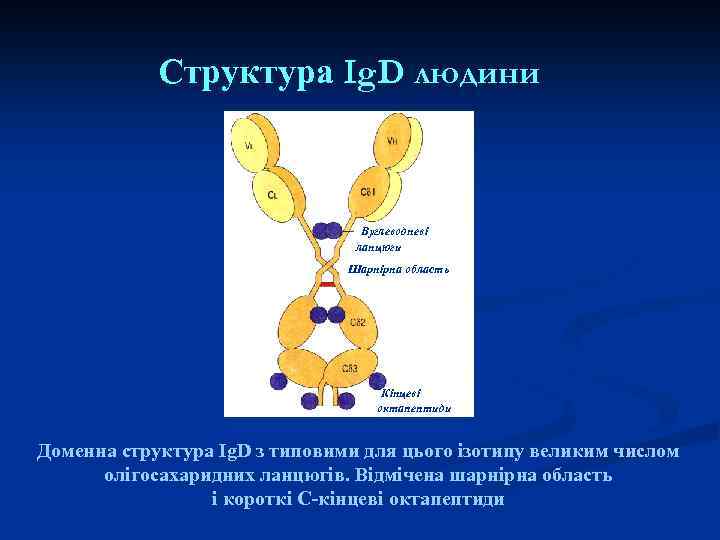
Структура Ig. D людини Вуглеводневі ланцюги Шарнірна область Кінцеві октапептиди Доменна структура Ig. D з типовими для цього ізотипу великим числом олігосахаридних ланцюгів. Відмічена шарнірна область і короткі С-кінцеві октапептиди

Будова різних класів імуноглобулінів та їх функції - Ig Е Концентрація Ig Е в нормальній сироватці дуже низька (0, 00005 мг/мл), але їх функції дуже важливі. Вони проявляють свої функції при паразитарних інфекціях та у випадку алергічних реакцій. При контакті з алергеном синтезується велика кількість Ig Е, які в свою чергу активують тучні клітини та базофіли, що секретують комплекс медіаторів (гістамін та серотонін), які викликають алергічні реакції. Ig Е лежать в основі таких захворювань, як бронхіальна астма, сінна лихоманка, атопічний дерматит, анафілактичний шок. Тому Ig Е – головні медіатори алергії. Важливо! Якщо в сироватці крові ідентифікують велику кількість Ig Е – це свідчить про наявність паразитарних інфекцій або алергії.
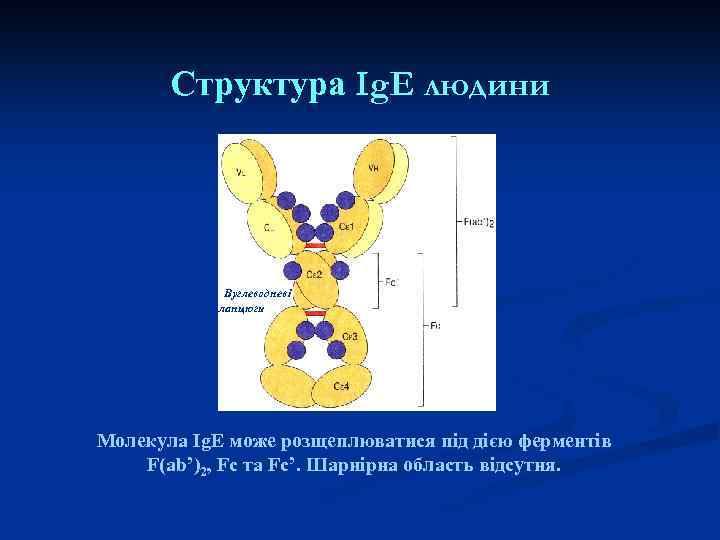
Структура Ig. Е людини Вуглеводневі ланцюги Молекула Ig. Е може розщеплюватися під дією ферментів F(ab’)2, Fc та Fc’. Шарнірна область відсутня.

Моноклональні антитіла Відомо, що антитіла, що утворюються в організмі в відповідь на введення антигену (бактерії, вірусу і т. ін. ), є білками, що називаються імуноглобулінами і захищають організм від хвороб. Але будь-яке чужорідне тіло, яке вводиться в організм, це суміш різних антигенів, що будуть збуджувати продукцію різних антитіл. До того ж в сироватці крові імунізованих тварин антитіло завжди є сумішшю, що складається з антитіл, які продукуються різними лімфоїдними клітинами. Та для практичних цілей необхідні антитіла одного типу, тобто моноспецифічні сироватки з одним типом антитіл. Очистка одного типу антитіл від сумішей – справа дуже складна і трудомістка. І ось в 1975 р. Келером і Мільдштеймом був розроблений спосіб отримання гібридів між лімфоцитами мишей, імунизованих перед цим якимось антигеном і культивуванням пухлинних клітин кісткового мозку (мієломними клітинами). Ці гібридні клітини отримали назву гібридоми. Вони об’єднали в собі здатність лімфоциту утворювати необхідні антитіла (одного типу) і здатність пухлинних безкінечно довго розмножуватись на штучних середовищах. Культивуючи гібридоми, а потім імізуючи ними тварин, можна отримати антитіла необхідного типу і в необмежених кількостях. Показано, наприклад, що з 50… 100 мишей можна отримати грами моноклональних антитіл. Моноклональні антитіла, отримані вказаним способом, зараз використовуються в різних областях медицини і біології. Виробництво моноклональних антитіл займає зараз одне з провідних місць в біотехнології. Крім широкого використання в фундаментальних дослідженнях вони застосовуються для отримання препаратів біологічно активних речовин високої чистоти, широко використовуються як діагностичні реагенти, наприклад для визначення груп крові. Моноклональні антитіла виявились перспективними для лікування ряду захворювань, і в особливості для лікування злоякісних пухлин.
антитела.ppt