Химическая кинетика.ppt
- Количество слайдов: 41
 Тема: «Кинетика химических реакций и катализ» План (см №… 1 -9.
Тема: «Кинетика химических реакций и катализ» План (см №… 1 -9.


 n Предмет химической кинетики Раздел химии, изучающий механизмы химических реакций и скорости их протекания называется химической кинетикой. Из сказанного следует, что для понимания законов, определяющих протекание химических и биохимических реакций, необходимо рассматривать их не только с позиций термодинамики (где рассматривается вопрос, насколько полно осуществится превращение исходных реагентов в продукты реакции, т. е. при этом не касаясь промежуточных ее состояний), но и химической кинетики, который именно позволяет узнать, как быстро совершается химическая реакция и каков ее механизм.
n Предмет химической кинетики Раздел химии, изучающий механизмы химических реакций и скорости их протекания называется химической кинетикой. Из сказанного следует, что для понимания законов, определяющих протекание химических и биохимических реакций, необходимо рассматривать их не только с позиций термодинамики (где рассматривается вопрос, насколько полно осуществится превращение исходных реагентов в продукты реакции, т. е. при этом не касаясь промежуточных ее состояний), но и химической кинетики, который именно позволяет узнать, как быстро совершается химическая реакция и каков ее механизм.
 Нормальные, медленные и быстрые реакции Химические реакции происходят с самыми разными скоростями Одни протекают медленно, месяцами (например, коррозия железа, биосинтез, в том числе фотосинтез и сбраживание). Так, белки обновляются наполовину за 70 суток, а неорганическая основа костных тканей полностью обмениваются за 4 -7 лет; Другие завершаются за несколько недель (например, ферментация этанола); Известны реакции, которые идут чрезвычайно быстро (например, большинство ионных взаимодействий в растворах– нейтрализация, образование осадка труднорастворимой соли и др, а реакция между водородом и кислородом развивается со скоростью взрыва.
Нормальные, медленные и быстрые реакции Химические реакции происходят с самыми разными скоростями Одни протекают медленно, месяцами (например, коррозия железа, биосинтез, в том числе фотосинтез и сбраживание). Так, белки обновляются наполовину за 70 суток, а неорганическая основа костных тканей полностью обмениваются за 4 -7 лет; Другие завершаются за несколько недель (например, ферментация этанола); Известны реакции, которые идут чрезвычайно быстро (например, большинство ионных взаимодействий в растворах– нейтрализация, образование осадка труднорастворимой соли и др, а реакция между водородом и кислородом развивается со скоростью взрыва.
 Общие представления о механизмах реакций n Механизм реакции– это последовательность и характер стадий химических реакций. Определить механизм реакции, исходя из стехиометрического уравнения, невозможно. n В зависимости от механизма реакции бывают: простые или элементарные (идут в одну стадию) и сложные (многостадийные). Например, разложения озона, описываемые простым уравнением: 2 О 3→ 3 О 2, является сложной реакцией, протекающей по следующему механизму: 1) О 3→O 2+O и 2) О 3+O→ 2 O 2 В пользу такого механизма свидетельствует наличие атомарного кислорода в реакционной смеси.
Общие представления о механизмах реакций n Механизм реакции– это последовательность и характер стадий химических реакций. Определить механизм реакции, исходя из стехиометрического уравнения, невозможно. n В зависимости от механизма реакции бывают: простые или элементарные (идут в одну стадию) и сложные (многостадийные). Например, разложения озона, описываемые простым уравнением: 2 О 3→ 3 О 2, является сложной реакцией, протекающей по следующему механизму: 1) О 3→O 2+O и 2) О 3+O→ 2 O 2 В пользу такого механизма свидетельствует наличие атомарного кислорода в реакционной смеси.
 Реакции могут быть: гомогенными и гетерогенными n n 1) Гомогенные реакции протекают в однородной среде (например, в газовой фазе или жидком растворе). Например: NH 4 C 1(водн) + Na. OH(водн)→ NH 3(г) + Н 2 О(ж) + Na. CI(водн) 2) Гетерогенные реакции протекают в неоднородной среде — между веществами, которые находятся в разных фазах (твердой и жидкой, газовой и жидкой и т. д. ). Например: СО 2(г) + Na. OH(водн) → Na. HCO 3(водн) Fe. S(т) + 2 НС 1(водн) →H 2 S(г) + Fe. Cl 2(водн) и т. д.
Реакции могут быть: гомогенными и гетерогенными n n 1) Гомогенные реакции протекают в однородной среде (например, в газовой фазе или жидком растворе). Например: NH 4 C 1(водн) + Na. OH(водн)→ NH 3(г) + Н 2 О(ж) + Na. CI(водн) 2) Гетерогенные реакции протекают в неоднородной среде — между веществами, которые находятся в разных фазах (твердой и жидкой, газовой и жидкой и т. д. ). Например: СО 2(г) + Na. OH(водн) → Na. HCO 3(водн) Fe. S(т) + 2 НС 1(водн) →H 2 S(г) + Fe. Cl 2(водн) и т. д.
 Влияние размера частиц на скорость реакции (См. видеофильм) n n Реакции быстрее проходят с участием твердых веществ, когда эти вещества тонко измельчены. Это вызвано тем, что отношение площади поверхности к массе у мелких частиц больше, чем у крупных, и, следовательно, площадь контакта твердого тела с жидкостью или газом больше. Например, реакции цинковой пыли и гранулированного Zn с кислотой или реакции порошка Ca. CO 3 и мраморной крошки с кислотой. Таким образом, гомогенные реакции происходят равномерно во всем объеме, заполненном реагентами, гетерогенные — только на некоторых пограничных поверхностях — на границе раздела фаз.
Влияние размера частиц на скорость реакции (См. видеофильм) n n Реакции быстрее проходят с участием твердых веществ, когда эти вещества тонко измельчены. Это вызвано тем, что отношение площади поверхности к массе у мелких частиц больше, чем у крупных, и, следовательно, площадь контакта твердого тела с жидкостью или газом больше. Например, реакции цинковой пыли и гранулированного Zn с кислотой или реакции порошка Ca. CO 3 и мраморной крошки с кислотой. Таким образом, гомогенные реакции происходят равномерно во всем объеме, заполненном реагентами, гетерогенные — только на некоторых пограничных поверхностях — на границе раздела фаз.
 4. Скорость (v, моль/л с) и константа скорости реакции (k). Кинетические уравнения n n Под скоростью химической реакции понимают изменение концентрации одного из реагирующих веществ в единицу времени. Например, за какой-то промежуток времени ∆t=t 2 t 1 - концентрация реагирующих веществ уменьшается на -∆C=C 1 — С 2 (рис. 1). Тогда средняя скорость реакции за промежуток времени ∆t равна:
4. Скорость (v, моль/л с) и константа скорости реакции (k). Кинетические уравнения n n Под скоростью химической реакции понимают изменение концентрации одного из реагирующих веществ в единицу времени. Например, за какой-то промежуток времени ∆t=t 2 t 1 - концентрация реагирующих веществ уменьшается на -∆C=C 1 — С 2 (рис. 1). Тогда средняя скорость реакции за промежуток времени ∆t равна:
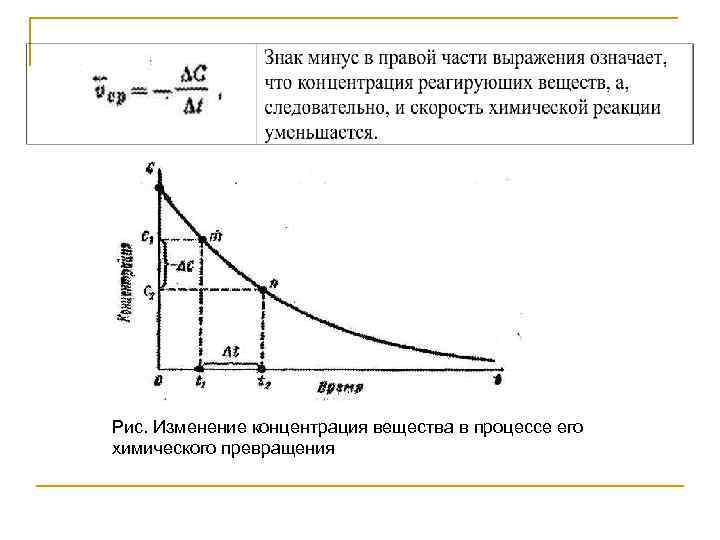 Рис. Изменение концентрация вещества в процессе его химического превращения
Рис. Изменение концентрация вещества в процессе его химического превращения
 Средняя скорость не отражает истинной скорости в каждый момент времени, n поэтому математически истинную скорость реакция в данный момент принято выражать отношением бесконечно малого изменения концентрации d. C к бесконечно малому отрезку времени dt в течение которого произошло изменение концентрации: V=+ d. C/dt, Если изучается изменение концентрации одного из исходных веществ, то d. C/dt<0, если одного из продуктов реакции, то d. C/dt>0.
Средняя скорость не отражает истинной скорости в каждый момент времени, n поэтому математически истинную скорость реакция в данный момент принято выражать отношением бесконечно малого изменения концентрации d. C к бесконечно малому отрезку времени dt в течение которого произошло изменение концентрации: V=+ d. C/dt, Если изучается изменение концентрации одного из исходных веществ, то d. C/dt<0, если одного из продуктов реакции, то d. C/dt>0.
 Скорость реакции зависит от: n n n 1) природы реагирующих веществ; 2) условий, при которых протекает реакция, — концентраций реагирующих веществ, температуры, давления (для газов), облучения квантами света и др. ; 3) присутствия катализаторов.
Скорость реакции зависит от: n n n 1) природы реагирующих веществ; 2) условий, при которых протекает реакция, — концентраций реагирующих веществ, температуры, давления (для газов), облучения квантами света и др. ; 3) присутствия катализаторов.
 Зависимость скорости реакции от концентраций реагирующих веществ описывается кинетическим уравнением и выражается законом действия масс: n скорость химической реакции прямо пропорциональна произведению молярных концентраций реагирующих веществ, взятых в степени, равной стехиометрическому коэффициенту данного вещества в уравнении реакции.
Зависимость скорости реакции от концентраций реагирующих веществ описывается кинетическим уравнением и выражается законом действия масс: n скорость химической реакции прямо пропорциональна произведению молярных концентраций реагирующих веществ, взятых в степени, равной стехиометрическому коэффициенту данного вещества в уравнении реакции.

 • Константа скорости численно равна скорости химической реакции, если концентрации реагирующих веществ равны единице (k=v). Она зависит от природы реагирующих веществ, температуры, наличия катализатора, но не зависит от концентрации.
• Константа скорости численно равна скорости химической реакции, если концентрации реагирующих веществ равны единице (k=v). Она зависит от природы реагирующих веществ, температуры, наличия катализатора, но не зависит от концентрации.
 5) Кинетика сложных реакций n n К сложным реакциям относятся: обратимые, параллельные, последовательные, сопряженные, цепные и др. реакции. К каждой из них в отдельности применимы уравнения кинетики простых реакций.
5) Кинетика сложных реакций n n К сложным реакциям относятся: обратимые, параллельные, последовательные, сопряженные, цепные и др. реакции. К каждой из них в отдельности применимы уравнения кинетики простых реакций.



 6. Кинетическая классификация химических реакций n n n Все химические реакции классифицируют nо: молекулярности и порядку реакции. 1) Молекулярностю химической реакции называется число молекул, непосредственно принимающих участие в элементарной реакции. Столкновение частиц исходных веществ является необходимым (хотя и недостаточным) условием столкновения или взаимодействия. Так как число столкновений зависит от концентрации, то с ее ростом должна возрастать и скорость химической реакции
6. Кинетическая классификация химических реакций n n n Все химические реакции классифицируют nо: молекулярности и порядку реакции. 1) Молекулярностю химической реакции называется число молекул, непосредственно принимающих участие в элементарной реакции. Столкновение частиц исходных веществ является необходимым (хотя и недостаточным) условием столкновения или взаимодействия. Так как число столкновений зависит от концентрации, то с ее ростом должна возрастать и скорость химической реакции
 Известны моно-, би- и тримолекулярные реакции.
Известны моно-, би- и тримолекулярные реакции.
 Кинетическое уравнение для моно-, би- и тримолекулярных реакций
Кинетическое уравнение для моно-, би- и тримолекулярных реакций
 Порядок реакции формально определяется суммой показателей степени (n 1+n 2+n 3+……) при концентрациях, входящих в кинетическое уравнение скорости химической реакции. n n n 2) Реакции могут быть первого (v = kc), второго (v = kc 2), третьего (v = kc 3), а также нулевого и дробного порядка. Дробный порядок характерен для сложных реакций, протекающих через промежуточные стадии. Нулевой порядок наблюдается в таких гетерогенных реакциях, в которых скорость подвода вещества больше скорости его расходования. В реакциях нулевого порядка скорость — постоянная величина (v = k, т. е. скорость процесса не зависит от концентраций реагирующих веществ ). Порядок реакции может быть определено только экспериментально.
Порядок реакции формально определяется суммой показателей степени (n 1+n 2+n 3+……) при концентрациях, входящих в кинетическое уравнение скорости химической реакции. n n n 2) Реакции могут быть первого (v = kc), второго (v = kc 2), третьего (v = kc 3), а также нулевого и дробного порядка. Дробный порядок характерен для сложных реакций, протекающих через промежуточные стадии. Нулевой порядок наблюдается в таких гетерогенных реакциях, в которых скорость подвода вещества больше скорости его расходования. В реакциях нулевого порядка скорость — постоянная величина (v = k, т. е. скорость процесса не зависит от концентраций реагирующих веществ ). Порядок реакции может быть определено только экспериментально.
 Для вычисления констант скоростей реакций 1–го, 2 -го, 3 го порядков дифференциальные уравнения (1 -5) интегрируют:
Для вычисления констант скоростей реакций 1–го, 2 -го, 3 го порядков дифференциальные уравнения (1 -5) интегрируют:
 Причины несовпадения порядка и молекулярности реакций n n Порядок и молекулярность совпадают лишь для простых одностадийных реакций. Можно назвать две причины несовпадения порядка и молекулярности: 1) постоянство концентрации одного или нескольких участников реакции. Например, в реакции омыления эфира: С 2 Н 5 СООСН 3 + Н 2 О → С 2 Н 5 ОН+СНз. СООН. Концентрация воды практически постоянна, поэтому выражение для скорости реакции v = k. Сэфира Своды = k'Сэфира. Реакция бимолекулярна, но первого порядка;
Причины несовпадения порядка и молекулярности реакций n n Порядок и молекулярность совпадают лишь для простых одностадийных реакций. Можно назвать две причины несовпадения порядка и молекулярности: 1) постоянство концентрации одного или нескольких участников реакции. Например, в реакции омыления эфира: С 2 Н 5 СООСН 3 + Н 2 О → С 2 Н 5 ОН+СНз. СООН. Концентрация воды практически постоянна, поэтому выражение для скорости реакции v = k. Сэфира Своды = k'Сэфира. Реакция бимолекулярна, но первого порядка;
 n n 2) ступенчатый характер реакции. Например, тримолекулярная реакция хлорирования оксида азота 2 NO + Cl 2 = 2 NOCl состоит из двух стадий: a) NO + СI 2→NOC 12, б) NOCI 2 + NO → 2 NOC 1. Первая стадия протекает быстро, образуется нестойкий продукт NOCI 2. Вторая стадия медленная и лимитирующая. Суммарная скорость реакции выражается равенством v =k. C NOCI 2 C NO. Реакция тримолекулярна, но второго порядка.
n n 2) ступенчатый характер реакции. Например, тримолекулярная реакция хлорирования оксида азота 2 NO + Cl 2 = 2 NOCl состоит из двух стадий: a) NO + СI 2→NOC 12, б) NOCI 2 + NO → 2 NOC 1. Первая стадия протекает быстро, образуется нестойкий продукт NOCI 2. Вторая стадия медленная и лимитирующая. Суммарная скорость реакции выражается равенством v =k. C NOCI 2 C NO. Реакция тримолекулярна, но второго порядка.
 n Таким образом, если скорости отдельных стадий сильно различаются, то скорость в целом и ее порядок определяются скоростью и порядком самой медленной стадии, называемой скоростьопределяющей или лимитирующей стадией.
n Таким образом, если скорости отдельных стадий сильно различаются, то скорость в целом и ее порядок определяются скоростью и порядком самой медленной стадии, называемой скоростьопределяющей или лимитирующей стадией.
 Период полупревращения n Иногда о скорости химической реакции судят по величине периода половины превращения t 1/2, который выражается временем, в течение которого претерпевает превращение половина взятого вещества. Для t 1/2 х — а/2, тогда формулы (6) и (8) можно записать так: (10) (11)
Период полупревращения n Иногда о скорости химической реакции судят по величине периода половины превращения t 1/2, который выражается временем, в течение которого претерпевает превращение половина взятого вещества. Для t 1/2 х — а/2, тогда формулы (6) и (8) можно записать так: (10) (11)
 n Период половины превращения t 1/2 для реакций первого порядка не зависит от начальной концентрации вещества, а для реакций второго порядка он обратно пропорционален начальной концентрации. Эта особенность используется для определения порядка реакции опытным путем.
n Период половины превращения t 1/2 для реакций первого порядка не зависит от начальной концентрации вещества, а для реакций второго порядка он обратно пропорционален начальной концентрации. Эта особенность используется для определения порядка реакции опытным путем.

 7. Влияние температуры на скорость химической реакции. Уравнение n Аррениуса На скорость химических реакций существенное влияние оказывает даже незначительное изменение температуры. У большинства гомогенных реакций при повышении температуры на 10° С скорость возрастает в 2— 4 раза (приближенное правило Вант. Гоффа). Увеличение скорости реакции при повышении температуры связано с возрастанием константы скорости реакции; концентрации реагирующих веществ при этом практически не изменяются.
7. Влияние температуры на скорость химической реакции. Уравнение n Аррениуса На скорость химических реакций существенное влияние оказывает даже незначительное изменение температуры. У большинства гомогенных реакций при повышении температуры на 10° С скорость возрастает в 2— 4 раза (приближенное правило Вант. Гоффа). Увеличение скорости реакции при повышении температуры связано с возрастанием константы скорости реакции; концентрации реагирующих веществ при этом практически не изменяются.
 n. Соотношение: (12) n называется температурным коэффициентом скорости реакции, где k — константы скорости при температурах t+10 и to С. Для различных реакций γ колеблется в пределах от 2 до 4. На основании (12) можно записать, что (12 а)
n. Соотношение: (12) n называется температурным коэффициентом скорости реакции, где k — константы скорости при температурах t+10 и to С. Для различных реакций γ колеблется в пределах от 2 до 4. На основании (12) можно записать, что (12 а)
 Логарифмируя (12 а), получим: (13) Где kt 1 и kt 2 – констаны скорости при температурах t 1 и t 2. Для ферментативных реакций температурный коэффициент может достигать значений γ=7 -9, поэтому колебания температуры тела человека в пределах даже 1 o сильно сказывается на его самочувствии.
Логарифмируя (12 а), получим: (13) Где kt 1 и kt 2 – констаны скорости при температурах t 1 и t 2. Для ферментативных реакций температурный коэффициент может достигать значений γ=7 -9, поэтому колебания температуры тела человека в пределах даже 1 o сильно сказывается на его самочувствии.
 Более точная зависимость константы скорости, а следовательно, и скорости реакции от температуры выражается уравнение Аррениуса. или Где R=8, 31 Дж/моль К– универсальная газовая постоянная. Еа данной реакции зависит от природы реагирующих веществ.
Более точная зависимость константы скорости, а следовательно, и скорости реакции от температуры выражается уравнение Аррениуса. или Где R=8, 31 Дж/моль К– универсальная газовая постоянная. Еа данной реакции зависит от природы реагирующих веществ.
 Энергия активация Еа, (Дж/моль) n n – это та минимальная избыточная энергия по сравнению со средней энергией, которой должны обладать молекулы, чтобы реакция между ними стала возможной. Преодоление этого энергетического барьера частицами исходных веществ связано с образованием активного комплекса, который затем превращается в продукты реакции за счет разрыва старых связей и образования новых. Например,
Энергия активация Еа, (Дж/моль) n n – это та минимальная избыточная энергия по сравнению со средней энергией, которой должны обладать молекулы, чтобы реакция между ними стала возможной. Преодоление этого энергетического барьера частицами исходных веществ связано с образованием активного комплекса, который затем превращается в продукты реакции за счет разрыва старых связей и образования новых. Например,
 8. Катализ (более подробно изучить самостоятельно) n Катализом называют изменение скорости химических реакций в присутствии веществ, которые сами после реакции остаются химически неизмененными. Обычно катализаторами называют только ускорители реакций, а ингибиторами — замедлители.
8. Катализ (более подробно изучить самостоятельно) n Катализом называют изменение скорости химических реакций в присутствии веществ, которые сами после реакции остаются химически неизмененными. Обычно катализаторами называют только ускорители реакций, а ингибиторами — замедлители.
 Если катализатор и реагирующие вещества находятся в одной фазе, то катализ называют гомогенным, если в разных фазах — гетерогенным. Действие катализаторов: n 1) не изменяет теплового эффекта реакции; n 2) снижает энергию активации как прямой, так и обратной реакции на одну и ту же величину ∆Е, поэтому не смещает равновесия; n 3) увеличивая в одинаковой степени скорость прямой и обратной реакции, сокращает время достижения равновесия; n 4) является избирательным, что определяется природой катализатора и условиями его применения.
Если катализатор и реагирующие вещества находятся в одной фазе, то катализ называют гомогенным, если в разных фазах — гетерогенным. Действие катализаторов: n 1) не изменяет теплового эффекта реакции; n 2) снижает энергию активации как прямой, так и обратной реакции на одну и ту же величину ∆Е, поэтому не смещает равновесия; n 3) увеличивая в одинаковой степени скорость прямой и обратной реакции, сокращает время достижения равновесия; n 4) является избирательным, что определяется природой катализатора и условиями его применения.
 Механизм гомогенного катализа состоит в том, что конечный продукт реакции АВ в присутствии катализатора К образуется не за счет непосредственного взаимодействия исходных веществ А и В, согласно уравнению А+В→АВ (Еа), а в результате реакции, протекающей в две стадии:
Механизм гомогенного катализа состоит в том, что конечный продукт реакции АВ в присутствии катализатора К образуется не за счет непосредственного взаимодействия исходных веществ А и В, согласно уравнению А+В→АВ (Еа), а в результате реакции, протекающей в две стадии:
 В случае гетерогенного катализа основную роль играет адсорбция молекул реагирующих веществ на поверхности катализатора, что приводит к повышению их энергии и снижению энергии активации катализируемой реакции. n n Примеры гомогенного катализа Кислотно-основной катализ (гидролиз сложного эфира с образованием карбоновой кислоты и спирта или фенола). Ферментативный катализ (энзимы – это специфические катализаторы белковой природы). Примеры гетерогенного катализа Многие переходные металлы (Fe, Ni) работают как гетрогенные катализаторы. Аутокатализ– встречаются реакции, в которых один из продуктов является катализатором (например, Mn 2+ катализирует реакцию окисление H 2 O 2 перманганатом (V) ) в кислой среде.
В случае гетерогенного катализа основную роль играет адсорбция молекул реагирующих веществ на поверхности катализатора, что приводит к повышению их энергии и снижению энергии активации катализируемой реакции. n n Примеры гомогенного катализа Кислотно-основной катализ (гидролиз сложного эфира с образованием карбоновой кислоты и спирта или фенола). Ферментативный катализ (энзимы – это специфические катализаторы белковой природы). Примеры гетерогенного катализа Многие переходные металлы (Fe, Ni) работают как гетрогенные катализаторы. Аутокатализ– встречаются реакции, в которых один из продуктов является катализатором (например, Mn 2+ катализирует реакцию окисление H 2 O 2 перманганатом (V) ) в кислой среде.
 9. Понятие о фармокинетике n n Фармакокинетика — это исследование кинетики всасывания, распределения, метаболизма и экскреции лекарств в сопоставлении с соответствующими фармакологическим, терапевтическим или токсическим эффектами у животных и человека» . Фармакокинетика — комплексная дисциплина, стоящая на стыке ряда наук — физической и аналитической химии, биофизики, фармакологии, фармации, медицины, математики, генетики и др. Основным инструментом современной фармакокинетики считается математическое моделирование процессов, происходящих с лекарственным средством в организме.
9. Понятие о фармокинетике n n Фармакокинетика — это исследование кинетики всасывания, распределения, метаболизма и экскреции лекарств в сопоставлении с соответствующими фармакологическим, терапевтическим или токсическим эффектами у животных и человека» . Фармакокинетика — комплексная дисциплина, стоящая на стыке ряда наук — физической и аналитической химии, биофизики, фармакологии, фармации, медицины, математики, генетики и др. Основным инструментом современной фармакокинетики считается математическое моделирование процессов, происходящих с лекарственным средством в организме.
 n n Для исследования фармакокинстики нового препарата подбирают больных, которым этот препарат показан. В некоторых странах такие исследования проводят на здоровых добровольцах, однако это не оправдано с этической и правовой сторон. Подбор больных проводят так, чтобы в исследуемую группу попали люди примерно одного возраста, со средней массой тела, без повреждений функции печени, почек, желудочнокишечного тракта, сердечно-сосудистой системы. Исключение составляют случаи, когда препарат предназначен специально для лечения какоголибо из этих органов или систем.
n n Для исследования фармакокинстики нового препарата подбирают больных, которым этот препарат показан. В некоторых странах такие исследования проводят на здоровых добровольцах, однако это не оправдано с этической и правовой сторон. Подбор больных проводят так, чтобы в исследуемую группу попали люди примерно одного возраста, со средней массой тела, без повреждений функции печени, почек, желудочнокишечного тракта, сердечно-сосудистой системы. Исключение составляют случаи, когда препарат предназначен специально для лечения какоголибо из этих органов или систем.


