Лекция 16-17 Интеграция метаболизма.ppt
- Количество слайдов: 53

Тема: Интеграция метаболизма 1

Интеграция (лат. , integer), не только метод математики, но в более широком смысле - процесс заполнения, объединения частей в целое, в т. ч. и в биологических науках. Так, говоря о круговороте атомов С, N, О, витаминов и др. веществ в природе, мы интегрируем их в представления о синтрофии, т. е. совместном питании таксонов в биосфере. Другой пример – цитология, сведенная к схеме из учебника Ю. Б. Филипповича. Основы биохимии. М. 1999. 2
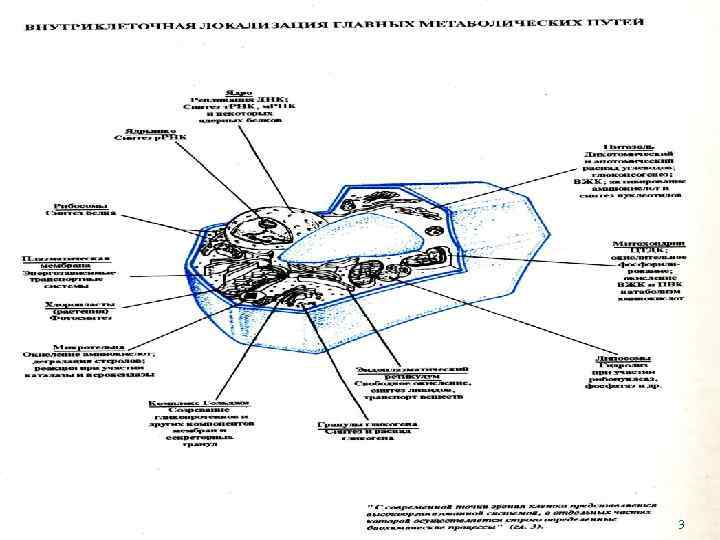
3

Компартментализация основных метаболических путей

Таким образом: метаболические процессы, связанные с биосинтезом и взаимопревращениями веществ, в основном связаны с цитозолем; NADPH, необходимый для реакций восстановления, образуется также в цитозоле в результате окислительной стадии пентозофосфатного пути превращения глюкозы; окислительные реакции в процессе катаболизма связаны с дыханием, протекают в митохондриях и используют в качестве коферментов NAD+ и флавопротеины.

К стратегическим целям питания, структуры и управляемого Е метаболизма относят: 1. Генерацию АТФ и/или электрохимического потенциала биомембран. 2. Поддержание восстановительной атмосферы (НАДФН 2) при окислении глюкозы в пентозофосфатном пути = ПФП 3. Получение строительных блоков для биосинтезов всех полимеров. 6

Непостоянство состава пищи и ее неполное соответствие потребностям клеток, вынуждает их к взаимопревращениям общих метаболитов в разных путях, т. е. интеграции метаболизма.
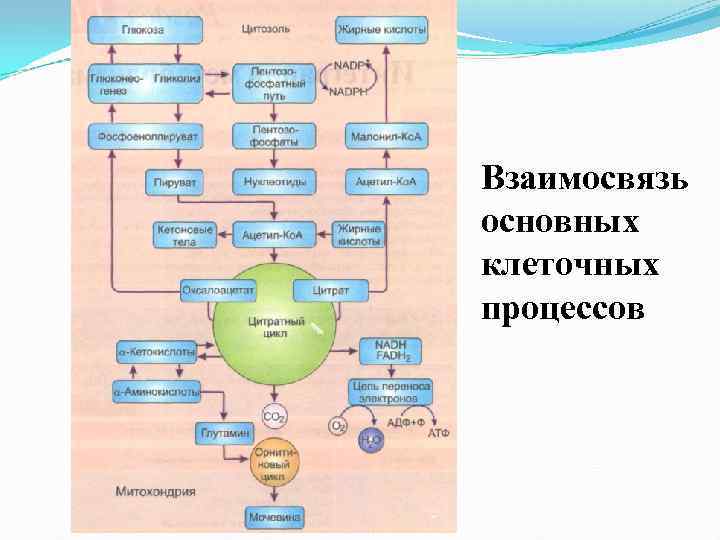
Взаимосвязь основных клеточных процессов
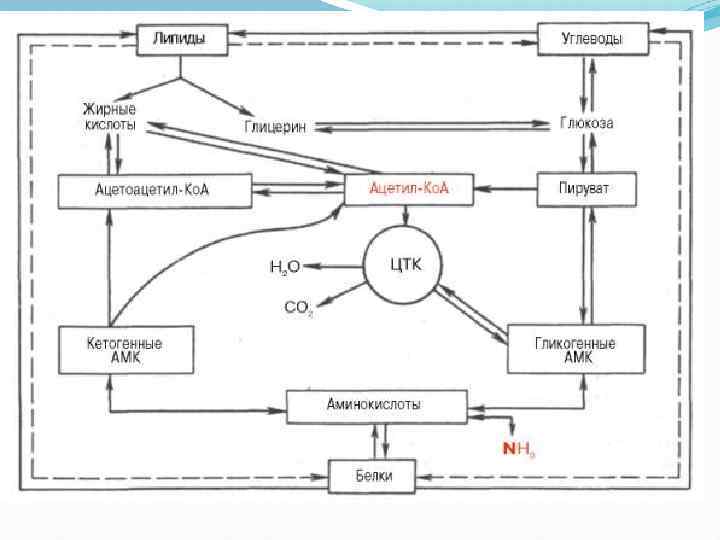

Интеграция метаболизма углеводов, жиров и белков обеспечивается: • наличием в метаболических путях общих промежуточных продуктов; • возможностью взаимопревращений веществ через общие метаболиты; • использованием общих коферментов; • существованием общего пути катаболизма и единой системы освобожде ния и использования энергии (дыхательная цепь); • использованием сходных механизмов регуляции.

Ключевые метаболиты, находящиеся в точках разветвления метаболических путей, обеспечивают переключение метаболизма с одного пути на другой в зависимости от потребностей организма. Эти вопросы частично рассматривались в основном курсе биохимии.

Глюкозо-6 -фосфат образуется из глюкозы и далее преобразуется по следующим путям: 1. Наличие глюкозо 6 фосфатазы в клетках печени и почек обеспечивает выделение этими органами свободной глюкозы в кровеносное русло. 2. Г 6 Ф может превращаться в гликоген через Г 1 Ф и УДФ глюкозу. 3. Г 6 Ф может превращаться в глюкозамин и глюкуроновую кислоту, которые необходимы для биосинтеза компонентов межклеточного вещества гликозамингликанов, а глюкуроновая кислота участвует во второй фазе обезвреживания ксенобиотиков в виде УДФ глюкуроновой кислоты (образование парных соединений для повышения гидрофильности выводимых веществ).

4. Г 6 Ф может превращаться в реакциях пентозофосфатного пути обмена углеводов. При этом образуются пентозофосфаты и затем фосфорибозилпи рофосфат, необходимый для биосинтеза нуклеотидов и нуклеиновых кислот (процессы физиологической и рспаративной регенерации тканей). Кроме того, образуемый НАДФН необходим для ряда биосинтезов (холестерола, жирных кислот и др ), а также используется в реакциях антиоксидантной защиты при свободнорадикальном повреждении клеток. 5. Г 6 Ф может превращаться в специфическом пути реакций от глюкозы до пирувата и затем в реакциях общего пути катаболизма.
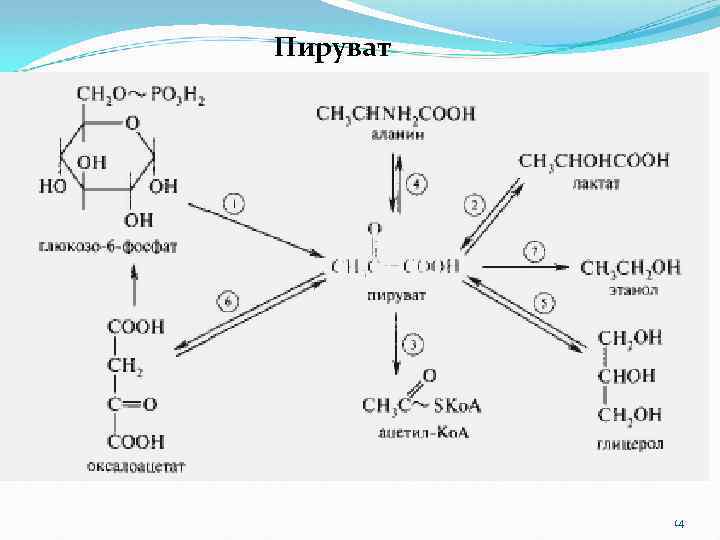
Пируват 14

Следующим важным пунктом переключения является пируват, который может метаболизироваться по следующим направлениям: 1. Реакции карбоксилирования пирувата ведут к образованию оксалоацетата (щавелевоуксусная кислота, ЩУК). 2. Реакции окислительного декарбоксилирования пирувата обеспечивают образование ацетил Ко. А. 3. В реакции, катализируемой аланинаминотранс феразой (Ал. АТ), из пирувата образуется аланин. 4. От пирувата начинается комплекс ферментативных реакций первого обходного пути глюконеогенеза, ведущий к образованию фосфоенолпирувата (обращение пируваткиназной реакции).

Ацетил-Со. А

Наиболее интересным пунктом переключения является ацетил Ко. А: 1. Ацетил Ко. А образуется из жирных кислот (β окис ление) и кетоновых тел обратимо, а из кетогенных амино кислот и глицерола, пирувата (углеводы) необратимо. 2. Ацетил Ко. А, конденсируясь с оксалоацетатом, вступает в цикл трикарбоновых кислот, в котором ацетильная группа полностью «сгорает» , поставляя атомы водорода в митохондриальныецепи переноса протонов и электронов, а также выделяя углекислый газ. 3. Ацетил Ко. А может карбоксилироваться и превращаться в малонил Ко. А и далее в жирные кислоты. 4. Три молекулы ацетил Ко. А конденсируются и ведут к образованию ГМГ Ко. А, а затем кетоновых тел или через мевалонат Ко. А обеспечивают синтез холестерола.
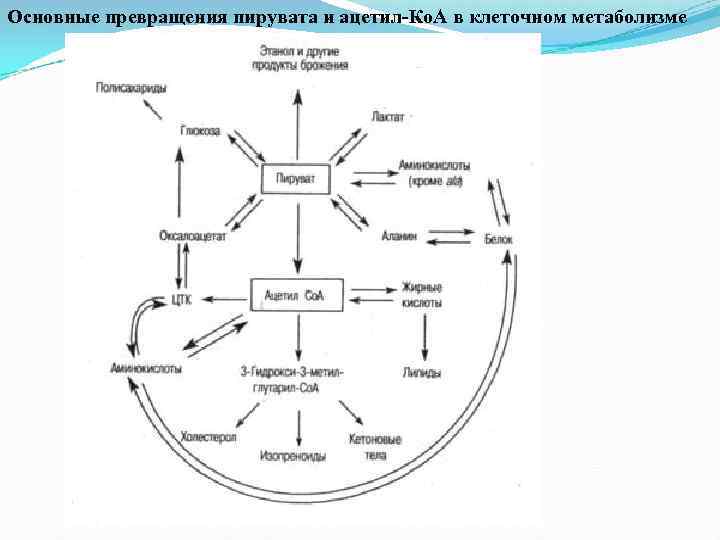
Основные превращения пирувата и ацетил-Ко. А в клеточном метаболизме

Регуляторные механизмы переключения одного метаболического пути на другой может осуществляться путем изменения: концентрации ферментов; активности ферментов; концентрации субстратов, продуктов, а также кофакторов. Переключение метаболических путей под влиянием гормонов происходит постоянно в зависимости от ритма питания, состава пищи и физиологической активности организма.
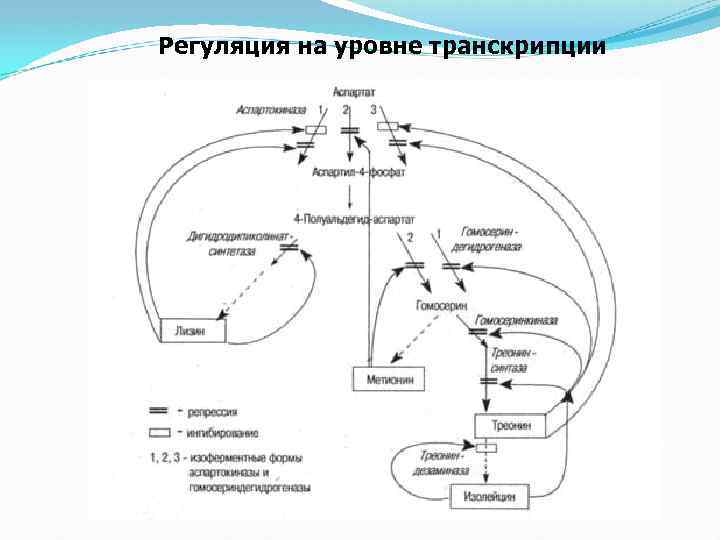
Регуляция на уровне транскрипции
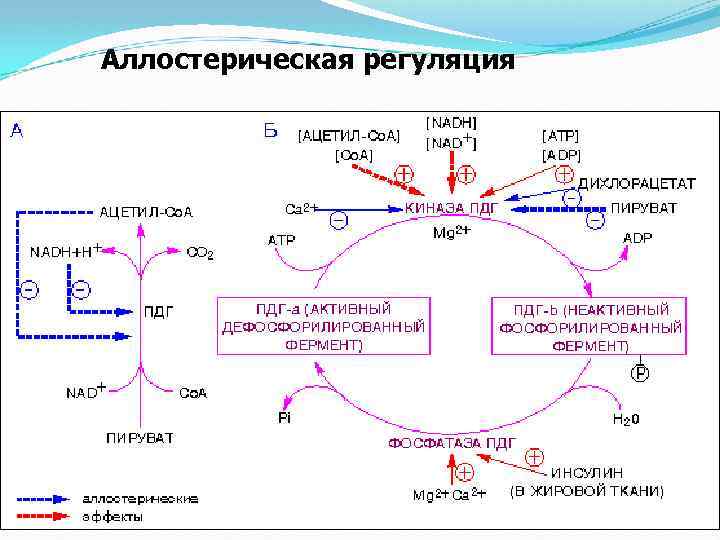
Аллостерическая регуляция
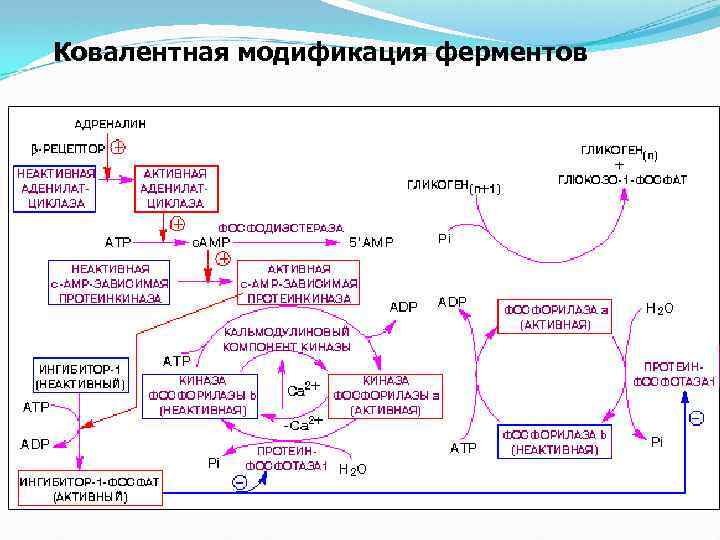
Ковалентная модификация ферментов

Кратковременно, автоматизм метаболических процессов в клетках достигается: До минут - с помощью аллостерических = метаболических обратных связей для ключевых Е: Другие примеры: гликолиз, гликонеогенез, ЦТК и т. д. 23
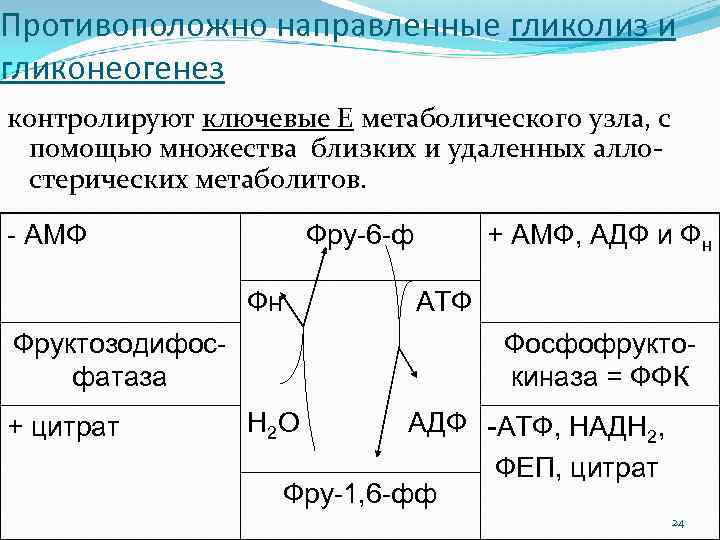
Противоположно направленные гликолиз и гликонеогенез контролируют ключевые Е метаболического узла, с помощью множества близких и удаленных аллостерических метаболитов. - АМФ Фру-6 -ф Фн Фруктозодифосфатаза + цитрат + АМФ, АДФ и Фн АТФ Фосфофруктокиназа = ФФК Н 2 О АДФ -АТФ, НАДН 2, ФЕП, цитрат Фру-1, 6 -фф 24

При этом Е гликолиза конституитивны, То есть const в цитозоле. Напротив, гликонеогенез развивается лишь при длительных стрессах (> 30 мин), с помощью индуцибельных Е специфических обходных реакций: ФЭП карбоксикиназы, ФДФ и Глк 6 фосфатаз. 25

На десятки минут – часы, метаболизмом управляют ковалентные модифика-ции белков: Один из примеров – активация сериновых протеиназ гемостаза, пищеварения, иммунитета: адрес зимоген = профермент H 2 N N N COOH Для переходов Е Е-Ф фосфорилазы и синтетазы гликогена в печени и мышцах и т. п. , нужны протеинкиназы и протеинфосфатазы. 26
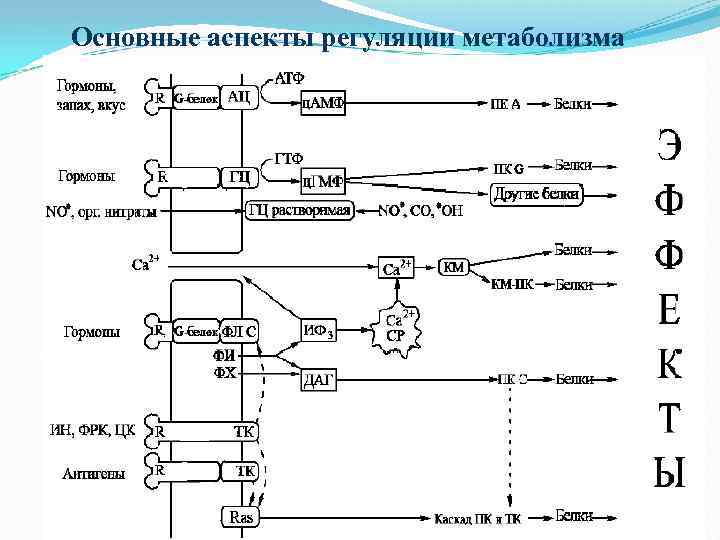
Основные аспекты регуляции метаболизма
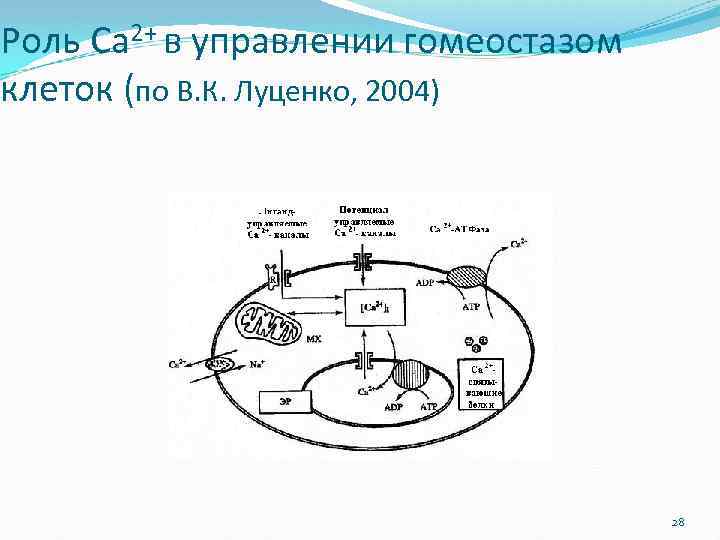
Роль Са 2+ в управлении гомеостазом клеток (по В. К. Луценко, 2004) 28
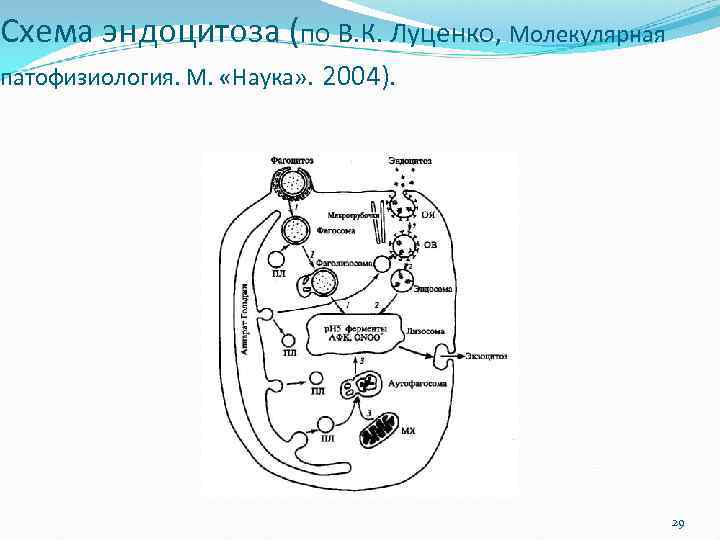
Схема эндоцитоза (по В. К. Луценко, Молекулярная патофизиология. М. «Наука» . 2004). 29
![Показатель энергетического статуса клетки ее «Энергетический потенциал» или соотношение компонентов адениловой системы = [АТФ] Показатель энергетического статуса клетки ее «Энергетический потенциал» или соотношение компонентов адениловой системы = [АТФ]](https://present5.com/presentation/3/49261992_437272694.pdf-img/49261992_437272694.pdf-30.jpg)
Показатель энергетического статуса клетки ее «Энергетический потенциал» или соотношение компонентов адениловой системы = [АТФ] + ½ [АДФ]/[АТФ] + [АДФ] + [АМФ] Теоретически он var от 0, когда есть только АМФ и до 1 - есть только АТФ. Но, большинство клеток поддерживает соотношение АТФ : АДФ : АМФ = 100 : 1. Т. е. в норме, энергетический заряд клетки = 0, 80, 95. 30
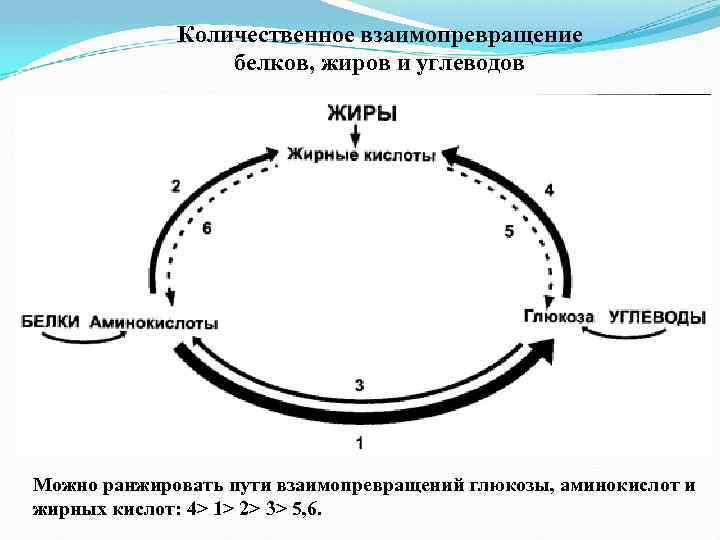
Количественное взаимопревращение белков, жиров и углеводов Можно ранжировать пути взаимопревращений глюкозы, аминокислот и жирных кислот: 4> 1> 2> 3> 5, 6.

Рассматривая степень взаимопревращений белков, жиров и углеводов, не обходимо, прежде всего, рассмотреть взаимопревращения аминокислот, жирных кислот и глюкозы. Рассмотрим возможные пути превращений: 1) синтез глюкозы из аминокислот (глюконеогенез) идет через фосфоенол пиру ват (гликогенные аминокислоты — арг, асп, асн, цис, глу, глн, гли, гис. мет, про, сер, тре, три, вал); глюконеогенез усилен при голоде, стрессе, диабете; 2) синтез жирных кислот из аминокислот идет через ацетил Ко. А (кетогенные аминокислоты — лей, лиз, фен, тир); при этом возможен синтез кетоновых тел через ацетоацетил Ко. А; 3) синтез заменимых аминокислот из глюкозы путем восстановительного аминирования и трансаминирования с тремя кетокислотами (пируват, оксалоацетат и 2 оксоглугарат); 4) синтез жирных кислот из глюкозы (через ацетил Ко. А) и глицерол через глицсральдсгил З фосфат, это путь депонирования энергии; 5) жирные кислоты весьма слабо превращаются в углеводы; 6) жирные кислоты практически не превращаются в аминокислоты.

Взаимосвязи тканей и органов Важную роль в осуществлении функций различных органов и тканей организма играет печень.

Роль кровеносного русла (некоторые механизмы управления микроциркуляцией). Известны многочисленные факты того, что изменение гемодинамики на микроциркуляторном уровне может существенно влиять на метаболизм в тканях. Рассмотрим например некоторые факторы, способствующие релаксации гладкой мускулатуры обменных сосудов и, таким образом, изменяющие интенсивность обмена газов и биомолекул в системе кровь ткани. Кининовую систему образуют каллидин, брадикинин и метионил лизилбрадикинин. Они обеспечивают регуляцию местного и общего кровотока, расслабляют гладкую мускулатуру сосудов, повышают проницаемость капиллярной мембраны и других мембран сосудистой стенки, оказывают провоспалительное действие.
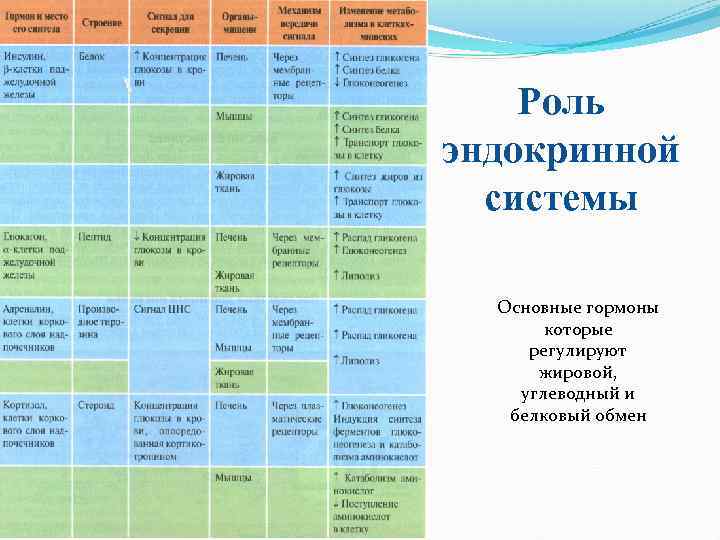
Роль эндокринной системы Основные гормоны которые регулируют жировой, углеводный и белковый обмен
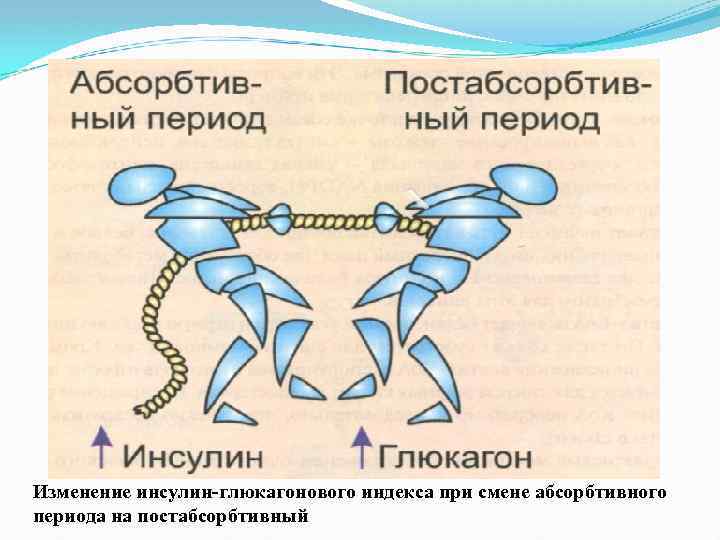
Изменение инсулин-глюкагонового индекса при смене абсорбтивного периода на постабсорбтивный
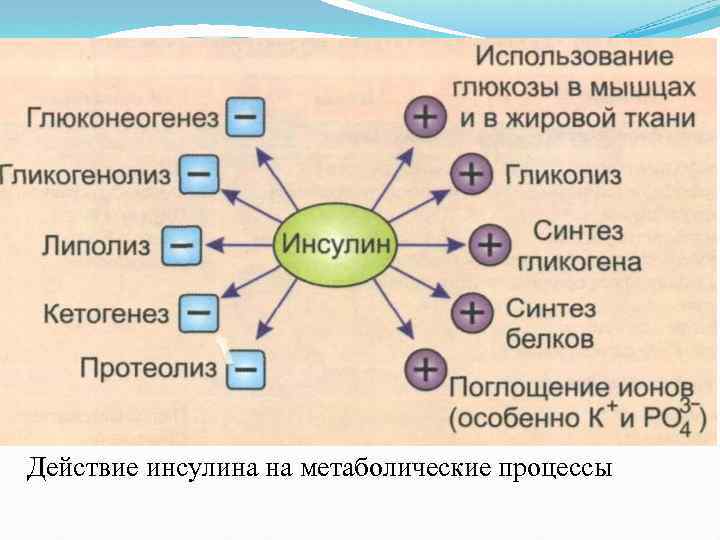
Действие инсулина на метаболические процессы
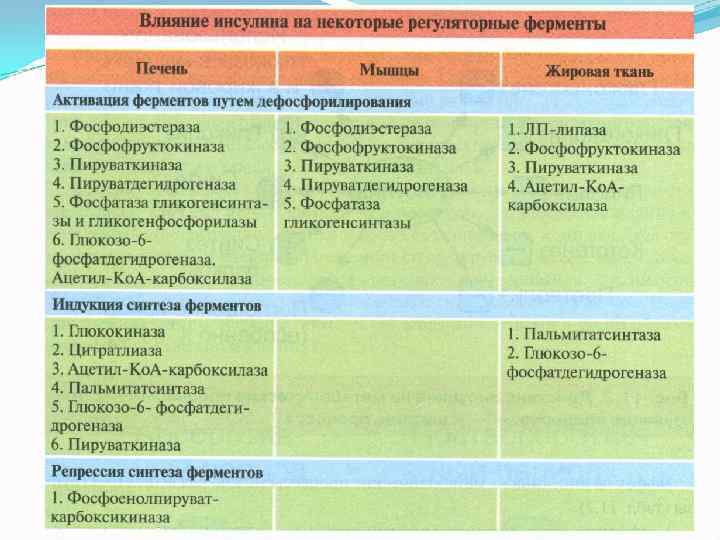

39
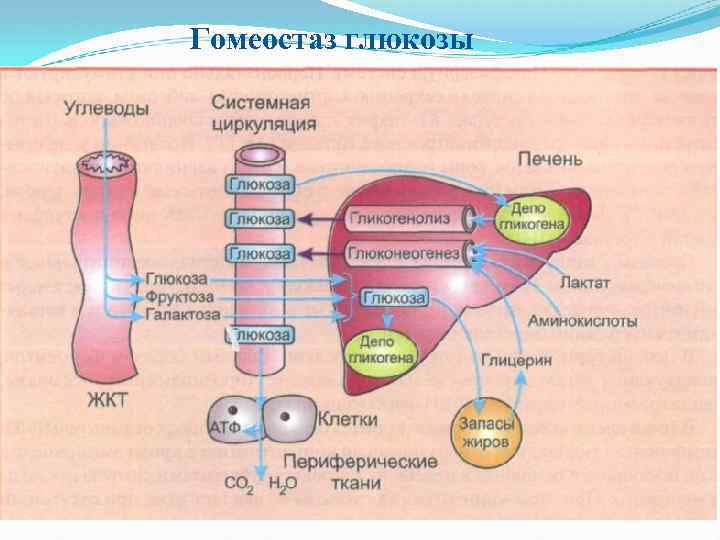
Гомеостаз глюкозы

41
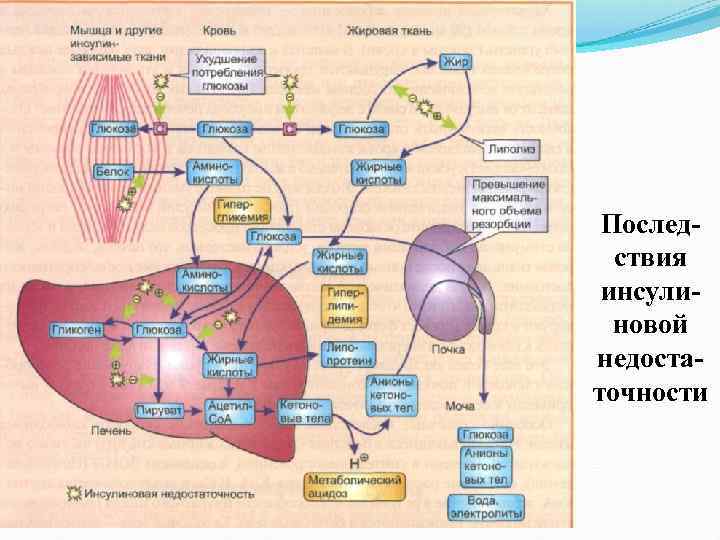
Последствия инсулиновой недостаточности
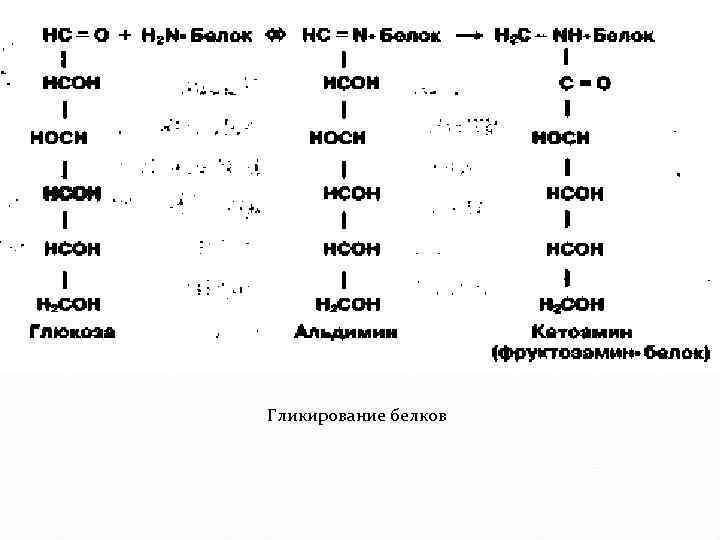
Гликирование белков

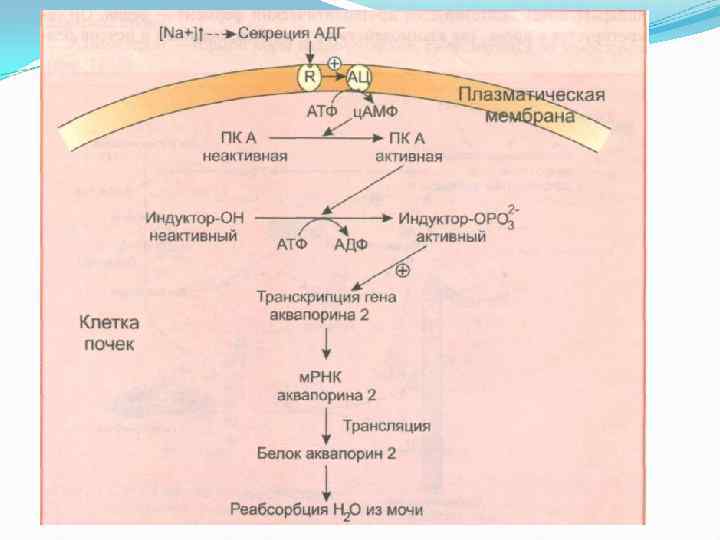
Регуляция водно-солевого обмена Антидиуретический гормон (АДГ) представляет собой нонапептид.
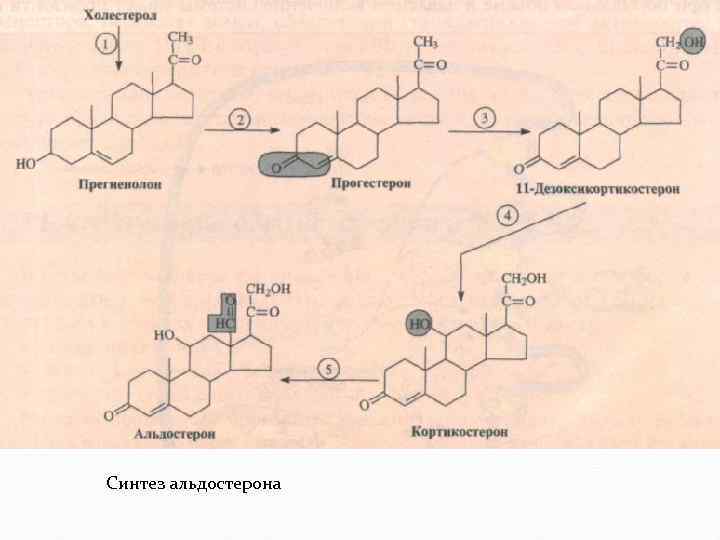
Синтез альдостерона
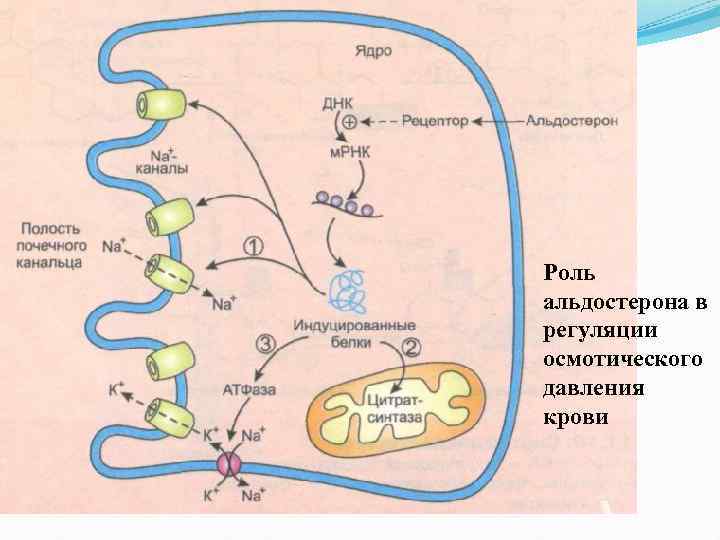
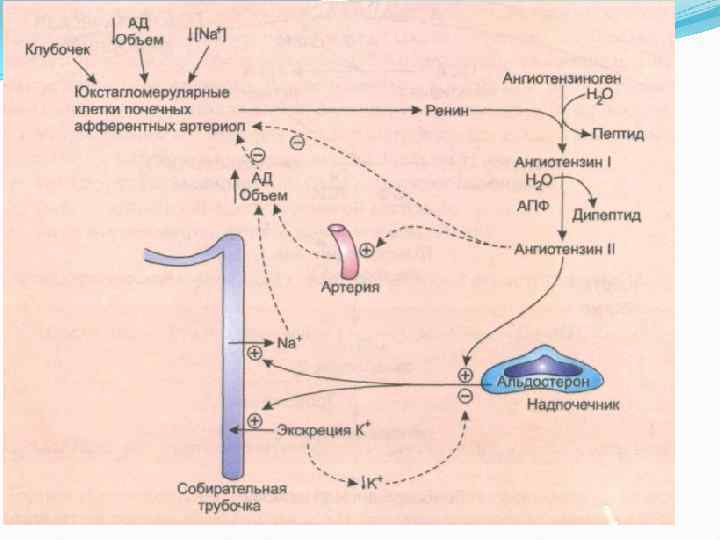
Роль альдостерона в регуляции осмотического давления крови
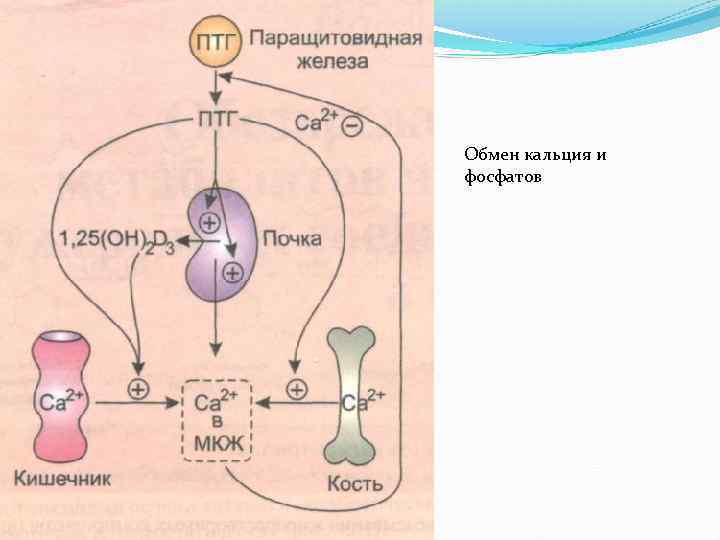
Обмен кальция и фосфатов
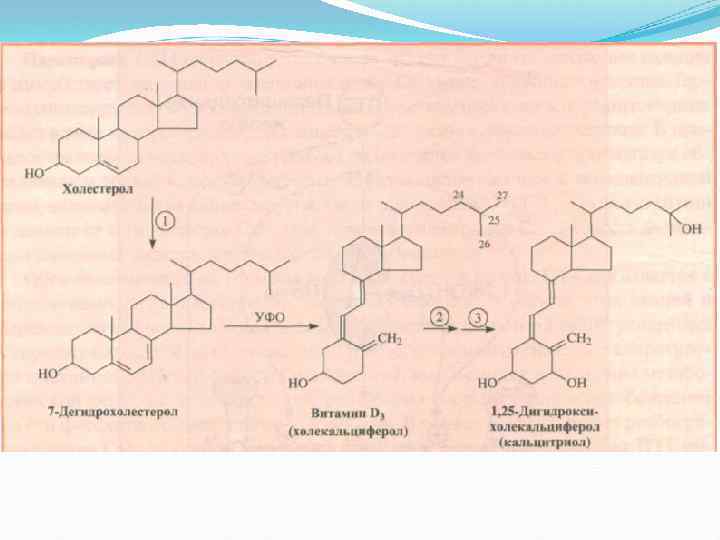

Малые и большие петли обратных связей придают клеткам автоматизм для: Поддержания внутриклеточного метаболизма в целях гомеостаза. 2. Своевременных переходов к следующим стадиям клеточного цикла. 3. Понимания внешних сигналов, если сенсорные механизмы могут их трансдуцировать = перевести в низкие (10 -7 -10 -8 М) концентрации вторых посредников – универсальных сигнальных молекул - регуляторов цитозоля. Их набор невелик: 1. Са 2+ и NO. 2. Циклонуклеотиды: ц. АМФ, ц. ГМФ, ц. АДФрибоза 3. Продукты распада мембранных ФЛ: эйкозаноиды, Ин. Ф 3, ДАГ. При действии внешних агентов, их концентрации в цитозоле меняются лавинообразно, кратковременно var активность белков и генов. Затем, вторые посредники разрушаются или удаляются, возвращая клетку в исходное состояние. 1. 52
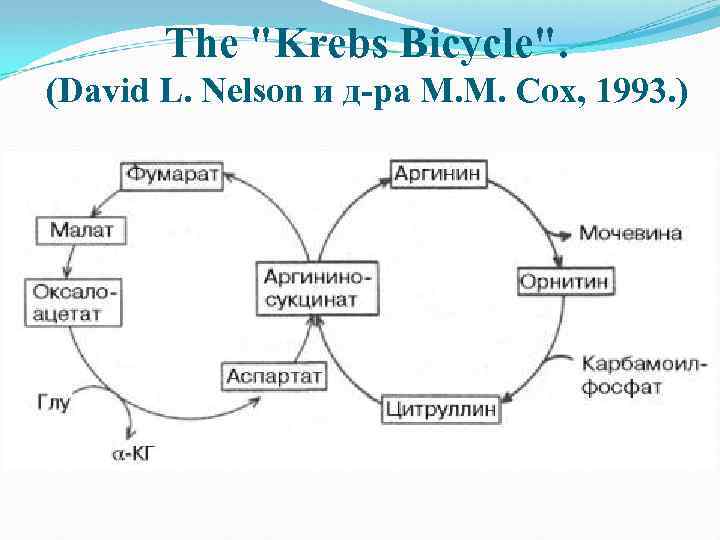
The "Krebs Bicycle". (David L. Nelson и д-ра М. М. Сох, 1993. )
Лекция 16-17 Интеграция метаболизма.ppt