afcf59fb65ac730d395d85434a0d0a06.ppt
- Количество слайдов: 45
 Тема: цели и задачи фармацевтической химии. Построение, показатели качества и виды нормативной документации Абдуллабекова Вилоятхон Нуруллабековна, д. ф. н. , зав. кафедрой фармацевтической химии Ташкент 2016
Тема: цели и задачи фармацевтической химии. Построение, показатели качества и виды нормативной документации Абдуллабекова Вилоятхон Нуруллабековна, д. ф. н. , зав. кафедрой фармацевтической химии Ташкент 2016
 План: n Предмет и содержание фармацевтической химии, её связь с другими науками n Классификация лекарственных средств (ЛС) n Пути получения лекарственных веществ (ЛВ) n Виды нормативной документации
План: n Предмет и содержание фармацевтической химии, её связь с другими науками n Классификация лекарственных средств (ЛС) n Пути получения лекарственных веществ (ЛВ) n Виды нормативной документации
 n Фармацевтическая химия — наука, которая, базируясь на общих законах химических наук, исследует способы по лучения, строение, физические и химические свойства лекарственных веществ, взаимосвязь между их химической струк турой и действием на организм, методы контроля качества и изменения, происходящие при хранении.
n Фармацевтическая химия — наука, которая, базируясь на общих законах химических наук, исследует способы по лучения, строение, физические и химические свойства лекарственных веществ, взаимосвязь между их химической струк турой и действием на организм, методы контроля качества и изменения, происходящие при хранении.
 n Основными методами исследования лекарственных веществ в фармацевтической химии являются анализ и син тез — диалектически тесно связанные между собой процессы, взаимно дополняющие друга. Анализ и синтез — мощ ные средства познания сущности явлений, происходящих в природе
n Основными методами исследования лекарственных веществ в фармацевтической химии являются анализ и син тез — диалектически тесно связанные между собой процессы, взаимно дополняющие друга. Анализ и синтез — мощ ные средства познания сущности явлений, происходящих в природе
 n Задачи, стоящие перед фармацевтической химией, решаются с помощью классических физических, химических и физико химических методов, которые используются как для синтеза, так и для анализа лекарственных веществ.
n Задачи, стоящие перед фармацевтической химией, решаются с помощью классических физических, химических и физико химических методов, которые используются как для синтеза, так и для анализа лекарственных веществ.
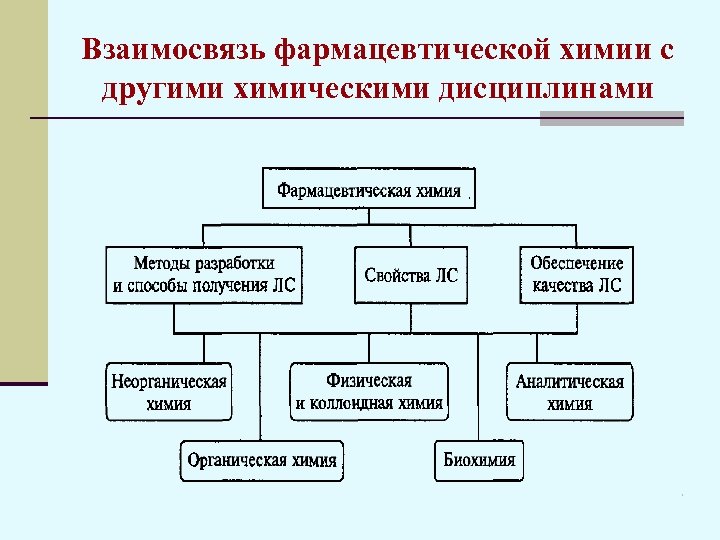 Взаимосвязь фармацевтической химии с другими химическими дисциплинами
Взаимосвязь фармацевтической химии с другими химическими дисциплинами
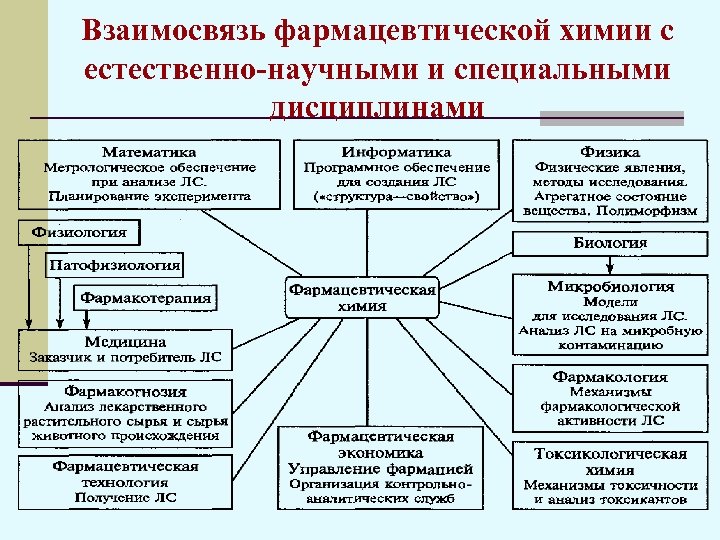 Взаимосвязь фармацевтической химии с естественно-научными и специальными дисциплинами
Взаимосвязь фармацевтической химии с естественно-научными и специальными дисциплинами
 Объекты фармацевтической химии n Лекарственные вещества (ЛВ) (субстанции) — разрешенные в медицинскую практику индивидуальные вещества растительного, животного, микробного или синтетического происхождения, обладающие фармакологической, иммунологической или метаболической активностью или предназначенные для диагностики. n Лекарственные средства –лекарственные вещества и средства, полученные на основе вспомогательных веществ, лекарственные препараты а разрешенные к применению для профилактики, диагностики и лечения, а также для изменения человеческого состояния и его функций.
Объекты фармацевтической химии n Лекарственные вещества (ЛВ) (субстанции) — разрешенные в медицинскую практику индивидуальные вещества растительного, животного, микробного или синтетического происхождения, обладающие фармакологической, иммунологической или метаболической активностью или предназначенные для диагностики. n Лекарственные средства –лекарственные вещества и средства, полученные на основе вспомогательных веществ, лекарственные препараты а разрешенные к применению для профилактики, диагностики и лечения, а также для изменения человеческого состояния и его функций.
 Объекты фармацевтической химии n Лекарственные препараты дозированные упакованные ЛС, готовые к применению лекарственные средства. n Лекарственная форма - придаваемое ЛС или лекарственному растительному сырью удобное для применения состояние, при котором достигается необходимый лечебный эффект. К их числу относятся таблетки, гранулы, капсулы, порошки, суппозитории, настойки, экстракты, аэрозоли, мази, плас тыри, капли глазные, различные инъекционные ЛФ, глазные лекарственные пленки (ГЛП).
Объекты фармацевтической химии n Лекарственные препараты дозированные упакованные ЛС, готовые к применению лекарственные средства. n Лекарственная форма - придаваемое ЛС или лекарственному растительному сырью удобное для применения состояние, при котором достигается необходимый лечебный эффект. К их числу относятся таблетки, гранулы, капсулы, порошки, суппозитории, настойки, экстракты, аэрозоли, мази, плас тыри, капли глазные, различные инъекционные ЛФ, глазные лекарственные пленки (ГЛП).
 Объекты фармацевтической химии n Генерические лекарственные средства (генерики) - произведенные лекарственные препараты, эквивалентные патентованным, но изготовленные другим производителем. n Гомеопатические средства - лекарства, применяемые по гомеопатическим правилам и включенные в специальный раздел государственного реестра. n Гомеопатические лекарственные средства одно или многокомпонентные препараты, содер жащие, как правило, микродозы активных соеди нений, производящиеся по специальной техно логии и предназначенные для перорального, инъекционного или местного применения в виде различных лекарственных форм.
Объекты фармацевтической химии n Генерические лекарственные средства (генерики) - произведенные лекарственные препараты, эквивалентные патентованным, но изготовленные другим производителем. n Гомеопатические средства - лекарства, применяемые по гомеопатическим правилам и включенные в специальный раздел государственного реестра. n Гомеопатические лекарственные средства одно или многокомпонентные препараты, содер жащие, как правило, микродозы активных соеди нений, производящиеся по специальной техно логии и предназначенные для перорального, инъекционного или местного применения в виде различных лекарственных форм.
 n исходные продукты, используемые для получения Л В, промежуточные и побочные продукты синтеза, остаточные растворители, вспомогательные и другие вещества. n дженерики (генерические препараты). (На разработанный оригинальный ЛП фармацевтическая компания производитель получает патент, который подтверждает, что он является собственностью компании на определенный срок (обычно 20 лет). Патент обеспечивает эксклюзивное право на его реа лизацию без конкуренции со стороны других производителей. После истечения срока действия патента свободное произ водствои реализация данного ЛП разрешается всем другим компаниям. Он становится генерическим препаратом, или дженериком, но должен быть абсолютно идентичен оригинальному. Разница состоит только в отличии наименования, ко торое дает компания производитель).
n исходные продукты, используемые для получения Л В, промежуточные и побочные продукты синтеза, остаточные растворители, вспомогательные и другие вещества. n дженерики (генерические препараты). (На разработанный оригинальный ЛП фармацевтическая компания производитель получает патент, который подтверждает, что он является собственностью компании на определенный срок (обычно 20 лет). Патент обеспечивает эксклюзивное право на его реа лизацию без конкуренции со стороны других производителей. После истечения срока действия патента свободное произ водствои реализация данного ЛП разрешается всем другим компаниям. Он становится генерическим препаратом, или дженериком, но должен быть абсолютно идентичен оригинальному. Разница состоит только в отличии наименования, ко торое дает компания производитель).
 История развития фармацевтической химии n Период иатрохимии (лечебная химия)(16 17 вв. ). Основатель Парацельс (1493 1541) n Период зарождения первых химических теорий (17 19 вв. ) Основатели Георг Шталь (1660 1734 гг, теория «флагистон» ), Роберт Бойль (1627 1692 гг), М. В. Ломоносов (1711 1765 гг), Т. Е. Ловиц (1757 1804 гг), А. А. Иовский, В. А. Тихомиров, Н. Н. Зинин, Д. И. Менделеев и др. Первый профессор в области фармации А. П. Нелюбин (1785 1858 гг) начальник отдела фармацевтики Петербургской академии медицины хирургии
История развития фармацевтической химии n Период иатрохимии (лечебная химия)(16 17 вв. ). Основатель Парацельс (1493 1541) n Период зарождения первых химических теорий (17 19 вв. ) Основатели Георг Шталь (1660 1734 гг, теория «флагистон» ), Роберт Бойль (1627 1692 гг), М. В. Ломоносов (1711 1765 гг), Т. Е. Ловиц (1757 1804 гг), А. А. Иовский, В. А. Тихомиров, Н. Н. Зинин, Д. И. Менделеев и др. Первый профессор в области фармации А. П. Нелюбин (1785 1858 гг) начальник отдела фармацевтики Петербургской академии медицины хирургии
 Ведущие ученые Востока n Абу Бакр ар Розий (865 925 гг) “Сирлар китоби” n Абу Али ибн Сино (980 1037 гг) «Тиб қонунлари» n Абу Райхон Беруний (937 1048 гг) «Табобатда доришунослик»
Ведущие ученые Востока n Абу Бакр ар Розий (865 925 гг) “Сирлар китоби” n Абу Али ибн Сино (980 1037 гг) «Тиб қонунлари» n Абу Райхон Беруний (937 1048 гг) «Табобатда доришунослик»
 История развития химикофармацевтической промышленности n 1928 1932 гг и 1941 1945 гг n 1950 1956 гг производство антибиотиков n 1971 1982 гг разработано свыше 430 препаратов n 1991 г 1 января в реестре было зарегис трировано свыше 3284 наименований
История развития химикофармацевтической промышленности n 1928 1932 гг и 1941 1945 гг n 1950 1956 гг производство антибиотиков n 1971 1982 гг разработано свыше 430 препаратов n 1991 г 1 января в реестре было зарегис трировано свыше 3284 наименований
 Центры по разработке лекарственных препаратов n Всесоюзный научно исследовательский химико фармацевтический институт (Москва, 1920 г). А. П. Орехов, А. Ю. Магидсон, А. А. Байчиков и др. n Экспериментальный химико фармацевтический институт (1920 г), в дальнейшем Харьковский химико фармацевтический институт (1947 г). Анализ ЛП, синтез, разработка технологий получения ЛС. n химико фармацевтический научно исследовательский институт (Тбилиси, 1932 г)
Центры по разработке лекарственных препаратов n Всесоюзный научно исследовательский химико фармацевтический институт (Москва, 1920 г). А. П. Орехов, А. Ю. Магидсон, А. А. Байчиков и др. n Экспериментальный химико фармацевтический институт (1920 г), в дальнейшем Харьковский химико фармацевтический институт (1947 г). Анализ ЛП, синтез, разработка технологий получения ЛС. n химико фармацевтический научно исследовательский институт (Тбилиси, 1932 г)
 Центры по разработке лекарственных препаратов РУз n Институт химии природных соединений при АН Уз. Р n Институт биоорганической и биологической химии при АН Уз. Р n Институт химии при АН Уз. Р n Уз. КФТИ институт n Ташкентский фармацевтический институт и др.
Центры по разработке лекарственных препаратов РУз n Институт химии природных соединений при АН Уз. Р n Институт биоорганической и биологической химии при АН Уз. Р n Институт химии при АН Уз. Р n Уз. КФТИ институт n Ташкентский фармацевтический институт и др.
 Классификация лекарственных средств (ЛС) n Фармакологическая классификация (отражает принципы преимущественного действия ЛВ на ту или иную физиологическую систему (сердечно сосудистую, центральную нервную и т. д. ). Однако в одну и ту же группу при этом попадают JIB, различные по химическому строению) n Химическая классификация : неорганическая и органическая (орга нические ЛВ подразделяют на алифатические (ациклические) и циклические, последние в свою очередь — на карбоциклические (алициклические и ароматические) и гетероциклические соединения (позволяет очень четко распределить все ЛВ по груп пам и классам соединений в соответствии с их химической структурой. Но в одной и той же группе могут оказаться ЛВ с различным фармакологическим действием.
Классификация лекарственных средств (ЛС) n Фармакологическая классификация (отражает принципы преимущественного действия ЛВ на ту или иную физиологическую систему (сердечно сосудистую, центральную нервную и т. д. ). Однако в одну и ту же группу при этом попадают JIB, различные по химическому строению) n Химическая классификация : неорганическая и органическая (орга нические ЛВ подразделяют на алифатические (ациклические) и циклические, последние в свою очередь — на карбоциклические (алициклические и ароматические) и гетероциклические соединения (позволяет очень четко распределить все ЛВ по груп пам и классам соединений в соответствии с их химической структурой. Но в одной и той же группе могут оказаться ЛВ с различным фармакологическим действием.
 Классификация ЛС n фармакотерапевтическая классификация, разработанная проф. М. Д. Машковским. Она помогает установить, к какой группе относится ЛС, является ли оно новым или аналогом существую щих, каковы его синонимы, состав. По этой классификации ЛС распределены по характеру действия на системы, органы, процессы по 13 основным классам. Эти классы разделены на группы, а последние — на подгруппы исходя из следующих признаков: основные фармакологические свойства, основные области медицинского применения, сходство в химической структуре. Это дает представление о существовании связи между химической структурой и фармакологическим действи ем субстанций. В каждой группе (подгруппе) первыми представлены ЛС — «родоначальники» , характеризующие основ ные черты данной группы. Описание остальных дополняет и развивает представление о группе в целом. Ориентацию в «потоке» названий дает включение, помимо основных названий, большого количества синонимов.
Классификация ЛС n фармакотерапевтическая классификация, разработанная проф. М. Д. Машковским. Она помогает установить, к какой группе относится ЛС, является ли оно новым или аналогом существую щих, каковы его синонимы, состав. По этой классификации ЛС распределены по характеру действия на системы, органы, процессы по 13 основным классам. Эти классы разделены на группы, а последние — на подгруппы исходя из следующих признаков: основные фармакологические свойства, основные области медицинского применения, сходство в химической структуре. Это дает представление о существовании связи между химической структурой и фармакологическим действи ем субстанций. В каждой группе (подгруппе) первыми представлены ЛС — «родоначальники» , характеризующие основ ные черты данной группы. Описание остальных дополняет и развивает представление о группе в целом. Ориентацию в «потоке» названий дает включение, помимо основных названий, большого количества синонимов.
 Основные направления создания новых ЛВ n Эмперическое получение (на основе экспериментов) n Целенаправленный синтез
Основные направления создания новых ЛВ n Эмперическое получение (на основе экспериментов) n Целенаправленный синтез
 Основные направления создания новых ЛВ n Выделения и изучение БАВ n Химическая модификация структуры известных n n n синтетических и природных ЛВ Воспроизведение биогенных физиологически активных веществ Принцип молекулярного моделирования Создание ЛВ на основе естественных метаболитов Использование антиметаболитов Генная фармакология (клонирование) Использование комбинаторной химии
Основные направления создания новых ЛВ n Выделения и изучение БАВ n Химическая модификация структуры известных n n n синтетических и природных ЛВ Воспроизведение биогенных физиологически активных веществ Принцип молекулярного моделирования Создание ЛВ на основе естественных метаболитов Использование антиметаболитов Генная фармакология (клонирование) Использование комбинаторной химии
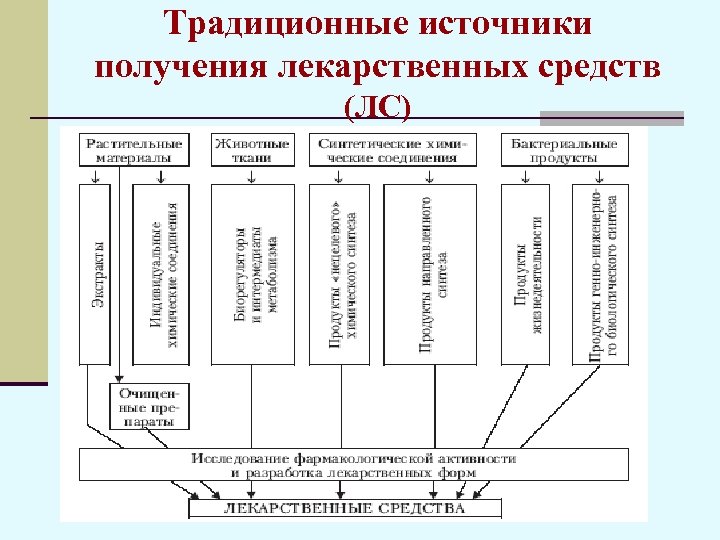 Традиционные источники получения лекарственных средств (ЛС)
Традиционные источники получения лекарственных средств (ЛС)
 Разработка нового JIB включает: n n n n Замысел создания нового ЛВ. Он возникает обычно в результате совместной работы ученых двух специальностей: фармакологов и химиков синтетиков. Уже на этой стадии осуществляется предварительный отбор синтезированных со единений, которые, по мнению специалистов, могут быть потенциально биологически активными веществами. Синтез предварительно отобранных структур. На этой стадии также осуществляется отбор, в результате которого ве щества, отличающиеся нестабильностью, невозможностью или чрезмерной трудоемкостью синтеза, дороговизной исход ных веществ и т. д. , не подвергаются дальнейшему исследованию. Фармакологический скрининг и доклинические испытания. Основной этап, во время которого отсеиваются неперспективные вещества, синтезированные на предыдущем этапе. Клиническая проверка. Ее выполняют только для перспективных БАВ, которые прошли все этапы фармакологиче ского скрининга. Разработка технологии производства нового Л В и наиболее рациональной ЛФ. Подготовка нормативной документации, включающей способы контроля качества как самого ЛВ, так и его ЛФ. Внедрение ЛВ в промышленное производство и отработка всех стадий его получения в заводских условиях.
Разработка нового JIB включает: n n n n Замысел создания нового ЛВ. Он возникает обычно в результате совместной работы ученых двух специальностей: фармакологов и химиков синтетиков. Уже на этой стадии осуществляется предварительный отбор синтезированных со единений, которые, по мнению специалистов, могут быть потенциально биологически активными веществами. Синтез предварительно отобранных структур. На этой стадии также осуществляется отбор, в результате которого ве щества, отличающиеся нестабильностью, невозможностью или чрезмерной трудоемкостью синтеза, дороговизной исход ных веществ и т. д. , не подвергаются дальнейшему исследованию. Фармакологический скрининг и доклинические испытания. Основной этап, во время которого отсеиваются неперспективные вещества, синтезированные на предыдущем этапе. Клиническая проверка. Ее выполняют только для перспективных БАВ, которые прошли все этапы фармакологиче ского скрининга. Разработка технологии производства нового Л В и наиболее рациональной ЛФ. Подготовка нормативной документации, включающей способы контроля качества как самого ЛВ, так и его ЛФ. Внедрение ЛВ в промышленное производство и отработка всех стадий его получения в заводских условиях.
 ЗАКОНОДАТЕЛЬНАЯ БАЗА, РЕГЛАМЕНТИРУЮЩАЯ ФАРМАЦЕВТИЧЕСКУЮ ДЕЯТЕЛЬНОСТЬ В УЗБЕКИСТАНЕ n n n n n «О ЛЕКАРСТВЕННЫХ СРЕДСТВАХ И ФАРМАЦЕВТИЧЕСКОЙ ДЕЯТЕЛЬНОСТИ» (25 апрель 1997, 1999, 2006, 2009, 2014, 2016 г 4 январь) «О СЕРТИФИКАЦИИ ПРОДУКЦИИ И УСЛУГ» (28 декабрь 1993 й. ) «ОБ ОХРАНЕ ЗДОРОВЬЯ ГРАЖДАН» (29 август 1996 й. ) (1997 й. , 1999 г, 2009 г, август) «О НАРКОТИЧЕСКИХ СРЕДСТВАХ И ПСИХОТРОПНЫХ ВЕЩЕСТВАХ» (19 август 1999 й. ) «О ЛИЦЕНЗИРОВАНИИ ОТДЕЛЬНЫХ ВИДОВ ДЕЯТЕЛЬНОСТИ» (25 май 2000 й. ) «О ЗАЩИТЕ ПРАВ ПОТРЕБИТЕЛЕЙ» (26 апрель 1996 й. ) «О СТАНДАРТИЗАЦИИ» 28 декабрь 1993 й. ) «О МЕТРОЛОГИИ» (29 август 1996 й. ) «О РЕКЛАМЕ» (25 декабрь 1998 й. )
ЗАКОНОДАТЕЛЬНАЯ БАЗА, РЕГЛАМЕНТИРУЮЩАЯ ФАРМАЦЕВТИЧЕСКУЮ ДЕЯТЕЛЬНОСТЬ В УЗБЕКИСТАНЕ n n n n n «О ЛЕКАРСТВЕННЫХ СРЕДСТВАХ И ФАРМАЦЕВТИЧЕСКОЙ ДЕЯТЕЛЬНОСТИ» (25 апрель 1997, 1999, 2006, 2009, 2014, 2016 г 4 январь) «О СЕРТИФИКАЦИИ ПРОДУКЦИИ И УСЛУГ» (28 декабрь 1993 й. ) «ОБ ОХРАНЕ ЗДОРОВЬЯ ГРАЖДАН» (29 август 1996 й. ) (1997 й. , 1999 г, 2009 г, август) «О НАРКОТИЧЕСКИХ СРЕДСТВАХ И ПСИХОТРОПНЫХ ВЕЩЕСТВАХ» (19 август 1999 й. ) «О ЛИЦЕНЗИРОВАНИИ ОТДЕЛЬНЫХ ВИДОВ ДЕЯТЕЛЬНОСТИ» (25 май 2000 й. ) «О ЗАЩИТЕ ПРАВ ПОТРЕБИТЕЛЕЙ» (26 апрель 1996 й. ) «О СТАНДАРТИЗАЦИИ» 28 декабрь 1993 й. ) «О МЕТРОЛОГИИ» (29 август 1996 й. ) «О РЕКЛАМЕ» (25 декабрь 1998 й. )
 Справочники «Фармацевтическая деятельность в Республике Узбекистан» (правовые, нормативные и справочные данные) 35
Справочники «Фармацевтическая деятельность в Республике Узбекистан» (правовые, нормативные и справочные данные) 35
 НОРМАТИВНЫЕ ДОКУМЕНТЫ n n n n ОСТ 42 1 71 «Порядок разработки, согласования и утверждения нормативно технической документации на лекарственные средства и лекарственное растительное сырье» . РД 42 28 36 90 “Методические указания. Маркировка потребительской, индивидуальной, групповой и транспортной тары на медицинские иммунобиологические препараты. Типы и размеры групповой и индивидуальной тары”. МУ СНГ – 01 96 «Методические указания по разработке проектов аналитической нормативной документации на лекарственные средства, представляемые на регистрацию в страны СНГ» . О`z. DSt 1. 0: 1998 «Государственная система стандартизации РУз. Основные положения» . О`z. DSt 1. 10: 1998 ГСС Уз «Основные термины и определения» . РСТ Уз 1. 1. 92 ГСС Уз «Порядок разработки, согласования, утверждения и регистрации государственных стандартов РУз» . РСТ 1. 9 95 ГСС Уз «Порядок разработки, согласования, утверждения и регистрации отраслевых стандартов» . RH 19 11 2000 «Графическое оформление упаковки лекарственных средств и рекламно сопроводительной документации» .
НОРМАТИВНЫЕ ДОКУМЕНТЫ n n n n ОСТ 42 1 71 «Порядок разработки, согласования и утверждения нормативно технической документации на лекарственные средства и лекарственное растительное сырье» . РД 42 28 36 90 “Методические указания. Маркировка потребительской, индивидуальной, групповой и транспортной тары на медицинские иммунобиологические препараты. Типы и размеры групповой и индивидуальной тары”. МУ СНГ – 01 96 «Методические указания по разработке проектов аналитической нормативной документации на лекарственные средства, представляемые на регистрацию в страны СНГ» . О`z. DSt 1. 0: 1998 «Государственная система стандартизации РУз. Основные положения» . О`z. DSt 1. 10: 1998 ГСС Уз «Основные термины и определения» . РСТ Уз 1. 1. 92 ГСС Уз «Порядок разработки, согласования, утверждения и регистрации государственных стандартов РУз» . РСТ 1. 9 95 ГСС Уз «Порядок разработки, согласования, утверждения и регистрации отраслевых стандартов» . RH 19 11 2000 «Графическое оформление упаковки лекарственных средств и рекламно сопроводительной документации» .
 Виды стандартов 1. Международные — принятые ИСО или др уполномоченными международными организациями по стандартизации отдельных видов продукции, например ЕКН и ЕКЭН; имеют рекомендательный статус. 2. Межгосударственные — принятые рядом стран Содружества независимых гос в (СНГ). Их применяют на основании постановления национального комитета по стандарт и без переоформления. Основное положения по этой категории стандартов регламентируются. ГОСТ 1. 0 – 92, ГОСТ 1. 1. – 2002, ГОСТ 1. 2 – 97, ГОСТ 1. 5 – 2001. 3. Национальные (принятые национальным органом РУз). Их разрабатывают на продукцию и услуги, имеющие межотраслевое значение.
Виды стандартов 1. Международные — принятые ИСО или др уполномоченными международными организациями по стандартизации отдельных видов продукции, например ЕКН и ЕКЭН; имеют рекомендательный статус. 2. Межгосударственные — принятые рядом стран Содружества независимых гос в (СНГ). Их применяют на основании постановления национального комитета по стандарт и без переоформления. Основное положения по этой категории стандартов регламентируются. ГОСТ 1. 0 – 92, ГОСТ 1. 1. – 2002, ГОСТ 1. 2 – 97, ГОСТ 1. 5 – 2001. 3. Национальные (принятые национальным органом РУз). Их разрабатывают на продукцию и услуги, имеющие межотраслевое значение.
 n Отраслевой стандарт (ОСТ) — принимается гос органом управления в пределах его компетенции. Он обязателен для всех предприятий и орг ций др отраслей, применяющих или потребляющих продукцию этой отрасли. Такие стандарты устанавливаются на сырье, полуфабрикаты, используемые в данной отрасли, а также на отдельные виды товаров народ го потреб я. Утверждаются ОСТ министерством (ведомством), являющимся ведущим в пр ве данной продукции. Осн е внимание при разработке этой группы стандартов обращается на переход от стандартизации однородных групп продукции к стандартам на технолог е процессы и комплексные методы оценки, а также вопросам техн го обслуживания и калибровки изделий. n Стандарт предприятия (СП) — принимается предприятием. Он отражает присущие каждому предприятию особенности технол го процесса получения товара и сод т перечень пок лей качества, кот д. б. не ниже треб й ГОСТа или ОСТа на аналогичную продукцию. n Технические условия (ТУ Уз)– НД, устанав щий техн е треб я на конкретную продукцию (услугу) утверждённый или разработчиком (изготовителем) по согласованию с заказчиком, или разработчиком (изготовителем) совместно с заказчиком.
n Отраслевой стандарт (ОСТ) — принимается гос органом управления в пределах его компетенции. Он обязателен для всех предприятий и орг ций др отраслей, применяющих или потребляющих продукцию этой отрасли. Такие стандарты устанавливаются на сырье, полуфабрикаты, используемые в данной отрасли, а также на отдельные виды товаров народ го потреб я. Утверждаются ОСТ министерством (ведомством), являющимся ведущим в пр ве данной продукции. Осн е внимание при разработке этой группы стандартов обращается на переход от стандартизации однородных групп продукции к стандартам на технолог е процессы и комплексные методы оценки, а также вопросам техн го обслуживания и калибровки изделий. n Стандарт предприятия (СП) — принимается предприятием. Он отражает присущие каждому предприятию особенности технол го процесса получения товара и сод т перечень пок лей качества, кот д. б. не ниже треб й ГОСТа или ОСТа на аналогичную продукцию. n Технические условия (ТУ Уз)– НД, устанав щий техн е треб я на конкретную продукцию (услугу) утверждённый или разработчиком (изготовителем) по согласованию с заказчиком, или разработчиком (изготовителем) совместно с заказчиком.
 Стандарты качества ЛС n Стандарт качества лекарственного средства - нормативный документ, содержащий перечень нормируемых показателей и методов контроля качества лекарственных средств. Он должен : n обеспечивать разработку и производство качественного, эффективного и безопасного ЛС. n своевременно пересматриваться с учетом новых достижений медицинской, фармацевтической и других наук и требований ведущих зарубежных фармакопей (рекомендаций ведущих международных организаций в области фармацевтической науки). n Требования Государственных стандартов качества ЛС являются обязательными для всех предприятий и организаций, занятых в сфере обращения ЛС.
Стандарты качества ЛС n Стандарт качества лекарственного средства - нормативный документ, содержащий перечень нормируемых показателей и методов контроля качества лекарственных средств. Он должен : n обеспечивать разработку и производство качественного, эффективного и безопасного ЛС. n своевременно пересматриваться с учетом новых достижений медицинской, фармацевтической и других наук и требований ведущих зарубежных фармакопей (рекомендаций ведущих международных организаций в области фармацевтической науки). n Требования Государственных стандартов качества ЛС являются обязательными для всех предприятий и организаций, занятых в сфере обращения ЛС.
 Стандарты качества ЛС n Фармакопея - сборник государственных стандартов и положений, нормирующих качество лекарственных средств, имеет законодательный характер. Изложенные стандарты и нормативы применяются при анализе, хранении ЛС, они являются обязательными для фармацевтов, врача, а также всех организаций и учреждений, которые изучают, хранят, отпускают, контролируют и применяют ЛС.
Стандарты качества ЛС n Фармакопея - сборник государственных стандартов и положений, нормирующих качество лекарственных средств, имеет законодательный характер. Изложенные стандарты и нормативы применяются при анализе, хранении ЛС, они являются обязательными для фармацевтов, врача, а также всех организаций и учреждений, которые изучают, хранят, отпускают, контролируют и применяют ЛС.

 Государственные стандарты качества лекарственных средств n Общая фармакопейная статья (ОФС) n Фармакопейная статья (ФС) n Временная фармакопейная статья (ВФС)
Государственные стандарты качества лекарственных средств n Общая фармакопейная статья (ОФС) n Фармакопейная статья (ФС) n Временная фармакопейная статья (ВФС)
 Стандарты качества ЛС n Временная фармакопейная статья (ВФС) - Государственный стандарт качества на лекарственные средства и лекарственное растительное сырьё, разрабатываемый на первые промышленные (установочные) серии новых лекарственных средств, рекомендованных для медицинского применения и намеченных к серийному производству. Утверждается Фармакопейным комитетом Главного управления по контролю качества лекарственных средств и медицинской техники Министерства здравоохранения Республики Узбекистан. n Фармакопейная статья предприятия (ФСП) - стандарт качества на лекарственное средство под торговым названием, содержащий перечень показателей и методов контроля качества лекарственного средства для производства конкретного предприятия, учитывающий конкретный состав и технологию данного предприятия, и прошедший экспертизу и регистрацию в Фармакопейном комитете Главного управления по контролю качества лекарственных средств и медицинской техники Министерства здравоохранения Республики Узбекистан.
Стандарты качества ЛС n Временная фармакопейная статья (ВФС) - Государственный стандарт качества на лекарственные средства и лекарственное растительное сырьё, разрабатываемый на первые промышленные (установочные) серии новых лекарственных средств, рекомендованных для медицинского применения и намеченных к серийному производству. Утверждается Фармакопейным комитетом Главного управления по контролю качества лекарственных средств и медицинской техники Министерства здравоохранения Республики Узбекистан. n Фармакопейная статья предприятия (ФСП) - стандарт качества на лекарственное средство под торговым названием, содержащий перечень показателей и методов контроля качества лекарственного средства для производства конкретного предприятия, учитывающий конкретный состав и технологию данного предприятия, и прошедший экспертизу и регистрацию в Фармакопейном комитете Главного управления по контролю качества лекарственных средств и медицинской техники Министерства здравоохранения Республики Узбекистан.
 Фармакопейная статья (ФС) n Государственный стандарт качества на ЛС серийного производства, утвержденный Фармакопейным комитетом Главного управления по контролю качества лекарственных средств и медицинской техники Министерства здравоохранения РУз. разрабатывается на лекарственное средство под МНН (для монокомпонентных лекарственных средств) и содержит обязательный перечень показателей и методов контроля качества (с учетом его лекарственной формы), соответствующих требованиям действующей фармакопеи. Общие фармакопейные статьи и фармакопейные статьи разрабатываются и пересматриваются через 5 лет. а ВФС не более 3 лет.
Фармакопейная статья (ФС) n Государственный стандарт качества на ЛС серийного производства, утвержденный Фармакопейным комитетом Главного управления по контролю качества лекарственных средств и медицинской техники Министерства здравоохранения РУз. разрабатывается на лекарственное средство под МНН (для монокомпонентных лекарственных средств) и содержит обязательный перечень показателей и методов контроля качества (с учетом его лекарственной формы), соответствующих требованиям действующей фармакопеи. Общие фармакопейные статьи и фармакопейные статьи разрабатываются и пересматриваются через 5 лет. а ВФС не более 3 лет.
 Общая фармакопейная статья (ОФС) n Государственный стандарт качества ЛС, содержащий основные требования к ЛФ и/или описание стандартных методов контроля ЛС. ОФС включает в себя перечень нормируемых показателей или методов испытания для конкретной ЛФ, описание физических, физико химических, биохимических, биологических, микробиологических методов анализа ЛС, требования к используемым реактивам, титрованным растворам, индикаторам. –
Общая фармакопейная статья (ОФС) n Государственный стандарт качества ЛС, содержащий основные требования к ЛФ и/или описание стандартных методов контроля ЛС. ОФС включает в себя перечень нормируемых показателей или методов испытания для конкретной ЛФ, описание физических, физико химических, биохимических, биологических, микробиологических методов анализа ЛС, требования к используемым реактивам, титрованным растворам, индикаторам. –
 Перечень разделов ФС, ВФС и ФСП * Лекарственное вещество (субстанция) 1. Название препарата на латинском, государственном и русском языках 2. Международное непатентованное название (МНН) 3. Химическое название в соответствии с требованиями ИЮПАК 4. Структурная и эмпирическая формулы и молекулярная масса 5. Содержание действующего вещества (в процентах или ЕД) 6. Описание 7. Растворимость 8. Подлинность 9. Температура плавления (разложения) или температура затвердевания, или температура кипения 10. Плотность 11. Удельное вращение 12. Удельный показатель поглощения 13. Показатель преломления 14. Прозрачность раствора 15. Цветность раствора 16. р. Н или кислотность, или щелочность 17. Механические включения 18. Посторонние примеси (родственные соединения) 19. Показатели чистоты (хлориды, сульфаты и т. п. )
Перечень разделов ФС, ВФС и ФСП * Лекарственное вещество (субстанция) 1. Название препарата на латинском, государственном и русском языках 2. Международное непатентованное название (МНН) 3. Химическое название в соответствии с требованиями ИЮПАК 4. Структурная и эмпирическая формулы и молекулярная масса 5. Содержание действующего вещества (в процентах или ЕД) 6. Описание 7. Растворимость 8. Подлинность 9. Температура плавления (разложения) или температура затвердевания, или температура кипения 10. Плотность 11. Удельное вращение 12. Удельный показатель поглощения 13. Показатель преломления 14. Прозрачность раствора 15. Цветность раствора 16. р. Н или кислотность, или щелочность 17. Механические включения 18. Посторонние примеси (родственные соединения) 19. Показатели чистоты (хлориды, сульфаты и т. п. )
 Перечень разделов ФС, ВФС и ФСП * Лекарственное вещество (субстанция) n 21. Потеря в массе при n n n n n высушивании или вода, определяемая методом К. Фишера 22. Остаточные органические растворители (в случае их использования на последней стадии технологического процесса) 23. Пирогенность или содержание бактериальных эндотоксинов (ЛАЛ тест) 24. Токсичность 25. Содержание веществ гистаминоподобного действия 26. Микробиологическая чистота (стерильность) 27. Количественное определение n 20. Сульфатная зола и n n n n тяжелые металлы 28. Упаковка 29. Маркировка 30. Транспортирование 31. Хранение 32. Срок годности 33. Основное фармакологической действие * По мере разработки новых лекарственных форм, внедрения современных методов контроля качества, использования новых упаковочных материалов возможно внесение дополнительных разделов в настоящие перечни
Перечень разделов ФС, ВФС и ФСП * Лекарственное вещество (субстанция) n 21. Потеря в массе при n n n n n высушивании или вода, определяемая методом К. Фишера 22. Остаточные органические растворители (в случае их использования на последней стадии технологического процесса) 23. Пирогенность или содержание бактериальных эндотоксинов (ЛАЛ тест) 24. Токсичность 25. Содержание веществ гистаминоподобного действия 26. Микробиологическая чистота (стерильность) 27. Количественное определение n 20. Сульфатная зола и n n n n тяжелые металлы 28. Упаковка 29. Маркировка 30. Транспортирование 31. Хранение 32. Срок годности 33. Основное фармакологической действие * По мере разработки новых лекарственных форм, внедрения современных методов контроля качества, использования новых упаковочных материалов возможно внесение дополнительных разделов в настоящие перечни
 Лекарственные формы для инъекций (растворы для инъекций, суспензии, эмульсии) 1. Название препарата на латинском, государственном и русском языках 2. МНН 3. Состав 4. Описание 5. Условия стерилизации и разлива 6. Подлинность 7. Прозрачность 8. Цветность 9. р. Н или кислотность, или щелочность 10. Механические включения 11. Плотность 12. Вязкость 13. Посторонние примеси (родственные соединения) 14. Осмолярность 15. Объем заполнения (ампул, флаконов и т. п. ) 16. Пирогенность или бактериальные эндотоксины (ЛАЛ тест) 17. Токсичность 18. Содержание веществ гистаминоподобного действия 19. Стерильность. 20. Размер частиц (в случае суспензии) 21. Количественное определение 22. Упаковка 23. Маркировка 24. Транспортирование 25. Хранение 26. Срок годности 27. Основное фармакологической действие
Лекарственные формы для инъекций (растворы для инъекций, суспензии, эмульсии) 1. Название препарата на латинском, государственном и русском языках 2. МНН 3. Состав 4. Описание 5. Условия стерилизации и разлива 6. Подлинность 7. Прозрачность 8. Цветность 9. р. Н или кислотность, или щелочность 10. Механические включения 11. Плотность 12. Вязкость 13. Посторонние примеси (родственные соединения) 14. Осмолярность 15. Объем заполнения (ампул, флаконов и т. п. ) 16. Пирогенность или бактериальные эндотоксины (ЛАЛ тест) 17. Токсичность 18. Содержание веществ гистаминоподобного действия 19. Стерильность. 20. Размер частиц (в случае суспензии) 21. Количественное определение 22. Упаковка 23. Маркировка 24. Транспортирование 25. Хранение 26. Срок годности 27. Основное фармакологической действие
 Фармацевтическая терминология n Стандартные образцы (СО), применяемые для контроля качества лекарственных средств - это вещества, с которыми проводят сравнение испытуемых лекарственных средств при проведении их анализа с использованием физико химических и биологических методов. СО подразделяются условно на химические и биологические; один и тот же СО в соответствии с указаниями фармакопейной статьи может быть использован и для физико химических, и для биологических анализов. n Государственный стандартный образец (ГСО) - это стандартный образец, параметры качества которого регламентируются фармакопейной статьей, утвержденной в установленном порядке. В анализе готовых лекарственных форм могут использоваться рабочие стандартные образцы (РСО) лекарственных веществ (субстанций). РСО это образец серийной субстанции, отвечающий требованиям соответствующего стандарта качества лекарственных средств.
Фармацевтическая терминология n Стандартные образцы (СО), применяемые для контроля качества лекарственных средств - это вещества, с которыми проводят сравнение испытуемых лекарственных средств при проведении их анализа с использованием физико химических и биологических методов. СО подразделяются условно на химические и биологические; один и тот же СО в соответствии с указаниями фармакопейной статьи может быть использован и для физико химических, и для биологических анализов. n Государственный стандартный образец (ГСО) - это стандартный образец, параметры качества которого регламентируются фармакопейной статьей, утвержденной в установленном порядке. В анализе готовых лекарственных форм могут использоваться рабочие стандартные образцы (РСО) лекарственных веществ (субстанций). РСО это образец серийной субстанции, отвечающий требованиям соответствующего стандарта качества лекарственных средств.
 Фармацевтическая терминология n Регистрационное удостоверение - документ, подтверждающий разрешение Министерства здравоохранения Республики Узбекистан на право медицинского применения лекарственного средства. n Государственный реестр лекарственных средств и изделий медицинского назначения официальный документ, представляющий собой перечень лекарственных средств и изделий медицинского назначения, разрешенных к применению в медицинской практике.
Фармацевтическая терминология n Регистрационное удостоверение - документ, подтверждающий разрешение Министерства здравоохранения Республики Узбекистан на право медицинского применения лекарственного средства. n Государственный реестр лекарственных средств и изделий медицинского назначения официальный документ, представляющий собой перечень лекарственных средств и изделий медицинского назначения, разрешенных к применению в медицинской практике.
 Фармацевтическая терминология n Международное непатентованное название (МНН) (International Nonproprietary Names) - название лекарственного средства, принятое Всемирной организацией здравоохранения (ВОЗ). (в названии ЛВ ориентировочно дается его групповая принадлежность. Это достигается за счет включения в название частей слов, соответствующих фармакотерапевтической группе, к которой относится данное ЛВ). n Патентованное лекарственное средство- это лекарственное средство, на которое имеется охранный документ (патент), наличие которого дает производителю исключительное право на его производство. n Серия - определенное количество готовой продукции (лекарственного средства), полученное в одном технологическом процессе или в ряде последовательных технологических процессов при обработке определенного количества исходного сырья, упаковочных материалов или полупродуктов, характерным качеством которой является однородность.
Фармацевтическая терминология n Международное непатентованное название (МНН) (International Nonproprietary Names) - название лекарственного средства, принятое Всемирной организацией здравоохранения (ВОЗ). (в названии ЛВ ориентировочно дается его групповая принадлежность. Это достигается за счет включения в название частей слов, соответствующих фармакотерапевтической группе, к которой относится данное ЛВ). n Патентованное лекарственное средство- это лекарственное средство, на которое имеется охранный документ (патент), наличие которого дает производителю исключительное право на его производство. n Серия - определенное количество готовой продукции (лекарственного средства), полученное в одном технологическом процессе или в ряде последовательных технологических процессов при обработке определенного количества исходного сырья, упаковочных материалов или полупродуктов, характерным качеством которой является однородность.
 Организация контроля качества ЛС n В концепции развития здравоохранения и медицинской науки одним из основополагающих принципов стало совершенствование лекарственного обеспечения, гарантии в области лекарственной и медицинской помощи. n Одной из основных задач государства является обеспечение высокого качества лекарственных средств и медицинских изделий. Это возможно лишь при эффективной системе контроля качества. n Закон Республики Узбекистан «О лекарственных средствах и фармацевтической деятельности» определил приоритетность государственного контроля производства, изготовления, качества, эффективности и безопасности лекарственных средств и медицинских изделий.
Организация контроля качества ЛС n В концепции развития здравоохранения и медицинской науки одним из основополагающих принципов стало совершенствование лекарственного обеспечения, гарантии в области лекарственной и медицинской помощи. n Одной из основных задач государства является обеспечение высокого качества лекарственных средств и медицинских изделий. Это возможно лишь при эффективной системе контроля качества. n Закон Республики Узбекистан «О лекарственных средствах и фармацевтической деятельности» определил приоритетность государственного контроля производства, изготовления, качества, эффективности и безопасности лекарственных средств и медицинских изделий.
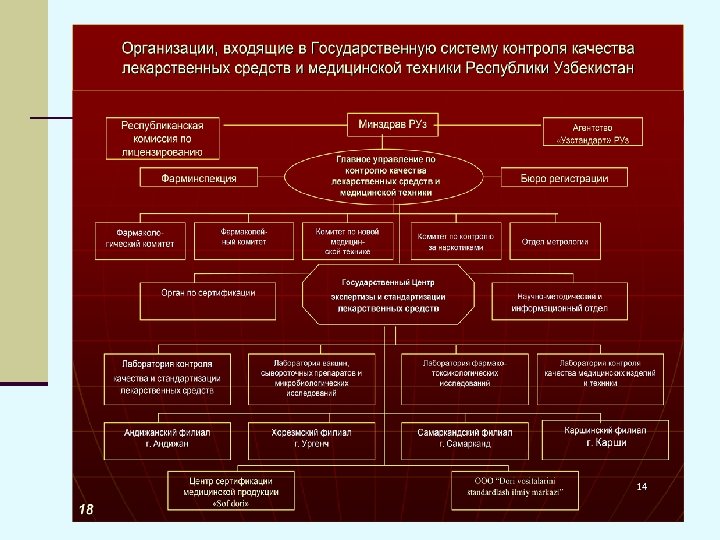
 Постановлением Кабинета Министров Республики Узбекистан № 181 от 25 мая 1995 г. организовано Главное управление по контролю качества лекарственных средств и медицинской техники МЗ РУз. n На Главное управление возложены вопросы организации и осуществление государственного контроля качества лекарственных и диагностических средств, медицинской техники и изделий медицинского назначения, координацию деятельности и руководство учреждениями и организациями, осуществляющими экспертизу, стандартизацию, регистрацию и сертификацию лекарственных средств и медицинских изделий, продуктов лечебного питания и медицинской техники.
Постановлением Кабинета Министров Республики Узбекистан № 181 от 25 мая 1995 г. организовано Главное управление по контролю качества лекарственных средств и медицинской техники МЗ РУз. n На Главное управление возложены вопросы организации и осуществление государственного контроля качества лекарственных и диагностических средств, медицинской техники и изделий медицинского назначения, координацию деятельности и руководство учреждениями и организациями, осуществляющими экспертизу, стандартизацию, регистрацию и сертификацию лекарственных средств и медицинских изделий, продуктов лечебного питания и медицинской техники.
 Вопросы n n Предмет фармацевтической химии. n Содержание фармацевтической химии. n Связь фармацевтической химии с другими науками n Краткая история развития фармацевтической химии n Классификация лекарственных средств (ЛС) n Пути получения лекарственных веществ (ЛВ) n Виды нормативной документации n Стандарты качества ЛС (ВФС, ФСП, ОФС) n Виды стандартов
Вопросы n n Предмет фармацевтической химии. n Содержание фармацевтической химии. n Связь фармацевтической химии с другими науками n Краткая история развития фармацевтической химии n Классификация лекарственных средств (ЛС) n Пути получения лекарственных веществ (ЛВ) n Виды нормативной документации n Стандарты качества ЛС (ВФС, ФСП, ОФС) n Виды стандартов
 Литература: n 1. Закон РУз «О стандартизации» от 28 декабря 1993 года. n 2. ГФ XI издания. Том 1. 1997 г. n 3. Узбекистон Республикасида фармацевтика фаолияти. I, III т. n n 2001, г 2003 г 4. Стандарты качества ЛС. Основные положения. TSt 42 01: 2002 5. Закон «О лекарственных средствах и фармацевтической деятельности» РУз от 04. 01. 2016 № 399 6. Беликов В. Г. Фармацевтическая химия, М. , “МЕДпресс информ”, 2009 г. 7. Арзамасцев А. П. Фармацевтическая химия, М. , ”ГЕОТАР Медиа”, 2008 г.
Литература: n 1. Закон РУз «О стандартизации» от 28 декабря 1993 года. n 2. ГФ XI издания. Том 1. 1997 г. n 3. Узбекистон Республикасида фармацевтика фаолияти. I, III т. n n 2001, г 2003 г 4. Стандарты качества ЛС. Основные положения. TSt 42 01: 2002 5. Закон «О лекарственных средствах и фармацевтической деятельности» РУз от 04. 01. 2016 № 399 6. Беликов В. Г. Фармацевтическая химия, М. , “МЕДпресс информ”, 2009 г. 7. Арзамасцев А. П. Фармацевтическая химия, М. , ”ГЕОТАР Медиа”, 2008 г.


