Методы цитологического анализа.ppt
- Количество слайдов: 29
 Тема 9. Методы цитологического анализа Световая микроскопия, электронная микроскопия, культура клеток, микробиохимия 1
Тема 9. Методы цитологического анализа Световая микроскопия, электронная микроскопия, культура клеток, микробиохимия 1
 Тема 9. Методы цитологического анализа Объекты цитологии • Объектами цитологии являются клетки в составе тканей, отдельные клетки, структуры межклеточного вещества, внутриклеточные органеллы клеток. • Для понимания функциональной организации клеток и внутриклеточных структур цитология изучает их химический состав, системы регуляции и физиологические параметры. • Для получения информации о клеточной биохимии используются не только данные класcичеcкой биохимии, но и специальные методы цито- и гистохимии и микробиохимии. • Объекты цитологии могут быть получены из естественных источников (дикие виды животных и растений, микроорганизмы, лабораторные виды животных и растений) и искусственных источников – культура тканей и клеток. • Цитология использует большой набор специальных методов и технологий для получения информации. Важнейшее место в этом наборе занимают различные методы микроскопии. Лекция 9(29) 2
Тема 9. Методы цитологического анализа Объекты цитологии • Объектами цитологии являются клетки в составе тканей, отдельные клетки, структуры межклеточного вещества, внутриклеточные органеллы клеток. • Для понимания функциональной организации клеток и внутриклеточных структур цитология изучает их химический состав, системы регуляции и физиологические параметры. • Для получения информации о клеточной биохимии используются не только данные класcичеcкой биохимии, но и специальные методы цито- и гистохимии и микробиохимии. • Объекты цитологии могут быть получены из естественных источников (дикие виды животных и растений, микроорганизмы, лабораторные виды животных и растений) и искусственных источников – культура тканей и клеток. • Цитология использует большой набор специальных методов и технологий для получения информации. Важнейшее место в этом наборе занимают различные методы микроскопии. Лекция 9(29) 2
 Тема 9. Методы цитологического анализа Масштабы объектов молекулярной биологии • На схеме приведены линейные размеры объектов молекулярной биологии. В центре в овале – диапазон размеров объектов цитологического анализа. • В основном объекты цитологии имеют размеры от 100 мкм до десятков нанометров. • Размер многих макромолекул, входящих в структуру внутриклеточных органелл имеют размеры до нескольких сотен нанометров. Размеры объектов молекулярной биологии (Рис, Стернберг, 1988) 3 Лекция 9(29)
Тема 9. Методы цитологического анализа Масштабы объектов молекулярной биологии • На схеме приведены линейные размеры объектов молекулярной биологии. В центре в овале – диапазон размеров объектов цитологического анализа. • В основном объекты цитологии имеют размеры от 100 мкм до десятков нанометров. • Размер многих макромолекул, входящих в структуру внутриклеточных органелл имеют размеры до нескольких сотен нанометров. Размеры объектов молекулярной биологии (Рис, Стернберг, 1988) 3 Лекция 9(29)
 Тема 9. Методы цитологического анализа Схема спектра электромагнитного излучения (внизу) и пределы разрешения глаза человека, светового и электронного микроскопов (Свенсон, Уэбстер, 1980) • Исходя из размеров цитологических объектов видно – они лежат за пределами разрешения человеческого глаза. • Поэтому для изучения структуры цитологических объектов используются световой и электронный микроскопы Лекция 9(29) 4
Тема 9. Методы цитологического анализа Схема спектра электромагнитного излучения (внизу) и пределы разрешения глаза человека, светового и электронного микроскопов (Свенсон, Уэбстер, 1980) • Исходя из размеров цитологических объектов видно – они лежат за пределами разрешения человеческого глаза. • Поэтому для изучения структуры цитологических объектов используются световой и электронный микроскопы Лекция 9(29) 4
 Тема 9. Методы цитологического анализа Что видит глаз человека? • Известно, что человеческий глаз может различать детали предметов, размеры которых меньше некоторых предельных размеров. В случае нормального зрения и хорошего освещения предмета (около 50 лк), детали предметов хорошо видны на расстоянии между глазом и предметом равном 250 мм, это расстояние называется расстоянием "наилучшего видения". При остроте зрения равном 2' глаз на этом расстоянии хорошо различает детали предмета, расстояние между которыми не меньше 0, 15 мм. • Таким образом, невооруженным глазом мы можем хорошо различить мелкие предметы величиной не менее 150 мкм (рис. ). Из рисунка видно, что для наблюдения более мелких предметов необходимо увеличить угол W, для чего необходимо применить специальные увеличительные приборы - лупы и микроскопы. • При изучении микроструктуры клеток и тканей в случае морфологичесмких или гистохимических исследований необходимо использовать увеличительные приборы, т. к. линейные размеры клеток и внутриклеточных органелл лежат ниже разрешающей способности человеческого глаза. Лекция 9(29) 5
Тема 9. Методы цитологического анализа Что видит глаз человека? • Известно, что человеческий глаз может различать детали предметов, размеры которых меньше некоторых предельных размеров. В случае нормального зрения и хорошего освещения предмета (около 50 лк), детали предметов хорошо видны на расстоянии между глазом и предметом равном 250 мм, это расстояние называется расстоянием "наилучшего видения". При остроте зрения равном 2' глаз на этом расстоянии хорошо различает детали предмета, расстояние между которыми не меньше 0, 15 мм. • Таким образом, невооруженным глазом мы можем хорошо различить мелкие предметы величиной не менее 150 мкм (рис. ). Из рисунка видно, что для наблюдения более мелких предметов необходимо увеличить угол W, для чего необходимо применить специальные увеличительные приборы - лупы и микроскопы. • При изучении микроструктуры клеток и тканей в случае морфологичесмких или гистохимических исследований необходимо использовать увеличительные приборы, т. к. линейные размеры клеток и внутриклеточных органелл лежат ниже разрешающей способности человеческого глаза. Лекция 9(29) 5
 Тема 9. Методы цитологического анализа Оптическое разрешение микроскопа • Оптическое разрешение микроскопа – способность микроскопа различить две близко лежащие точки в объекте. При определении разрешения микроскопа изображение объекта рассматривается как совокупность освещенных точек. • Каждая точка объекта, в связи с дифракцией при прохождении через линзы, в плоскости изображения образует дифракционные фигуры, состоящие из центрального пятна (кружка Эри) и серии дифракционных колец, окружающих его (рис. а). • Расчеты показали, что в центральном пятне сконцентрировано около 83, 4% энергии, в первом кольце - 7, 2%, во втором - 2, 8%, в третьем 1, 4%, в четвертом - 0, 9% и в остальных кольцах - 3, 9%. Практически установлено, что в большинстве случаев глаз способен различать две точки в объекте, если падение освещенности между двумя максимумами в кружках Эри, образованными этими точками, будет составлять не менее 5%, что соответствует расстоянию между максимумами (рис. , б): R = 0, 61 / A , Где - длина волны , А – числовая апертура объектива микроскопа. Таким образом, разрешающая сила микроскопа увеличивается при уменьшении длины волны и увеличивается при увеличении числовой апертуры объектива микроскопа. Лекция 9(29) 6
Тема 9. Методы цитологического анализа Оптическое разрешение микроскопа • Оптическое разрешение микроскопа – способность микроскопа различить две близко лежащие точки в объекте. При определении разрешения микроскопа изображение объекта рассматривается как совокупность освещенных точек. • Каждая точка объекта, в связи с дифракцией при прохождении через линзы, в плоскости изображения образует дифракционные фигуры, состоящие из центрального пятна (кружка Эри) и серии дифракционных колец, окружающих его (рис. а). • Расчеты показали, что в центральном пятне сконцентрировано около 83, 4% энергии, в первом кольце - 7, 2%, во втором - 2, 8%, в третьем 1, 4%, в четвертом - 0, 9% и в остальных кольцах - 3, 9%. Практически установлено, что в большинстве случаев глаз способен различать две точки в объекте, если падение освещенности между двумя максимумами в кружках Эри, образованными этими точками, будет составлять не менее 5%, что соответствует расстоянию между максимумами (рис. , б): R = 0, 61 / A , Где - длина волны , А – числовая апертура объектива микроскопа. Таким образом, разрешающая сила микроскопа увеличивается при уменьшении длины волны и увеличивается при увеличении числовой апертуры объектива микроскопа. Лекция 9(29) 6
 Тема 9. Методы цитологического анализа • Практически все клетки, особенно живые клетки (за исключением содержащих пигменты и другие хромофорные соединения), прозрачны для видимого света. Световая волна, проходя через такие объекты, не изменяет свою амплитуду, но изменяется только ее фаза, количественная оценка которой зависит от произведения показателя преломления микрообъекта на его толщину. • Такие микрообъекты называются фазовыми. Сдвиг фаз не различается глазом, фоточувствительными материалами или фотоэлектронными приборами, так как указанные фотоприемники могут реагировать только на изменение амплитуды падающего света. • Эндогенные химические соединения в большинстве клеток животных и растений не обладают поглощением света в видимой области света и поэтому их также можно отнести к фазовым объектам. Поэтому, одной из важных задач в области светооптической микроскопии является превращение "фазовых объектов" в объекты, которые изменяют амплитуду проходящего через них света (такие микрообъекты называются "амплитудными объектами"). • Это превращение "фазовых объектов" в "амплитудные объекты" достигается четырьмя принципиально различными путями: 1) С использованием специальных приемов физической оптики, реализуемых в темнопольной, фазово-контрастной и интерференционной микроскопии); 2) С использованием свойства ряда внутриклеточных соединений поглощать свет в ультрафиолетовой области спектра (ультрафиолетовая микроскопия); 3) С использованием свойства ряда эндогенных соединений флуоресцировать (микроскопия собственной флуоресценции клеток и тканей); 4) С использованием свойства различных внутриклеточных и внутритканевых веществ специфически взаимодействовать с красителями, флуорохромами, соединениями с радиоактивными метками, меченными антителами, зондами-фрагментами м. РНК и др. Для этой цели разработано много методов окрашивания, радиоавтографии, иммуногистохимии и гибридизации м. РНК in situ. Окрашенные или меченные соответствующими метками препараты анализируются при помощи обычных светооптических и флуоресцентных микроскопов. Лекция 9(29) 7
Тема 9. Методы цитологического анализа • Практически все клетки, особенно живые клетки (за исключением содержащих пигменты и другие хромофорные соединения), прозрачны для видимого света. Световая волна, проходя через такие объекты, не изменяет свою амплитуду, но изменяется только ее фаза, количественная оценка которой зависит от произведения показателя преломления микрообъекта на его толщину. • Такие микрообъекты называются фазовыми. Сдвиг фаз не различается глазом, фоточувствительными материалами или фотоэлектронными приборами, так как указанные фотоприемники могут реагировать только на изменение амплитуды падающего света. • Эндогенные химические соединения в большинстве клеток животных и растений не обладают поглощением света в видимой области света и поэтому их также можно отнести к фазовым объектам. Поэтому, одной из важных задач в области светооптической микроскопии является превращение "фазовых объектов" в объекты, которые изменяют амплитуду проходящего через них света (такие микрообъекты называются "амплитудными объектами"). • Это превращение "фазовых объектов" в "амплитудные объекты" достигается четырьмя принципиально различными путями: 1) С использованием специальных приемов физической оптики, реализуемых в темнопольной, фазово-контрастной и интерференционной микроскопии); 2) С использованием свойства ряда внутриклеточных соединений поглощать свет в ультрафиолетовой области спектра (ультрафиолетовая микроскопия); 3) С использованием свойства ряда эндогенных соединений флуоресцировать (микроскопия собственной флуоресценции клеток и тканей); 4) С использованием свойства различных внутриклеточных и внутритканевых веществ специфически взаимодействовать с красителями, флуорохромами, соединениями с радиоактивными метками, меченными антителами, зондами-фрагментами м. РНК и др. Для этой цели разработано много методов окрашивания, радиоавтографии, иммуногистохимии и гибридизации м. РНК in situ. Окрашенные или меченные соответствующими метками препараты анализируются при помощи обычных светооптических и флуоресцентных микроскопов. Лекция 9(29) 7
 Тема 9. Методы цитологического анализа Метод темного поля Схема темнопольного микроскопа • При критическом освещении объектов в микроскопе, в плоскости объекта образуется сплошной конус света и поле зрения микроскопа равномерно освещено. Однако, если перед конденсором (1) со стороны осветителя ввести поперек оптической оси микроскопа непрозрачный экран (диск) с прозрачной кольцевой диафрагмой (2) таким образом, чтобы свет не заполнял в плоскости микрообъекта (3) апертуры объектива (4), то поле зрения микроскопа в отсутствие микрообъекта соответственно будет темным (рис. справа). • Но если в препарате имеются микроструктуры, свет на них будет рассеиваться и дифрагированный свет от таких микроструктур попадет в объектив. Рассеивание света происходит вследствие того, что элементы структуры отличаются от окружающей их среды по показателю преломления. В этом случае на темном фоне будет видно светлое изображение объекта. • Интенсивность света от объекта при таком микроскопировании невысокая, но тем не менее этот метод позволяет визуализировать мелкие структуры, недоступные по разрешению для обычного микроскопа, которые трудно увидеть на светлом фоне. В связи с этим, иногда микроскопию в темном поле называют ультрамикроскопией. Лекция 9(29) 8
Тема 9. Методы цитологического анализа Метод темного поля Схема темнопольного микроскопа • При критическом освещении объектов в микроскопе, в плоскости объекта образуется сплошной конус света и поле зрения микроскопа равномерно освещено. Однако, если перед конденсором (1) со стороны осветителя ввести поперек оптической оси микроскопа непрозрачный экран (диск) с прозрачной кольцевой диафрагмой (2) таким образом, чтобы свет не заполнял в плоскости микрообъекта (3) апертуры объектива (4), то поле зрения микроскопа в отсутствие микрообъекта соответственно будет темным (рис. справа). • Но если в препарате имеются микроструктуры, свет на них будет рассеиваться и дифрагированный свет от таких микроструктур попадет в объектив. Рассеивание света происходит вследствие того, что элементы структуры отличаются от окружающей их среды по показателю преломления. В этом случае на темном фоне будет видно светлое изображение объекта. • Интенсивность света от объекта при таком микроскопировании невысокая, но тем не менее этот метод позволяет визуализировать мелкие структуры, недоступные по разрешению для обычного микроскопа, которые трудно увидеть на светлом фоне. В связи с этим, иногда микроскопию в темном поле называют ультрамикроскопией. Лекция 9(29) 8
 Тема 9. Методы цитологического анализа Метод фазового контраста • Голландский физик Ф. Цернике развил теорию метода фазового контраста метода, разработал удобное геометрическое представление о методе и осуществил его на практике в 30 -х годах (Zernike F. , Physica, 9, 656, 914, 1942). • Известно, что различия в показателях преломления между внутриклеточными структурами и окружающей их средой незначительные, в связи с чем сдвиг между фазами света, прошедшими через внутриклеточные микроструктуры и среду, практически не приводит при их сложении (интерференции) к изменению амплитуды суммированной волны. • Ф. Цернике показал, что если фазу прямого света (света, прошедшего через среду) сдвинуть искусственно на 90 градусов относительно света, прошедшего через объект ("отклоненного", дифрагированного света), то фазовые различия между светом, прошедшим через объект и среду, будут практически равны четверти длины волны и в этом случае их интерференция будет приводить к изменению амплитуды световой волны, а сами структуры будут видны при микроскопическом анализе, за счет увеличения их контраста относительно окружающей их среды. Лекция 9(29) 9
Тема 9. Методы цитологического анализа Метод фазового контраста • Голландский физик Ф. Цернике развил теорию метода фазового контраста метода, разработал удобное геометрическое представление о методе и осуществил его на практике в 30 -х годах (Zernike F. , Physica, 9, 656, 914, 1942). • Известно, что различия в показателях преломления между внутриклеточными структурами и окружающей их средой незначительные, в связи с чем сдвиг между фазами света, прошедшими через внутриклеточные микроструктуры и среду, практически не приводит при их сложении (интерференции) к изменению амплитуды суммированной волны. • Ф. Цернике показал, что если фазу прямого света (света, прошедшего через среду) сдвинуть искусственно на 90 градусов относительно света, прошедшего через объект ("отклоненного", дифрагированного света), то фазовые различия между светом, прошедшим через объект и среду, будут практически равны четверти длины волны и в этом случае их интерференция будет приводить к изменению амплитуды световой волны, а сами структуры будут видны при микроскопическом анализе, за счет увеличения их контраста относительно окружающей их среды. Лекция 9(29) 9
 Тема 9. Методы цитологического анализа Метод фазового контраста (прдолжение) • На практике это реализуется следующим образом (рис): свет от источника попадает на кольцевую диафрагму (1), изображение которой строится конденсором(2) в фокальной плоскости объектива (3). В этой плоскости устанавливается фазовая пластинка (4), представляющая диск с кольцевой канавкой (или напылением), создающая опережение(или отставание) по фазе равное π / 2. • Размер фазового кольца должен точно совпадать с кольцевой диафрагмой конденсора. Таким образом, весь прямой свет, прошедший через кольцевую диафрагму конденсора, проходя Метод фазового контраста через фазовую пластинку, изменяет свою фазу на π / 2. Свет, дифрагированный на объекте (5), будет проходить через остальную апертуру объектива и не претерпевать ни фазовых, ни амплитудных изменений. • При интерференции прямого и дифрагмированного света разность фаз между ними практически становится равной π / 2, что приводит к изменению амплитуды света, проходящего через микроструктуры анализируемого препарата, вследствие чего в плоскости (6) получается контрастное изображение, в котором структурам с большим показателем преломления будут соответствовать более темные участки ("позитивный контраст"). Для получения "негативного контраста", когда структурам с большим показателем преломления будут соответствовать более светлые участки изображения, фазовая кольцевая пластинка в фокальной плоскости объектива изготавливается путем напыления, что приводит к отставанию фазы прямого света на π / 2. Лекция 9(29) 10
Тема 9. Методы цитологического анализа Метод фазового контраста (прдолжение) • На практике это реализуется следующим образом (рис): свет от источника попадает на кольцевую диафрагму (1), изображение которой строится конденсором(2) в фокальной плоскости объектива (3). В этой плоскости устанавливается фазовая пластинка (4), представляющая диск с кольцевой канавкой (или напылением), создающая опережение(или отставание) по фазе равное π / 2. • Размер фазового кольца должен точно совпадать с кольцевой диафрагмой конденсора. Таким образом, весь прямой свет, прошедший через кольцевую диафрагму конденсора, проходя Метод фазового контраста через фазовую пластинку, изменяет свою фазу на π / 2. Свет, дифрагированный на объекте (5), будет проходить через остальную апертуру объектива и не претерпевать ни фазовых, ни амплитудных изменений. • При интерференции прямого и дифрагмированного света разность фаз между ними практически становится равной π / 2, что приводит к изменению амплитуды света, проходящего через микроструктуры анализируемого препарата, вследствие чего в плоскости (6) получается контрастное изображение, в котором структурам с большим показателем преломления будут соответствовать более темные участки ("позитивный контраст"). Для получения "негативного контраста", когда структурам с большим показателем преломления будут соответствовать более светлые участки изображения, фазовая кольцевая пластинка в фокальной плоскости объектива изготавливается путем напыления, что приводит к отставанию фазы прямого света на π / 2. Лекция 9(29) 10
 Тема 9. Методы цитологического анализа Фазово-контрастная микроскопия • Фазово-контрастная микроскопия играет важную роль в изучении живых клеток, клеточных культур и тонких тканевых эксплантатов (переживающей ткани). • При помощи фазово-контрастной микроскопии изучается влияние гистохимических фиксаторов на морфологию клеток, влияние различных физико-химических факторов на изменение клеточных микроструктур. Кроме этого, фазово-контрастная микроскопия играет незаменимую роль в изучении движения клеток и внутриклеточных органелл в нормальных условиях и при патологических процессах. Лекция 9(29) 11
Тема 9. Методы цитологического анализа Фазово-контрастная микроскопия • Фазово-контрастная микроскопия играет важную роль в изучении живых клеток, клеточных культур и тонких тканевых эксплантатов (переживающей ткани). • При помощи фазово-контрастной микроскопии изучается влияние гистохимических фиксаторов на морфологию клеток, влияние различных физико-химических факторов на изменение клеточных микроструктур. Кроме этого, фазово-контрастная микроскопия играет незаменимую роль в изучении движения клеток и внутриклеточных органелл в нормальных условиях и при патологических процессах. Лекция 9(29) 11
 Тема 9. Методы цитологического анализа Интерференционная микроскопия • Явление интерференции представляет сложение двух когерентных волн, в результате которого возникает третья волна. Амплитуда и фаза результирующей волны зависят от того, насколько одна из составляющих волн опережает другую, т. е. от величины разности хода Т, или сдвига фаз между ними - Δ: Δ = 2 π T / λ , λ - длина волны света. • Амплитуда А результирующей волны при Δ = 0 равна (а 1+а 2), а при Δ = π равна (а 1 а 2). Разность хода волн Т зависит от толщины микрообъекта (d) и разницы показателей преломления объекта (no) и среды (nc): Т=d(no-nc), поэтому сдвиг фаз связан с параметрами микрообъекта и условий измерения следующим соотношением: Δ = 2 π T d(no-nc) / λ • Нетрудно видеть, что в основе интерференционной микроскопии и, рассмотренной выше фазово-контрастной микроскопии, лежит использование законов интерференции света для визуализации "фазовых" микрообъектов, т. е. для превращения "фазовых объектов" в "амплитудные объекты". Лекция 9(29) 12
Тема 9. Методы цитологического анализа Интерференционная микроскопия • Явление интерференции представляет сложение двух когерентных волн, в результате которого возникает третья волна. Амплитуда и фаза результирующей волны зависят от того, насколько одна из составляющих волн опережает другую, т. е. от величины разности хода Т, или сдвига фаз между ними - Δ: Δ = 2 π T / λ , λ - длина волны света. • Амплитуда А результирующей волны при Δ = 0 равна (а 1+а 2), а при Δ = π равна (а 1 а 2). Разность хода волн Т зависит от толщины микрообъекта (d) и разницы показателей преломления объекта (no) и среды (nc): Т=d(no-nc), поэтому сдвиг фаз связан с параметрами микрообъекта и условий измерения следующим соотношением: Δ = 2 π T d(no-nc) / λ • Нетрудно видеть, что в основе интерференционной микроскопии и, рассмотренной выше фазово-контрастной микроскопии, лежит использование законов интерференции света для визуализации "фазовых" микрообъектов, т. е. для превращения "фазовых объектов" в "амплитудные объекты". Лекция 9(29) 12
 Тема 9. Методы цитологического анализа Интерференционный микроскоп • Свет от источника S (рис. ) в точке А раздваивается на два луча - АВD - опорный луч (волна сравнения) и ACD - рабочий луч, который проходит через изучаемый микрообъект (О). Оба луча в точке D интерферируют и образуют результирующий луч. В опорном луче - ABD при помощи фазовой пластинки можно создать любую разность хода по сравнению с лучом в плече ACD, в котором фаза волны изменяется объектом О. • Как указывалось выше, "фазовый микрообъект" О приводит к незначительному сдвигу фазы световой волны и если в луч ABD ввести Схема интерферометра фазовую пластинку сдвигающую фазу опорного луча на π / 2, то такой микроскоп будет работать как рассмотренный выше фазовоконтрастный микроскоп. • В отличие от фазово-контрастной микроскопии, в интерференционном микроскопе образуется более качественное изображение объекта, лишенное недостатков (ореол вокруг микроструктур), характерное для фазово-контрастного микроскопа. Так как лучи АВD и АСD разнесены в пространстве, в ход опорного луча AВD можно ввести компенсатор (К), при помощи которого можно плавно и непрерывно менять оптическую длину опорного луча, т. е. приводить к плавному изменению сдвига между опорным лучом и лучом, в который помещен микрообъект. Если компенсатор снабжен приспособлением для отсчета величины перемещения луча AВD, можно измерять разность хода луча (Т), вносимой объектом в луче АСD. Таким образом, интерференционная микроскопия позволяет не только получить качественный фазовый контраст, но и измерять сдвиг фаз, вносимых микроструктурами объекта. • При помощи компенсатора интерференционного микроскопа можно проводить количественные измерения оптической разности хода (Т) опорного и дифрагированного на объекте лучей и, на основе этих измерений, рассчитывать важные оптические характеристики микрообъектов: показатель преломления микроструктур, толщину микрообъектов, вес сухого вещества в клетках. Лекция 9(29) 13
Тема 9. Методы цитологического анализа Интерференционный микроскоп • Свет от источника S (рис. ) в точке А раздваивается на два луча - АВD - опорный луч (волна сравнения) и ACD - рабочий луч, который проходит через изучаемый микрообъект (О). Оба луча в точке D интерферируют и образуют результирующий луч. В опорном луче - ABD при помощи фазовой пластинки можно создать любую разность хода по сравнению с лучом в плече ACD, в котором фаза волны изменяется объектом О. • Как указывалось выше, "фазовый микрообъект" О приводит к незначительному сдвигу фазы световой волны и если в луч ABD ввести Схема интерферометра фазовую пластинку сдвигающую фазу опорного луча на π / 2, то такой микроскоп будет работать как рассмотренный выше фазовоконтрастный микроскоп. • В отличие от фазово-контрастной микроскопии, в интерференционном микроскопе образуется более качественное изображение объекта, лишенное недостатков (ореол вокруг микроструктур), характерное для фазово-контрастного микроскопа. Так как лучи АВD и АСD разнесены в пространстве, в ход опорного луча AВD можно ввести компенсатор (К), при помощи которого можно плавно и непрерывно менять оптическую длину опорного луча, т. е. приводить к плавному изменению сдвига между опорным лучом и лучом, в который помещен микрообъект. Если компенсатор снабжен приспособлением для отсчета величины перемещения луча AВD, можно измерять разность хода луча (Т), вносимой объектом в луче АСD. Таким образом, интерференционная микроскопия позволяет не только получить качественный фазовый контраст, но и измерять сдвиг фаз, вносимых микроструктурами объекта. • При помощи компенсатора интерференционного микроскопа можно проводить количественные измерения оптической разности хода (Т) опорного и дифрагированного на объекте лучей и, на основе этих измерений, рассчитывать важные оптические характеристики микрообъектов: показатель преломления микроструктур, толщину микрообъектов, вес сухого вещества в клетках. Лекция 9(29) 13
 Тема 9. Методы цитологического анализа Поляризационная микроскопия • Метод исследования микрообъектов в поляризованном свете используется для изучения анизатропных объектов, т. е. микрообъектов, у которых оптические свойства не одинаковы по различным направлениям. Знание анизотропии микрообъектов позволяет судить об их структуре и физикохимических свойствах. • Как известно, плоско-поляризованные волны можно получить при помощи специальных оптических устройств - поляроидов или призм, приготовленных из двоякопреломляющих материалов. • На рис. (а) представлена схема поляризационного микроскопа. Если после источника света (1) и коллекторной линзы осветителя (2) поставить первый поляроид - поляризатор (3), свет в конденсор (4) будет проходить плоскополяризованным и попадать на препарат (5), расположенный на вращающемся столике (6). После объектива (7) в оптической схеме поляризационного микроскопа имеются компенсатор (8), второй поляроид – анализатор (9) и окуляр (10). Если ось поляризатора (плоскость поляризации) перпендикулярна оси анализатора, то поле зрения микроскопа в отсутствии двоякопреломляющего объекта выглядит равномерно - темным. Однако, если в плоскости препарата имеется двоякопреломляющий объект и его ось поляризации отлична от 0 градусов и 90 градусов, т. е. не совпадает с осями поляризатора и анализатора, такой объект будет виден на темном фоне как светящийся предмет. При вращении объекта, что достигается вращением поворотного столика микроскопа, яркость изображения объекта будет изменяться и достигнет максимума при положении плоскости поляризации микрообъектов под 45 градусов относительно осей поляризатора и анализатора (рис. (б). Лекция 9(29) 14
Тема 9. Методы цитологического анализа Поляризационная микроскопия • Метод исследования микрообъектов в поляризованном свете используется для изучения анизатропных объектов, т. е. микрообъектов, у которых оптические свойства не одинаковы по различным направлениям. Знание анизотропии микрообъектов позволяет судить об их структуре и физикохимических свойствах. • Как известно, плоско-поляризованные волны можно получить при помощи специальных оптических устройств - поляроидов или призм, приготовленных из двоякопреломляющих материалов. • На рис. (а) представлена схема поляризационного микроскопа. Если после источника света (1) и коллекторной линзы осветителя (2) поставить первый поляроид - поляризатор (3), свет в конденсор (4) будет проходить плоскополяризованным и попадать на препарат (5), расположенный на вращающемся столике (6). После объектива (7) в оптической схеме поляризационного микроскопа имеются компенсатор (8), второй поляроид – анализатор (9) и окуляр (10). Если ось поляризатора (плоскость поляризации) перпендикулярна оси анализатора, то поле зрения микроскопа в отсутствии двоякопреломляющего объекта выглядит равномерно - темным. Однако, если в плоскости препарата имеется двоякопреломляющий объект и его ось поляризации отлична от 0 градусов и 90 градусов, т. е. не совпадает с осями поляризатора и анализатора, такой объект будет виден на темном фоне как светящийся предмет. При вращении объекта, что достигается вращением поворотного столика микроскопа, яркость изображения объекта будет изменяться и достигнет максимума при положении плоскости поляризации микрообъектов под 45 градусов относительно осей поляризатора и анализатора (рис. (б). Лекция 9(29) 14
 Тема 9. Методы цитологического анализа Поляризационная микроскопия (продолжение) • Анализируя состояние поляризации света, прошедшего через объект, можно точно вычислить вносимую им разность фаз и измерить, таким образом, его двойное лучепреломление. Обычно компенсатор, например для метода Сенармона, устанавливается перед анализатором и после того как объект установлен под 45 градусов относительно поляризатора и анализатора вращением компенсатора нужно достичь затемнения объекта целиком или его внутренней структуры и зафиксировать угол поворота компенсатора. Угол поворота компенсатора обычно выражается в виде долей длин волн и эта величина запаздывания фаз (Г) между двумя составляющими волнами, возникшими в двоякопреломляющем объекте равна: Г = d (nc - no), где d - толщина микрообъекта, nc - показатель преломления среды, no - показатель преломления микрообъекта. Например, если обнаружено, что Г = λ / 2, при λ = 550 нм, и толщине микрообъекта 10 мкм = 104 нм, то nc - no равно: 225 нм / 104 нм = 0, 0225. Зная значение nc можно рассчитать значение no. • Микроскопия в поляризованном свете играет важную роль в изучении анизатропии в расположении внутриклеточных органелл и упаковке больших молекул, что наряду с электронной микроскопией дает большую информацию о субмикроскопическом строении внутриклеточных органелл. Лекция 9(29) 15
Тема 9. Методы цитологического анализа Поляризационная микроскопия (продолжение) • Анализируя состояние поляризации света, прошедшего через объект, можно точно вычислить вносимую им разность фаз и измерить, таким образом, его двойное лучепреломление. Обычно компенсатор, например для метода Сенармона, устанавливается перед анализатором и после того как объект установлен под 45 градусов относительно поляризатора и анализатора вращением компенсатора нужно достичь затемнения объекта целиком или его внутренней структуры и зафиксировать угол поворота компенсатора. Угол поворота компенсатора обычно выражается в виде долей длин волн и эта величина запаздывания фаз (Г) между двумя составляющими волнами, возникшими в двоякопреломляющем объекте равна: Г = d (nc - no), где d - толщина микрообъекта, nc - показатель преломления среды, no - показатель преломления микрообъекта. Например, если обнаружено, что Г = λ / 2, при λ = 550 нм, и толщине микрообъекта 10 мкм = 104 нм, то nc - no равно: 225 нм / 104 нм = 0, 0225. Зная значение nc можно рассчитать значение no. • Микроскопия в поляризованном свете играет важную роль в изучении анизатропии в расположении внутриклеточных органелл и упаковке больших молекул, что наряду с электронной микроскопией дает большую информацию о субмикроскопическом строении внутриклеточных органелл. Лекция 9(29) 15
 Тема 9. Методы цитологического анализа Ультрафиолетовая микроскопия • Микроскопия в ультрафиолетовой области спектра практически не отличается от микроскопии в видимой области спектра, за исключением того, что при этом для освещения микрообъектов используется ультрафиолетовый свет. В связи с этим, в ультрафиолетовых микроскопах используется оптика, изготовленная из материалов, пропускающих ультрафиолетовый свет, в основном, из разных марок кварцевого стекла. • Главные достоинства и особенности ультрафиолетовой микроскопии: 1). В ультрафиолетовой области спектра обладают специфическим поглощением нуклеиновые кислоты (λ = 275 -280 нм) и белки (λ = 250 -280 нм). Поглощение глобулинов и нуклеиновых кислот перекрывается в области 280 нм, однако, нуклеиновые кислоты поглощают в этой области в 10 раз сильнее, чем глобулины. Кроме поглощения, многие внутриклеточные соединения обладают выраженной собственной флуоресценцией в ультрафиолетовой части спектра: витамин В 12 - 305 нм, витамин Е (α-токоферол) - 340 нм, эстрогены - 325 -330 нм и т. д. Наиболее интенсивная флуоресценция обнаружена у белков, содержащих ароматические аминокислоты. 2). Как указывалось выше, разрешающая сила микроскопа зависит от длины волны света, используемого при освещении препаратов, причем разрешение увеличивается при использовании света в коротковолновой части спектра. Поэтому в ультрафиолетовой области спектра разрешение микрообъектов выше, чем в видимой области спектра, например, при длине волны 250 нм разрешение микроскопа увеличится вдвое по сравнению с длиной волны 500 нм. Лекция 9(29) 16
Тема 9. Методы цитологического анализа Ультрафиолетовая микроскопия • Микроскопия в ультрафиолетовой области спектра практически не отличается от микроскопии в видимой области спектра, за исключением того, что при этом для освещения микрообъектов используется ультрафиолетовый свет. В связи с этим, в ультрафиолетовых микроскопах используется оптика, изготовленная из материалов, пропускающих ультрафиолетовый свет, в основном, из разных марок кварцевого стекла. • Главные достоинства и особенности ультрафиолетовой микроскопии: 1). В ультрафиолетовой области спектра обладают специфическим поглощением нуклеиновые кислоты (λ = 275 -280 нм) и белки (λ = 250 -280 нм). Поглощение глобулинов и нуклеиновых кислот перекрывается в области 280 нм, однако, нуклеиновые кислоты поглощают в этой области в 10 раз сильнее, чем глобулины. Кроме поглощения, многие внутриклеточные соединения обладают выраженной собственной флуоресценцией в ультрафиолетовой части спектра: витамин В 12 - 305 нм, витамин Е (α-токоферол) - 340 нм, эстрогены - 325 -330 нм и т. д. Наиболее интенсивная флуоресценция обнаружена у белков, содержащих ароматические аминокислоты. 2). Как указывалось выше, разрешающая сила микроскопа зависит от длины волны света, используемого при освещении препаратов, причем разрешение увеличивается при использовании света в коротковолновой части спектра. Поэтому в ультрафиолетовой области спектра разрешение микрообъектов выше, чем в видимой области спектра, например, при длине волны 250 нм разрешение микроскопа увеличится вдвое по сравнению с длиной волны 500 нм. Лекция 9(29) 16
 Тема 9. Методы цитологического анализа Ультрафиолетовая микроскопия (продолжение) • В связи с тем, что для человеческого глаза ультрафиолетовый свет невидим, для наблюдения изображения в ультрафиолетовом микроскопе используются флуоресцирующие экраны (как в электронной микроскопии) или изображение регистрируется на фотоматериалы. В более сложных конструкциях для наблюдения изображений в ультрафиолетовом микроскопе используются электроннооптические преобразователи, а для регистрации величины поглощения ультрафиолетового света микрообъектами - фотоумножители. В связи с этим количественные методы анализа, основанные на микроспектрофотометрии и микроденситометрии, в ультрафиолетовой области спектра широко развиты. • Конструкция и принципиальная оптическая схема ультрафиолетового микроскопа практически ничем не отличаются от обычного микроскопа. Однако, в качестве источника света обычно используются ртутные или ксеноновые лампы, обладающие мощным излучением в ультрафиолетовой области спектра, и специальные объективы, окуляры и другие преломляющие элементы, изготовленные из оптических материалов, хорошо пропускающих ультафиолетовый свет. Лекция 9(29) 17
Тема 9. Методы цитологического анализа Ультрафиолетовая микроскопия (продолжение) • В связи с тем, что для человеческого глаза ультрафиолетовый свет невидим, для наблюдения изображения в ультрафиолетовом микроскопе используются флуоресцирующие экраны (как в электронной микроскопии) или изображение регистрируется на фотоматериалы. В более сложных конструкциях для наблюдения изображений в ультрафиолетовом микроскопе используются электроннооптические преобразователи, а для регистрации величины поглощения ультрафиолетового света микрообъектами - фотоумножители. В связи с этим количественные методы анализа, основанные на микроспектрофотометрии и микроденситометрии, в ультрафиолетовой области спектра широко развиты. • Конструкция и принципиальная оптическая схема ультрафиолетового микроскопа практически ничем не отличаются от обычного микроскопа. Однако, в качестве источника света обычно используются ртутные или ксеноновые лампы, обладающие мощным излучением в ультрафиолетовой области спектра, и специальные объективы, окуляры и другие преломляющие элементы, изготовленные из оптических материалов, хорошо пропускающих ультафиолетовый свет. Лекция 9(29) 17
 Тема 9. Методы цитологического анализа Флуоресцентная микроскопия • Принципиальная оптическая схема современного флуоресцентного (люминесцентного) микроскопа с освещением препарата "падающим светом" приведена на рис. (а). Свет от источника света (1) (ртутная лампа) через систему коллекторных линз осветителя (2) и водяной фильтр (3), поглощающего тепловое (инфракрасное) излучение, попадает на специальную спектральную светоделительную пластинку (4), устроенную таким образом, что она сильно отражает коротковолновую часть видимой области спектра и пропускает видимую часть спектра. Для возбуждения флуоресценции имеется специальный фильтр 1(5). Возбуждающий свет через объектив (6) попадает на препарат (7) сверху ("падающий свет"). Свет флуоресценции проходит также через объектив (6), светоделительную пластинку (4), "запирающий" фильтр 2 (8), отсекающий возбуждающий свет и через окуляр (9) наблюдается исследователем. • На рис. (б) видно распределение интенсивности света, пропущенного фильтром 1(5) - возбуждающий свет (св); фильтром 2(8) - "запирающий" фильтр и свет флуоресценции объекта (сф). Из этого рисунка видна роль "запирающего" фильтра - предотвратить попадание возбуждающего света (за счет отражения от препарата) в канал визуального наблюдения флуоресценции микрообъекта. В описанном варианте флуоресцентного микроскопа реализована схема микроскопов в "падающем" (отраженном) свете, но имеются конструкции флуоресцентных микроскопов, которые работают в проходящем ("просвечивающем") свете. Лекция 9(29) 18
Тема 9. Методы цитологического анализа Флуоресцентная микроскопия • Принципиальная оптическая схема современного флуоресцентного (люминесцентного) микроскопа с освещением препарата "падающим светом" приведена на рис. (а). Свет от источника света (1) (ртутная лампа) через систему коллекторных линз осветителя (2) и водяной фильтр (3), поглощающего тепловое (инфракрасное) излучение, попадает на специальную спектральную светоделительную пластинку (4), устроенную таким образом, что она сильно отражает коротковолновую часть видимой области спектра и пропускает видимую часть спектра. Для возбуждения флуоресценции имеется специальный фильтр 1(5). Возбуждающий свет через объектив (6) попадает на препарат (7) сверху ("падающий свет"). Свет флуоресценции проходит также через объектив (6), светоделительную пластинку (4), "запирающий" фильтр 2 (8), отсекающий возбуждающий свет и через окуляр (9) наблюдается исследователем. • На рис. (б) видно распределение интенсивности света, пропущенного фильтром 1(5) - возбуждающий свет (св); фильтром 2(8) - "запирающий" фильтр и свет флуоресценции объекта (сф). Из этого рисунка видна роль "запирающего" фильтра - предотвратить попадание возбуждающего света (за счет отражения от препарата) в канал визуального наблюдения флуоресценции микрообъекта. В описанном варианте флуоресцентного микроскопа реализована схема микроскопов в "падающем" (отраженном) свете, но имеются конструкции флуоресцентных микроскопов, которые работают в проходящем ("просвечивающем") свете. Лекция 9(29) 18
 Тема 9. Методы цитологического анализа Флуоресцентная микроскопия (продолжение) • Флуоресцентная микроскопия в падающем свете является наиболее оптимальным методом т. к. : 1). Конденсором является сам объектив и поэтому достигается полное соответствие апертур конденсора и объектива, что очень важно, так как интенсивность света флуоресценции не очень высокая. 2). При освещении "падающим" светом, флуоресценция микроструктур возбуждается в поверхностных слоях препарата и свет флуоресценции объекта не проходит через всю массу препарата, где возможно его поглощение и, таким образом, искажение изображения флуоресцирующего объекта и уменьшение разрешения микроскопа. 3). Использование специальной спектральной светоделительной пластинки значительно улучшает спектральные качества описанной схемы флуоресцентного микроскопа, особенно для разделения возбуждающего света и света флуоресценции объекта. • Флуоресцентная микроскопия широко используется в цитологии и цито- и гистохимии для: 1) Изучения собственной флуоресценции внутриклеточных эндогенных химических соединений – некоторые витамины, ряд коферментов дыхательной цепи в митохондриях и др. ; 2). Гистохимических реакций, основанные на изучении флуоресцирующих соединений, образующихся в ходе таких реакций (например, реакция формальдегида с биогенными монами, приводящая к образованию флуоресцирующих тетраизохинолинов и карболинов); 3). Исследований с использованием окраски внутриклеточных соединений при помощи специальных красителей - флуорохромов, обладающих высоким сродством к разным эндогенным соединениям и высоким квантовым выходом флуоресценции (интравитальная флуоресцентная микроскопией, потенциалчувствительные флуорохромы, флуоресцирующие мембранные зонды, меченные антитела и др. ). Лекция 9(29) 19
Тема 9. Методы цитологического анализа Флуоресцентная микроскопия (продолжение) • Флуоресцентная микроскопия в падающем свете является наиболее оптимальным методом т. к. : 1). Конденсором является сам объектив и поэтому достигается полное соответствие апертур конденсора и объектива, что очень важно, так как интенсивность света флуоресценции не очень высокая. 2). При освещении "падающим" светом, флуоресценция микроструктур возбуждается в поверхностных слоях препарата и свет флуоресценции объекта не проходит через всю массу препарата, где возможно его поглощение и, таким образом, искажение изображения флуоресцирующего объекта и уменьшение разрешения микроскопа. 3). Использование специальной спектральной светоделительной пластинки значительно улучшает спектральные качества описанной схемы флуоресцентного микроскопа, особенно для разделения возбуждающего света и света флуоресценции объекта. • Флуоресцентная микроскопия широко используется в цитологии и цито- и гистохимии для: 1) Изучения собственной флуоресценции внутриклеточных эндогенных химических соединений – некоторые витамины, ряд коферментов дыхательной цепи в митохондриях и др. ; 2). Гистохимических реакций, основанные на изучении флуоресцирующих соединений, образующихся в ходе таких реакций (например, реакция формальдегида с биогенными монами, приводящая к образованию флуоресцирующих тетраизохинолинов и карболинов); 3). Исследований с использованием окраски внутриклеточных соединений при помощи специальных красителей - флуорохромов, обладающих высоким сродством к разным эндогенным соединениям и высоким квантовым выходом флуоресценции (интравитальная флуоресцентная микроскопией, потенциалчувствительные флуорохромы, флуоресцирующие мембранные зонды, меченные антитела и др. ). Лекция 9(29) 19
 Тема 9. Методы цитологического анализа Электронная микроскопия • Возможности светового микроскопа, как указывалось, ограничиваются длиной волны видимого света. Его максимальная разрешающая способность составляет примерно 0, 2 мкм. • В 20 -х годах прошлого века было обнаружено, что специальные «электромагнитные линзы» можно использовать, подобно линзам светового микроскопа, для формирования и фокусирования пучков электронов. • На основе всего этого был создан микроскоп, в котором вместо света используется пучок электронов. Разрешающая способность наиболее совершенных из современных электронных микроскопов приближается к 0, 2 нм. • Первые электронные микроскопы были сконструированы в 30 -х годах прошлого века, но только в 50 -х годах были разработаны методы изготовления срезов для электронной микроскопии. Лекция 9(29) 20
Тема 9. Методы цитологического анализа Электронная микроскопия • Возможности светового микроскопа, как указывалось, ограничиваются длиной волны видимого света. Его максимальная разрешающая способность составляет примерно 0, 2 мкм. • В 20 -х годах прошлого века было обнаружено, что специальные «электромагнитные линзы» можно использовать, подобно линзам светового микроскопа, для формирования и фокусирования пучков электронов. • На основе всего этого был создан микроскоп, в котором вместо света используется пучок электронов. Разрешающая способность наиболее совершенных из современных электронных микроскопов приближается к 0, 2 нм. • Первые электронные микроскопы были сконструированы в 30 -х годах прошлого века, но только в 50 -х годах были разработаны методы изготовления срезов для электронной микроскопии. Лекция 9(29) 20
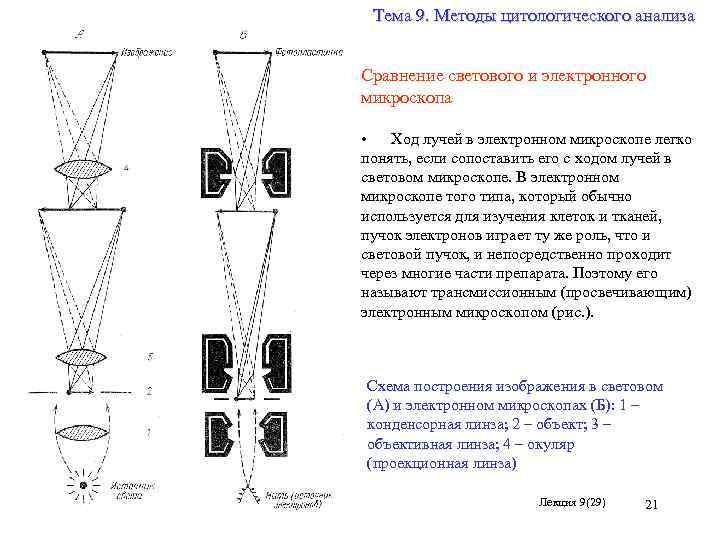 Тема 9. Методы цитологического анализа Сравнение светового и электронного микроскопа • Ход лучей в электронном микроскопе легко понять, если сопоставить его с ходом лучей в световом микроскопе. В электронном микроскопе того типа, который обычно используется для изучения клеток и тканей, пучок электронов играет ту же роль, что и световой пучок, и непосредственно проходит через многие части препарата. Поэтому его называют трансмиссионным (просвечивающим) электронным микроскопом (рис. ). Схема построения изображения в световом (А) и электронном микроскопах (Б): 1 – конденсорная линза; 2 – объект; 3 – объективная линза; 4 – окуляр (проекционная линза) Лекция 9(29) 21
Тема 9. Методы цитологического анализа Сравнение светового и электронного микроскопа • Ход лучей в электронном микроскопе легко понять, если сопоставить его с ходом лучей в световом микроскопе. В электронном микроскопе того типа, который обычно используется для изучения клеток и тканей, пучок электронов играет ту же роль, что и световой пучок, и непосредственно проходит через многие части препарата. Поэтому его называют трансмиссионным (просвечивающим) электронным микроскопом (рис. ). Схема построения изображения в световом (А) и электронном микроскопах (Б): 1 – конденсорная линза; 2 – объект; 3 – объективная линза; 4 – окуляр (проекционная линза) Лекция 9(29) 21
 Тема 9. Методы цитологического анализа Трансмиссионный электронный микроскоп • Оптическая система трансмиссионного электронного микроскопа: электроны движутся под действием электромагнитных полей, подобно тому как световые лучи направляются стеклянными линзами. • Внутри электронного микроскопа поддерживается вакуум, так как в воздухе длина свободного пробега электронов очень мала. Нагреваемый электрическим током катод, который представляет собой V-образную вольфрамовую нить, испускает электроны, которые ускоряются в направлении анода (обычно под влиянием разности потенциалов 50 -100 к. В). В аноде имеется отверстие, через которое поток электронов может проходить и фокусироваться конденсорной линзой; последняя направляет его на объект - обычно очень тонкий срез ткани, подвергшейся специальной обработке. • При прохождении пучка электронов через объект некоторые из них рассеиваются и отклоняются электроно-плотными участками объекта. Прошедшие через объект электроны фокусируются «объективом» , формирующей увеличенное первичное изображение объекта, которое после дополнительного увеличения проецируется на флуоресцирующий экран или на фотопленку. • Длина волны потока электронов является функцией ускоряющего напряжения (V) и может быть приблизительно вычислена из формулы де Бройля: = 12, 2 / V ½ ангстрем Например, при ускоряющем напряжении в 50 тыс. вольт =0, 0535 ангстрем. При этой длине волны и значении числовой апертуры 1, 4, разрешающая сила микроскопа увеличивается в 80 тыс. раз Лекция 9(29) 22
Тема 9. Методы цитологического анализа Трансмиссионный электронный микроскоп • Оптическая система трансмиссионного электронного микроскопа: электроны движутся под действием электромагнитных полей, подобно тому как световые лучи направляются стеклянными линзами. • Внутри электронного микроскопа поддерживается вакуум, так как в воздухе длина свободного пробега электронов очень мала. Нагреваемый электрическим током катод, который представляет собой V-образную вольфрамовую нить, испускает электроны, которые ускоряются в направлении анода (обычно под влиянием разности потенциалов 50 -100 к. В). В аноде имеется отверстие, через которое поток электронов может проходить и фокусироваться конденсорной линзой; последняя направляет его на объект - обычно очень тонкий срез ткани, подвергшейся специальной обработке. • При прохождении пучка электронов через объект некоторые из них рассеиваются и отклоняются электроно-плотными участками объекта. Прошедшие через объект электроны фокусируются «объективом» , формирующей увеличенное первичное изображение объекта, которое после дополнительного увеличения проецируется на флуоресцирующий экран или на фотопленку. • Длина волны потока электронов является функцией ускоряющего напряжения (V) и может быть приблизительно вычислена из формулы де Бройля: = 12, 2 / V ½ ангстрем Например, при ускоряющем напряжении в 50 тыс. вольт =0, 0535 ангстрем. При этой длине волны и значении числовой апертуры 1, 4, разрешающая сила микроскопа увеличивается в 80 тыс. раз Лекция 9(29) 22
 Тема 9. Методы цитологического анализа Изготовление препаратов для трансмиссионного электронного микроскопа • Приготовление препаратов для электронной просвечивающей микрскопии включает практически те же операции, что и приготовление препаратов для световой микроскопии. • Фиксация. Основные фиксаторы: осмиевая кислота, глутаральдегид , формалин и др. • Обезвоживание. После фиксации кусочек ткани обезвоживают, проводя его через спирты возрастающей концентрации, и специальные органические соединения для заливки в полимерные материалы. • Заливка. Для изготовлеия тонкие срезы, которые можно было бы исследовать в электронном микроскопе, используются, чаще всего, эпоксидные смолы – эпон, аралдит и др. • Изготовление срезов. Срезы для электронной микроскопии называют ультратонкими и изготавливаются на ультрамикротоме, толщина срезов – 40 -80 нм. Срезы помещают на маленькие медные сеточки, предварительно покрытые подложкой из пластмассы (формвар) или углерода, и на специальном держателе вводятся в электронный микроскоп. • Окрашивание. В электронной микроскопии окрашиванием называют обработку срезов растворами солей тяжелых металлов для увеличения электронной плотности структур клетки и, т. о. , повышения контрастности изображений структуры клеток и ее органелл. Используются: осмиевая кислота, уранилацетат, гидрат окиси свинца и др. Лекция 9(29) 23
Тема 9. Методы цитологического анализа Изготовление препаратов для трансмиссионного электронного микроскопа • Приготовление препаратов для электронной просвечивающей микрскопии включает практически те же операции, что и приготовление препаратов для световой микроскопии. • Фиксация. Основные фиксаторы: осмиевая кислота, глутаральдегид , формалин и др. • Обезвоживание. После фиксации кусочек ткани обезвоживают, проводя его через спирты возрастающей концентрации, и специальные органические соединения для заливки в полимерные материалы. • Заливка. Для изготовлеия тонкие срезы, которые можно было бы исследовать в электронном микроскопе, используются, чаще всего, эпоксидные смолы – эпон, аралдит и др. • Изготовление срезов. Срезы для электронной микроскопии называют ультратонкими и изготавливаются на ультрамикротоме, толщина срезов – 40 -80 нм. Срезы помещают на маленькие медные сеточки, предварительно покрытые подложкой из пластмассы (формвар) или углерода, и на специальном держателе вводятся в электронный микроскоп. • Окрашивание. В электронной микроскопии окрашиванием называют обработку срезов растворами солей тяжелых металлов для увеличения электронной плотности структур клетки и, т. о. , повышения контрастности изображений структуры клеток и ее органелл. Используются: осмиевая кислота, уранилацетат, гидрат окиси свинца и др. Лекция 9(29) 23
 Тема 9. Методы цитологического анализа Сканирующий электронный микроскоп • Сканирующий электронный микроскоп отличается от трансмиссионного электронного микроскопа тем, что в нем электроны не проходят сквозь объект: изображение микрообъекта формируется энергией отраженных электронов. • В сканирующем электронном микроскопе пучок электронов также формируется электромагнитными линзами, но в дальнейшем этот пучок используется совершенно иным образом. • Конденсорная линза создает очень тонкий пучок электронов (зонд); этот пучок проходит через отклоняющую катушку, которая сканирует его по поверхности препарата. На каждом участке препарата, на который попадает сканирующий пучок, из поверхности препарата выбиваются вторичные электроны, которые собираются детекторами электронов, и их энергия превращается в электрический сигнал, интенсивность которого передается точкой в соответствующем месте телевизионного экрана. Сканирование приводит к формированию полного изображения объектов на экране монитора. Лекция 9(29) 24
Тема 9. Методы цитологического анализа Сканирующий электронный микроскоп • Сканирующий электронный микроскоп отличается от трансмиссионного электронного микроскопа тем, что в нем электроны не проходят сквозь объект: изображение микрообъекта формируется энергией отраженных электронов. • В сканирующем электронном микроскопе пучок электронов также формируется электромагнитными линзами, но в дальнейшем этот пучок используется совершенно иным образом. • Конденсорная линза создает очень тонкий пучок электронов (зонд); этот пучок проходит через отклоняющую катушку, которая сканирует его по поверхности препарата. На каждом участке препарата, на который попадает сканирующий пучок, из поверхности препарата выбиваются вторичные электроны, которые собираются детекторами электронов, и их энергия превращается в электрический сигнал, интенсивность которого передается точкой в соответствующем месте телевизионного экрана. Сканирование приводит к формированию полного изображения объектов на экране монитора. Лекция 9(29) 24
 Тема 9. Методы цитологического анализа Сканирующий электронный микроскоп (продолжение) • Объекты перед изучением при помощи сканирующего электронного микроскопа, подвергаются специальной обработке: после соответствующей фиксации кусочек ткани сначала обезвоживают затем помещают на объектодержатель и покрывают тонким слоем металла, например золота или платины, который рассеивает электроны и тем самым выявляет особенности строения поверхности изучаемого объекта. • Сканирующий электронный микроскоп дает детальное объемное изображение объектов, что очень важно для понимания трехмерной структуры клеток и ее органелл. • При помощи сканирующей электронной микроскопии и метода замораживанияскалывания и метода замораживания-травления можно изучать структуру мембран клеток и внутриклеточных структур. Лекция 9(29) 25
Тема 9. Методы цитологического анализа Сканирующий электронный микроскоп (продолжение) • Объекты перед изучением при помощи сканирующего электронного микроскопа, подвергаются специальной обработке: после соответствующей фиксации кусочек ткани сначала обезвоживают затем помещают на объектодержатель и покрывают тонким слоем металла, например золота или платины, который рассеивает электроны и тем самым выявляет особенности строения поверхности изучаемого объекта. • Сканирующий электронный микроскоп дает детальное объемное изображение объектов, что очень важно для понимания трехмерной структуры клеток и ее органелл. • При помощи сканирующей электронной микроскопии и метода замораживанияскалывания и метода замораживания-травления можно изучать структуру мембран клеток и внутриклеточных структур. Лекция 9(29) 25
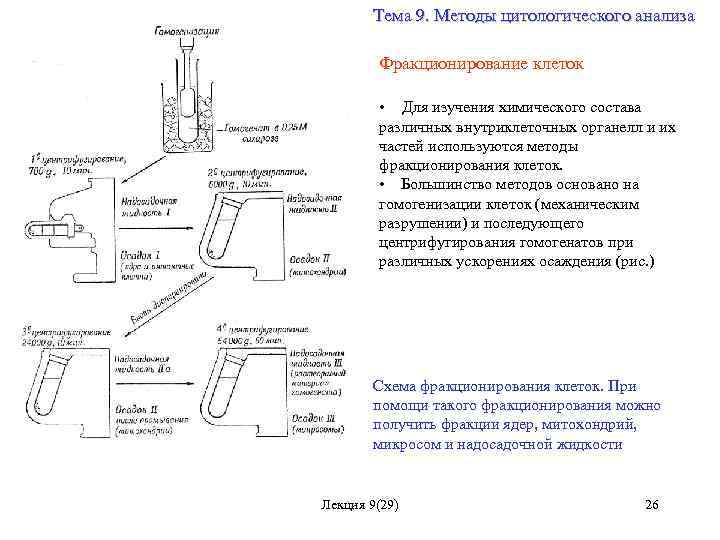 Тема 9. Методы цитологического анализа Фракционирование клеток • Для изучения химического состава различных внутриклеточных органелл и их частей используются методы фракционирования клеток. • Большинство методов основано на гомогенизации клеток (механическим разрушении) и последующего центрифугирования гомогенатов при различных ускорениях осаждения (рис. ) Схема фракционирования клеток. При помощи такого фракционирования можно получить фракции ядер, митохондрий, микросом и надосадочной жидкости Лекция 9(29) 26
Тема 9. Методы цитологического анализа Фракционирование клеток • Для изучения химического состава различных внутриклеточных органелл и их частей используются методы фракционирования клеток. • Большинство методов основано на гомогенизации клеток (механическим разрушении) и последующего центрифугирования гомогенатов при различных ускорениях осаждения (рис. ) Схема фракционирования клеток. При помощи такого фракционирования можно получить фракции ядер, митохондрий, микросом и надосадочной жидкости Лекция 9(29) 26
 Тема 9. Методы цитологического анализа Изучение клеток in vitro (культура клеток) • Одно из важнейших направлений клеточной биологии связано с технологией – культурой клеток – заключающейся в выделении клеток из определенных частей организма и выращивании их in vitro на специальных питательных средах. • В таких культурах клетки могут делиться, перемещаться, вырабатывать различные вещества и выполнять многие из тех функций, которые бы они выполняли в организме. • Более того, при создании соответствующих условий клетки в культуре могут стать более специализированными и проявлять новые черты и новые функции. • Используя методы клеточной микрохирургии, можно производить операции на клетках in vitro, например пересаживать ядра от одной клетки другой, вызывать слияние клеток двух разных тканей и даже двух разных видов. • Культура клеток и тканей используется, например, для определения токсичности того или иного вещества для живых клеток, для изучения специализации клеток и их злокачественного перерождения, для криоконсервации клеток и т. д. Лекция 9(29) 27
Тема 9. Методы цитологического анализа Изучение клеток in vitro (культура клеток) • Одно из важнейших направлений клеточной биологии связано с технологией – культурой клеток – заключающейся в выделении клеток из определенных частей организма и выращивании их in vitro на специальных питательных средах. • В таких культурах клетки могут делиться, перемещаться, вырабатывать различные вещества и выполнять многие из тех функций, которые бы они выполняли в организме. • Более того, при создании соответствующих условий клетки в культуре могут стать более специализированными и проявлять новые черты и новые функции. • Используя методы клеточной микрохирургии, можно производить операции на клетках in vitro, например пересаживать ядра от одной клетки другой, вызывать слияние клеток двух разных тканей и даже двух разных видов. • Культура клеток и тканей используется, например, для определения токсичности того или иного вещества для живых клеток, для изучения специализации клеток и их злокачественного перерождения, для криоконсервации клеток и т. д. Лекция 9(29) 27
 Тема 9. Методы цитологического анализа Культура клеток • Для приготовления клеточных культур обычно при помощи протеолитических ферментов, например трипсина, вызывают диссоциацию ткани. Выделенные из тканей клетки инкубируют при температуре тела в специальной питательной среде, обычно с добавлением сыворотки. В соответствующей среде клетки растут в виде либо суспензии, либо, чаще, монослоя на дне культурального сосуда. • Очень немногие клетки, находясь в культуре, способны продолжать деление в течение нескольких месяцев и более. Однако некоторые клетки могут сохраняться в культуральной среде и пролиферировать более или менее бесконечно благодаря изменению в их генетической конституции. Такие клетки образуют так называемые непрерывные клеточные линии. • Если осторожно заморозить такие клетки с добавлением криопротекторов – особых веществ, предохраняющих клетки от летальных воздействий кристаллов льда, то их можно довольно долго хранить в жидком азоте, а затем по мере надобности использовать для закладки новых культур. • Важное преимущество изучения клеток in vitro – возможность проводить наблюдения в контролируемых условиях среды, которая имитирует среду организма, но вместе с тем позволяет избежать тех сложных влияний, которым клетки подвергаются в целом организме. Недостаток: перенос в искусственную среду оказывает сильное влияние на организацию и функции клеток. Лекция 9(29) 28
Тема 9. Методы цитологического анализа Культура клеток • Для приготовления клеточных культур обычно при помощи протеолитических ферментов, например трипсина, вызывают диссоциацию ткани. Выделенные из тканей клетки инкубируют при температуре тела в специальной питательной среде, обычно с добавлением сыворотки. В соответствующей среде клетки растут в виде либо суспензии, либо, чаще, монослоя на дне культурального сосуда. • Очень немногие клетки, находясь в культуре, способны продолжать деление в течение нескольких месяцев и более. Однако некоторые клетки могут сохраняться в культуральной среде и пролиферировать более или менее бесконечно благодаря изменению в их генетической конституции. Такие клетки образуют так называемые непрерывные клеточные линии. • Если осторожно заморозить такие клетки с добавлением криопротекторов – особых веществ, предохраняющих клетки от летальных воздействий кристаллов льда, то их можно довольно долго хранить в жидком азоте, а затем по мере надобности использовать для закладки новых культур. • Важное преимущество изучения клеток in vitro – возможность проводить наблюдения в контролируемых условиях среды, которая имитирует среду организма, но вместе с тем позволяет избежать тех сложных влияний, которым клетки подвергаются в целом организме. Недостаток: перенос в искусственную среду оказывает сильное влияние на организацию и функции клеток. Лекция 9(29) 28
 Тема 9. Методы цитологического анализа Дополнительная литература 1. Свенсон К. , , Уэбстер П. . Клетка, М. , Мир, 1980 2. Ченцов Ю. С. , Общая цитология, Изд. МГУ, 1978, стр. 209 -220 3. Де. Робертис Е. , Новинский В. , Саэс Ф. , Общая цитология, ИИЛ, М. , 1962 4. Хэм А. , Кормак Д. , Гистология, т. 1, М. , Мир, 1982 5. Рис Э. , Стернберг М. От клеток к атомам (Иллюстрированное введение в молекулярную биологию), М. , Мир, 1988 29
Тема 9. Методы цитологического анализа Дополнительная литература 1. Свенсон К. , , Уэбстер П. . Клетка, М. , Мир, 1980 2. Ченцов Ю. С. , Общая цитология, Изд. МГУ, 1978, стр. 209 -220 3. Де. Робертис Е. , Новинский В. , Саэс Ф. , Общая цитология, ИИЛ, М. , 1962 4. Хэм А. , Кормак Д. , Гистология, т. 1, М. , Мир, 1982 5. Рис Э. , Стернберг М. От клеток к атомам (Иллюстрированное введение в молекулярную биологию), М. , Мир, 1988 29


