слайд л-44.ppt
- Количество слайдов: 44
 ТЕМА 14 Элементы классической и квантовой статистик Лекция № 44 Основные понятия статистики. Молекулярная физика Учебные вопросы: 1. Статистический и термодинамический методы изучения систем многих частиц. 2. Распределение Максвелла и Больцмана в классической статистике. 3. Экспериментальная достоверность распределения Максвелла. 1
ТЕМА 14 Элементы классической и квантовой статистик Лекция № 44 Основные понятия статистики. Молекулярная физика Учебные вопросы: 1. Статистический и термодинамический методы изучения систем многих частиц. 2. Распределение Максвелла и Больцмана в классической статистике. 3. Экспериментальная достоверность распределения Максвелла. 1
![ОСНОВНАЯ ЛИТЕРАТУРА: [10] Маркеев Б. М. Физика ч. IV. Квантовая физика. МВУРЭ, 1996 г, ОСНОВНАЯ ЛИТЕРАТУРА: [10] Маркеев Б. М. Физика ч. IV. Квантовая физика. МВУРЭ, 1996 г,](https://present5.com/presentation/9391476_169805112/image-2.jpg) ОСНОВНАЯ ЛИТЕРАТУРА: [10] Маркеев Б. М. Физика ч. IV. Квантовая физика. МВУРЭ, 1996 г, лекция № 42. [13] Маркеев Б. Н. , Кульбицкий Ю. Н. и др. Физика. Задания для самостоятельной работы, МВУРЭ, 1997 г, лекция № 43. ДОПОЛНИТЕЛЬНАЯ: [3] Трофимова Т. И. Курс физики М. - Высшая школа, 1994 г. , § 44 – 45. [2] Савельев И. В. Курс общей физики, Т. 1. - М. : Наука, 1982 г. , § 73 -77. 2
ОСНОВНАЯ ЛИТЕРАТУРА: [10] Маркеев Б. М. Физика ч. IV. Квантовая физика. МВУРЭ, 1996 г, лекция № 42. [13] Маркеев Б. Н. , Кульбицкий Ю. Н. и др. Физика. Задания для самостоятельной работы, МВУРЭ, 1997 г, лекция № 43. ДОПОЛНИТЕЛЬНАЯ: [3] Трофимова Т. И. Курс физики М. - Высшая школа, 1994 г. , § 44 – 45. [2] Савельев И. В. Курс общей физики, Т. 1. - М. : Наука, 1982 г. , § 73 -77. 2
 1. 1. Предмет молекулярной физики Молекулярной физикой называется наука, изучающая физические свойства систем в зависимости от их молекулярного строения, сил взаимодействия между частицами системы и характера теплового движения этих частиц. статистический термодинамический 3
1. 1. Предмет молекулярной физики Молекулярной физикой называется наука, изучающая физические свойства систем в зависимости от их молекулярного строения, сил взаимодействия между частицами системы и характера теплового движения этих частиц. статистический термодинамический 3
 1. 2. Общая характеристика двух методов молекулярной физики Статистическая физика или статистика раздел физики, в котором свойства макроскопических тел или систем изучаются на основе свойств и взаимодействий микроскопических частиц, образующих тело или систему. Термодинамика, в отличие от статистики, изучает свойства и процессы в макроскопических телах, не рассматривая микроскопическую природу 4 тел.
1. 2. Общая характеристика двух методов молекулярной физики Статистическая физика или статистика раздел физики, в котором свойства макроскопических тел или систем изучаются на основе свойств и взаимодействий микроскопических частиц, образующих тело или систему. Термодинамика, в отличие от статистики, изучает свойства и процессы в макроскопических телах, не рассматривая микроскопическую природу 4 тел.
 1. 3. Основные положения статистики Основные положения кинетической теории: молекулярно- 1. Все вещества состоят из большого числа частиц (молекул, атомов, ионов, элементарных частиц). 2. Частицы находятся в беспорядочном тепловом движении, средняя кинетическая энергия которого определяет температуру тела. 3. Частицы взаимодействуют между собой. 5
1. 3. Основные положения статистики Основные положения кинетической теории: молекулярно- 1. Все вещества состоят из большого числа частиц (молекул, атомов, ионов, элементарных частиц). 2. Частицы находятся в беспорядочном тепловом движении, средняя кинетическая энергия которого определяет температуру тела. 3. Частицы взаимодействуют между собой. 5
 В классической статистике в дополнение к перечисленным важнейшим положениям молекулярно-кинетической теории приняты также следующие: 1. Все молекулы движутся в соответствии с законами механики Ньютона, обладая в каждый момент времени определенными значениями координат и вектора скорости. 2. При взаимодействии молекул выполняются законы сохранения энергии, импульса, момента импульса. 3. Выполняется принцип различимости частиц молекул. 6
В классической статистике в дополнение к перечисленным важнейшим положениям молекулярно-кинетической теории приняты также следующие: 1. Все молекулы движутся в соответствии с законами механики Ньютона, обладая в каждый момент времени определенными значениями координат и вектора скорости. 2. При взаимодействии молекул выполняются законы сохранения энергии, импульса, момента импульса. 3. Выполняется принцип различимости частиц молекул. 6
 1. 4. Сведения из теории вероятности х1, х2, . . . , хi, . . . N: N 1 хi Ni х1 х2 N 2 7
1. 4. Сведения из теории вероятности х1, х2, . . . , хi, . . . N: N 1 хi Ni х1 х2 N 2 7
 ТЕОРЕМА СЛОЖЕНИЯ ВЕРОЯТНОСТЕЙ . 8
ТЕОРЕМА СЛОЖЕНИЯ ВЕРОЯТНОСТЕЙ . 8
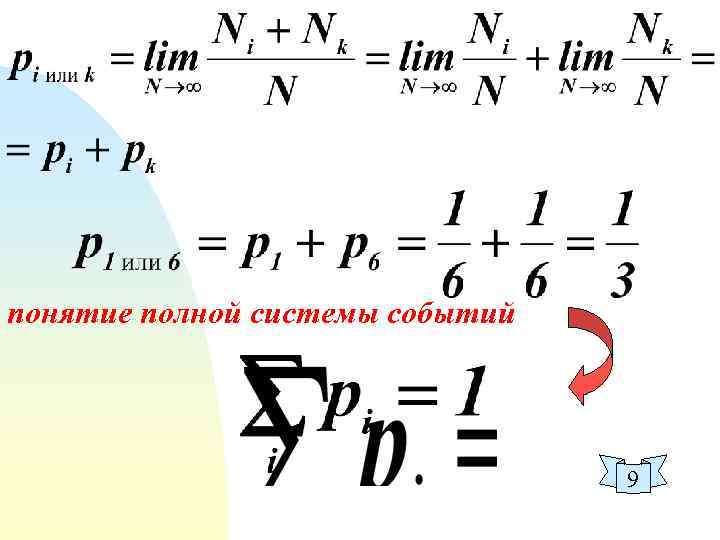 понятие полной системы событий 9
понятие полной системы событий 9
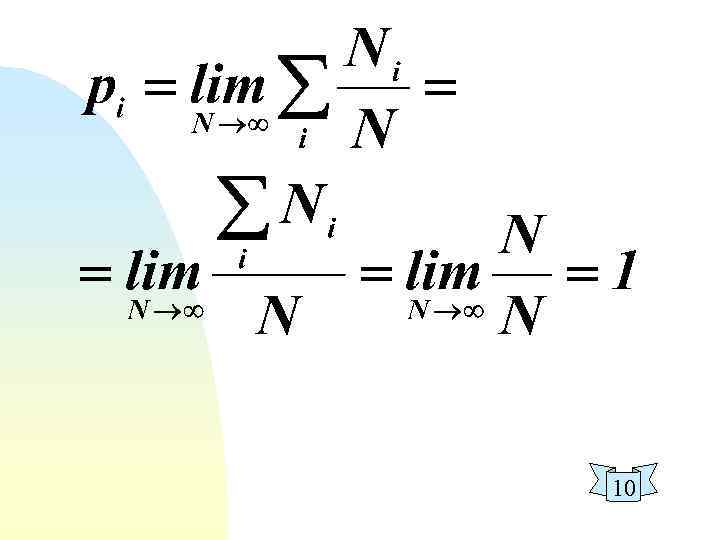 10
10
 ТЕОРЕМА УМНОЖЕНИЯ 11 ВЕРОЯТНОСТЕЙ
ТЕОРЕМА УМНОЖЕНИЯ 11 ВЕРОЯТНОСТЕЙ
 1. 5. Функция распределения dp - х: от х до х + dх f(х) - функция распределения вероятности плотность вероятности 12
1. 5. Функция распределения dp - х: от х до х + dх f(х) - функция распределения вероятности плотность вероятности 12
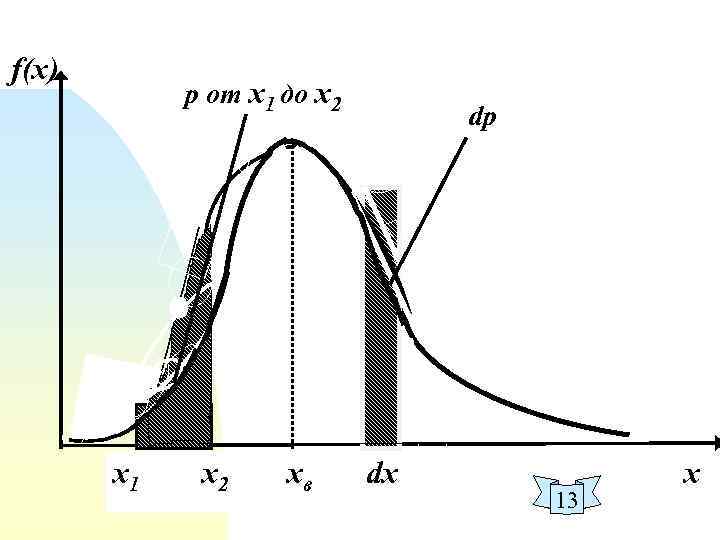 f(x) р от x 1 до x 2 x 1 x 2 xв dp dx 13 x
f(x) р от x 1 до x 2 x 1 x 2 xв dp dx 13 x
 Свойства функции распределения вероятности 1. f(x) 0 2. 3. условие нормировки 14
Свойства функции распределения вероятности 1. f(x) 0 2. 3. условие нормировки 14
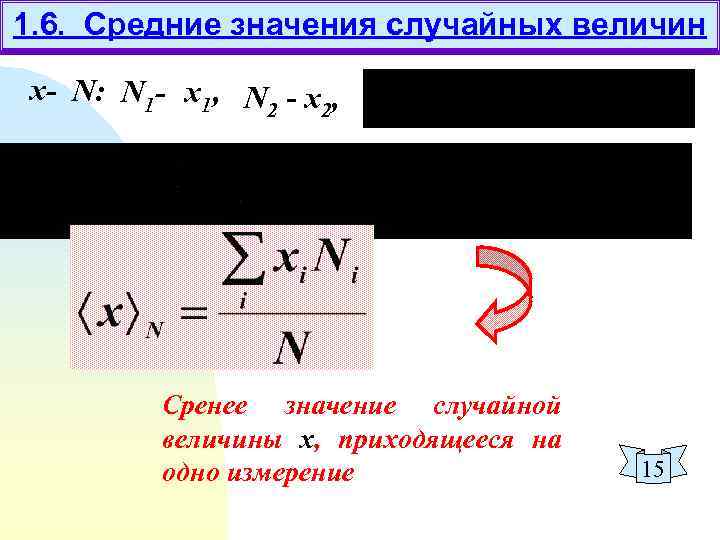 1. 6. Средние значения случайных величин х- N: N 1 - х1, N - х , 2 2 Сренее значение случайной величины x, приходящееся на одно измерение 15
1. 6. Средние значения случайных величин х- N: N 1 - х1, N - х , 2 2 Сренее значение случайной величины x, приходящееся на одно измерение 15
 теорема Чебышева математическое ожидание 16
теорема Чебышева математическое ожидание 16
 Свойства средних величин: 1. Среднее значение постоянной величины равно самой постоянной величине 2. Среднее значение суммы нескольких случайных величин равно сумме средних значений этих величин 3. Среднее значение произведения взаимно независимых случайных величин равно произведению средних значений каждой из них 17
Свойства средних величин: 1. Среднее значение постоянной величины равно самой постоянной величине 2. Среднее значение суммы нескольких случайных величин равно сумме средних значений этих величин 3. Среднее значение произведения взаимно независимых случайных величин равно произведению средних значений каждой из них 17
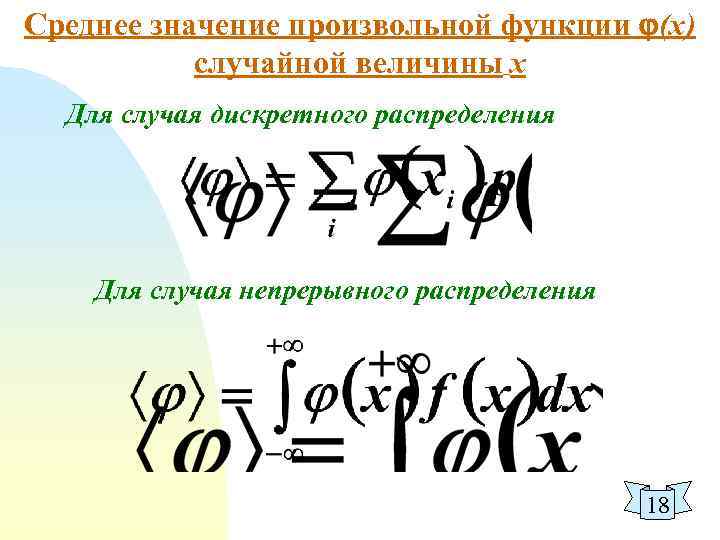 Среднее значение произвольной функции (х) случайной величины х Для случая дискретного распределения Для случая непрерывного распределения 18
Среднее значение произвольной функции (х) случайной величины х Для случая дискретного распределения Для случая непрерывного распределения 18
 В Ы В О Д Ы: 1. Статистика изучает свойства макроскопических тел или систем на основе свойств составляющих систему микроскопических частиц, термодинамика же не рассматривает микроскопическую природу тел. 2. Статистическая физика использует вероятностные методы и опирается на основные положения молекулярно-кинетической теории. 19
В Ы В О Д Ы: 1. Статистика изучает свойства макроскопических тел или систем на основе свойств составляющих систему микроскопических частиц, термодинамика же не рассматривает микроскопическую природу тел. 2. Статистическая физика использует вероятностные методы и опирается на основные положения молекулярно-кинетической теории. 19
 2. 1. Предмет классической статистики Классическая статистика изучает закономерности, характеризующие поведение и свойства систем, состоящих из очень большого числа частиц (например, молекул), движение которых подчиняется законам классической механики. 20
2. 1. Предмет классической статистики Классическая статистика изучает закономерности, характеризующие поведение и свойства систем, состоящих из очень большого числа частиц (например, молекул), движение которых подчиняется законам классической механики. 20
 2. 2. Понятие v - пространства v-пространство или пространство скоростей воображаемое пространство, вдоль осей декартовых координат которого откладываются значения компонент скорости vx, vy, vz, отдельных молекул vz dv vv vy vx Объем шарового слоя в v-пространстве 21
2. 2. Понятие v - пространства v-пространство или пространство скоростей воображаемое пространство, вдоль осей декартовых координат которого откладываются значения компонент скорости vx, vy, vz, отдельных молекул vz dv vv vy vx Объем шарового слоя в v-пространстве 21
 2. 3. Функция распределения молекул по скоростям от х до х + dx, от y до y + dy, от z до z + dz Z dz dy dx 0 y х 22
2. 3. Функция распределения молекул по скоростям от х до х + dx, от y до y + dy, от z до z + dz Z dz dy dx 0 y х 22
 элемент объема в v-пространстве: v. Z от dvz до dvy dvx vy 0 v. Х функция распределения газовых молекул по скоростям или плотность вероятности распределения по скоростям 23
элемент объема в v-пространстве: v. Z от dvz до dvy dvx vy 0 v. Х функция распределения газовых молекул по скоростям или плотность вероятности распределения по скоростям 23
 - концентрация молекул 24
- концентрация молекул 24
 стационарное равновесное состояние газа: 25
стационарное равновесное состояние газа: 25
 функция распределения газовых молекул по абсолютным скоростям 26
функция распределения газовых молекул по абсолютным скоростям 26
 27
27
 2. 4. Распределение Максвелла Максвелл, 1860 г. k = 1, 38 10 -23 Дж/К- постоянная Больцмана Из условия нормировки: 28
2. 4. Распределение Максвелла Максвелл, 1860 г. k = 1, 38 10 -23 Дж/К- постоянная Больцмана Из условия нормировки: 28
 функция F(v) распределения Максвелла по абсолютным скоростям: функция f(v) распределения Максвелла по скоростям: 29
функция F(v) распределения Максвелла по абсолютным скоростям: функция f(v) распределения Максвелла по скоростям: 29
 функция распределения молекул по энергиям теплового движения 30
функция распределения молекул по энергиям теплового движения 30
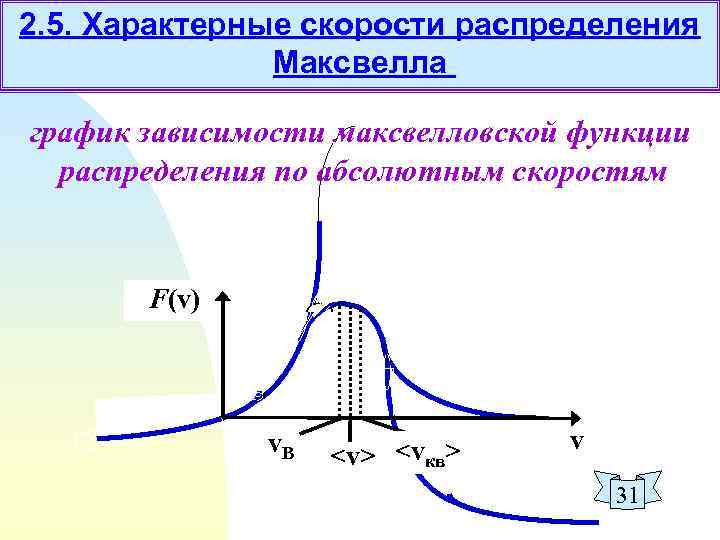 2. 5. Характерные скорости распределения Максвелла график зависимости максвелловской функции распределения по абсолютным скоростям F(v) v. В
2. 5. Характерные скорости распределения Максвелла график зависимости максвелловской функции распределения по абсолютным скоростям F(v) v. В
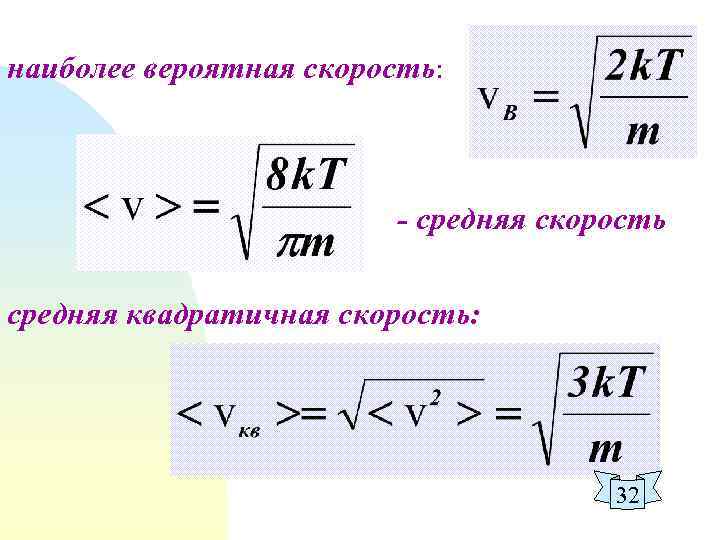 наиболее вероятная скорость: - средняя скорость средняя квадратичная скорость: 32
наиболее вероятная скорость: - средняя скорость средняя квадратичная скорость: 32
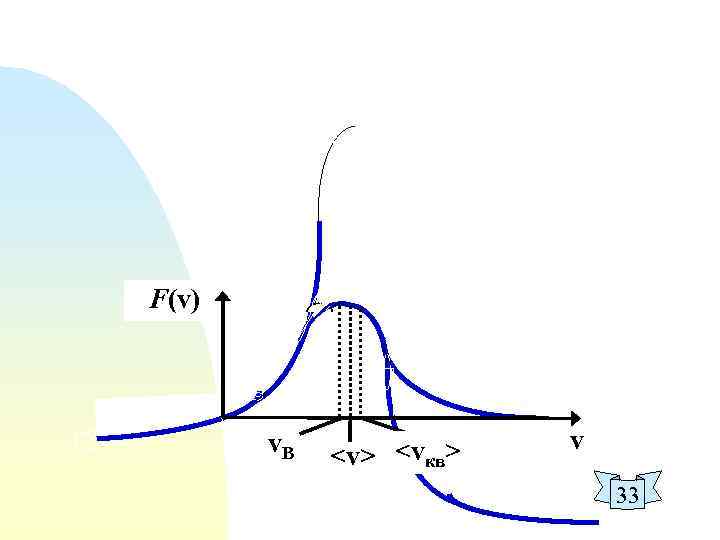 F(v) v. В
F(v) v. В
 средняя кинетическая энергия молекулы газа 34
средняя кинетическая энергия молекулы газа 34
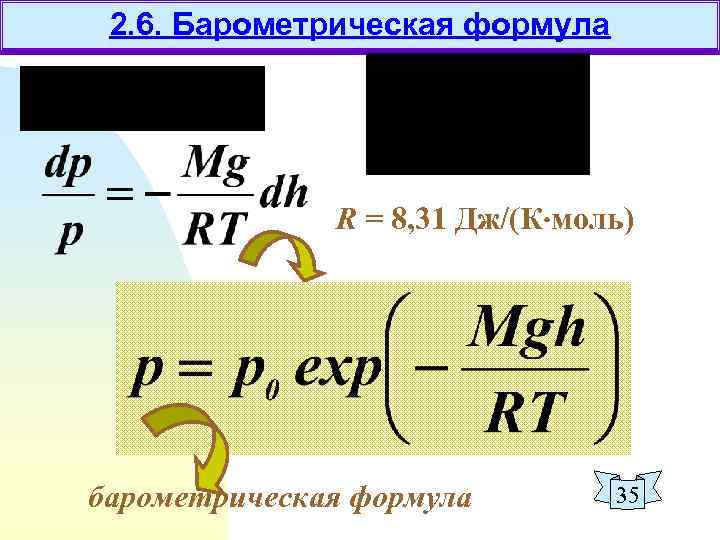 2. 6. Барометрическая формула R = 8, 31 Дж/(К моль) барометрическая формула 35
2. 6. Барометрическая формула R = 8, 31 Дж/(К моль) барометрическая формула 35
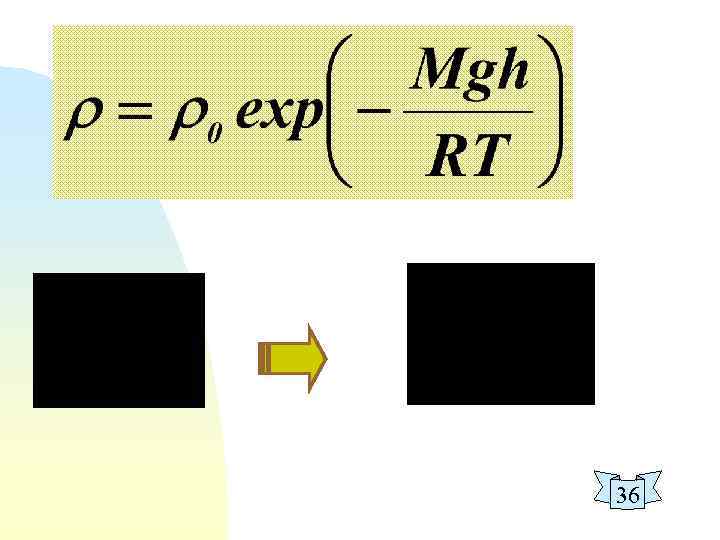 36
36
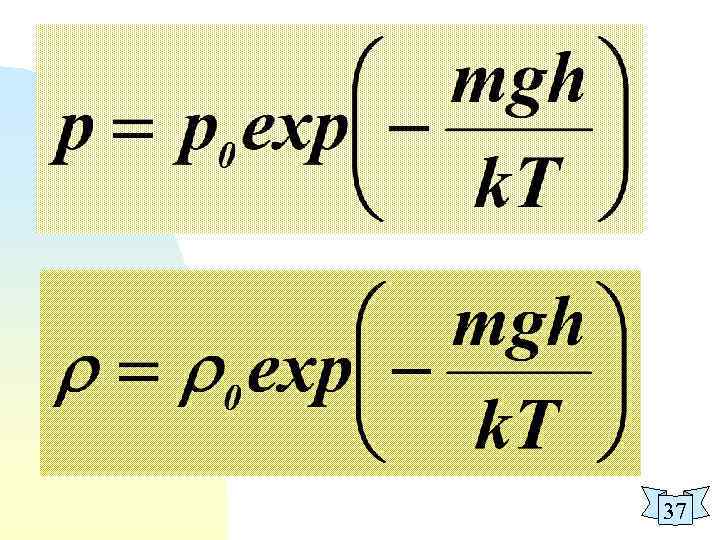 37
37
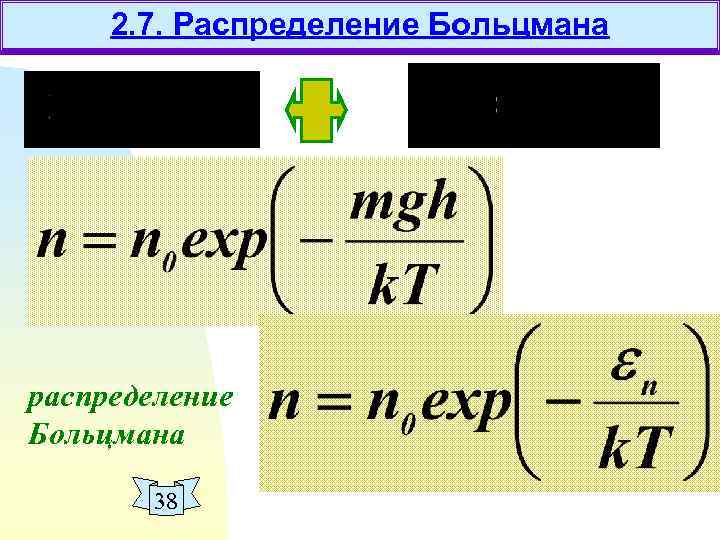 2. 7. Распределение Больцмана распределение Больцмана 38
2. 7. Распределение Больцмана распределение Больцмана 38
 2. 8. Распределение Больцмана в дискретном случае 39
2. 8. Распределение Больцмана в дискретном случае 39
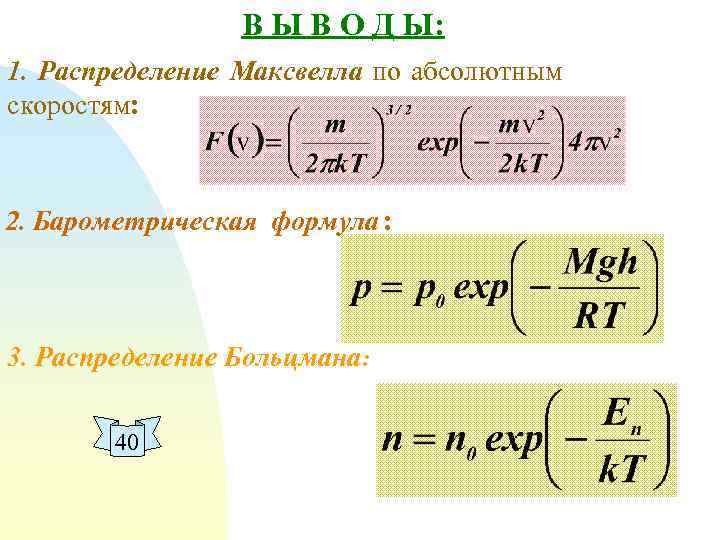 В Ы В О Д Ы: 1. Распределение Максвелла по абсолютным скоростям: 2. Барометрическая формула : 3. Распределение Больцмана: 40
В Ы В О Д Ы: 1. Распределение Максвелла по абсолютным скоростям: 2. Барометрическая формула : 3. Распределение Больцмана: 40
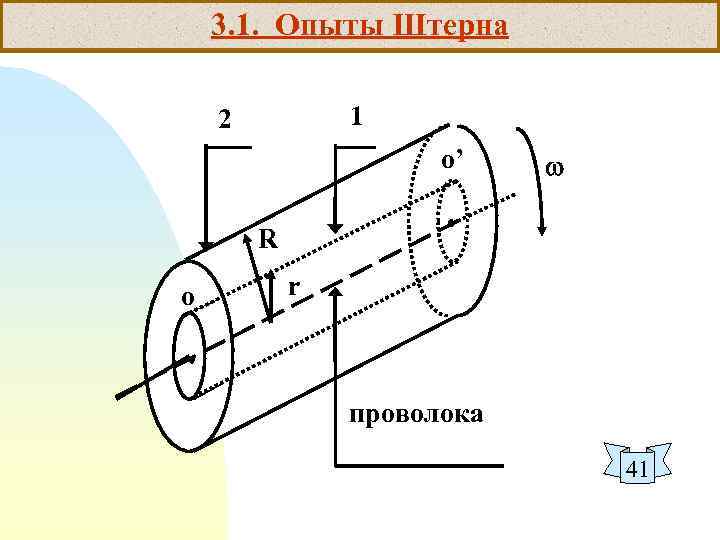 3. 1. Опыты Штерна 1 2 о’ R о r проволока 41
3. 1. Опыты Штерна 1 2 о’ R о r проволока 41
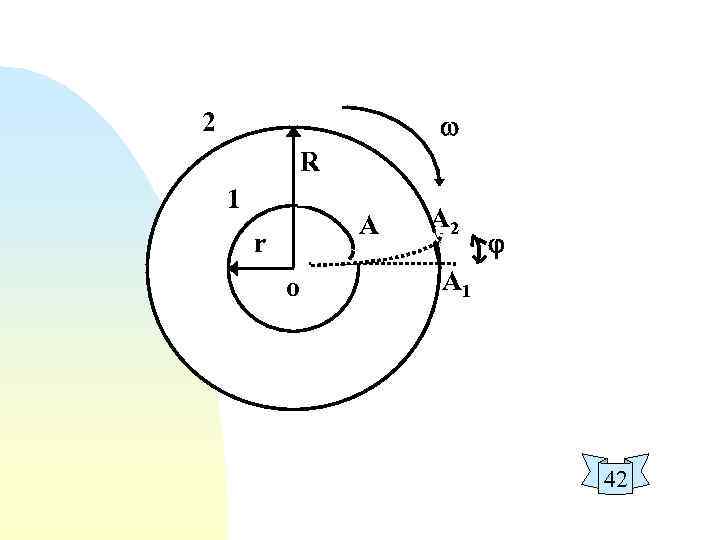 2 R 1 A r о А 2 А 1 42
2 R 1 A r о А 2 А 1 42
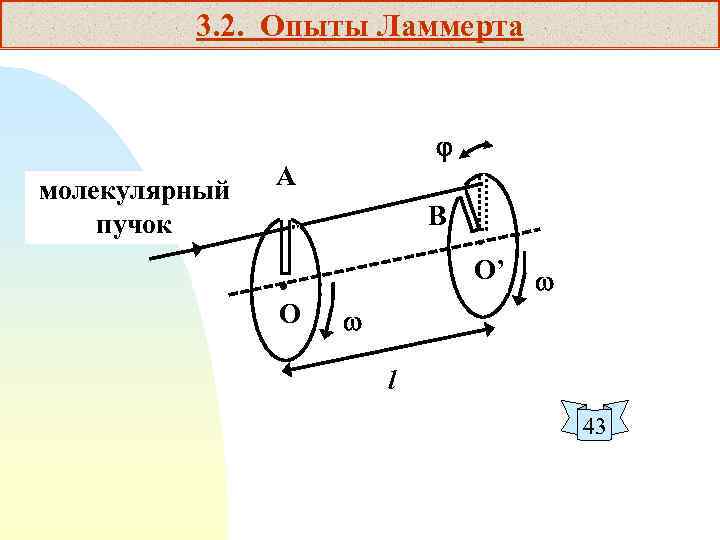 3. 2. Опыты Ламмерта молекулярный пучок А В О’ О l 43
3. 2. Опыты Ламмерта молекулярный пучок А В О’ О l 43
 В Ы В О Д Ы: 1. Распределение Максвелла было много раз проверено тщательными экспериментами. Наиболее известными из них являются опыты Штерна (1920) и Ламмерта (1929). 44
В Ы В О Д Ы: 1. Распределение Максвелла было много раз проверено тщательными экспериментами. Наиболее известными из них являются опыты Штерна (1920) и Ламмерта (1929). 44


