12 Свойства металлов.ppt
- Количество слайдов: 28

Тема 12. Химические свойства металлов. 12. 1. Общие представления о взаимодействии металлов с окислителями

В любых химических реакциях металлы всегда выступают в качестве восстановителей. n Технически важные металлы в природе встречаются только в окисленном состоянии Магнитный железняк Галенит Fe. O, Fe 2 O 3, Fe 3 O 4 Pb. S Киноварь Hg. S Железный колчедан Fe. S Бленда Zn. S n При выплавке затрачивают энергию и переводят металл в свободное состояние: Fe 2 O 3 +CO→ Fe + CO 2 n Поэтому обратная реакция, окисление металлов, – энергетически выгодный процесс (ΔG<0).

Пути протекания реакций взаимодействия металлов с окислителями: n Химический – связан с непосредственным окислением металла окислителем. Характеризуется высокой энергией активации. Протекает лишь при высоких температурах. Fe + O 2 → Fe 2 O 3 (t >300 o. C); Fe + H 2 S → Fe. S (t >260 o. C); n Электрохимический – связан с участием в процессе окисления электролита, снижающего энергию активации процесса окисления. Протекает при любых температурах, при которых раствор электролита находится в жидком состоянии. Характерен для химических реакций, лежащих в основе коррозии нефтяного оборудования. Fe → Fe 2+ +2 e. Fe 2++ 2 OH- → Fe(OH)2 + 2 H 2 O + O 2 → Fe(OH)3 O 2 + 2 H 2 O + 4 e- → 4 OHFe(OH)3 → Fe 2 O 3 + H 2 O
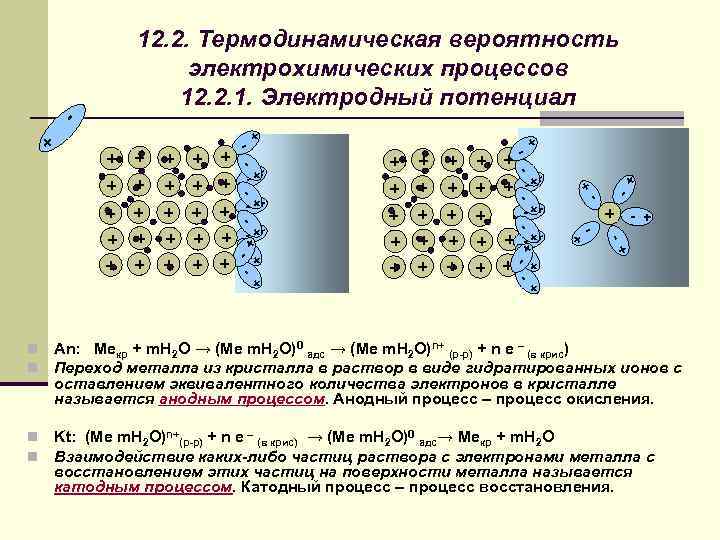
12. 2. Термодинамическая вероятность электрохимических процессов 12. 2. 1. Электродный потенциал - + - + - + + - + - + + + + - - + - + + + + + - + + - + + + + + + - + + n n An: Meкр + m. H 2 O → (Me m. H 2 O)0 адс → (Me m. H 2 O)n+ (р-р) + n e – (в крис) Переход металла из кристалла в раствор в виде гидратированных ионов с оставлением эквивалентного количества электронов в кристалле называется анодным процессом. Анодный процесс – процесс окисления. n n Kt: (Me m. H 2 O)n+(р-р) + n e – (в крис) → (Me m. H 2 O)0 адс→ Meкр + m. H 2 O Взаимодействие каких-либо частиц раствора с электронами металла с восстановлением этих частиц на поверхности металла называется катодным процессом. Катодный процесс – процесс восстановления.
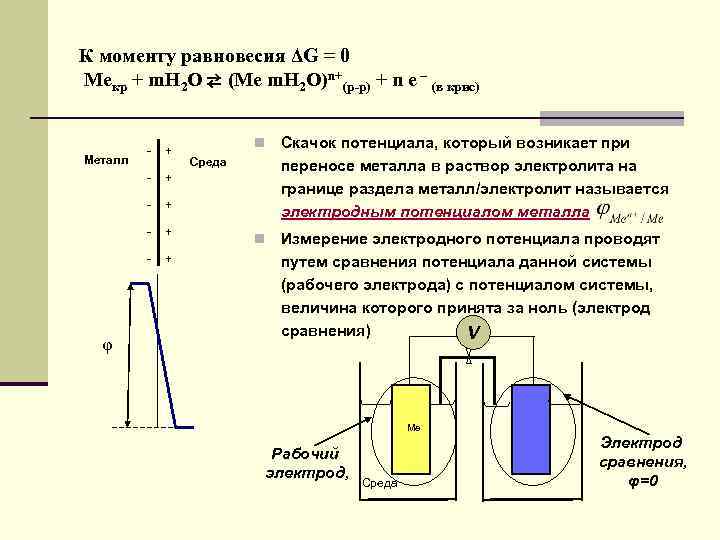
К моменту равновесия ΔG = 0 Meкр + m. H 2 O ⇄ (Me m. H 2 O)n+(р-р) + n e – (в крис) - + - Металл Скачок потенциала, который возникает при переносе металла в раствор электролита на границе раздела металл/электролит называется электродным потенциалом металла n Измерение электродного потенциала проводят путем сравнения потенциала данной системы (рабочего электрода) с потенциалом системы, величина которого принята за ноль (электрод сравнения) V + - + + + - φ n + Среда Me Рабочий электрод, Среда Электрод сравнения, φ=0
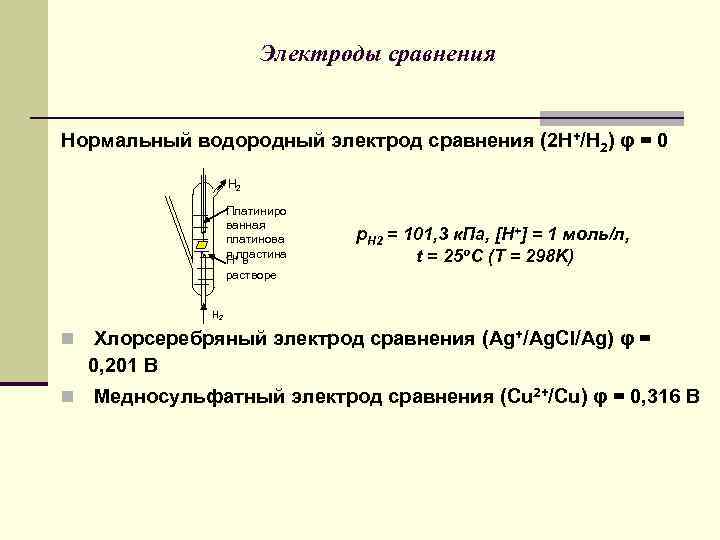
Электроды сравнения Нормальный водородный электрод сравнения (2 H+/H 2) φ = 0 H 2 Платиниро ванная платинова я+ пластина Н в растворе р. Н 2 = 101, 3 к. Па, [H+] = 1 моль/л, t = 25 o. C (T = 298 K) Н 2 n n Хлорсеребряный электрод сравнения (Ag+/Ag. Cl/Ag) φ = 0, 201 В Медносульфатный электрод сравнения (Cu 2+/Cu) φ = 0, 316 В
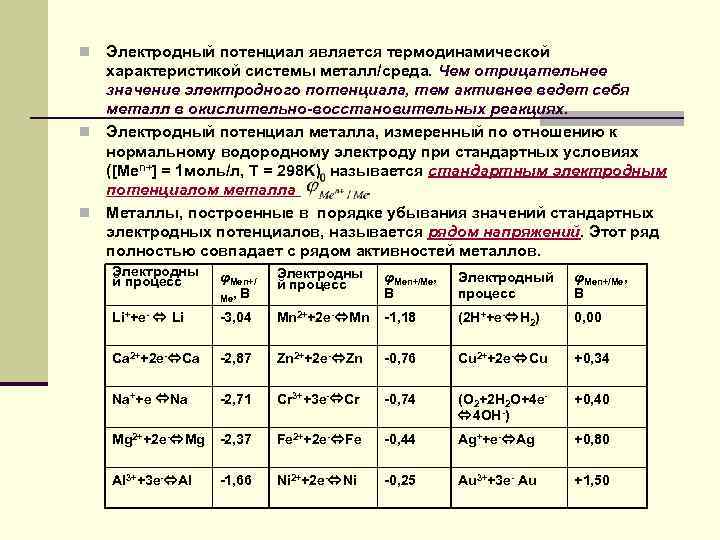
Электродный потенциал является термодинамической характеристикой системы металл/среда. Чем отрицательнее значение электродного потенциала, тем активнее ведет себя металл в окислительно-восстановительных реакциях. n Электродный потенциал металла, измеренный по отношению к нормальному водородному электроду при стандартных условиях ([Men+] = 1 моль/л, T = 298 K) называется стандартным электродным потенциалом металла. n Металлы, построенные в порядке убывания значений стандартных электродных потенциалов, называется рядом напряжений. Этот ряд полностью совпадает с рядом активностей металлов. n Электродны й процесс φMen+/ Me, В Электродны й процесс φMen+/Me, В Электродный процесс φMen+/Me, В Li++e- Li -3, 04 Mn 2++2 e- Mn -1, 18 (2 H++e- H 2) 0, 00 Ca 2++2 e- Ca -2, 87 Zn 2++2 e- Zn -0, 76 Cu 2++2 e- Cu +0, 34 Na++e Na -2, 71 Cr 3++3 e- Cr -0, 74 (O 2+2 H 2 O+4 e 4 OH-) +0, 40 Mg 2++2 e- Mg -2, 37 Fe 2++2 e- Fe -0, 44 Ag++e- Ag +0, 80 Al 3++3 e- Al -1, 66 Ni 2++2 e- Ni -0, 25 Au 3++3 e- Au +1, 50

Уравнение Нернста - потенциал системы металл/электролит, В - стандартный потенциал системы металл/электролит, В R - универсальная газовая постоянная, = 8, 31 Дж/моль К T - температура системы, К n - количество электронов, участвующих в процессе при растворении 1 моля металла, моль n F - число Фарадея, = 96500 кулон n [Ox] – концентрация участника реакции в окисленной форме, моль/л n [Red] – концентрация участника реакции в восстановленной форме, моль/л n n n Для металлов:

12. 3. Гальванический элемент ε = φ Cu 2+/Cu - φ Zn 2+/Zn = 0, 34 -(-0, 76)=1, 1 (В) e- Гальваническим элементом называется система из двух электродов, обладающая электронной и ионной проводимостью. Cu Zn Zn. SO 4, 1 моль/л Cu. SO 4, 1 моль/л ЭДС гальванического элемента определяется как разность потенциалов между анодом и катодом. T = 298 К Zn 2+ + 2 e- φ Zn 2+/Zn = -0, 76 В Анодом называется электрод, с которого электроны стекают по внешней цепи. Катодом называется электрод, к которому электроны поступают по внешней цепи. Cu 2+ + 2 e- φ Cu 2+/Cu = +0, 34 В Схема гальванического элемента записывается по направлению электрического тока: от анода к катоду: Zn/ Zn. SO 4//Cu. SO 4/Cu
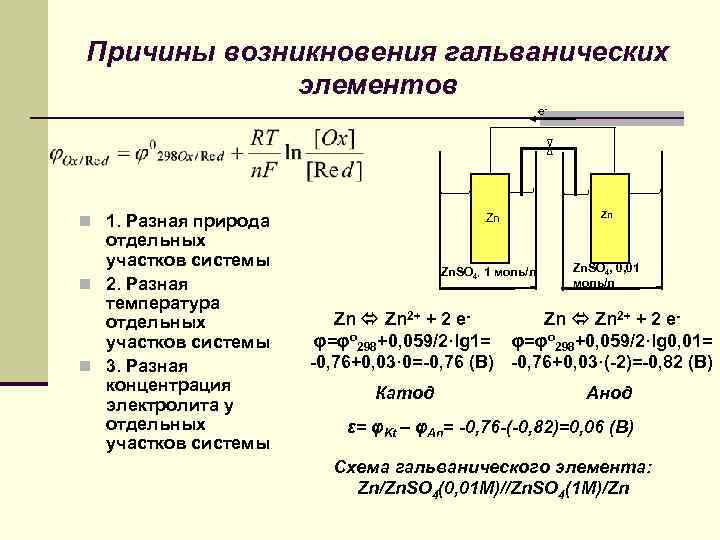
Причины возникновения гальванических элементов e- n 1. Разная природа отдельных участков системы n 2. Разная температура отдельных участков системы n 3. Разная концентрация электролита у отдельных участков системы Zn Zn. SO 4, 1 моль/л Zn Zn. SO 4, 0, 01 моль/л Zn 2+ + 2 eφ=φo 298+0, 059/2·lg 1= φ=φo 298+0, 059/2·lg 0, 01= -0, 76+0, 03· 0=-0, 76 (В) -0, 76+0, 03·(-2)=-0, 82 (В) Катод Анод ε= φKt – φAn= -0, 76 -(-0, 82)=0, 06 (В) Схема гальванического элемента: Zn/Zn. SO 4(0, 01 M)//Zn. SO 4(1 M)/Zn
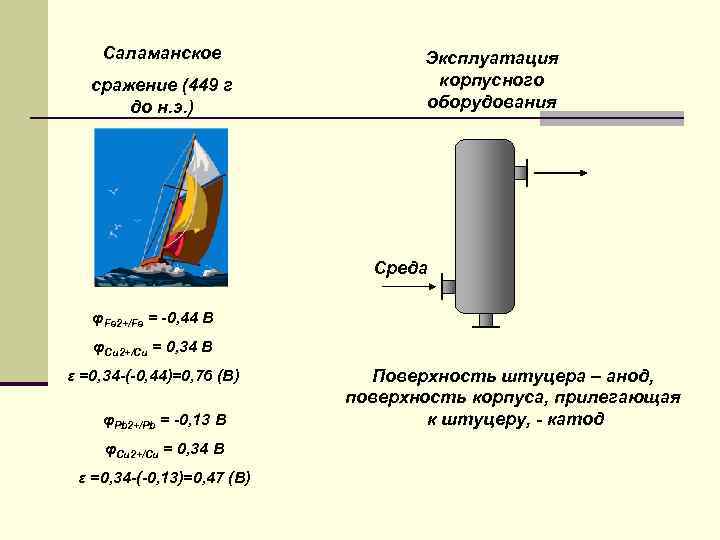
Саламанское сражение (449 г до н. э. ) Эксплуатация корпусного оборудования Среда φFe 2+/Fe = -0, 44 В φCu 2+/Cu = 0, 34 В ε =0, 34 -(-0, 44)=0, 76 (В) φPb 2+/Pb = -0, 13 В φCu 2+/Cu = 0, 34 В ε =0, 34 -(-0, 13)=0, 47 (В) Поверхность штуцера – анод, поверхность корпуса, прилегающая к штуцеру, - катод

12. 4. Кинетика электрохимических процессов n Скорость электрохимического процесса: V – скорость, г/м 2 час n Δm – масса металла, перешедшего в ионное состояние, n S – площадь поверхности раздела металл/электролит n τ – продолжительность контакта металла с электролитом n

Законы Фарадея (1830 г) 1791 -1867 1. 2. 3. 4. 5. 6. 7. Масса образующегося или растворяющегося в результате электрохимической реакции вещества пропорциональна количеству прошедшего через раствор электричества 2. Равные количества электричества приводят к электрохимическому превращению эквивалентных Количеств разных веществ Q – количество электричества, прошедшего через систему; F – число Фарадея, νэ – количество эквивалентов металла, перешедшего в ионное состояние, I – сила тока, τ - продолжительность контакта металла с электролитом, i – плотность тока, S – площадь поверхности раздела металл/электролит, Δm – масса металла, перешедшего в ионное состояние, M – молярная масса металла, n - количество электронов, участвующих в процессе при растворении 1 моля металла, V – скорость электрохимической реакции Плотность тока и скорость электрохимической реакции пропорциональны другу. Плотность тока является кинетической характеристикой системы металл/электролит
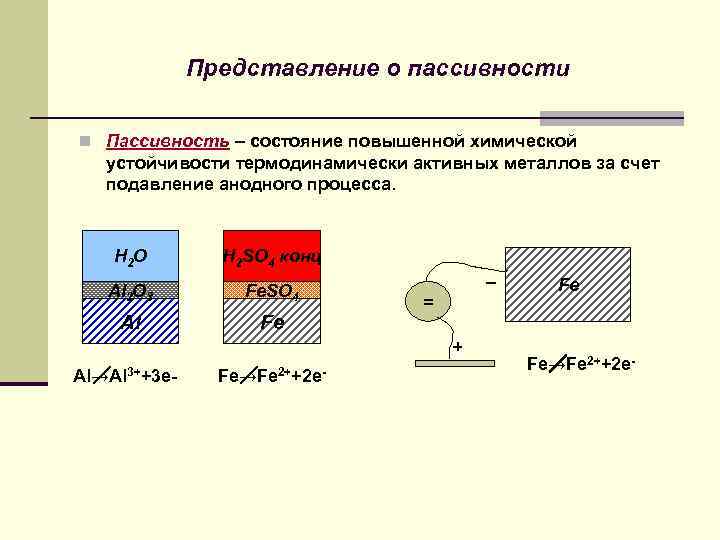
Представление о пассивности n Пассивность – состояние повышенной химической устойчивости термодинамически активных металлов за счет подавление анодного процесса. H 2 O H 2 SO 4 конц Al 2 O 3 Fe. SO 4 Al Fe _ = + Al→Al 3++3 e- Fe→Fe 2++2 e- Fe Fe→Fe 2++2 e-

12. 5. Общее представление о коррозии металлов. n Коррозия – это самопроизвольно протекающее химическое взаимодействие металла со средой, приводящее к изменению свойств этого металла или изготовленной из него металлоконструкции.
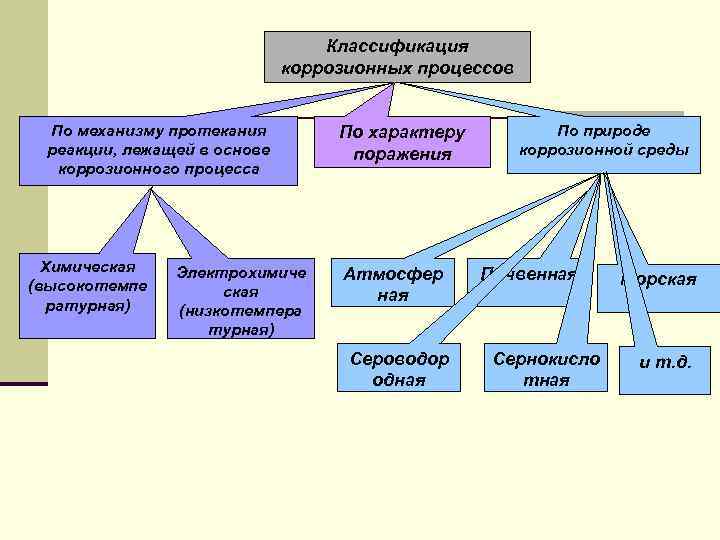
Классификация коррозионных процессов По механизму протекания реакции, лежащей в основе коррозионного процесса Химическая (высокотемпе ратурная) Электрохимиче ская (низкотемпера турная) По характеру поражения Атмосфер ная Сероводор одная По природе коррозионной среды Почвенная Сернокисло тная Морская и т. д.
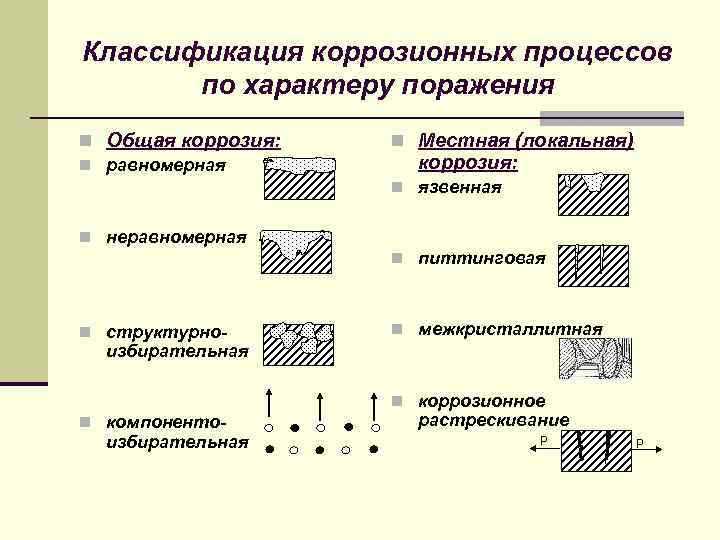
Классификация коррозионных процессов по характеру поражения n Общая коррозия: n равномерная n Местная (локальная) коррозия: n язвенная n неравномерная n питтинговая n структурно- n межкристаллитная избирательная n коррозионное n компоненто- избирательная растрескивание Р Р

Основные закономерности коррозионных процессов n n n n Все рассмотренные выше закономерности протекания окислительновосстановительных реакций, в которых участвуют металлы, характерны и для коррозионных процессов При протекании по электрохимическому механизму основными стадиями коррозии являются: - анодный процесс; - катодный процесс; - перенос зарядов Все три процесса взаимосвязаны и не могут протекать друг без друга. При коррозии железа в воде (р. Н =7): - анодная полуреакция Fe 2++2 e- ⇄ Fe φFe 2+/Fe= - 0, 44 B - катодная полуреакция 2 H++2 e- ⇄ H 2 φFe 2+/Fe= - 0, 415 B - катодная полуреакция O 2+2 H 2 O+4 e- ⇄ 4 OH- φFe 2+/Fe= + 0, 805 B Если катодный процесс протекает в основном за счет молекул кислорода, говорят, что реакция идет с кислородной деполяризацией (нейтральные и слабощелочные среды). n Если катодный процесс протекает в основном за счет ионов водорода, говорят, что реакция идет с водородной деполяризацией (кислые среды). n
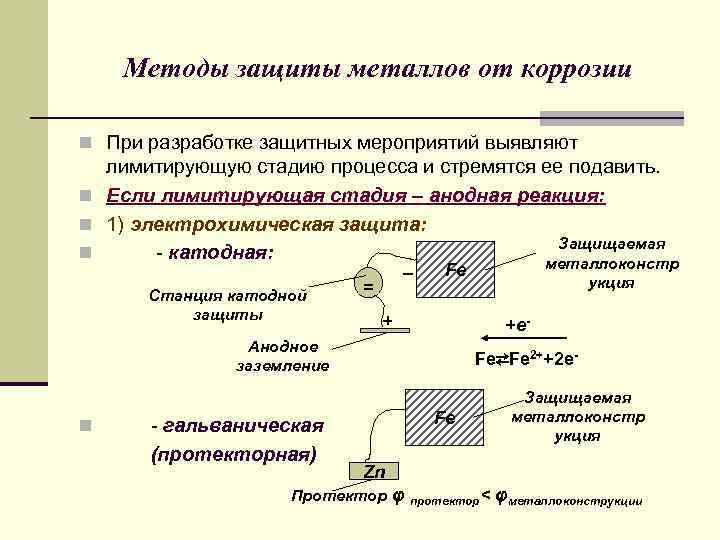
Методы защиты металлов от коррозии n При разработке защитных мероприятий выявляют лимитирующую стадию процесса и стремятся ее подавить. n Если лимитирующая стадия – анодная реакция: n 1) электрохимическая защита: Защищаемая n - катодная: металлоконстр _ Станция катодной защиты = Fe + +е- Анодное заземление n - гальваническая (протекторная) укция Fe⇄Fe 2++2 e. Fe Защищаемая металлоконстр укция Zn Протектор φ протектор< φметаллоконструкции

n 2) металлизационные покрытия: n - катодные: φNi=-0, 25 В Ni Fe φFe=-0, 44 В n - анодные: Zn. O Zn φNi=-0, 76 В Fe φFe=-0, 44 В Анодная реакция на поверхности металла затруднена, в связи с тем, что потенциал покрытия (никеля) благороднее потенциала основного металла Анодная реакция на поверхности металла затруднена, в связи с тем, что поверхность основного металла покрыта активным металлопокрытием, на котором легко образуется защитная пленка продуктов коррозии. В порах: Zn Fe Zn - анод, протектор, Fe - катод
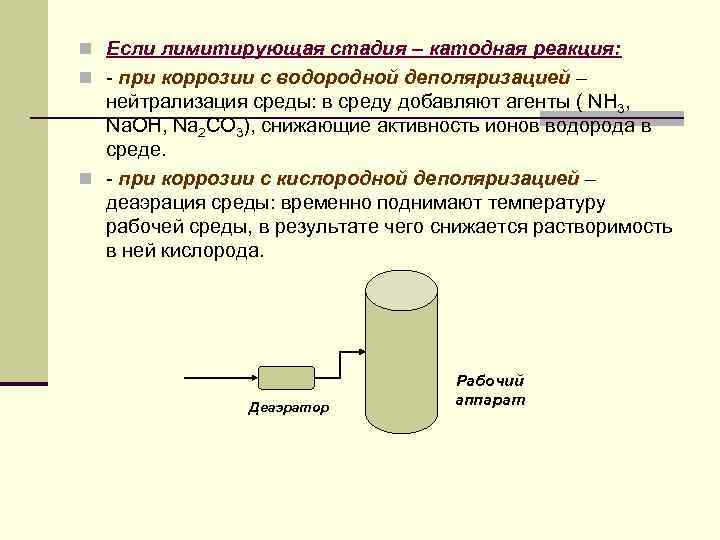
n Если лимитирующая стадия – катодная реакция: n - при коррозии с водородной деполяризацией – нейтрализация среды: в среду добавляют агенты ( NH 3, Na. OH, Na 2 CO 3), снижающие активность ионов водорода в среде. n - при коррозии с кислородной деполяризацией – деаэрация среды: временно поднимают температуру рабочей среды, в результате чего снижается растворимость в ней кислорода. Деаэратор Рабочий аппарат

Если лимитирующая стадия – процесс переноса зарядов: n - применение изоляционных покрытий: n - экструзионных полимерных (при изготовлении трубопровода на горячую поверхность трубы распылением наносят порошок полиэтилена. Он расплавляется и хорошо сорбируется поверхностью). n - битумно-полимерных n - лакокрасочных и др.
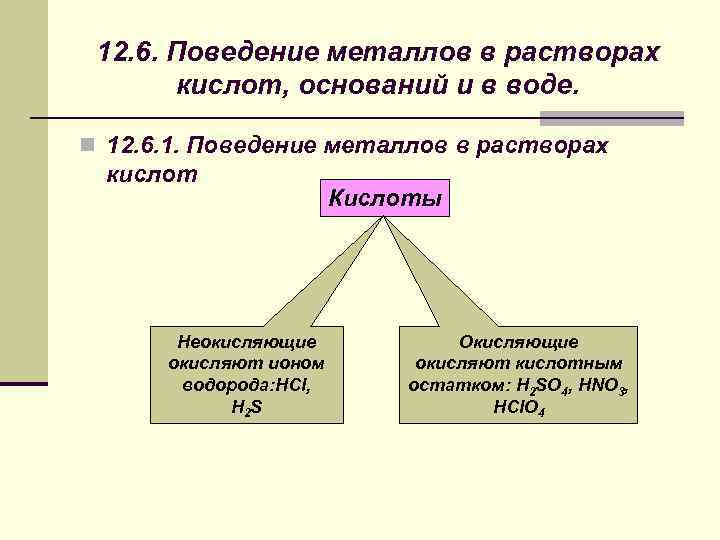
12. 6. Поведение металлов в растворах кислот, оснований и в воде. n 12. 6. 1. Поведение металлов в растворах кислот Неокисляющие окисляют ионом водорода: HCl, H 2 S Кислоты Окисляющие окисляют кислотным остатком: H 2 SO 4, HNO 3, HCl. O 4

Поведение металлов в растворах неокисляющих кислот n Металлы, потенциал которых в данных условиях n n n отрицательнее потенциала восстановления ионов водорода, вытеснят его из растворов неокисляющих кислот. Остальные металлы с окисляющими кислотами не взаимодействуют: Me + HCl → Me. Cln + H 2 если φMen+/Me< φ2 H+/H 2 Me + HCl ↛ если φMen+/Me> φ2 H+/H 2 При стандартных условиях с неокисляющими кислотами взаимодействуют только металлы, стоящие в ряду напряжений до водорода: Fe + 2 HCl → Fe. Cl 2 + H 2 Cu + 2 HCl ↛ n Разбавленная серная кислота (ω<40%) ведет себя как неокисляющая кислота: n Fe + H 2 SO 4 → Fe. SO 4 + H 2 n Cu + H 2 SO 4 ↛

Основные закономерности взаимодействия металлов с растворами окисляющих кислот n Металлы, потенциал которых в данных условиях отрицательнее потенциала восстановления кислотного остатка, окисляются за счет восстановления этого кислотного остатка n Глубина восстановления кислотного остатка тем выше, чем активнее взаимодействующий с ней металл, выше температура и ниже концентрация кислоты. n В концентрированных растворах серной и азотной кислот Fe, Al и Cr при низких температурах (до 40 o. С) пассивируются и не взаимодействуют с кислотами. При повышении температуры и при разбавлении кислоты пассивное состояние нарушается и металлы взаимодействуют с раствором кислоты.

n Взаимодействие металлов с концентрированной серной кислотой n Me + H 2 S+6 O 4 → Men(SO 4)m + (S+4 O 3, S 0, H 2 S 2 -) + H 2 O Глубина восстановления (SO 4)2 - возрастает n n Cu + H 2 SO 4 → Cu. SO 4 + SO 3 + H 2 O to C Ca + H 2 SO 4 → Ca. SO 4 + H 2 S + H 2 O Fe + H 2 SO 4 конц ↛ (пассивация) o Fe + H 2 SO 4 t CFe 2(SO 4)3 + S + H 2 O → n Взаимодействие металлов с азотной кислотой n Me + HN+5 O 3 → Me(NO 3)m + (N+4 O 2, N+32 O 3, …N-3 H 4 NO 3) + H 2 O Глубина восстановления (NO 3)2 - возрастает n n Cu + HNO 3 → Cu(NO 3)2 + NO 2 + H 2 O o. C Zn + HNO 3 разбt → Zn(NO 3)2 + NH 4 NO 3 + H 2 O Fe + HNO 3 конц ↛ (пассивация) o Fe + HNO 3 разб t CFe(NO 3)3 + NO + H 2 O →

12. 6. 2. Поведение металлов в воде n В воде φ2 H+/H 2 = -0, 415 В n Металлы, потенциал которых отрицательнее потенциала n n n восстановления ионов водорода (-0, 415 В) окисляются, вытесняя водород из воды. Эти металлы стоят в ряду напряжений до Fe (включительно). Металлы, образующие растворимые оксиды, взаимодействуют с водой, образуя основания. Эти металлы стоят в ряду напряжений до Mg. Mg, Al, Zn и Cr в воде пассивируются и не взаимодействуют с ней. Na + H 2 O → Na. OH + H 2 Fe + H 2 O → Fe. O + H 2 Al + H 2 O ↛ (пассивация)

12. 6. 3. Поведение металлов в растворах щелочей n С растворами щелочей реагируют металлы, образующие амфотерные гидроксиды: n Al + H 2 O + Na. OH → Na 3[Al(OH)6]+ H 2 n Zn + H 2 O + Na. OH → Na 2[Zn(OH)4] + H 2 n Na 3[Al(OH)6] и Na 2[Zn(OH)4] – комплексные соли. n Диссоциация: n Na 2[Zn(OH)4] ⇄ 2 Na+ + [Zn(OH)4]2+ n Анион – сложный, состоит из комплексообразователя (Al 3+, Zn 2+) и лигандов (OH-). Между анионом и катионом – связь ионная, внутри комплексного аниона , между комплексообразователем и лигандами, - ковалентная.
12 Свойства металлов.ppt