 Тема: 1)Тепловые эффекты реакций. Закон Гесса и следствия из него. 2)Скорость химических реакций. Понятие о катализе. 3)Необратимые и обратимые химические реакции. Химическое равновесие.
Тема: 1)Тепловые эффекты реакций. Закон Гесса и следствия из него. 2)Скорость химических реакций. Понятие о катализе. 3)Необратимые и обратимые химические реакции. Химическое равновесие.
 Тепловые эффекты реакций. Закон Гесса и следствия из него. Экзотермические реакции Эндотермические реакции
Тепловые эффекты реакций. Закон Гесса и следствия из него. Экзотермические реакции Эндотермические реакции
 Тепловой эффект реакции – количество теплоты, которое выделяется или поглощается.
Тепловой эффект реакции – количество теплоты, которое выделяется или поглощается.
 Энергия выделяется Энергия поглощается
Энергия выделяется Энергия поглощается
 Энтальпия – характеризует энергетическое состояние вещества (теплосодержание). Теплосодержание включает в себя внутреннюю энергию вещества и энергию, направленную на преодоление давления.
Энтальпия – характеризует энергетическое состояние вещества (теплосодержание). Теплосодержание включает в себя внутреннюю энергию вещества и энергию, направленную на преодоление давления.
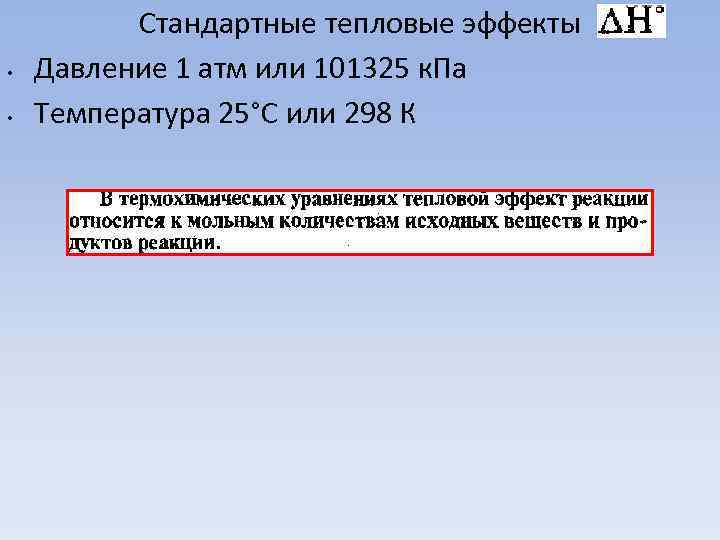 • • Стандартные тепловые эффекты Давление 1 атм или 101325 к. Па Температура 25°С или 298 К
• • Стандартные тепловые эффекты Давление 1 атм или 101325 к. Па Температура 25°С или 298 К
 Задачи на составление термохимических уравнений:
Задачи на составление термохимических уравнений:
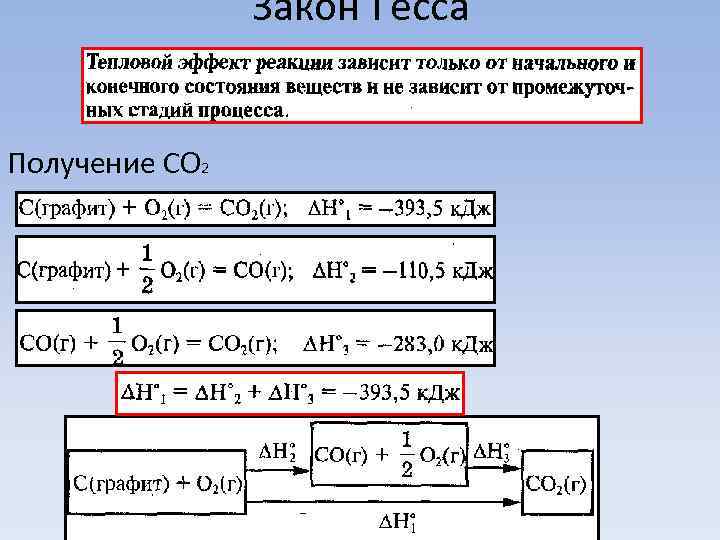 Закон Гесса Получение СО 2
Закон Гесса Получение СО 2
 Следствия из закона Гесса Первое следствие из закона Гесса
Следствия из закона Гесса Первое следствие из закона Гесса
 Второе следствие из закона Гесса
Второе следствие из закона Гесса
 Скорость химических реакций. Понятие о катализе.
Скорость химических реакций. Понятие о катализе.
 Скорость любой химической реакции зависит от: • • • v v Природы реагирующих веществ Концентрации реагирующих веществ Температуры Присутствия катализатора Скорость гетерогенной реакции зависит также от: Величины поверхности раздела фаз Скорости подвода реагирующих веществ к поверхности раздела фаз и отвода от нее продуктов реакции
Скорость любой химической реакции зависит от: • • • v v Природы реагирующих веществ Концентрации реагирующих веществ Температуры Присутствия катализатора Скорость гетерогенной реакции зависит также от: Величины поверхности раздела фаз Скорости подвода реагирующих веществ к поверхности раздела фаз и отвода от нее продуктов реакции
 Количественно зависимость скорости реакции от концентрации реагирующих веществ выражается законом действующих масс. Для простейших одностадийных реакций концентрации веществ берутся в степенях, равных коэффициентам перед формулами веществ в уравнении реакции. Например: Кинетическое уравнение реакции К – константа скорости реакции, которая равна скорости реакции при концентрациях реагирующих веществ 1 моль/л (зависит от природы реагирующих веществ, температуры, но не зависит от окнцентрации)
Количественно зависимость скорости реакции от концентрации реагирующих веществ выражается законом действующих масс. Для простейших одностадийных реакций концентрации веществ берутся в степенях, равных коэффициентам перед формулами веществ в уравнении реакции. Например: Кинетическое уравнение реакции К – константа скорости реакции, которая равна скорости реакции при концентрациях реагирующих веществ 1 моль/л (зависит от природы реагирующих веществ, температуры, но не зависит от окнцентрации)
 В кинетическое уравнение входят концентрации газообразных и растворенных веществ, но не входят концентрации твердых веществ
В кинетическое уравнение входят концентрации газообразных и растворенных веществ, но не входят концентрации твердых веществ
 При увеличении температуры скорость химических реакций повышается. Правила Вант-Гоффа - температурный коэффициент, который показывает во сколько раз увеличилась скорость реакции при повышении температуры на 10°С.
При увеличении температуры скорость химических реакций повышается. Правила Вант-Гоффа - температурный коэффициент, который показывает во сколько раз увеличилась скорость реакции при повышении температуры на 10°С.
 Катализ • Гомогенный • Гетерогенный Ингибиторы – вещества, в присутствии которых реакции замедляются.
Катализ • Гомогенный • Гетерогенный Ингибиторы – вещества, в присутствии которых реакции замедляются.