Lektsii_FKhOTES.ppt
- Количество слайдов: 144
 Тема 1 Основы химической термодинамики 1. 2. 3. 4. Основные понятия термодинамики (ТД). Первый закон ТД. Закон Гесса. Второй закон ТД. Понятие энтропии. Третий закон ТД. 1
Тема 1 Основы химической термодинамики 1. 2. 3. 4. Основные понятия термодинамики (ТД). Первый закон ТД. Закон Гесса. Второй закон ТД. Понятие энтропии. Третий закон ТД. 1
 Основные понятия ТД Термодинамика (ТД) – это раздел теоретической физики, в котором изучают наиболее общие свойства систем, находящихся в состоянии теплового равновесия, и процессы перехода между этими состояниями, сопровождаемые превращением теплоты в другие виды энергии. Химическая ТД – это раздел физической химии, в котором свойства вещества, химические реакции, фазовые переходы и др. процессы рассматриваются с точки зрения ТД. Ограничения: классическая термодинамика рассматривает тела, состоящие из большого числа молекул, т. е. макроскопические системы. В термодинамике не рассматривается внутреннее строение тела и характер движения отдельных частиц, составляющих это тело. 2
Основные понятия ТД Термодинамика (ТД) – это раздел теоретической физики, в котором изучают наиболее общие свойства систем, находящихся в состоянии теплового равновесия, и процессы перехода между этими состояниями, сопровождаемые превращением теплоты в другие виды энергии. Химическая ТД – это раздел физической химии, в котором свойства вещества, химические реакции, фазовые переходы и др. процессы рассматриваются с точки зрения ТД. Ограничения: классическая термодинамика рассматривает тела, состоящие из большого числа молекул, т. е. макроскопические системы. В термодинамике не рассматривается внутреннее строение тела и характер движения отдельных частиц, составляющих это тело. 2
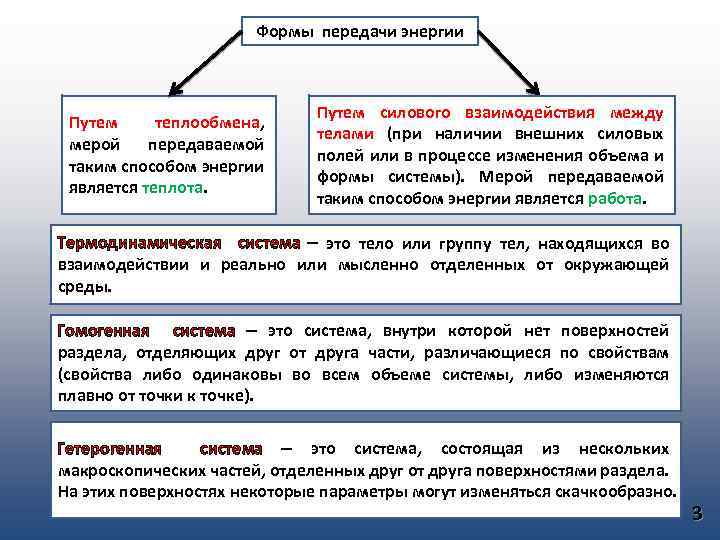 Формы передачи энергии Путем теплообмена, мерой передаваемой таким способом энергии является теплота. Путем силового взаимодействия между телами (при наличии внешних силовых полей или в процессе изменения объема и формы системы). Мерой передаваемой таким способом энергии является работа. Термодинамическая система – это тело или группу тел, находящихся во взаимодействии и реально или мысленно отделенных от окружающей среды. Гомогенная система – это система, внутри которой нет поверхностей раздела, отделяющих друг от друга части, различающиеся по свойствам (свойства либо одинаковы во всем объеме системы, либо изменяются плавно от точки к точке). Гетерогенная система – это система, состоящая из нескольких макроскопических частей, отделенных друг от друга поверхностями раздела. На этих поверхностях некоторые параметры могут изменяться скачкообразно. 3
Формы передачи энергии Путем теплообмена, мерой передаваемой таким способом энергии является теплота. Путем силового взаимодействия между телами (при наличии внешних силовых полей или в процессе изменения объема и формы системы). Мерой передаваемой таким способом энергии является работа. Термодинамическая система – это тело или группу тел, находящихся во взаимодействии и реально или мысленно отделенных от окружающей среды. Гомогенная система – это система, внутри которой нет поверхностей раздела, отделяющих друг от друга части, различающиеся по свойствам (свойства либо одинаковы во всем объеме системы, либо изменяются плавно от точки к точке). Гетерогенная система – это система, состоящая из нескольких макроскопических частей, отделенных друг от друга поверхностями раздела. На этих поверхностях некоторые параметры могут изменяться скачкообразно. 3
 Однородная система – это система, в которой все части объема обладают одинаковым составом (химически однородная система) и одинаковыми свойствами (физически однородная система). В противном случае система неоднородная. Фаза – это совокупность всех гомогенных частей системы, одинаковых по составу, физическим и химическим свойствам и отделенных от других частей системы поверхностью раздела. Изолированная система – это система, которая не может обмениваться веществом и энергией (в форме теплоты и работы) с окружающей средой и имеет постоянный объем. Закрытая система – это система, которая не может обмениваться веществом с окружающей средой, но способна обмениваться энергией и может не сохранять постоянным свой объем. Открытая система – это система, в которой существует обмен энергией и веществом с окружающей средой. 4
Однородная система – это система, в которой все части объема обладают одинаковым составом (химически однородная система) и одинаковыми свойствами (физически однородная система). В противном случае система неоднородная. Фаза – это совокупность всех гомогенных частей системы, одинаковых по составу, физическим и химическим свойствам и отделенных от других частей системы поверхностью раздела. Изолированная система – это система, которая не может обмениваться веществом и энергией (в форме теплоты и работы) с окружающей средой и имеет постоянный объем. Закрытая система – это система, которая не может обмениваться веществом с окружающей средой, но способна обмениваться энергией и может не сохранять постоянным свой объем. Открытая система – это система, в которой существует обмен энергией и веществом с окружающей средой. 4
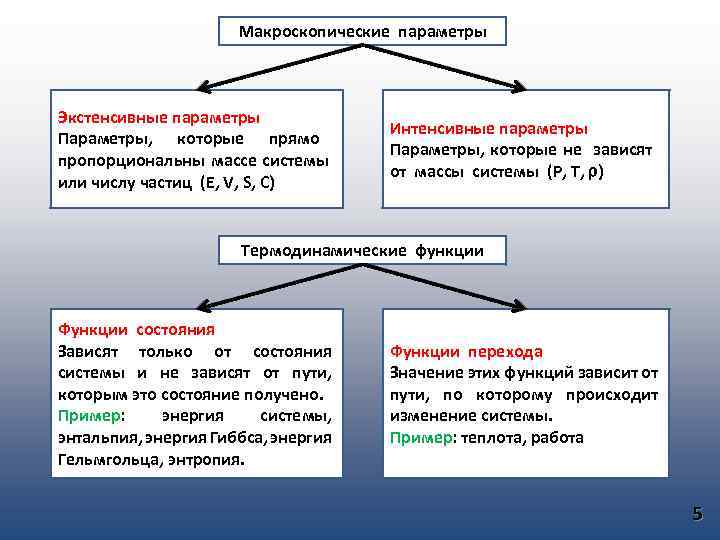 Макроскопические параметры Экстенсивные параметры Параметры, которые прямо пропорциональны массе системы или числу частиц (E, V, S, C) Интенсивные параметры Параметры, которые не зависят от массы системы (P, T, ρ) Термодинамические функции Функции состояния Зависят только от состояния системы и не зависят от пути, которым это состояние получено. Пример: энергия системы, энтальпия, энергия Гиббса, энергия Гельмгольца, энтропия. Функции перехода Значение этих функций зависит от пути, по которому происходит изменение системы. Пример: теплота, работа. 5
Макроскопические параметры Экстенсивные параметры Параметры, которые прямо пропорциональны массе системы или числу частиц (E, V, S, C) Интенсивные параметры Параметры, которые не зависят от массы системы (P, T, ρ) Термодинамические функции Функции состояния Зависят только от состояния системы и не зависят от пути, которым это состояние получено. Пример: энергия системы, энтальпия, энергия Гиббса, энергия Гельмгольца, энтропия. Функции перехода Значение этих функций зависит от пути, по которому происходит изменение системы. Пример: теплота, работа. 5
 Термодинамический процесс – это всякое изменение, происходящее в системе, при котором происходит изменение хотя бы одного параметра. Изотермический процесс – процесс, происходящий при постоянной температуре Изобарный процесс – процесс, происходящий при постоянном давлении Изохорный процесс – процесс, происходящий при постоянном объеме Адиабатный процесс – процессы, которые происходят без теплообмена между системой и окружающей средой, хотя система может быть связана с окружающей средой работой, которая может совершаться над системой или наоборот. Обратимый термодинамический процесс – это процесс, при котором система возвращается в первоначальное состояние без оставления в ОС каких-либо макроскопических изменений. Обратимые процессы протекают последовательно через ряд состояний равновесия. 6
Термодинамический процесс – это всякое изменение, происходящее в системе, при котором происходит изменение хотя бы одного параметра. Изотермический процесс – процесс, происходящий при постоянной температуре Изобарный процесс – процесс, происходящий при постоянном давлении Изохорный процесс – процесс, происходящий при постоянном объеме Адиабатный процесс – процессы, которые происходят без теплообмена между системой и окружающей средой, хотя система может быть связана с окружающей средой работой, которая может совершаться над системой или наоборот. Обратимый термодинамический процесс – это процесс, при котором система возвращается в первоначальное состояние без оставления в ОС каких-либо макроскопических изменений. Обратимые процессы протекают последовательно через ряд состояний равновесия. 6
 Первый закон ТД. Закон Гесса. Wкмех – это энергия механического движения системы как единого целого Wпотвнеш – это потенциальная энергия системы во внешнем поле (гравитационном, электромагнитном и др. ) U - внутренняя энергия системы. Включает в себя энергию всевозможных вводов движения и взаимодействия всех частиц (молекул, атомов, ионов, электронов), образующих рассматриваемую систему. Закон сохранения энергии Если в каком-нибудь процессе энергия одного вида исчезает, то взамен ее появляется энергия в другой форме, количестве строго эквивалентном первому 7
Первый закон ТД. Закон Гесса. Wкмех – это энергия механического движения системы как единого целого Wпотвнеш – это потенциальная энергия системы во внешнем поле (гравитационном, электромагнитном и др. ) U - внутренняя энергия системы. Включает в себя энергию всевозможных вводов движения и взаимодействия всех частиц (молекул, атомов, ионов, электронов), образующих рассматриваемую систему. Закон сохранения энергии Если в каком-нибудь процессе энергия одного вида исчезает, то взамен ее появляется энергия в другой форме, количестве строго эквивалентном первому 7
 ПЕРВЫЙ ЗАКОН ТЕРМОДИНАМИКИ Внутренняя энергия системы, находящейся в данном состоянии, имеет одно и то же значение и не зависит от того, каким изменениям подвергалась система при переходе к данному состоянию. Изменение внутренней энергии системы при переходе из одного состояния в другое не зависит от пути процесса, а зависит только от начального и конечного состояния системы. СЛЕДСТВИЕ: В любой изолированной системе общий запас внутренней энергии сохраняется постоянным. Теплота, сообщаемая системе, расходуется на изменение внутренней энергии системы и на совершении системой работы против внешних сил. 8
ПЕРВЫЙ ЗАКОН ТЕРМОДИНАМИКИ Внутренняя энергия системы, находящейся в данном состоянии, имеет одно и то же значение и не зависит от того, каким изменениям подвергалась система при переходе к данному состоянию. Изменение внутренней энергии системы при переходе из одного состояния в другое не зависит от пути процесса, а зависит только от начального и конечного состояния системы. СЛЕДСТВИЕ: В любой изолированной системе общий запас внутренней энергии сохраняется постоянным. Теплота, сообщаемая системе, расходуется на изменение внутренней энергии системы и на совершении системой работы против внешних сил. 8
 ЗАКОН ГЕССА (1840 г. ) Если из данных исходных веществ можно различными путями получить заданные конечные продукты, то независимо от пути получения, т. е. от вида промежуточных реакций, суммарный тепловой эффект для всех путей будет одним и тем же. Тепловой эффект – это сумма поглощенной теплоты и всей работы, выполняемой окружающей средой над данной системой, за вычетом работы внешнего давления. Паровой трактор Паровой грузовик 9
ЗАКОН ГЕССА (1840 г. ) Если из данных исходных веществ можно различными путями получить заданные конечные продукты, то независимо от пути получения, т. е. от вида промежуточных реакций, суммарный тепловой эффект для всех путей будет одним и тем же. Тепловой эффект – это сумма поглощенной теплоты и всей работы, выполняемой окружающей средой над данной системой, за вычетом работы внешнего давления. Паровой трактор Паровой грузовик 9
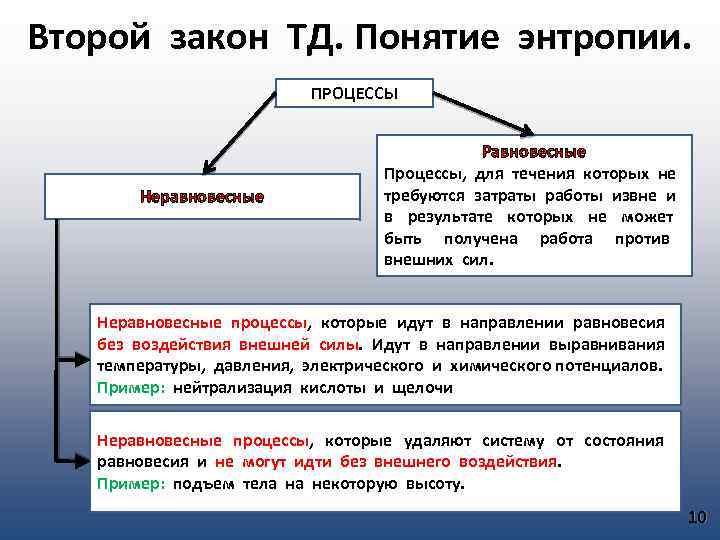 Второй закон ТД. Понятие энтропии. ПРОЦЕССЫ Неравновесные Равновесные Процессы, для течения которых не требуются затраты работы извне и в результате которых не может быть получена работа против внешних сил. Неравновесные процессы, которые идут в направлении равновесия без воздействия внешней силы. Идут в направлении выравнивания температуры, давления, электрического и химического потенциалов. Пример: нейтрализация кислоты и щелочи Неравновесные процессы, которые удаляют систему от состояния равновесия и не могут идти без внешнего воздействия. Пример: подъем тела на некоторую высоту. 10
Второй закон ТД. Понятие энтропии. ПРОЦЕССЫ Неравновесные Равновесные Процессы, для течения которых не требуются затраты работы извне и в результате которых не может быть получена работа против внешних сил. Неравновесные процессы, которые идут в направлении равновесия без воздействия внешней силы. Идут в направлении выравнивания температуры, давления, электрического и химического потенциалов. Пример: нейтрализация кислоты и щелочи Неравновесные процессы, которые удаляют систему от состояния равновесия и не могут идти без внешнего воздействия. Пример: подъем тела на некоторую высоту. 10
 ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ 1850 г. – постулат Клаузиуса Единственным результатом любой совокупности процессов не может быть переход теплоты от менее нагретой системы к более нагретой 1851 г. – постулат Томсона Теплота наиболее холодного тела из участвующих в круговом процессе не может служить источником работы 11
ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ 1850 г. – постулат Клаузиуса Единственным результатом любой совокупности процессов не может быть переход теплоты от менее нагретой системы к более нагретой 1851 г. – постулат Томсона Теплота наиболее холодного тела из участвующих в круговом процессе не может служить источником работы 11
 Энтропия – это функция состояния системы, изменение которой равно сумме приведенных теплот, поглощенных системой в равновесном состоянии. Для обратимого процесса Для необратимых процессов Для обратимого изотермического процесса 12
Энтропия – это функция состояния системы, изменение которой равно сумме приведенных теплот, поглощенных системой в равновесном состоянии. Для обратимого процесса Для необратимых процессов Для обратимого изотермического процесса 12
 Статистический характер второго закона термодинамики Первый закон ТД справедлив для систем, состоящих из любого количества частиц. Второй закон имеет статистический характер и относится только к системам, состоящим из очень большого числа частиц. Закон устанавливает критерий большей или меньшей вероятности сравниваемых состояний. В системе, состоящей из большого числа частиц самопроизвольно могут происходить переходы из менее вероятного состояния в более вероятное (например, расширение газов). Вероятность каждого макросостояния пропорциональна числу микросостояний, которыми оно осуществляется. Это число называется термодинамической вероятностью. Чтобы от ТД вероятности перейти к математической необходимо значение ТД вероятности разделить на полное число всех возможных распределений молекул по данному признаку. Расширение газа 13
Статистический характер второго закона термодинамики Первый закон ТД справедлив для систем, состоящих из любого количества частиц. Второй закон имеет статистический характер и относится только к системам, состоящим из очень большого числа частиц. Закон устанавливает критерий большей или меньшей вероятности сравниваемых состояний. В системе, состоящей из большого числа частиц самопроизвольно могут происходить переходы из менее вероятного состояния в более вероятное (например, расширение газов). Вероятность каждого макросостояния пропорциональна числу микросостояний, которыми оно осуществляется. Это число называется термодинамической вероятностью. Чтобы от ТД вероятности перейти к математической необходимо значение ТД вероятности разделить на полное число всех возможных распределений молекул по данному признаку. Расширение газа 13
 Третий закон ТД Теорема Нэрнста (1906 г. ) Вблизи абсолютного нуля все ТД процессы протекают без изменения энтропии Постулат Планка Энтропия индивидуального идеального кристаллического вещества при абсолютном нуле равна нулю. Для идеального твердого тела Для плавления твердого тела Энтропия пара 14
Третий закон ТД Теорема Нэрнста (1906 г. ) Вблизи абсолютного нуля все ТД процессы протекают без изменения энтропии Постулат Планка Энтропия индивидуального идеального кристаллического вещества при абсолютном нуле равна нулю. Для идеального твердого тела Для плавления твердого тела Энтропия пара 14
 Тема 2 Характеристические функции и термодинамические потенциалы 1. Характеристические функции. 2. Уравнение Гиббса - Гельмгольца. 15
Тема 2 Характеристические функции и термодинамические потенциалы 1. Характеристические функции. 2. Уравнение Гиббса - Гельмгольца. 15
 Характеристические функции В изолированных системах самопроизвольное течение процессов и условия равновесия могут быть однозначно выражены через энтропию и ее изменение. В конце XIX века были открыты термодинамические функции, изменение которых при определенных условиях существования системы давали возможность определить направление самопроизвольного течения процесса и условия равновесия. Энтропия Внутренняя энергия ХАРАКТЕРИСТИЧЕСКИЕ ФУНКЦИИ Энергия Гиббса Энергия Гельмгольца Энтальпия 16
Характеристические функции В изолированных системах самопроизвольное течение процессов и условия равновесия могут быть однозначно выражены через энтропию и ее изменение. В конце XIX века были открыты термодинамические функции, изменение которых при определенных условиях существования системы давали возможность определить направление самопроизвольного течения процесса и условия равновесия. Энтропия Внутренняя энергия ХАРАКТЕРИСТИЧЕСКИЕ ФУНКЦИИ Энергия Гиббса Энергия Гельмгольца Энтальпия 16
 1. Внутренняя энергия При одинаковых условиях количество внутренней энергии прямо пропорционально количеству вещества. Изменение энергии положительно, если энтропия возрастает. 2. Энтропия Это функция состояния системы, изменение которой равно сумме приведенных теплот, поглощенных системой в равновесном состоянии. 17
1. Внутренняя энергия При одинаковых условиях количество внутренней энергии прямо пропорционально количеству вещества. Изменение энергии положительно, если энтропия возрастает. 2. Энтропия Это функция состояния системы, изменение которой равно сумме приведенных теплот, поглощенных системой в равновесном состоянии. 17
 3. Энтальпия При рассмотрении процессов, протекающих при постоянном объеме удобно пользоваться изменением внутренней энергии. При изобарных процессах удобнее пользоваться энтальпией Для изобарно-изотермических процессов тепловой эффект равен изменению внутренней энергии Для изохорно-изотермических процессов тепловой эффект равен изменению энтальпии системы 18
3. Энтальпия При рассмотрении процессов, протекающих при постоянном объеме удобно пользоваться изменением внутренней энергии. При изобарных процессах удобнее пользоваться энтальпией Для изобарно-изотермических процессов тепловой эффект равен изменению внутренней энергии Для изохорно-изотермических процессов тепловой эффект равен изменению энтальпии системы 18
 4. Энергия Гельмгольца Работа, производимая системой будет наибольшей, когда процесс обратим. Для процессов, протекающих при постоянной температуре в случае конечного изменения Энергия Гельмгольца Это функция определяет направление и предел течения самопроизвольных процессов для систем, находящихся при постоянной температуре и постоянном объеме 19
4. Энергия Гельмгольца Работа, производимая системой будет наибольшей, когда процесс обратим. Для процессов, протекающих при постоянной температуре в случае конечного изменения Энергия Гельмгольца Это функция определяет направление и предел течения самопроизвольных процессов для систем, находящихся при постоянной температуре и постоянном объеме 19
 5. Энергия Гиббса Функция Гиббса определяет направление и предел течения самопроизвольных процессов для систем, находящихся при постоянной температуре и постоянном давлении Величина TS=U-F называется связанной энергией. Это часть внутренней энергии, которая не может быть превращена в работу в изотермических процессах. Величины F и G – свободная энергия, которая может быть превращена в работу. 20
5. Энергия Гиббса Функция Гиббса определяет направление и предел течения самопроизвольных процессов для систем, находящихся при постоянной температуре и постоянном давлении Величина TS=U-F называется связанной энергией. Это часть внутренней энергии, которая не может быть превращена в работу в изотермических процессах. Величины F и G – свободная энергия, которая может быть превращена в работу. 20
 Уравнения Гиббса - Гельмгольца Термодинамическая система, стремясь к равновесию, высвобождает часть внутренней энергии, передавая ее в окружающую среду в виде теплоты или работы. Эта составляющая называется свободной энергией. Свободная энергия является функцией состояния системы. Пусть в систему входит k компонентов, тогда 21
Уравнения Гиббса - Гельмгольца Термодинамическая система, стремясь к равновесию, высвобождает часть внутренней энергии, передавая ее в окружающую среду в виде теплоты или работы. Эта составляющая называется свободной энергией. Свободная энергия является функцией состояния системы. Пусть в систему входит k компонентов, тогда 21
 Рассмотрим частный случай, т. е. электрические, магнитные, гравитационные поля отсутствуют, внешняя поверхность не учитывается, система сохраняет постоянную массу. 22
Рассмотрим частный случай, т. е. электрические, магнитные, гравитационные поля отсутствуют, внешняя поверхность не учитывается, система сохраняет постоянную массу. 22
 В системах при постоянной температуре и постоянном объеме самопроизвольно могут протекать только процессы, которые сопровождаются уменьшением энергии Гельмгольца и условием равновесия служит достижение некоторого минимального для данных условий значения F. При постоянном давлении и температуре в системе самопроизвольно могут протекать только процессы, которые сопровождаются уменьшением энергии Гиббса и условием равновесия служит достижение некоторого минимального для данных условий значения G. Уравнения Гиббса-Гельмгольца 23
В системах при постоянной температуре и постоянном объеме самопроизвольно могут протекать только процессы, которые сопровождаются уменьшением энергии Гельмгольца и условием равновесия служит достижение некоторого минимального для данных условий значения F. При постоянном давлении и температуре в системе самопроизвольно могут протекать только процессы, которые сопровождаются уменьшением энергии Гиббса и условием равновесия служит достижение некоторого минимального для данных условий значения G. Уравнения Гиббса-Гельмгольца 23
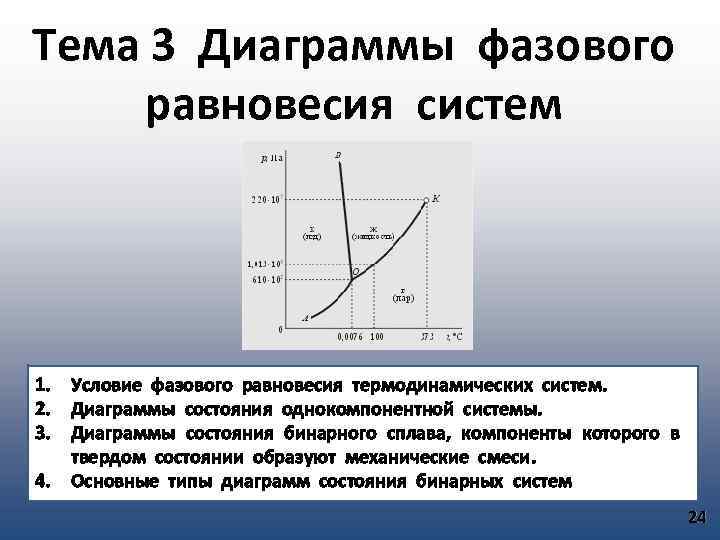 Тема 3 Диаграммы фазового равновесия систем 1. Условие фазового равновесия термодинамических систем. 2. Диаграммы состояния однокомпонентной системы. 3. Диаграммы состояния бинарного сплава, компоненты которого в твердом состоянии образуют механические смеси. 4. Основные типы диаграмм состояния бинарных систем 24
Тема 3 Диаграммы фазового равновесия систем 1. Условие фазового равновесия термодинамических систем. 2. Диаграммы состояния однокомпонентной системы. 3. Диаграммы состояния бинарного сплава, компоненты которого в твердом состоянии образуют механические смеси. 4. Основные типы диаграмм состояния бинарных систем 24
 Условие фазового равновесия термодинамической системы Фазовое равновесие – это равновесие в системах, в которых не происходит химического взаимодействия между компонентами, а происходят лишь фазовые переходы компонентов из одной фазы в другую Условия равновесия гетерогенной системы 1. Во всех фазах должна быть одинаковая температура 2. Во всех фазах должно быть одинаковое давление 3. Химические потенциалы каждого из компонентов равны μ – мольный химический потенциал i-го компонента при неизменном числе молей других компонентов и других параметров 25
Условие фазового равновесия термодинамической системы Фазовое равновесие – это равновесие в системах, в которых не происходит химического взаимодействия между компонентами, а происходят лишь фазовые переходы компонентов из одной фазы в другую Условия равновесия гетерогенной системы 1. Во всех фазах должна быть одинаковая температура 2. Во всех фазах должно быть одинаковое давление 3. Химические потенциалы каждого из компонентов равны μ – мольный химический потенциал i-го компонента при неизменном числе молей других компонентов и других параметров 25
 Одним из основных законов физической химии является закон равновесия фаз (правило фаз), относящееся к системам, находящимся в равновесии. Рассмотрим систему, содержащую n независимых компонентов и состоящую из k фаз (все n компонентов входят во все k фаз) Для выражения состава любой фазы, содержащей n компонентов, достаточно указать процентное содержание (n-1) компонентов. Для описания состава всех k фаз потребуется k(n-1) данных. Общее количество независимых переменных k(n-1)+2. 26
Одним из основных законов физической химии является закон равновесия фаз (правило фаз), относящееся к системам, находящимся в равновесии. Рассмотрим систему, содержащую n независимых компонентов и состоящую из k фаз (все n компонентов входят во все k фаз) Для выражения состава любой фазы, содержащей n компонентов, достаточно указать процентное содержание (n-1) компонентов. Для описания состава всех k фаз потребуется k(n-1) данных. Общее количество независимых переменных k(n-1)+2. 26
 Если число независимых переменных равно числу связывающих уравнений, то каждая переменная принимает свое, строго определенное значение, и вся система может существовать при этом в единственно возможном сочетании Р, Т, и С во всех фазах. Если число уравнений меньше числа независимых переменных, то появляются переменные, которым можно придавать произвольные значения и состояние при этом не нарушится. Правило фаз Гиббса Число степеней свободы равновесной термодинамической системы, на которую из внешних факторов влияют только температура и давление, равно числу независимых компонентов системы минус число фаз плюс 2 Число термодинамических степеней свободы (вариантность системы) - определяет число параметров, которые можно произвольно менять в некоторых пределах, не изменяя при этом числа или вида фаз системы. f=0 – система нонвариантна f=1– система моновариантна f=2 – система бивариантна 27
Если число независимых переменных равно числу связывающих уравнений, то каждая переменная принимает свое, строго определенное значение, и вся система может существовать при этом в единственно возможном сочетании Р, Т, и С во всех фазах. Если число уравнений меньше числа независимых переменных, то появляются переменные, которым можно придавать произвольные значения и состояние при этом не нарушится. Правило фаз Гиббса Число степеней свободы равновесной термодинамической системы, на которую из внешних факторов влияют только температура и давление, равно числу независимых компонентов системы минус число фаз плюс 2 Число термодинамических степеней свободы (вариантность системы) - определяет число параметров, которые можно произвольно менять в некоторых пределах, не изменяя при этом числа или вида фаз системы. f=0 – система нонвариантна f=1– система моновариантна f=2 – система бивариантна 27
 Диаграммы состояния однокомпонентной системы Фазы в однокомпонентной системе – это вещество в различных агрегатных состояниях. Вид уравнения состояния различных фаз в общем случае неизвестен, поэтому для нахождения зависимости между значениями параметров, определяющих состояние системы непосредственно изменяют параметры (Р, Т, С) или (Р, Т, V). Рассмотрим плоскую диаграмму однокомпонентной системы для переменных Т и Р. Каждая точка на плоскости диаграмм состояния отражает условия, при которых находится система. Фигуративные точки - точки, отражающие состояние и условия существования системы. 28
Диаграммы состояния однокомпонентной системы Фазы в однокомпонентной системе – это вещество в различных агрегатных состояниях. Вид уравнения состояния различных фаз в общем случае неизвестен, поэтому для нахождения зависимости между значениями параметров, определяющих состояние системы непосредственно изменяют параметры (Р, Т, С) или (Р, Т, V). Рассмотрим плоскую диаграмму однокомпонентной системы для переменных Т и Р. Каждая точка на плоскости диаграмм состояния отражает условия, при которых находится система. Фигуративные точки - точки, отражающие состояние и условия существования системы. 28
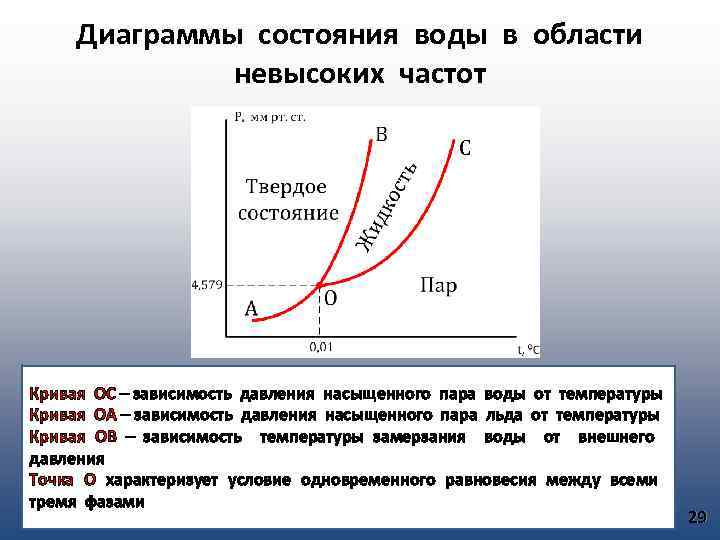 Диаграммы состояния воды в области невысоких частот Кривая ОС – зависимость давления насыщенного пара воды от температуры Кривая ОА – зависимость давления насыщенного пара льда от температуры Кривая ОВ – зависимость температуры замерзания воды от внешнего давления Точка О характеризует условие одновременного равновесия между всеми тремя фазами 29
Диаграммы состояния воды в области невысоких частот Кривая ОС – зависимость давления насыщенного пара воды от температуры Кривая ОА – зависимость давления насыщенного пара льда от температуры Кривая ОВ – зависимость температуры замерзания воды от внешнего давления Точка О характеризует условие одновременного равновесия между всеми тремя фазами 29
 Диаграммы состояния бинарного сплава, компоненты которого в твердом состоянии образуют механические смеси По числу независимых компонентов системы подразделяются на однокомпонентные, двухкомпонентные (бинарные или двойные), трехкомпонентные и т. д. В зависимости от характера взаимодействия компонентов в твердом состоянии различают Твердые растворы Механические смеси Химические соединения Для построения диаграмм состояния выполняют термический анализ, в ходе которого выделяют критические точки при нагревании и охлаждении, затем строят кривые охлаждения. По кривым охлаждения строят диаграммы фазового состояния 30
Диаграммы состояния бинарного сплава, компоненты которого в твердом состоянии образуют механические смеси По числу независимых компонентов системы подразделяются на однокомпонентные, двухкомпонентные (бинарные или двойные), трехкомпонентные и т. д. В зависимости от характера взаимодействия компонентов в твердом состоянии различают Твердые растворы Механические смеси Химические соединения Для построения диаграмм состояния выполняют термический анализ, в ходе которого выделяют критические точки при нагревании и охлаждении, затем строят кривые охлаждения. По кривым охлаждения строят диаграммы фазового состояния 30
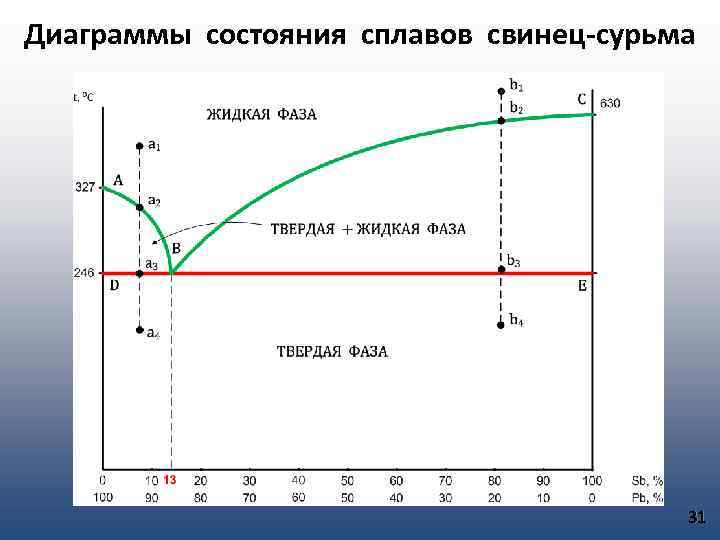 Диаграммы состояния сплавов свинец-сурьма 31
Диаграммы состояния сплавов свинец-сурьма 31
 1. По линии АВ начинается кристаллизация свинца. 2. В области диаграммы ABD находятся кристаллы свинца и расплав, состав которого около линии BD приближается к эвтектическому. 3. По линии BD затвердевает весь оставшийся раствор эвтектического состава. 4. Ниже линии BD находятся твердые сплавы, состоящие из кристаллов свинца и эвтектики. 5. По линии BC начинается выделение кристаллов сурьмы. 6. В области диаграммы ВСЕ находятся кристаллы сурьмы и жидкий раствор, состав которого по линии BE приближается к эвтектическому. 7. По линии ВЕ затвердевает весь оставшийся расплав эвтектического состава. 8. Ниже линии ВЕ сплавы находятся в твердом состоянии и состоят из кристаллов сурьмы и эвтектики. 9. Ниже точки В сплав (13% сурьмы и 87% свинца) находится в твердом состоянии и представляет собой эвтектику (механическая смесь мелких кристаллов сурьмы и свинца). 32
1. По линии АВ начинается кристаллизация свинца. 2. В области диаграммы ABD находятся кристаллы свинца и расплав, состав которого около линии BD приближается к эвтектическому. 3. По линии BD затвердевает весь оставшийся раствор эвтектического состава. 4. Ниже линии BD находятся твердые сплавы, состоящие из кристаллов свинца и эвтектики. 5. По линии BC начинается выделение кристаллов сурьмы. 6. В области диаграммы ВСЕ находятся кристаллы сурьмы и жидкий раствор, состав которого по линии BE приближается к эвтектическому. 7. По линии ВЕ затвердевает весь оставшийся расплав эвтектического состава. 8. Ниже линии ВЕ сплавы находятся в твердом состоянии и состоят из кристаллов сурьмы и эвтектики. 9. Ниже точки В сплав (13% сурьмы и 87% свинца) находится в твердом состоянии и представляет собой эвтектику (механическая смесь мелких кристаллов сурьмы и свинца). 32
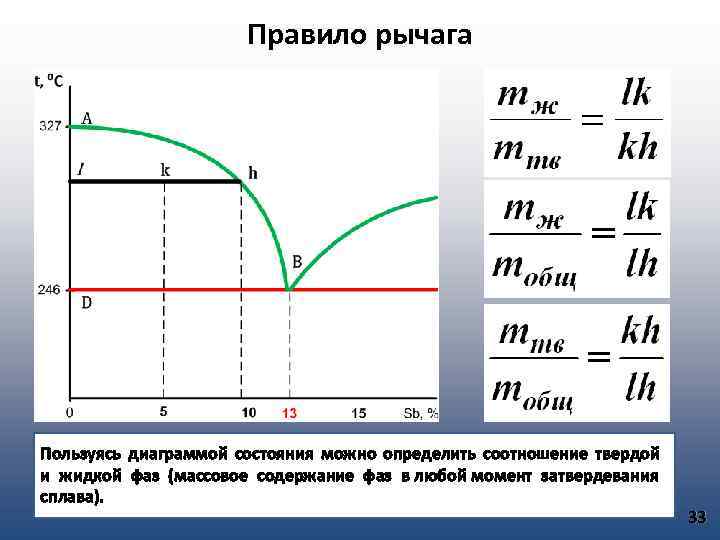 Правило рычага Пользуясь диаграммой состояния можно определить соотношение твердой и жидкой фаз (массовое содержание фаз в любой момент затвердевания сплава). 33
Правило рычага Пользуясь диаграммой состояния можно определить соотношение твердой и жидкой фаз (массовое содержание фаз в любой момент затвердевания сплава). 33
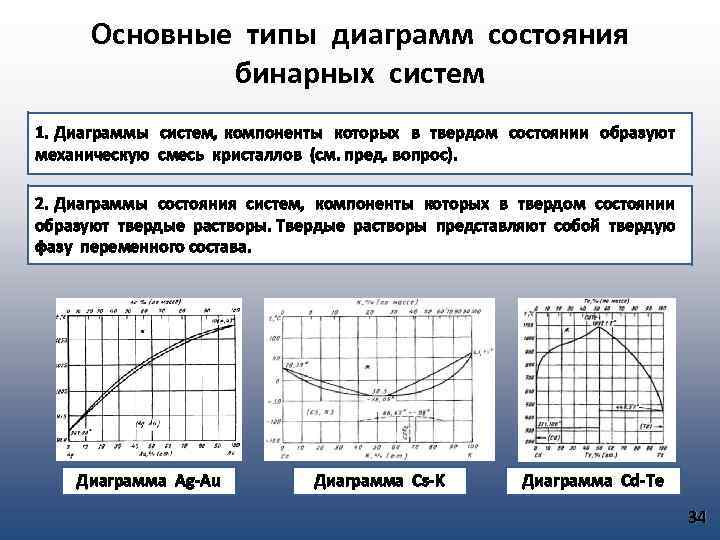 Основные типы диаграмм состояния бинарных систем 1. Диаграммы систем, компоненты которых в твердом состоянии образуют механическую смесь кристаллов (см. пред. вопрос). 2. Диаграммы состояния систем, компоненты которых в твердом состоянии образуют твердые растворы. Твердые растворы представляют собой твердую фазу переменного состава. Диаграмма Ag-Au Диаграмма Cs-K Диаграмма Cd-Te 34
Основные типы диаграмм состояния бинарных систем 1. Диаграммы систем, компоненты которых в твердом состоянии образуют механическую смесь кристаллов (см. пред. вопрос). 2. Диаграммы состояния систем, компоненты которых в твердом состоянии образуют твердые растворы. Твердые растворы представляют собой твердую фазу переменного состава. Диаграмма Ag-Au Диаграмма Cs-K Диаграмма Cd-Te 34
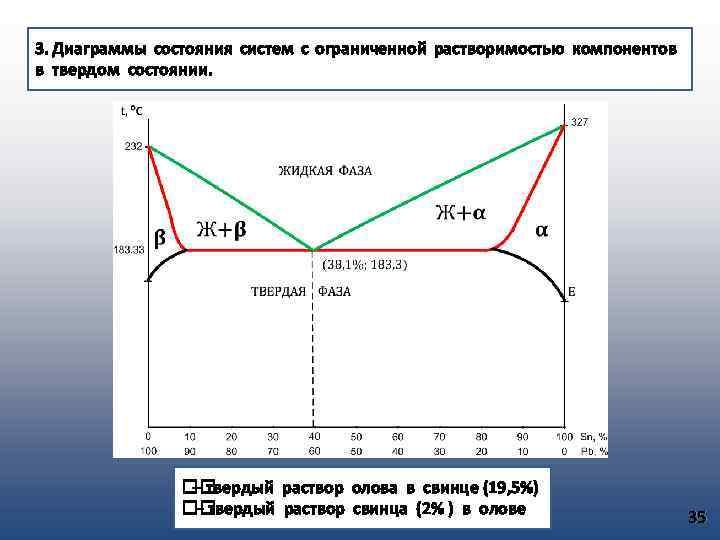 3. Диаграммы состояния систем с ограниченной растворимостью компонентов в твердом состоянии. – твердый раствор олова в свинце (19, 5%) – твердый раствор свинца (2% ) в олове 35
3. Диаграммы состояния систем с ограниченной растворимостью компонентов в твердом состоянии. – твердый раствор олова в свинце (19, 5%) – твердый раствор свинца (2% ) в олове 35
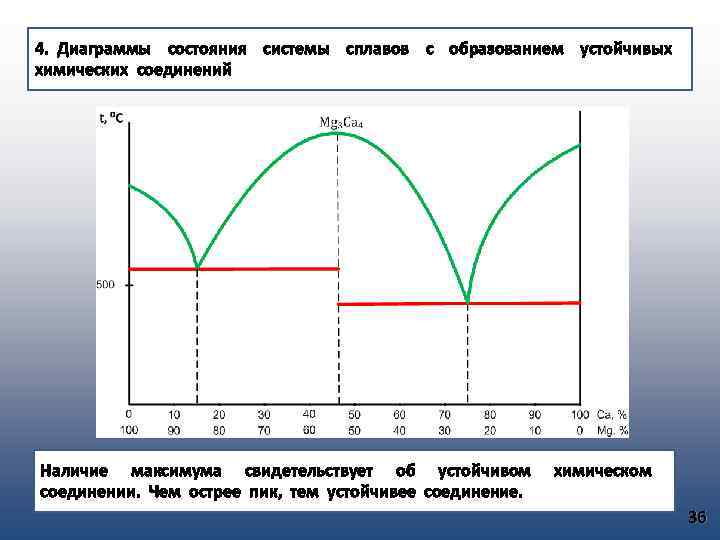 4. Диаграммы состояния системы сплавов с образованием устойчивых химических соединений Наличие максимума свидетельствует об устойчивом химическом соединении. Чем острее пик, тем устойчивее соединение. 36
4. Диаграммы состояния системы сплавов с образованием устойчивых химических соединений Наличие максимума свидетельствует об устойчивом химическом соединении. Чем острее пик, тем устойчивее соединение. 36
 Тема 4 Процессы на поверхности раздела двух фаз 1. Виды адсорбции. 2. Термодинамические параметры поверхности. 37
Тема 4 Процессы на поверхности раздела двух фаз 1. Виды адсорбции. 2. Термодинамические параметры поверхности. 37
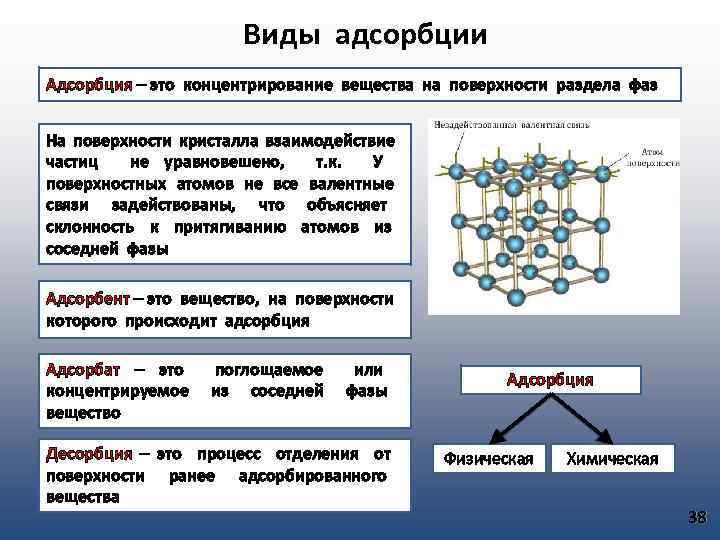 Виды адсорбции Адсорбция – это концентрирование вещества на поверхности раздела фаз На поверхности кристалла взаимодействие частиц не уравновешено, т. к. У поверхностных атомов не все валентные связи задействованы, что объясняет склонность к притягиванию атомов из соседней фазы Адсорбент – это вещество, на поверхности которого происходит адсорбция Адсорбат – это поглощаемое или концентрируемое из соседней фазы вещество Десорбция – это процесс отделения от поверхности ранее адсорбированного вещества Адсорбция Физическая Химическая 38
Виды адсорбции Адсорбция – это концентрирование вещества на поверхности раздела фаз На поверхности кристалла взаимодействие частиц не уравновешено, т. к. У поверхностных атомов не все валентные связи задействованы, что объясняет склонность к притягиванию атомов из соседней фазы Адсорбент – это вещество, на поверхности которого происходит адсорбция Адсорбат – это поглощаемое или концентрируемое из соседней фазы вещество Десорбция – это процесс отделения от поверхности ранее адсорбированного вещества Адсорбция Физическая Химическая 38
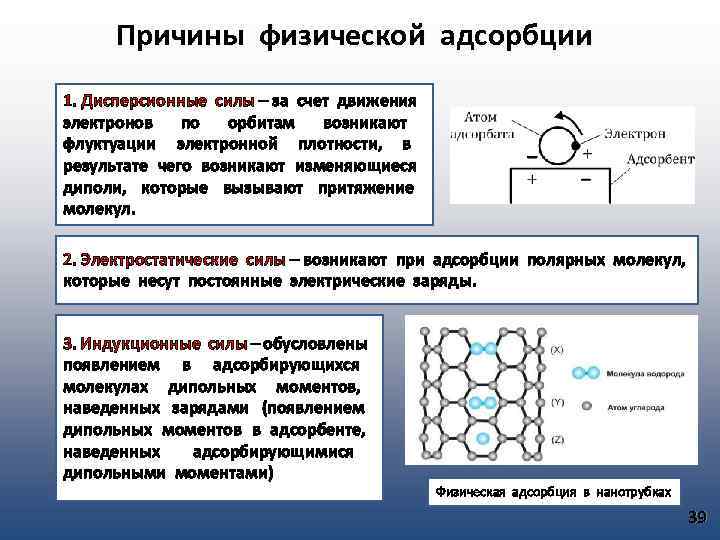 Причины физической адсорбции 1. Дисперсионные силы – за счет движения электронов по орбитам возникают флуктуации электронной плотности, в результате чего возникают изменяющиеся диполи, которые вызывают притяжение молекул. 2. Электростатические силы – возникают при адсорбции полярных молекул, которые несут постоянные электрические заряды. 3. Индукционные силы – обусловлены появлением в адсорбирующихся молекулах дипольных моментов, наведенных зарядами (появлением дипольных моментов в адсорбенте, наведенных адсорбирующимися дипольными моментами) Физическая адсорбция в нанотрубках 39
Причины физической адсорбции 1. Дисперсионные силы – за счет движения электронов по орбитам возникают флуктуации электронной плотности, в результате чего возникают изменяющиеся диполи, которые вызывают притяжение молекул. 2. Электростатические силы – возникают при адсорбции полярных молекул, которые несут постоянные электрические заряды. 3. Индукционные силы – обусловлены появлением в адсорбирующихся молекулах дипольных моментов, наведенных зарядами (появлением дипольных моментов в адсорбенте, наведенных адсорбирующимися дипольными моментами) Физическая адсорбция в нанотрубках 39
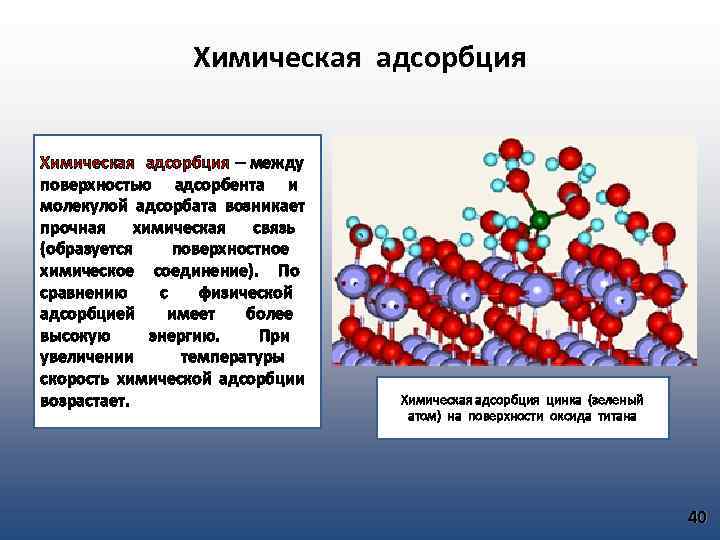 Химическая адсорбция – между поверхностью адсорбента и молекулой адсорбата возникает прочная химическая связь (образуется поверхностное химическое соединение). По сравнению с физической адсорбцией имеет более высокую энергию. При увеличении температуры скорость химической адсорбции возрастает. Химическая адсорбция цинка (зеленый атом) на поверхности оксида титана 40
Химическая адсорбция – между поверхностью адсорбента и молекулой адсорбата возникает прочная химическая связь (образуется поверхностное химическое соединение). По сравнению с физической адсорбцией имеет более высокую энергию. При увеличении температуры скорость химической адсорбции возрастает. Химическая адсорбция цинка (зеленый атом) на поверхности оксида титана 40
 Термодинамические параметры поверхности Термодинамические параметры определяются физической природой материала. Одним из параметров является полная поверхностная энергия. Часть этой энергии представляет собой работу, затрачиваемую на создание поверхности. Эта часть полной энергии называется поверхностной энергией Гиббса. Величина этой работы, отнесенная к единице площади поверхности, называется удельной поверхностной энергией Гиббса или поверхностным натяжением. Для жидких материалов поверхностное натяжение определяется экспериментально и приводится в справочниках. Для твердых материалов поверхностное натяжение рассчитывают по формуле 41
Термодинамические параметры поверхности Термодинамические параметры определяются физической природой материала. Одним из параметров является полная поверхностная энергия. Часть этой энергии представляет собой работу, затрачиваемую на создание поверхности. Эта часть полной энергии называется поверхностной энергией Гиббса. Величина этой работы, отнесенная к единице площади поверхности, называется удельной поверхностной энергией Гиббса или поверхностным натяжением. Для жидких материалов поверхностное натяжение определяется экспериментально и приводится в справочниках. Для твердых материалов поверхностное натяжение рассчитывают по формуле 41
 Поверхностная энергия Гиббса влияет на свободную энергию системы только в том случае, когда слагаемые, в которые входит поверхностное натяжение, соизмеримы с другими составляющими уравнения Значимость σ определяется следующим образом: Если площадью поверхности системы нельзя пренебречь по сравнению с объемом, то поверхностное натяжение необходимо учитывать. Мелкие капли дождя имеют круглую форму за счет превалирующих сил поверхностного натяжения (площадь поверхности соизмерима с объемом ) Крупные капли имеют вытянутую форму за счет влияния сил не только поверхностного натяжения, но и гравитационных (площадь поверхности менее соизмерима с объемом) 42
Поверхностная энергия Гиббса влияет на свободную энергию системы только в том случае, когда слагаемые, в которые входит поверхностное натяжение, соизмеримы с другими составляющими уравнения Значимость σ определяется следующим образом: Если площадью поверхности системы нельзя пренебречь по сравнению с объемом, то поверхностное натяжение необходимо учитывать. Мелкие капли дождя имеют круглую форму за счет превалирующих сил поверхностного натяжения (площадь поверхности соизмерима с объемом ) Крупные капли имеют вытянутую форму за счет влияния сил не только поверхностного натяжения, но и гравитационных (площадь поверхности менее соизмерима с объемом) 42
 При увеличении температуры происходит расширение тел и ослабление сил связи взаимного притяжения частиц как в объеме, так и на его поверхности, т. е. с увеличением температуры поверхностное натяжение ослабевает. Этот процесс можно описать уравнением Существует критическая температура, при которой поверхностное натяжение равно 0, т. е. при этом раздела фаз не существует. В конденсированном твердом и жидком состояниях вещество не может находится при температурах, меньших, чем критическая При постоянных температуре и давлении самопроизвольно протекают процессы, при которых энергия Гиббса уменьшается. Такие процессы сопровождаются самопроизвольным уменьшением поверхности раздела фаз. 43
При увеличении температуры происходит расширение тел и ослабление сил связи взаимного притяжения частиц как в объеме, так и на его поверхности, т. е. с увеличением температуры поверхностное натяжение ослабевает. Этот процесс можно описать уравнением Существует критическая температура, при которой поверхностное натяжение равно 0, т. е. при этом раздела фаз не существует. В конденсированном твердом и жидком состояниях вещество не может находится при температурах, меньших, чем критическая При постоянных температуре и давлении самопроизвольно протекают процессы, при которых энергия Гиббса уменьшается. Такие процессы сопровождаются самопроизвольным уменьшением поверхности раздела фаз. 43
 Тема 5 Растворы и их применение в технологии ЭС 1. Виды растворов. 2. Жидкие растворы. Диаграмма «состав-температура кипения» двойных смесей. Азеотропные растворы. Дистилляция двойных смесей 44
Тема 5 Растворы и их применение в технологии ЭС 1. Виды растворов. 2. Жидкие растворы. Диаграмма «состав-температура кипения» двойных смесей. Азеотропные растворы. Дистилляция двойных смесей 44
 Виды растворов Растворы - это системы, в которых одно вещество равномерно распределено в среде другого или других веществ Компоненты раствора - это простейшие составляющие части раствора, которые могут быть выделены в чистом виде и смешением которых можно получить растворы любого состава этой системы. Деление на растворитель и растворенное вещество Деление чисто условное. Обычно, компонент, которого в смеси больше – растворитель, остальные – растворенные вещества. Если один компонент жидкость, а остальные – твердые вещества или газы, то жидкость является растворителем. 45
Виды растворов Растворы - это системы, в которых одно вещество равномерно распределено в среде другого или других веществ Компоненты раствора - это простейшие составляющие части раствора, которые могут быть выделены в чистом виде и смешением которых можно получить растворы любого состава этой системы. Деление на растворитель и растворенное вещество Деление чисто условное. Обычно, компонент, которого в смеси больше – растворитель, остальные – растворенные вещества. Если один компонент жидкость, а остальные – твердые вещества или газы, то жидкость является растворителем. 45
 Растворы Электролиты Неэлектролиты Металлические расплавы Обладают высокой электропроводностью, диэлектрической проницаемостью. Молекулы компонентов полярны. Свойственна электролитическая диссоциация молекул на ионы. К ним относятся растворы солей, кислот, щелочей, а также расплавы солей Обладают низкой электропроводностью, теплопроводностью, низкой теплоемкостью. Молекулы компонентов нейтральны либо слабо полярны. К ним относится большинство растворов углеводородов Обладают высокой электропроводностью, теплопроводностью. Отсутствует электролитическая диссоциация. Растворы Газообразные (смеси) Жидкие Твердые 46
Растворы Электролиты Неэлектролиты Металлические расплавы Обладают высокой электропроводностью, диэлектрической проницаемостью. Молекулы компонентов полярны. Свойственна электролитическая диссоциация молекул на ионы. К ним относятся растворы солей, кислот, щелочей, а также расплавы солей Обладают низкой электропроводностью, теплопроводностью, низкой теплоемкостью. Молекулы компонентов нейтральны либо слабо полярны. К ним относится большинство растворов углеводородов Обладают высокой электропроводностью, теплопроводностью. Отсутствует электролитическая диссоциация. Растворы Газообразные (смеси) Жидкие Твердые 46
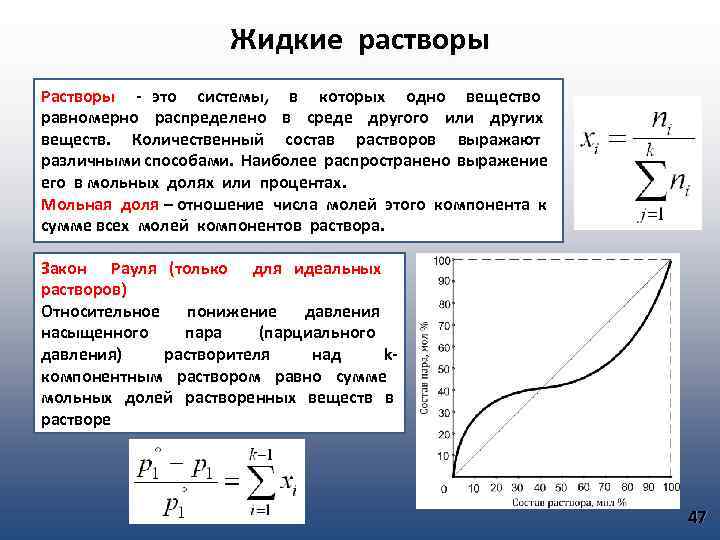 Жидкие растворы Растворы - это системы, в которых одно вещество равномерно распределено в среде другого или других веществ. Количественный состав растворов выражают различными способами. Наиболее распространено выражение его в мольных долях или процентах. Мольная доля – отношение числа молей этого компонента к сумме всех молей компонентов раствора. Закон Рауля (только для идеальных растворов) Относительное понижение давления насыщенного пара (парциального давления) растворителя над kкомпонентным раствором равно сумме мольных долей растворенных веществ в растворе 47
Жидкие растворы Растворы - это системы, в которых одно вещество равномерно распределено в среде другого или других веществ. Количественный состав растворов выражают различными способами. Наиболее распространено выражение его в мольных долях или процентах. Мольная доля – отношение числа молей этого компонента к сумме всех молей компонентов раствора. Закон Рауля (только для идеальных растворов) Относительное понижение давления насыщенного пара (парциального давления) растворителя над kкомпонентным раствором равно сумме мольных долей растворенных веществ в растворе 47
 Закон Генри Парциальное давление пара растворенного вещества пропорционально его мольной доле. Закон Рауля - Генри В идеальном растворе при малых давлениях насыщенного пара парциальное пара растворенного вещества равно Первый закон Коновалова 1. Повышение относительного содержания одного компонента в жидкой фазе всегда вызывает увеличение относительного содержания его и в парах 2. В двойной системе пар, по сравнению с находящейся с ним в равновесии жидкостью, относительно богаче тем из компонентов, прибавление которого к системе повышает общее давление пара, т. е. понижает температуру кипения смеси при данном давлении. Второй закон Коновалова Точки максимума и минимума на кривой общего давления пара (или температур кипения) отвечает растворам, состав которых одинаков с составом равновесного с ними пара. 48
Закон Генри Парциальное давление пара растворенного вещества пропорционально его мольной доле. Закон Рауля - Генри В идеальном растворе при малых давлениях насыщенного пара парциальное пара растворенного вещества равно Первый закон Коновалова 1. Повышение относительного содержания одного компонента в жидкой фазе всегда вызывает увеличение относительного содержания его и в парах 2. В двойной системе пар, по сравнению с находящейся с ним в равновесии жидкостью, относительно богаче тем из компонентов, прибавление которого к системе повышает общее давление пара, т. е. понижает температуру кипения смеси при данном давлении. Второй закон Коновалова Точки максимума и минимума на кривой общего давления пара (или температур кипения) отвечает растворам, состав которых одинаков с составом равновесного с ними пара. 48
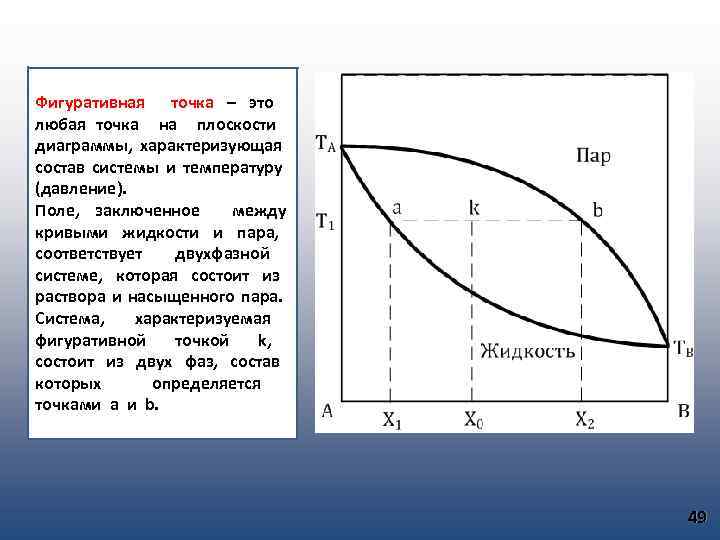 Фигуративная точка – это любая точка на плоскости диаграммы, характеризующая состав системы и температуру (давление). Поле, заключенное между кривыми жидкости и пара, соответствует двухфазной системе, которая состоит из раствора и насыщенного пара. Система, характеризуемая фигуративной точкой k, состоит из двух фаз, состав которых определяется точками a и b. 49
Фигуративная точка – это любая точка на плоскости диаграммы, характеризующая состав системы и температуру (давление). Поле, заключенное между кривыми жидкости и пара, соответствует двухфазной системе, которая состоит из раствора и насыщенного пара. Система, характеризуемая фигуративной точкой k, состоит из двух фаз, состав которых определяется точками a и b. 49
 Дистилляция - это процесс разделения раствора на те или иные части путем перегонки. В системе типа I любую двойную смесь можно разделить путем дистилляции на чистые компоненты. В системах типа II или III осуществить разделение раствора на чистые компоненты путем дистилляции невозможно. 50
Дистилляция - это процесс разделения раствора на те или иные части путем перегонки. В системе типа I любую двойную смесь можно разделить путем дистилляции на чистые компоненты. В системах типа II или III осуществить разделение раствора на чистые компоненты путем дистилляции невозможно. 50
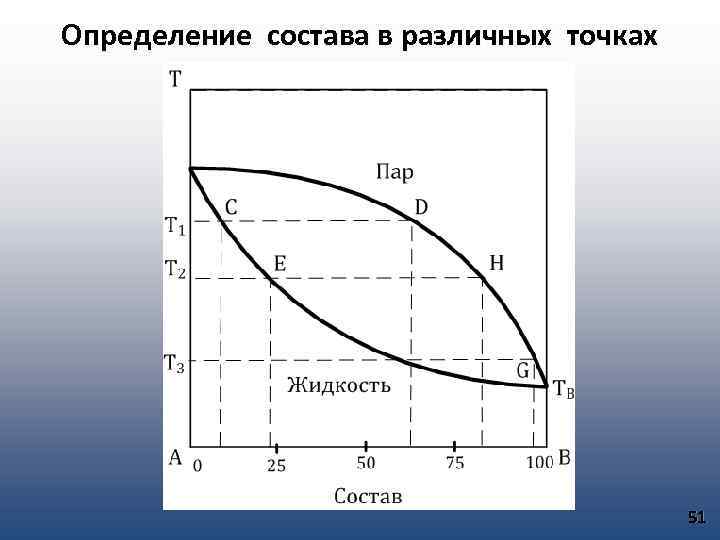 Определение состава в различных точках 51
Определение состава в различных точках 51
 Тема 6 Жидкие кристаллы 1. Структура жидкости. 2. Структура жидких кристаллов. 52
Тема 6 Жидкие кристаллы 1. Структура жидкости. 2. Структура жидких кристаллов. 52
 Структура жидкости В газах расстояние между частицами довольно большие, частицы свободны, взаимодействие между ними сводиться только к случайным столкновениям. В жидкостях расстояние между частицами уменьшается, сила взаимодействия между ними растут, каждая частица располагается в некотором окружении соседних частиц и совершает хаотические колебания около временного положения равновесия. Число возможных переходов частицы из одного равновесного состояния в другое в единицу времени можно определить как: τ0– период колебания частицы в жидкости около временного положения равновесия. U – высота потенциального барьера. 1 – Молекулы водяного пара; 2 – Молекулы воды. 53
Структура жидкости В газах расстояние между частицами довольно большие, частицы свободны, взаимодействие между ними сводиться только к случайным столкновениям. В жидкостях расстояние между частицами уменьшается, сила взаимодействия между ними растут, каждая частица располагается в некотором окружении соседних частиц и совершает хаотические колебания около временного положения равновесия. Число возможных переходов частицы из одного равновесного состояния в другое в единицу времени можно определить как: τ0– период колебания частицы в жидкости около временного положения равновесия. U – высота потенциального барьера. 1 – Молекулы водяного пара; 2 – Молекулы воды. 53
 Структура жидких кристаллов Жидкие кристаллы – органические вещества, молекул которых имеют удлиненную форму. При нагревании они переходят в жидкую фазу через мезофазу. Первоткрыватель – Рейнитцер 1888 г В состоянии мезофазы жидким кристаллам присущи следующие особенности: молекулы определенным образом ориентируются, т. е. образуют одномерную структуру. Поэтому жидкие кристаллы обладают свойствами жидкости (текучесть) и кристаллов (ориентационный порядок). Ориентация молекул приводит к анизотропии диэлектрических , магнитных, оптических свойств. Структура жидких кристаллов 54
Структура жидких кристаллов Жидкие кристаллы – органические вещества, молекул которых имеют удлиненную форму. При нагревании они переходят в жидкую фазу через мезофазу. Первоткрыватель – Рейнитцер 1888 г В состоянии мезофазы жидким кристаллам присущи следующие особенности: молекулы определенным образом ориентируются, т. е. образуют одномерную структуру. Поэтому жидкие кристаллы обладают свойствами жидкости (текучесть) и кристаллов (ориентационный порядок). Ориентация молекул приводит к анизотропии диэлектрических , магнитных, оптических свойств. Структура жидких кристаллов 54
 Основные разновидности жидких кристаллов Нематические Смектические Холестерические В нематических жидких кристаллах молекулы ориентированы в одном направлении, но центры их располагаются хаотично, поэтому слои молекул не образуются. В смектических жидких кристаллах молекулы располагаются параллельно их длинным осям и образуют в жидкости чередующиеся слои, толщиной в одну молекулу В холестерических жидких кристаллах молекулы группируются в слои, причем оси молекул лежат в плоскости этих слоев. Внутри каждой плоскости ориентация всех молекул одинакова, а направление этой ориентации постепенно изменяется от слоя к слою, поворачиваясь на некоторый угол. 55
Основные разновидности жидких кристаллов Нематические Смектические Холестерические В нематических жидких кристаллах молекулы ориентированы в одном направлении, но центры их располагаются хаотично, поэтому слои молекул не образуются. В смектических жидких кристаллах молекулы располагаются параллельно их длинным осям и образуют в жидкости чередующиеся слои, толщиной в одну молекулу В холестерических жидких кристаллах молекулы группируются в слои, причем оси молекул лежат в плоскости этих слоев. Внутри каждой плоскости ориентация всех молекул одинакова, а направление этой ориентации постепенно изменяется от слоя к слою, поворачиваясь на некоторый угол. 55
 Тема 7 Строение кристаллов 1. Равновесное состояние кристаллической решетки. 2. Основные типы кристаллических решеток. 3. Дефекты структуры. 56
Тема 7 Строение кристаллов 1. Равновесное состояние кристаллической решетки. 2. Основные типы кристаллических решеток. 3. Дефекты структуры. 56
 Равновесное состояние кристаллической решетки Между атомами действуют силы химической связи, которые притягивают атом. Они уравновешиваются силами отталкивания. И силы притяжения и силы отталкивания зависят от расстояния. Силы притяжения – дальнодействующие. Они возрастают сравнительно медленно с уменьшением расстояния между атомами. Сила отталкивания очень резко возрастают при уменьшении расстояния (короткодействующие). - b и m постоянные, зависящие от типа химической связи. - C и n постоянные, зависящие от природы атомов. При определенном расстоянии r 0 Fпр=Fот и в результате атомы оказываются в равновесном состоянии. Равновесному состоянию атомов (Fрез=0) соответствует минимальное отрицательное значение потенциальной энергии => равновесное состояние является устойчивым; при всяком малом отклонении атомы возвращаются в исходное состояние. 57
Равновесное состояние кристаллической решетки Между атомами действуют силы химической связи, которые притягивают атом. Они уравновешиваются силами отталкивания. И силы притяжения и силы отталкивания зависят от расстояния. Силы притяжения – дальнодействующие. Они возрастают сравнительно медленно с уменьшением расстояния между атомами. Сила отталкивания очень резко возрастают при уменьшении расстояния (короткодействующие). - b и m постоянные, зависящие от типа химической связи. - C и n постоянные, зависящие от природы атомов. При определенном расстоянии r 0 Fпр=Fот и в результате атомы оказываются в равновесном состоянии. Равновесному состоянию атомов (Fрез=0) соответствует минимальное отрицательное значение потенциальной энергии => равновесное состояние является устойчивым; при всяком малом отклонении атомы возвращаются в исходное состояние. 57
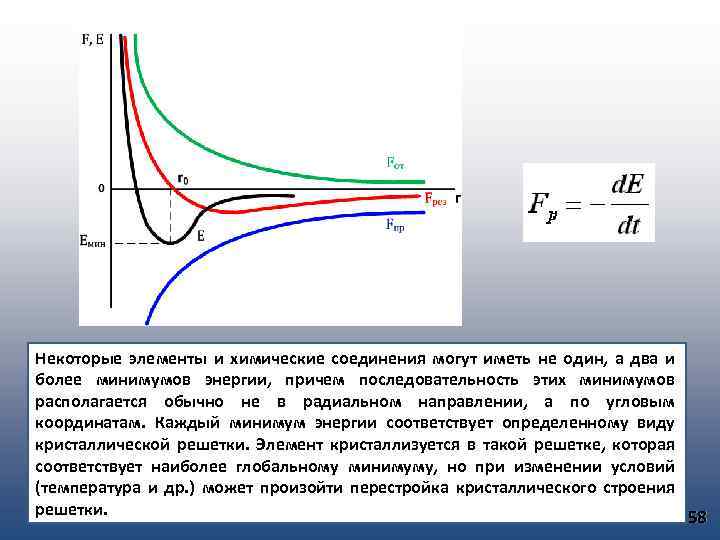 Некоторые элементы и химические соединения могут иметь не один, а два и более минимумов энергии, причем последовательность этих минимумов располагается обычно не в радиальном направлении, а по угловым координатам. Каждый минимум энергии соответствует определенному виду кристаллической решетки. Элемент кристаллизуется в такой решетке, которая соответствует наиболее глобальному минимуму, но при изменении условий (температура и др. ) может произойти перестройка кристаллического строения решетки. 58
Некоторые элементы и химические соединения могут иметь не один, а два и более минимумов энергии, причем последовательность этих минимумов располагается обычно не в радиальном направлении, а по угловым координатам. Каждый минимум энергии соответствует определенному виду кристаллической решетки. Элемент кристаллизуется в такой решетке, которая соответствует наиболее глобальному минимуму, но при изменении условий (температура и др. ) может произойти перестройка кристаллического строения решетки. 58
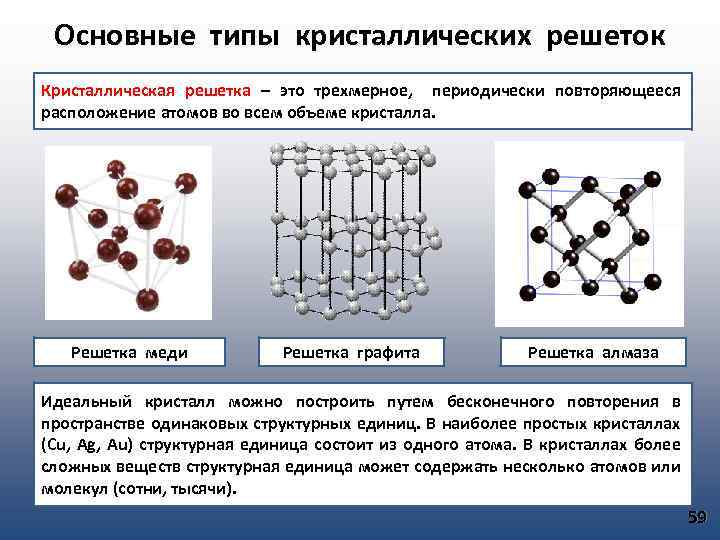 Основные типы кристаллических решеток Кристаллическая решетка – это трехмерное, периодически повторяющееся расположение атомов во всем объеме кристалла. Решетка меди Решетка графита Решетка алмаза Идеальный кристалл можно построить путем бесконечного повторения в пространстве одинаковых структурных единиц. В наиболее простых кристаллах (Cu, Ag, Au) структурная единица состоит из одного атома. В кристаллах более сложных веществ структурная единица может содержать несколько атомов или молекул (сотни, тысячи). 59
Основные типы кристаллических решеток Кристаллическая решетка – это трехмерное, периодически повторяющееся расположение атомов во всем объеме кристалла. Решетка меди Решетка графита Решетка алмаза Идеальный кристалл можно построить путем бесконечного повторения в пространстве одинаковых структурных единиц. В наиболее простых кристаллах (Cu, Ag, Au) структурная единица состоит из одного атома. В кристаллах более сложных веществ структурная единица может содержать несколько атомов или молекул (сотни, тысячи). 59
 Трансляционные решетки Наименьший объем кристаллического вещества, перемещением которого вдоль трех независимых направлений можно получить весь кристалл называется элементарной ячейкой. Количество атомов, приходящихся на одну элементарную ячейку называется базисом. Элементарная ячейка характеризуется набором шести параметров - базисными векторами. Посредством операции трансляции с помощью элементарной ячейки можно заполнить весь объем кристаллического вещества – трансляционные решетки (Бравэ, 1848 г) Сингония – (“сходноугольность”) кристаллическая система, объединяющая кристаллы с одинаковыми углами между базисными векторами и относительными величинами длин базисных векторов. В некоторых кристаллических решетках атомы могут располагаться в центре элементарных ячеек и граней. 60
Трансляционные решетки Наименьший объем кристаллического вещества, перемещением которого вдоль трех независимых направлений можно получить весь кристалл называется элементарной ячейкой. Количество атомов, приходящихся на одну элементарную ячейку называется базисом. Элементарная ячейка характеризуется набором шести параметров - базисными векторами. Посредством операции трансляции с помощью элементарной ячейки можно заполнить весь объем кристаллического вещества – трансляционные решетки (Бравэ, 1848 г) Сингония – (“сходноугольность”) кристаллическая система, объединяющая кристаллы с одинаковыми углами между базисными векторами и относительными величинами длин базисных векторов. В некоторых кристаллических решетках атомы могут располагаться в центре элементарных ячеек и граней. 60
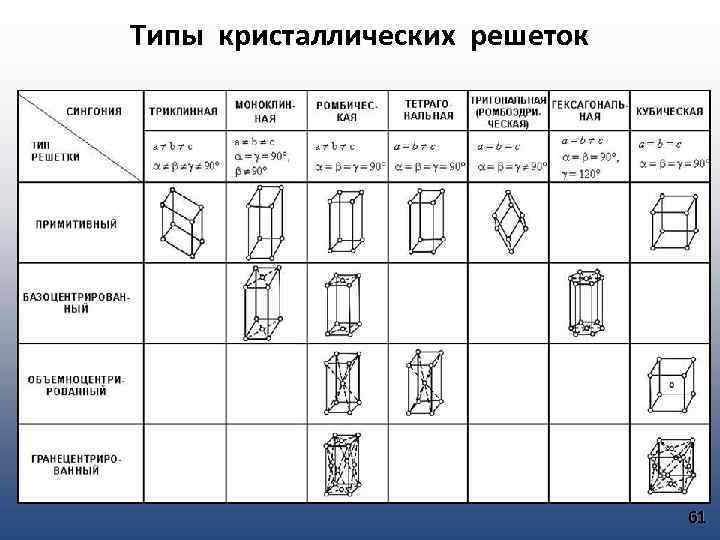 Типы кристаллических решеток 61
Типы кристаллических решеток 61
 Координаты узла выражаются через длины базисных векторов. Запись производится в двойных квадратных скобках. Для задания направления в решетке достаточно указать координаты любого атома, лежащего на прямой, проходящей через начало координат. Координаты направления записывают в одинарных квадратных скобках. Для задания кристаллографической плоскости удобно использовать длины отрезков, отсекаемых ею по осям координат. Для записи используют индексы Миллера (в круглых скобках). Получают индексы следующим способом: 62
Координаты узла выражаются через длины базисных векторов. Запись производится в двойных квадратных скобках. Для задания направления в решетке достаточно указать координаты любого атома, лежащего на прямой, проходящей через начало координат. Координаты направления записывают в одинарных квадратных скобках. Для задания кристаллографической плоскости удобно использовать длины отрезков, отсекаемых ею по осям координат. Для записи используют индексы Миллера (в круглых скобках). Получают индексы следующим способом: 62
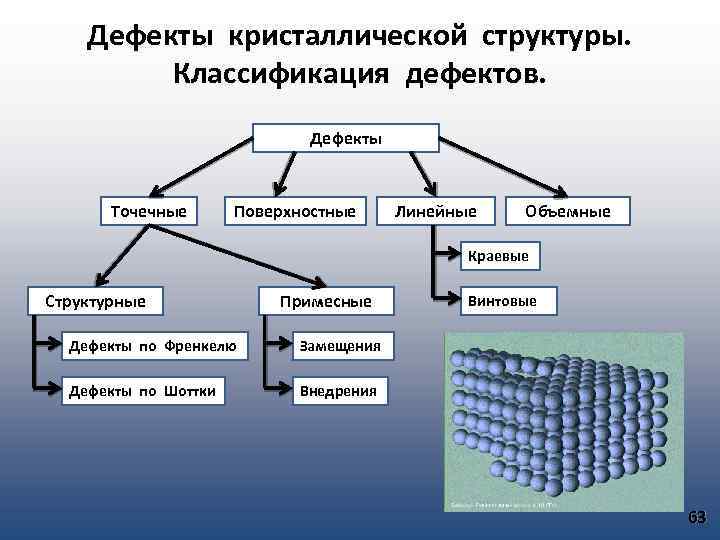 Дефекты кристаллической структуры. Классификация дефектов. Дефекты Точечные Поверхностные Линейные Объемные Краевые Структурные Примесные Дефекты по Френкелю Замещения Дефекты по Шоттки Винтовые Внедрения 63
Дефекты кристаллической структуры. Классификация дефектов. Дефекты Точечные Поверхностные Линейные Объемные Краевые Структурные Примесные Дефекты по Френкелю Замещения Дефекты по Шоттки Винтовые Внедрения 63
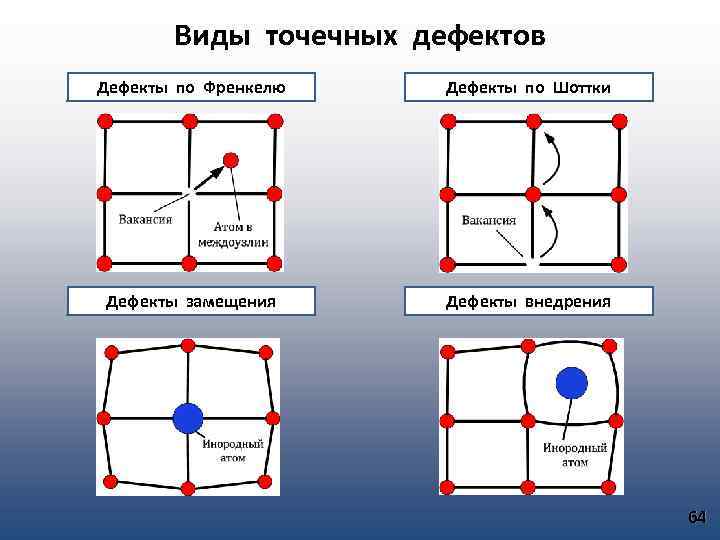 Виды точечных дефектов Дефекты по Френкелю Дефекты по Шоттки Дефекты замещения Дефекты внедрения 64
Виды точечных дефектов Дефекты по Френкелю Дефекты по Шоттки Дефекты замещения Дефекты внедрения 64
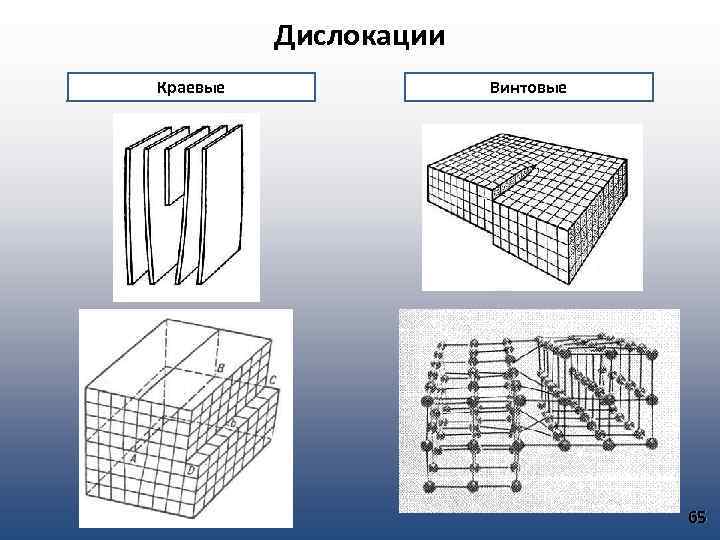 Дислокации Краевые Винтовые 65
Дислокации Краевые Винтовые 65
 Тема 8 Физико-химические основы термического вакуумного напыления тонких пленок 1. Процесс испарения веществ. 2. Создание направленного потока пара вещества. 3. Конденсация пара на подложке и рост пленки. 66
Тема 8 Физико-химические основы термического вакуумного напыления тонких пленок 1. Процесс испарения веществ. 2. Создание направленного потока пара вещества. 3. Конденсация пара на подложке и рост пленки. 66
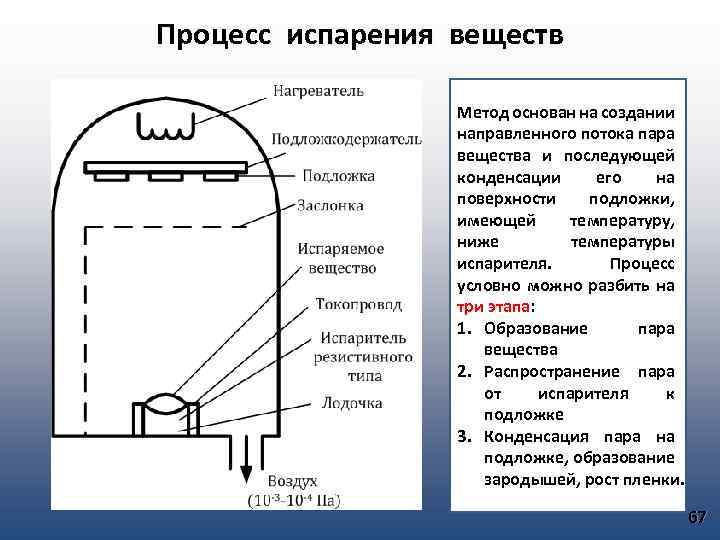 Процесс испарения веществ Метод основан на создании направленного потока пара вещества и последующей конденсации его на поверхности подложки, имеющей температуру, ниже температуры испарителя. Процесс условно можно разбить на три этапа: 1. Образование пара вещества 2. Распространение пара от испарителя к подложке 3. Конденсация пара на подложке, образование зародышей, рост пленки. 67
Процесс испарения веществ Метод основан на создании направленного потока пара вещества и последующей конденсации его на поверхности подложки, имеющей температуру, ниже температуры испарителя. Процесс условно можно разбить на три этапа: 1. Образование пара вещества 2. Распространение пара от испарителя к подложке 3. Конденсация пара на подложке, образование зародышей, рост пленки. 67
 Движущей силой любого процесса является величина свободной энергии, которую нельзя получить из системы, находящейся в равновесии. Движущей силой процесса переноса вещества при испарении и конденсации является различие в давлении насыщенных паров вещества над источником испарения и над подложкой. Чтобы вещество испарялось, необходимо чтобы молекулы имели энергию для преодоления сил межатомных связей. При испарении имеются молекулы, которые возвращаются. Число молекул, покидающих поверхность величивается, у при этом число возвращающихся молекул увеличивается. Термодинамическое равновесие Некоторые вещества достаточно интенсивно испаряются из твердой фазы. Такой процесс называют возгонкой (сублимацией) – Cd, Cr. Наиболее благоприятные условия для испарения, когда давление насыщенного пара не более 1 мм рт. ст. 68
Движущей силой любого процесса является величина свободной энергии, которую нельзя получить из системы, находящейся в равновесии. Движущей силой процесса переноса вещества при испарении и конденсации является различие в давлении насыщенных паров вещества над источником испарения и над подложкой. Чтобы вещество испарялось, необходимо чтобы молекулы имели энергию для преодоления сил межатомных связей. При испарении имеются молекулы, которые возвращаются. Число молекул, покидающих поверхность величивается, у при этом число возвращающихся молекул увеличивается. Термодинамическое равновесие Некоторые вещества достаточно интенсивно испаряются из твердой фазы. Такой процесс называют возгонкой (сублимацией) – Cd, Cr. Наиболее благоприятные условия для испарения, когда давление насыщенного пара не более 1 мм рт. ст. 68
 Создание направленного потока пара вещества к подложкам Для получения приемлемых скоростей роста пленки необходимо создать условия движения молекул вещества преимущественно по направлению к подложке. Это создается за счет: 1. Создания глубокого вакуума и исключение столкновений молекул вещества с молекулами остаточного газа. 2. Соответствующего формирования поверхности вещества, излучающего молекулы. Для исключения столкновений молекул вещества с молекулами воздуха необходимо, чтобы длина свободного пробега была не меньше расстояния от испарителя до подложки. 69
Создание направленного потока пара вещества к подложкам Для получения приемлемых скоростей роста пленки необходимо создать условия движения молекул вещества преимущественно по направлению к подложке. Это создается за счет: 1. Создания глубокого вакуума и исключение столкновений молекул вещества с молекулами остаточного газа. 2. Соответствующего формирования поверхности вещества, излучающего молекулы. Для исключения столкновений молекул вещества с молекулами воздуха необходимо, чтобы длина свободного пробега была не меньше расстояния от испарителя до подложки. 69
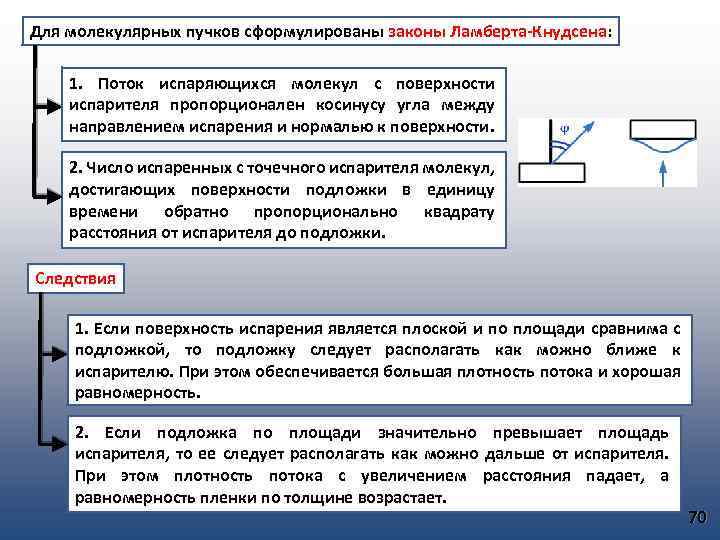 Для молекулярных пучков сформулированы законы Ламберта-Кнудсена: 1. Поток испаряющихся молекул с поверхности испарителя пропорционален косинусу угла между направлением испарения и нормалью к поверхности. 2. Число испаренных с точечного испарителя молекул, достигающих поверхности подложки в единицу времени обратно пропорционально квадрату расстояния от испарителя до подложки. Следствия 1. Если поверхность испарения является плоской и по площади сравнима с подложкой, то подложку следует располагать как можно ближе к испарителю. При этом обеспечивается большая плотность потока и хорошая равномерность. 2. Если подложка по площади значительно превышает площадь испарителя, то ее следует располагать как можно дальше от испарителя. При этом плотность потока с увеличением расстояния падает, а равномерность пленки по толщине возрастает. 70
Для молекулярных пучков сформулированы законы Ламберта-Кнудсена: 1. Поток испаряющихся молекул с поверхности испарителя пропорционален косинусу угла между направлением испарения и нормалью к поверхности. 2. Число испаренных с точечного испарителя молекул, достигающих поверхности подложки в единицу времени обратно пропорционально квадрату расстояния от испарителя до подложки. Следствия 1. Если поверхность испарения является плоской и по площади сравнима с подложкой, то подложку следует располагать как можно ближе к испарителю. При этом обеспечивается большая плотность потока и хорошая равномерность. 2. Если подложка по площади значительно превышает площадь испарителя, то ее следует располагать как можно дальше от испарителя. При этом плотность потока с увеличением расстояния падает, а равномерность пленки по толщине возрастает. 70
 Конденсация пара на подложке и рост пленки Молекула обладая энергией к. Т сталкивается с подложкой и отдает ей свою энергию, но при этом молекула может сохранить часть энергии и способна мигрировать по поверхности подложки, постепенно теряя свой избыток энергии стремясь к тепловому равновесию с подложкой. 1. В процессе миграции молекула может встретить на своем пути потенциальную яму (сильная связь с подложкой). Молекула теряет избыток энергии и фиксируется на подложке, становясь центром кристаллизации. 2. Встретив на своем пути потенциальный бугор, т. е. слабую связь с подложкой, и обладая достаточным избытком энергии, молекула покидает подложку (вторичное испарение, десорбция). 3. Мигрируя по подложке, молекула может встретить другую мигрирующую молекулу или группу молекул. Эта молекула может присоединиться к ним. При этом эта группа может потерять подвижность и зафиксироваться на подложке. Эта группа становится центром кристаллизации. 71
Конденсация пара на подложке и рост пленки Молекула обладая энергией к. Т сталкивается с подложкой и отдает ей свою энергию, но при этом молекула может сохранить часть энергии и способна мигрировать по поверхности подложки, постепенно теряя свой избыток энергии стремясь к тепловому равновесию с подложкой. 1. В процессе миграции молекула может встретить на своем пути потенциальную яму (сильная связь с подложкой). Молекула теряет избыток энергии и фиксируется на подложке, становясь центром кристаллизации. 2. Встретив на своем пути потенциальный бугор, т. е. слабую связь с подложкой, и обладая достаточным избытком энергии, молекула покидает подложку (вторичное испарение, десорбция). 3. Мигрируя по подложке, молекула может встретить другую мигрирующую молекулу или группу молекул. Эта молекула может присоединиться к ним. При этом эта группа может потерять подвижность и зафиксироваться на подложке. Эта группа становится центром кристаллизации. 71
 Основные преимущества вакуумного напыления Чистота получаемой пленки Удобство контроля толщины пленки Наличие высокопроизводительного оборудования Основные недостатки вакуумного напыления Возможное изменение состава сложных сплавов и соединение при испарении (сформированный режим испарения, метод микродозирования) Трудность испарения тугоплавких материалов Высокая инерционность процесса при использовании резистивных испарителей Неравномерность толщины пленки при испарении из точечного испарителя Сравнительно невысокая прочность сцепления пленки с подложкой 72
Основные преимущества вакуумного напыления Чистота получаемой пленки Удобство контроля толщины пленки Наличие высокопроизводительного оборудования Основные недостатки вакуумного напыления Возможное изменение состава сложных сплавов и соединение при испарении (сформированный режим испарения, метод микродозирования) Трудность испарения тугоплавких материалов Высокая инерционность процесса при использовании резистивных испарителей Неравномерность толщины пленки при испарении из точечного испарителя Сравнительно невысокая прочность сцепления пленки с подложкой 72
 Тема 9 Физико-химические основы ионного распыления 1. Катодное распыление. 2. Ионно-плазменное распыление. 3. Магнетронное распыление. 73
Тема 9 Физико-химические основы ионного распыления 1. Катодное распыление. 2. Ионно-плазменное распыление. 3. Магнетронное распыление. 73
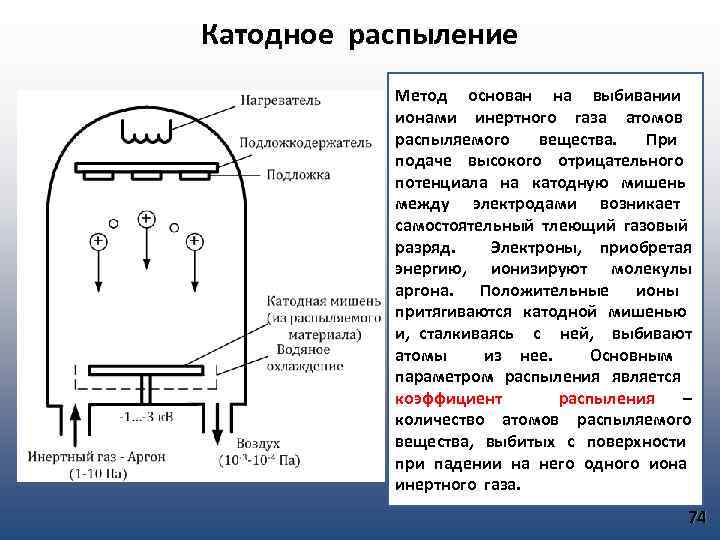 Катодное распыление Метод основан на выбивании ионами инертного газа атомов распыляемого вещества. При подаче высокого отрицательного потенциала на катодную мишень между электродами возникает самостоятельный тлеющий газовый разряд. Электроны, приобретая энергию, ионизируют молекулы аргона. Положительные ионы притягиваются катодной мишенью и, сталкиваясь с ней, выбивают атомы из нее. Основным параметром распыления является коэффициент распыления – количество атомов распыляемого вещества, выбитых с поверхности при падении на него одного иона инертного газа. 74
Катодное распыление Метод основан на выбивании ионами инертного газа атомов распыляемого вещества. При подаче высокого отрицательного потенциала на катодную мишень между электродами возникает самостоятельный тлеющий газовый разряд. Электроны, приобретая энергию, ионизируют молекулы аргона. Положительные ионы притягиваются катодной мишенью и, сталкиваясь с ней, выбивают атомы из нее. Основным параметром распыления является коэффициент распыления – количество атомов распыляемого вещества, выбитых с поверхности при падении на него одного иона инертного газа. 74
 75
75
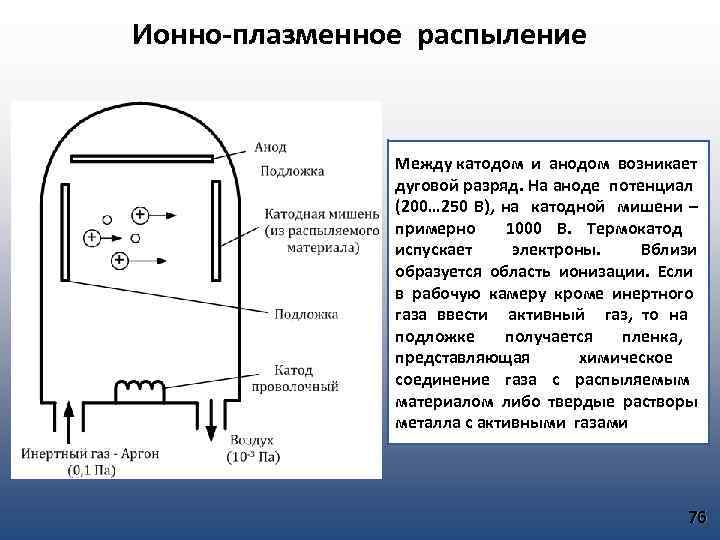 Ионно-плазменное распыление Между катодом и анодом возникает дуговой разряд. На аноде потенциал (200… 250 В), на катодной мишени – примерно 1000 В. Термокатод испускает электроны. Вблизи образуется область ионизации. Если в рабочую камеру кроме инертного газа ввести активный газ, то на подложке получается пленка, представляющая химическое соединение газа с распыляемым материалом либо твердые растворы металла с активными газами 76
Ионно-плазменное распыление Между катодом и анодом возникает дуговой разряд. На аноде потенциал (200… 250 В), на катодной мишени – примерно 1000 В. Термокатод испускает электроны. Вблизи образуется область ионизации. Если в рабочую камеру кроме инертного газа ввести активный газ, то на подложке получается пленка, представляющая химическое соединение газа с распыляемым материалом либо твердые растворы металла с активными газами 76
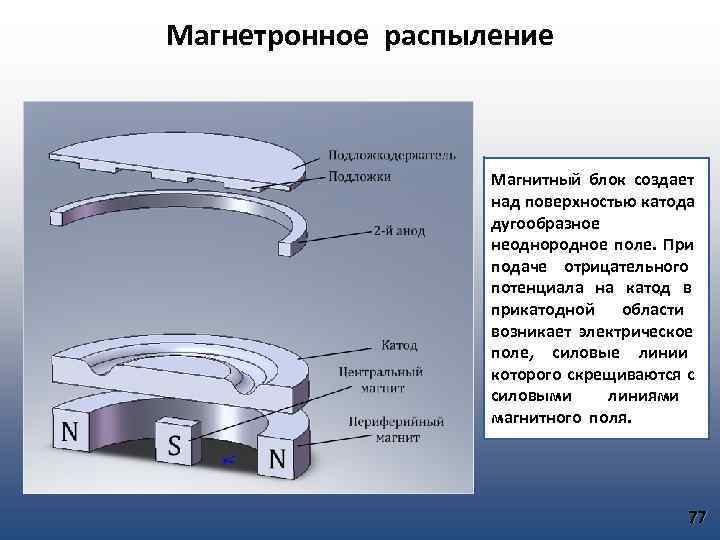 Магнетронное распыление Магнитный блок создает над поверхностью катода дугообразное неоднородное поле. При подаче отрицательного потенциала на катод в прикатодной области возникает электрическое поле, силовые линии которого скрещиваются с силовыми линиями магнитного поля. 77
Магнетронное распыление Магнитный блок создает над поверхностью катода дугообразное неоднородное поле. При подаче отрицательного потенциала на катод в прикатодной области возникает электрическое поле, силовые линии которого скрещиваются с силовыми линиями магнитного поля. 77
 Основные преимущества Возможность получения пленок из тугоплавких материалов Возможность получения пленок стехеометрического состава из сплавов и сложных химических соединений Равномерность толщин пленок вследствие большой площади катодной мишени Возможность получения окисных, нитридных и других пленок за счет химического взаимодействия напыляемого материала с вводимыми в камеру активными газами Основные недостатки Высокие требования к чистоте газов Сравнительно меньшая скорость распыления Более сложные источники питания, более сложное оборудование Сравнительно низкий вакуум и возможность загрязнение пленок 78
Основные преимущества Возможность получения пленок из тугоплавких материалов Возможность получения пленок стехеометрического состава из сплавов и сложных химических соединений Равномерность толщин пленок вследствие большой площади катодной мишени Возможность получения окисных, нитридных и других пленок за счет химического взаимодействия напыляемого материала с вводимыми в камеру активными газами Основные недостатки Высокие требования к чистоте газов Сравнительно меньшая скорость распыления Более сложные источники питания, более сложное оборудование Сравнительно низкий вакуум и возможность загрязнение пленок 78
 Тема 10 Физико-химические основы процесса эпитаксии 1. Виды эпитаксии. 2. Эпитаксиальное наращивание кремния из газовой фазы. 79
Тема 10 Физико-химические основы процесса эпитаксии 1. Виды эпитаксии. 2. Эпитаксиальное наращивание кремния из газовой фазы. 79
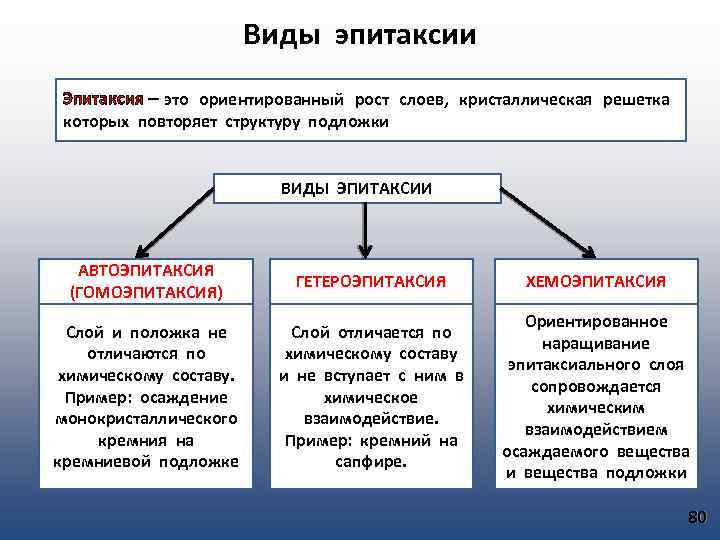 Виды эпитаксии Эпитаксия – это ориентированный рост слоев, кристаллическая решетка которых повторяет структуру подложки ВИДЫ ЭПИТАКСИИ АВТОЭПИТАКСИЯ (ГОМОЭПИТАКСИЯ) ГЕТЕРОЭПИТАКСИЯ ХЕМОЭПИТАКСИЯ Слой и положка не отличаются по химическому составу. Пример: осаждение монокристаллического кремния на кремниевой подложке Слой отличается по химическому составу и не вступает с ним в химическое взаимодействие. Пример: кремний на сапфире. Ориентированное наращивание эпитаксиального слоя сопровождается химическим взаимодействием осаждаемого вещества и вещества подложки 80
Виды эпитаксии Эпитаксия – это ориентированный рост слоев, кристаллическая решетка которых повторяет структуру подложки ВИДЫ ЭПИТАКСИИ АВТОЭПИТАКСИЯ (ГОМОЭПИТАКСИЯ) ГЕТЕРОЭПИТАКСИЯ ХЕМОЭПИТАКСИЯ Слой и положка не отличаются по химическому составу. Пример: осаждение монокристаллического кремния на кремниевой подложке Слой отличается по химическому составу и не вступает с ним в химическое взаимодействие. Пример: кремний на сапфире. Ориентированное наращивание эпитаксиального слоя сопровождается химическим взаимодействием осаждаемого вещества и вещества подложки 80
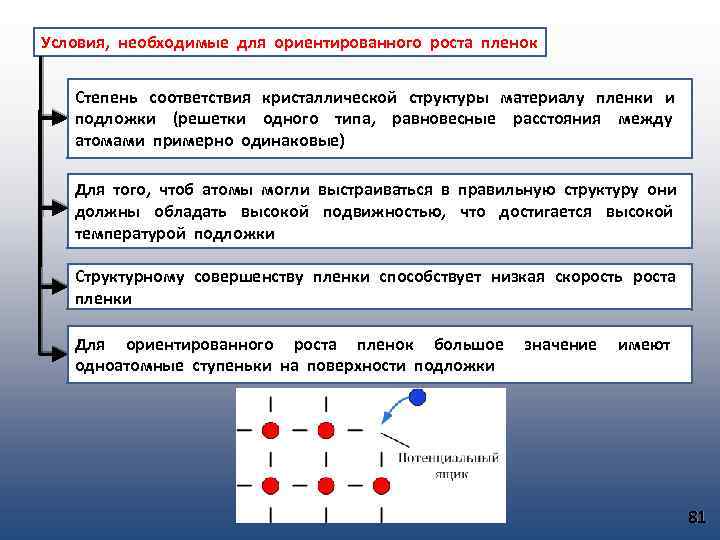 Условия, необходимые для ориентированного роста пленок Степень соответствия кристаллической структуры материалу пленки и подложки (решетки одного типа, равновесные расстояния между атомами примерно одинаковые) Для того, чтоб атомы могли выстраиваться в правильную структуру они должны обладать высокой подвижностью, что достигается высокой температурой подложки Структурному совершенству пленки способствует низкая скорость роста пленки Для ориентированного роста пленок большое значение имеют одноатомные ступеньки на поверхности подложки 81
Условия, необходимые для ориентированного роста пленок Степень соответствия кристаллической структуры материалу пленки и подложки (решетки одного типа, равновесные расстояния между атомами примерно одинаковые) Для того, чтоб атомы могли выстраиваться в правильную структуру они должны обладать высокой подвижностью, что достигается высокой температурой подложки Структурному совершенству пленки способствует низкая скорость роста пленки Для ориентированного роста пленок большое значение имеют одноатомные ступеньки на поверхности подложки 81
 Методы проведения эпитаксии 1. Конденсация из паровой фазы в вакууме Конденсация на горячей подложке (для кремния >900 °C) позволяет получать монокристаллическую пленку. 2. Кристаллизация из газовой фазы Атомы полупроводникового материала переносятся в составе химического соединения к нагретым подложкам, где химическое соединение диссоциирует, полупроводниковое вещество выделяется и конденсируется на подложке. 3. Жидкофазная эпитаксия Наращивают монокристаллические пленки из металлических расплавов, насыщенных полупроводниковых веществом. 4. Твердофазная эпитаксия На монокристаллическую подложку наносится несколько тонких слоев вещества пленки, а затем многослойную структуру подвергают изотермическому отжигу. 5. Молекулярно-лучевая эпитаксия Заключается во взаимодействии нескольких молекулярных пучков разного состава и плотности с нагретой монокристаллической подложкой, в результате чего на подложке осаждаются элементарные компоненты, образуя монокристаллическую пленку. Этим методом получают тройные, четверные химические соединения. 6. Эпитаксия с использованием сканирования лучом лазера 82
Методы проведения эпитаксии 1. Конденсация из паровой фазы в вакууме Конденсация на горячей подложке (для кремния >900 °C) позволяет получать монокристаллическую пленку. 2. Кристаллизация из газовой фазы Атомы полупроводникового материала переносятся в составе химического соединения к нагретым подложкам, где химическое соединение диссоциирует, полупроводниковое вещество выделяется и конденсируется на подложке. 3. Жидкофазная эпитаксия Наращивают монокристаллические пленки из металлических расплавов, насыщенных полупроводниковых веществом. 4. Твердофазная эпитаксия На монокристаллическую подложку наносится несколько тонких слоев вещества пленки, а затем многослойную структуру подвергают изотермическому отжигу. 5. Молекулярно-лучевая эпитаксия Заключается во взаимодействии нескольких молекулярных пучков разного состава и плотности с нагретой монокристаллической подложкой, в результате чего на подложке осаждаются элементарные компоненты, образуя монокристаллическую пленку. Этим методом получают тройные, четверные химические соединения. 6. Эпитаксия с использованием сканирования лучом лазера 82
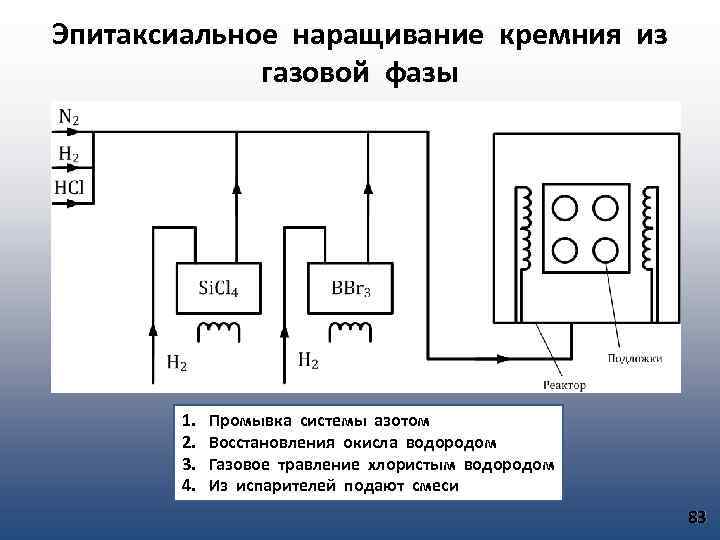 Эпитаксиальное наращивание кремния из газовой фазы 1. 2. 3. 4. Промывка системы азотом Восстановления окисла водородом Газовое травление хлористым водородом Из испарителей подают смеси 83
Эпитаксиальное наращивание кремния из газовой фазы 1. 2. 3. 4. Промывка системы азотом Восстановления окисла водородом Газовое травление хлористым водородом Из испарителей подают смеси 83
 Тема 11 Особенности структуры и свойства пленок 1. Особенности структуры пленок. 2. Влияние физико-химических факторов на структуру и свойства пленок. 84
Тема 11 Особенности структуры и свойства пленок 1. Особенности структуры пленок. 2. Влияние физико-химических факторов на структуру и свойства пленок. 84
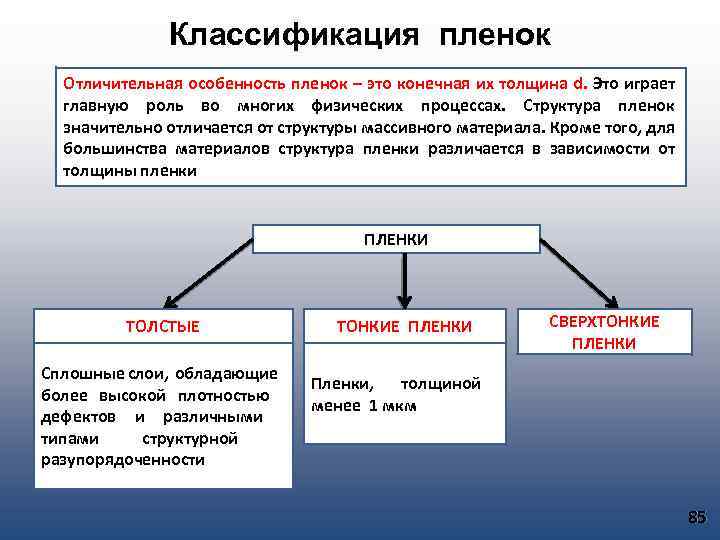 Классификация пленок Отличительная особенность пленок – это конечная их толщина d. Это играет главную роль во многих физических процессах. Структура пленок значительно отличается от структуры массивного материала. Кроме того, для большинства материалов структура пленки различается в зависимости от толщины пленки. ПЛЕНКИ ТОЛСТЫЕ Сплошные слои, обладающие более высокой плотностью дефектов и различными типами структурной разупорядоченности ТОНКИЕ ПЛЕНКИ СВЕРХТОНКИЕ ПЛЕНКИ Пленки, толщиной менее 1 мкм 85
Классификация пленок Отличительная особенность пленок – это конечная их толщина d. Это играет главную роль во многих физических процессах. Структура пленок значительно отличается от структуры массивного материала. Кроме того, для большинства материалов структура пленки различается в зависимости от толщины пленки. ПЛЕНКИ ТОЛСТЫЕ Сплошные слои, обладающие более высокой плотностью дефектов и различными типами структурной разупорядоченности ТОНКИЕ ПЛЕНКИ СВЕРХТОНКИЕ ПЛЕНКИ Пленки, толщиной менее 1 мкм 85
 Особенности структуры пленок Структура тонких пленок зависит от: Температуры подложки и состояния ее поверхности Скорости осаждения Давления и состава остаточного газа Свойств испаряемого материала и материала подложки Один из основных параметров контролируемых в процессе напыления – это удельное сопротивление пленки. Тонкие металлические пленки на неметаллической подложке обладают удельным сопротивлением значительно более высоким, чем удельное сопротивление массивного материала. Электропроводность возникает тогда, когда размеры островков достаточны для их соприкосновения. Критическая толщина пленки – это такая толщина пленки, при которой она становится проводящей. 86
Особенности структуры пленок Структура тонких пленок зависит от: Температуры подложки и состояния ее поверхности Скорости осаждения Давления и состава остаточного газа Свойств испаряемого материала и материала подложки Один из основных параметров контролируемых в процессе напыления – это удельное сопротивление пленки. Тонкие металлические пленки на неметаллической подложке обладают удельным сопротивлением значительно более высоким, чем удельное сопротивление массивного материала. Электропроводность возникает тогда, когда размеры островков достаточны для их соприкосновения. Критическая толщина пленки – это такая толщина пленки, при которой она становится проводящей. 86
 Структура тонких пленок, получаемых методом термовакуумного напыления зависит от 1. Температуры напыления материала металлы с температурой плавления выше 1900 С тугоплавкие (вольфрам, молибден, тантал); металлы с температурой плавления от 600 С до 1900 С (Au, Fe, Ni, Pt, Ag, Ti, Cr) металлы с температурой плавления меньше 600 С (висмут, индий, кадмий, магний, цинк). 2. Скорости испарения (подвижность конденсируемых атомов в процессе испарения и в процессе роста различна для различных групп металлов) 3. Парциального давления остаточных газов 4. Температуры подложки 87
Структура тонких пленок, получаемых методом термовакуумного напыления зависит от 1. Температуры напыления материала металлы с температурой плавления выше 1900 С тугоплавкие (вольфрам, молибден, тантал); металлы с температурой плавления от 600 С до 1900 С (Au, Fe, Ni, Pt, Ag, Ti, Cr) металлы с температурой плавления меньше 600 С (висмут, индий, кадмий, магний, цинк). 2. Скорости испарения (подвижность конденсируемых атомов в процессе испарения и в процессе роста различна для различных групп металлов) 3. Парциального давления остаточных газов 4. Температуры подложки 87
 Влияние физико-химических факторов на структуру и свойства пленок Электрофизические свойства пленок, независимо то способа их получения, зависят от: толщины, с увеличением толщины удельное сопротивление уменьшается, а теплопроводность увеличивается. Длина свободного пробега электронов в пленке оказывается меньше, чем в массивном материале, так как электроны в пленке испытывают дополнительные столкновения с границами поверхностей пленки. Для различных соотношений между толщиной пленки d и длинной свободного пробега для электрона можно записать: 88
Влияние физико-химических факторов на структуру и свойства пленок Электрофизические свойства пленок, независимо то способа их получения, зависят от: толщины, с увеличением толщины удельное сопротивление уменьшается, а теплопроводность увеличивается. Длина свободного пробега электронов в пленке оказывается меньше, чем в массивном материале, так как электроны в пленке испытывают дополнительные столкновения с границами поверхностей пленки. Для различных соотношений между толщиной пленки d и длинной свободного пробега для электрона можно записать: 88
 На структуру пленки влияет температура подложки в момент осаждения, поэтому удельное сопротивление зависит от температуры подложки. Если получить пленку на холодной подложке, то можно улучшить её параметры путем технологического отжига. В пленках осажденных на холодную подложку возникают механические напряжения, чтобы убрать этот дефект применяют технологический отжиг, он еще удаляет примеси попавшие в материал пленки при её нанесении. Установка для отжига в вакууме Рекристаллизация металла – это процесс образования и роста одних зерен, за счет соседних зерен соседней фазы. Образование и рост зерен с более совершенной структурой, за счет исходных деформированных зерен с менее совершенной структурой называют первичной рекристаллизацией. На следующем этапе – который называют собирательной рекристаллизацией, идет рост одних рекристаллизованных зерен за счет таких же соседних зерен, в результате мелкокристаллическая структура преобразовывается в крупнокристаллическую. 89
На структуру пленки влияет температура подложки в момент осаждения, поэтому удельное сопротивление зависит от температуры подложки. Если получить пленку на холодной подложке, то можно улучшить её параметры путем технологического отжига. В пленках осажденных на холодную подложку возникают механические напряжения, чтобы убрать этот дефект применяют технологический отжиг, он еще удаляет примеси попавшие в материал пленки при её нанесении. Установка для отжига в вакууме Рекристаллизация металла – это процесс образования и роста одних зерен, за счет соседних зерен соседней фазы. Образование и рост зерен с более совершенной структурой, за счет исходных деформированных зерен с менее совершенной структурой называют первичной рекристаллизацией. На следующем этапе – который называют собирательной рекристаллизацией, идет рост одних рекристаллизованных зерен за счет таких же соседних зерен, в результате мелкокристаллическая структура преобразовывается в крупнокристаллическую. 89
 Для любой толщины пленки справедливы соотношения: R – сопротивление пленки; ρП – удельное сопротивление материала пленки; j. П – плотность пленки; l, a, d – длина, ширина и толщина пленки Следовательно, если определить соотношение между электрическим сопротивлением слоя и его массой, то можно найти изменение произведения плотности на удельное сопротивление пленки при различной толщине, меняя параметры технологического процесса и режимы обработки. 90
Для любой толщины пленки справедливы соотношения: R – сопротивление пленки; ρП – удельное сопротивление материала пленки; j. П – плотность пленки; l, a, d – длина, ширина и толщина пленки Следовательно, если определить соотношение между электрическим сопротивлением слоя и его массой, то можно найти изменение произведения плотности на удельное сопротивление пленки при различной толщине, меняя параметры технологического процесса и режимы обработки. 90
 Тема 12 Закономерности и механизмы диффузии в твердых телах 1. Механизмы диффузии. 2. Законы Фика. Закон Аррениуса. 3. Диффузия из ограниченного и неограниченного источника. 4. Применение диффузии для введения примесей в полупроводниковый кристалл. 91
Тема 12 Закономерности и механизмы диффузии в твердых телах 1. Механизмы диффузии. 2. Законы Фика. Закон Аррениуса. 3. Диффузия из ограниченного и неограниченного источника. 4. Применение диффузии для введения примесей в полупроводниковый кристалл. 91
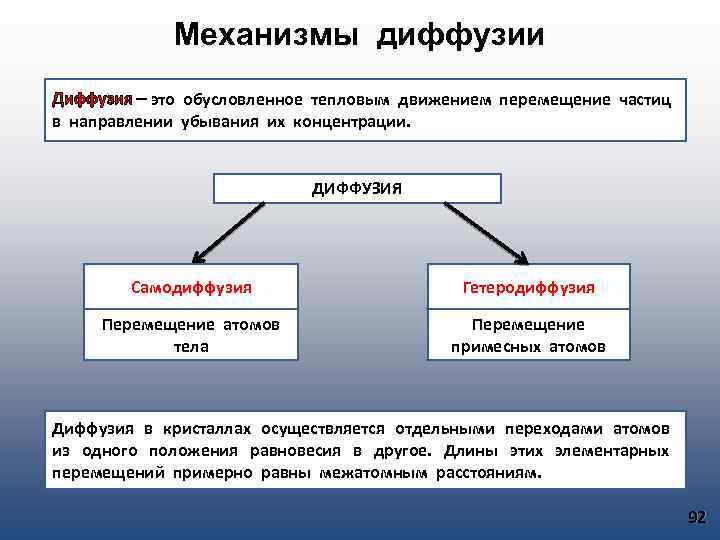 Механизмы диффузии Диффузия – это обусловленное тепловым движением перемещение частиц в направлении убывания их концентрации. ДИФФУЗИЯ Самодиффузия Гетеродиффузия Перемещение атомов тела Перемещение примесных атомов Диффузия в кристаллах осуществляется отдельными переходами атомов из одного положения равновесия в другое. Длины этих элементарных перемещений примерно равны межатомным расстояниям. 92
Механизмы диффузии Диффузия – это обусловленное тепловым движением перемещение частиц в направлении убывания их концентрации. ДИФФУЗИЯ Самодиффузия Гетеродиффузия Перемещение атомов тела Перемещение примесных атомов Диффузия в кристаллах осуществляется отдельными переходами атомов из одного положения равновесия в другое. Длины этих элементарных перемещений примерно равны межатомным расстояниям. 92
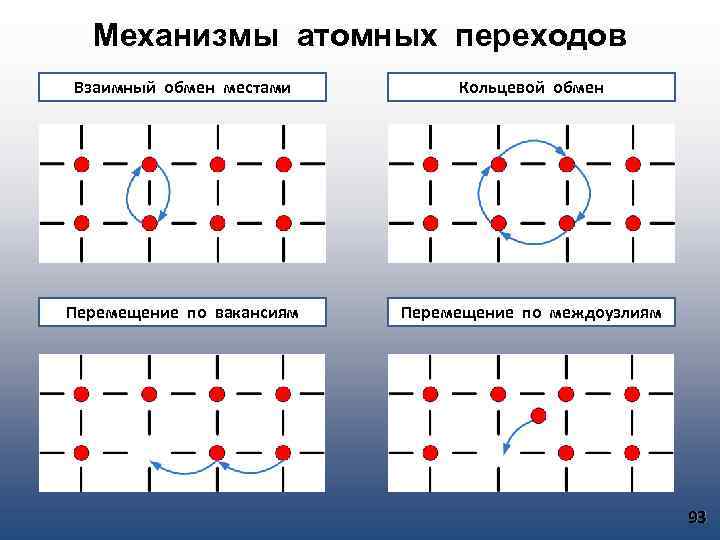 Механизмы атомных переходов Взаимный обмен местами Кольцевой обмен Перемещение по вакансиям Перемещение по междоузлиям 93
Механизмы атомных переходов Взаимный обмен местами Кольцевой обмен Перемещение по вакансиям Перемещение по междоузлиям 93
 Законы Фика. Закон Аррениуса. 1 -й ЗАКОН ФИКА Плотность потока атомов из одного вещества в другое определяется как J – вектор плотности потока атомов вещества, 1/(м 2·с) D – коэффициент диффузии, м 2/с ∇N – вектор градиента концентрации диффундирующих атомов, м-3 Чаще в технологии рассматривается диффузия в одном направлении по отношению к кристаллу, поэтому уравнение преобразуется к виду 94
Законы Фика. Закон Аррениуса. 1 -й ЗАКОН ФИКА Плотность потока атомов из одного вещества в другое определяется как J – вектор плотности потока атомов вещества, 1/(м 2·с) D – коэффициент диффузии, м 2/с ∇N – вектор градиента концентрации диффундирующих атомов, м-3 Чаще в технологии рассматривается диффузия в одном направлении по отношению к кристаллу, поэтому уравнение преобразуется к виду 94
 2 -й ЗАКОН ФИКА Закон определяет распределение концентрации примеси по глубине в различные моменты времени При D=const ЗАКОН АРРЕНИУСА Закон отражает зависимость коэффициента диффузии от температуры ΔЕа – энергия активации – та энергия, которую должен иметь каждый атом, чтобы диффундировать через кристаллическую решетку. D 0 – постоянная, которая зависит от геометрии элементарной ячейки, от параметра решетки, от механизма диффузии. 95
2 -й ЗАКОН ФИКА Закон определяет распределение концентрации примеси по глубине в различные моменты времени При D=const ЗАКОН АРРЕНИУСА Закон отражает зависимость коэффициента диффузии от температуры ΔЕа – энергия активации – та энергия, которую должен иметь каждый атом, чтобы диффундировать через кристаллическую решетку. D 0 – постоянная, которая зависит от геометрии элементарной ячейки, от параметра решетки, от механизма диффузии. 95
 Диффузия из ограниченного и неограниченного источника Решая второе уравнение Фика, можно определить распределение концентрации примеси по глубине диффузионного слоя в различные моменты времени Для поиска решений необходимо наличие граничных и начальных условий: Начальное условие Граничные условия Второе граничное условие имеет 2 варианта, которые соответствуют 2 -м вариантам технологического процесса диффузии 96
Диффузия из ограниченного и неограниченного источника Решая второе уравнение Фика, можно определить распределение концентрации примеси по глубине диффузионного слоя в различные моменты времени Для поиска решений необходимо наличие граничных и начальных условий: Начальное условие Граничные условия Второе граничное условие имеет 2 варианта, которые соответствуют 2 -м вариантам технологического процесса диффузии 96
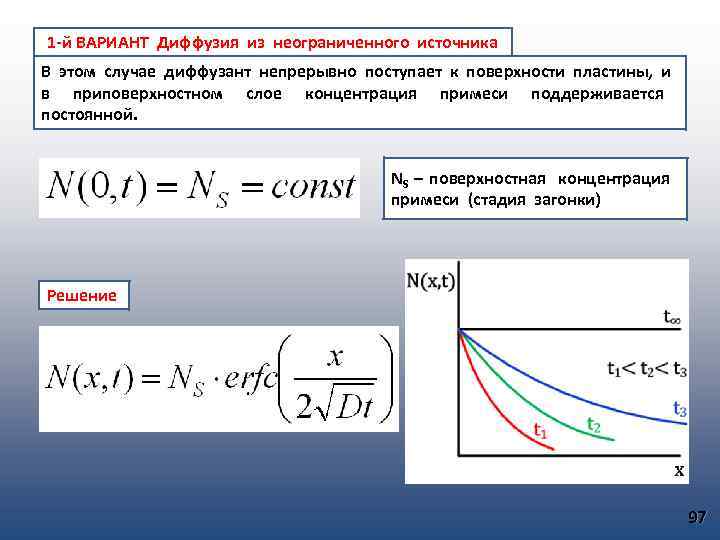 1 -й ВАРИАНТ Диффузия из неограниченного источника В этом случае диффузант непрерывно поступает к поверхности пластины, и в приповерхностном слое концентрация примеси поддерживается постоянной. NS – поверхностная концентрация примеси (стадия загонки) Решение 97
1 -й ВАРИАНТ Диффузия из неограниченного источника В этом случае диффузант непрерывно поступает к поверхности пластины, и в приповерхностном слое концентрация примеси поддерживается постоянной. NS – поверхностная концентрация примеси (стадия загонки) Решение 97
 2 -й ВАРИАНТ Диффузия из ограниченного источника В начале в тонкий приповерхностный слой вводят некоторое количество атомов примеси. Затем источник диффузанта убирают и пластину нагревают, в результате чего введенные атомы примеси перераспределяются на нужную глубину (стадия разгонки) Решение 98
2 -й ВАРИАНТ Диффузия из ограниченного источника В начале в тонкий приповерхностный слой вводят некоторое количество атомов примеси. Затем источник диффузанта убирают и пластину нагревают, в результате чего введенные атомы примеси перераспределяются на нужную глубину (стадия разгонки) Решение 98
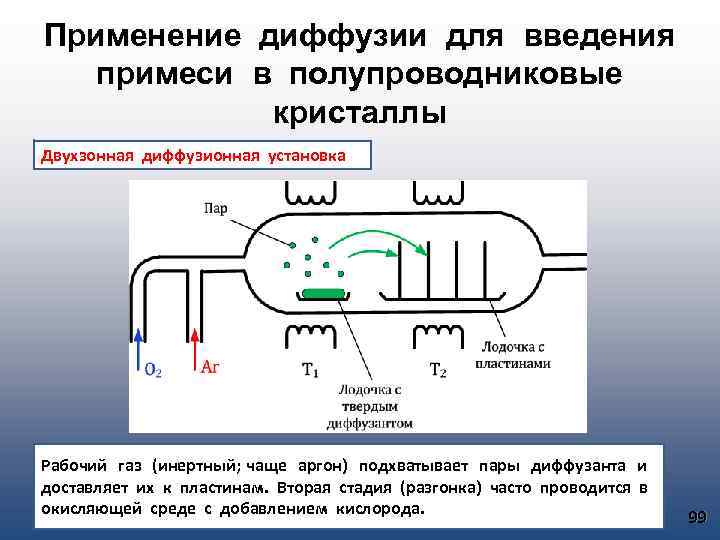 Применение диффузии для введения примеси в полупроводниковые кристаллы Двухзонная диффузионная установка Рабочий газ (инертный; чаще аргон) подхватывает пары диффузанта и доставляет их к пластинам. Вторая стадия (разгонка) часто проводится в окисляющей среде с добавлением кислорода. 99
Применение диффузии для введения примеси в полупроводниковые кристаллы Двухзонная диффузионная установка Рабочий газ (инертный; чаще аргон) подхватывает пары диффузанта и доставляет их к пластинам. Вторая стадия (разгонка) часто проводится в окисляющей среде с добавлением кислорода. 99
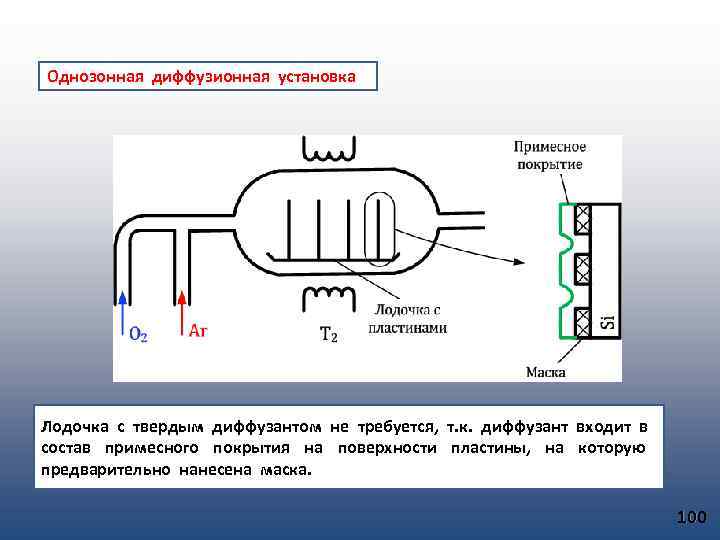 Однозонная диффузионная установка Лодочка с твердым диффузантом не требуется, т. к. диффузант входит в состав примесного покрытия на поверхности пластины, на которую предварительно нанесена маска. 100
Однозонная диффузионная установка Лодочка с твердым диффузантом не требуется, т. к. диффузант входит в состав примесного покрытия на поверхности пластины, на которую предварительно нанесена маска. 100
 Тема 13 Физические основы ионного легирования 1. Основные закономерности процесса ионной имплантации. 2. Параметры процесса, оборудование. 101
Тема 13 Физические основы ионного легирования 1. Основные закономерности процесса ионной имплантации. 2. Параметры процесса, оборудование. 101
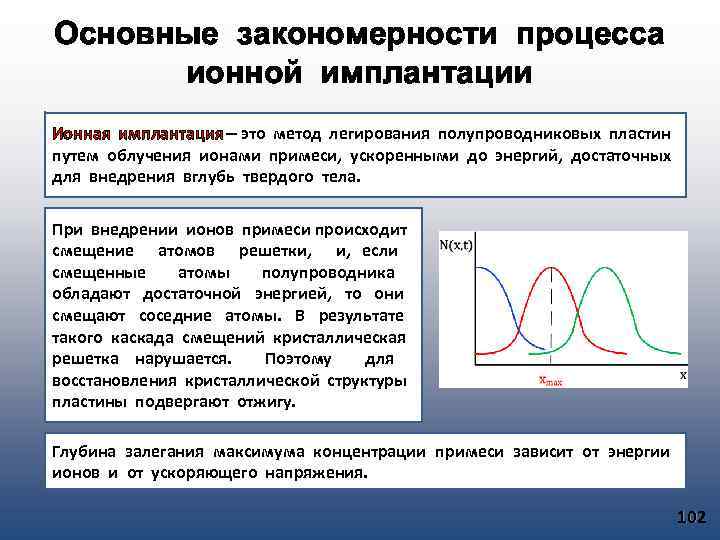 Основные закономерности процесса ионной имплантации Ионная имплантация – это метод легирования полупроводниковых пластин путем облучения ионами примеси, ускоренными до энергий, достаточных для внедрения вглубь твердого тела. При внедрении ионов примеси происходит смещение атомов решетки, и, если смещенные атомы полупроводника обладают достаточной энергией, то они смещают соседние атомы. В результате такого каскада смещений кристаллическая решетка нарушается. Поэтому для восстановления кристаллической структуры пластины подвергают отжигу. Глубина залегания максимума концентрации примеси зависит от энергии ионов и от ускоряющего напряжения. 102
Основные закономерности процесса ионной имплантации Ионная имплантация – это метод легирования полупроводниковых пластин путем облучения ионами примеси, ускоренными до энергий, достаточных для внедрения вглубь твердого тела. При внедрении ионов примеси происходит смещение атомов решетки, и, если смещенные атомы полупроводника обладают достаточной энергией, то они смещают соседние атомы. В результате такого каскада смещений кристаллическая решетка нарушается. Поэтому для восстановления кристаллической структуры пластины подвергают отжигу. Глубина залегания максимума концентрации примеси зависит от энергии ионов и от ускоряющего напряжения. 102
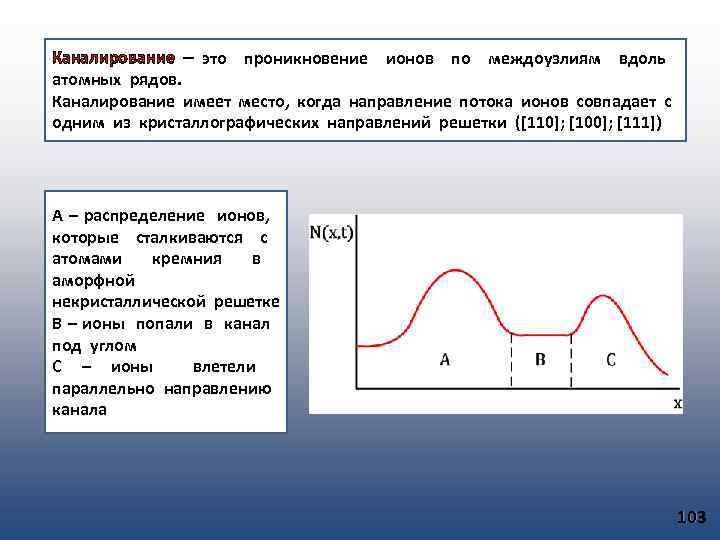 Каналирование – это проникновение ионов по междоузлиям вдоль атомных рядов. Каналирование имеет место, когда направление потока ионов совпадает с одним из кристаллографических направлений решетки ([110]; [100]; [111]) А – распределение ионов, которые сталкиваются с атомами кремния в аморфной некристаллической решетке В – ионы попали в канал под углом С – ионы влетели параллельно направлению канала 103
Каналирование – это проникновение ионов по междоузлиям вдоль атомных рядов. Каналирование имеет место, когда направление потока ионов совпадает с одним из кристаллографических направлений решетки ([110]; [100]; [111]) А – распределение ионов, которые сталкиваются с атомами кремния в аморфной некристаллической решетке В – ионы попали в канал под углом С – ионы влетели параллельно направлению канала 103
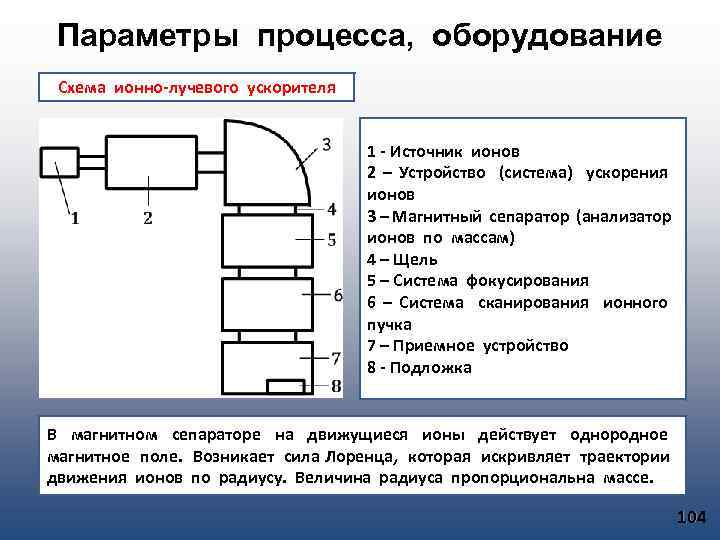 Параметры процесса, оборудование Схема ионно-лучевого ускорителя 1 - Источник ионов 2 – Устройство (система) ускорения ионов 3 – Магнитный сепаратор (анализатор ионов по массам) 4 – Щель 5 – Система фокусирования 6 – Система сканирования ионного пучка 7 – Приемное устройство 8 - Подложка В магнитном сепараторе на движущиеся ионы действует однородное магнитное поле. Возникает сила Лоренца, которая искривляет траектории движения ионов по радиусу. Величина радиуса пропорциональна массе. 104
Параметры процесса, оборудование Схема ионно-лучевого ускорителя 1 - Источник ионов 2 – Устройство (система) ускорения ионов 3 – Магнитный сепаратор (анализатор ионов по массам) 4 – Щель 5 – Система фокусирования 6 – Система сканирования ионного пучка 7 – Приемное устройство 8 - Подложка В магнитном сепараторе на движущиеся ионы действует однородное магнитное поле. Возникает сила Лоренца, которая искривляет траектории движения ионов по радиусу. Величина радиуса пропорциональна массе. 104
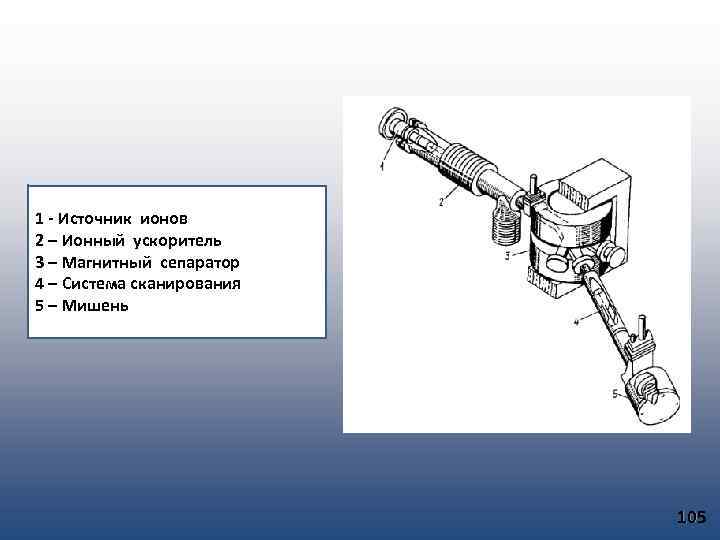 1 - Источник ионов 2 – Ионный ускоритель 3 – Магнитный сепаратор 4 – Система сканирования 5 – Мишень 105
1 - Источник ионов 2 – Ионный ускоритель 3 – Магнитный сепаратор 4 – Система сканирования 5 – Мишень 105
 Тема 14 Химические методы осаждения пленок 1. Теоретические основы химических методов. 2. Осаждение пленок из газовой фазы. 3. Химическое осаждение металлических пленок из растворов 106
Тема 14 Химические методы осаждения пленок 1. Теоретические основы химических методов. 2. Осаждение пленок из газовой фазы. 3. Химическое осаждение металлических пленок из растворов 106
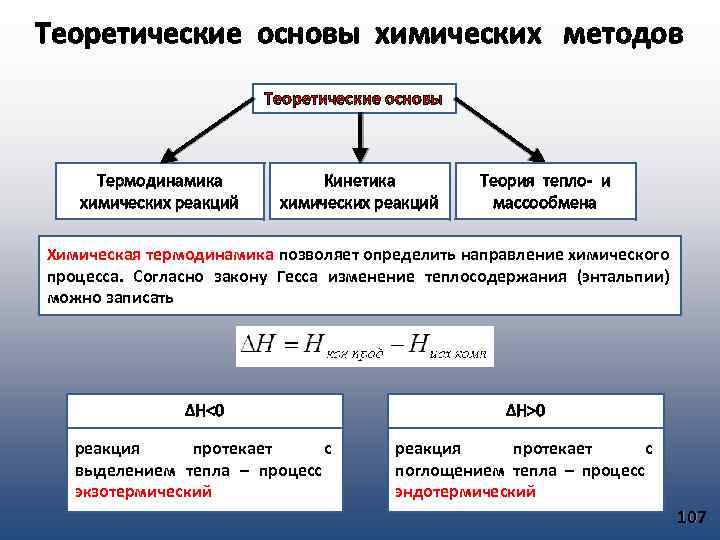 Теоретические основы химических методов Теоретические основы Термодинамика химических реакций Кинетика химических реакций Теория тепло- и массообмена Химическая термодинамика позволяет определить направление химического процесса. Согласно закону Гесса изменение теплосодержания (энтальпии) можно записать ΔН<0 ΔН>0 реакция протекает с выделением тепла – процесс экзотермический реакция протекает с поглощением тепла – процесс эндотермический 107
Теоретические основы химических методов Теоретические основы Термодинамика химических реакций Кинетика химических реакций Теория тепло- и массообмена Химическая термодинамика позволяет определить направление химического процесса. Согласно закону Гесса изменение теплосодержания (энтальпии) можно записать ΔН<0 ΔН>0 реакция протекает с выделением тепла – процесс экзотермический реакция протекает с поглощением тепла – процесс эндотермический 107
 Факторы, определяющие направление химической реакции: Стремление системы отдать энергию, поэтому легче протекают процессы экзотермические. Мерой изменения энергии является величина и знак ΔН. Стремление системы достигнуть наиболее вероятного состояния, которое в первом приближении можно считать как наиболее неупорядоченное. Статистическая вероятность состояния системы измеряется ее энтропией. ΔН<0, ΔS>0 ΔН<0, ΔS<0, |ΔН|>|TΔS| ΔН>0, ΔS>0, |ΔН|<|TΔS| 108
Факторы, определяющие направление химической реакции: Стремление системы отдать энергию, поэтому легче протекают процессы экзотермические. Мерой изменения энергии является величина и знак ΔН. Стремление системы достигнуть наиболее вероятного состояния, которое в первом приближении можно считать как наиболее неупорядоченное. Статистическая вероятность состояния системы измеряется ее энтропией. ΔН<0, ΔS>0 ΔН<0, ΔS<0, |ΔН|>|TΔS| ΔН>0, ΔS>0, |ΔН|<|TΔS| 108
 Кинетика химических реакций Процесс осаждения можно условно разделить на четыре стадии: 1. Перенос исходных компонентов к поверхности подложки 2. Адсорбция и поверхностная диффузия реагентов на подложке 3. Химическая реакция на подложке 4. Удаление побочных продуктов реакции Скорость роста пленки ограничивается стадией, протекающей с наименьшей скоростью. Оптимальные условия создаются в том случае, когда скорости всех стадий одинаковы. Обычно такие условия создать трудно, т. к. в приповерхностном слое у подложки образуется пограничный слой, параметры которого отличаются от параметров всего потока. 109
Кинетика химических реакций Процесс осаждения можно условно разделить на четыре стадии: 1. Перенос исходных компонентов к поверхности подложки 2. Адсорбция и поверхностная диффузия реагентов на подложке 3. Химическая реакция на подложке 4. Удаление побочных продуктов реакции Скорость роста пленки ограничивается стадией, протекающей с наименьшей скоростью. Оптимальные условия создаются в том случае, когда скорости всех стадий одинаковы. Обычно такие условия создать трудно, т. к. в приповерхностном слое у подложки образуется пограничный слой, параметры которого отличаются от параметров всего потока. 109
 Важнейшей характеристикой процесса осаждения является скорость реакции. Скорость реакции оценивается количеством вещества, осажденного в единицу времени на единицу площади поверхности подложки или толщиной пленки, полученной в единицу времени на единице площади подложки. Скорость химической реакции зависит от Т, Р, состава сферы. Скорость реакции экспоненциально зависит от температуры по закону Аррениуса. J 0 - скорость реакции при стандартной температуре, JT- скорость реакции при данной температуре ΔEa- энергия активации. В кинетике химических процессов скорость реакции принято характеризовать изменением концентрации реагирующих веществ в единицу времени. 110
Важнейшей характеристикой процесса осаждения является скорость реакции. Скорость реакции оценивается количеством вещества, осажденного в единицу времени на единицу площади поверхности подложки или толщиной пленки, полученной в единицу времени на единице площади подложки. Скорость химической реакции зависит от Т, Р, состава сферы. Скорость реакции экспоненциально зависит от температуры по закону Аррениуса. J 0 - скорость реакции при стандартной температуре, JT- скорость реакции при данной температуре ΔEa- энергия активации. В кинетике химических процессов скорость реакции принято характеризовать изменением концентрации реагирующих веществ в единицу времени. 110
 Закон действия масс При постоянной температуре скорость данной реакции прямо пропорциональна произведению концентраций реагирующих веществ. Причем каждая из концентраций участвует в степени, в простейшем случае равной коэффициенту перед формулой вещества в уравнении реакции. k – константа скорости реакции 111
Закон действия масс При постоянной температуре скорость данной реакции прямо пропорциональна произведению концентраций реагирующих веществ. Причем каждая из концентраций участвует в степени, в простейшем случае равной коэффициенту перед формулой вещества в уравнении реакции. k – константа скорости реакции 111
 Осаждение пленок из газовой фазы Рассмотрим на примере осаждения окислов фосфора на кремниевую подложку. В исходную газовую смесь входят галогенид фосфора, кислород в разбавлении инертного газа (чаще аргон). Процесс происходит в кварцевом горизонтальном цилиндрическом реакторе (диффузионная печь). Температура процесса 800 -1100 С. Часть окисла фосфора восстанавливается кремнием. При указанных температурах окислы фосфора и кремния находятся в размягченном состоянии. Перемешиваясь, они образуют фосфоросиликатное стекло (ФСС). 112
Осаждение пленок из газовой фазы Рассмотрим на примере осаждения окислов фосфора на кремниевую подложку. В исходную газовую смесь входят галогенид фосфора, кислород в разбавлении инертного газа (чаще аргон). Процесс происходит в кварцевом горизонтальном цилиндрическом реакторе (диффузионная печь). Температура процесса 800 -1100 С. Часть окисла фосфора восстанавливается кремнием. При указанных температурах окислы фосфора и кремния находятся в размягченном состоянии. Перемешиваясь, они образуют фосфоросиликатное стекло (ФСС). 112
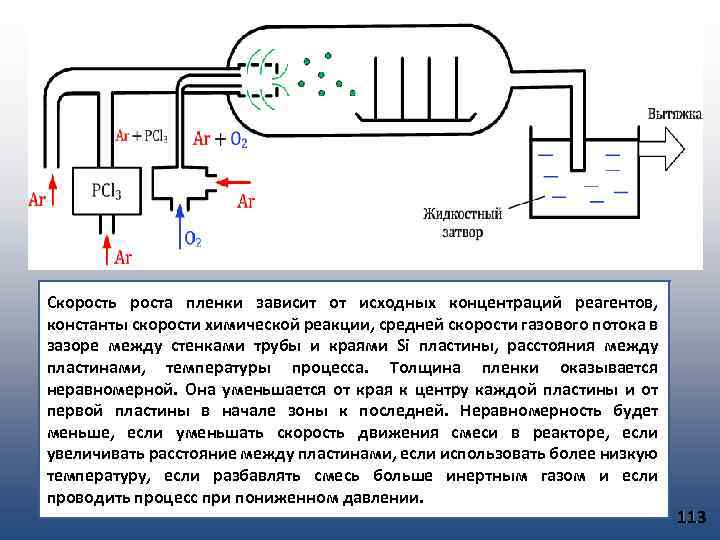 Скорость роста пленки зависит от исходных концентраций реагентов, константы скорости химической реакции, средней скорости газового потока в зазоре между стенками трубы и краями Si пластины, расстояния между пластинами, температуры процесса. Толщина пленки оказывается неравномерной. Она уменьшается от края к центру каждой пластины и от первой пластины в начале зоны к последней. Неравномерность будет меньше, если уменьшать скорость движения смеси в реакторе, если увеличивать расстояние между пластинами, если использовать более низкую температуру, если разбавлять смесь больше инертным газом и если проводить процесс при пониженном давлении. 113
Скорость роста пленки зависит от исходных концентраций реагентов, константы скорости химической реакции, средней скорости газового потока в зазоре между стенками трубы и краями Si пластины, расстояния между пластинами, температуры процесса. Толщина пленки оказывается неравномерной. Она уменьшается от края к центру каждой пластины и от первой пластины в начале зоны к последней. Неравномерность будет меньше, если уменьшать скорость движения смеси в реакторе, если увеличивать расстояние между пластинами, если использовать более низкую температуру, если разбавлять смесь больше инертным газом и если проводить процесс при пониженном давлении. 113
 Химическое осаждение металлических пленок из растворов Химическая металлизация используется в аддитивных, комбинированных методах изготовления печатных плат (в основном для осаждения меди и никеля). А также используется для осаждения золота, серебра при изготовлении ИМС. Используется в других случаях, когда необходимо получить слой металла на диэлектрике (на пластмассе, керамике). В основе химической металлизации лежат окислительновосстановительные реакции Осаждение методом погружения Контактная металлизация Восстановительное осаждение 114
Химическое осаждение металлических пленок из растворов Химическая металлизация используется в аддитивных, комбинированных методах изготовления печатных плат (в основном для осаждения меди и никеля). А также используется для осаждения золота, серебра при изготовлении ИМС. Используется в других случаях, когда необходимо получить слой металла на диэлектрике (на пластмассе, керамике). В основе химической металлизации лежат окислительновосстановительные реакции Осаждение методом погружения Контактная металлизация Восстановительное осаждение 114
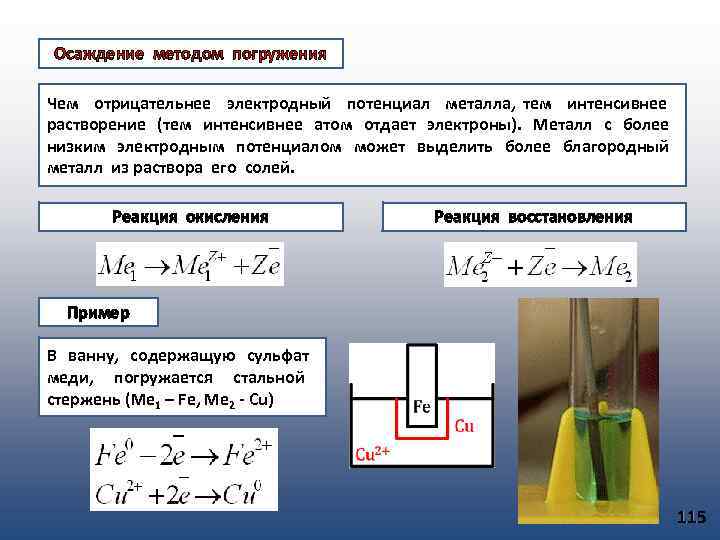 Осаждение методом погружения Чем отрицательнее электродный потенциал металла, тем интенсивнее растворение (тем интенсивнее атом отдает электроны). Металл с более низким электродным потенциалом может выделить более благородный металл из раствора его солей. Реакция окисления Реакция восстановления Пример В ванну, содержащую сульфат меди, погружается стальной стержень (Ме 1 – Fe, Me 2 - Cu) 115
Осаждение методом погружения Чем отрицательнее электродный потенциал металла, тем интенсивнее растворение (тем интенсивнее атом отдает электроны). Металл с более низким электродным потенциалом может выделить более благородный металл из раствора его солей. Реакция окисления Реакция восстановления Пример В ванну, содержащую сульфат меди, погружается стальной стержень (Ме 1 – Fe, Me 2 - Cu) 115
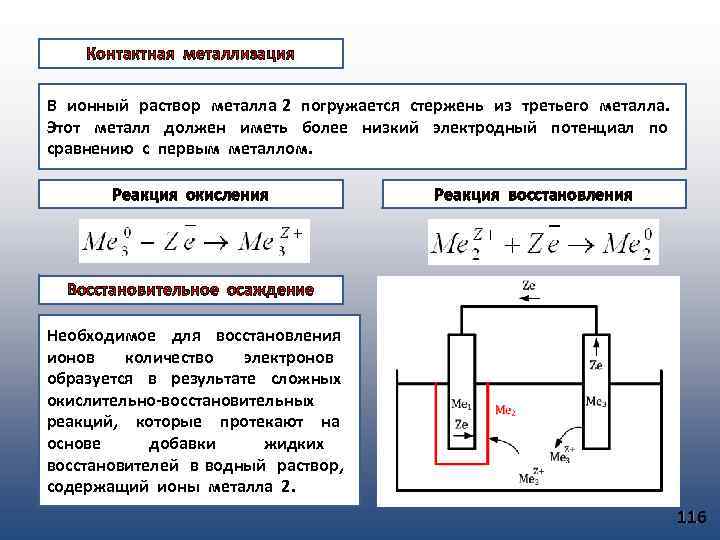 Контактная металлизация В ионный раствор металла 2 погружается стержень из третьего металла. Этот металл должен иметь более низкий электродный потенциал по сравнению с первым металлом. Реакция окисления Реакция восстановления Восстановительное осаждение Необходимое для восстановления ионов количество электронов образуется в результате сложных окислительно-восстановительных реакций, которые протекают на основе добавки жидких восстановителей в водный раствор, содержащий ионы металла 2. 116
Контактная металлизация В ионный раствор металла 2 погружается стержень из третьего металла. Этот металл должен иметь более низкий электродный потенциал по сравнению с первым металлом. Реакция окисления Реакция восстановления Восстановительное осаждение Необходимое для восстановления ионов количество электронов образуется в результате сложных окислительно-восстановительных реакций, которые протекают на основе добавки жидких восстановителей в водный раствор, содержащий ионы металла 2. 116
 Достоинства химической металлизации Отлаженность технологического процесса Возможность нанесения покрытия на диэлектрик Меньшая, чем при гальваническом покрытии, пористость пленки Равномерное распределение толщины слоя на деталях сложной конфигурации Недостатки химической металлизации Низкая стабильность ванн Высокая стоимость процесса Невозможность осаждения всех металлов Необходимость предварительной обработки материала основания (активация, сенсибилизация) 117
Достоинства химической металлизации Отлаженность технологического процесса Возможность нанесения покрытия на диэлектрик Меньшая, чем при гальваническом покрытии, пористость пленки Равномерное распределение толщины слоя на деталях сложной конфигурации Недостатки химической металлизации Низкая стабильность ванн Высокая стоимость процесса Невозможность осаждения всех металлов Необходимость предварительной обработки материала основания (активация, сенсибилизация) 117
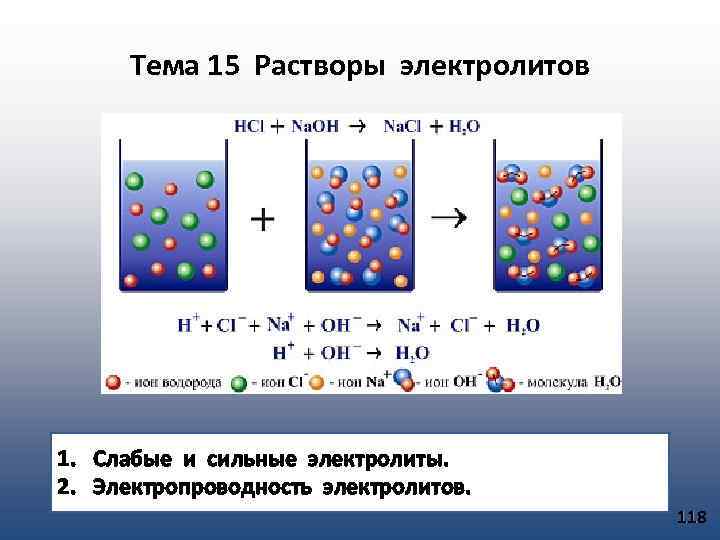 Тема 15 Растворы электролитов 1. Слабые и сильные электролиты. 2. Электропроводность электролитов. 118
Тема 15 Растворы электролитов 1. Слабые и сильные электролиты. 2. Электропроводность электролитов. 118
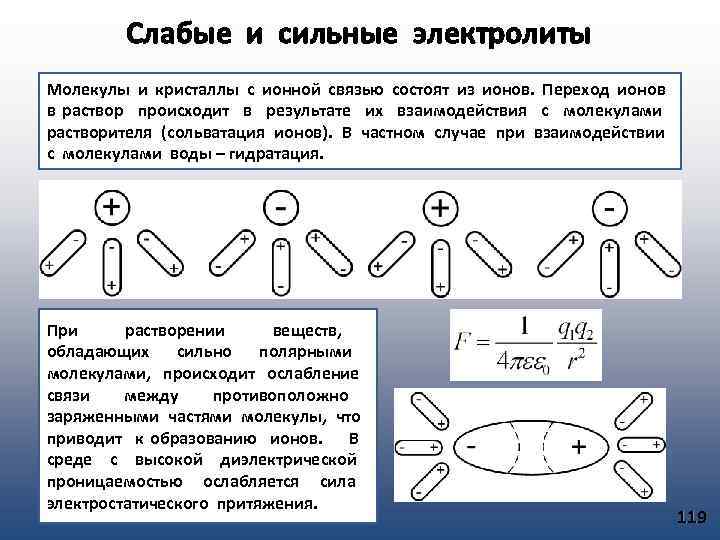 Слабые и сильные электролиты Молекулы и кристаллы с ионной связью состоят из ионов. Переход ионов в раствор происходит в результате их взаимодействия с молекулами растворителя (сольватация ионов). В частном случае при взаимодействии с молекулами воды – гидратация. При растворении веществ, обладающих сильно полярными молекулами, происходит ослабление связи между противоположно заряженными частями молекулы, что приводит к образованию ионов. В среде с высокой диэлектрической проницаемостью ослабляется сила электростатического притяжения. 119
Слабые и сильные электролиты Молекулы и кристаллы с ионной связью состоят из ионов. Переход ионов в раствор происходит в результате их взаимодействия с молекулами растворителя (сольватация ионов). В частном случае при взаимодействии с молекулами воды – гидратация. При растворении веществ, обладающих сильно полярными молекулами, происходит ослабление связи между противоположно заряженными частями молекулы, что приводит к образованию ионов. В среде с высокой диэлектрической проницаемостью ослабляется сила электростатического притяжения. 119
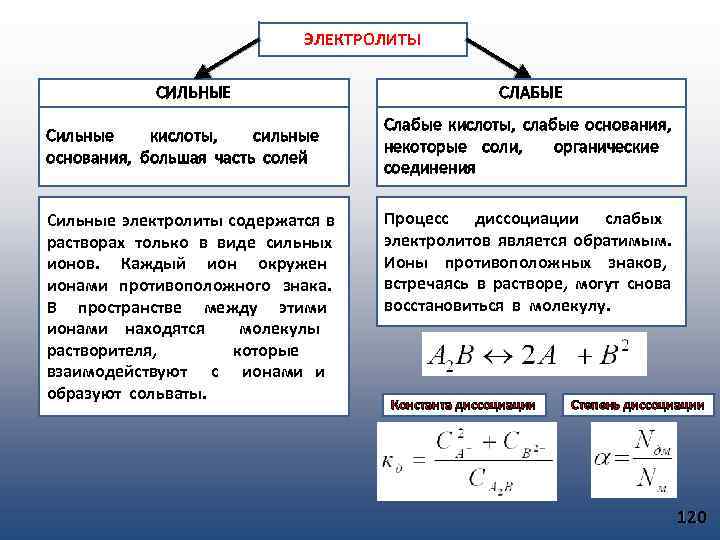 ЭЛЕКТРОЛИТЫ СИЛЬНЫЕ Сильные кислоты, сильные основания, большая часть солей Сильные электролиты содержатся в растворах только в виде сильных ионов. Каждый ион окружен ионами противоположного знака. В пространстве между этими ионами находятся молекулы растворителя, которые взаимодействуют с ионами и образуют сольваты. СЛАБЫЕ Слабые кислоты, слабые основания, некоторые соли, органические соединения Процесс диссоциации слабых электролитов является обратимым. Ионы противоположных знаков, встречаясь в растворе, могут снова восстановиться в молекулу. Константа диссоциации Степень диссоциации 120
ЭЛЕКТРОЛИТЫ СИЛЬНЫЕ Сильные кислоты, сильные основания, большая часть солей Сильные электролиты содержатся в растворах только в виде сильных ионов. Каждый ион окружен ионами противоположного знака. В пространстве между этими ионами находятся молекулы растворителя, которые взаимодействуют с ионами и образуют сольваты. СЛАБЫЕ Слабые кислоты, слабые основания, некоторые соли, органические соединения Процесс диссоциации слабых электролитов является обратимым. Ионы противоположных знаков, встречаясь в растворе, могут снова восстановиться в молекулу. Константа диссоциации Степень диссоциации 120
 Электропроводность электролитов Удельная электропроводность σ – это электропроводность слоя раствора длиной 1 см, заключенного между электродами, площадью 1 см 2 (Ом-1·см-1) Эквивалентная электропроводность – это электропроводность такого объема раствора, в котором содержатся 1 грамм-эквивалент растворенного вещества при условия, что электроды находятся на расстоянии 1 см друг от друга. С – эквивалентная концентрация раствора; V – это объем, в котором содержится 1 грамм-эквивалент растворенного вещества Электропроводность электролитов связана со скоростью движения ионов в растворе. Подвижность иона 121
Электропроводность электролитов Удельная электропроводность σ – это электропроводность слоя раствора длиной 1 см, заключенного между электродами, площадью 1 см 2 (Ом-1·см-1) Эквивалентная электропроводность – это электропроводность такого объема раствора, в котором содержатся 1 грамм-эквивалент растворенного вещества при условия, что электроды находятся на расстоянии 1 см друг от друга. С – эквивалентная концентрация раствора; V – это объем, в котором содержится 1 грамм-эквивалент растворенного вещества Электропроводность электролитов связана со скоростью движения ионов в растворе. Подвижность иона 121
 Основные причины торможения ионов Влияние релаксации ионной атмосферы Электрофоретический эффект Сила трения Влияние релаксации ионной атмосферы Каждый ион в растворе окружен ионами противоположного знака, создающими ионную атмосферу. При перемещении иона под действием внешнего поля он частично выходит из этого окружения, которое вновь создается в новом положении иона. Время, в течение которого происходит восстановление ионной атмосферы – время релаксации. При движении иона в каждый момент времени сзади него концентрация ионов противоположного знака несколько выше, чем впереди. Такая асимметрия ионной атмосферы тормозит движение иона. Электрофоретический эффект Под действием электрического поля ионы, составляющие ионную атмосферу сами перемещаются в противоположную сторону вместе с сольватирующими их молекулами растворителя. 122
Основные причины торможения ионов Влияние релаксации ионной атмосферы Электрофоретический эффект Сила трения Влияние релаксации ионной атмосферы Каждый ион в растворе окружен ионами противоположного знака, создающими ионную атмосферу. При перемещении иона под действием внешнего поля он частично выходит из этого окружения, которое вновь создается в новом положении иона. Время, в течение которого происходит восстановление ионной атмосферы – время релаксации. При движении иона в каждый момент времени сзади него концентрация ионов противоположного знака несколько выше, чем впереди. Такая асимметрия ионной атмосферы тормозит движение иона. Электрофоретический эффект Под действием электрического поля ионы, составляющие ионную атмосферу сами перемещаются в противоположную сторону вместе с сольватирующими их молекулами растворителя. 122
 Тема 16 Электролиз 1. Химические процессы при электролизе. 2. Количественные законы электролиза. 3. Электрохимическая коррозия металлов. 123
Тема 16 Электролиз 1. Химические процессы при электролизе. 2. Количественные законы электролиза. 3. Электрохимическая коррозия металлов. 123
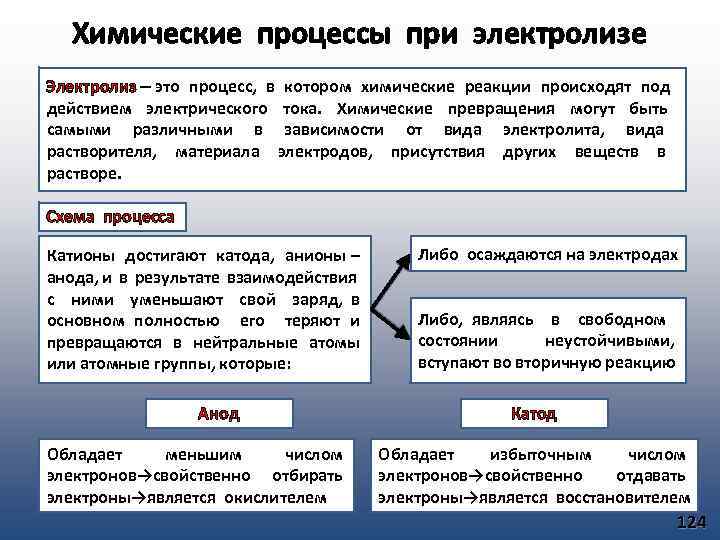 Химические процессы при электролизе Электролиз – это процесс, в котором химические реакции происходят под действием электрического тока. Химические превращения могут быть самыми различными в зависимости от вида электролита, вида растворителя, материала электродов, присутствия других веществ в растворе. Схема процесса Катионы достигают катода, анионы – анода, и в результате взаимодействия с ними уменьшают свой заряд, в основном полностью его теряют и превращаются в нейтральные атомы или атомные группы, которые: Анод Обладает меньшим числом электронов→свойственно отбирать электроны→является окислителем Либо осаждаются на электродах Либо, являясь в свободном состоянии неустойчивыми, вступают во вторичную реакцию Катод Обладает избыточным числом электронов→свойственно отдавать электроны→является восстановителем 124
Химические процессы при электролизе Электролиз – это процесс, в котором химические реакции происходят под действием электрического тока. Химические превращения могут быть самыми различными в зависимости от вида электролита, вида растворителя, материала электродов, присутствия других веществ в растворе. Схема процесса Катионы достигают катода, анионы – анода, и в результате взаимодействия с ними уменьшают свой заряд, в основном полностью его теряют и превращаются в нейтральные атомы или атомные группы, которые: Анод Обладает меньшим числом электронов→свойственно отбирать электроны→является окислителем Либо осаждаются на электродах Либо, являясь в свободном состоянии неустойчивыми, вступают во вторичную реакцию Катод Обладает избыточным числом электронов→свойственно отдавать электроны→является восстановителем 124
 Пример 1 Пусть имеется водный раствор соляной кислоты. Электроды выполнены из инертного материала (например, платина). Ионы Cl- идут к аноду, ионы Н+ - к катоду. Ионы превращаются в нейтральные атомы Образующиеся нейтральные атомы в свободном состоянии неустойчивы, поэтому, соединяясь попарно, они образуют двухатомные молекулы: на аноде - газообразный хлор, на катоде – газообразный водород 125
Пример 1 Пусть имеется водный раствор соляной кислоты. Электроды выполнены из инертного материала (например, платина). Ионы Cl- идут к аноду, ионы Н+ - к катоду. Ионы превращаются в нейтральные атомы Образующиеся нейтральные атомы в свободном состоянии неустойчивы, поэтому, соединяясь попарно, они образуют двухатомные молекулы: на аноде - газообразный хлор, на катоде – газообразный водород 125
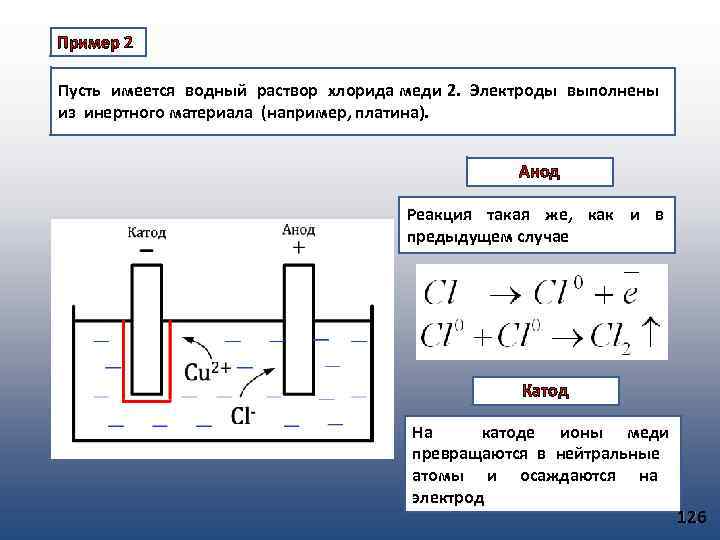 Пример 2 Пусть имеется водный раствор хлорида меди 2. Электроды выполнены из инертного материала (например, платина). Анод Реакция такая же, как и в предыдущем случае Катод На катоде ионы меди превращаются в нейтральные атомы и осаждаются на электрод 126
Пример 2 Пусть имеется водный раствор хлорида меди 2. Электроды выполнены из инертного материала (например, платина). Анод Реакция такая же, как и в предыдущем случае Катод На катоде ионы меди превращаются в нейтральные атомы и осаждаются на электрод 126
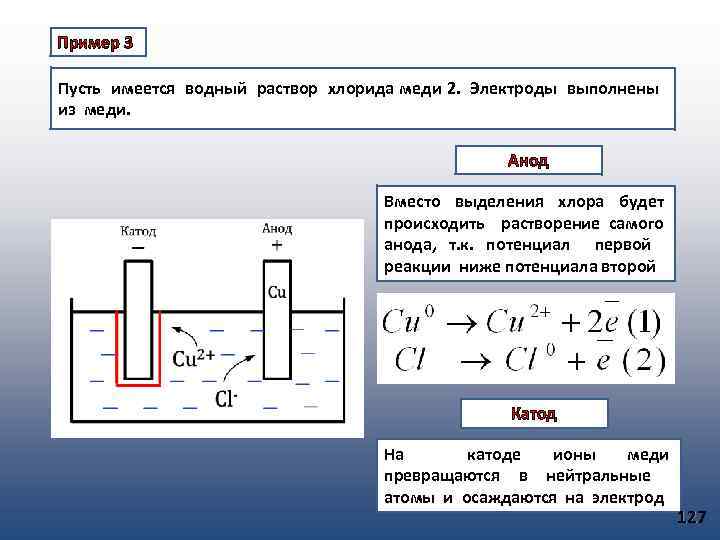 Пример 3 Пусть имеется водный раствор хлорида меди 2. Электроды выполнены из меди. Анод Вместо выделения хлора будет происходить растворение самого анода, т. к. потенциал первой реакции ниже потенциала второй Катод На катоде ионы меди превращаются в нейтральные атомы и осаждаются на электрод 127
Пример 3 Пусть имеется водный раствор хлорида меди 2. Электроды выполнены из меди. Анод Вместо выделения хлора будет происходить растворение самого анода, т. к. потенциал первой реакции ниже потенциала второй Катод На катоде ионы меди превращаются в нейтральные атомы и осаждаются на электрод 127
 Количественные законы электролиза Первый закон Фарадея Для любого электродного процесса количество вещества, превращаемого при электролизе прямо пропорционально силе тока и времени его прохождения, т. е. количеству прошедшего электричества. Второй закон Фарадея При прохождении одинакового количества электричества через растворы различных электролитов количества каждого из веществ, претерпевающих превращения, пропорциональны их химическим эквивалентам, причем для выделения одного грамм-эквивалента любого вещества требуется пропустить 96487 Кл (26, 8 А·ч) Замечания 1. Отношение количества действительно получаемого вещества к тому, которое должно быть получено при расчете по расходу тока, называется выходом по току. 2. Расход тока не определяет расход энергии, т. к. Для расчетов необходима еще и величина напряжения, которая зависит от расстояния между электродами, концентрации раствора, температуры и др. 128
Количественные законы электролиза Первый закон Фарадея Для любого электродного процесса количество вещества, превращаемого при электролизе прямо пропорционально силе тока и времени его прохождения, т. е. количеству прошедшего электричества. Второй закон Фарадея При прохождении одинакового количества электричества через растворы различных электролитов количества каждого из веществ, претерпевающих превращения, пропорциональны их химическим эквивалентам, причем для выделения одного грамм-эквивалента любого вещества требуется пропустить 96487 Кл (26, 8 А·ч) Замечания 1. Отношение количества действительно получаемого вещества к тому, которое должно быть получено при расчете по расходу тока, называется выходом по току. 2. Расход тока не определяет расход энергии, т. к. Для расчетов необходима еще и величина напряжения, которая зависит от расстояния между электродами, концентрации раствора, температуры и др. 128
 Электрохимическая коррозия металлов Электрохимическая коррозия протекает в результате электрохимического взаимодействия различных составных частей металлического материала или металлического изделия Электрохимическая коррозия Жидкостная Атмосферная Происходит взаимодействие металлического материала изделия с водой, раствором электролита или другой жидкой средой Происходит при образовании на поверхности металла тонкой пленки влаги Электрохимическая коррозия является следствием образования гальванической пары, в результате чего происходит растворение металла, обладающего более отрицательным электродным потенциалом. 129
Электрохимическая коррозия металлов Электрохимическая коррозия протекает в результате электрохимического взаимодействия различных составных частей металлического материала или металлического изделия Электрохимическая коррозия Жидкостная Атмосферная Происходит взаимодействие металлического материала изделия с водой, раствором электролита или другой жидкой средой Происходит при образовании на поверхности металла тонкой пленки влаги Электрохимическая коррозия является следствием образования гальванической пары, в результате чего происходит растворение металла, обладающего более отрицательным электродным потенциалом. 129
 Электрохимическая коррозия имеет место: 1. Когда металлы контактируют между собой 2. Когда металлы связаны проводником 3. В сплавах, состоящих из различных фаз Сущность процесса коррозии В паре двух металлов растворяется металл (окисляется) с более отрицательным электродным потенциалом. Если образующиеся на анодных участках электроны не связывать, то процесс растворения прекратится. Металл более благородный, находящийся в контакте с анодным, связывает эти электроны, т. е. Электроны переходят с анодных участков на катодные, и это обеспечивает возможность дальнейшего протекания процесса 130
Электрохимическая коррозия имеет место: 1. Когда металлы контактируют между собой 2. Когда металлы связаны проводником 3. В сплавах, состоящих из различных фаз Сущность процесса коррозии В паре двух металлов растворяется металл (окисляется) с более отрицательным электродным потенциалом. Если образующиеся на анодных участках электроны не связывать, то процесс растворения прекратится. Металл более благородный, находящийся в контакте с анодным, связывает эти электроны, т. е. Электроны переходят с анодных участков на катодные, и это обеспечивает возможность дальнейшего протекания процесса 130
 Защита от коррозии Одним из наиболее часто используемых методов защиты является создание на поверхности изделия защитного покрытия, т. е. Изоляция изделия от действия окружающей среды. Покрытия Металлические Неметаллические Металлические покрытия Анодное Катодное Покрывающий металл обладает более отрицательным электродным потенциалом в данной сфере Покрытия с противоположным соотношением электродных потенциалов При сохранении целостности защитного покрытия разницы в степени защиты нет, но при нарушении целостности катодное покрытия перестает защищать основной металл, образуя с ним гальванопару, а анодное покрытие будет само разрушаться, защищая основной металл 131
Защита от коррозии Одним из наиболее часто используемых методов защиты является создание на поверхности изделия защитного покрытия, т. е. Изоляция изделия от действия окружающей среды. Покрытия Металлические Неметаллические Металлические покрытия Анодное Катодное Покрывающий металл обладает более отрицательным электродным потенциалом в данной сфере Покрытия с противоположным соотношением электродных потенциалов При сохранении целостности защитного покрытия разницы в степени защиты нет, но при нарушении целостности катодное покрытия перестает защищать основной металл, образуя с ним гальванопару, а анодное покрытие будет само разрушаться, защищая основной металл 131
 Тема 17 Физико-химические основы литографии 1. 2. 3. 4. Основные типы фотохимических реакций. Виды литографии. Типы и свойства фоторезистов. Основные операции фотолитографии. 132
Тема 17 Физико-химические основы литографии 1. 2. 3. 4. Основные типы фотохимических реакций. Виды литографии. Типы и свойства фоторезистов. Основные операции фотолитографии. 132
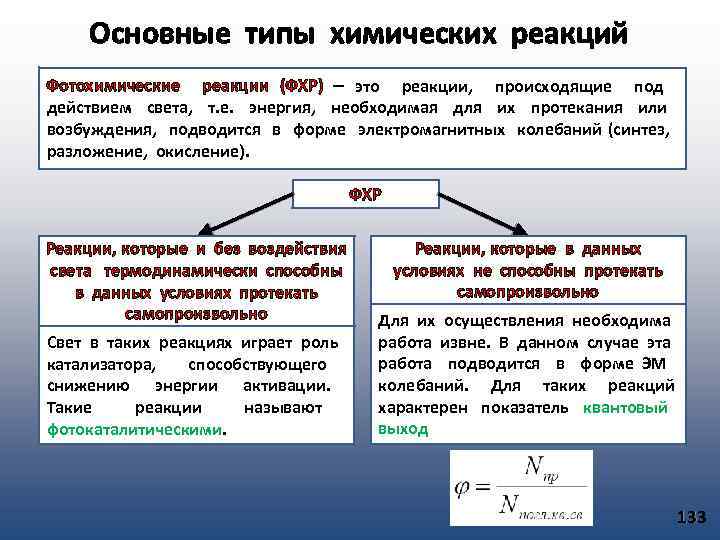 Основные типы химических реакций Фотохимические реакции (ФХР) – это реакции, происходящие под действием света, т. е. энергия, необходимая для их протекания или возбуждения, подводится в форме электромагнитных колебаний (синтез, разложение, окисление). ФХР Реакции, которые и без воздействия света термодинамически способны в данных условиях протекать самопроизвольно Свет в таких реакциях играет роль катализатора, способствующего снижению энергии активации. Такие реакции называют фотокаталитическими. Реакции, которые в данных условиях не способны протекать самопроизвольно Для их осуществления необходима работа извне. В данном случае эта работа подводится в форме ЭМ колебаний. Для таких реакций характерен показатель квантовый выход 133
Основные типы химических реакций Фотохимические реакции (ФХР) – это реакции, происходящие под действием света, т. е. энергия, необходимая для их протекания или возбуждения, подводится в форме электромагнитных колебаний (синтез, разложение, окисление). ФХР Реакции, которые и без воздействия света термодинамически способны в данных условиях протекать самопроизвольно Свет в таких реакциях играет роль катализатора, способствующего снижению энергии активации. Такие реакции называют фотокаталитическими. Реакции, которые в данных условиях не способны протекать самопроизвольно Для их осуществления необходима работа извне. В данном случае эта работа подводится в форме ЭМ колебаний. Для таких реакций характерен показатель квантовый выход 133
 Виды литографии Литография – это процесс формирования в актиночувствительном слое, нанесенном на подложку, рельефного рисунка, который повторяет требуемую конфигурацию элементов слоя. С помощью нее формируют защитную маску из резистивного материала, т. е. материала, стойкого к травителям. В зависимости от длины волны используемого излучения различают следующие виды литографии: 1. Фотолитография (УФ излучение) 2. Рентгенолитография (R излучение, 0, 5 -2 нм) 3. Электронолитография (поток электронов с энергиями 10 -100 кэ. В, 0, 05 нм) 4. Ионолитография (0, 05 -0, 1 нм) 134
Виды литографии Литография – это процесс формирования в актиночувствительном слое, нанесенном на подложку, рельефного рисунка, который повторяет требуемую конфигурацию элементов слоя. С помощью нее формируют защитную маску из резистивного материала, т. е. материала, стойкого к травителям. В зависимости от длины волны используемого излучения различают следующие виды литографии: 1. Фотолитография (УФ излучение) 2. Рентгенолитография (R излучение, 0, 5 -2 нм) 3. Электронолитография (поток электронов с энергиями 10 -100 кэ. В, 0, 05 нм) 4. Ионолитография (0, 05 -0, 1 нм) 134
 Способы переноса изображений: 1. Контактная литография Шаблон находится в контакте с резистом, нанесенным на подложку 2. Проекционная литография Шаблон находится на некотором расстоянии 3. Непосредственная генерация изображения на резисте (без шаблона) Фотолитография Рентгенолитография Электронолитография Ионолитография Фотошаблон Рентгеношаблон Электроношаблон Ионошаблон Фоторезист Рентгенорезист Электронорезист Ионорезист Контактная Проекционная без изменения масштаба Проекционная с уменьшением масштаба Непосредственное экспонирование Проекционная Непосредственное экспонирование 135
Способы переноса изображений: 1. Контактная литография Шаблон находится в контакте с резистом, нанесенным на подложку 2. Проекционная литография Шаблон находится на некотором расстоянии 3. Непосредственная генерация изображения на резисте (без шаблона) Фотолитография Рентгенолитография Электронолитография Ионолитография Фотошаблон Рентгеношаблон Электроношаблон Ионошаблон Фоторезист Рентгенорезист Электронорезист Ионорезист Контактная Проекционная без изменения масштаба Проекционная с уменьшением масштаба Непосредственное экспонирование Проекционная Непосредственное экспонирование 135
 Типы и свойства фоторезистов Фоторезист – это светочувствительные материалы, в которых под действием света изменяется растворимость, т. е. устойчивость к воздействию травителей. В качестве компонентов в состав фоторезистов входят: 1. Светочувствительные составляющие 2. Пленкообразующие составляющие 3. Растворители 136
Типы и свойства фоторезистов Фоторезист – это светочувствительные материалы, в которых под действием света изменяется растворимость, т. е. устойчивость к воздействию травителей. В качестве компонентов в состав фоторезистов входят: 1. Светочувствительные составляющие 2. Пленкообразующие составляющие 3. Растворители 136
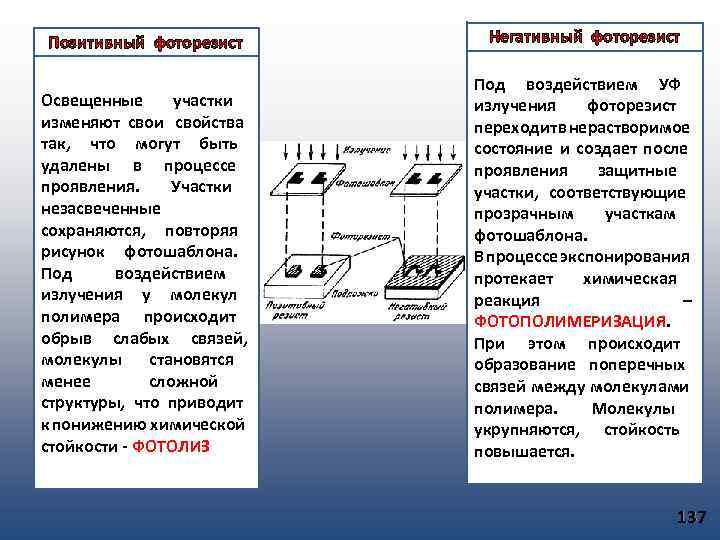 Позитивный фоторезист Негативный фоторезист Освещенные участки изменяют свои свойства так, что могут быть удалены в процессе проявления. Участки незасвеченные сохраняются, повторяя рисунок фотошаблона. Под воздействием излучения у молекул полимера происходит обрыв слабых связей, молекулы становятся менее сложной структуры, что приводит к понижению химической стойкости - ФОТОЛИЗ Под воздействием УФ излучения фоторезист переходит в нерастворимое состояние и создает после проявления защитные участки, соответствующие прозрачным участкам фотошаблона. В процессе экспонирования протекает химическая реакция – ФОТОПОЛИМЕРИЗАЦИЯ. При этом происходит образование поперечных связей между молекулами полимера. Молекулы укрупняются, стойкость повышается. 137
Позитивный фоторезист Негативный фоторезист Освещенные участки изменяют свои свойства так, что могут быть удалены в процессе проявления. Участки незасвеченные сохраняются, повторяя рисунок фотошаблона. Под воздействием излучения у молекул полимера происходит обрыв слабых связей, молекулы становятся менее сложной структуры, что приводит к понижению химической стойкости - ФОТОЛИЗ Под воздействием УФ излучения фоторезист переходит в нерастворимое состояние и создает после проявления защитные участки, соответствующие прозрачным участкам фотошаблона. В процессе экспонирования протекает химическая реакция – ФОТОПОЛИМЕРИЗАЦИЯ. При этом происходит образование поперечных связей между молекулами полимера. Молекулы укрупняются, стойкость повышается. 137
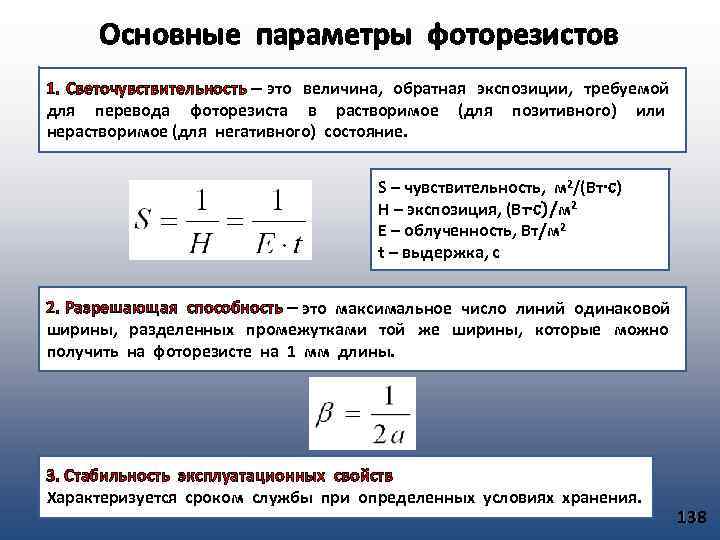 Основные параметры фоторезистов 1. Светочувствительность – это величина, обратная экспозиции, требуемой для перевода фоторезиста в растворимое (для позитивного) или нерастворимое (для негативного) состояние. S – чувствительность, м 2/(Вт·с) Н – экспозиция, (Вт·с)/м 2 Е – облученность, Вт/м 2 t – выдержка, с 2. Разрешающая способность – это максимальное число линий одинаковой ширины, разделенных промежутками той же ширины, которые можно получить на фоторезисте на 1 мм длины. 3. Стабильность эксплуатационных свойств Характеризуется сроком службы при определенных условиях хранения. 138
Основные параметры фоторезистов 1. Светочувствительность – это величина, обратная экспозиции, требуемой для перевода фоторезиста в растворимое (для позитивного) или нерастворимое (для негативного) состояние. S – чувствительность, м 2/(Вт·с) Н – экспозиция, (Вт·с)/м 2 Е – облученность, Вт/м 2 t – выдержка, с 2. Разрешающая способность – это максимальное число линий одинаковой ширины, разделенных промежутками той же ширины, которые можно получить на фоторезисте на 1 мм длины. 3. Стабильность эксплуатационных свойств Характеризуется сроком службы при определенных условиях хранения. 138
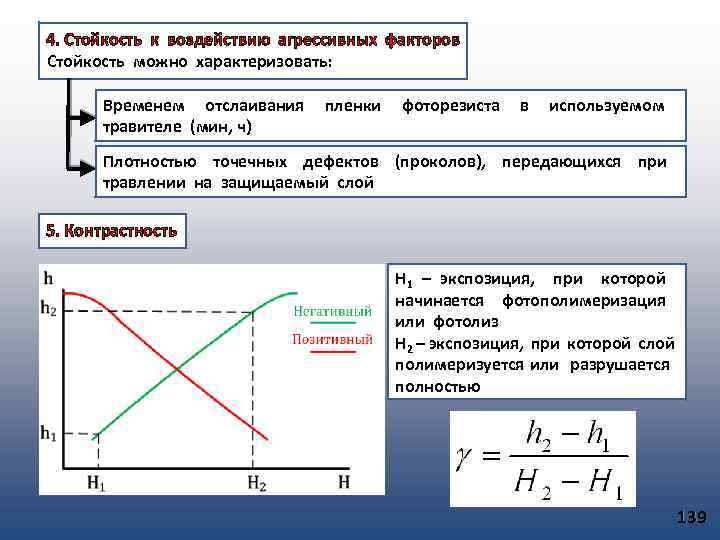 4. Стойкость к воздействию агрессивных факторов Стойкость можно характеризовать: Временем отслаивания пленки фоторезиста в используемом травителе (мин, ч) Плотностью точечных дефектов (проколов), передающихся при травлении на защищаемый слой 5. Контрастность Н 1 – экспозиция, при которой начинается фотополимеризация или фотолиз Н 2 – экспозиция, при которой слой полимеризуется или разрушается полностью 139
4. Стойкость к воздействию агрессивных факторов Стойкость можно характеризовать: Временем отслаивания пленки фоторезиста в используемом травителе (мин, ч) Плотностью точечных дефектов (проколов), передающихся при травлении на защищаемый слой 5. Контрастность Н 1 – экспозиция, при которой начинается фотополимеризация или фотолиз Н 2 – экспозиция, при которой слой полимеризуется или разрушается полностью 139
 Основные операции фотолитографии При изготовлении печатных плат применяется пленочный фоторезист. В общем случае он состоит из трех слоев, указанных на рисунке 140
Основные операции фотолитографии При изготовлении печатных плат применяется пленочный фоторезист. В общем случае он состоит из трех слоев, указанных на рисунке 140
 1. Подготовка поверхности заготовки фольгированного диэлектрика Подготовка заключается в проведении таких операций, как удаление окисного слоя с поверхности меди, обезжиривание поверхности, антикоррозийная обработка и т. д. 141
1. Подготовка поверхности заготовки фольгированного диэлектрика Подготовка заключается в проведении таких операций, как удаление окисного слоя с поверхности меди, обезжиривание поверхности, антикоррозийная обработка и т. д. 141
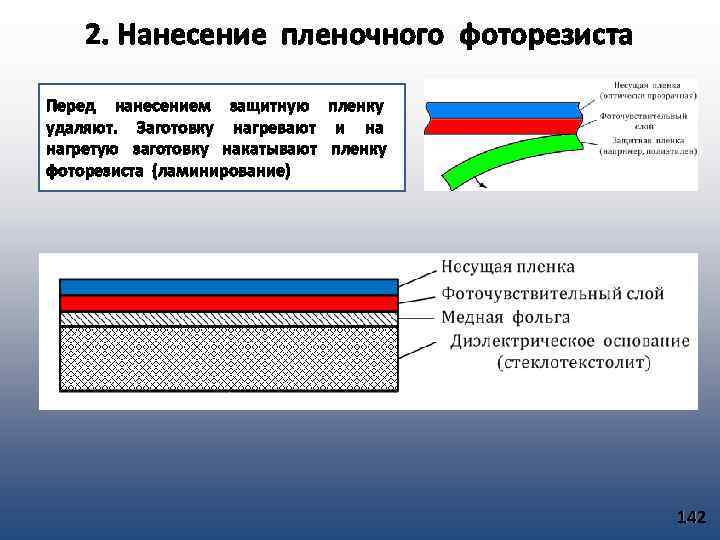 2. Нанесение пленочного фоторезиста Перед нанесением защитную пленку удаляют. Заготовку нагревают и нагретую заготовку накатывают пленку фоторезиста (ламинирование) 142
2. Нанесение пленочного фоторезиста Перед нанесением защитную пленку удаляют. Заготовку нагревают и нагретую заготовку накатывают пленку фоторезиста (ламинирование) 142
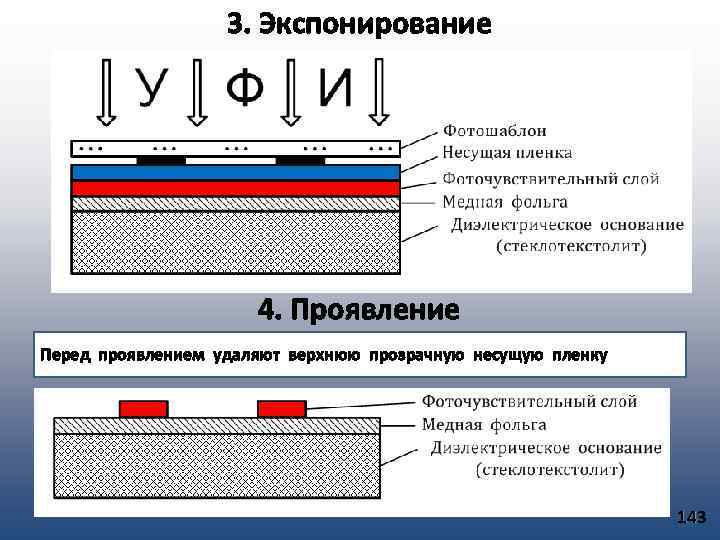 3. Экспонирование 4. Проявление Перед проявлением удаляют верхнюю прозрачную несущую пленку 143
3. Экспонирование 4. Проявление Перед проявлением удаляют верхнюю прозрачную несущую пленку 143
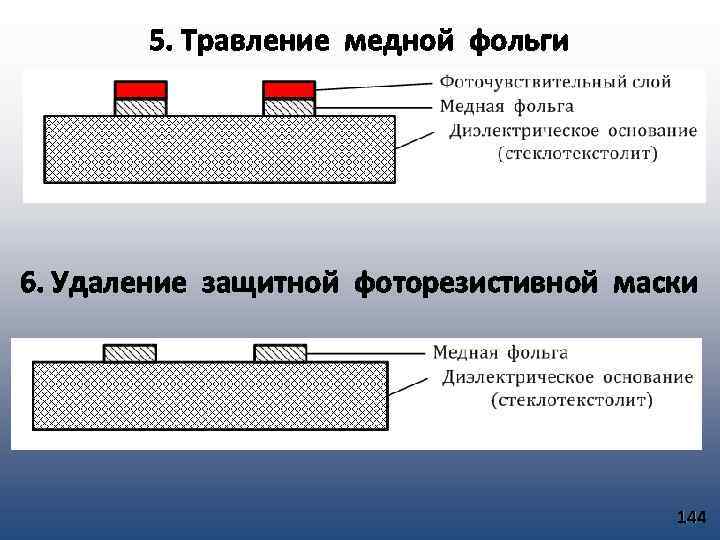 5. Травление медной фольги 6. Удаление защитной фоторезистивной маски 144
5. Травление медной фольги 6. Удаление защитной фоторезистивной маски 144


