Основы органической химии)))))))).pptx
- Количество слайдов: 70
 Тема 1 ОСНОВНЫЕ ПОНЯТИЯ ОРГАНИЧЕСКОЙ ХИМИИ
Тема 1 ОСНОВНЫЕ ПОНЯТИЯ ОРГАНИЧЕСКОЙ ХИМИИ
 • • • Типовые гетероатомы: Кислород О – кислородсодержащие органические соединения; Азот N – азотсодержащие органические соединения; Сера S – серосодержащие органические соединения; Галогены Hal=F, Cl, Br, I – галогенпроизводные; Фосфор P – фосфорсодержащие органические соединения; Некоторые металлы (Na, Mg, Cu, Ag).
• • • Типовые гетероатомы: Кислород О – кислородсодержащие органические соединения; Азот N – азотсодержащие органические соединения; Сера S – серосодержащие органические соединения; Галогены Hal=F, Cl, Br, I – галогенпроизводные; Фосфор P – фосфорсодержащие органические соединения; Некоторые металлы (Na, Mg, Cu, Ag).

 Виды химических формул Простейшая формула (эмпирическая формула) не обозначает реальных веществ, а только показывает соотношение числа атомов элементов в веществе. Эмпирической формуле СН отвечают несколько веществ: ацетилен С 2 Н 2, бензол С 6 Н 6, винилбензол С 8 Н 8. Молекулярная формула (или брутто-формула, истинная формула) отражает только качественный и количественный состав соединения. Н 2 О вода C 2 H 4 O 2 этановая кислота Ba. N 2 O 4 нитрит бария Рациональная формула. В рациональных формулах выделяются группы атомов, характерные для классов химических соединений. Н 2 О CH 3 СОOН Ba(NO 2)2 вода этановая кислота нитрит бария
Виды химических формул Простейшая формула (эмпирическая формула) не обозначает реальных веществ, а только показывает соотношение числа атомов элементов в веществе. Эмпирической формуле СН отвечают несколько веществ: ацетилен С 2 Н 2, бензол С 6 Н 6, винилбензол С 8 Н 8. Молекулярная формула (или брутто-формула, истинная формула) отражает только качественный и количественный состав соединения. Н 2 О вода C 2 H 4 O 2 этановая кислота Ba. N 2 O 4 нитрит бария Рациональная формула. В рациональных формулах выделяются группы атомов, характерные для классов химических соединений. Н 2 О CH 3 СОOН Ba(NO 2)2 вода этановая кислота нитрит бария
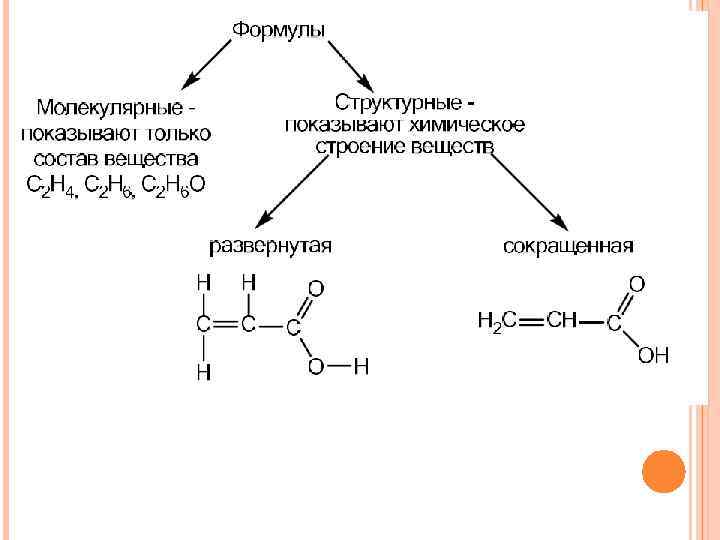
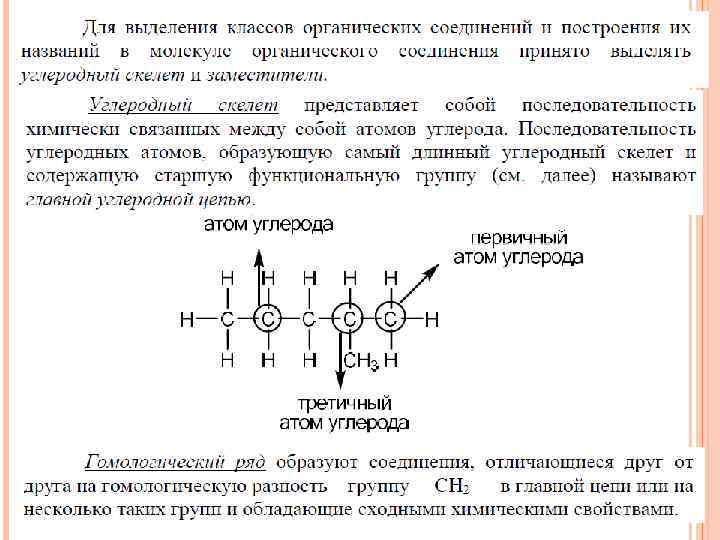
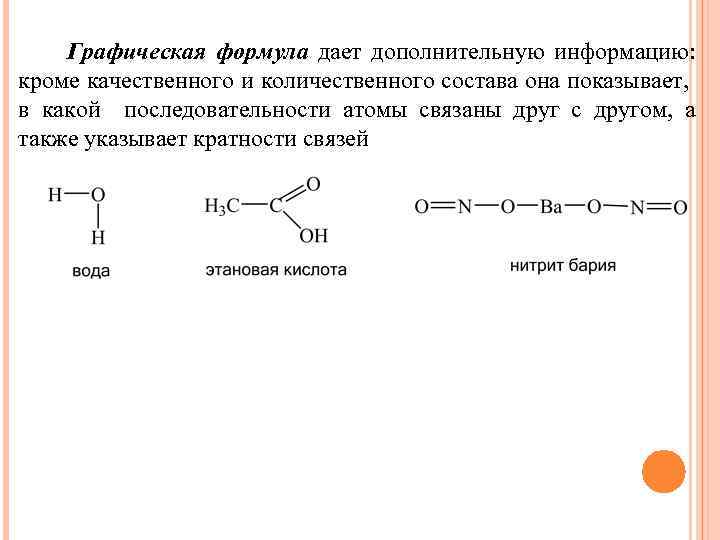 Графическая формула дает дополнительную информацию: кроме качественного и количественного состава она показывает, в какой последовательности атомы связаны друг с другом, а также указывает кратности связей
Графическая формула дает дополнительную информацию: кроме качественного и количественного состава она показывает, в какой последовательности атомы связаны друг с другом, а также указывает кратности связей
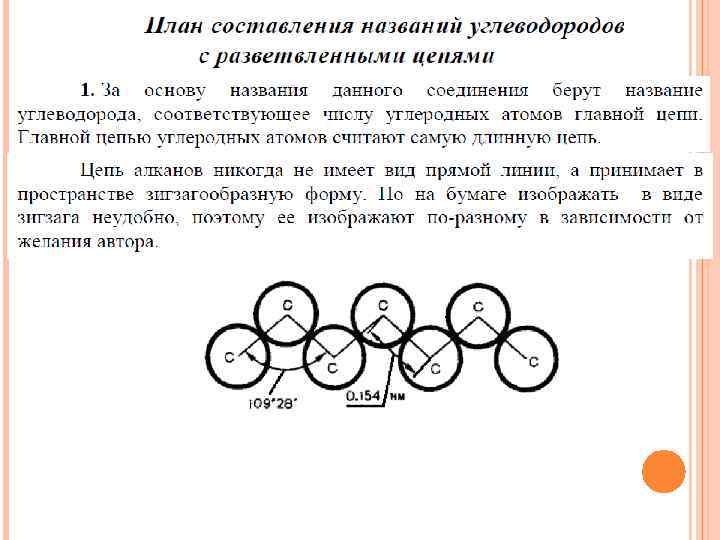
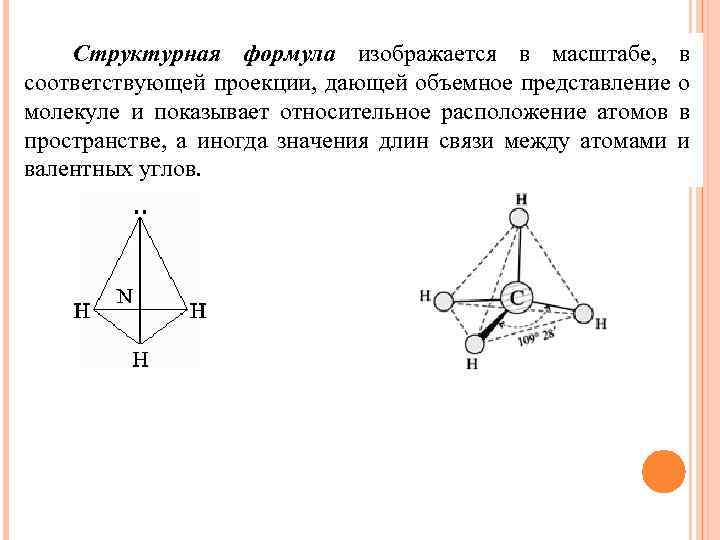 Структурная формула изображается в масштабе, в соответствующей проекции, дающей объемное представление о молекуле и показывает относительное расположение атомов в пространстве, а иногда значения длин связи между атомами и валентных углов.
Структурная формула изображается в масштабе, в соответствующей проекции, дающей объемное представление о молекуле и показывает относительное расположение атомов в пространстве, а иногда значения длин связи между атомами и валентных углов.
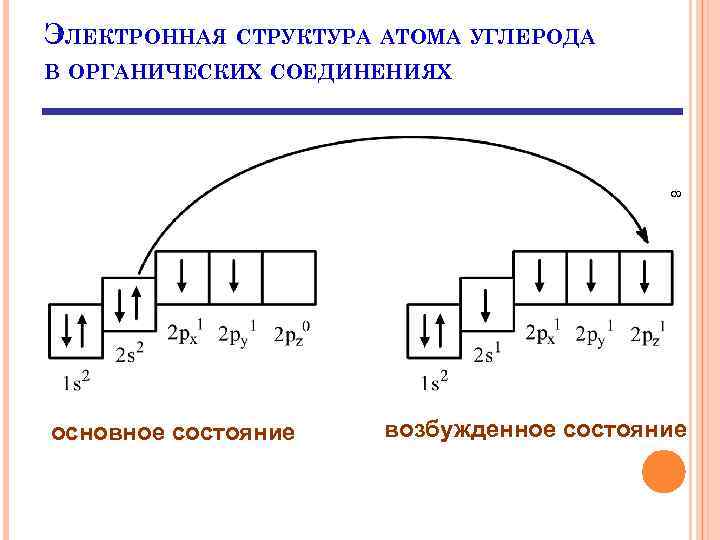 ЭЛЕКТРОННАЯ СТРУКТУРА АТОМА УГЛЕРОДА В ОРГАНИЧЕСКИХ СОЕДИНЕНИЯХ 8 основное состояние возбужденное состояние
ЭЛЕКТРОННАЯ СТРУКТУРА АТОМА УГЛЕРОДА В ОРГАНИЧЕСКИХ СОЕДИНЕНИЯХ 8 основное состояние возбужденное состояние


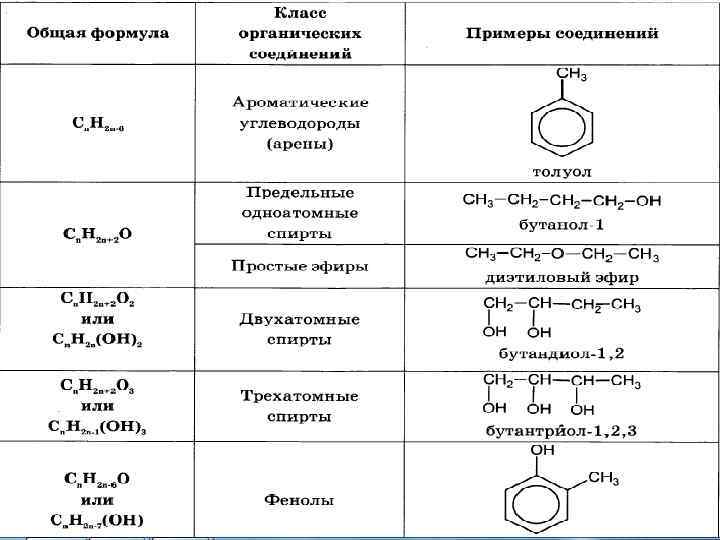
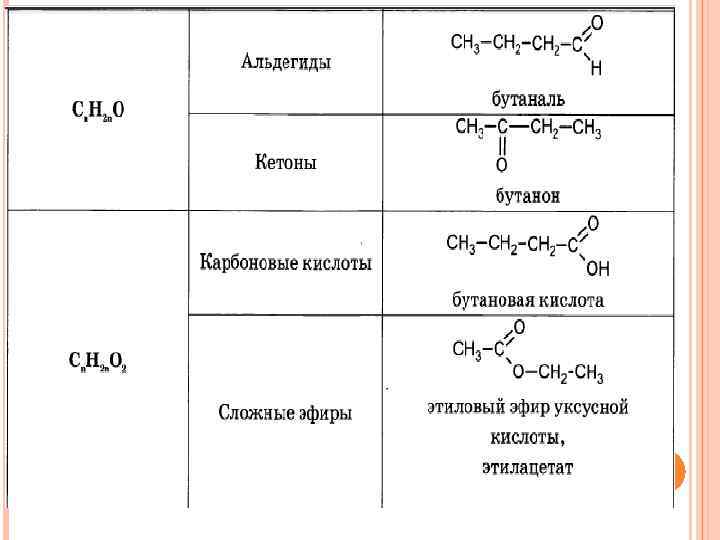
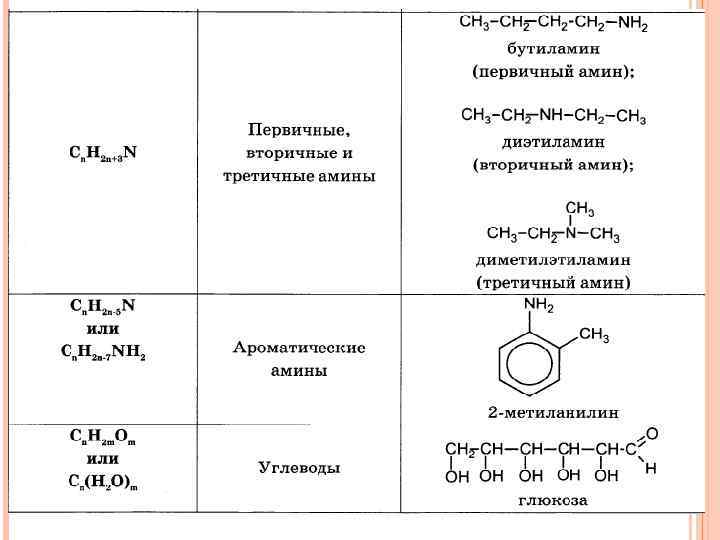
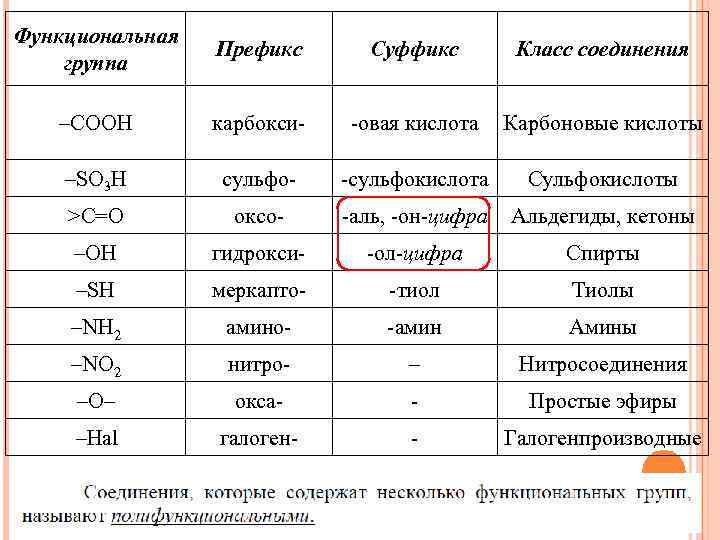 Функциональная группа Префикс Суффикс Класс соединения –СООН карбокси- -овая кислота Карбоновые кислоты –SO 3 H сульфо- -сульфокислота Сульфокислоты >С=О оксо- -аль, -он-цифра Альдегиды, кетоны –OH гидрокси- -ол-цифра Спирты –SH меркапто- -тиол Тиолы –NH 2 амино- -амин Амины –NO 2 нитро- – Нитросоединения –O– окса- - Простые эфиры –Hal галоген- - Галогенпроизводные
Функциональная группа Префикс Суффикс Класс соединения –СООН карбокси- -овая кислота Карбоновые кислоты –SO 3 H сульфо- -сульфокислота Сульфокислоты >С=О оксо- -аль, -он-цифра Альдегиды, кетоны –OH гидрокси- -ол-цифра Спирты –SH меркапто- -тиол Тиолы –NH 2 амино- -амин Амины –NO 2 нитро- – Нитросоединения –O– окса- - Простые эфиры –Hal галоген- - Галогенпроизводные
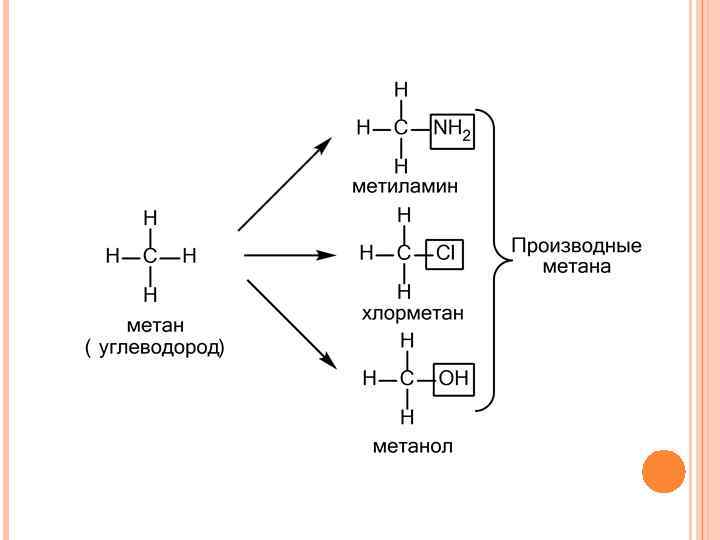
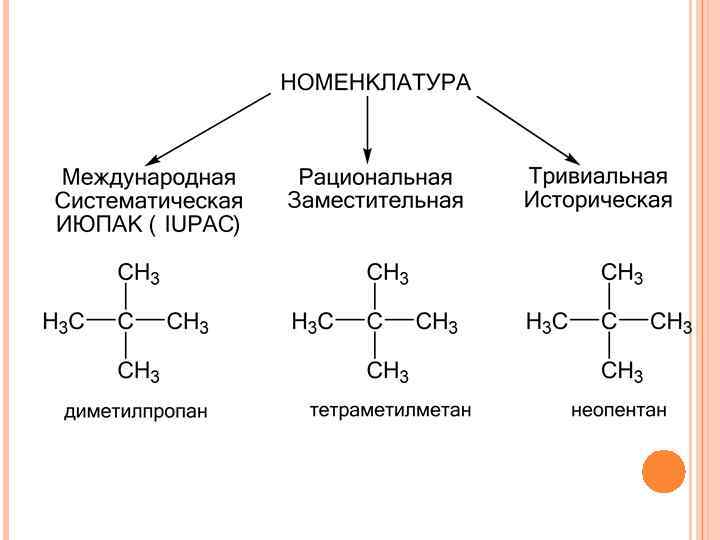
 Номенклатура ИЮПАК (IUPAC ) IUPAC - International Union of Pure and Applied Chemistry 19
Номенклатура ИЮПАК (IUPAC ) IUPAC - International Union of Pure and Applied Chemistry 19
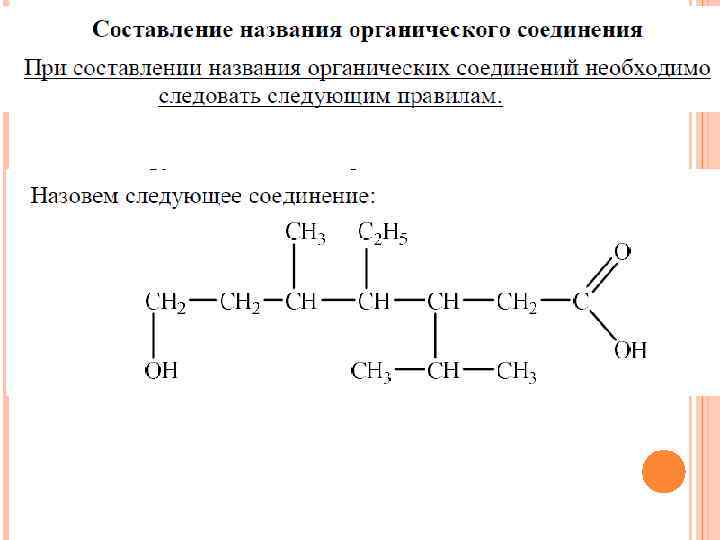


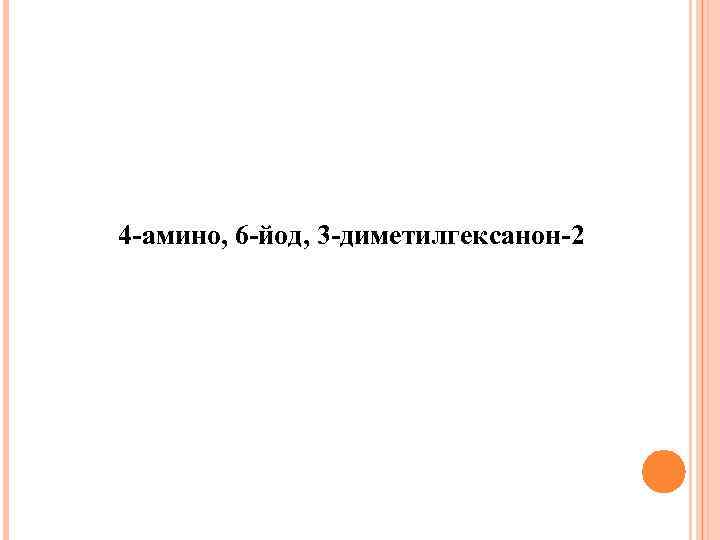 4 -амино, 6 -йод, 3 -диметилгексанон-2
4 -амино, 6 -йод, 3 -диметилгексанон-2



 КЛАССИФИКАЦИЯ РЕАКЦИЙ И РЕАГЕНТОВ В ОРГАНИЧЕСКОЙ ХИМИИ III. КЛАССИФИКАЦИЯ РЕАКЦИЙ ПО МЕХАНИЗМУ ЭЛЕМЕНТАРНЫХ СТАДИЙ Это наиболее сложный тип, классифицирующий реакции. Он соответствует двум предыдущим. По электронной природе По результату: реагента: 1. Замещение (S) 1. Электрофильные (Е+) 2. Присоединение (A) 2. Нуклеофильные (: Nu-) 3. Отщепление 3. Радикальные (R)
КЛАССИФИКАЦИЯ РЕАКЦИЙ И РЕАГЕНТОВ В ОРГАНИЧЕСКОЙ ХИМИИ III. КЛАССИФИКАЦИЯ РЕАКЦИЙ ПО МЕХАНИЗМУ ЭЛЕМЕНТАРНЫХ СТАДИЙ Это наиболее сложный тип, классифицирующий реакции. Он соответствует двум предыдущим. По электронной природе По результату: реагента: 1. Замещение (S) 1. Электрофильные (Е+) 2. Присоединение (A) 2. Нуклеофильные (: Nu-) 3. Отщепление 3. Радикальные (R)
 КЛАССИФИКАЦИЯ РЕАКЦИЙ И РЕАГЕНТОВ В ОРГАНИЧЕСКОЙ ХИМИИ Гомологический (радикальный) разрыв ковалентной связи: Из схемы видно, что при А: В А • + • В этом способе связывающая электронная пара делится радикалы пополам между партнерами связи. Гетеролитический (ионный) разрыв ковалентной связи: А: В При гетероциклическом взрыве А+ + (: В− ) связующая электронная пара целиком отходит к одному из партнеров, который приобретает ионы отрицательный заряд (-1).
КЛАССИФИКАЦИЯ РЕАКЦИЙ И РЕАГЕНТОВ В ОРГАНИЧЕСКОЙ ХИМИИ Гомологический (радикальный) разрыв ковалентной связи: Из схемы видно, что при А: В А • + • В этом способе связывающая электронная пара делится радикалы пополам между партнерами связи. Гетеролитический (ионный) разрыв ковалентной связи: А: В При гетероциклическом взрыве А+ + (: В− ) связующая электронная пара целиком отходит к одному из партнеров, который приобретает ионы отрицательный заряд (-1).
 КЛАССИФИКАЦИЯ РЕАКЦИЙ И РЕАГЕНТОВ В ОРГАНИЧЕСКОЙ ХИМИИ Реагенты, в органической химии, вступающие в реакцию, подразделяют на субстраты и реагенты. Какое из двух реагирующих веществ можно считать субстратом, а какое реагентом? Это соображение удобства. Обычно более сложное вещество называют субстратом (как правило, органическое вещество). Менее сложное – реактивом (неорганическое вещество). Если в реакции 2 органических вещества, то любое из них можно считать субстратом.
КЛАССИФИКАЦИЯ РЕАКЦИЙ И РЕАГЕНТОВ В ОРГАНИЧЕСКОЙ ХИМИИ Реагенты, в органической химии, вступающие в реакцию, подразделяют на субстраты и реагенты. Какое из двух реагирующих веществ можно считать субстратом, а какое реагентом? Это соображение удобства. Обычно более сложное вещество называют субстратом (как правило, органическое вещество). Менее сложное – реактивом (неорганическое вещество). Если в реакции 2 органических вещества, то любое из них можно считать субстратом.
 КЛАССИФИКАЦИЯ РЕАКЦИЙ И РЕАГЕНТОВ В ОРГАНИЧЕСКОЙ ХИМИИ IV. Классификация реакций по частным признакам. Реакции называют в честь реагента. Примеры: • Гидратация (реакция присоединения воды); • Гидрогалогенирование (реакция присоединения галогеноводорода); • Дегидратация (реакция отщепления воды); • Дегидрогалогенирование галогеноводорода) и др. (реакция отщепления
КЛАССИФИКАЦИЯ РЕАКЦИЙ И РЕАГЕНТОВ В ОРГАНИЧЕСКОЙ ХИМИИ IV. Классификация реакций по частным признакам. Реакции называют в честь реагента. Примеры: • Гидратация (реакция присоединения воды); • Гидрогалогенирование (реакция присоединения галогеноводорода); • Дегидратация (реакция отщепления воды); • Дегидрогалогенирование галогеноводорода) и др. (реакция отщепления
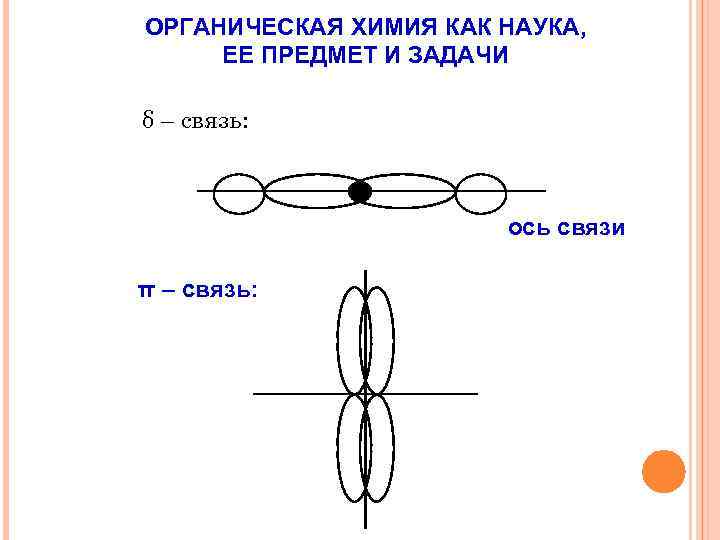 ОРГАНИЧЕСКАЯ ХИМИЯ КАК НАУКА, ЕЕ ПРЕДМЕТ И ЗАДАЧИ δ – связь: ось связи π – связь:
ОРГАНИЧЕСКАЯ ХИМИЯ КАК НАУКА, ЕЕ ПРЕДМЕТ И ЗАДАЧИ δ – связь: ось связи π – связь:


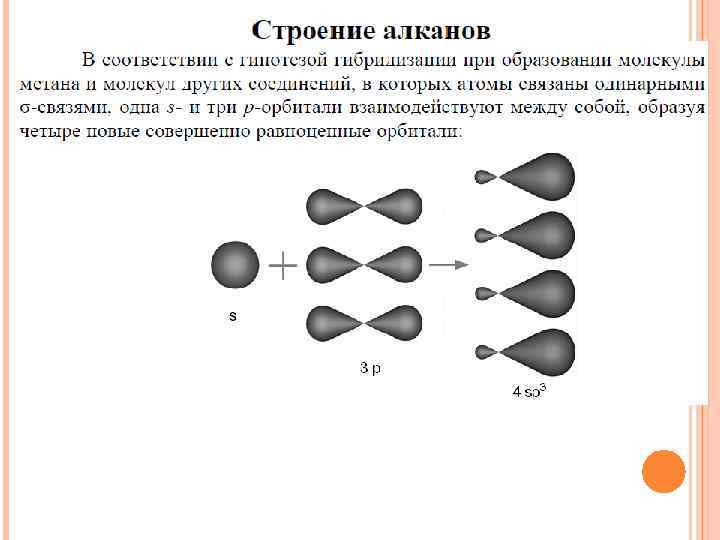
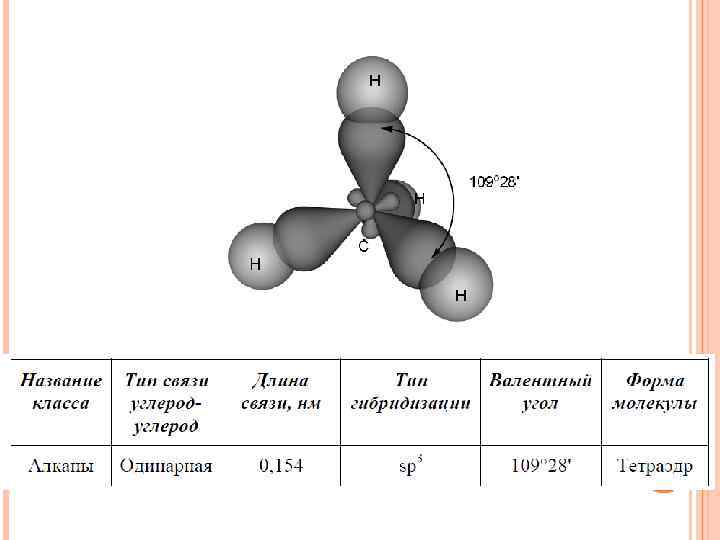
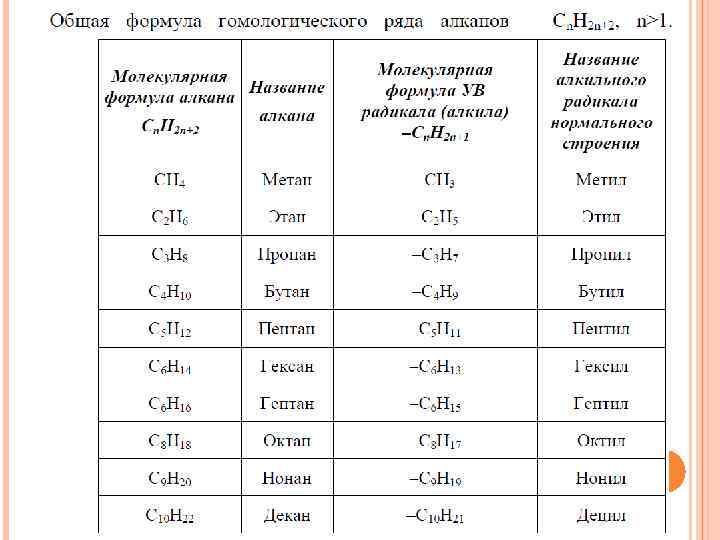
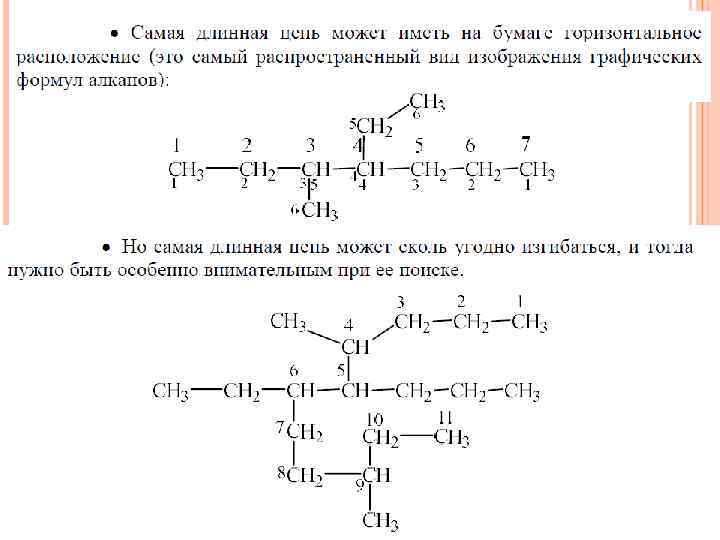



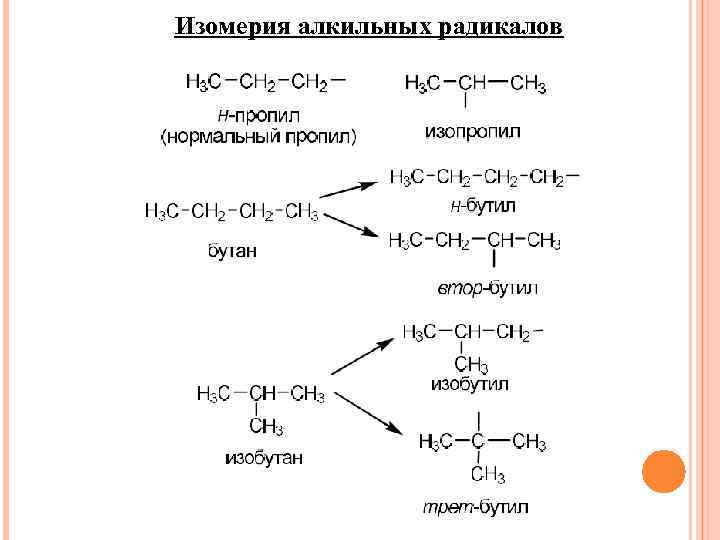 Изомерия алкильных радикалов
Изомерия алкильных радикалов
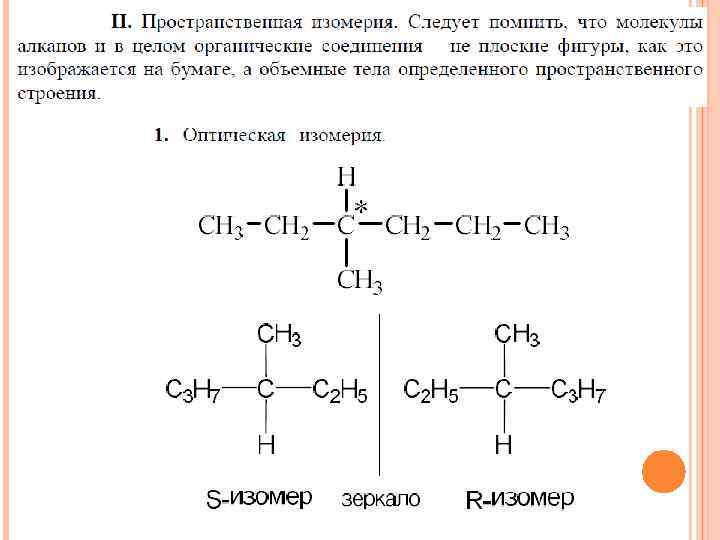
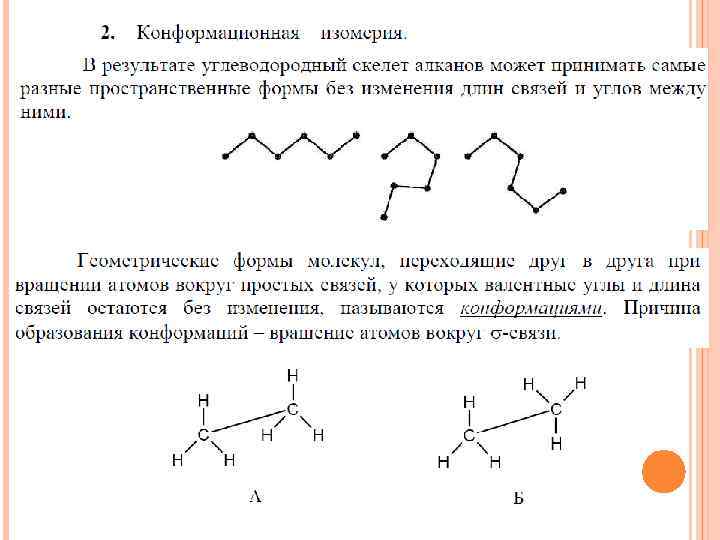

 Способы генерации радикалов 1. Высокая температура. 2. Действие излучением c энергией Е=hv.
Способы генерации радикалов 1. Высокая температура. 2. Действие излучением c энергией Е=hv.

 Устойчивость радикалов
Устойчивость радикалов










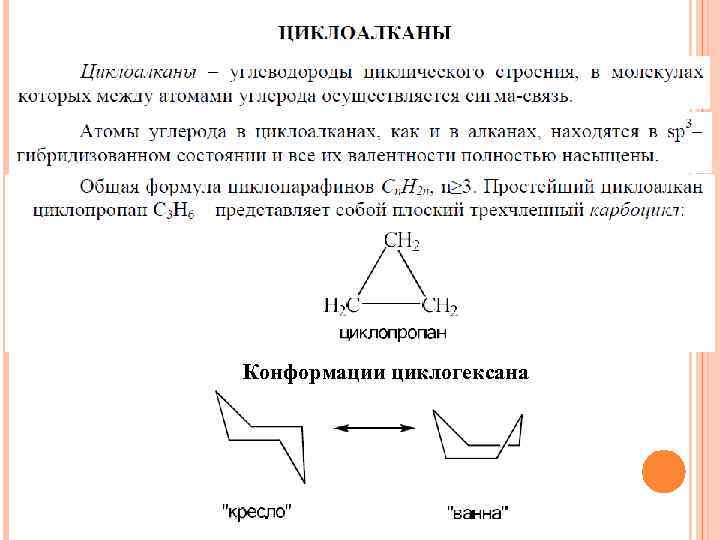 Конформации циклогексана
Конформации циклогексана