6 Кинетика.ppt
- Количество слайдов: 12
 Тема 1. 6. Химическая кинетика
Тема 1. 6. Химическая кинетика
 Химическая кинетика (ХК) – раздел физической химии, изучающий скорость и механизм протекания химических реакций, а также зависимость скорости протекания от различных факторов. Законы ХК используют в химической и металлургической промышленности с целью интенсификации производственных процессов.
Химическая кинетика (ХК) – раздел физической химии, изучающий скорость и механизм протекания химических реакций, а также зависимость скорости протекания от различных факторов. Законы ХК используют в химической и металлургической промышленности с целью интенсификации производственных процессов.
 Скорость химической реакции О скорости химических реакций судят по изменению концентрации реагирующих веществ (продуктов реакции) в единицу времени. В начальный момент концентрации исходных веществ и скорость реакции наибольшие; к концу реакции скорость становится малой, поскольку основные массы веществ уже прореагировали.
Скорость химической реакции О скорости химических реакций судят по изменению концентрации реагирующих веществ (продуктов реакции) в единицу времени. В начальный момент концентрации исходных веществ и скорость реакции наибольшие; к концу реакции скорость становится малой, поскольку основные массы веществ уже прореагировали.
 Средняя скорость реакции В момент времени τ1 концентрация вещества составляет С 1, а в момент τ2 она стала С 2. Средняя скорость реакции для отрезка времени τ2 – τ1 будет равна: υ = ±(C 2 – C 1)/ (τ2 – τ1) Знак «- « пишут в том случае, когда концентрация вещества во времени уменьшается, знак «+» если она увеличивается. Скорость всегда положительна.
Средняя скорость реакции В момент времени τ1 концентрация вещества составляет С 1, а в момент τ2 она стала С 2. Средняя скорость реакции для отрезка времени τ2 – τ1 будет равна: υ = ±(C 2 – C 1)/ (τ2 – τ1) Знак «- « пишут в том случае, когда концентрация вещества во времени уменьшается, знак «+» если она увеличивается. Скорость всегда положительна.
 Истинная скорость реакции Если τ2 – τ1 сделать малой величиной, то и изменение концентрации будет мало: τ2 – τ1 = Δτ и C 2 – C 1 = ΔС. является истинной скоростью химической реакции, т. е. скоростью в данный момент времени: υист = ±d. C/dτ Истинная скорость химической реакции есть первая производная концентрации по времени.
Истинная скорость реакции Если τ2 – τ1 сделать малой величиной, то и изменение концентрации будет мало: τ2 – τ1 = Δτ и C 2 – C 1 = ΔС. является истинной скоростью химической реакции, т. е. скоростью в данный момент времени: υист = ±d. C/dτ Истинная скорость химической реакции есть первая производная концентрации по времени.
 Факторы, влияющие на скорость химических реакций • концентрации реагирующих веществ; • природа реагирующих веществ; • температура и природа растворителя (для реакций в растворах); • присутствие катализаторов; • скорость и давление (для газовых реакций).
Факторы, влияющие на скорость химических реакций • концентрации реагирующих веществ; • природа реагирующих веществ; • температура и природа растворителя (для реакций в растворах); • присутствие катализаторов; • скорость и давление (для газовых реакций).
 Закон действующих масс Скорость химической реакции при постоянной температуре прямо пропорциональна произведению молярных концентраций реагирующих веществ, взятых в степени, равной стехиометрическому коэффициенту соответствующего вещества в уравнении реакции. Для реакции: n 1 A + n 2 B + n 3 C → n 1´D + n 2´E + n 3´F Если реагируют газы, вместо концентраций учитывают величины парциальных давлений.
Закон действующих масс Скорость химической реакции при постоянной температуре прямо пропорциональна произведению молярных концентраций реагирующих веществ, взятых в степени, равной стехиометрическому коэффициенту соответствующего вещества в уравнении реакции. Для реакции: n 1 A + n 2 B + n 3 C → n 1´D + n 2´E + n 3´F Если реагируют газы, вместо концентраций учитывают величины парциальных давлений.
 Константа скорости химической реакции Константа скорости k – это такая скорость, когда концентрации реагирующих веществ равны 1 моль/л. Она зависит от природы реагирующих веществ и температуры, но не зависит от изменения концентрации участвующих в реакции веществ. Чем больше константа скорости реакции, тем больше ее скорость по сравнению с другими реакциями прочих равных условиях.
Константа скорости химической реакции Константа скорости k – это такая скорость, когда концентрации реагирующих веществ равны 1 моль/л. Она зависит от природы реагирующих веществ и температуры, но не зависит от изменения концентрации участвующих в реакции веществ. Чем больше константа скорости реакции, тем больше ее скорость по сравнению с другими реакциями прочих равных условиях.
 Правило Вант-Гоффа При повышении температуры на 100 (при P = const) cкорость реакции увеличивается в 2 – 4 раза. Отношение kt+10/k = γ называют температурным коэффициентом реакции, где kt+10 – константа скорости при температуре t+10, kt константа скорости при температуре t. Используют для ориентировочного подсчета изменения скорости химической реакции: или
Правило Вант-Гоффа При повышении температуры на 100 (при P = const) cкорость реакции увеличивается в 2 – 4 раза. Отношение kt+10/k = γ называют температурным коэффициентом реакции, где kt+10 – константа скорости при температуре t+10, kt константа скорости при температуре t. Используют для ориентировочного подсчета изменения скорости химической реакции: или
 Классификация химических реакций Изучаемые кинетикой химические реакции классифицируют: • по молекулярности – т. е. по числу частиц, принимающих участие в отдельном элементарном акте реакции; • по порядку уравнения для скорости реакции, т. е. по порядку реакции.
Классификация химических реакций Изучаемые кинетикой химические реакции классифицируют: • по молекулярности – т. е. по числу частиц, принимающих участие в отдельном элементарном акте реакции; • по порядку уравнения для скорости реакции, т. е. по порядку реакции.
 Cхема реакции Одномолекулярная A → B + C + D Двухмолекулярная 2 A → E + F +… A + B → M + N +… Трехмолекулярные (очень редки) 3 A → C + E +… 2 A + B → F + D +… A + B + R →G + M +… Примеры Реакции внутримолекулярных перегруппировок, разложения, радиоактивный распад элементов, диффузия газов I 2 = I + I N 2 O = N 2 + O 2 HI ↔ H 2 + I 2 CH 3 I + C 2 H 5 ONa ↔ CH 3 OC 2 H 5 + Na. I 2 NO + O 2 ↔ 2 NO 2 2 Fe. Cl 3 + Sn. Cl 2 ↔ 2 Fe. Cl 2 + Sn. Cl 4
Cхема реакции Одномолекулярная A → B + C + D Двухмолекулярная 2 A → E + F +… A + B → M + N +… Трехмолекулярные (очень редки) 3 A → C + E +… 2 A + B → F + D +… A + B + R →G + M +… Примеры Реакции внутримолекулярных перегруппировок, разложения, радиоактивный распад элементов, диффузия газов I 2 = I + I N 2 O = N 2 + O 2 HI ↔ H 2 + I 2 CH 3 I + C 2 H 5 ONa ↔ CH 3 OC 2 H 5 + Na. I 2 NO + O 2 ↔ 2 NO 2 2 Fe. Cl 3 + Sn. Cl 2 ↔ 2 Fe. Cl 2 + Sn. Cl 4
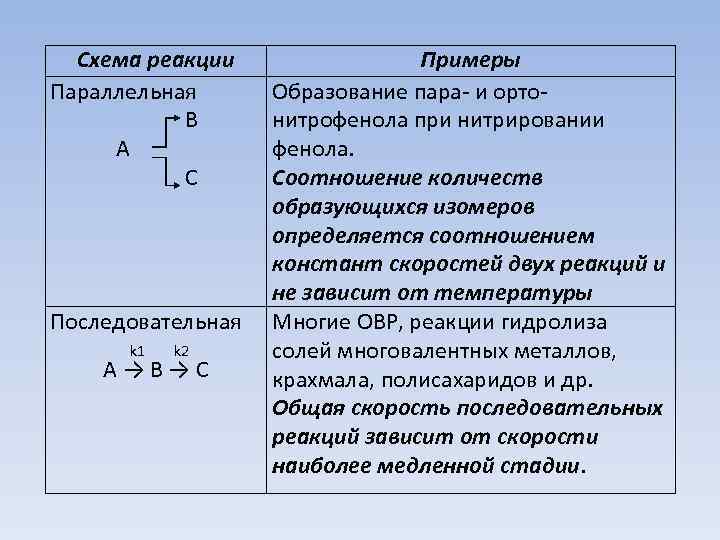 Cхема реакции Параллельная B A C Последовательная k 1 k 2 A → B → C Примеры Образование пара- и ортонитрофенола при нитрировании фенола. Соотношение количеств образующихся изомеров определяется соотношением констант скоростей двух реакций и не зависит от температуры Многие ОВР, реакции гидролиза солей многовалентных металлов, крахмала, полисахаридов и др. Общая скорость последовательных реакций зависит от скорости наиболее медленной стадии.
Cхема реакции Параллельная B A C Последовательная k 1 k 2 A → B → C Примеры Образование пара- и ортонитрофенола при нитрировании фенола. Соотношение количеств образующихся изомеров определяется соотношением констант скоростей двух реакций и не зависит от температуры Многие ОВР, реакции гидролиза солей многовалентных металлов, крахмала, полисахаридов и др. Общая скорость последовательных реакций зависит от скорости наиболее медленной стадии.


