Ведение беременность после ИВФ.ppt
- Количество слайдов: 28

ТАКТИКА ВЕДЕНИЯ БЕРЕМЕННОСТИ ПОСЛЕ IVF КАФЕДРА АКУШЕРСТВА И ГИНЕКОЛОГИИ № 1

Особенности течения беременности после IVF • тенденция к невынашиванию • многоплодная беременность • повышенный риск ВПР (врожденных пороков развития) плода • высокая вероятность развития плацентарной дисфункции и гестоза • изменения в системе гемостаза • высокий инфекционный индекс

Течение и исход беременности после IVF в 1 триместре зависят от причины бесплодия При трубно-перитонеальном бесплодии беременность с первой попытки наступает в среднем в 1/3 наблюдений, а у 50% пациенток со 2– 4 -й попытки. Беременность протекает без осложнений более чем у 1/3 женщин. Среди осложнений в I и II триместре чаще всего имеет место угрожающий аборт (более 40%). У большинства женщин (до 90%) беременность заканчивается своевременными родами. При эндокринном бесплодии в 50% наблюдений беременность наступает только со 2– 4 -й попытки, в 1/3 наблюдений – с 5– 7 -й попытки. Беременность протекает без осложнений и заканчивается своевременными родами только у каждой пятой пациентки. При выполнении ЭКО по поводу мужского фактора бесплодия, наступление беременности с первой попытки происходит в 2/3 наблюдений. Своевременные роды происходят у 3/4 женщин этой группы.

Частота угрозы прерывания беременности после ЭКО составляет 30– 70% самопроизвольные преждевременные роды аборты 19, 4 - 37, 6% 18 - 44%

Предрасполагающие факторы повышения частоты невынашивания беременности после применения ЭКО: • применение препаратов – индукторов суперовуляции, которые создают предпосылки для прерывания беременности наряду с высоким уровнем содержания фолликулостимулирующего гормона; • изменение гормонального фона в результате проведения мероприятий, направленных на созревание фолликулов, гиперстимуляция яичников; • агрессивный способ получения гамет, временное пребывание гамет и эмбрионов вне организма женщины, микроманипуляции с ними, перенос эмбрионов в матку; • многоплодие; • иммуногенетические факторы: • наличие антител (АТ) к хорионическому гонадотропину человека (ХГЧ); • антифосфолипидный синдром (АФС); • несовместимость по системе HLA; • «малые формы» хромосомных нарушений у супругов вследствие их полиморфизма; • эндокринные нарушения, сопровождающиеся недостаточностью желтого тела; • инфекционно-воспалительные факторы.
наступает и развивается на фоне высокого уровня эстрогенов и при относительно низком уровне прогестерона. Возникающая гиперэстрогения, которая является следствием стимуляции яичников, нарушает секреторную трансформацию эндометрия, создает неблагоприятный фон для процессов инвазии цитотрофобласта, ангиогенеза, васкулогенеза повышает риск невынашивания у пациенток после ЭКО.
Массивная гормональная терапия, направленная сначала на стимуляцию фолликулогенеза, а затем на поддержку желтого тела беременности и продолжающаяся до 14 – 16 недель, может приводить к нарушению системы гемостаза, особенно у первобеременных. Возникают изменения в плазменном звене системы гемостаза по типу гиперкоагуляции наряду с повышением агрегации.
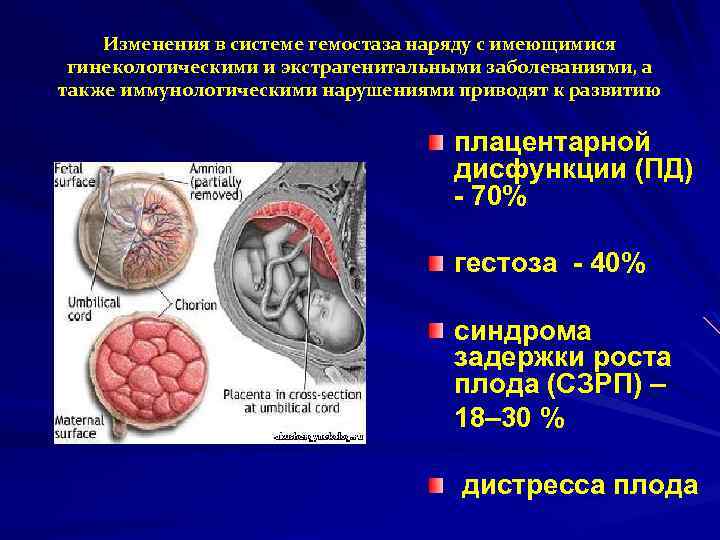
Изменения в системе гемостаза наряду с имеющимися гинекологическими и экстрагенитальными заболеваниями, а также иммунологическими нарушениями приводят к развитию плацентарной дисфункции (ПД) - 70% гестоза - 40% синдрома задержки роста плода (СЗРП) – 18– 30 % дистресса плода
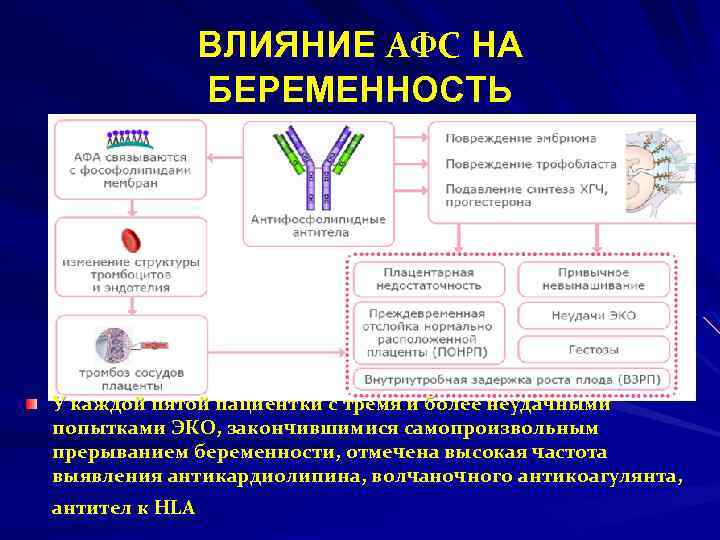
ВЛИЯНИЕ АФС НА БЕРЕМЕННОСТЬ У каждой пятой пациентки с тремя и более неудачными попытками ЭКО, закончившимися самопроизвольным прерыванием беременности, отмечена высокая частота выявления антикардиолипина, волчаночного антикоагулянта, антител к HLA

Особенности ведения беременных после применения ЭКО Поддержка беременности, наступившей в результате ЭКО, начинается с самых ранних сроков, сразу после переноса эмбрионов в матку женщины. Мероприятия, проводимые с целью сохранения беременности, наступившей после ЭКО, значительно более «агрессивны» , чем общепринятые. В частности, это касается более высоких доз эстрогенных и гестагенных препаратов. Ведение беременных после применения ЭКО требует более пристального внимания врача.
РЕКОМЕНДУЕМЫЕ СРОКИ ВИЗИТОВ БЕРЕМЕННОЙ К ВРАЧУ до 9 недели) Первый визит – до 12 недель (желательно Второй визит – не позднее 2 – х недель после первого Третий визит – 19 – 21 неделя Четвертый визит – 25 – 26 недель Пятый визит – 30 недель Шестой визит – 34 – 35 недель Седьмой визит – 37 недель 37 – 38 недель – госпитализация в стационар для подготовки к родоразрешению

ОСНОВНЫЕ ДИАГНОСТИЧЕСКИЕ МЕРОПРИЯТИЯ Первый визит • стандартное обследование беременной, согласно приказу МОЗ Украины № 417 от 15. 07. 2011 г. • определение содержания прогестерона, эстрадиола в крови, определение коэффициента прогестерон/эстрадиол • исследование параметров системы гемостаза, включая маркёры активации внутрисосудистого тромбогенеза • определение уровня гомоцистеина • диагностика антифосфолипидного синдрома • первый УЗИ скрининг + двойной биохимический тест (свободный β – ХГЧ + РАРР – А) Второй визит • стандартное обследование беременной, согласно приказу МОЗ Украины № 417 от 15. 07. 2011 г. • определение содержания прогестерона, эстрадиола в крови, определение коэффициента прогестерон/эстрадиол

ОСНОВНЫЕ ДИАГНОСТИЧЕСКИЕ МЕРОПРИЯТИЯ Третий визит • стандартное обследование беременной, согласно приказу МОЗ Украины № 417 от 15. 07. 2011 г. • определение содержания прогестерона, эстрадиола в крови, определение коэффициента прогестерон /эстрадиол • второй УЗИ скрининг + тройной биохимический тест (АФП + свободный β – ХГЧ + свободный эстриол) • исследование параметров системы гемостаза, определение уровня гомоцистеинемии по показаниям, при назначении соответствующей терапии Четвертый, пятый, шестой, • стандартное обследование беременной, согласно приказу МОЗ Украины № 417 от 15. 07. 2011 г. • исследование параметров системы гемостаза, определение уровня гомоцистеинемии по показаниям, при назначении соответствующей

НЕОБХОДИМЫЙ КОМПЛЕКС ОБСЛЕДОВАНИЯ БЕРЕМЕННЫХ ПОСЛЕ IVF ДИАГНОСТИКА АНТИФОСФОЛИПИДНОГО СИНДРОМА - Антикардлиолипиновые антитела класса Ig G и Ig M, - Антитела к β 2 гликопротеину – 1 класса Ig G и Ig M, - Волчаночный антикоагулянт ОПРЕДЕЛЕНИЕ УРОВНЯ ГОМОЦИСТЕИНА ИССЛЕДОВАНИЕ СИСТЕМЫ ГЕМОСТАЗА - Агрегация тромоцитов, - Активность Д - Димера, - Система фибринолиза

Контроль за течением беременности женщин с гиперандрогенией ( определение надпочечниковых фракций андрогенов: дегидроэпиандростерона сульфат (ДГЭА-с), 17 -гидроксипрогестерон (17 -ОП) в крови) должен проводиться с учетом критических периодов беременности, характерных для данной патологии: 13 нед (выброс тестостерона яичниками плода мужского пола), 20– 24 нед (начало гормональной продукции коркового вещества надпочечников), 28 нед (выброс АКТГ гипофизом плода).

При ведении беременных после ЭКО необходим дифференцированный подход с учетом этиологического фактора бесплодия, причем особое внимание следует уделять 1 триместру беременности, который характеризуется наибольшей частотой осложнений и репродуктивных потерь

ЛЕЧЕБНО – РЕАБИЛИТАЦИОННЫЕ МЕРОПРИЯТИЯ С целью воздействия на эндокринные причины невынашивания все беременные после ЭКО получают гормональную поддержку. Решение вопроса о назначении определённых доз гормонов и длительности терапии определяется исходным гормональным профилем женщины, особенностями модулированного фолликулогенеза, количеством фолликулов, количеством жёлтых тел. Рекомендуют применение: препаратов натурального прогестерона (прогестерон в/м по 1– 2 мл ежедневно или микронизированный прогестерон (Утрожестан) по 300– 400 мг с постепенным снижением дозы при отсутствии признаков угрозы прерывания к 12– 14 нед); аналогов (изомеров) прогестерона (дидрогестерон по 10– 30 мг до 16 нед). Беременным с селективной редукцией эмбрионов рекомендовано проведение поддерживающей терапии прогестинами до 18 – 20 недели беременности с одновременным определением концентрации прогестерона и эстрадиола в крови.

Функция эндогенного прогестерона секреторная трансформация эндометрия, необходимая для внедрения бластоцисты рост, развитие и васкуляризация миометрия во время беременности снижение сократительной активности миометрия закрытие цервикального канала модуляция иммунной системы матери (продукция PIBF – Прогестерониндуцированного блокирующего фактора )

Назначение эстрогенов (при наличии информированного согласия женщины) показано: при гипофункции яичников, донации яйцеклетки, замедленных темпах роста эндометрия, чистой формы дисгенезии гонад, внутриматочных синехиях. Фоликуллин по 2 – 5 тыс. МЕ (не более 10 тыс. МЕ) в/м ежедневно Их применение оправдано до 12– 15 нед беременности
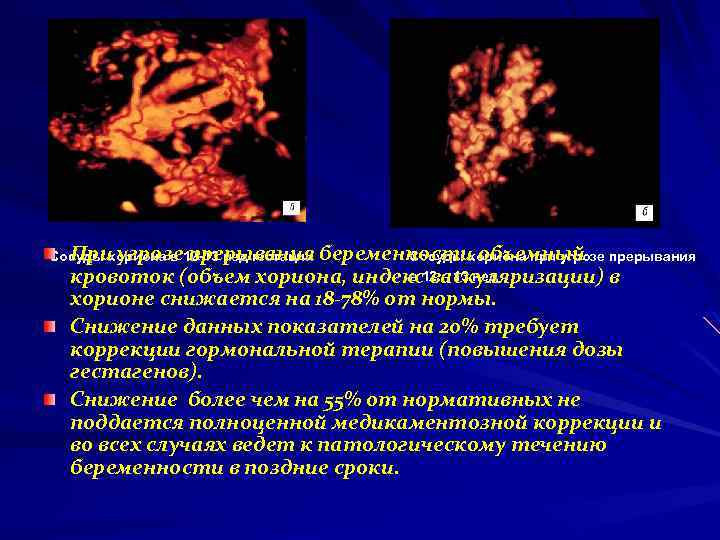
При угрозе прерывания Сосуды хориона в 12 -13 нед гестации беременности объемный Сосуды хориона при угрозе прерывания в васкуляризации) в кровоток (объем хориона, индекс12 – 13 нед хорионе снижается на 18 -78% от нормы. Снижение данных показателей на 20% требует коррекции гормональной терапии (повышения дозы гестагенов). Снижение более чем на 55% от нормативных не поддается полноценной медикаментозной коррекции и во всех случаях ведет к патологическому течению беременности в поздние сроки.

ПАТОГЕНЕТИЧЕСКАЯ КОРРЕКЦИЯ ТРОМБОФИЛИЧЕСКИХ НАРУШЕНИЙ Фолиевая кислота 4 – 8 мг в сутки на протяжении всей беременности Нейровитан (В 1 25 мг, В 2 2, 5 мг, В 6 40 мг, В 12 0, 25 мг) 1 таб x 3 р/сутки на протяжении всей беременности Курантил (дипиридамол) по 25 мг x 3 р/сутки 21 день Сулодексид 600 LSO/ 2 мл в/м 1 р/сутки 10 – 15 дней, далее per os по 1 капсуле (250 LSO) 2 р/сутки на протяжении всей беременности Глутаргин 0, 75 (1 таб) x 3 р/сутки курсами по 10 – 15 дней Магне В 6 по 1 таб x 3 р/сутки 21 день

Фолиевая кислота – снижение уровня гомоцистеина в крови Нейровитан – снижение уровня гомоцистеина в крови Аспирин – активирует синтез эндотелием простациклина, индуктор интерлейкина 3 и активный фактор роста трофобласта Сулодексид - антиагрегантная, антикоагулянтная, фибринолитическая, антитромботическая и эндотелийпротектерная активность Глутаргин - эндотелийпротекторное действие, нормализует нарушенную проницаемость и тромборезистентность сосудов, предотвращает гиперкоагуляцию, снижает чувствительность сосудов к сосудосуживающим агентам Дипиридамол - потенцирует антиагрегантное действие простациклина, индуцирует биосинтез интерферона, улучшает плацентарный кровоток, активизирует ангиогенез Магне В 6 – эндотелиомодулирующее действие

При гиперкоагуляции и / или активации внутрисосудистого свертывания крови (повышение концентрации Д – Димер, растворимых фибрин – мономерных единиц комплексов (РФМК) – антикоагулянтная терапия - Низкомолекулярные гепарины – Цибор 2500 ЕД (вес женщины < 70 кг) } п/к 1 раз/день 3500 ЕД (вес женщины > 70 кг) Аспирин 75 мг в сутки на протяжении всей беременности

Контроль параметров свертывания крови у пациенток с тромбофилическими нарушениями необходимо проводить каждые 2 – 3 недели в зависимости от тяжести нарушения свертывания крови

ПРОФИЛАКТИКА ПЛАЦЕНТАРНОЙ ДИСФУНКЦИИ Актовегин 0, 2 x 2 раза в день 14 – 21 день, в 16, 24, 32 недели беременности Витамин Е внутрь 1 раз в день по 200 мг в течение 10– 14 дней Аскорбиновая кислота внутрь по 0, 1– 0, 3 г 3 раза в день или в/в с глюкозой по 5 мл в течение 10– 14 дней Эссенциале форте внутрь по 2 капсулы 3 раза в день во время еды в течение 4 нед Фолиевая кислота по 400 мкг в день

В тактике ведения беременности после ВРТ отчетливо прослеживается тенденция, которую можно обозначить как приоритет сохранения беременности перед соображениями осторожности в отношении здоровья потомства.

С позиций перинатологии эффективность ЭКО следует оценивать не по частоте наступления беременности, а по показателю «take home baby» , который наиболее ясно отражает частоту рождения здоровых детей

СПАСИБО ЗА ВНИМАНИЕ!
Ведение беременность после ИВФ.ppt