Лекция рак и пр. 14 апреля.ppt
- Количество слайдов: 32

Тактика генной терапии онкологических заболеваний. Е. В. Парфенова ФГУ РКНПК МЗ СР РФ

ГЕННАЯ ТЕРАПИЯ – лечение болезней путем введения ДНК или РНК специфических генов в клетки организма Стратегии генной терапии Цель Усиление продукции терапевтического белка Подавление продукции патогенного белка Механизм Экспрессия с помощью вектора (плазмиды, вирусы Подавление экспрессии, например, с помощью АСОН, ми. РНК, РНК рибозимы, доминант негативных мутантных белков. Примеры Тер. ангиогенез (Увеличение количества Сосудов) Опухоли (Р 53 заместительная терапия Рестенозы, опухоли (Подавление пролиферации)

Генная терапия опухолейвведение В 2005 году в США 1 372 910 человек заболели раком и 570280 умерли от рака. 5 -летняя выживаемость – 15% при эпителиальных формах рака. Причина – неэффективное лечение метастазов. Для эффективного лечения требуется: 1. Системная доставка лекарства 2. Доставка в раковые клетки и аккумуляция в них. 3. Селективное убийство раковых клеток при отсутствии токсического влияния на нормальные клетки. Ни одно лекарство или метод лечения рака не обеспечивает этих условий.

Клинические протоколы по генной терапии

Основные методологические подходы к генной терапии онкологических заболеваний Вводимые гены Принцип 1. Повышение иммунореактивности опухоли. 2. Cелективные по репликации онколитические аденовирусы 3. Инсерция генов «чувствительности» или генов «самоубийц» 4. Блок экспрессии онкогенов 5. Инсерция генов-супрессоров опухолей 6. Защита нормальных клеток от химиотерапии 7. Индукция синтеза противоопухолевых веществ нормальными клетками 8. Продукция противоопухолевых рекомбинантных вакцин 9. Локальная радиопротекция нормальных тканей с помощью антиоксидантов 1. 2. 3. 4. 5. 6. 7. 8. 9. Гены чужеродных антигенов, цитокинов Гены цитокинов и ко-стимуляторов Ген тимидинкиназы HSV, цитозиндезаминазы. АСОН, si. RNA P 53 Гены лекарственной устойчивости тип 1 Гены интерлейкина-2, интерферона Вакцины типа БЦЖ, экспрессирующие опухолевые антигены Гены трансферазы, глутатионсинтетазы и пр.

Повышение иммунореактивности опухоли: I. обоснование §Гипотеза «иммунного надзора» , Ehrlich (1909); гипотеза иммунного ответа на опухоль Burnet, Thomas (1970), основанная на идентификации антигенов, специфически экспрессирующихся клетками опухоли – tumor-associated antigens (TAA). §Дендридные клетки, контактируя с опухолью, захватывают эти антигены и процессируют их (незрелая, антигензахватывающая ДК) и по афферентным лимфатическим путям попадают в ренгионарные лимфитические узлы, где и презентируют их в виде эпитопов на главном комплексе гистосовместимости (MHC – I, II class molecules) (зрелая, антигенпредставляющая ДК) вместе с костимулирующими молекулами (CD 80, CD 86, CD 54, CD 40). § Распознавание этих эпитопов на МНС 1 класса наивными Т-клетками , что активирует их дифференцировку в CD 8+ ЦТЛ. § ЦТЛ мигрируют в опухоль и уничтожают опухолевые клетки.

Повышение иммунореактивности опухоли: I. обоснование § Развитие опухоли сопряжено с толерантностью иммунной системы к опухоли и с подавлением антиопухолевого иммунитета. §Механизмы - нарушение экспрессии МНС-1 в опухолевых дендридных клетках и распознавания МНС СD 8+ T-клетками, сигналинга через костимуляторные молекулы, паракринная активность опухолевых клеток (IL -10, TGF-beta, PGE 2) и др. §Основы: 1. Молекулярная идентификация ТАА (клонирование, в основном из меланомы). 2. Эксплуатация центрального значения АРС в генерации анти-опухолевого иммунного ответа.

Повышение иммунореактивности опухоли: II. Цель и подходы § Цель - разрушение опухолевых клеток путем их адекватного распознавания иммунной системой «хозяина» . §Подходы: 1. Генная терапия in vivo 2. Генная терапия ex vivo 3. Генная терапия с применением антигенпрезентирующих клеток (АРС). 4. Экспрессия генов-иммуномодуляторов. клеток. 5. Генетическая модификация иммунных

Повышение иммунореактивности опухоли: III. подходы § ВАКЦИНАЦИЯ IN VIVO 1. В опухоль вводится вектор, несущий ген, кодирующий продукцию определенного опухоль-специфического антигена (ТАА) [MART-1/Melan-A, MAGE-3, NY-ESO, TRP-2 etc. ]. 2. 3. 4. 5. Продукция опухолью этого белка. Улучшение распознавания опухолевого антигена. Экспансия цитотоксических CD 8+ Т-лимфоцитов. Уничтожение опухолевых клеток. Преимущества – довольно сильный иммунный ответ на опухоль. Недостатки – расхождение между иммунным и антиопухолевым ответом.
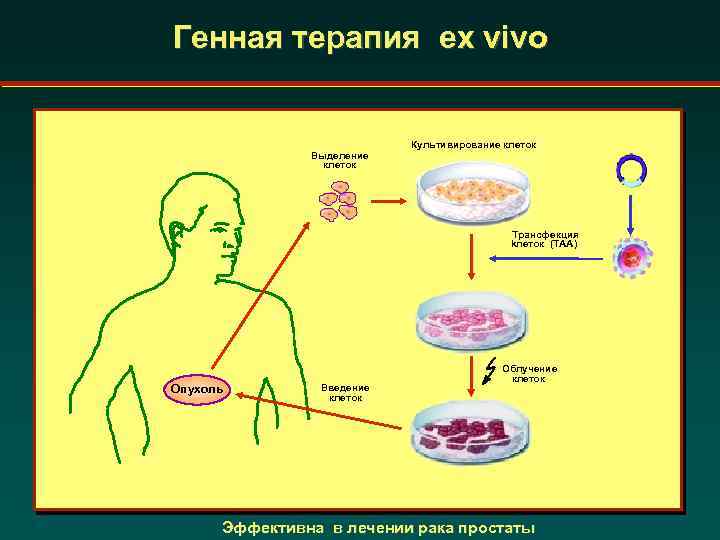
Генная терапия ex vivo Выделение клеток Культивирование клеток Трансфекция kлеток (TAA) Опухоль Введение клеток Облучение клеток Эффективна в лечении рака простаты

Повышение иммунореактивности опухоли: III. подходы § Генная терапия с применением антигенпрезентирующих клеток (АРС). Дендридные клетки – основные АРС в противоопухолевом иммунитете. АРС – мигрируют к опухоли. АРС – захватывают и процессируют опухолевые антигены. АРС – возвращаются в лимфатические узлы. АРС – активируют цитотоксические Т-лимфоциты. ЦТЛ – уничтожают опухолевые клетки.

Генная терапия с применением антиген-презентирующих клеток Культивирование клеток Выделение клеток Антигенпрезентирующие клетки Периферическая кровь Опухоль Трансфекция клеток Введение клеток Борьба с метастазирующими опухолевыми клетками на стадии единичных клеток или несформированных метастатических узлов.

Повышение иммунореактивности опухоли: III. подходы • Экспрессия генов иммуномодуляторов – иммуностимуляторов. При онкологических заболеваниях нарушена стимуляция иммунной системы через компоненты антиген-презентирующей системы (МНС-1) – в опухолях снижена концентрация бета 2 -микроглобулина, тяжелой цепи МНС-1. Используют экспрессию цитокинов и интерлейкинов, стимулирующих иммунную систему независимо от МНС-1 (GM-CSF, IL-12, IL-2, INF-beta). В вирусном векторе их гены вводятся в клетки опухоли – стимулируется противооопухолевый иммунитет.

«Суицидальная» генная терапия Основной принцип: введение в клетки генов энзимов, активирующих пролекарство в активный метаболит, убивающий клетки-мишени (GPAT – Genetic Prodrag Activation Therapy) Примеры: (1) Ген тимидин киназы вируса простого герпеса (HSV-tk) в вирусном векторе вводится в клетки опухоли, затем дается ганцикловир, который фосфорилируется тимидинкиназой до токсичного метаболита, нарушающего синтез ДНК – гибель раковых клеток. (2) Ген цитозин деаминазы - 5 -флюороцитозин (5 -FC) – 5 -флюороурацил – подавление пролиферации клеток опухоли.

«Суицидальная» генная терапия Для попадания только в опухоль: вектор, трансфицирующий только делящиеся клетки (для опухолей мозга) или «суицидальный» ген под опухоль специфическим промотером. Механизм: (1) Токсичный продукт фосфо-ГЦВ проникает через gap-junction в окружающие клетки. (2) Развивается противоопухолевый иммунитет в результате гибели клеток опухоли или стимуляции иммунного ответа аденовирусом. Для усиления иммунного ответа используют сочетание введения «суицидного» гена с геном цитокинов (IL-12, IL-2, GM-CSF, IFNbeta). “Bystander” effect: разрушаются не только клетки опухоли, но и окружающие клетки.

Инсерция генов-супрессоров опухолей • Семейство генов-супрессоров опухолей поддерживает необходимое число клеток в ткани путем подавления пролиферации, индукции апоптоза и детекции и восстановления поврежденной ДНК (р53, р73, р16, р21, ген ретинобластомы, ген опухоли Вильямса, ген карциномы кишечника). • р53 - интегральная роль в основных биохимических путях, регулирующих нормальную функцию клетки, “ The guardian of the genome” Функции – детекция поврежденной ДНК и остановка пролиферации, индукция апоптоза.

Р 53 генная заместительная терапия Обоснование : В клетках 50% опухолей - нефункциональный белок р53 в результате мутаций гена. Связь с плохим прогнозом и нечувствительностью к лечению. Гипотеза: Введение в клетки опухоли нормального р53 гена Восстановит баланс между пролиферацией и клеточной смертью – подавление роста опухоли.

Р 53 генная заместительная терапия На моделях опухоли легкого : Р 53 в ретровир. векторе - подавление роста опухоли, Гибель клеток как трансдуцированных, так и нетрансдуцированных (“bystander effect”) за счет подавления ангиогенеза, иммунного ответа, секреции трансдуцированными клетками проапоптотических белков. Клинические испытания: Мелкоклеточный рак легкого – 20% больных регрессия опухоли. Рак шеи и головы – 50% больных уменьшение опухоли, 10% полное исчезновение. Достоинство: значительное усиление эффективности химио- и радиотерапии. Препарат «ГЕНДИЦИН» , р53 в Ad. V, Китай.

Cелективные по репликации онколитические аденовирусы Обоснование: Вирус, размножаясь в опухолевых клетках, вызывает их лизис; выходя из разрушенных клеток он инфицирует другие клетки опухоли и так убивает всю опухоль. Как сделать, чтобы вирус убивал только клетки опухоли? 1. Поставить его репликацию под опухольспецифический промотер. 2. Использовать особенности опухолевых клеток.

Cелективные по репликации онколитические аденовирусы T. Fujiwara et al. , Frontiers in Bioscience 2008, 13, 1881 -1886

Теломераза-специфический онколитический аденовирус В аденовирусе 5 гены репликации Е 1 А и Е 1 В поставлены под промотер h. TERT, управляющий экспрессией обратной транскриптазы теломеразы, он может активироваться только в клетках, где высокая активность теломеразы, так как там есть соответствующие транскрипционные факторы. Вирус распространяется и в метастазы лимф. узлов при введении в опухоль!!!! T. Fujiwara et al. , Frontiers in Bioscience 2008, 13, 1881 -1886

Инактивация или блокирование экспрессии онкогенов, ингибиторов апоптоза, регуляторов клеточного цикла. Подходы: 1. Антисмысловые олигонуклеотиды (АСОН) 2. Малые интерферирующие РНК (ми. РНК). 3. Векторы, кодирующие короткие фрагменты антител к онкогенам. Недостатки: необходимо повторное введение в раковые клетки, подавление экспрессии нескольких онкогенов и пр. , Пик действия 36 -48 часов, после 96 значительно уменьшается, длительность действия зависит от интенсивности деления клеток, в раковых клетках – 37 дней подавление экспрессии. Разрушаются РНКазами плазмы – введение в вирусном векторе или липосомы, полимеры.

Мишени для АСОН и ми. РНК Target genes Cancer model Oncogenesis pathways Raf BCR-ABL с-Met β-catenin c-Myc HIF-1 Human pancreatic cancer, ovarian cancer, melanoma Human melanoma, prostate cancer, breast cancer Human CML Mouse mammary adenocarcinoma Human colon cancer Human breast carcinoma Human cervical and colon cancer, breast cancer and glioma Apoptosis Bcl-2 Survivin Bcl-2 and XIAP Human prostate cancer Human esophageal carcinoma, glioma, rhabdomyosarcoma Human breast cancer Cell cycle regulators E 2 F 4 E 6, E 7 Cyclin B 1 Human prostate carcinoma Human cervical cancer Cell senescence h. TERT Human colon and melanoma cancer Human bladder carcinoma Tumor–host interactions VEGF FGF-4 CD 31 u. PA/u. PAR Heparanase Rho. A/Rho. C CXCR 4 IL-10 Human Ewing’s sarcoma, CML, prostate cancer Human nonseminomatous germ line tumor Human prostate cancer and Rasv 12 - transformed rat fibroblast tumor Human meningioma Human breast carcinoma, murine lymphoma and melanoma Human breast cancer Murine CLL Chemotherapy resistance MDR 1 Ribonucleotide reductase Human pancreatic and gastric carcinoma, uterine sarcoma Murin pancreatic carcinoma

Направленная (таргетная) генная терапия Обоснование: Аденовирусы связываются с клеточными рецепторами вируса К Каксаки через файбер-белки на капсиде. Чтобы направить их к клетками опухоли, нужно, чтобы он связывался с рецепторами на клетках опухоли. Фьюжн-белок – фрагмент АТ к файберу, связанный с EGF , блокирует связывание вируса с рецептором Коксаки и перенаправляет его на связывание с рецептором EGF – HER 2, который экспрессируется клетками многих эпителиальных опухолей (рак легкого). Показана эффективность при лечении метастазов, когда нужно вводить в кровоток.

Синтетические векторы для доставки ДНК в клетки Dufes C. et al, Advanced Drug Delivery Reviews , 2005, 57, 2177 -2202

Структура и синтез дендримеров Divergent syntesis Convergent syntesis Dufes C. et al, Advanced Drug Delivery Reviews, 2005, 57, 2177 -2202

Структура и размер дендримеров различных генераций Svenson S. , Tomalia D. , Advanced Drug Delivery Reviews, 2005, 57, 2106 -2129

Электростатическое взаимодействие ДНК/ РНК с дендримером Адаптировано из проспекта STARPHARMA Holding Ltd.

Свойства дендримеров зависит от генерации Svenson S. , Tomalia D. , Advanced Drug Delivery Reviews, 2005, 57, 2106 -2129

Дендримеры эндоцитируются клеткой благодаря поливалентному связыванию с ее рецепторами Эндоцитоз

«Активная» направленная доставка Lim et. al. Nanomedicine. 2005; 1: 110 -114.

Почему дендримеры привлекательны в качестве системы доставки ДНК/РНК для генной терапии? § Предсказуемые, контролируемые и воспроизволимые размеры и структура макромолекул дендримеров § Высокая плотность поверхностных терминальных групп § Наличие каналов и пор для капсулирования и иммобилизации физиологически активных гостевых молекул
Лекция рак и пр. 14 апреля.ppt