кремний.pptx
- Количество слайдов: 14

Тақырып: Кремний орындаған: Сембай Алибек тексерген: Дүйсенбиев М. Ж.

Кремний (Sіlіcіum), Sі – элементтердің периодтық жүйесінің ІV тобындағы элемент. Тұрақты 3 изотопы – 28 Sі, 29 Sі және 30 Sі бар. Жер қыртысындағы мөлшері 29, 5%. Атомдық массасы (молярлы масса) - [28, 084; 28, 086]а. е. м. (г/моль) Электронды конфигурациясы -3 s 2 3 p 2; 3 s 3 p 3 Радиус атома - 132 пм

Ашылуы: Кремнийді алғаш рет 1811 жылы Гей Люссак пен Л. Ж. Тенар ашқан. 1824 – 1825 жылдары швед хи мигі Я. Берцелиу с фторлы кремнийді калиймен тотықсыздандырып, ал 1865 жылы орыс ғалымы Н. Н. Бекетов төрт хлорлы кремний мен мырышты әре кеттестіріп жеке бөліп алған.

Физикалық қасиеті: Салмағы 2, 32 г/м 3 Балқу t 1420 С Қайнау t 2600 С-қа жуық. Молярлы жылусыйымдылығы - 20, 16 Дж/(K·моль) Молярлы көлемі -12, 1 см³/моль Өнеркәсіпте Кремний кремнеземді қыздырып, кокспен тотықсыздандыру, ал таза кремний төрт хлорлы кремнийді мырыш буымен тотықсыздандыру арқылы алынады. Қыздырғанда сутектен басқа кез-келген бейметалмен қосыла алады. Төменгі температурада инертті. Таза кремний темір, мыс, алюминий, қорғасын қорытпаларын да қолданылады. Ол мұндай қорытпалардың қышқылдарға төзімді, мықты, электрлік және магниттік қасиеттерін арттырады.

Жай заттың сыртқы түрі Кристалл формада - кремнийдің түсі күңгірт-сұр, шайырдай жылтыр Аморфты формада – коңыр түсті ұнтақ

Химиялық қасиеті: Ковалентті радиус -111 пм Радиус иона - 42 (+4 e) 271 (-4 e) пм Электртрістілік- 1, 90 (Полинг шкаласы) Электр потенциалдық - 0 Қышқылдану дәрежесі - +4, +2, 0, − 4 Иондану энергиясы(I электрон)-786, 0 (8, 15) к. Дж/моль (э. В)
Жай заттармен: Si + 02 = Si 02 (кремний оксиді) Si + 2 F 2= Si. F 4 (кремний фториді) Si + C = Si. C (карборунд) Si + 2 Mg = Mg 2 Si (магний силициді) Күрделі заттармен: Сілтінің ерітіндісімен қыздырғанда әрекеттеседі Si + 2 Na. OH + Н 20 = Na 2 Si 03 + 2 Н 2↑
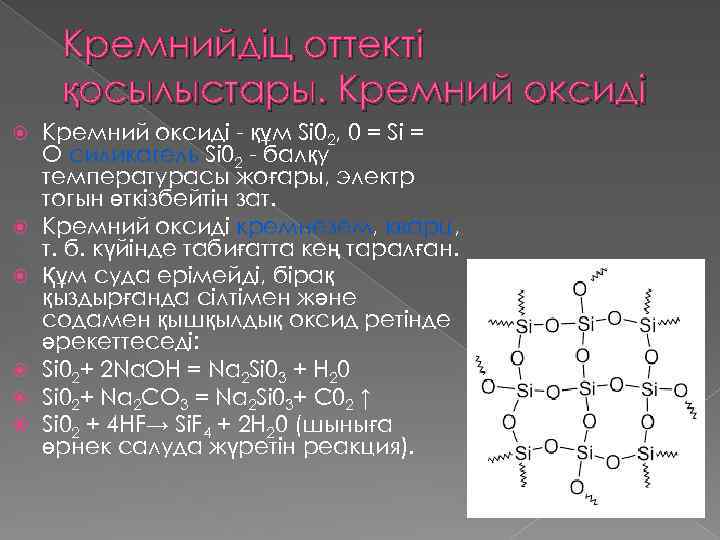
Кремнийдіц оттекті қосылыстары. Кремний оксиді Кремний оксиді - құм Si 02, 0 = Si = О силикагель Si 02 - балқу температурасы жоғары, электр тогын өткізбейтін зат. Кремний оксиді кремнезем, кварц, т. б. күйінде табиғатта кең таралған. Құм суда ерімейді, бірақ қыздырғанда сілтімен және содамен қышқылдық оксид ретінде әрекеттеседі: Si 02+ 2 Na. OH = Na 2 Si 03 + Н 20 Si 02+ Na 2 CO 3 = Na 2 Si 03+ C 02 ↑ Si 02 + 4 HF→ Si. F 4 + 2 H 20 (шыныға өрнек салуда жүретін реакция).

Кремний қышқылы. Силикаттар H 2 Si 03 - метакремний қышқылы H 4 Si 04 - ортокремний қышқылы Тұздары силикаттар деп аталады. Na 2 Si 03 + H 2 S 04 (конц. ) = H 2 Si 03 ↓+ Na 2 S 04

Метакремний қышқылы іркілдек (коллоид) күйінде болады. H 2 Si 03 - екі негізді, әлсіз, тұрақсыз қышқыл. Ол оңай айырылады. H 2 Si 03 = Н 20 + Si 02 Пайда болатын силикаттарына Na 2 Si 03, K 2 Si 03 - ерімтал тұздары жатады. Оларды сұйық шыны деп атайды, желім ретінде қолданылады.

Шыны алу Na 2 C 03 + Si 02 = Na 2 Si 03 + C 02↑ Ca. C 03 + Si 02 = Ca. Si 03 + C 02↑ К 20 • Са. О • 6 Si 02. Ол қиын балқиды. Лағыл (рубин) шыныда Сr 3+ ионы болады. Таза құмнан кварц шыны өндіріледі, ол медицинада (ультракүлгін сәулелерді өткізетіндіктен), химиялық ыдыстар жасауда қолданылады. .

Цемент ендірісі Аl 203 • 2 Si 02 • 2 Н 20 = Аl 203 • 2 Si 02+ 2 H 20 Са. С 03 = Са. О + С 02↑ Са. О + Si 02 = Ca. Si 03

Қазақстанда силикат енеркөсібінің кәсіпорындары төмендегідей болып шоғырланған: Маңғыстауда - Са. СО 3 әктас; Жітіқарада (Қостанай облысы) - асбест; Семейде - цемент зауыты; Өскеменде - «Аютас» зауыты; Ақтөбе, Таразда - шыны ендірісі; Ленгер, Есік, Өскеменде - кірпіш зауыттары бар.

НАЗАРЫҢЫЗҒА РАХМЕТ!
кремний.pptx