2013_КИО.ppt
- Количество слайдов: 115
 Т-лимфоциты (Тл) Клеточный иммунный ответ (КИО) Иммунологическая память (ИП) Иммунологическая толерантность (ИТ) Трансплантационный иммунитет Протитивоопухолевый иммунитет Шабан Ж. Г.
Т-лимфоциты (Тл) Клеточный иммунный ответ (КИО) Иммунологическая память (ИП) Иммунологическая толерантность (ИТ) Трансплантационный иммунитет Протитивоопухолевый иммунитет Шабан Ж. Г.
 ОБЩИЕ СВОЙСТВА Тл и Вл 1. Двойная дифференцировка (созревание): I этап (АГнезависимый, Ø Ø лимфопоэз) происходит в центральных органах ИС не зависит от АГ раздражения заканчивается образованием основных субпопуляций Лф на поверхности Лф формируются АГ-распознающие рецепторы II этап (вторичная АГзависимая дифференцировка) Ø происходит в периферических органах ИС Ø индуцируется АГ Ø заканчивается образованием функционально различных клеток
ОБЩИЕ СВОЙСТВА Тл и Вл 1. Двойная дифференцировка (созревание): I этап (АГнезависимый, Ø Ø лимфопоэз) происходит в центральных органах ИС не зависит от АГ раздражения заканчивается образованием основных субпопуляций Лф на поверхности Лф формируются АГ-распознающие рецепторы II этап (вторичная АГзависимая дифференцировка) Ø происходит в периферических органах ИС Ø индуцируется АГ Ø заканчивается образованием функционально различных клеток
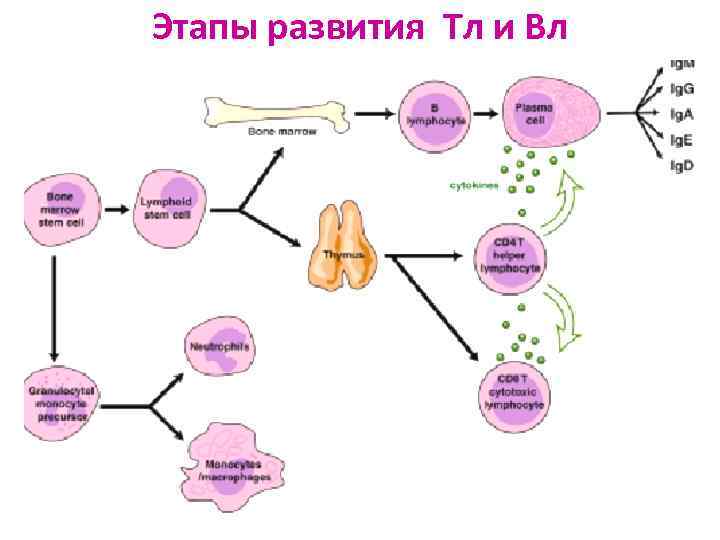 Этапы развития Тл и Вл
Этапы развития Тл и Вл
 2. Способность к высокоспецифичному распознаванию чужеродных структур с помощью узкоспециализированных АГ-распознающих рецепторов каждая клетка отвечает на индивидуальный АГ. По специфичности этих рецепторов популяции Тл и Вл клонированы, каждый клон имеет свой специфический рецептор. 3. Клональная пролиферация. 4. Рециркуляция из тканей обратно в кровоток специфическая память после локального ответа на АГ распространяется по всему организму. 5. Длительная продолжительность жизни клеток ИП, которые формируются из АГстимулированных Лф и обеспечивают быстрый и эффективный ВИО при повторной встрече с тем же АГ.
2. Способность к высокоспецифичному распознаванию чужеродных структур с помощью узкоспециализированных АГ-распознающих рецепторов каждая клетка отвечает на индивидуальный АГ. По специфичности этих рецепторов популяции Тл и Вл клонированы, каждый клон имеет свой специфический рецептор. 3. Клональная пролиферация. 4. Рециркуляция из тканей обратно в кровоток специфическая память после локального ответа на АГ распространяется по всему организму. 5. Длительная продолжительность жизни клеток ИП, которые формируются из АГстимулированных Лф и обеспечивают быстрый и эффективный ВИО при повторной встрече с тем же АГ.
 Тл Ø Ø Ø Ø До 80 % всех Лф (=5 х1011 клеток , 1% веса тела) Происходят от полипотентной СКК, созревают и дифференцируются в тимусе; 109 Тл ежедневно покидают тимус и уходят в периферические органы ИС Созреванием, дифференцировкой, активностью Тл управляют цитокины По морфологии практически не отличаются от Вл По функциям и поверхностным АГ – обособленная группа ИКК, основной маркёр – CD 3 Сложная по составу группа клеток: субпопуляции по функциональным и структурным характеристикам Обеспечивают КИО, определяют длительность и силу иммунной реакции, помогают Вл в продукции АТ
Тл Ø Ø Ø Ø До 80 % всех Лф (=5 х1011 клеток , 1% веса тела) Происходят от полипотентной СКК, созревают и дифференцируются в тимусе; 109 Тл ежедневно покидают тимус и уходят в периферические органы ИС Созреванием, дифференцировкой, активностью Тл управляют цитокины По морфологии практически не отличаются от Вл По функциям и поверхностным АГ – обособленная группа ИКК, основной маркёр – CD 3 Сложная по составу группа клеток: субпопуляции по функциональным и структурным характеристикам Обеспечивают КИО, определяют длительность и силу иммунной реакции, помогают Вл в продукции АТ
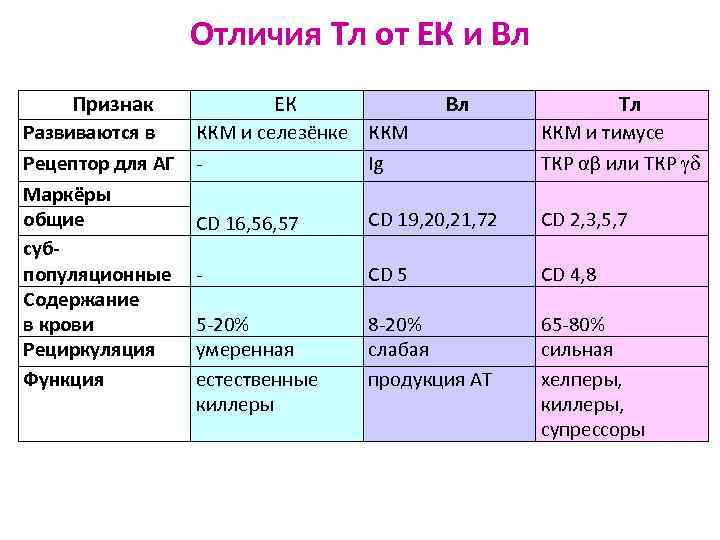 Отличия Тл от ЕК и Вл Признак Развиваются в Рецептор для АГ Маркёры общие субпопуляционные Содержание в крови Рециркуляция Функция ЕК ККМ и селезёнке ККМ Ig Вл Тл ККМ и тимусе ТКР αβ или ТКР СD 16, 57 СD 19, 20, 21, 72 СD 2, 3, 5, 7 - CD 5 CD 4, 8 5 -20% умеренная естественные киллеры 8 -20% слабая продукция АТ 65 -80% сильная хелперы, киллеры, супрессоры
Отличия Тл от ЕК и Вл Признак Развиваются в Рецептор для АГ Маркёры общие субпопуляционные Содержание в крови Рециркуляция Функция ЕК ККМ и селезёнке ККМ Ig Вл Тл ККМ и тимусе ТКР αβ или ТКР СD 16, 57 СD 19, 20, 21, 72 СD 2, 3, 5, 7 - CD 5 CD 4, 8 5 -20% умеренная естественные киллеры 8 -20% слабая продукция АТ 65 -80% сильная хелперы, киллеры, супрессоры
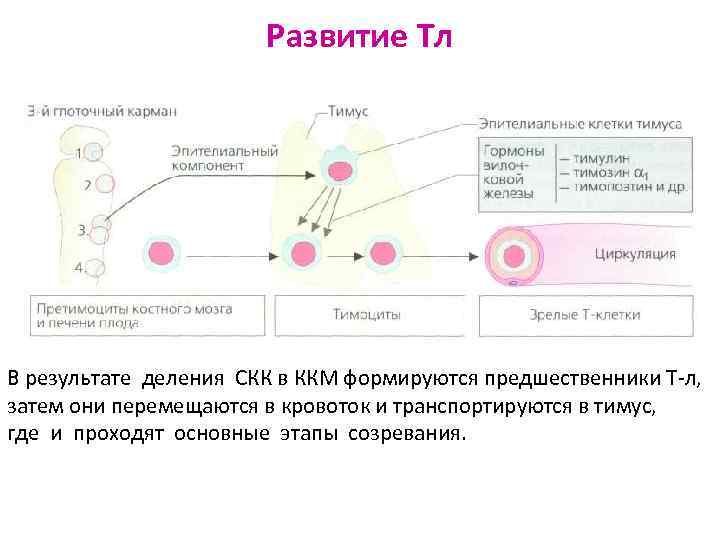 Развитие Тл В результате деления СКК в ККМ формируются предшественники Т-л, затем они перемещаются в кровоток и транспортируются в тимус, где и проходят основные этапы созревания.
Развитие Тл В результате деления СКК в ККМ формируются предшественники Т-л, затем они перемещаются в кровоток и транспортируются в тимус, где и проходят основные этапы созревания.
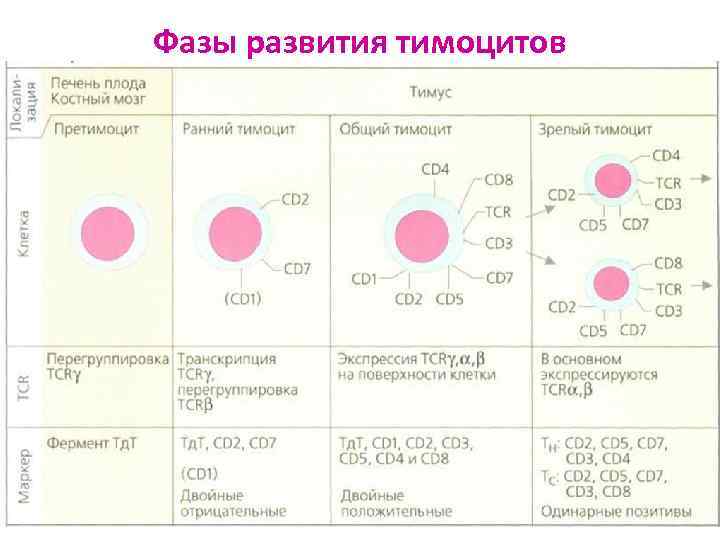 Фазы развития тимоцитов
Фазы развития тимоцитов
 РАЗВИТИЕ Тл на разных этапах дифференцировки Тл имеют различные маркёры и выполняют различные функции СКК Пре-Т-л Лимфобласты Малые (ранние) тимоциты Средние (общие) тимоциты Зрелые Тл
РАЗВИТИЕ Тл на разных этапах дифференцировки Тл имеют различные маркёры и выполняют различные функции СКК Пре-Т-л Лимфобласты Малые (ранние) тимоциты Средние (общие) тимоциты Зрелые Тл
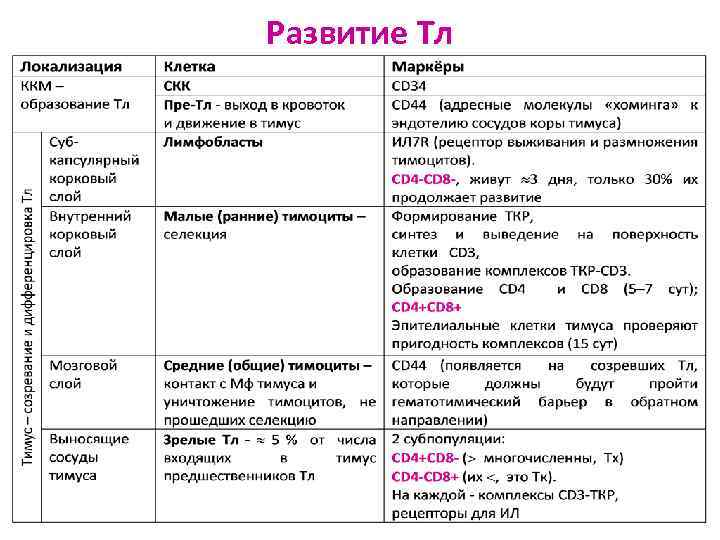 Развитие Тл
Развитие Тл
 «Обучение» Тл в тимусе Положительная селекция Отрицательная селекция
«Обучение» Тл в тимусе Положительная селекция Отрицательная селекция
 Положительная селекция Ø Определяется аффинность (сродство) молекул CD 4 к белкам ГКГС I и CD 8 к белкам ГКГС II на эпителиальных клетках коркового слоя тимуса Ø Зреющие тимоциты должны «узнавать» молекулы ГКГС только того организма, в котором они образуются. Такие клетки получают сигнал на выживание и размножение (ростовые факторы тимуса) Ø Если такое «узнавание» не происходит, тимоцит получает сигнал апоптоза и погибает
Положительная селекция Ø Определяется аффинность (сродство) молекул CD 4 к белкам ГКГС I и CD 8 к белкам ГКГС II на эпителиальных клетках коркового слоя тимуса Ø Зреющие тимоциты должны «узнавать» молекулы ГКГС только того организма, в котором они образуются. Такие клетки получают сигнал на выживание и размножение (ростовые факторы тимуса) Ø Если такое «узнавание» не происходит, тимоцит получает сигнал апоптоза и погибает
 Отрицательная селекция Ø Проверяется специфичность ТКР Ø Ø в корково-мозговой зоне тимуса Зреющим тимоцитам эпителиальные клетки представляют сочетания белков ГКГС с собственными процессированными АГ Селекция необходима, т. к. в каждом тимоците специфичность рецептора определяется сочетанием случайно выбранных генов и среди зреющих тимоцитов имеются и такие, которые будут реагировать на АГ своего организма Довести аутореактивные тимоциты до окончательного созревания для организма недопустимо, т. к. атаке ИС будут подвергаться собственные ткани и органы Клетки, реагирующие с «собственными» АГ, уничтожаются путём апоптоза
Отрицательная селекция Ø Проверяется специфичность ТКР Ø Ø в корково-мозговой зоне тимуса Зреющим тимоцитам эпителиальные клетки представляют сочетания белков ГКГС с собственными процессированными АГ Селекция необходима, т. к. в каждом тимоците специфичность рецептора определяется сочетанием случайно выбранных генов и среди зреющих тимоцитов имеются и такие, которые будут реагировать на АГ своего организма Довести аутореактивные тимоциты до окончательного созревания для организма недопустимо, т. к. атаке ИС будут подвергаться собственные ткани и органы Клетки, реагирующие с «собственными» АГ, уничтожаются путём апоптоза
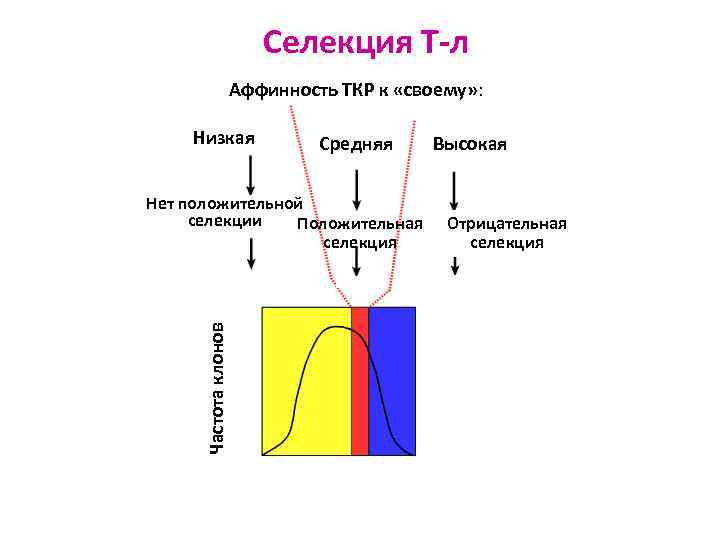 Селекция Т-л Аффинность ТКР к «своему» : Низкая Средняя Частота клонов Нет положительной селекции Положительная селекция Высокая Отрицательная селекция
Селекция Т-л Аффинность ТКР к «своему» : Низкая Средняя Частота клонов Нет положительной селекции Положительная селекция Высокая Отрицательная селекция
 Итоги селекционной работы в тимусе Ø 95 % Тл не выдерживают испытаний и погибают Ø 5 % клеток превращается в зрелые Тл, способные распознать в комплексе с ГКГС только чужеродные биополимеры Ø Этих клеток хватает для того, чтобы ИС могла отреагировать на весь спектр АГ
Итоги селекционной работы в тимусе Ø 95 % Тл не выдерживают испытаний и погибают Ø 5 % клеток превращается в зрелые Тл, способные распознать в комплексе с ГКГС только чужеродные биополимеры Ø Этих клеток хватает для того, чтобы ИС могла отреагировать на весь спектр АГ
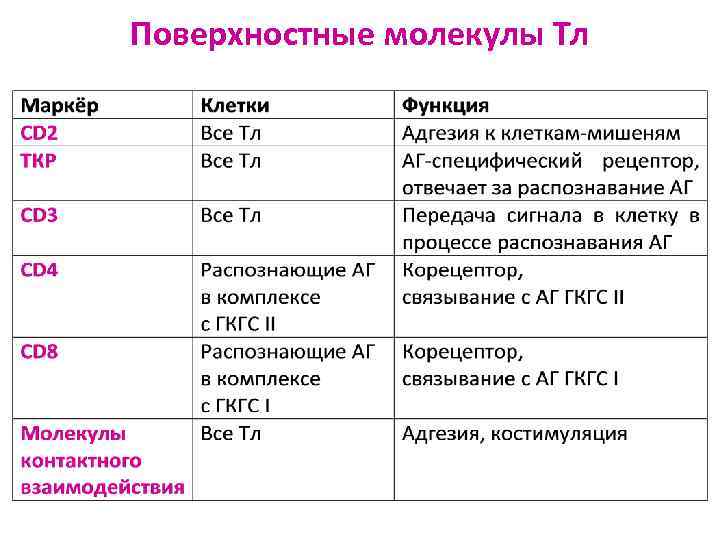 Поверхностные молекулы Тл
Поверхностные молекулы Тл
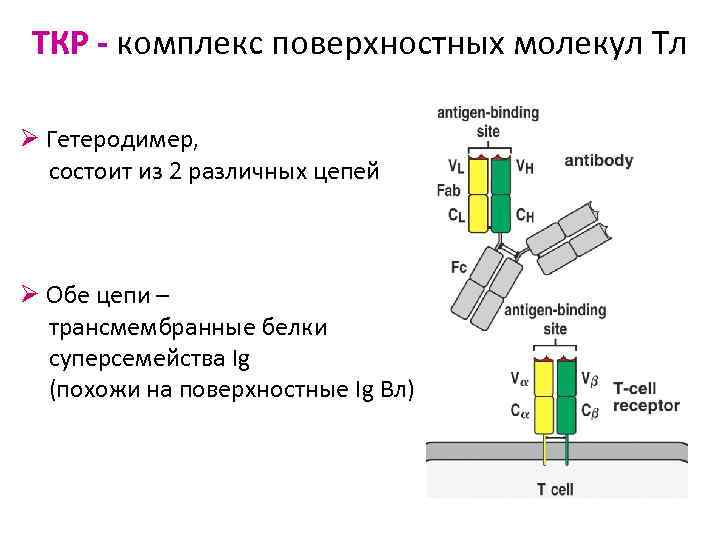 ТКР - комплекс поверхностных молекул Тл Ø Гетеродимер, состоит из 2 различных цепей Ø Обе цепи – трансмембранные белки суперсемейства Ig (похожи на поверхностные Ig Вл)
ТКР - комплекс поверхностных молекул Тл Ø Гетеродимер, состоит из 2 различных цепей Ø Обе цепи – трансмембранные белки суперсемейства Ig (похожи на поверхностные Ig Вл)
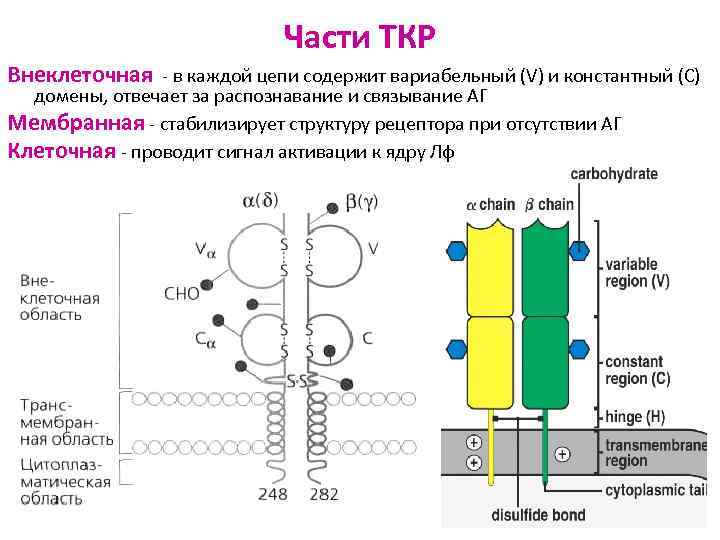 Части ТКР Внеклеточная - в каждой цепи содержит вариабельный (V) и константный (С) домены, отвечает за распознавание и связывание АГ Мембранная - стабилизирует структуру рецептора при отсутствии АГ Клеточная - проводит сигнал активации к ядру Лф
Части ТКР Внеклеточная - в каждой цепи содержит вариабельный (V) и константный (С) домены, отвечает за распознавание и связывание АГ Мембранная - стабилизирует структуру рецептора при отсутствии АГ Клеточная - проводит сигнал активации к ядру Лф
 ТИПЫ ТКР 1 ТИП: + цепи, 5% Тл 2 ТИП: α+ цепи, 95% Тл
ТИПЫ ТКР 1 ТИП: + цепи, 5% Тл 2 ТИП: α+ цепи, 95% Тл
 / Тл Ø Первыми появляются в онтогенезе, относятся к системе врождённого иммунитета Ø Заселяют покровные ткани (кожа, слизистые), поддерживают их целостность, регулируют процессы воспаления и репарации Ø Не распознают пептиды в комплексе с ГКГС Ø Распознают: - липидные и липопротеидные АГ - внутриклеточные АГ - молекулы, появляющиеся на клетках при повреждениях Ø Продуцируют широкий спектр цитокинов, в т. ч. ростовые факторы (ФР кератиноцитов, эпителия) и «лечат» повреждения Ø Цитотоксичны Ø Большинство CD 4 -CD 8 - , кишечные - CD 4 -CD 8+
/ Тл Ø Первыми появляются в онтогенезе, относятся к системе врождённого иммунитета Ø Заселяют покровные ткани (кожа, слизистые), поддерживают их целостность, регулируют процессы воспаления и репарации Ø Не распознают пептиды в комплексе с ГКГС Ø Распознают: - липидные и липопротеидные АГ - внутриклеточные АГ - молекулы, появляющиеся на клетках при повреждениях Ø Продуцируют широкий спектр цитокинов, в т. ч. ростовые факторы (ФР кератиноцитов, эпителия) и «лечат» повреждения Ø Цитотоксичны Ø Большинство CD 4 -CD 8 - , кишечные - CD 4 -CD 8+
 / Тл Ø отвечают за все известные функции Тл Ø циркулируют в тканях, периферической крови, заселяют л/у
/ Тл Ø отвечают за все известные функции Тл Ø циркулируют в тканях, периферической крови, заселяют л/у
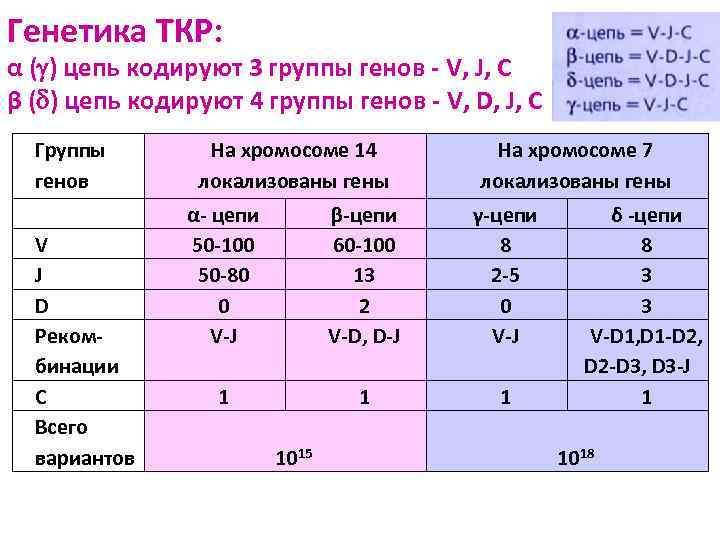 Генетика ТКР: α ( ) цепь кодируют 3 группы генов - V, J, C β ( ) цепь кодируют 4 группы генов - V, D, J, C Группы генов V J D Рекомбинации C Всего вариантов На хромосоме 14 локализованы гены На хромосоме 7 локализованы гены α- цепи 50 -100 50 -80 0 V-J β-цепи 60 -100 13 2 V-D, D-J γ-цепи 8 2 -5 0 V-J 1 1015 δ -цепи 8 3 3 V-D 1, D 1 -D 2, D 2 -D 3, D 3 -J 1 1018
Генетика ТКР: α ( ) цепь кодируют 3 группы генов - V, J, C β ( ) цепь кодируют 4 группы генов - V, D, J, C Группы генов V J D Рекомбинации C Всего вариантов На хромосоме 14 локализованы гены На хромосоме 7 локализованы гены α- цепи 50 -100 50 -80 0 V-J β-цепи 60 -100 13 2 V-D, D-J γ-цепи 8 2 -5 0 V-J 1 1015 δ -цепи 8 3 3 V-D 1, D 1 -D 2, D 2 -D 3, D 3 -J 1 1018
 РАЗНООБРАЗИЕ ТКР и их уникальная АГ-распознающая способность обеспечивается перестройкой генов в Тл Ø Гены TКР: - расположены на хромосоме ч/з некоторые промежутки - не проявляют активности до попадания предшественников Тл в тимус Ø Под влиянием выделяемых клетками тимуса веществ начинаются перестройки в одной хромосоме, где находятся гены α-цепи ТКР. Старт этим событиям дает активация генов Rag-1 и Rag-2, в результате чего в клетке появляются рекомбиназы RAG-1 и RAG-2. Под действием рекомбиназ случайным образом V-ген объединяется с J-геном, сочетание VJ смыкается с С-геном α-цепи Ø Сходным образом осуществляются перестройки в одной хромосоме, где находятся гены β-цепи. Наличие здесь D-генов число возможных вариантов β-цепей, т. к. при перестройках должны случайно объединиться по одному из генов в последовательности VDJC
РАЗНООБРАЗИЕ ТКР и их уникальная АГ-распознающая способность обеспечивается перестройкой генов в Тл Ø Гены TКР: - расположены на хромосоме ч/з некоторые промежутки - не проявляют активности до попадания предшественников Тл в тимус Ø Под влиянием выделяемых клетками тимуса веществ начинаются перестройки в одной хромосоме, где находятся гены α-цепи ТКР. Старт этим событиям дает активация генов Rag-1 и Rag-2, в результате чего в клетке появляются рекомбиназы RAG-1 и RAG-2. Под действием рекомбиназ случайным образом V-ген объединяется с J-геном, сочетание VJ смыкается с С-геном α-цепи Ø Сходным образом осуществляются перестройки в одной хромосоме, где находятся гены β-цепи. Наличие здесь D-генов число возможных вариантов β-цепей, т. к. при перестройках должны случайно объединиться по одному из генов в последовательности VDJC
 Реанжировка (перестройка) генов в Тл Ø Осуществляется в каждом созревающем тимоците по описанной схеме случайно Ø Уникальность белковых цепей TКР каждого тимоцита Ø Специфичность рецептора определяется сочетанием цепей количество вариантов рецепторов (и созревающих тимоцитов) равно произведению вариантов каждой цепи Ø Имеет место полное аллельное исключение: - перестройкам подвергаются гены одной хромосомы из пары гомологичных эта хромосома будет в дальнейшем активна в плане формирования TКР гены TКР второй хромосомы в течение всей жизни клетки будут закрыты для активации и перестроек зрелый Тл и образующиеся после его активации дочерние клетки никогда не поменяют специфичность в плане распознавания АГ
Реанжировка (перестройка) генов в Тл Ø Осуществляется в каждом созревающем тимоците по описанной схеме случайно Ø Уникальность белковых цепей TКР каждого тимоцита Ø Специфичность рецептора определяется сочетанием цепей количество вариантов рецепторов (и созревающих тимоцитов) равно произведению вариантов каждой цепи Ø Имеет место полное аллельное исключение: - перестройкам подвергаются гены одной хромосомы из пары гомологичных эта хромосома будет в дальнейшем активна в плане формирования TКР гены TКР второй хромосомы в течение всей жизни клетки будут закрыты для активации и перестроек зрелый Тл и образующиеся после его активации дочерние клетки никогда не поменяют специфичность в плане распознавания АГ
 Факторы, обеспечивающие специфичность ТКР 1) множественность исходных генов каждой группы 2) комбинирование этих генов 3) вариабельность размеров J-сегментов 4) изменение длины J-сегмента при соединении с V-сегментом 5) возможность использования различных рамок считывания в D-сегменте 6) многообразие формирующихся Р- и N-фрагментов 7) сочетание двух цепей Число вариантов ТКР перекрывает возможное количество различных по АГ характеристикам молекул, с которыми организм может контактировать в течение жизни ИС способна реагировать практически на любой чужеродный агент, если он обладает АГ свойствами
Факторы, обеспечивающие специфичность ТКР 1) множественность исходных генов каждой группы 2) комбинирование этих генов 3) вариабельность размеров J-сегментов 4) изменение длины J-сегмента при соединении с V-сегментом 5) возможность использования различных рамок считывания в D-сегменте 6) многообразие формирующихся Р- и N-фрагментов 7) сочетание двух цепей Число вариантов ТКР перекрывает возможное количество различных по АГ характеристикам молекул, с которыми организм может контактировать в течение жизни ИС способна реагировать практически на любой чужеродный агент, если он обладает АГ свойствами
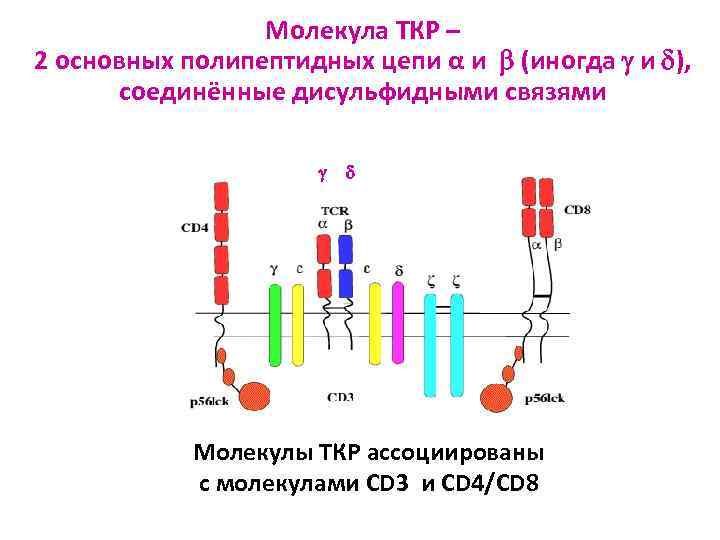 Молекула ТКР – 2 основных полипептидных цепи α и (иногда и ), соединённые дисульфидными связями Молекулы ТКР ассоциированы с молекулами CD 3 и CD 4/CD 8
Молекула ТКР – 2 основных полипептидных цепи α и (иногда и ), соединённые дисульфидными связями Молекулы ТКР ассоциированы с молекулами CD 3 и CD 4/CD 8
 Молекула CD 3 (3 димера, составляют единый комплекс с TКР) Ø Комплексная молекула, состоит из 5 полипептидных цепей: γ (гамма), δ (дельта), ε (эпсилон), ζ (дзета), η (эта) Ø 2 типа молекулярных комплексов CD 3: - 90 % - по одной цепи γ, δ, две цепи ε, две ζ-цепи 10 % - по одной цепи γ, δ, две цепи ε, ζ-цепь, η-цепь Отличительные черты комплексов: - обязательное соседство с двумя близко расположенными TКР протяжённые внутриклеточные домены, чем у α- и β-цепей Ø Функция CD 3 - передача в ядро сигнала, возникающего при контакте TКР с АГ: с ЦП участками комплекса CD 3 взаимодействуют ЦП молекулы из семейства киназ , запускающие внутриклеточные процессы активации Для передачи сигнала важны все входящие в CD 3 белковые цепи, но предпочтение в запуске внутриклеточных изменений отдаётся ζ-цепи (её ЦП часть длиннее, составляет 112 АК из входящих в эту цепь 143)
Молекула CD 3 (3 димера, составляют единый комплекс с TКР) Ø Комплексная молекула, состоит из 5 полипептидных цепей: γ (гамма), δ (дельта), ε (эпсилон), ζ (дзета), η (эта) Ø 2 типа молекулярных комплексов CD 3: - 90 % - по одной цепи γ, δ, две цепи ε, две ζ-цепи 10 % - по одной цепи γ, δ, две цепи ε, ζ-цепь, η-цепь Отличительные черты комплексов: - обязательное соседство с двумя близко расположенными TКР протяжённые внутриклеточные домены, чем у α- и β-цепей Ø Функция CD 3 - передача в ядро сигнала, возникающего при контакте TКР с АГ: с ЦП участками комплекса CD 3 взаимодействуют ЦП молекулы из семейства киназ , запускающие внутриклеточные процессы активации Для передачи сигнала важны все входящие в CD 3 белковые цепи, но предпочтение в запуске внутриклеточных изменений отдаётся ζ-цепи (её ЦП часть длиннее, составляет 112 АК из входящих в эту цепь 143)
 Молекула CD 8 Ø Структурные гены молекулы CD 4 расположены в 2 хромосоме Ø Молекула CD 8 - гетеродимер из α- и β-цепей, в каждой цепи имеется: - один внеклеточный домен довольно протяжённый (30 АК остатков в α-цепи и 50 – в β-цепи) связующий (спейсерный) участок - трансмембранный домен - хорошо выраженный ЦП домен, - внутриклеточный участок α-цепи молекулы CD 8 связан с тирозинкиназой p 56 lck Ø Функции молекулы CD 8: - тесно связана с ТКР - нужна клеткам для передачи внешних сигналов внутрь клетки, сигнал о связывании АГ - корецептор, играет важную роль в межклеточных взаимодействиях, специфически взаимодействует с молекулами ГКГС I обеспечивает рестрикцию распознавания (CD 8+ Тл распознают «свою» АПК через «узнавание» своих молекул ГКГС I)
Молекула CD 8 Ø Структурные гены молекулы CD 4 расположены в 2 хромосоме Ø Молекула CD 8 - гетеродимер из α- и β-цепей, в каждой цепи имеется: - один внеклеточный домен довольно протяжённый (30 АК остатков в α-цепи и 50 – в β-цепи) связующий (спейсерный) участок - трансмембранный домен - хорошо выраженный ЦП домен, - внутриклеточный участок α-цепи молекулы CD 8 связан с тирозинкиназой p 56 lck Ø Функции молекулы CD 8: - тесно связана с ТКР - нужна клеткам для передачи внешних сигналов внутрь клетки, сигнал о связывании АГ - корецептор, играет важную роль в межклеточных взаимодействиях, специфически взаимодействует с молекулами ГКГС I обеспечивает рестрикцию распознавания (CD 8+ Тл распознают «свою» АПК через «узнавание» своих молекул ГКГС I)
 Субпопуляции CD 8+ Тл Ø Т-цитотоксические лимфоциты (=ЦТЛ, Тк) – эффекторная функция: клетки-киллеры. Активированные Тк уничтожают клетки-мишени (вирусинфицированные, опухолевые) в результате контакта и участия перфорина, гранзимов, Fas-рецепторов и ФНО Ø Т-супрессоры – регуляторная функция: пролиферацию других типов клеток Ø Клетки-памяти
Субпопуляции CD 8+ Тл Ø Т-цитотоксические лимфоциты (=ЦТЛ, Тк) – эффекторная функция: клетки-киллеры. Активированные Тк уничтожают клетки-мишени (вирусинфицированные, опухолевые) в результате контакта и участия перфорина, гранзимов, Fas-рецепторов и ФНО Ø Т-супрессоры – регуляторная функция: пролиферацию других типов клеток Ø Клетки-памяти
 Молекула CD 4 Ø Структурные гены молекулы CD 4 расположены в 3 хромосоме Ø Структура молекула CD 4: - одна белковая цепь, внеклеточная часть которой имеет 4 домена трансмембранный домен относительно короткий внутриклеточный домен, который связан с тирозинкиназой p 56 lck Ø Функции молекулы CD 4: - тесно связана с ТКР - нужна клеткам для передачи внешних сигналов внутрь клетки, сигнал о связывании АГ - корецептор, играет важную роль в межклеточных взаимодействиях, специфически взаимодействует с молекулами ГКГС II обеспечивает рестрикцию распознавания (CD 4+ Тл распознают «свою» АПК через «узнавание» своих молекул ГКГС II)
Молекула CD 4 Ø Структурные гены молекулы CD 4 расположены в 3 хромосоме Ø Структура молекула CD 4: - одна белковая цепь, внеклеточная часть которой имеет 4 домена трансмембранный домен относительно короткий внутриклеточный домен, который связан с тирозинкиназой p 56 lck Ø Функции молекулы CD 4: - тесно связана с ТКР - нужна клеткам для передачи внешних сигналов внутрь клетки, сигнал о связывании АГ - корецептор, играет важную роль в межклеточных взаимодействиях, специфически взаимодействует с молекулами ГКГС II обеспечивает рестрикцию распознавания (CD 4+ Тл распознают «свою» АПК через «узнавание» своих молекул ГКГС II)
 Субпопуляции CD 4+ Тл Ø Т-хелперы. По спектру цитокинов выделяют Тх0, Тх1, Тх2, Тх3, Тх17 регуляторная функция. Взаимодействуют преимущественно с Вл Ø Т-индукторы. Взаимодействуют с Тх, Тс, ЦТЛ, Мф Ø Т-эффекторы ГЗТ. Секретируют лимфокины (MAF, MIF), обеспечивают эффекторный тип КИО и локализацию инфекции Ø Клетки-памяти. В основном, это Тх. Выживают в организме 40 лет, но эффективный ответ на АГ сохраняется 10 -15 лет
Субпопуляции CD 4+ Тл Ø Т-хелперы. По спектру цитокинов выделяют Тх0, Тх1, Тх2, Тх3, Тх17 регуляторная функция. Взаимодействуют преимущественно с Вл Ø Т-индукторы. Взаимодействуют с Тх, Тс, ЦТЛ, Мф Ø Т-эффекторы ГЗТ. Секретируют лимфокины (MAF, MIF), обеспечивают эффекторный тип КИО и локализацию инфекции Ø Клетки-памяти. В основном, это Тх. Выживают в организме 40 лет, но эффективный ответ на АГ сохраняется 10 -15 лет
 Соотношение основных популяций Лф
Соотношение основных популяций Лф
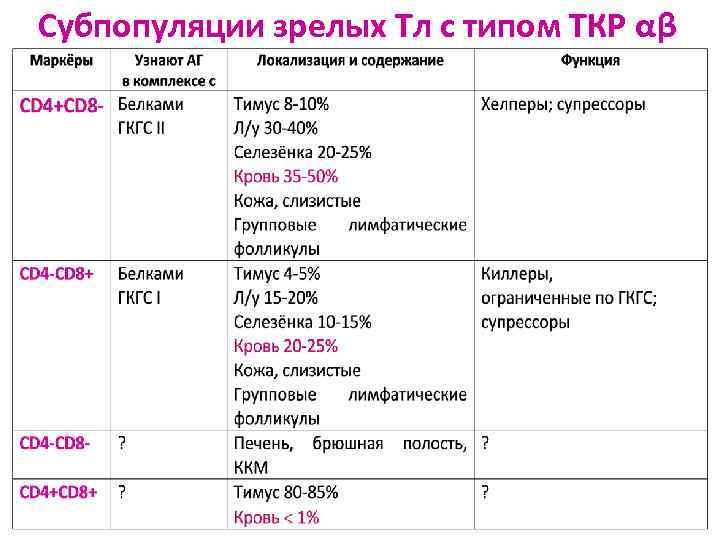 Субпопуляции зрелых Тл с типом ТКР αβ
Субпопуляции зрелых Тл с типом ТКР αβ
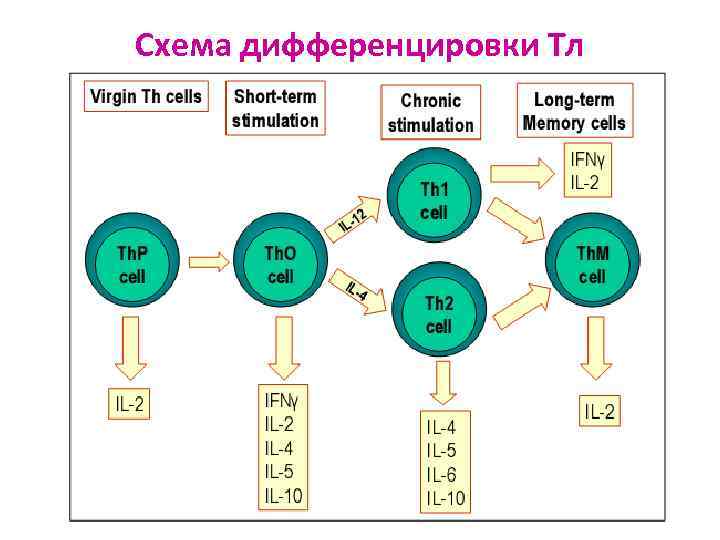 Схема дифференцировки Тл
Схема дифференцировки Тл
 Tх0 Ø узнают детерминантные группы АГ на мембране Мф, соединяются с ними, дают импульс к пролиферации и дифференцировке Ø секретируют все типы цитокинов Ø посредством цитокинов или образование Tх1, Tх2, Тх3, Тх17
Tх0 Ø узнают детерминантные группы АГ на мембране Мф, соединяются с ними, дают импульс к пролиферации и дифференцировке Ø секретируют все типы цитокинов Ø посредством цитокинов или образование Tх1, Tх2, Тх3, Тх17
 Ø Тh 3 – подавляют ИО: посредством цитокинов пролиферацию и дифференцировку Тл и Вл Ø Тh 17 – поддерживают воспаление, привлекают нейтрофилы
Ø Тh 3 – подавляют ИО: посредством цитокинов пролиферацию и дифференцировку Тл и Вл Ø Тh 17 – поддерживают воспаление, привлекают нейтрофилы
 Tх1 – воспалительные Ø активируют инфицированные Мф, что вызывает разрушение внутриклеточных МИО Ø стимулируют размножение и активность ЕК Ø синтезируют INF- , ИЛ 2, ФНО Ø за счёт выработки ИЛ 2 стимулируют пролиферацию и дифференцировку CD 8+ Тл в зрелые Тк
Tх1 – воспалительные Ø активируют инфицированные Мф, что вызывает разрушение внутриклеточных МИО Ø стимулируют размножение и активность ЕК Ø синтезируют INF- , ИЛ 2, ФНО Ø за счёт выработки ИЛ 2 стимулируют пролиферацию и дифференцировку CD 8+ Тл в зрелые Тк
 Tх2 – хелперные Ø экспрессируют мембрансвязанные адгезивные молекулы CD 40 L, которые связываются с CD 40 рецептором на Вл и индуцируют пролиферацию Вл Ø секретируют набор цитокинов, необходимый для ГИО: ростовые факторы Вл (ИЛ 4, ИЛ 5, ИЛ 6), а также ИЛ 10 Ø с помощью цитокинов активируют Вл, вызывая дифференцировку их в ПК, продуцирующие АТ Ø переключают синтез классов Ig Ø продуцируют ИЛ 4 эозинофилия Ø дегрануляция тучных клеток и Бф
Tх2 – хелперные Ø экспрессируют мембрансвязанные адгезивные молекулы CD 40 L, которые связываются с CD 40 рецептором на Вл и индуцируют пролиферацию Вл Ø секретируют набор цитокинов, необходимый для ГИО: ростовые факторы Вл (ИЛ 4, ИЛ 5, ИЛ 6), а также ИЛ 10 Ø с помощью цитокинов активируют Вл, вызывая дифференцировку их в ПК, продуцирующие АТ Ø переключают синтез классов Ig Ø продуцируют ИЛ 4 эозинофилия Ø дегрануляция тучных клеток и Бф
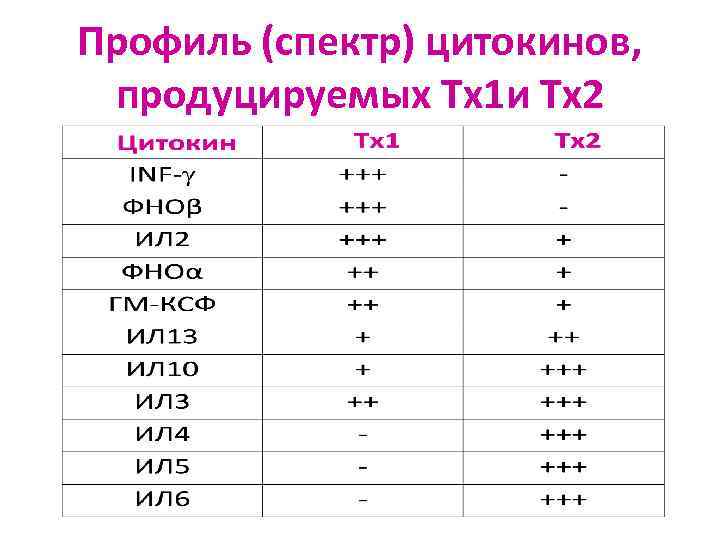 Профиль (спектр) цитокинов, продуцируемых Tх1 и Tх2
Профиль (спектр) цитокинов, продуцируемых Tх1 и Tх2
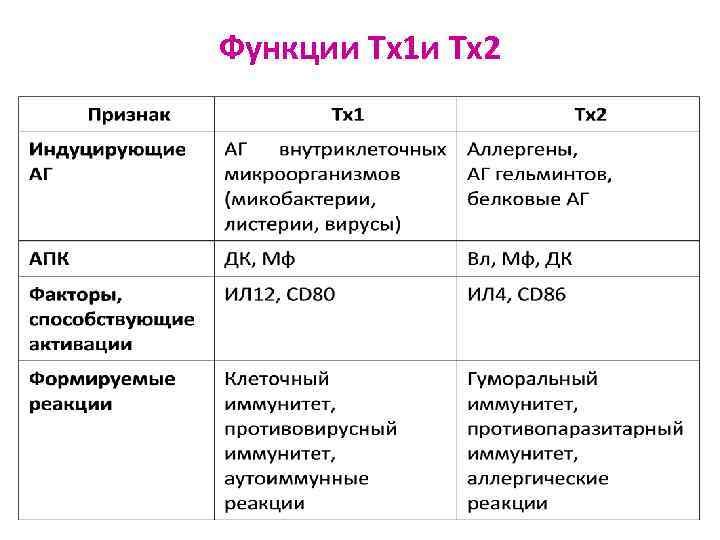 Функции Tх1 и Tх2
Функции Tх1 и Tх2
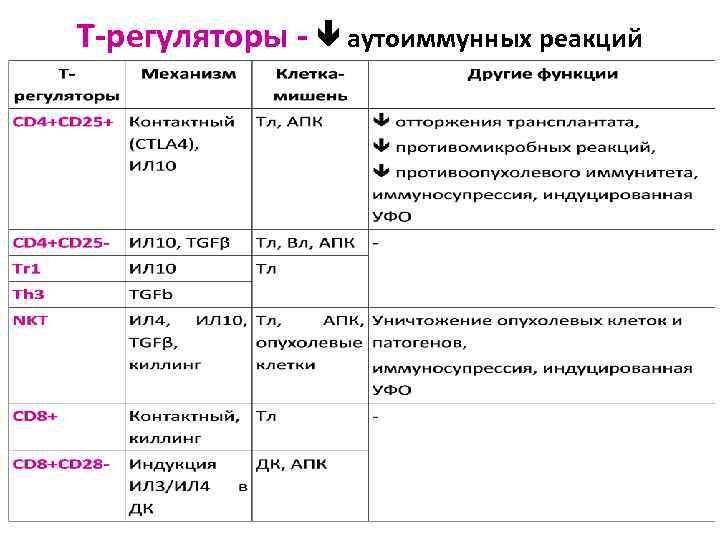 Т-регуляторы - аутоиммунных реакций
Т-регуляторы - аутоиммунных реакций
 Функция ТКР При помощи TКР Тл распознаёт специфический АГ в комплексе с молекулой ГКГС Тл активируется и выполняет свои функции (хелперные, цитотоксические)
Функция ТКР При помощи TКР Тл распознаёт специфический АГ в комплексе с молекулой ГКГС Тл активируется и выполняет свои функции (хелперные, цитотоксические)
 Антигены ГКГС (=МНС, HLA) Ø гликопротеины Ø прочно связанны с клеточной мембраной Ø играют ключевую роль в механизме распознавания чужеродного АГ: транспортируют пептиды (АГ) на клеточную поверхность и презентируют их Тл Ø !!! Тл распознают именно комплекс чужеродного АГ с антигеном ГКГС
Антигены ГКГС (=МНС, HLA) Ø гликопротеины Ø прочно связанны с клеточной мембраной Ø играют ключевую роль в механизме распознавания чужеродного АГ: транспортируют пептиды (АГ) на клеточную поверхность и презентируют их Тл Ø !!! Тл распознают именно комплекс чужеродного АГ с антигеном ГКГС
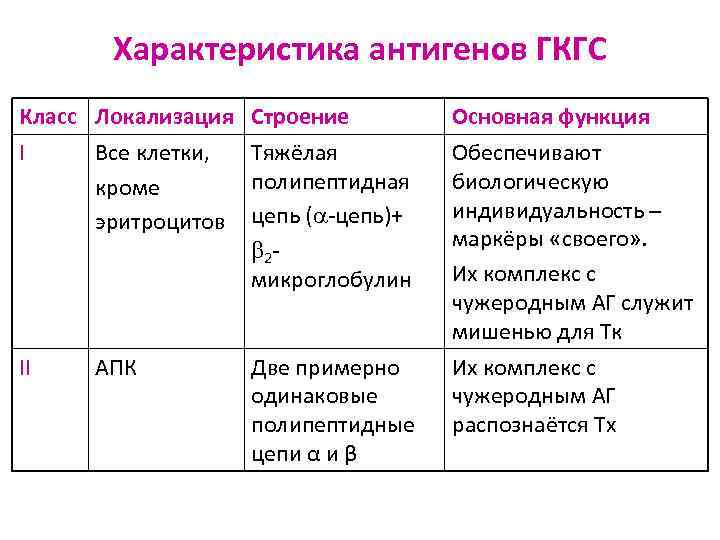 Характеристика антигенов ГКГС Класс Локализация Строение I Все клетки, Тяжёлая полипептидная кроме эритроцитов цепь ( -цепь)+ 2 микроглобулин Основная функция Обеспечивают биологическую индивидуальность – маркёры «своего» . Их комплекс с чужеродным АГ служит мишенью для Тк II Их комплекс с чужеродным АГ распознаётся Тх АПК Две примерно одинаковые полипептидные цепи α и β
Характеристика антигенов ГКГС Класс Локализация Строение I Все клетки, Тяжёлая полипептидная кроме эритроцитов цепь ( -цепь)+ 2 микроглобулин Основная функция Обеспечивают биологическую индивидуальность – маркёры «своего» . Их комплекс с чужеродным АГ служит мишенью для Тк II Их комплекс с чужеродным АГ распознаётся Тх АПК Две примерно одинаковые полипептидные цепи α и β
 Строение молекулы ГКГС I Молекула ГКГС I состоит из: - белковой α-цепи, которая имеет: 3 внеклеточных домена трансмембранный домен ЦП домен (он закрепляет α-цепь в мембране) - β 2 -микроглобулина, который нековалентно присоединяется к α-цепи после закрепления её в мембране Щель Бьоркмана для присоединения фрагментов чужеродного АГ находится между первыми двумя внеклеточными доменами α-цепи. В отсутствие фрагментов чужеродного АГ здесь находится стабилизирующий шаперон – белок калнексин
Строение молекулы ГКГС I Молекула ГКГС I состоит из: - белковой α-цепи, которая имеет: 3 внеклеточных домена трансмембранный домен ЦП домен (он закрепляет α-цепь в мембране) - β 2 -микроглобулина, который нековалентно присоединяется к α-цепи после закрепления её в мембране Щель Бьоркмана для присоединения фрагментов чужеродного АГ находится между первыми двумя внеклеточными доменами α-цепи. В отсутствие фрагментов чужеродного АГ здесь находится стабилизирующий шаперон – белок калнексин
 Образование комплекса АГ+молекула ГКГС I на мембране СD 8+ Тл Чужеродные АГ (напр. , АГвирусов), проникшие в клетку без формирования фаголизосомы, находятся в цитозоле. Для их процессинга образуется специальная структура – протеосома, где чужеродный АГ гидролитически фрагментируется. Образующиеся фрагменты связываются с белками ТАР-1 и ТАР-2 (англ. Transporters associated with Antigen Processing). Эти белки обеспечивают энергозависимый транспорт фрагментов внутрь тех участков ЭПС, где происходит сборка молекул ГКГС I. Фрагмент чужеродного АГ попадает в щель Бьоркмана, когда αцепь уже закреплена в мембране, но свободна от β 2 -микроглобулина. Прикрепление β 2 -микроглобулина – сигнал для отщепления калнексина, т. к. «загруженный» чужеродным пептидом ГКГС I уже не нуждается в стабилизации и сохраняет конформацию после выноса на наружную поверхность мембраны фагоцита.
Образование комплекса АГ+молекула ГКГС I на мембране СD 8+ Тл Чужеродные АГ (напр. , АГвирусов), проникшие в клетку без формирования фаголизосомы, находятся в цитозоле. Для их процессинга образуется специальная структура – протеосома, где чужеродный АГ гидролитически фрагментируется. Образующиеся фрагменты связываются с белками ТАР-1 и ТАР-2 (англ. Transporters associated with Antigen Processing). Эти белки обеспечивают энергозависимый транспорт фрагментов внутрь тех участков ЭПС, где происходит сборка молекул ГКГС I. Фрагмент чужеродного АГ попадает в щель Бьоркмана, когда αцепь уже закреплена в мембране, но свободна от β 2 -микроглобулина. Прикрепление β 2 -микроглобулина – сигнал для отщепления калнексина, т. к. «загруженный» чужеродным пептидом ГКГС I уже не нуждается в стабилизации и сохраняет конформацию после выноса на наружную поверхность мембраны фагоцита.
 Строение молекула ГКГС II Молекула ГКГС II состоит из: 2 полипептидных цепей α и β, каждая из которых имеет: небольшой ЦП участок, трансмембранный домен и внеклеточный регион. Щель Бьоркмана для присоединения фрагментов чужеродного АГ находится между внеклеточными областями цепей. В отсутствие фрагментов чужеродного АГ она заполнена белком с Мм 35 k. D (= инвариантная цепь, Ii-цепь). Размер щели невелик, поэтому в неё входит только определённый участок Ii-цепи (25 АК остатков). Такое заполнение щели защищает формирующийся комплекс от случайного попадания в него собственных пептидов. Фрагмент ЭПС отделяется, образовавшаяся мембранная везикула направляется к наружной ЦПМ. Если в клетке отсутствуют фаголизосомы, эта везикула достигает мембраны, и на поверхность клетки путём экзоцитоза выводится «пустой» белок ГКГС II.
Строение молекула ГКГС II Молекула ГКГС II состоит из: 2 полипептидных цепей α и β, каждая из которых имеет: небольшой ЦП участок, трансмембранный домен и внеклеточный регион. Щель Бьоркмана для присоединения фрагментов чужеродного АГ находится между внеклеточными областями цепей. В отсутствие фрагментов чужеродного АГ она заполнена белком с Мм 35 k. D (= инвариантная цепь, Ii-цепь). Размер щели невелик, поэтому в неё входит только определённый участок Ii-цепи (25 АК остатков). Такое заполнение щели защищает формирующийся комплекс от случайного попадания в него собственных пептидов. Фрагмент ЭПС отделяется, образовавшаяся мембранная везикула направляется к наружной ЦПМ. Если в клетке отсутствуют фаголизосомы, эта везикула достигает мембраны, и на поверхность клетки путём экзоцитоза выводится «пустой» белок ГКГС II.
 Образование комплекса АГ+молекула ГКГС II на мембране СD 4+ Тл Если Мф начал процессинг поглощённого чужеродного АГ, то везикулы сливаются с фаголизосомами, и формируются компартменты «загрузки» белка ГКГС II (англ. CPL - Compartment for Peptide Loading) Кислые протеазы фаголизосом расщепляют Ii-цепь, АГсвязывающая щель освобождается, и в неё встраивается фрагмент чужеродного АГ Далее CPL достигает наружной ЦПМ, и на поверхность клетки выставляется «загруженный» белок ГКГС II, который должен распознаваться в дальнейшем Тх
Образование комплекса АГ+молекула ГКГС II на мембране СD 4+ Тл Если Мф начал процессинг поглощённого чужеродного АГ, то везикулы сливаются с фаголизосомами, и формируются компартменты «загрузки» белка ГКГС II (англ. CPL - Compartment for Peptide Loading) Кислые протеазы фаголизосом расщепляют Ii-цепь, АГсвязывающая щель освобождается, и в неё встраивается фрагмент чужеродного АГ Далее CPL достигает наружной ЦПМ, и на поверхность клетки выставляется «загруженный» белок ГКГС II, который должен распознаваться в дальнейшем Тх
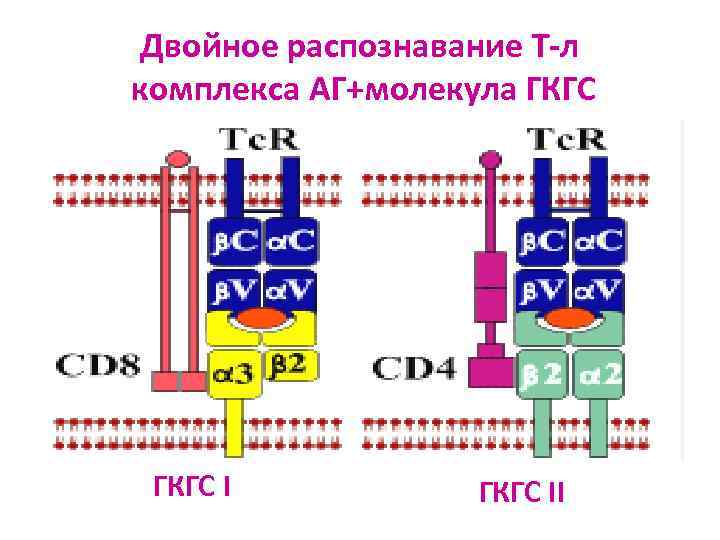 Двойное распознавание Т-л комплекса АГ+молекула ГКГС II
Двойное распознавание Т-л комплекса АГ+молекула ГКГС II
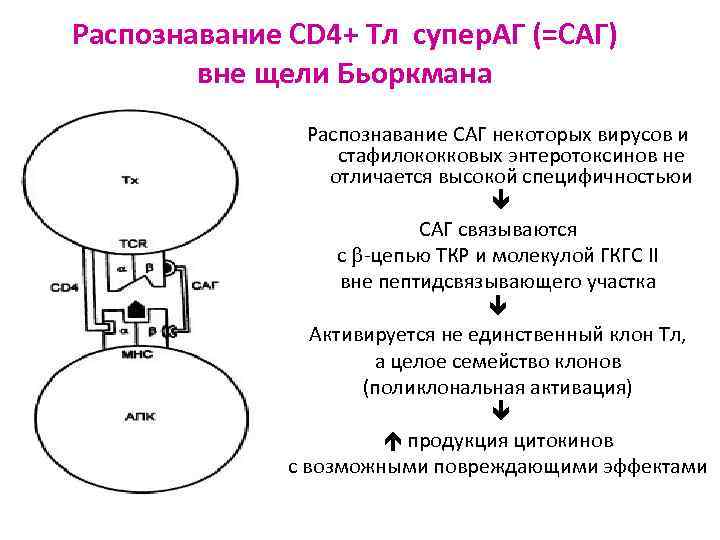 Распознавание СD 4+ Тл супер. АГ (=САГ) вне щели Бьоркмана Распознавание САГ некоторых вирусов и стафилококковых энтеротоксинов не отличается высокой специфичностьюи САГ связываются с -цепью TКР и молекулой ГКГС II вне пептидсвязывающего участка Активируется не единственный клон Тл, а целое семейство клонов (поликлональная активация) продукция цитокинов с возможными повреждающими эффектами
Распознавание СD 4+ Тл супер. АГ (=САГ) вне щели Бьоркмана Распознавание САГ некоторых вирусов и стафилококковых энтеротоксинов не отличается высокой специфичностьюи САГ связываются с -цепью TКР и молекулой ГКГС II вне пептидсвязывающего участка Активируется не единственный клон Тл, а целое семейство клонов (поликлональная активация) продукция цитокинов с возможными повреждающими эффектами
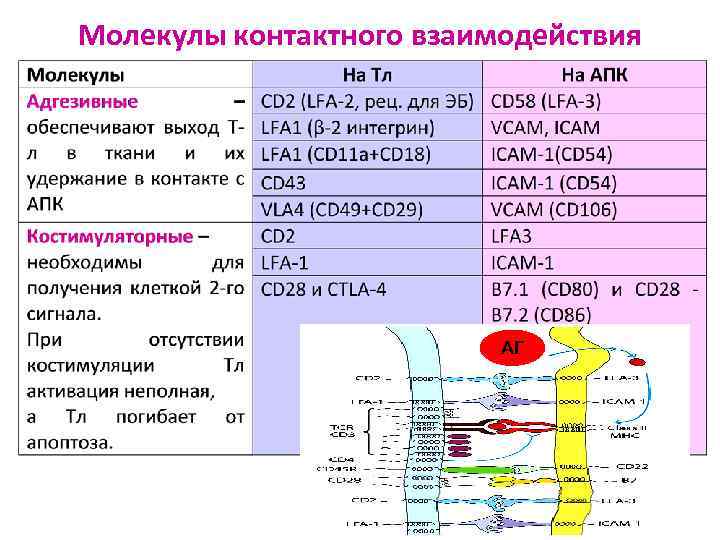 Молекулы контактного взаимодействия АГ АГ
Молекулы контактного взаимодействия АГ АГ
 При кооперации АПК и Тл происходит множественное взаимодействие молекул 1. TКР узнает пептид 2. Дополнительно взаимодействуют корецепторные молекулы: CD 4 с молекулами ГКГС II или CD 8 с молекулами ГКГС I 3. Обязательно участвуют молекулы контактного взаимодействия (адгезивные, костимуляторные)
При кооперации АПК и Тл происходит множественное взаимодействие молекул 1. TКР узнает пептид 2. Дополнительно взаимодействуют корецепторные молекулы: CD 4 с молекулами ГКГС II или CD 8 с молекулами ГКГС I 3. Обязательно участвуют молекулы контактного взаимодействия (адгезивные, костимуляторные)
 ЭТАПЫ АКТИВАЦИИ Тл 1. Мембранный - распознавание Тл комплекса пептид+ГКГС I или II и костимуляторное взаимодействие CD 28 - CD 80/86 2. Цитоплазматический - активация белков, связанных с ДНК Т-л 3. Активация генов ИЛ 2 и его рецептора синтез ИЛ 2, пролиферация Тл и дифференцировка в зрелые Тл
ЭТАПЫ АКТИВАЦИИ Тл 1. Мембранный - распознавание Тл комплекса пептид+ГКГС I или II и костимуляторное взаимодействие CD 28 - CD 80/86 2. Цитоплазматический - активация белков, связанных с ДНК Т-л 3. Активация генов ИЛ 2 и его рецептора синтез ИЛ 2, пролиферация Тл и дифференцировка в зрелые Тл
 Мембранный этап активации Тл включает 2 сигнала 1. Связывание ТКР с комплексом пептид-ГКГС I или II: - изменение конформации CD 3 (сближение CD 3 и корецепторов CD 4 или CD 8) - фосфорилирование тирозина - активация киназ активация транскрипционных факторов (NFAT и частично АР-1), изменение цитоскелета, отмена апоптоза 2. Костимуляторное взаимодействие CD 28 - CD 80/86 Образуются транскрипционные факторы (активный NFk. B и полноценный АР-1) При получении 2 сигналов активируются 3 транскрипционных фактора (NFAT, NFk. B и AP-1), необходимые для активации генов ИЛ 2 и его рецептора
Мембранный этап активации Тл включает 2 сигнала 1. Связывание ТКР с комплексом пептид-ГКГС I или II: - изменение конформации CD 3 (сближение CD 3 и корецепторов CD 4 или CD 8) - фосфорилирование тирозина - активация киназ активация транскрипционных факторов (NFAT и частично АР-1), изменение цитоскелета, отмена апоптоза 2. Костимуляторное взаимодействие CD 28 - CD 80/86 Образуются транскрипционные факторы (активный NFk. B и полноценный АР-1) При получении 2 сигналов активируются 3 транскрипционных фактора (NFAT, NFk. B и AP-1), необходимые для активации генов ИЛ 2 и его рецептора
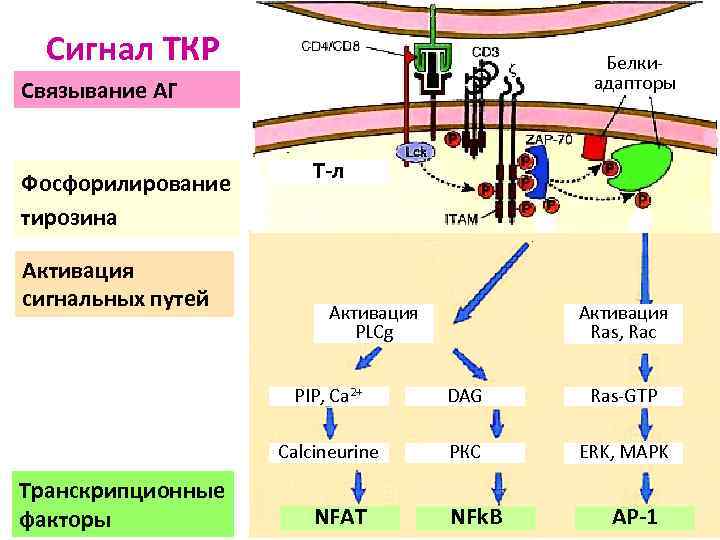 Сигнал ТКР Белкиадапторы Связывание АГ Фосфорилирование тирозина Активация сигнальных путей Т-л Активация PLCg Активация Ras, Rac PIP, Ca 2+ Ras-GTP Calcineurine Транскрипционные факторы DAG PКС ERK, MAPK NFAT NFk. B AP-1
Сигнал ТКР Белкиадапторы Связывание АГ Фосфорилирование тирозина Активация сигнальных путей Т-л Активация PLCg Активация Ras, Rac PIP, Ca 2+ Ras-GTP Calcineurine Транскрипционные факторы DAG PКС ERK, MAPK NFAT NFk. B AP-1
 Цитоплазматический этап активации Тл при распознавании АГ сигнал с мембраны клетки запускается каскад протеинкиназ (с ними связаны цитозольные хвосты рецепторов) вовлекается фосфолипаза С активируются белки, связанные с ДНК Тл
Цитоплазматический этап активации Тл при распознавании АГ сигнал с мембраны клетки запускается каскад протеинкиназ (с ними связаны цитозольные хвосты рецепторов) вовлекается фосфолипаза С активируются белки, связанные с ДНК Тл
 Активация генов ИЛ 2 и его рецептора клетки синтезируют и рецептируют ИЛ 2 под действием ИЛ 2 ч/з 12 ч Тл трансформируются в бласты пролиферируют дифференцируются в зрелые Тл
Активация генов ИЛ 2 и его рецептора клетки синтезируют и рецептируют ИЛ 2 под действием ИЛ 2 ч/з 12 ч Тл трансформируются в бласты пролиферируют дифференцируются в зрелые Тл
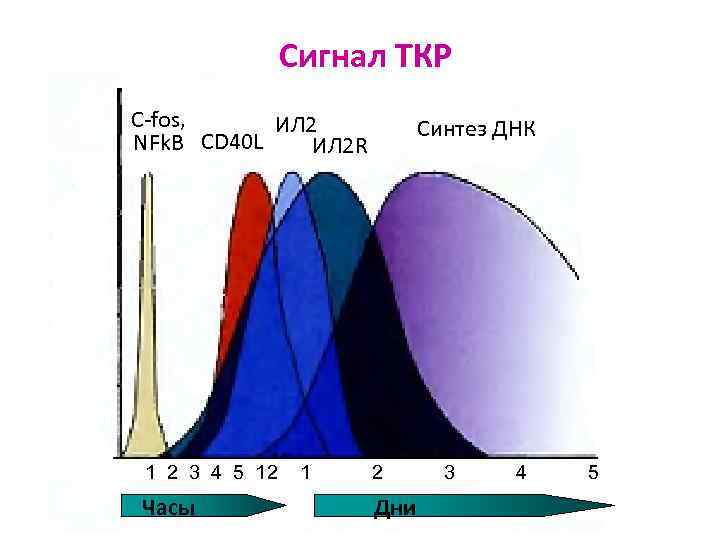 Сигнал ТКР С-fos, ИЛ 2 NFk. B CD 40 L ИЛ 2 R 1 2 3 4 5 12 Часы 1 Синтез ДНК 2 Дни 3 4 5
Сигнал ТКР С-fos, ИЛ 2 NFk. B CD 40 L ИЛ 2 R 1 2 3 4 5 12 Часы 1 Синтез ДНК 2 Дни 3 4 5
 Иммунный ответ Гуморальный (ГИО) Клеточный (КИО)
Иммунный ответ Гуморальный (ГИО) Клеточный (КИО)
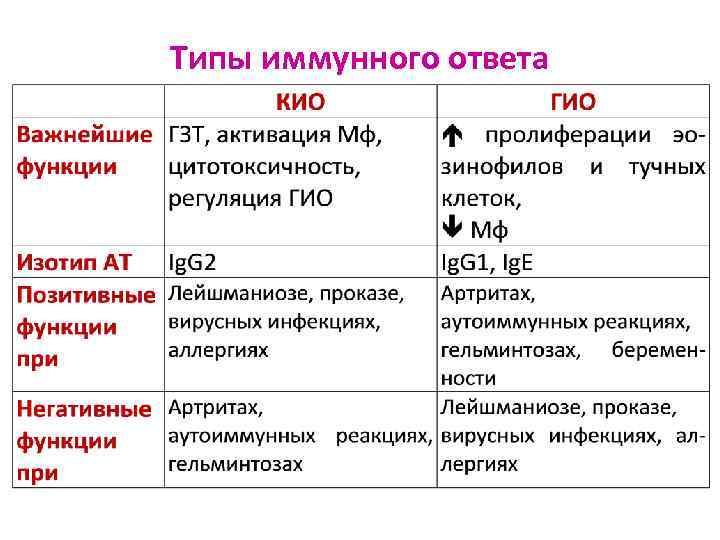 Типы иммунного ответа
Типы иммунного ответа
 КИО - кооперативная реакция ИС Ø Ø Ø индуцируется АГ реализуется Тл в кооперации с АПК представляют Тл АГ в ассоциации с молекулами ГКГС завершается формированием АГспецифических Тл, выполняющих регуляторную (регуляция ИО) и эффекторную (элиминация АГ) функции характеризуется специфичностью и иммунологической памятью
КИО - кооперативная реакция ИС Ø Ø Ø индуцируется АГ реализуется Тл в кооперации с АПК представляют Тл АГ в ассоциации с молекулами ГКГС завершается формированием АГспецифических Тл, выполняющих регуляторную (регуляция ИО) и эффекторную (элиминация АГ) функции характеризуется специфичностью и иммунологической памятью
 Индукторы КИО - Т-зависимые АГ Ø Белковые АГ: - собственные изменённые АГ (опухолевые, ауто. АГ) - внутриклеточно расположенные МИО (вирусы, бактерии, грибы, простейшие) - простые химические вещества (бытовые, промышленные, с/х, лекарственные), если они связались с белками организма (осели на клетках) и стали АГ Ø Не нативная молекула АГ, а его переработанная (процессированная) форма - пептид АГ должен ассоциироваться с молекулами ГКГС I или II
Индукторы КИО - Т-зависимые АГ Ø Белковые АГ: - собственные изменённые АГ (опухолевые, ауто. АГ) - внутриклеточно расположенные МИО (вирусы, бактерии, грибы, простейшие) - простые химические вещества (бытовые, промышленные, с/х, лекарственные), если они связались с белками организма (осели на клетках) и стали АГ Ø Не нативная молекула АГ, а его переработанная (процессированная) форма - пептид АГ должен ассоциироваться с молекулами ГКГС I или II
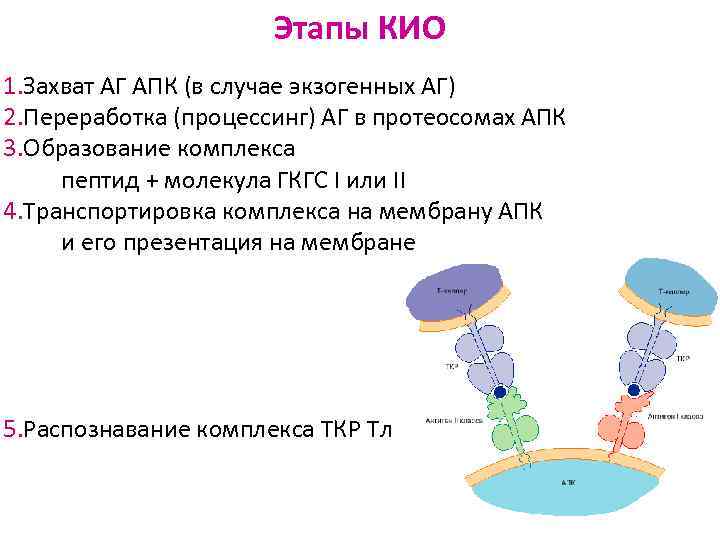 Этапы КИО 1. Захват АГ АПК (в случае экзогенных АГ) 2. Переработка (процессинг) АГ в протеосомах АПК 3. Образование комплекса пептид + молекула ГКГС I или II 4. Транспортировка комплекса на мембрану АПК и его презентация на мембране 5. Распознавание комплекса ТКР Тл
Этапы КИО 1. Захват АГ АПК (в случае экзогенных АГ) 2. Переработка (процессинг) АГ в протеосомах АПК 3. Образование комплекса пептид + молекула ГКГС I или II 4. Транспортировка комплекса на мембрану АПК и его презентация на мембране 5. Распознавание комплекса ТКР Тл
 Этапы КИО (продолжение) 6. Активация Тл 7. АГ-зависимая пролиферация и дифференцировка Тл 8. Образование зрелых клеток-эффекторов разных субпопуляций; клеток памяти 6. Взаимодействие клеток-эффекторов с АГ и реализация конечных эффектов ИО: Tх1 регуляция КИО Tх2 регуляция ГИО цитотоксическая реакция уничтожение клеток-мишеней
Этапы КИО (продолжение) 6. Активация Тл 7. АГ-зависимая пролиферация и дифференцировка Тл 8. Образование зрелых клеток-эффекторов разных субпопуляций; клеток памяти 6. Взаимодействие клеток-эффекторов с АГ и реализация конечных эффектов ИО: Tх1 регуляция КИО Tх2 регуляция ГИО цитотоксическая реакция уничтожение клеток-мишеней
 Индукторная стадия генерации Тх Ø ДК поглощает АГ, процессирует его по эндосомному пути, перемещается в л/у (клетка Лангерганса) Ø Наивный Тх0 в Т-клеточной зоне л/уз распознаёт пептид АГ в комплексе с ГКГС II. Костимуляция осуществляется ч/з CD 28 -CD 80/86. Тип ответа определяется цитокинами: под действием ИЛ 12 генерируются Тх1, под действием ИЛ 4 генерируются Тх2 Ø Тх активируется превращается в бласт пролиферирует дифференцируется на Тх памяти и зрелые Тх Ø Зрелый специализированный Тх выходит в кровоток и вступает в рециркуляцию
Индукторная стадия генерации Тх Ø ДК поглощает АГ, процессирует его по эндосомному пути, перемещается в л/у (клетка Лангерганса) Ø Наивный Тх0 в Т-клеточной зоне л/уз распознаёт пептид АГ в комплексе с ГКГС II. Костимуляция осуществляется ч/з CD 28 -CD 80/86. Тип ответа определяется цитокинами: под действием ИЛ 12 генерируются Тх1, под действием ИЛ 4 генерируются Тх2 Ø Тх активируется превращается в бласт пролиферирует дифференцируется на Тх памяти и зрелые Тх Ø Зрелый специализированный Тх выходит в кровоток и вступает в рециркуляцию
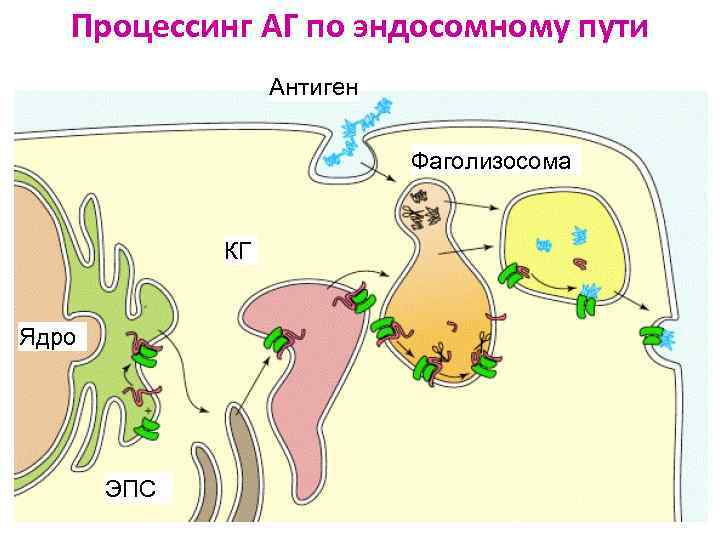 Процессинг АГ по эндосомному пути Антиген Фаголизосома КГ Ядро ЭПС
Процессинг АГ по эндосомному пути Антиген Фаголизосома КГ Ядро ЭПС
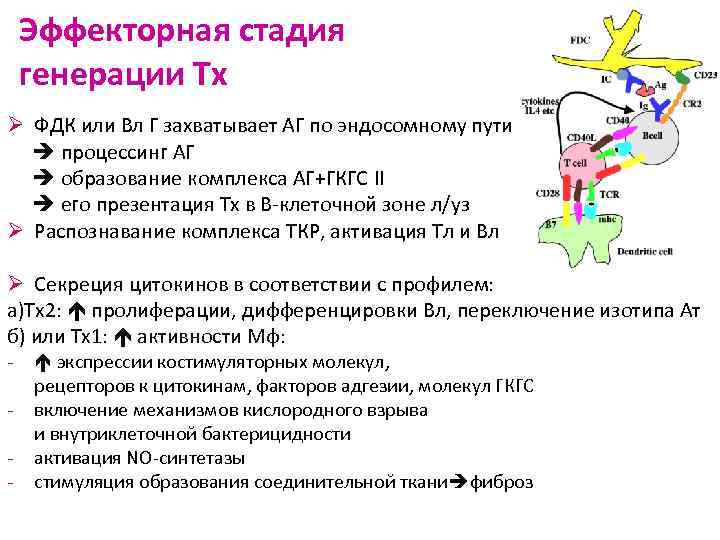 Эффекторная стадия генерации Тх Ø ФДК или Вл Г захватывает АГ по эндосомному пути процессинг АГ образование комплекса АГ+ГКГС II его презентация Тх в В-клеточной зоне л/уз Ø Распознавание комплекса TКР, активация Тл и Вл Ø Секреция цитокинов в соответствии с профилем: а)Tх2: пролиферации, дифференцировки Вл, переключение изотипа Ат б) или Tх1: активности Мф: - экспрессии костимуляторных молекул, рецепторов к цитокинам, факторов адгезии, молекул ГКГС включение механизмов кислородного взрыва и внутриклеточной бактерицидности активация NO-синтетазы стимуляция образования соединительной ткани фиброз
Эффекторная стадия генерации Тх Ø ФДК или Вл Г захватывает АГ по эндосомному пути процессинг АГ образование комплекса АГ+ГКГС II его презентация Тх в В-клеточной зоне л/уз Ø Распознавание комплекса TКР, активация Тл и Вл Ø Секреция цитокинов в соответствии с профилем: а)Tх2: пролиферации, дифференцировки Вл, переключение изотипа Ат б) или Tх1: активности Мф: - экспрессии костимуляторных молекул, рецепторов к цитокинам, факторов адгезии, молекул ГКГС включение механизмов кислородного взрыва и внутриклеточной бактерицидности активация NO-синтетазы стимуляция образования соединительной ткани фиброз
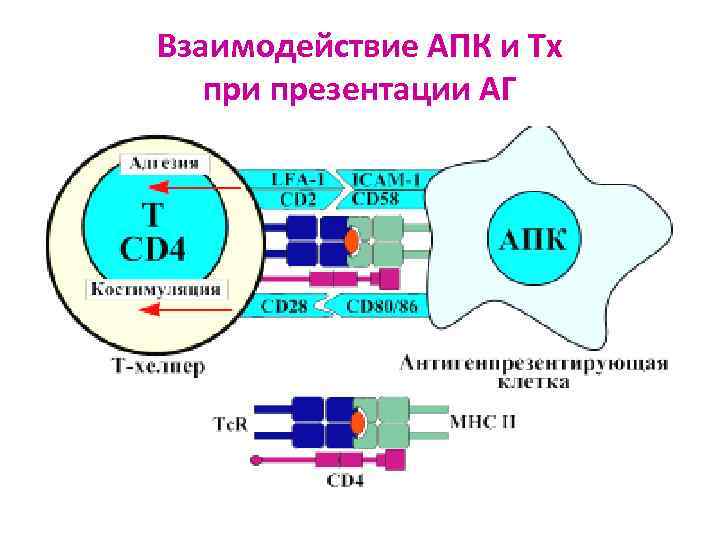 Взаимодействие АПК и Тх при презентации АГ
Взаимодействие АПК и Тх при презентации АГ
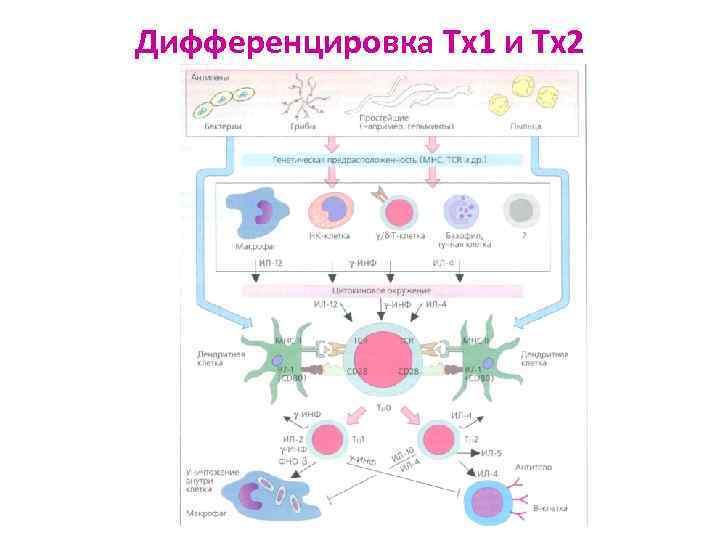 Дифференцировка Тх1 и Тх2
Дифференцировка Тх1 и Тх2
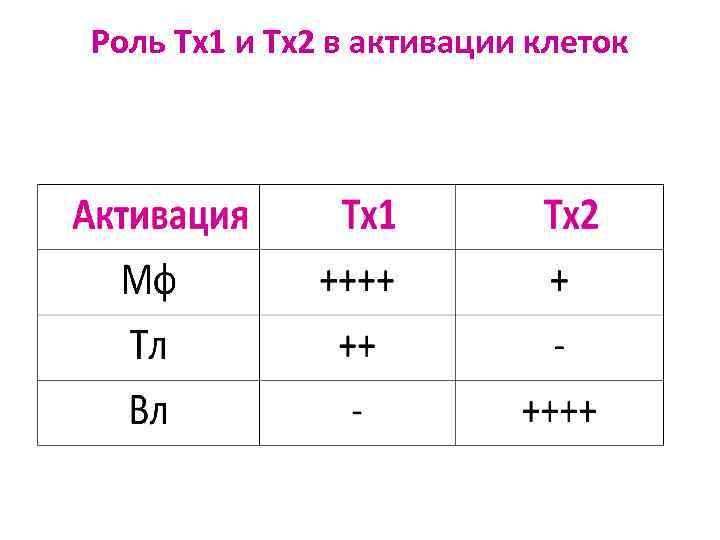 Роль Тх1 и Тх2 в активации клеток
Роль Тх1 и Тх2 в активации клеток
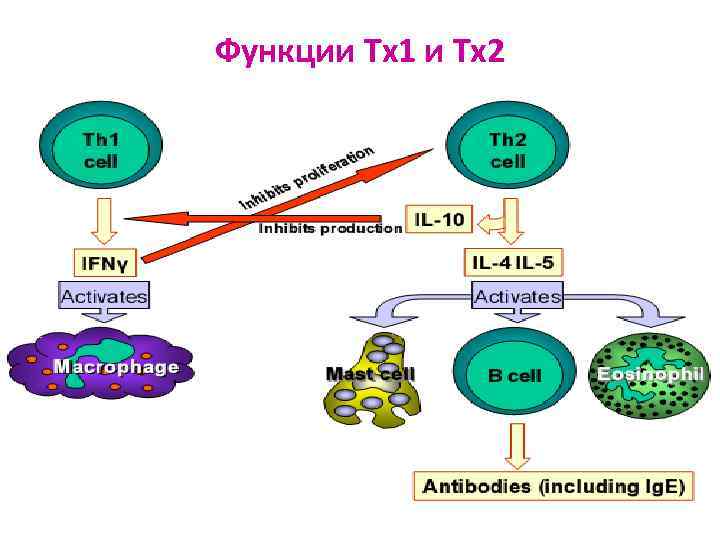 Функции Tх1 и Tх2
Функции Tх1 и Tх2
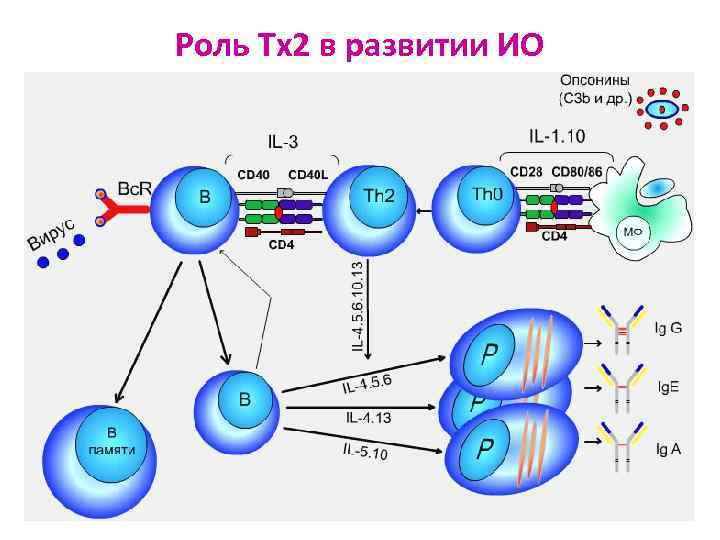 Роль Тх2 в развитии ИО
Роль Тх2 в развитии ИО
 Управление переключением изотипа АТ
Управление переключением изотипа АТ
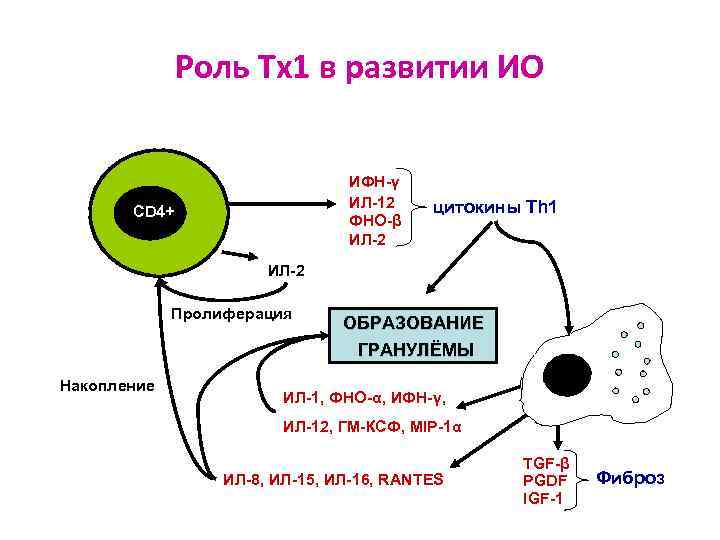 Роль Тх1 в развитии ИО ИФН-γ ИЛ-12 ФНО-β ИЛ-2 CD 4+ цитокины Th 1 ИЛ-2 Пролиферация Накопление ОБРАЗОВАНИЕ ГРАНУЛЁМЫ ИЛ-1, ФНО-α, ИФН-γ, ИЛ-12, ГМ-КСФ, MIP-1α ИЛ-8, ИЛ-15, ИЛ-16, RANTES TGF-β PGDF IGF-1 Фиброз
Роль Тх1 в развитии ИО ИФН-γ ИЛ-12 ФНО-β ИЛ-2 CD 4+ цитокины Th 1 ИЛ-2 Пролиферация Накопление ОБРАЗОВАНИЕ ГРАНУЛЁМЫ ИЛ-1, ФНО-α, ИФН-γ, ИЛ-12, ГМ-КСФ, MIP-1α ИЛ-8, ИЛ-15, ИЛ-16, RANTES TGF-β PGDF IGF-1 Фиброз
 Т-эффекторный путь ИО Реализуется Т-эффекторами, которые продуцируют лимфокины ( 30): Ø Хемотаксический фактор - способствует миграции клеток к месту реакции. Ø Фактор проницаемости сосудов. Ø Фактор, миграцию Мф - для предотвращения разноса непереваренного микроба макрофагами по организму. Ø Фактор агрегации тромбоцитов - для нарушения реалогии крови. Ø Фактор активации деятельности фибробластов. В результате действия лимфокинов очаг ограничивается и формируется инфекционная гранулёма
Т-эффекторный путь ИО Реализуется Т-эффекторами, которые продуцируют лимфокины ( 30): Ø Хемотаксический фактор - способствует миграции клеток к месту реакции. Ø Фактор проницаемости сосудов. Ø Фактор, миграцию Мф - для предотвращения разноса непереваренного микроба макрофагами по организму. Ø Фактор агрегации тромбоцитов - для нарушения реалогии крови. Ø Фактор активации деятельности фибробластов. В результате действия лимфокинов очаг ограничивается и формируется инфекционная гранулёма
 Индукторная стадия генерации Тк Ø АГ должен поступить в цитоплазматический путь. ДК захватывают АГ по эндосомному пути (лизис фагосом, транспорт полипептидов в ЦП и в везикулы комплекса Гольджи) Ø Образование комплекса полипептид АГ+ГКГС I, презентация комплекса пре-Тк в Т-клеточной зоне л/уз Ø Распознавание комплекса TКР, активация пре-Тк и Тх (пре-Тк нужна помощь Тх) Ø Костимуляция ч/з CD 28 -CD 80/86, CD 40 L-CD 40, секрецию цитокинов (ИЛ 2, 15) Ø Пре-Тк активируется пролиферирует дифференцируется в зрелые Тк (из 1 клетки получается до 100000 зрелых Тк) Ø Зрелые Тк покидают л/уз и вступают в рециркуляцию
Индукторная стадия генерации Тк Ø АГ должен поступить в цитоплазматический путь. ДК захватывают АГ по эндосомному пути (лизис фагосом, транспорт полипептидов в ЦП и в везикулы комплекса Гольджи) Ø Образование комплекса полипептид АГ+ГКГС I, презентация комплекса пре-Тк в Т-клеточной зоне л/уз Ø Распознавание комплекса TКР, активация пре-Тк и Тх (пре-Тк нужна помощь Тх) Ø Костимуляция ч/з CD 28 -CD 80/86, CD 40 L-CD 40, секрецию цитокинов (ИЛ 2, 15) Ø Пре-Тк активируется пролиферирует дифференцируется в зрелые Тк (из 1 клетки получается до 100000 зрелых Тк) Ø Зрелые Тк покидают л/уз и вступают в рециркуляцию
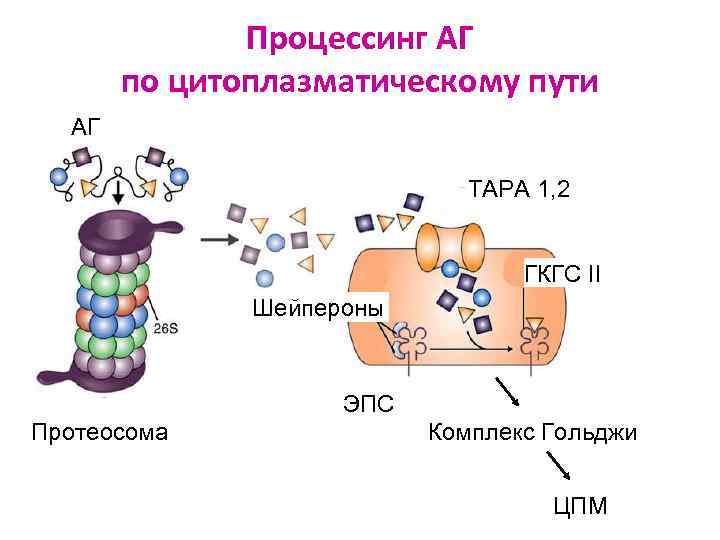 Процессинг АГ по цитоплазматическому пути АГ TAPA 1, 2 ГКГС II Шейпероны ЭПС Протеосома Комплекс Гольджи ЦПМ
Процессинг АГ по цитоплазматическому пути АГ TAPA 1, 2 ГКГС II Шейпероны ЭПС Протеосома Комплекс Гольджи ЦПМ
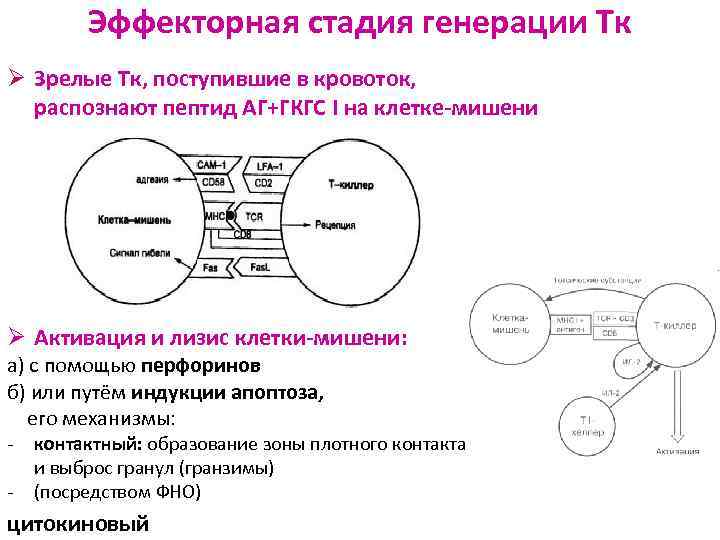 Эффекторная стадия генерации Тк Ø Зрелые Тк, поступившие в кровоток, распознают пептид АГ+ГКГС I на клетке-мишени Ø Активация и лизис клетки-мишени: а) с помощью перфоринов б) или путём индукции апоптоза, его механизмы: - контактный: образование зоны плотного контакта и выброс гранул (гранзимы) (посредством ФНО) цитокиновый
Эффекторная стадия генерации Тк Ø Зрелые Тк, поступившие в кровоток, распознают пептид АГ+ГКГС I на клетке-мишени Ø Активация и лизис клетки-мишени: а) с помощью перфоринов б) или путём индукции апоптоза, его механизмы: - контактный: образование зоны плотного контакта и выброс гранул (гранзимы) (посредством ФНО) цитокиновый
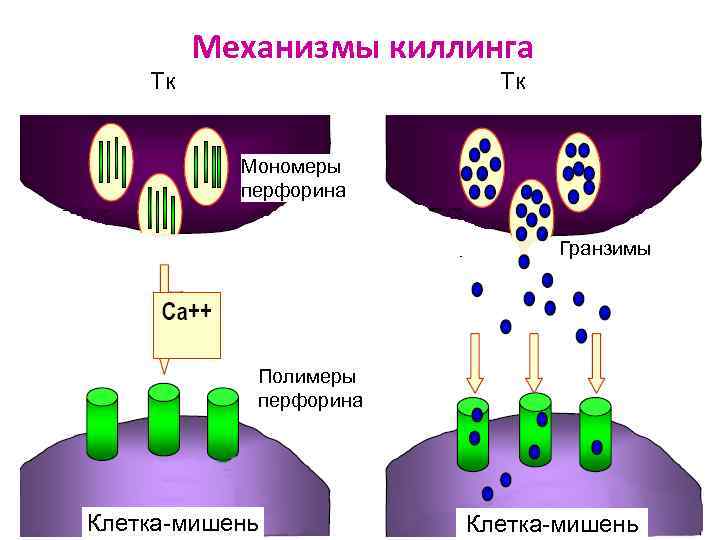 Механизмы киллинга Тк Тк Мономеры перфорина Гранзимы Полимеры перфорина Клетка-мишень
Механизмы киллинга Тк Тк Мономеры перфорина Гранзимы Полимеры перфорина Клетка-мишень
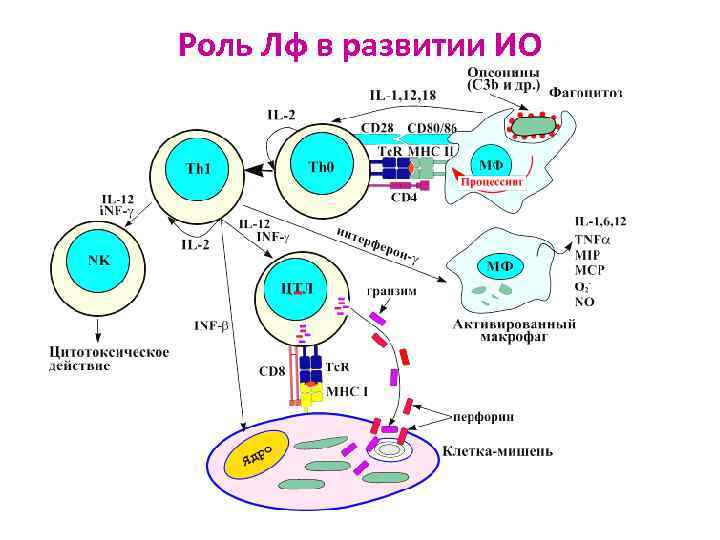 Роль Лф в развитии ИО
Роль Лф в развитии ИО
 Формы и проявления КИО Ø противоинфекционный иммунитет: • противовирусный • против внутриклеточных бактерий • противопаразитарный Ø Ø Ø иммунологическая Т-память аллергические реакции IV типа (ГЗТ) противоопухолевый иммунитет трансплантационный иммунитет ИТ (физиология беременности и толерантность к АГ плода) Нежелательные последствия КИО: Ø хроническое воспаление Ø аутоиммунные клеточно-опосредованные реакции (повреждение тканей) Ø отторжение трансплантата
Формы и проявления КИО Ø противоинфекционный иммунитет: • противовирусный • против внутриклеточных бактерий • противопаразитарный Ø Ø Ø иммунологическая Т-память аллергические реакции IV типа (ГЗТ) противоопухолевый иммунитет трансплантационный иммунитет ИТ (физиология беременности и толерантность к АГ плода) Нежелательные последствия КИО: Ø хроническое воспаление Ø аутоиммунные клеточно-опосредованные реакции (повреждение тканей) Ø отторжение трансплантата
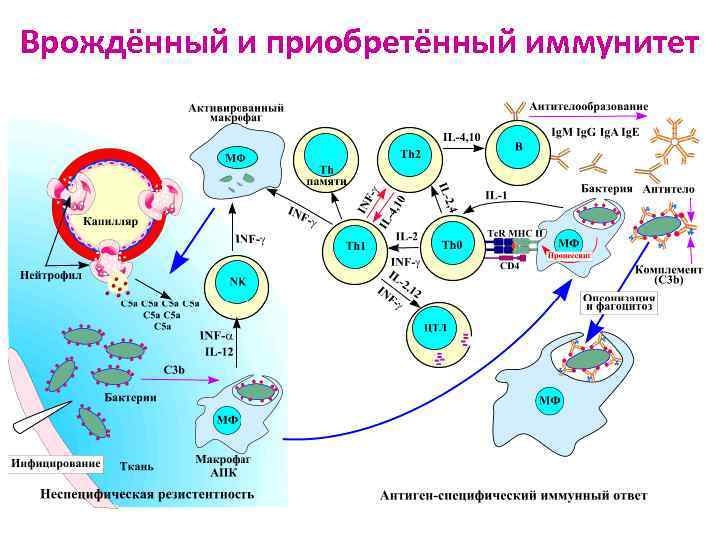 Врождённый и приобретённый иммунитет
Врождённый и приобретённый иммунитет
 АНЕРГИЯ – полная или частичная утрата организмом специфической иммунологической реактивности (=развитие неотвечаемости на АГ) In vitro и in vivo характерно или отсутствие пролиферативного ответа CD 4+ Тл на специфические АГ и митогены Ø Ø Ø In vivo выявляется с помощью внутрикожных тестов на анамнестические АГ. Отрицательные результаты наблюдаются при ВИЧ-инфекции, туберкулёзе, лепре, у онкобольных.
АНЕРГИЯ – полная или частичная утрата организмом специфической иммунологической реактивности (=развитие неотвечаемости на АГ) In vitro и in vivo характерно или отсутствие пролиферативного ответа CD 4+ Тл на специфические АГ и митогены Ø Ø Ø In vivo выявляется с помощью внутрикожных тестов на анамнестические АГ. Отрицательные результаты наблюдаются при ВИЧ-инфекции, туберкулёзе, лепре, у онкобольных.
 Виды анергии 1. Центральная - формируется внутриутробно к собственным АГ (ауто. АГ) Механизм: на ранних стадиях развития плода аутореактивные клоны незрелых Лф элиминируются 2. Периферическая - полная или частичная утрата способности ИКК к активации Механизмы: блокирование АГ-специфических рецепторов, повреждение механизмов костимуляции
Виды анергии 1. Центральная - формируется внутриутробно к собственным АГ (ауто. АГ) Механизм: на ранних стадиях развития плода аутореактивные клоны незрелых Лф элиминируются 2. Периферическая - полная или частичная утрата способности ИКК к активации Механизмы: блокирование АГ-специфических рецепторов, повреждение механизмов костимуляции
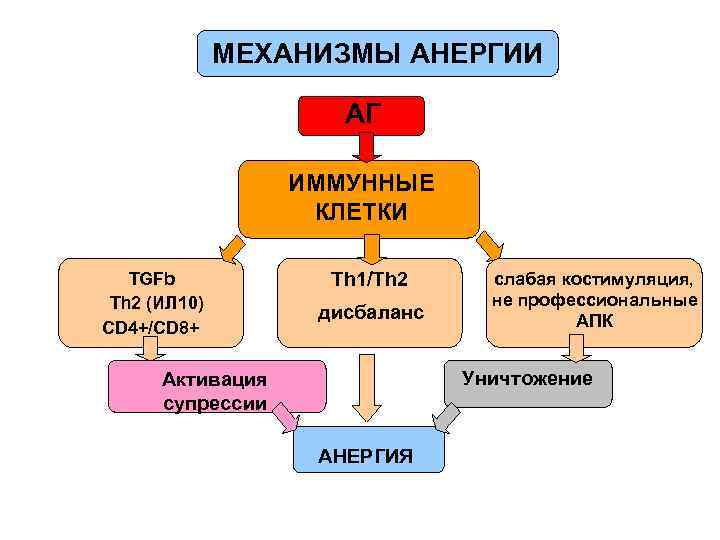 МЕХАНИЗМЫ АНЕРГИИ АГ ИММУННЫЕ КЛЕТКИ TGFb Th 2 (ИЛ 10) CD 4+/CD 8+ Th 1/Th 2 дисбаланс слабая костимуляция, не профессиональные АПК Уничтожение Активация супрессии АНЕРГИЯ
МЕХАНИЗМЫ АНЕРГИИ АГ ИММУННЫЕ КЛЕТКИ TGFb Th 2 (ИЛ 10) CD 4+/CD 8+ Th 1/Th 2 дисбаланс слабая костимуляция, не профессиональные АПК Уничтожение Активация супрессии АНЕРГИЯ
 АПОПТОЗ ( «опадание листьев» ) - запрограммированная, естественная, физиологическая гибель клетки или группы клеток без вреда для окружающих тканей Ø Ø Ø активный процесс самоубийства во всех клетках протекает одинаково контролируется генетически Большое количество Вл и Тл погибает в результате апоптоза, если: Ø в них не произошла перестройка генов рецепторов Ø они становятся аутореактивными Противоположный апоптозу процесс - некроз повреждение нормальных тканей
АПОПТОЗ ( «опадание листьев» ) - запрограммированная, естественная, физиологическая гибель клетки или группы клеток без вреда для окружающих тканей Ø Ø Ø активный процесс самоубийства во всех клетках протекает одинаково контролируется генетически Большое количество Вл и Тл погибает в результате апоптоза, если: Ø в них не произошла перестройка генов рецепторов Ø они становятся аутореактивными Противоположный апоптозу процесс - некроз повреждение нормальных тканей
 ИНДУКТОРЫ АПОПТОЗА 1. Естественного - сигналы, активирующие ферменты, вызывающие фрагментацию ДНК на участки 50 -300 п. н. и разрушение клетки: Ø Ø сигналы от гормонов, цитокинов, АГ, супер. АГ, мк. АТ малые концентрации веществ, вызывающих некроз 2. Бактериозависимого - шигеллы, сальмонеллы, иерсинии Элиминация апоптозных телец - фагоцитоз Мф
ИНДУКТОРЫ АПОПТОЗА 1. Естественного - сигналы, активирующие ферменты, вызывающие фрагментацию ДНК на участки 50 -300 п. н. и разрушение клетки: Ø Ø сигналы от гормонов, цитокинов, АГ, супер. АГ, мк. АТ малые концентрации веществ, вызывающих некроз 2. Бактериозависимого - шигеллы, сальмонеллы, иерсинии Элиминация апоптозных телец - фагоцитоз Мф
 МОРФОЛОГИЧЕСКИЕ ПРИЗНАКИ АПОПТОЗА Ø размеров клетки Ø объёма цитоплазмы Ø уплотнение и фрагментация хроматина Ø скопление хроматина возле ядерной мембраны Ø фрагментация ДНК Ø образование пузырей из ЦПМ Ø экспрессия на ЦПМ фосфатидил-серина ОТЛИЧИЯ ОТ НЕКРОЗА: Ø сохраняется целостность ЦПМ и мембран органелл Ø отсутствует воспаление и повреждение тканей
МОРФОЛОГИЧЕСКИЕ ПРИЗНАКИ АПОПТОЗА Ø размеров клетки Ø объёма цитоплазмы Ø уплотнение и фрагментация хроматина Ø скопление хроматина возле ядерной мембраны Ø фрагментация ДНК Ø образование пузырей из ЦПМ Ø экспрессия на ЦПМ фосфатидил-серина ОТЛИЧИЯ ОТ НЕКРОЗА: Ø сохраняется целостность ЦПМ и мембран органелл Ø отсутствует воспаление и повреждение тканей
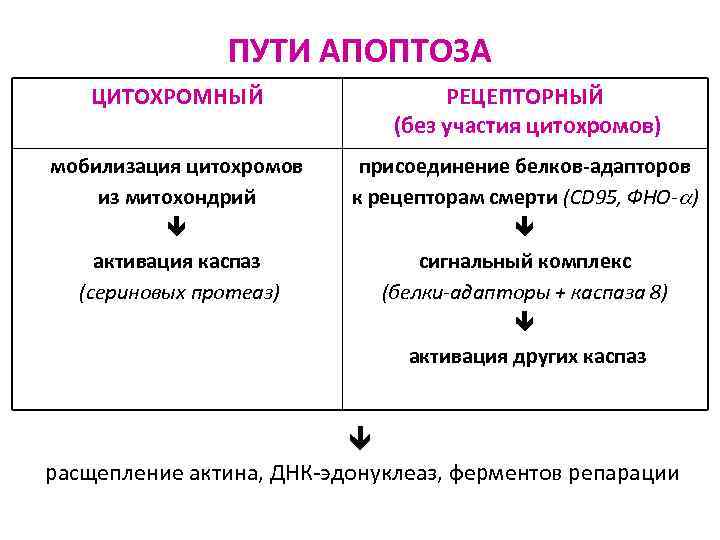 ПУТИ АПОПТОЗА ЦИТОХРОМНЫЙ РЕЦЕПТОРНЫЙ (без участия цитохромов) мобилизация цитохромов из митохондрий активация каспаз (сериновых протеаз) присоединение белков-адапторов к рецепторам смерти (СD 95, ФНО- ) сигнальный комплекс (белки-адапторы + каспаза 8) активация других каспаз расщепление актина, ДНК-эдонуклеаз, ферментов репарации
ПУТИ АПОПТОЗА ЦИТОХРОМНЫЙ РЕЦЕПТОРНЫЙ (без участия цитохромов) мобилизация цитохромов из митохондрий активация каспаз (сериновых протеаз) присоединение белков-адапторов к рецепторам смерти (СD 95, ФНО- ) сигнальный комплекс (белки-адапторы + каспаза 8) активация других каспаз расщепление актина, ДНК-эдонуклеаз, ферментов репарации
 РЕГУЛЯЦИЯ АПОПТОЗА Ø Bsl-2 в норме связан с мембраной митохондрий и стабилизирует ее Ø Bax (экспрессия контролируется р53): - в норме плавает в цитоплазме и следит за маркерами клеточного стресса - при патологии клетки встраивается в ЦПМ, высвобождает цитохром С, который активирует каспазу 9 и т. д.
РЕГУЛЯЦИЯ АПОПТОЗА Ø Bsl-2 в норме связан с мембраной митохондрий и стабилизирует ее Ø Bax (экспрессия контролируется р53): - в норме плавает в цитоплазме и следит за маркерами клеточного стресса - при патологии клетки встраивается в ЦПМ, высвобождает цитохром С, который активирует каспазу 9 и т. д.
 ЗНАЧЕНИЕ АПОПТОЗА 1. Регулятор количества клеточных популяций в организме 2. Фактор селекции клонов Лф 3. Важная роль в: Ø эмбриогенезе Ø формировании нейронов Ø функционировании ИС Ø тканевом гомеостазе Ø ИТ
ЗНАЧЕНИЕ АПОПТОЗА 1. Регулятор количества клеточных популяций в организме 2. Фактор селекции клонов Лф 3. Важная роль в: Ø эмбриогенезе Ø формировании нейронов Ø функционировании ИС Ø тканевом гомеостазе Ø ИТ
 БОЛЕЗНИ АПОПТОЗА Повышенного: Ø СПИД Ø ишемии (инфаркты, инсульты) Ø нейропролиферативнные заболевания Сниженного: Ø Ø опухоли аутоиммунные заболевания вирусные заболевания (герпес, аденовирусная инф. ) нейро-дегенеративные заболевания (б. Альцгеймера, б. Паркинсона)
БОЛЕЗНИ АПОПТОЗА Повышенного: Ø СПИД Ø ишемии (инфаркты, инсульты) Ø нейропролиферативнные заболевания Сниженного: Ø Ø опухоли аутоиммунные заболевания вирусные заболевания (герпес, аденовирусная инф. ) нейро-дегенеративные заболевания (б. Альцгеймера, б. Паркинсона)
 ИММУНОЛОГИЧЕСКАЯ ПАМЯТЬ (ИП) § одна из форм ИО § обеспечивает способность организма сохранять информацию об АГ, с которым он ранее встречался § обеспечивает быструю и сильную реакцию на повторное введение этого АГ
ИММУНОЛОГИЧЕСКАЯ ПАМЯТЬ (ИП) § одна из форм ИО § обеспечивает способность организма сохранять информацию об АГ, с которым он ранее встречался § обеспечивает быструю и сильную реакцию на повторное введение этого АГ
 ХАРАКТЕРИСТИКА ИП • Не формируется в ослабленном организме • Не формируется при иммунизации ПС (слабые АГ) • Носители ИП – АГ-стимулированные Т- и В-л: после 2 -3 делений переходят в покоящееся состояние, длительно (месяц - десятилетия) рециркулируют в организме, имеют на поверхности рецепторы к АГ, при повторном контакте с АГ индуцируют ВИО • При стимуляции малыми дозами АГ клетки памяти образуются без образования АТ ОТЛИЧИЯ ВИО: Ø индуцируется меньшими дозами АГ, Ø эффекторных Лф вырабатывается в 10 -100 раз >, Ø быстрый - индуктивный период короче: продукция АТ начинается раньше и достигает максимума раньше, Ø отличается по спектру АТ: ПИО - Ig. M, ВИО- Ig. G – аффинность (сродство к АГ) >
ХАРАКТЕРИСТИКА ИП • Не формируется в ослабленном организме • Не формируется при иммунизации ПС (слабые АГ) • Носители ИП – АГ-стимулированные Т- и В-л: после 2 -3 делений переходят в покоящееся состояние, длительно (месяц - десятилетия) рециркулируют в организме, имеют на поверхности рецепторы к АГ, при повторном контакте с АГ индуцируют ВИО • При стимуляции малыми дозами АГ клетки памяти образуются без образования АТ ОТЛИЧИЯ ВИО: Ø индуцируется меньшими дозами АГ, Ø эффекторных Лф вырабатывается в 10 -100 раз >, Ø быстрый - индуктивный период короче: продукция АТ начинается раньше и достигает максимума раньше, Ø отличается по спектру АТ: ПИО - Ig. M, ВИО- Ig. G – аффинность (сродство к АГ) >
 ИСПОЛЬЗОВАНИЕ ИП • Ревакцинации – путём многократных иммунизаций удаётся индуцировать очень сильную иммунную реакцию • Получение иммунных диагностических, лечебных и профилактических сывороток путём гипериммунизации животных
ИСПОЛЬЗОВАНИЕ ИП • Ревакцинации – путём многократных иммунизаций удаётся индуцировать очень сильную иммунную реакцию • Получение иммунных диагностических, лечебных и профилактических сывороток путём гипериммунизации животных
 Явление, противоположное ИП ИММУНОЛОГИЧЕСКАЯ ТОЛЕРАНТНОСТЬ (ИТ) § специфическая ареактивность к конкретному АГ § при сохранении способности к ИО на любой другой АГ § приобретается организмом в результате предшествующего контакта с этим АГ
Явление, противоположное ИП ИММУНОЛОГИЧЕСКАЯ ТОЛЕРАНТНОСТЬ (ИТ) § специфическая ареактивность к конкретному АГ § при сохранении способности к ИО на любой другой АГ § приобретается организмом в результате предшествующего контакта с этим АГ
 ВИДЫ ИТ: 1) врождённая (естественная). В норме организм толерантен к собственным АГ (ауто. АГ) – на ранних стадиях развития плода аутореактивные клоны незрелых Лф элиминируются будущий ребёнок навсегда лишается способности вырабатывать АТ к АГ, с которыми контактирует внутриутробно. 2) приобретённая (искусственная) – при введении аллогенных АГ в постнатальном периоде: - ВДИТ - при однократном введении большой дозы АГ реактивные к нему Лф погибают. Анергия - вариант ВДИТ на фоне ИО. - НДИТ - при многократном введении малых возрастающих доз АГ активируются клетки-супрессоры, иммунологическую реактивность.
ВИДЫ ИТ: 1) врождённая (естественная). В норме организм толерантен к собственным АГ (ауто. АГ) – на ранних стадиях развития плода аутореактивные клоны незрелых Лф элиминируются будущий ребёнок навсегда лишается способности вырабатывать АТ к АГ, с которыми контактирует внутриутробно. 2) приобретённая (искусственная) – при введении аллогенных АГ в постнатальном периоде: - ВДИТ - при однократном введении большой дозы АГ реактивные к нему Лф погибают. Анергия - вариант ВДИТ на фоне ИО. - НДИТ - при многократном введении малых возрастающих доз АГ активируются клетки-супрессоры, иммунологическую реактивность.
 РАЗВИТИЕ ИТ ЗАВИСИТ ОТ: • Ø Ø Ø • • • ХАРАКТЕРА АГ - легко вызывают: неметаболизируемые АГ – микробные полисахариды низкомолекулярные вещества АГ с малой степенью генетической чужеродности ДОЗЫ АГ: чем > доза, тем > степень ИТ, она дольше сохраняется ДЛИТЕЛЬНОСТИ ПРЕБЫВАНИЯ АГ В ОРГАНИЗМЕ: чем дольше, тем ИТ > ВОЗРАСТА: легче – в эмбриональном периоде, зрелые Лф труднее инактивируются толерогенами ФИЗИОЛОГИЧЕСКОГО СОСТОЯНИЯ ОРГАНИЗМА: любые воздействия, ИО, способствуют развитию ИТ СПОСОБА ВВЕДЕНИЯ АГ: чем < контакт с ИС, тем лучше развивается ИТ введение АГ в желудок ч/з зонд НАРУШЕНИЯ НОРМАЛЬНОГО ИО: нарушение этапа ко-стимуляции формирование ареактивности АГ-специфических Т-л и возникновение анергии (гипоергии) к АГ
РАЗВИТИЕ ИТ ЗАВИСИТ ОТ: • Ø Ø Ø • • • ХАРАКТЕРА АГ - легко вызывают: неметаболизируемые АГ – микробные полисахариды низкомолекулярные вещества АГ с малой степенью генетической чужеродности ДОЗЫ АГ: чем > доза, тем > степень ИТ, она дольше сохраняется ДЛИТЕЛЬНОСТИ ПРЕБЫВАНИЯ АГ В ОРГАНИЗМЕ: чем дольше, тем ИТ > ВОЗРАСТА: легче – в эмбриональном периоде, зрелые Лф труднее инактивируются толерогенами ФИЗИОЛОГИЧЕСКОГО СОСТОЯНИЯ ОРГАНИЗМА: любые воздействия, ИО, способствуют развитию ИТ СПОСОБА ВВЕДЕНИЯ АГ: чем < контакт с ИС, тем лучше развивается ИТ введение АГ в желудок ч/з зонд НАРУШЕНИЯ НОРМАЛЬНОГО ИО: нарушение этапа ко-стимуляции формирование ареактивности АГ-специфических Т-л и возникновение анергии (гипоергии) к АГ
 ХАРАКТЕРИСТИКА ИТ • СПЕЦИФИЧНОСТЬ: проявляется только к тому АГ, введением которого она была индуцирована • СТЕПЕНЬ ВЫРАЖЕННОСТИ: - абсолютная (полная) – ко всем иммунологическим реакциям - относительная (частичная) – к одной иммунологической реакции (различная степень угнетения КИО и ГИО) • РАЗЛИЧНАЯ ПРОДОЛЖИТЕЛЬНОСТЬ Естественная ИТ в норме сохраняется в течение жизни и обеспечивает гомеостаз. Нарушение естественной ИТ аутоиммунные заболевания: Ø взаимодействие ИС с ПРАГ (белки КС стрептококков тканевые АГ сердца ревматизм), Ø связывание чужеродных АГ детерминант с клетками организма лекарственно-индуцированные гемолитические анемии. Искусственная ИТ обратима.
ХАРАКТЕРИСТИКА ИТ • СПЕЦИФИЧНОСТЬ: проявляется только к тому АГ, введением которого она была индуцирована • СТЕПЕНЬ ВЫРАЖЕННОСТИ: - абсолютная (полная) – ко всем иммунологическим реакциям - относительная (частичная) – к одной иммунологической реакции (различная степень угнетения КИО и ГИО) • РАЗЛИЧНАЯ ПРОДОЛЖИТЕЛЬНОСТЬ Естественная ИТ в норме сохраняется в течение жизни и обеспечивает гомеостаз. Нарушение естественной ИТ аутоиммунные заболевания: Ø взаимодействие ИС с ПРАГ (белки КС стрептококков тканевые АГ сердца ревматизм), Ø связывание чужеродных АГ детерминант с клетками организма лекарственно-индуцированные гемолитические анемии. Искусственная ИТ обратима.
 ИТ МОЖЕТ БЫТЬ ОСЛАБЛЕНА ИЛИ УТРАЧЕНА: • ПРИ ОТСУТСТВИИ АГ • ПРИЁМАМИ, АКТИВИРУЮЩИМИ ИММУНИТЕТ: - иммунизация модифицированными АГ - активация Лф адъювантами - отмена иммунодепрессантов • ПРИЁМАМИ, УСТРАНЯЮЩИМИ ДЕЙСТВИЕ АГ: - введение АТ, связывающих АГ - введение нормальных лимфоидных клеток
ИТ МОЖЕТ БЫТЬ ОСЛАБЛЕНА ИЛИ УТРАЧЕНА: • ПРИ ОТСУТСТВИИ АГ • ПРИЁМАМИ, АКТИВИРУЮЩИМИ ИММУНИТЕТ: - иммунизация модифицированными АГ - активация Лф адъювантами - отмена иммунодепрессантов • ПРИЁМАМИ, УСТРАНЯЮЩИМИ ДЕЙСТВИЕ АГ: - введение АТ, связывающих АГ - введение нормальных лимфоидных клеток
 ИСПОЛЬЗОВАНИЕ ИТ • ЕСТЕСТВЕННОЙ: - поддержание антигенного гомеостаза организма - нормальное протекание беременности - нормальное протекание инфекции - нормальное протекание вакцинации • ИСКУССТВЕННОЙ: - аллергии - аутоиммунных реакций - трансплантация органов и тканей
ИСПОЛЬЗОВАНИЕ ИТ • ЕСТЕСТВЕННОЙ: - поддержание антигенного гомеостаза организма - нормальное протекание беременности - нормальное протекание инфекции - нормальное протекание вакцинации • ИСКУССТВЕННОЙ: - аллергии - аутоиммунных реакций - трансплантация органов и тканей
 ТРАНСПЛАНТАЦИОННЫЙ ИММУНИТЕТ (ТИ) (лат. transplantatio - пересаживание) n Ответная иммунологическая реакция организма против АГ чужеродной ткани (трансплантата) – РХПТ или ИКК трансплантата против хозяина – РТПХ n Обусловлена содержанием в трансплантате генетически чуждых мембранных гликопротеидов – АГ гистосовместимости (ГКГС, МНС, HLA)
ТРАНСПЛАНТАЦИОННЫЙ ИММУНИТЕТ (ТИ) (лат. transplantatio - пересаживание) n Ответная иммунологическая реакция организма против АГ чужеродной ткани (трансплантата) – РХПТ или ИКК трансплантата против хозяина – РТПХ n Обусловлена содержанием в трансплантате генетически чуждых мембранных гликопротеидов – АГ гистосовместимости (ГКГС, МНС, HLA)
 ТИПЫ ТРАНСПЛАНТАТОВ • АУТОТРАНСПЛАНТАТЫ – В ДРУГОЙ БИОТОП ОДНОГО ОРГАНИЗМА, ПЕРЕСАДКИ ПОЧТИ ВСЕГДА УСПЕШНЫ (кожа при лечении ожогов). • СИНГЕННЫЕ – ГЕНЕТИЧЕСКИ ИДЕНТИЧНЫМ ИНДИВИДАМ (МОНОЗИГОТНЫМ БЛИЗНЕЦАМ ИЛИ ИНБРЕДНЫМ ЖИВОТНЫМ), ПЕРЕСАДКИ ПРАКТИЧЕСКИ ВСЕГДА УСПЕШНЫ. • АЛЛОГЕННЫЕ – МЕЖДУ ГЕНЕТИЧЕСКИ РАЗЛИЧНЫМИ ИНДИВИДАМИ ОДНОГО ВИДА, ОТЛИЧАЮЩИМИСЯ ПО ИЗОАГ. Иммуносупрессивная терапия позволяет трансплантатам не отторгаться, если Д и Р отличаются только по ГКГС II, но она недостаточна, если имеются различия по ГКГС I. Самая высокая эффективность при отсутствии несовместимых HLA-B и HLA-Dr АГ у Д и Р. • КСЕНОГЕННЫЕ (гетеротрансплантаты) – между индивидами разных видов, отторгаются в кратчайшие сроки.
ТИПЫ ТРАНСПЛАНТАТОВ • АУТОТРАНСПЛАНТАТЫ – В ДРУГОЙ БИОТОП ОДНОГО ОРГАНИЗМА, ПЕРЕСАДКИ ПОЧТИ ВСЕГДА УСПЕШНЫ (кожа при лечении ожогов). • СИНГЕННЫЕ – ГЕНЕТИЧЕСКИ ИДЕНТИЧНЫМ ИНДИВИДАМ (МОНОЗИГОТНЫМ БЛИЗНЕЦАМ ИЛИ ИНБРЕДНЫМ ЖИВОТНЫМ), ПЕРЕСАДКИ ПРАКТИЧЕСКИ ВСЕГДА УСПЕШНЫ. • АЛЛОГЕННЫЕ – МЕЖДУ ГЕНЕТИЧЕСКИ РАЗЛИЧНЫМИ ИНДИВИДАМИ ОДНОГО ВИДА, ОТЛИЧАЮЩИМИСЯ ПО ИЗОАГ. Иммуносупрессивная терапия позволяет трансплантатам не отторгаться, если Д и Р отличаются только по ГКГС II, но она недостаточна, если имеются различия по ГКГС I. Самая высокая эффективность при отсутствии несовместимых HLA-B и HLA-Dr АГ у Д и Р. • КСЕНОГЕННЫЕ (гетеротрансплантаты) – между индивидами разных видов, отторгаются в кратчайшие сроки.
 РХПТ: • Клеточные реакции. 1. Презентация АГ и их распознавание Тh пролиферация и дифференцировка Тh продукция лимфокинов скопление вокруг трансплантата Лф, плазмоцитов, Мф инфильтрация трансплантата ИКК и деструкция клеток трансплантата воспаление и тромбоз сосудов нарушение питания трансплантата гибель и отторжение. 2. Распознавание АГ аллотрансплантата Тк лизируют клетки трансплантата погибшие клетки фагоцитируются Мф. • Гуморальные реакции. В течение 4 дней наблюдается приживление трансплантата, васкуляризация трансплантата происходит за счёт Д. Затем прорастают сосуды реципиента. Если имеется >50% несовпадения между Д и Р по АГ ГКГС успех маловероятен, т. к. АТ к АГ трансплантата связываются с эндотелиоцитами: 1) активация комплемента о. воспалительная реакция препятствие поступлению крови в трансплантат гибель трансплантата; 2) индукция АЗКЦ разрушение трансплантата ПЯЛ и Мф реципиента; 3) разрушение клеток трансплантата по иммунокомплексному типу.
РХПТ: • Клеточные реакции. 1. Презентация АГ и их распознавание Тh пролиферация и дифференцировка Тh продукция лимфокинов скопление вокруг трансплантата Лф, плазмоцитов, Мф инфильтрация трансплантата ИКК и деструкция клеток трансплантата воспаление и тромбоз сосудов нарушение питания трансплантата гибель и отторжение. 2. Распознавание АГ аллотрансплантата Тк лизируют клетки трансплантата погибшие клетки фагоцитируются Мф. • Гуморальные реакции. В течение 4 дней наблюдается приживление трансплантата, васкуляризация трансплантата происходит за счёт Д. Затем прорастают сосуды реципиента. Если имеется >50% несовпадения между Д и Р по АГ ГКГС успех маловероятен, т. к. АТ к АГ трансплантата связываются с эндотелиоцитами: 1) активация комплемента о. воспалительная реакция препятствие поступлению крови в трансплантат гибель трансплантата; 2) индукция АЗКЦ разрушение трансплантата ПЯЛ и Мф реципиента; 3) разрушение клеток трансплантата по иммунокомплексному типу.
 ОТТОРЖЕНИЕ ТРАНСПЛАНТАТОВ: Ø сверхострое (минуты) - АТ и комплемент Ø ускоренное - 1 -7 дней - Т-л и АТ Ø острое – 7 -21 день - Т-л Ø хроническое – месяцы, годы - Т-л и АТ
ОТТОРЖЕНИЕ ТРАНСПЛАНТАТОВ: Ø сверхострое (минуты) - АТ и комплемент Ø ускоренное - 1 -7 дней - Т-л и АТ Ø острое – 7 -21 день - Т-л Ø хроническое – месяцы, годы - Т-л и АТ
 ПРЕДУПРЕЖДЕНИЕ ОТТОРЖЕНИЯ • ПОДБОР ДОНОРА И РЕЦИПИЕНТА ПО ТКАНЕВОЙ СОВМЕСТИМОСТИ Банк данных «Евротрасплантат» • НЕСПЕЦИФИЧЕСКАЯ ИММУНОСУПРЕССИЯ РЕЦИПИЕНТА С ПОМОЩЬЮ ПРЕПАРАТОВ, ИНГИБИРУЮЩИХ КЛЕТОЧНОЕ ДЕЛЕНИЕ циклоспорин А, меркаптопурин, кортикостероиды, облучение • СОЗДАНИЕ ТОЛЕРАНТНОСТИ ПУТЁМ ПЕРЕСАДКИ КЛЕТОК СЕЛЕЗЁНКИ И ККМ ПЛОДУ ИЛИ НОВОРОЖДЕННОМУ – применяется на животных до момента полного созревания ИС ! человек проходит эту стадию в конце II триместра внутриутробного развития
ПРЕДУПРЕЖДЕНИЕ ОТТОРЖЕНИЯ • ПОДБОР ДОНОРА И РЕЦИПИЕНТА ПО ТКАНЕВОЙ СОВМЕСТИМОСТИ Банк данных «Евротрасплантат» • НЕСПЕЦИФИЧЕСКАЯ ИММУНОСУПРЕССИЯ РЕЦИПИЕНТА С ПОМОЩЬЮ ПРЕПАРАТОВ, ИНГИБИРУЮЩИХ КЛЕТОЧНОЕ ДЕЛЕНИЕ циклоспорин А, меркаптопурин, кортикостероиды, облучение • СОЗДАНИЕ ТОЛЕРАНТНОСТИ ПУТЁМ ПЕРЕСАДКИ КЛЕТОК СЕЛЕЗЁНКИ И ККМ ПЛОДУ ИЛИ НОВОРОЖДЕННОМУ – применяется на животных до момента полного созревания ИС ! человек проходит эту стадию в конце II триместра внутриутробного развития
 РТПХ: ЕСЛИ АКТИВНОСТЬ ИС Р ОБЛУЧЕНИЕМ, А В ТКАНИ ТРАНСПЛАНТАТА ИМЕЮТСЯ ИКК, ОНИ ОТВЕЧАЮТ НА АГ ХОЗЯИНА Механизм: Тк Д распознают клетки Р как генетически чужеродные и разрушают их Возникает при трансплантации клеток л/у, селезёнки, тимуса, ККМ При пересадке ККМ ч/з 10 -30 дней – дерматит, диарея, желтушный гепатит. Длится несколько суток. Исходы: - смерть или выздоровление в результате возникновения толерантности к Тк реципиента
РТПХ: ЕСЛИ АКТИВНОСТЬ ИС Р ОБЛУЧЕНИЕМ, А В ТКАНИ ТРАНСПЛАНТАТА ИМЕЮТСЯ ИКК, ОНИ ОТВЕЧАЮТ НА АГ ХОЗЯИНА Механизм: Тк Д распознают клетки Р как генетически чужеродные и разрушают их Возникает при трансплантации клеток л/у, селезёнки, тимуса, ККМ При пересадке ККМ ч/з 10 -30 дней – дерматит, диарея, желтушный гепатит. Длится несколько суток. Исходы: - смерть или выздоровление в результате возникновения толерантности к Тк реципиента
 ПРОБЛЕМЫ ТРАНСПЛАНТАЦИИ • ПОТРЕБНОСТИ РАСТУТ • ОГРАНИЧЕННЫЕ ВОЗМОЖНОСТИ • ПРОБЛЕМА СОВМЕСТИМОСТИ • ИДЕАЛЬНЫЙ ДОНОР - только в реанимации: мозг умер, но искусственно поддерживается дыхание, сохраняется температура и равномерное сильное сердцебиение, желателен молодой возраст, есть 30 -40 минут для взятия органа • ЭТИЧЕСКИЙ АСПЕКТ • ЭКОНОМИЧЕСКИЙ АСПЕКТ
ПРОБЛЕМЫ ТРАНСПЛАНТАЦИИ • ПОТРЕБНОСТИ РАСТУТ • ОГРАНИЧЕННЫЕ ВОЗМОЖНОСТИ • ПРОБЛЕМА СОВМЕСТИМОСТИ • ИДЕАЛЬНЫЙ ДОНОР - только в реанимации: мозг умер, но искусственно поддерживается дыхание, сохраняется температура и равномерное сильное сердцебиение, желателен молодой возраст, есть 30 -40 минут для взятия органа • ЭТИЧЕСКИЙ АСПЕКТ • ЭКОНОМИЧЕСКИЙ АСПЕКТ
 ПЕРСПЕКТИВНЫЕ ВЫХОДЫ • СОЗДАНИЕ ИСКУССТВЕННЫХ ОРГАНОВ Необходимы материалы: - нейтральные по отношению к тканям - не приводящие к отторжению - поддающиеся обработке - долго служащие - прочные - приемлемые по цене • ПЕРЕСАДКА ОРГАНОВ ЖИВОТНЫХ !в организме свиньи могут оказаться латентные вирусы • ВЫРАЩИВАНИЕ ТКАНЕЙ И ОРГАНОВ ЧЕЛОВЕКА in vitro (клонирование)
ПЕРСПЕКТИВНЫЕ ВЫХОДЫ • СОЗДАНИЕ ИСКУССТВЕННЫХ ОРГАНОВ Необходимы материалы: - нейтральные по отношению к тканям - не приводящие к отторжению - поддающиеся обработке - долго служащие - прочные - приемлемые по цене • ПЕРЕСАДКА ОРГАНОВ ЖИВОТНЫХ !в организме свиньи могут оказаться латентные вирусы • ВЫРАЩИВАНИЕ ТКАНЕЙ И ОРГАНОВ ЧЕЛОВЕКА in vitro (клонирование)
 ПРОТИВООПУХОЛЕВЫЙ ИММУНИТЕТ Концепция иммунного надзора (Ф. М. Бернет): Ø Ø контроль со стороны ИС за соматическими клетками элиминация любых клеток, несущих чужеродную генетическую информацию
ПРОТИВООПУХОЛЕВЫЙ ИММУНИТЕТ Концепция иммунного надзора (Ф. М. Бернет): Ø Ø контроль со стороны ИС за соматическими клетками элиминация любых клеток, несущих чужеродную генетическую информацию
 Уровни иммунного надзора за опухолевыми клетками 1. Немедленный – ЕК, цитотоксические Мн, Мф, Гц, Тк 2. Последующий – специфический ИО с участием цитотоксических Тл, Мф, АТ, INF
Уровни иммунного надзора за опухолевыми клетками 1. Немедленный – ЕК, цитотоксические Мн, Мф, Гц, Тк 2. Последующий – специфический ИО с участием цитотоксических Тл, Мф, АТ, INF
 Опухолевые АГ Ø Эмбриональные белки: - α-фетопротеин - хорионический гонадотропин - раковоэмбриональный АГ Ø Опухольспецифические АГ: - Тканеспецифические (ПСА) - нетканеспецифические - уникальные – продукты мутантных генов (β-катенин)
Опухолевые АГ Ø Эмбриональные белки: - α-фетопротеин - хорионический гонадотропин - раковоэмбриональный АГ Ø Опухольспецифические АГ: - Тканеспецифические (ПСА) - нетканеспецифические - уникальные – продукты мутантных генов (β-катенин)
 Механизмы ускользания опухолей от иммунного надзора 1. Низкая экспрессия молекул ГКГС I нарушение распознавания 2. Не экспрессируются CD 80 и CD 86 анергия 3. АТ защищают опухоли от действия Тл (феномен опухолевого роста) 4. Феномен модуляции мембранных АГ (погружение внутрь клетки) 4. Выделение растворимых форм АГ 5. Мутации генов опухолевых клеток 6. Индукция иммуносупрессии: - продукция цитокинов, ИО (трансформирующие факторы α и β, ИЛ 10, простагландин Е 2) - формирование иммунологической толерантности к опухолевому АГ - активация супрессоров
Механизмы ускользания опухолей от иммунного надзора 1. Низкая экспрессия молекул ГКГС I нарушение распознавания 2. Не экспрессируются CD 80 и CD 86 анергия 3. АТ защищают опухоли от действия Тл (феномен опухолевого роста) 4. Феномен модуляции мембранных АГ (погружение внутрь клетки) 4. Выделение растворимых форм АГ 5. Мутации генов опухолевых клеток 6. Индукция иммуносупрессии: - продукция цитокинов, ИО (трансформирующие факторы α и β, ИЛ 10, простагландин Е 2) - формирование иммунологической толерантности к опухолевому АГ - активация супрессоров
 Подходы к активации иммунной защиты от опухолей 1. Применение адъювантов – эффекта не дало 2. Цитокиновая терапия, в т. ч. генная цитокинотерапия 3. Обработка клеток (ЕК, Тк) цитокинами и введение в организм (=адоптивная (воспринимающая) терапия) 4. Создание противоопухолевых вакцин 5. Применение иммунотоксинов
Подходы к активации иммунной защиты от опухолей 1. Применение адъювантов – эффекта не дало 2. Цитокиновая терапия, в т. ч. генная цитокинотерапия 3. Обработка клеток (ЕК, Тк) цитокинами и введение в организм (=адоптивная (воспринимающая) терапия) 4. Создание противоопухолевых вакцин 5. Применение иммунотоксинов
 СПАСИБО ЗА ВНИМАНИЕ!
СПАСИБО ЗА ВНИМАНИЕ!


