Л 13 Т 7 Германий, Олово,.ppt
- Количество слайдов: 44
 Т 7 Л 13 Германий, Олово, Свинец Германий Gе, олово Sn и свинец Рb — полные электронные аналоги. Как и у типических элементов группы, валентными у них являются (4, 5, 6) s 2 р2 электроны. В ряду Gе — Sn — Рb уменьшается роль внешней s-электронной пары в образовании химических связей (участвуют уже не четыре, а только два электрона). Так, если для германия (подобно углероду и кремнию) наиболее характерна степень окисления +4, то для свинца +2; в соединениях олова различие в степенях окисления проявляется менее резко, хотя производные олова (IV) более устойчивы (относительно свинца). 1
Т 7 Л 13 Германий, Олово, Свинец Германий Gе, олово Sn и свинец Рb — полные электронные аналоги. Как и у типических элементов группы, валентными у них являются (4, 5, 6) s 2 р2 электроны. В ряду Gе — Sn — Рb уменьшается роль внешней s-электронной пары в образовании химических связей (участвуют уже не четыре, а только два электрона). Так, если для германия (подобно углероду и кремнию) наиболее характерна степень окисления +4, то для свинца +2; в соединениях олова различие в степенях окисления проявляется менее резко, хотя производные олова (IV) более устойчивы (относительно свинца). 1
 • Изменение характерных степеней окисления в ряду С—Si—Gе—Sn—Рb можно объяснить вторичной периодичностью в различии энергии ns- и nр-орбиталей. • Рост устойчивости соединений со степенью окисления +2 в ряду Gе Sn Рb и ее уменьшение для соединений Э(IV) в обратной последовательности, хорошо иллюстрируют значения величины G для процессов диспропорционирования: 2
• Изменение характерных степеней окисления в ряду С—Si—Gе—Sn—Рb можно объяснить вторичной периодичностью в различии энергии ns- и nр-орбиталей. • Рост устойчивости соединений со степенью окисления +2 в ряду Gе Sn Рb и ее уменьшение для соединений Э(IV) в обратной последовательности, хорошо иллюстрируют значения величины G для процессов диспропорционирования: 2
 • Первый процесс должен протекать справа налево, т. е. Gе. O 2 устойчивее, чем Gе. О. • Третья реакция, наоборот, должна протекать слева направо: для Gе более характерна степень окисления +4, а для Рb — степень окисления +2. Об этом же свидетельствует сопоставление значений стандартных электродных потенциалов соответствующих процессов: 3
• Первый процесс должен протекать справа налево, т. е. Gе. O 2 устойчивее, чем Gе. О. • Третья реакция, наоборот, должна протекать слева направо: для Gе более характерна степень окисления +4, а для Рb — степень окисления +2. Об этом же свидетельствует сопоставление значений стандартных электродных потенциалов соответствующих процессов: 3
 • Иногда элементы подгруппы германия называют металлами IVA-группы. Формально в их число входит и сам германий. Однако германий является типичным полупроводником с преимущественно ковалентной связью, а следовательно, металлом в свободном состоянии быть не может. Тем не менее в большом числе соединений с более электроотрицательными элементами выступает в роли катионообразователя, что с химической точки зрения отражает металлическую природу элемента. • В бинарных соединениях с металлами германий – анионообразователь, однако все эти соединения обладают металлическими свойствами, что характеризует германий как плохой 4 анионообразователь.
• Иногда элементы подгруппы германия называют металлами IVA-группы. Формально в их число входит и сам германий. Однако германий является типичным полупроводником с преимущественно ковалентной связью, а следовательно, металлом в свободном состоянии быть не может. Тем не менее в большом числе соединений с более электроотрицательными элементами выступает в роли катионообразователя, что с химической точки зрения отражает металлическую природу элемента. • В бинарных соединениях с металлами германий – анионообразователь, однако все эти соединения обладают металлическими свойствами, что характеризует германий как плохой 4 анионообразователь.
 • В пределах IVA-группы наблюдается немонотонная зависимость свойств от положения в элемента группе. Так, ОЭО германия больше, чем кремния, хотя первый потенциал ионизации германия меньше. Это объясняется существованием у атома германия в отличие от кремния заполненного внутреннего 3 d-уровня, который служит экраном для рэлектронов. С учетом четырех потенциалов ионизации оказывается, что прочность связи валентных электронов с ядром выше у атома германия. Этим и объясняется более высокое значение ОЭО германия по сравнению с кремнием. ОЭО - С (2, 5), Si (1, 74), Gе (2, 02), 5 Sn (1, 72), Рb (1, 55).
• В пределах IVA-группы наблюдается немонотонная зависимость свойств от положения в элемента группе. Так, ОЭО германия больше, чем кремния, хотя первый потенциал ионизации германия меньше. Это объясняется существованием у атома германия в отличие от кремния заполненного внутреннего 3 d-уровня, который служит экраном для рэлектронов. С учетом четырех потенциалов ионизации оказывается, что прочность связи валентных электронов с ядром выше у атома германия. Этим и объясняется более высокое значение ОЭО германия по сравнению с кремнием. ОЭО - С (2, 5), Si (1, 74), Gе (2, 02), 5 Sn (1, 72), Рb (1, 55).
 • Радиусы элементов также изменяются немонотонно. При переходе от C к Si наблюдается резкое возрастание атомного радиуса, а затем радиус меняется незначительно. Это можно объяснить влиянием присутствия d-электронов соответствующих слоев у германия и олова. 6
• Радиусы элементов также изменяются немонотонно. При переходе от C к Si наблюдается резкое возрастание атомного радиуса, а затем радиус меняется незначительно. Это можно объяснить влиянием присутствия d-электронов соответствующих слоев у германия и олова. 6
 • Германий — рассеянный элемент; образование рудных скоплений для него не характерно. Он в основном сопутствует природным силикатам и сульфидам, содержится в некоторых углях. Основной минерал олова — касситерит Sn. О 2 (оловянный камень), свинца — галенит Рb. S (свинцовый блеск). Свинец как конечный продукт радиоактивного распада U и Тh содержится в урановых и ториевых минералах. 7
• Германий — рассеянный элемент; образование рудных скоплений для него не характерно. Он в основном сопутствует природным силикатам и сульфидам, содержится в некоторых углях. Основной минерал олова — касситерит Sn. О 2 (оловянный камень), свинца — галенит Рb. S (свинцовый блеск). Свинец как конечный продукт радиоактивного распада U и Тh содержится в урановых и ториевых минералах. 7
 • Простые вещества. В ряду Gе—Sn—Рb отчетливо усиливаются металлические свойства. простых веществ. • Германий — серебристо-белый с желтоватым оттенком, внешне похож на металл, но имеет алмазоподобную решетку (ковалентная связь). • Олово полиморфно. В обычных условиях оно существует в виде -модификации (белое олово), устойчивой выше 13, 2 °С; это — серебристо-белый металл, кристаллическая решетка его тетрагональной структуры с октаэдрической координацией атомов. При охлаждении белое олово переходит в -модификацию (серое олово) со структурой типа алмаза (пл. 5, 85 г/см 3). • Переход - сопровождается увеличением удельного объема (на 25, 6%), в связи с чем олово рассыпается в порошок. • Свинец — темно-серый металл с типичной для металлов структурой гранецентрированного куба. 8
• Простые вещества. В ряду Gе—Sn—Рb отчетливо усиливаются металлические свойства. простых веществ. • Германий — серебристо-белый с желтоватым оттенком, внешне похож на металл, но имеет алмазоподобную решетку (ковалентная связь). • Олово полиморфно. В обычных условиях оно существует в виде -модификации (белое олово), устойчивой выше 13, 2 °С; это — серебристо-белый металл, кристаллическая решетка его тетрагональной структуры с октаэдрической координацией атомов. При охлаждении белое олово переходит в -модификацию (серое олово) со структурой типа алмаза (пл. 5, 85 г/см 3). • Переход - сопровождается увеличением удельного объема (на 25, 6%), в связи с чем олово рассыпается в порошок. • Свинец — темно-серый металл с типичной для металлов структурой гранецентрированного куба. 8
 • Изменение структуры простых веществ в ряду Gе—Sn—Рb соответствует изменению их физических свойств. Так, германий ( Е = 0, 78 э. В) и – олово ( Е = 0, 08 э. В) — полупроводники, а – олово и свинец — металлы. • Изменение типа химической связи от преимущественно ковалентной к металлической сопровождается понижением твердости простых веществ. Так, германий тверд и хрупок, свинец же легко прокатывается в тонкие листы… 9
• Изменение структуры простых веществ в ряду Gе—Sn—Рb соответствует изменению их физических свойств. Так, германий ( Е = 0, 78 э. В) и – олово ( Е = 0, 08 э. В) — полупроводники, а – олово и свинец — металлы. • Изменение типа химической связи от преимущественно ковалентной к металлической сопровождается понижением твердости простых веществ. Так, германий тверд и хрупок, свинец же легко прокатывается в тонкие листы… 9
 • Получают германий, олово, свинец по реакциям: Ge. O 2 + 2 H 2 = Ge + 2 H 2 O; Sn. O 2 + 2 C = Sn + 2 CO; 2 Pb. S + 3 O 2 = 2 Pb. O + 2 SO 2, Pb. O + CO = Pb + CO 2. 10
• Получают германий, олово, свинец по реакциям: Ge. O 2 + 2 H 2 = Ge + 2 H 2 O; Sn. O 2 + 2 C = Sn + 2 CO; 2 Pb. S + 3 O 2 = 2 Pb. O + 2 SO 2, Pb. O + CO = Pb + CO 2. 10
 • Различия в структуре простых веществ сказываются также на их взаимной растворимости. Германий и кремний неограниченно растворяются друг в друге в жидком и твердом состоянии: Gе, Sn и Рb образуют друг с другом твердые растворы в очень ограниченных пределах; с германием и друг с другом олово и свинец образуют эвтектику. Так, температура плавления сплава состава 73, 9% Sn и 26, 1 % Рb равна 181°С. • Образование металлических твердых растворов для германия и его аналогов не характерно, но весьма типичны эвтектические смеси (Sn — Вi, Sn — Сd, Рb — Sn, Рb — Sb, Рb — Вi и др. ). Эвтектические сплавы олова и свинца находят широкое применение. • (Благодаря близости параметров кристаллических решеток сурьма образует твердые растворы с мышьяком и висмутом, но последние друг с другом их не образуют. ) 11
• Различия в структуре простых веществ сказываются также на их взаимной растворимости. Германий и кремний неограниченно растворяются друг в друге в жидком и твердом состоянии: Gе, Sn и Рb образуют друг с другом твердые растворы в очень ограниченных пределах; с германием и друг с другом олово и свинец образуют эвтектику. Так, температура плавления сплава состава 73, 9% Sn и 26, 1 % Рb равна 181°С. • Образование металлических твердых растворов для германия и его аналогов не характерно, но весьма типичны эвтектические смеси (Sn — Вi, Sn — Сd, Рb — Sn, Рb — Sb, Рb — Вi и др. ). Эвтектические сплавы олова и свинца находят широкое применение. • (Благодаря близости параметров кристаллических решеток сурьма образует твердые растворы с мышьяком и висмутом, но последние друг с другом их не образуют. ) 11
 • Из сплавов олова и свинца важнейшими являются следующие: типографские (84— 62% Рb, 4— 8% Sn, 10 — 25% Sb, 2— 4% Аs), подшипниковые (80— 60% Рb или Sn с добавками Sb и Сu), легкоплавкие припои (80 — 60% Рb, 17— 40% Sn, до 2, 5% Sb или 90— 50% Sn, остальное Рb). • Усиление металлических признаков у простых веществ в ряду Gе — Sn — Рb отчетливо наблюдается и в характере изменения их химических свойств. В обычных условиях Gе и Sn устойчивы по отношению к воздуху и воде. Свинец на воздухе окисляется — покрывается синевато-серой оксидной пленкой, поэтому не имеет металлического блеска. При нагревании Gе, Sn и Рb взаимодействуют с большинством неметаллов. При этом образуются соединения Gе (IV), Sn (IV) и Рb (II), например Gе. O 2, 12 Sn. O 2 и Рb. О; Gе. Сl 4, Sn. Сl 4 и Рb. Сl 2.
• Из сплавов олова и свинца важнейшими являются следующие: типографские (84— 62% Рb, 4— 8% Sn, 10 — 25% Sb, 2— 4% Аs), подшипниковые (80— 60% Рb или Sn с добавками Sb и Сu), легкоплавкие припои (80 — 60% Рb, 17— 40% Sn, до 2, 5% Sb или 90— 50% Sn, остальное Рb). • Усиление металлических признаков у простых веществ в ряду Gе — Sn — Рb отчетливо наблюдается и в характере изменения их химических свойств. В обычных условиях Gе и Sn устойчивы по отношению к воздуху и воде. Свинец на воздухе окисляется — покрывается синевато-серой оксидной пленкой, поэтому не имеет металлического блеска. При нагревании Gе, Sn и Рb взаимодействуют с большинством неметаллов. При этом образуются соединения Gе (IV), Sn (IV) и Рb (II), например Gе. O 2, 12 Sn. O 2 и Рb. О; Gе. Сl 4, Sn. Сl 4 и Рb. Сl 2.
 • В ряду напряжений Gе расположен после водорода, а Sn и Рb — непосредственно перед водородом. • Поэтому германий с разбавленными кислотами типа НСl и Н 2 SO 4 не взаимодействует. • Вследствие образования на поверхности нерастворимых солей Рb. Сl 2 и Рb. SО 4 свинец устойчив по отношению к разбавленным НСl и Н 2 SО 4. • Вода не действует на олово. Разбавленные HCl и H 2 SO 4 – действуют очень медленно. В концентрированной соляной кислоте (особенно при нагревании) Sn и Рb дают: Sn + 2 HCl (конц. ) (t) = Sn. Cl 2 + H 2. Sn + 4 H 2 SO 4 (конц. ) = Sn(SO 4)2 + SO 2 + 4 H 2 O. Окислительная активность Рb+4 проявляется в реакциях, происходящих при разряде свинцового аккумулятора: Рb + Рb. О 2 + Н 2 SO 4 = 2 Рb. SO 4 + 2 Н 2 О. катод анод 13
• В ряду напряжений Gе расположен после водорода, а Sn и Рb — непосредственно перед водородом. • Поэтому германий с разбавленными кислотами типа НСl и Н 2 SO 4 не взаимодействует. • Вследствие образования на поверхности нерастворимых солей Рb. Сl 2 и Рb. SО 4 свинец устойчив по отношению к разбавленным НСl и Н 2 SО 4. • Вода не действует на олово. Разбавленные HCl и H 2 SO 4 – действуют очень медленно. В концентрированной соляной кислоте (особенно при нагревании) Sn и Рb дают: Sn + 2 HCl (конц. ) (t) = Sn. Cl 2 + H 2. Sn + 4 H 2 SO 4 (конц. ) = Sn(SO 4)2 + SO 2 + 4 H 2 O. Окислительная активность Рb+4 проявляется в реакциях, происходящих при разряде свинцового аккумулятора: Рb + Рb. О 2 + Н 2 SO 4 = 2 Рb. SO 4 + 2 Н 2 О. катод анод 13
 • Различия в химической природе простых веществ особо отчетливо проявляются в их отношении к азотной кислоте. • При окислении концентрированной азотной кислотой Gе переходит в германиевую кислоту Н 2 Gе. О 3 (Gе. О 2 n. Н 2 О), • а Sn в -оловянную кислоту Н 2 Sn. О 3 (Sn. O 2 n. Н 2 О): Э + 4 HNO 3(конц) = H 2 ЭO 3 + 4 NO 2 + H 2 O; 14
• Различия в химической природе простых веществ особо отчетливо проявляются в их отношении к азотной кислоте. • При окислении концентрированной азотной кислотой Gе переходит в германиевую кислоту Н 2 Gе. О 3 (Gе. О 2 n. Н 2 О), • а Sn в -оловянную кислоту Н 2 Sn. О 3 (Sn. O 2 n. Н 2 О): Э + 4 HNO 3(конц) = H 2 ЭO 3 + 4 NO 2 + H 2 O; 14
 • В разбавленной НNО 3 олово ведет себя как металл, т. е. переходит в нитрат олова (II) и могут образовываться продукты восстановления HNO 3 (NH 4 NO 3 и др. ): 3 Sn + 8 HNO 3 (разб. ) = 3 Sn(NO 3)2 + 2 NO + 4 H 2 O • Свинец по отношению к НNО 3 любых концентраций выступает как металл и образует с ней Рb(NО 3)2. Рb + 4 HNO 3(конц) = Рb(NO 3)2 + 2 NO 2 + H 2 O. 15
• В разбавленной НNО 3 олово ведет себя как металл, т. е. переходит в нитрат олова (II) и могут образовываться продукты восстановления HNO 3 (NH 4 NO 3 и др. ): 3 Sn + 8 HNO 3 (разб. ) = 3 Sn(NO 3)2 + 2 NO + 4 H 2 O • Свинец по отношению к НNО 3 любых концентраций выступает как металл и образует с ней Рb(NО 3)2. Рb + 4 HNO 3(конц) = Рb(NO 3)2 + 2 NO 2 + H 2 O. 15
 • При нагревании олово и свинец взаимодействуют с водными растворами щелочей (чем выше концентрация, тем ниже температура): Sn 0 + 2 KOH + 2 H 2 O = K 2[Sn+2(OH)4] + H 2 Pb 0 + 2 KOH + 2 H 2 O = K 2[Pb+2(OH)4] + H 2 • Германий же растворяется в щелочах лишь в присутствии окислителей, например Н 2 О 2: Ge 0 + 2 KOH + 2 H 2 O 2 = K 2[Ge+4(OH)6] 16
• При нагревании олово и свинец взаимодействуют с водными растворами щелочей (чем выше концентрация, тем ниже температура): Sn 0 + 2 KOH + 2 H 2 O = K 2[Sn+2(OH)4] + H 2 Pb 0 + 2 KOH + 2 H 2 O = K 2[Pb+2(OH)4] + H 2 • Германий же растворяется в щелочах лишь в присутствии окислителей, например Н 2 О 2: Ge 0 + 2 KOH + 2 H 2 O 2 = K 2[Ge+4(OH)6] 16
 • Германий получают из побочных продуктов переработки руд цветных металлов, а также выделяют из золы, полученной от сжигания некоторых видов угля, из отходов коксохимического производства. Рядом последовательных операций соединения Gе переводят в Gе. O 2, который затем восстанавливают водородом. Дополнительно очищают германий зонной плавкой достигая содержания примесей 10 -6 %. Основная масса Gе расходуется в полупроводниковой технике. 17
• Германий получают из побочных продуктов переработки руд цветных металлов, а также выделяют из золы, полученной от сжигания некоторых видов угля, из отходов коксохимического производства. Рядом последовательных операций соединения Gе переводят в Gе. O 2, который затем восстанавливают водородом. Дополнительно очищают германий зонной плавкой достигая содержания примесей 10 -6 %. Основная масса Gе расходуется в полупроводниковой технике. 17
 • Зонная плавка основана на различной растворимости примесей в твердой и жидкой фазах – в твердой фазе она значительно меньше. Очищаемый образец находится в длинной узкой лодочке, помещенной в вакуумированную камеру или инертную среду. Лодочку размещают внутри кольцевого электрического нагревателя, под действием которого плавится только небольшой участок образца. Нагреватель медленно, со скоростью 1 см/час автоматически передвигают вдоль образца, вместе с нагревателем смещается расплавленная зона. Поскольку растворимость примеси в жидкой фазе выше, примесь собирается в расплавленной зоне и вместе с ней перемещается к концу образца. Проход зоны можно повторять несколько раз, добиваясь все большей очистки. Конец слитка, содержащего 18 загрязнения, отрезают.
• Зонная плавка основана на различной растворимости примесей в твердой и жидкой фазах – в твердой фазе она значительно меньше. Очищаемый образец находится в длинной узкой лодочке, помещенной в вакуумированную камеру или инертную среду. Лодочку размещают внутри кольцевого электрического нагревателя, под действием которого плавится только небольшой участок образца. Нагреватель медленно, со скоростью 1 см/час автоматически передвигают вдоль образца, вместе с нагревателем смещается расплавленная зона. Поскольку растворимость примеси в жидкой фазе выше, примесь собирается в расплавленной зоне и вместе с ней перемещается к концу образца. Проход зоны можно повторять несколько раз, добиваясь все большей очистки. Конец слитка, содержащего 18 загрязнения, отрезают.
 • Олово получают восстановлением касситерита (Sn. О 2) углем. Большое значение имеет регенерация (обратное получение) олова за счет растворения его покрытий на железе (старые консервные банки) в щелочах и последующего выделения из раствора электролитическим путем. • Для получения свинца галенит (Рb. S) переводят в Рb. О, который также восстанавливают углем. • Олово главным образом используется для лужения железа — получения «белой жести» , которая расходуется в основном в консервной промышленности. Оловянная фольга (станиоль) применяется для изготовления конденсаторов в электротехнической промышленности. Из свинца делают аккумуляторные пластины, обкладки электрических кабелей, свинец применяется для защиты от радиоактивных и рентгеновских излучений, в качестве коррозионностойкого материала используется в химической промышленности. Оба металла применяются для изготовления легкоплавких 19 сплавов.
• Олово получают восстановлением касситерита (Sn. О 2) углем. Большое значение имеет регенерация (обратное получение) олова за счет растворения его покрытий на железе (старые консервные банки) в щелочах и последующего выделения из раствора электролитическим путем. • Для получения свинца галенит (Рb. S) переводят в Рb. О, который также восстанавливают углем. • Олово главным образом используется для лужения железа — получения «белой жести» , которая расходуется в основном в консервной промышленности. Оловянная фольга (станиоль) применяется для изготовления конденсаторов в электротехнической промышленности. Из свинца делают аккумуляторные пластины, обкладки электрических кабелей, свинец применяется для защиты от радиоактивных и рентгеновских излучений, в качестве коррозионностойкого материала используется в химической промышленности. Оба металла применяются для изготовления легкоплавких 19 сплавов.
 • Соединения со степенью окисления германия, олова и свинца -4. Усиление в ряду простых веществ Gе—Sn—Рb металлических свойств проявляется также в их отношении к металлам. Подобно кремнию, германий и его аналоги с магнием образуют соединения состава Мg 2 Э. Называются они соответственно германид, станнид и плюмбид. В ряду Мg 2 Si—Мg 2 Gе— Мg 2 Sn—Мg 2 Рb в соответствии с повышением доли металлической связи уменьшаются температура плавления, энтальпия образования и ширина запрещенной зоны: 20
• Соединения со степенью окисления германия, олова и свинца -4. Усиление в ряду простых веществ Gе—Sn—Рb металлических свойств проявляется также в их отношении к металлам. Подобно кремнию, германий и его аналоги с магнием образуют соединения состава Мg 2 Э. Называются они соответственно германид, станнид и плюмбид. В ряду Мg 2 Si—Мg 2 Gе— Мg 2 Sn—Мg 2 Рb в соответствии с повышением доли металлической связи уменьшаются температура плавления, энтальпия образования и ширина запрещенной зоны: 20
 • Таким образом, в этом ряду усиливается склонность к образованию металлических соединений. Наиболее типичны металлические соединения олова и свинца с s-элементами, например Nа 2 Sn, Nа. Sn 2. 21
• Таким образом, в этом ряду усиливается склонность к образованию металлических соединений. Наиболее типичны металлические соединения олова и свинца с s-элементами, например Nа 2 Sn, Nа. Sn 2. 21
 • Соединения германия (IV), олова (IV) и свинца (IV). В ряду Gе(IV)–Sn(IV)–Рb(IV) устойчивость бинарных соединений в целом уменьшается. Об этом, например, свидетельствуют значения энергии Гиббса Gof, 298 образования соединений (в к. Дж/моль): Ge. O 2 Sn. O 2 Pb. O 2 -481 -521 -220 Ge. Cl 4 Sn. Cl 4 Pb. Cl 4 -473 -463 -410 Ge. F 4 Sn. F 4 Pb. F 4 -1135 -992 -846 22
• Соединения германия (IV), олова (IV) и свинца (IV). В ряду Gе(IV)–Sn(IV)–Рb(IV) устойчивость бинарных соединений в целом уменьшается. Об этом, например, свидетельствуют значения энергии Гиббса Gof, 298 образования соединений (в к. Дж/моль): Ge. O 2 Sn. O 2 Pb. O 2 -481 -521 -220 Ge. Cl 4 Sn. Cl 4 Pb. Cl 4 -473 -463 -410 Ge. F 4 Sn. F 4 Pb. F 4 -1135 -992 -846 22
 • Для всех трех элементов известны оксиды ЭО 2, фториды ЭF 4 и хлориды ЭСl 4 (Рb. Сl 4 крайне неустойчив). • Бромиды ЭВr 4 и иодиды ЭI 4, сульфиды ЭS 2 и нитриды Э 3 N 4 известны лишь для Gе (IV) и Sn (IV). • В степени окисления +4 германий и его аналоги чаще всего имеют координационное число 6 и 4, что отвечает октаэдрической и тетраэдрической структурной единице. • По мере увеличения размеров атомов при переходе от С и Si к ряду Gе—Sn—Рb координационное число 4 становится все менее характерным. Напротив, становится более 23 типичным координационное число 6.
• Для всех трех элементов известны оксиды ЭО 2, фториды ЭF 4 и хлориды ЭСl 4 (Рb. Сl 4 крайне неустойчив). • Бромиды ЭВr 4 и иодиды ЭI 4, сульфиды ЭS 2 и нитриды Э 3 N 4 известны лишь для Gе (IV) и Sn (IV). • В степени окисления +4 германий и его аналоги чаще всего имеют координационное число 6 и 4, что отвечает октаэдрической и тетраэдрической структурной единице. • По мере увеличения размеров атомов при переходе от С и Si к ряду Gе—Sn—Рb координационное число 4 становится все менее характерным. Напротив, становится более 23 типичным координационное число 6.
 • Диоксиды Gе. O 2 и Sn. O 2 (оба белого цвета), подобно Si. О 2, тугоплавки (1100— 2000 °С). Черно-коричневый Рb. О 2 при нагревании разлагается. Подобно Si. О 2, диоксид германия легко переходит в стеклообразное состояние. При добавке диоксида германия в кварцевое стекло получаются очень прозрачные, сильно преломляющие свет стекла, что определяет важное значение Gе. O 2 в производстве оптического стекла. Диоксид олова применяется в керамической промышленности для изготовления эмалей и глазурей. 24
• Диоксиды Gе. O 2 и Sn. O 2 (оба белого цвета), подобно Si. О 2, тугоплавки (1100— 2000 °С). Черно-коричневый Рb. О 2 при нагревании разлагается. Подобно Si. О 2, диоксид германия легко переходит в стеклообразное состояние. При добавке диоксида германия в кварцевое стекло получаются очень прозрачные, сильно преломляющие свет стекла, что определяет важное значение Gе. O 2 в производстве оптического стекла. Диоксид олова применяется в керамической промышленности для изготовления эмалей и глазурей. 24
 • При нагревании Ge и Sn в присутствии кислорода получаются Ge. О 2 и Sn. О 2. При нагревании же Pb образуется желтый монооксид Pb. О и ярко-красный Pb 3 О 4 [соль ортосвинцовой кислоты Pb 22+(Pb 4+О 4)]. • В лаборатории Pb. О 2 получают окислением: Pb+2(CH 3 COO)2 + Ca. OCl 2 + H 2 O = Pb+4 O 2 + Ca. Cl 2 + 2 CH 3 COOH. Pb. O 2 + 4 HCl = Pb. Cl 4 + 2 H 2 O Pb. Cl 2 + Cl 2. Pb. Cl 4 – желтая тяжелая жидкость, более устойчива при низкой температуре. • Диоксиды химически малоактивны, в воде не растворяются. В ряду Gе. О 2—Sn. O 2—Рb. О 2 несколько усиливаются основные свойства: Gе. O 2 (подобно Si. О 2) — кислотное соединение, растворяется в горячих щелочах; Sn. O 2 — амфотерен, при продолжительном нагревании с концентрированной Н 2 SO 4 дает Sn(SО 4252. )
• При нагревании Ge и Sn в присутствии кислорода получаются Ge. О 2 и Sn. О 2. При нагревании же Pb образуется желтый монооксид Pb. О и ярко-красный Pb 3 О 4 [соль ортосвинцовой кислоты Pb 22+(Pb 4+О 4)]. • В лаборатории Pb. О 2 получают окислением: Pb+2(CH 3 COO)2 + Ca. OCl 2 + H 2 O = Pb+4 O 2 + Ca. Cl 2 + 2 CH 3 COOH. Pb. O 2 + 4 HCl = Pb. Cl 4 + 2 H 2 O Pb. Cl 2 + Cl 2. Pb. Cl 4 – желтая тяжелая жидкость, более устойчива при низкой температуре. • Диоксиды химически малоактивны, в воде не растворяются. В ряду Gе. О 2—Sn. O 2—Рb. О 2 несколько усиливаются основные свойства: Gе. O 2 (подобно Si. О 2) — кислотное соединение, растворяется в горячих щелочах; Sn. O 2 — амфотерен, при продолжительном нагревании с концентрированной Н 2 SO 4 дает Sn(SО 4252. )
 • Диоксиды германия, олова и свинца взаимодействуют со щелочами, образуя гидроксогерманаты (гидроксостаннаты, гидроксоплюмбаты): ЭО 2 + 2 КОН + 2 Н 2 О = К 2[Э(ОН)6]. • При сплавлении ЭО 2 со щелочами или соответствующими оксидами образуются соединения состава М+12 Э+4 О 3 и М+2 Э+4 О 3, М+14 Э+4 О 4 и М+22 Э+4 О 4: 2 Са. О + Pb. O 2 = Ca 2 Pb. O 4; 2 Pb. O + Pb. O 2 = Pb 2 Pb. O 4 (Pb 3 O 4). Оксиды Gе. O и Sn. O получают, нагревая Э(ОН)2 в токе азота, Pb. O – по реакции: 2 Pb(NO 3)2 = Pb. O + 4 NO 2 + O 2 Монооксиды в воде практически не растворимы. Gе. O и Sn. O – сильные восстановители, Pb+4 - окислитель. Соединения ЭО и Э(ОН)2 – амфотерны (уменьшение кислотных и увеличение основных свойств – сверху вниз). 26
• Диоксиды германия, олова и свинца взаимодействуют со щелочами, образуя гидроксогерманаты (гидроксостаннаты, гидроксоплюмбаты): ЭО 2 + 2 КОН + 2 Н 2 О = К 2[Э(ОН)6]. • При сплавлении ЭО 2 со щелочами или соответствующими оксидами образуются соединения состава М+12 Э+4 О 3 и М+2 Э+4 О 3, М+14 Э+4 О 4 и М+22 Э+4 О 4: 2 Са. О + Pb. O 2 = Ca 2 Pb. O 4; 2 Pb. O + Pb. O 2 = Pb 2 Pb. O 4 (Pb 3 O 4). Оксиды Gе. O и Sn. O получают, нагревая Э(ОН)2 в токе азота, Pb. O – по реакции: 2 Pb(NO 3)2 = Pb. O + 4 NO 2 + O 2 Монооксиды в воде практически не растворимы. Gе. O и Sn. O – сильные восстановители, Pb+4 - окислитель. Соединения ЭО и Э(ОН)2 – амфотерны (уменьшение кислотных и увеличение основных свойств – сверху вниз). 26
 • Из оксогерманатов, оксостаннатов и оксоплюмбатов в воде растворимы лишь производные щелочных металлов. При этом они сильно гидролизуются. • В качестве ортоплюмбата (IV) свинца (II) Рb 2 Рb. О 4 (Рb+22 Рb+4 О 4) можно рассматривать смешанный оксид — так называемый свинцовый сурик. • В разном валентном состоянии атомов Рb 3 O 4 можно легко убедиться: при действии разбавленной НNО 3 протекает обменная реакция и образуются производные Рb (II) и Рb(IV): Pb 2(Pb. О 4) Pb 3 О 4 + 4 HNO 3 (р) = Pb. O 2 + 2 Pb(NO 3)2 + 2 H 2 O 27
• Из оксогерманатов, оксостаннатов и оксоплюмбатов в воде растворимы лишь производные щелочных металлов. При этом они сильно гидролизуются. • В качестве ортоплюмбата (IV) свинца (II) Рb 2 Рb. О 4 (Рb+22 Рb+4 О 4) можно рассматривать смешанный оксид — так называемый свинцовый сурик. • В разном валентном состоянии атомов Рb 3 O 4 можно легко убедиться: при действии разбавленной НNО 3 протекает обменная реакция и образуются производные Рb (II) и Рb(IV): Pb 2(Pb. О 4) Pb 3 О 4 + 4 HNO 3 (р) = Pb. O 2 + 2 Pb(NO 3)2 + 2 H 2 O 27
 • Сурик (оранжево-красного цвета) применяется в производстве красок, предохраняющих металлы от коррозии, для приготовления высокотемпературных замазок, в качестве окислителя и др. • Германиевые, оловянные и свинцовые кислоты (как и кремневые) в индивидуальном состоянии выделить весьма трудно. При их получении обычно образуются коллоидные растворы кислот различного состава, превращающиеся в белые студенистые осадки с переменным и неопределенным составом ЭО 2 n. Н 2 О. • Для Sn. О 2 n. Н 2 О известны две формы - и . • -Форма растворима в кислотах и основаниях, нет. • -оловянную кислоту получают действием HNO 3 конц. на металлическое олово. 28
• Сурик (оранжево-красного цвета) применяется в производстве красок, предохраняющих металлы от коррозии, для приготовления высокотемпературных замазок, в качестве окислителя и др. • Германиевые, оловянные и свинцовые кислоты (как и кремневые) в индивидуальном состоянии выделить весьма трудно. При их получении обычно образуются коллоидные растворы кислот различного состава, превращающиеся в белые студенистые осадки с переменным и неопределенным составом ЭО 2 n. Н 2 О. • Для Sn. О 2 n. Н 2 О известны две формы - и . • -Форма растворима в кислотах и основаниях, нет. • -оловянную кислоту получают действием HNO 3 конц. на металлическое олово. 28
 -Оловянная кислота получается из растворов солей Sn+4 при действии оснований, (при действии избытка NH 4 OH не происходит растворения осадка): Sn. Cl 4 + NH 4 OH = Sn. О 2 n. Н 2 О + NH 4 Cl. -Sn + 4 HNO 3(конц. ) = Sn. О 2 n. Н 2 О + 4 NO 2 + + H 2 O; В последнем случае образуется - форма. При действии водных растворов аммиака на растворы Sn. Сl 4 вначале получается гексагидроксооловянная кислота: Sn. Сl 4 + 4 Н 3 N + 6 Н 2 О = Н 2[Sn(ОН)6] + 4 NН 4 Сl 29
-Оловянная кислота получается из растворов солей Sn+4 при действии оснований, (при действии избытка NH 4 OH не происходит растворения осадка): Sn. Cl 4 + NH 4 OH = Sn. О 2 n. Н 2 О + NH 4 Cl. -Sn + 4 HNO 3(конц. ) = Sn. О 2 n. Н 2 О + 4 NO 2 + + H 2 O; В последнем случае образуется - форма. При действии водных растворов аммиака на растворы Sn. Сl 4 вначале получается гексагидроксооловянная кислота: Sn. Сl 4 + 4 Н 3 N + 6 Н 2 О = Н 2[Sn(ОН)6] + 4 NН 4 Сl 29
 • При стоянии она более или менее быстро полимеризуется вплоть до выпадения Sn. О 2 n. Н 2 О. • Свежеполученные -оловянные и свинцовые кислоты растворяются в кислотах и щелочах. В последнем случае образуются гидроксосоединения типа М+12[Э(ОН)6]: ЭО 2 + 2 КОН + 2 Н 2 О = К 2[Э(ОН)6] 30
• При стоянии она более или менее быстро полимеризуется вплоть до выпадения Sn. О 2 n. Н 2 О. • Свежеполученные -оловянные и свинцовые кислоты растворяются в кислотах и щелочах. В последнем случае образуются гидроксосоединения типа М+12[Э(ОН)6]: ЭО 2 + 2 КОН + 2 Н 2 О = К 2[Э(ОН)6] 30
 • Изменение структуры и состава оловянных кислот сопровождается изменением их химической активности. Так, свежеполученный осадок ( -оловянная кислота) легко растворяется в щелочах и даже кислотах. После стояния осадок ( -оловянная кислота) по химической активности напоминает Sb. O 2. Он взаимодействует только со щелочами и то лишь при сплавлении. Неактивная форма оловянных кислот ( -оловянная кислота) образуется, кроме того, при окислении олова в концентрированной HNО 3. • Различие в химической активности так называемых - и -оловянных кислот обусловлено различием в их строении: уменьшением при переходе от - к -формам числа активных ОН-групп и образованием 31 устойчивых Sn—О—Sn - связей.
• Изменение структуры и состава оловянных кислот сопровождается изменением их химической активности. Так, свежеполученный осадок ( -оловянная кислота) легко растворяется в щелочах и даже кислотах. После стояния осадок ( -оловянная кислота) по химической активности напоминает Sb. O 2. Он взаимодействует только со щелочами и то лишь при сплавлении. Неактивная форма оловянных кислот ( -оловянная кислота) образуется, кроме того, при окислении олова в концентрированной HNО 3. • Различие в химической активности так называемых - и -оловянных кислот обусловлено различием в их строении: уменьшением при переходе от - к -формам числа активных ОН-групп и образованием 31 устойчивых Sn—О—Sn - связей.
 • Вследствие координационной ненасыщенности молекул тетрагалогениды молекулярной структуры химически активны. Подобно другим ковалентным соединениям этого типа, их гидролиз протекает последовательно через стадии присоединения воды и отщепления молекул галогенводородов, вплоть до образования гидроксидов: Sn. Cl 4 + 4 H 2 O = Sn(OH)4 + 4 HCl • которые за счет полимеризации переходят в гидратированные оксиды, например Sn. O 2 n. Н 2 О. 32
• Вследствие координационной ненасыщенности молекул тетрагалогениды молекулярной структуры химически активны. Подобно другим ковалентным соединениям этого типа, их гидролиз протекает последовательно через стадии присоединения воды и отщепления молекул галогенводородов, вплоть до образования гидроксидов: Sn. Cl 4 + 4 H 2 O = Sn(OH)4 + 4 HCl • которые за счет полимеризации переходят в гидратированные оксиды, например Sn. O 2 n. Н 2 О. 32
 • Из тетрагалогенидов наибольшее значение имеет Sn. Сl 4 — в обычных условиях жидкость, вследствие гидролиза дымящая на воздухе. Получают Sn. Сl 4 действием сухого хлора на жидкое олово. В частности, на этой реакции основан один из методов регенерации оловянных покрытий на железе (консервных банок). • Sn. Сl 4 и (NН 4)2 Sn. Сl 6 в основном используют в красильном деле в качестве протравы, применяют для получения других соединений олова. • Тетрахлорид олова хорошо растворяется в малополярных растворителях, а сам растворяет иод, серу, фосфор и др. 33
• Из тетрагалогенидов наибольшее значение имеет Sn. Сl 4 — в обычных условиях жидкость, вследствие гидролиза дымящая на воздухе. Получают Sn. Сl 4 действием сухого хлора на жидкое олово. В частности, на этой реакции основан один из методов регенерации оловянных покрытий на железе (консервных банок). • Sn. Сl 4 и (NН 4)2 Sn. Сl 6 в основном используют в красильном деле в качестве протравы, применяют для получения других соединений олова. • Тетрахлорид олова хорошо растворяется в малополярных растворителях, а сам растворяет иод, серу, фосфор и др. 33
 • Гидриды элементов подгруппы германия немногочисленны и малоустойчивы. Это связано с дальнейшим уменьшением в ряду Gе—Sn—Рb прочности связи Э—Э и Э—Н по сравнению с Si—Si и Si—Н. • В ряду Si. Н 4 (силан) — Gе. Н 4 (герман) — Sn. Н 4 (станнан) — Рb. Н 4 (плюмбан) устойчивость понижается. • Плюмбан настолько неустойчив, что о его существовании можно заключить лишь по косвенным признакам. • При пропускании через нагретую докрасна стеклянную трубку герман и станнан разлагаются, осаждаясь в виде металлического зеркала. 34
• Гидриды элементов подгруппы германия немногочисленны и малоустойчивы. Это связано с дальнейшим уменьшением в ряду Gе—Sn—Рb прочности связи Э—Э и Э—Н по сравнению с Si—Si и Si—Н. • В ряду Si. Н 4 (силан) — Gе. Н 4 (герман) — Sn. Н 4 (станнан) — Рb. Н 4 (плюмбан) устойчивость понижается. • Плюмбан настолько неустойчив, что о его существовании можно заключить лишь по косвенным признакам. • При пропускании через нагретую докрасна стеклянную трубку герман и станнан разлагаются, осаждаясь в виде металлического зеркала. 34
 • Гидриды Э (IV) выделяются при действии разбавленных кислот на некоторые германиды и станниды (аналогично силану): Mg 2 Э + 4 HCl = 2 Mg. Cl 2 + ЭН 4 (в воде) Mg 2 Э +4 NH 4 Cl= 2 Mg. Cl 2+ ЭН 4 + 4 NH 3 (в аммиаке) При действии кислот на Мg 2 Gе кроме Gе. Н 4 одновременно получается дигерман Gе 2 Н 6 (Тпл. — 109 °С, Ткип. 31 o. С) и тригерман Gе 3 Н 8 (Тпл. — 106 °С, Ткип. — 52 °С). Известны также более сложные германы, а также дистаннан Sn 2 Н 6. Sn. Н 4 (газ) – мало устойчив. Еще менее устойчив Pb. H 4 (газ). 35
• Гидриды Э (IV) выделяются при действии разбавленных кислот на некоторые германиды и станниды (аналогично силану): Mg 2 Э + 4 HCl = 2 Mg. Cl 2 + ЭН 4 (в воде) Mg 2 Э +4 NH 4 Cl= 2 Mg. Cl 2+ ЭН 4 + 4 NH 3 (в аммиаке) При действии кислот на Мg 2 Gе кроме Gе. Н 4 одновременно получается дигерман Gе 2 Н 6 (Тпл. — 109 °С, Ткип. 31 o. С) и тригерман Gе 3 Н 8 (Тпл. — 106 °С, Ткип. — 52 °С). Известны также более сложные германы, а также дистаннан Sn 2 Н 6. Sn. Н 4 (газ) – мало устойчив. Еще менее устойчив Pb. H 4 (газ). 35
 • Соединения германия (II), олова (II) и свинца (II). • Степень окисления +2 наиболее характерна для свинца и проявляется в его разнообразных соединениях, а для германия (II) известны лишь немногочисленные бинарные соединения. • Большинство производных Рb (II) кристаллические вещества. За исключением нитрата Рb(NО 3)2 и ацетата Рb(СН 3 СОО)2, они плохо растворимы (Рb. Наl 2) или почти нерастворимы (Рb. SO 4, Рb. Сr. О 4, Рb. СО 3) в воде. • Этим, в частности, объясняется устойчивость свинца к действию большинства кислот. • Соединения Э (II) обычно бесцветны. 36
• Соединения германия (II), олова (II) и свинца (II). • Степень окисления +2 наиболее характерна для свинца и проявляется в его разнообразных соединениях, а для германия (II) известны лишь немногочисленные бинарные соединения. • Большинство производных Рb (II) кристаллические вещества. За исключением нитрата Рb(NО 3)2 и ацетата Рb(СН 3 СОО)2, они плохо растворимы (Рb. Наl 2) или почти нерастворимы (Рb. SO 4, Рb. Сr. О 4, Рb. СО 3) в воде. • Этим, в частности, объясняется устойчивость свинца к действию большинства кислот. • Соединения Э (II) обычно бесцветны. 36
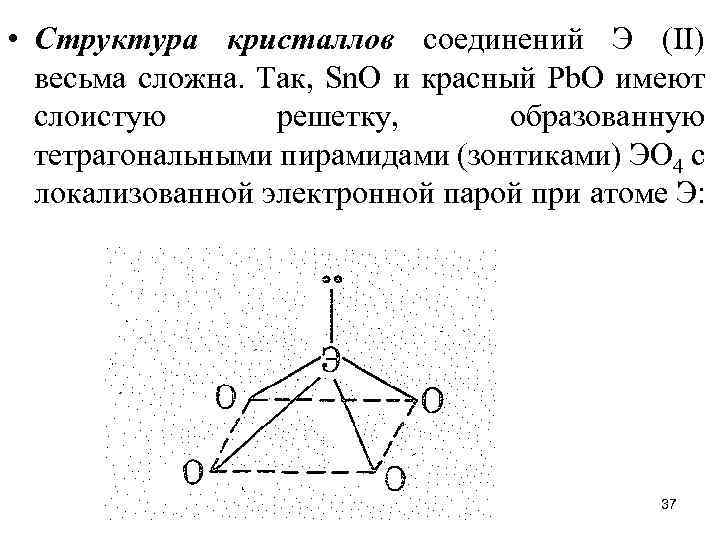 • Структура кристаллов соединений Э (II) весьма сложна. Так, Sn. О и красный Pb. O имеют слоистую решетку, образованную тетрагональными пирамидами (зонтиками) ЭО 4 с локализованной электронной парой при атоме Э: 37
• Структура кристаллов соединений Э (II) весьма сложна. Так, Sn. О и красный Pb. O имеют слоистую решетку, образованную тетрагональными пирамидами (зонтиками) ЭО 4 с локализованной электронной парой при атоме Э: 37
 • Оксиды ЭО и гидроксиды Э(ОН)2 амфотерны. Они взаимодействуют как с кислотами, так и со щелочами: Э(ОН)2 + 2 HCl = ЭCl 2 + 2 H 2 O; Э(ОН)2 + KOH = K[Э(ОН)3]. • У производных Рb (II) преобладают основные, а у Gе (II) кислотные свойства. • Основной характер оксидов и гидроксидов усиливается с ростом радиусов ионов Э 2+. 38
• Оксиды ЭО и гидроксиды Э(ОН)2 амфотерны. Они взаимодействуют как с кислотами, так и со щелочами: Э(ОН)2 + 2 HCl = ЭCl 2 + 2 H 2 O; Э(ОН)2 + KOH = K[Э(ОН)3]. • У производных Рb (II) преобладают основные, а у Gе (II) кислотные свойства. • Основной характер оксидов и гидроксидов усиливается с ростом радиусов ионов Э 2+. 38
 • Производные Gе (II) и Sn (II) — сильные восстановители. Так, Gе. Сl 2 реагируют с Сl 2 почти мгновенно, Sn. Сl 2 при комнатной температуре — быстро, а Рb. Сl 2 в обычных условиях с хлором не взаимодействует вообще. • Производные Gе (II) и Sn (II) восстанавливают некоторые металлы из соединений, например: 2 Bi(NO 3)3 + 3 Na[Sn(OH)3] + 9 Na. OH = 2 Bi + 3 Na[Sn(OH)6] + 6 Na. NO 3. Они переводят Fе 3+ в Fе 2+, Cr. О 42 - в Сr 3+ и т. д. 39
• Производные Gе (II) и Sn (II) — сильные восстановители. Так, Gе. Сl 2 реагируют с Сl 2 почти мгновенно, Sn. Сl 2 при комнатной температуре — быстро, а Рb. Сl 2 в обычных условиях с хлором не взаимодействует вообще. • Производные Gе (II) и Sn (II) восстанавливают некоторые металлы из соединений, например: 2 Bi(NO 3)3 + 3 Na[Sn(OH)3] + 9 Na. OH = 2 Bi + 3 Na[Sn(OH)6] + 6 Na. NO 3. Они переводят Fе 3+ в Fе 2+, Cr. О 42 - в Сr 3+ и т. д. 39
 • Соединения Рb (IV), наоборот, — сильные окислители, в особенности в кислой среде. Они, например, даже окисляют Мn+2 до Мn. О 4 -: 2 Mn 2+ + 5 Pb. O 2 + 4 H+ = 5 Pb 2+ + 2 Mn. O 4 - + 2 H 2 O • Рb. О 2 и Рb 3 О 4 используются в качестве окислителей в спичечной промышленности. • Галогениды ЭГ 4 похожи на галогениды неметаллов, а ЭГ 2, особенно Pb. Г 2 - соли. 40
• Соединения Рb (IV), наоборот, — сильные окислители, в особенности в кислой среде. Они, например, даже окисляют Мn+2 до Мn. О 4 -: 2 Mn 2+ + 5 Pb. O 2 + 4 H+ = 5 Pb 2+ + 2 Mn. O 4 - + 2 H 2 O • Рb. О 2 и Рb 3 О 4 используются в качестве окислителей в спичечной промышленности. • Галогениды ЭГ 4 похожи на галогениды неметаллов, а ЭГ 2, особенно Pb. Г 2 - соли. 40
 • Перевод Рb (II) в Рb (IV) возможен лишь при электролитическом окислении или действием наиболее сильных окислителей [Сl 2, белильная известь (смесь Cа. Cl 2 и Са(Cl. О)2) и др. ] при нагревании в щелочной среде. Например: Рb(СН 3 СOO)2 + Сl 2 + 4 КОН = Рb. О 2↓ + 2 КСl + 2 КСН 3 СОО + 2 Н 2 O Рb(СН 3 СOO)2 + Са. ОCl 2 + Н 2 О = Рb. О 2↓ + Са. Cl 2 + 2 СН 3 СOOН 41
• Перевод Рb (II) в Рb (IV) возможен лишь при электролитическом окислении или действием наиболее сильных окислителей [Сl 2, белильная известь (смесь Cа. Cl 2 и Са(Cl. О)2) и др. ] при нагревании в щелочной среде. Например: Рb(СН 3 СOO)2 + Сl 2 + 4 КОН = Рb. О 2↓ + 2 КСl + 2 КСН 3 СОО + 2 Н 2 O Рb(СН 3 СOO)2 + Са. ОCl 2 + Н 2 О = Рb. О 2↓ + Са. Cl 2 + 2 СН 3 СOOН 41
 • Из соединений свинца (II) Рb. О применяется в производстве оптического стекла, хрусталя, глазурей и олиф; Рb. Сr. О 4 (оранжево-красного цвета) входит в состав минеральных красок; 2 Рb. СО 3 Рb(ОН)2 используют для изготовления свинцовых белил. Малорастворимый Sn. F 2 применяют как фторсодержащую добавку к зубным пастам. В последнее время большое теоретическое в практическое значение приобретают олово- и свинецорганические соединения. Рb. СО 3 Рb(ОН)2 реагирует с содержащимися в воздухе сернистыми соединениями и превращается в Рb. S (черного цвета). Рb. S + 4 Н 2 О 2 = Рb. SО 4 + 4 Н 2 О 42 • Рb. SО 4 –соль белого цвета.
• Из соединений свинца (II) Рb. О применяется в производстве оптического стекла, хрусталя, глазурей и олиф; Рb. Сr. О 4 (оранжево-красного цвета) входит в состав минеральных красок; 2 Рb. СО 3 Рb(ОН)2 используют для изготовления свинцовых белил. Малорастворимый Sn. F 2 применяют как фторсодержащую добавку к зубным пастам. В последнее время большое теоретическое в практическое значение приобретают олово- и свинецорганические соединения. Рb. СО 3 Рb(ОН)2 реагирует с содержащимися в воздухе сернистыми соединениями и превращается в Рb. S (черного цвета). Рb. S + 4 Н 2 О 2 = Рb. SО 4 + 4 Н 2 О 42 • Рb. SО 4 –соль белого цвета.
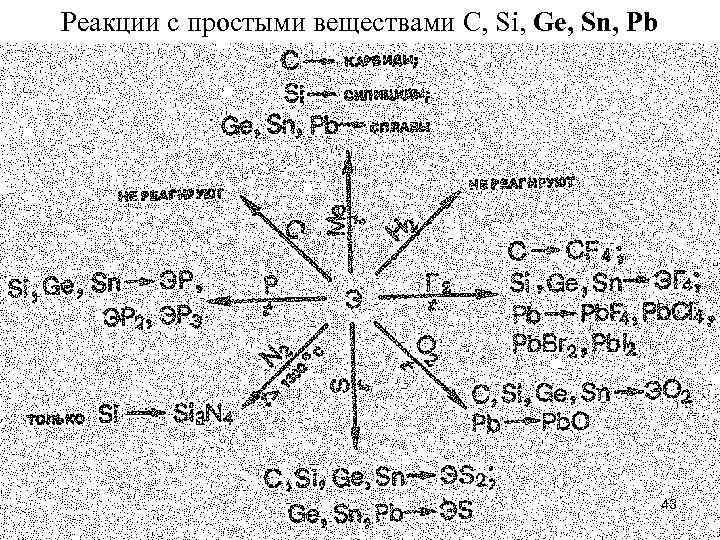 Реакции с простыми веществами C, Si, Ge, Sn, Pb 43
Реакции с простыми веществами C, Si, Ge, Sn, Pb 43
 44
44


