 Т 3 Л 5 p-Элементы группы VIA К р-элементам VI группы относятся типические элементы — кислород О, сера S и элементы подгруппы селена – селен Sе, теллур Те, полоний Ро. O 1 s 22 p 4 S 2 s 2 p 63 s 23 p 4 Se 3 s 23 p 64 s 23 d 104 p 4 Te 4 s 24 p 65 s 24 d 105 p 4 Po 5 s 25 p 66 s 25 d 104 f 146 p 4 1
Т 3 Л 5 p-Элементы группы VIA К р-элементам VI группы относятся типические элементы — кислород О, сера S и элементы подгруппы селена – селен Sе, теллур Те, полоний Ро. O 1 s 22 p 4 S 2 s 2 p 63 s 23 p 4 Se 3 s 23 p 64 s 23 d 104 p 4 Te 4 s 24 p 65 s 24 d 105 p 4 Po 5 s 25 p 66 s 25 d 104 f 146 p 4 1
 • В ряду О—S—Sе—Те—Ро уменьшаются энергии ионизации, увеличиваются размеры атомов и ионов. Это ослабляет неметаллические признаки элементов: кислород—элементнеметалл, полоний — элемент-металл. • Подобно фтору, кислород образует соединения почти со всеми элементами (кроме гелия, неона и аргона). ОЭО кислорода 3, 5. Поскольку по электроотрицательности кислород уступает только фтору, степень окисления кислорода в подавляющем большинстве соединений равна — 2. Кроме того, кислород проявляет степени окисления +2, а также +1 и – 1 в соединениях со связью О—О. 2
• В ряду О—S—Sе—Те—Ро уменьшаются энергии ионизации, увеличиваются размеры атомов и ионов. Это ослабляет неметаллические признаки элементов: кислород—элементнеметалл, полоний — элемент-металл. • Подобно фтору, кислород образует соединения почти со всеми элементами (кроме гелия, неона и аргона). ОЭО кислорода 3, 5. Поскольку по электроотрицательности кислород уступает только фтору, степень окисления кислорода в подавляющем большинстве соединений равна — 2. Кроме того, кислород проявляет степени окисления +2, а также +1 и – 1 в соединениях со связью О—О. 2
 • Кислород — самый распространенный элемент (58, 0 мол. доли) на Земле. Состоит из трех стабильных изотопов: 16 О (99, 759%), 17 О (0, 037%) и 18 O (0, 204%). Искусственно получены также изотопы 14 O, 15 O и 19 О, период полураспада которых исчисляется десятками секунд. Вследствие количественного преобладания и большой окислительной активности кислород предопределяет форму существования на Земле всех остальных элементов. Его значение было особенно велико в период образования земной коры. Предполагается, что наличие кислорода в атмосфере обусловлено вторичными процессами 3 деятельностью зеленых растений.
• Кислород — самый распространенный элемент (58, 0 мол. доли) на Земле. Состоит из трех стабильных изотопов: 16 О (99, 759%), 17 О (0, 037%) и 18 O (0, 204%). Искусственно получены также изотопы 14 O, 15 O и 19 О, период полураспада которых исчисляется десятками секунд. Вследствие количественного преобладания и большой окислительной активности кислород предопределяет форму существования на Земле всех остальных элементов. Его значение было особенно велико в период образования земной коры. Предполагается, что наличие кислорода в атмосфере обусловлено вторичными процессами 3 деятельностью зеленых растений.
 • Простые вещества. Наиболее устойчива двухатомная молекула кислорода О 2. Как показывают магнитные исследования, она парамагнитна. При этом величина ее парамагнетизма отвечает наличию двух непарных электронов: • В молекуле О 2 на 8 связывающих электронов приходится 4 разрыхляющих, поэтому порядок связи в ней равен двум. 4
• Простые вещества. Наиболее устойчива двухатомная молекула кислорода О 2. Как показывают магнитные исследования, она парамагнитна. При этом величина ее парамагнетизма отвечает наличию двух непарных электронов: • В молекуле О 2 на 8 связывающих электронов приходится 4 разрыхляющих, поэтому порядок связи в ней равен двум. 4
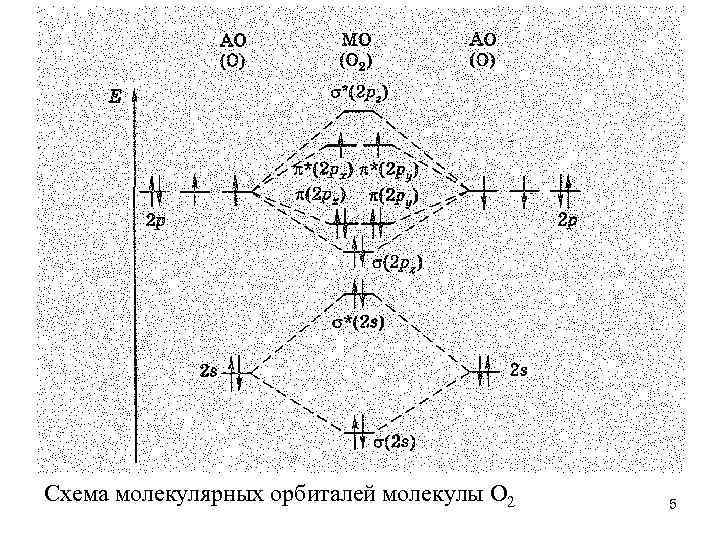 Схема молекулярных орбиталей молекулы O 2 5
Схема молекулярных орбиталей молекулы O 2 5
 • Вследствие кратности связи межатомное расстояние в О 2 (0, 1207 нм) меньше длины одинарной связи O—О (0, 148 нм). По этой же причине молекула О 2 весьма устойчива, ее энергия диссоциации равна 494 к. Дж/моль, в то время как энергия одинарной связи О–О всего 210 к. Дж/моль. Диссоциация молекул О 2 на атомы становится заметной лишь при 2000 °С; диссоциация имеет место также при поглощении ультрафиолетового излучения (фотолиз). 6
• Вследствие кратности связи межатомное расстояние в О 2 (0, 1207 нм) меньше длины одинарной связи O—О (0, 148 нм). По этой же причине молекула О 2 весьма устойчива, ее энергия диссоциации равна 494 к. Дж/моль, в то время как энергия одинарной связи О–О всего 210 к. Дж/моль. Диссоциация молекул О 2 на атомы становится заметной лишь при 2000 °С; диссоциация имеет место также при поглощении ультрафиолетового излучения (фотолиз). 6
 • Температуры плавления (-218, 9 °С) и кипения (-183 °С) кислорода очень низкие. Он плохо растворяется в воде (5 объемов О 2 в 100 объемах Н 2 О при 0 °С). Жидкий и твёрдый кислород притягивается магнитом. • Аллотропическую модификацию кислорода озон О 3 можно рассматривать как соединение О (IV). • Кислород обладает высокой химической активностью, особенно при нагревании и в присутствии катализатора; с большинством простых веществ он взаимодействует непосредственно, образуя оксиды; лишь по отношению к фтору проявляет восстановительные свойства. • Получают действием электрического разряда на воздух или кислород. 7
• Температуры плавления (-218, 9 °С) и кипения (-183 °С) кислорода очень низкие. Он плохо растворяется в воде (5 объемов О 2 в 100 объемах Н 2 О при 0 °С). Жидкий и твёрдый кислород притягивается магнитом. • Аллотропическую модификацию кислорода озон О 3 можно рассматривать как соединение О (IV). • Кислород обладает высокой химической активностью, особенно при нагревании и в присутствии катализатора; с большинством простых веществ он взаимодействует непосредственно, образуя оксиды; лишь по отношению к фтору проявляет восстановительные свойства. • Получают действием электрического разряда на воздух или кислород. 7
 • Кислород получают ректификацией жидкого воздуха, а также как побочный продукт при электролизе воды. В лаборатории для его получения используют термическое разложение богатых кислородом соединений (КМn. О 4, КСl. O 3 и др. ). t • 2 Hg. O = 2 Hg + O 2; t, Mn. O 2 • 2 KCl. O 3 === 2 KCl + 3 O 2; t • 2 KMn. O 4 = K 2 Mn. O 4 + Mn. O 2 + O 2; электролиз воды (электролит 30% КОН): • катод 4 H 2 O + 4 e = 2 H 2 + 4 OH • анод 4 OH- - 4 e = O 2 + 2 H 2 O 8
• Кислород получают ректификацией жидкого воздуха, а также как побочный продукт при электролизе воды. В лаборатории для его получения используют термическое разложение богатых кислородом соединений (КМn. О 4, КСl. O 3 и др. ). t • 2 Hg. O = 2 Hg + O 2; t, Mn. O 2 • 2 KCl. O 3 === 2 KCl + 3 O 2; t • 2 KMn. O 4 = K 2 Mn. O 4 + Mn. O 2 + O 2; электролиз воды (электролит 30% КОН): • катод 4 H 2 O + 4 e = 2 H 2 + 4 OH • анод 4 OH- - 4 e = O 2 + 2 H 2 O 8
 • Соединения со степенью окисления кислорода -2. По химической активности кислород уступает только фтору. С большинством простых веществ он реагирует непосредственно, за исключением галогенов, He, Ne и Ar, платины и золота. • Образование двухи многозарядных одноатомных анионов Эn- энергетически невыгодно. • Даже в кристаллических оксидах наиболее активных металлических элементов типа Nа 2 O и Са. О эффективный заряд атома кислорода составляет всего около -1. 9
• Соединения со степенью окисления кислорода -2. По химической активности кислород уступает только фтору. С большинством простых веществ он реагирует непосредственно, за исключением галогенов, He, Ne и Ar, платины и золота. • Образование двухи многозарядных одноатомных анионов Эn- энергетически невыгодно. • Даже в кристаллических оксидах наиболее активных металлических элементов типа Nа 2 O и Са. О эффективный заряд атома кислорода составляет всего около -1. 9
 • Как и для других р-элементов 2 -го периода, максимальная валентность (число двухэлектронных двухцентровых связей) кислорода равна четырем. При этом атомы кислорода могут находиться в состоянии sр-, sр2 и sр3 -гибридизации, что соответствует линейному, треугольному и тетраэдрическому расположению –связей. В качестве примера соединений, в которых проявляются эти гибридные состояния орбиталей кислорода, можно указать соответственно кристаллические Вe. О, Тi. O 2 и Si. O 2. 10
• Как и для других р-элементов 2 -го периода, максимальная валентность (число двухэлектронных двухцентровых связей) кислорода равна четырем. При этом атомы кислорода могут находиться в состоянии sр-, sр2 и sр3 -гибридизации, что соответствует линейному, треугольному и тетраэдрическому расположению –связей. В качестве примера соединений, в которых проявляются эти гибридные состояния орбиталей кислорода, можно указать соответственно кристаллические Вe. О, Тi. O 2 и Si. O 2. 10
 • Весьма разнообразны также оксиды, в которых координационное число кислорода превышает значение его максимальной валентности, т. е. больше четырех. Например, в кристалле Мg. O координационное число кислорода равно шести, а в кристалле Nа 2 O восьми. Согласно теории молекулярных орбиталей это обусловлено тем, что в кристалле Mg. O (структурный тип Nа. Сl) каждый атом О (за счет 2 pх-, 2 рy- и 2 рz-орбиталей) объединяется с шестью соседними атомами Мg посредством трехцентровых связей. Аналогично построены кристаллические Мn. О, Fе. О, Со. О, Ni. O и другие оксиды со структурой типа Nа. Сl. 11
• Весьма разнообразны также оксиды, в которых координационное число кислорода превышает значение его максимальной валентности, т. е. больше четырех. Например, в кристалле Мg. O координационное число кислорода равно шести, а в кристалле Nа 2 O восьми. Согласно теории молекулярных орбиталей это обусловлено тем, что в кристалле Mg. O (структурный тип Nа. Сl) каждый атом О (за счет 2 pх-, 2 рy- и 2 рz-орбиталей) объединяется с шестью соседними атомами Мg посредством трехцентровых связей. Аналогично построены кристаллические Мn. О, Fе. О, Со. О, Ni. O и другие оксиды со структурой типа Nа. Сl. 11
 • В оксидах типа Nа 2 O (К 2 O, Rb 2 O, Li 2 O) атомы кислорода (за счет 2 s, 2 рx-, 2 pу- и 2 рz-орбиталей) с восемью соседними атомами металла объединяются посредством четырех трехцентровых связей. • Состав кристаллических оксидов (в особенности d-элементов) в большей или меньшей степени переменный. Так, для Мn. О он изменяется в пределах от Мn. О до Мn. О 1. 5, а для Мn. О 2 — от Мn. O 1, 5 до Мn. О 2, 6. Если в оксидах содержание кислорода выше стехиометрического, они проявляют дырочную проводимость, а если содержание металла выше стехиометрического, то электронную. Полупроводниками с дырочной 12 проводимостью являются Мn. О, Сu 2 О, Fе. О н др.
• В оксидах типа Nа 2 O (К 2 O, Rb 2 O, Li 2 O) атомы кислорода (за счет 2 s, 2 рx-, 2 pу- и 2 рz-орбиталей) с восемью соседними атомами металла объединяются посредством четырех трехцентровых связей. • Состав кристаллических оксидов (в особенности d-элементов) в большей или меньшей степени переменный. Так, для Мn. О он изменяется в пределах от Мn. О до Мn. О 1. 5, а для Мn. О 2 — от Мn. O 1, 5 до Мn. О 2, 6. Если в оксидах содержание кислорода выше стехиометрического, они проявляют дырочную проводимость, а если содержание металла выше стехиометрического, то электронную. Полупроводниками с дырочной 12 проводимостью являются Мn. О, Сu 2 О, Fе. О н др.
 • С ростом степени окисления металлического элемента возрастает ковалентный вклад в химическую связь. Химическое строение таких оксидов молекулярное (Cr. O 3, Mn 2 O 7, Re 2 O 7, Os. O 4). Для таких оксидов нарушение стехиометрии невозможно. • Для оксидов металлов с преимущественно ионной связью (координационные решетки) нарушение стехиометрии термодинамически обосновано, так как при этом растет энтропия. Нестехиометрические оксидные фазы могут быть как односторонние (Fe. O), так и двухсторонние (Ti. O). 13
• С ростом степени окисления металлического элемента возрастает ковалентный вклад в химическую связь. Химическое строение таких оксидов молекулярное (Cr. O 3, Mn 2 O 7, Re 2 O 7, Os. O 4). Для таких оксидов нарушение стехиометрии невозможно. • Для оксидов металлов с преимущественно ионной связью (координационные решетки) нарушение стехиометрии термодинамически обосновано, так как при этом растет энтропия. Нестехиометрические оксидные фазы могут быть как односторонние (Fe. O), так и двухсторонние (Ti. O). 13
 • Важнейшим из оксидов является оксид водорода Н 2 O — вода. Достаточно сказать, что она составляет 50— 99% массы любого живого существа. Кровь человека содержит более 4/5 воды, мускулы — 35% воды. При средней продолжительности жизни (70 лет) человек выпивает около 25 т воды. 14
• Важнейшим из оксидов является оксид водорода Н 2 O — вода. Достаточно сказать, что она составляет 50— 99% массы любого живого существа. Кровь человека содержит более 4/5 воды, мускулы — 35% воды. При средней продолжительности жизни (70 лет) человек выпивает около 25 т воды. 14
 • Молекула воды имеет угловую форму, что согласно теории валентных связей соответствует sр3 -гибридвому состоянию атома кислорода. В молекуле Н 2 O две sр3 гибридные орбитали атома кислорода участвуют в образовании двух связей О— Н. На двух других sр3 -гибридных орбиталях расположены две несвязывающие электронные пары. Валентный угол в молекуле воды НOН составляет 104, 5 о. 15
• Молекула воды имеет угловую форму, что согласно теории валентных связей соответствует sр3 -гибридвому состоянию атома кислорода. В молекуле Н 2 O две sр3 гибридные орбитали атома кислорода участвуют в образовании двух связей О— Н. На двух других sр3 -гибридных орбиталях расположены две несвязывающие электронные пары. Валентный угол в молекуле воды НOН составляет 104, 5 о. 15
 • В рамках теории молекулярных орбиталей модель молекулы воды соответствует распределению восьми валентных электронов по двум связывающим и двум несвязывающим молекулярным орбиталям и наличию двух свободных разрыхляющих орбиталей. Такое объяснение подтверждается наличием у молекулы Н 2 О четырех первых потенциалов ионизации (27, 3; 16, 2; 14, 5 и 12, 6 э. В). 16
• В рамках теории молекулярных орбиталей модель молекулы воды соответствует распределению восьми валентных электронов по двум связывающим и двум несвязывающим молекулярным орбиталям и наличию двух свободных разрыхляющих орбиталей. Такое объяснение подтверждается наличием у молекулы Н 2 О четырех первых потенциалов ионизации (27, 3; 16, 2; 14, 5 и 12, 6 э. В). 16
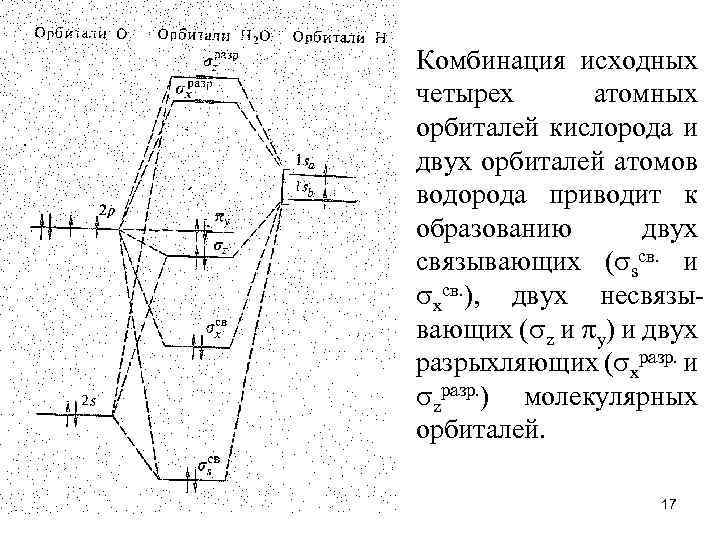 Комбинация исходных четырех атомных орбиталей кислорода и двух орбиталей атомов водорода приводит к образованию двух связывающих ( sсв. и xсв. ), двух несвязывающих ( z и y) и двух разрыхляющих ( xразр. и zразр. ) молекулярных орбиталей. 17
Комбинация исходных четырех атомных орбиталей кислорода и двух орбиталей атомов водорода приводит к образованию двух связывающих ( sсв. и xсв. ), двух несвязывающих ( z и y) и двух разрыхляющих ( xразр. и zразр. ) молекулярных орбиталей. 17
 • С позиций теории молекулярных орбиталей строение молекулы Н 2 О можно объяснить следующим образом. Молекулярные орбитали Н 2 О образуются за счет 2 s-, и 2 р-орбиталей атома кислорода и 1 s-орбиталей двух атомов водорода. Перекрывание 2 рx-орбитали атома кислорода и 1 sорбиталей двух атомов водорода приводит к возникновению молекулярных xсв. - и хразр. орбиталей, характер перекрывания 2 s- и 2 рzорбиталей кислорода одинаков. В результате образуются три молекулярные орбитали: связывающая sсв. , почти несвязывающая z и разрыхляющая zразр. Орбиталь 2 рy, расположенная перпендикулярно плоскости расположения атомов Н и О, с 1 s-орбиталями атомов Н не перекрывается и в молекуле Н 2 O играет роль несвязывающей молекулярной y -орбитали 18
• С позиций теории молекулярных орбиталей строение молекулы Н 2 О можно объяснить следующим образом. Молекулярные орбитали Н 2 О образуются за счет 2 s-, и 2 р-орбиталей атома кислорода и 1 s-орбиталей двух атомов водорода. Перекрывание 2 рx-орбитали атома кислорода и 1 sорбиталей двух атомов водорода приводит к возникновению молекулярных xсв. - и хразр. орбиталей, характер перекрывания 2 s- и 2 рzорбиталей кислорода одинаков. В результате образуются три молекулярные орбитали: связывающая sсв. , почти несвязывающая z и разрыхляющая zразр. Орбиталь 2 рy, расположенная перпендикулярно плоскости расположения атомов Н и О, с 1 s-орбиталями атомов Н не перекрывается и в молекуле Н 2 O играет роль несвязывающей молекулярной y -орбитали 18
 • В соответствии с природой элемента в положительной степени окисления характер оксидов в периодах и группах периодической системы закономерно изменяется. В периодах уменьшается отрицательный эффективный заряд на атомах кислорода о и осуществляется постепенный переход от основных через амфотерные оксиды к кислотным, например: • 19
• В соответствии с природой элемента в положительной степени окисления характер оксидов в периодах и группах периодической системы закономерно изменяется. В периодах уменьшается отрицательный эффективный заряд на атомах кислорода о и осуществляется постепенный переход от основных через амфотерные оксиды к кислотным, например: • 19
 • Различие в свойствах оксидов разного типа проявляется при их взаимодействии с водой: • Na 2 O + H 2 O = 2 Na. OH основный • 3 H 2 O + P 2 O 5 = 2 H 3 PO 4 кислотный а также при взаимодействии оксидов разного типа друг с другом: • 3 Са. О + Р 2 О 5 = Са 3(РО 4)2 основный кислотный 20
• Различие в свойствах оксидов разного типа проявляется при их взаимодействии с водой: • Na 2 O + H 2 O = 2 Na. OH основный • 3 H 2 O + P 2 O 5 = 2 H 3 PO 4 кислотный а также при взаимодействии оксидов разного типа друг с другом: • 3 Са. О + Р 2 О 5 = Са 3(РО 4)2 основный кислотный 20
 • Амфотерные оксиды с водой, как правило, не взаимодействуют, но могут реагировать и с кислотами, и с щелочами: Al 2 O 3(к) + 6 HCl(р) + 9 H 2 O(ж) = 2[Al(OH 2)6]Cl 3(р) основный 6 Na. OH(р) + Al 2 O 3(к) + 3 H 2 O(ж)=2 Na 3[Al(OH)6](р) кислотный • а при сплавлении — с основными и кислотными оксидами. • Al 2 O 3 + Na 2 O = 2 Na. Al. O 2 • Al 2 O 3 + 3 Si. O 2 = Al 2(Si. O 3)3 (Al 2 O 3 3 Si. O 2) 21
• Амфотерные оксиды с водой, как правило, не взаимодействуют, но могут реагировать и с кислотами, и с щелочами: Al 2 O 3(к) + 6 HCl(р) + 9 H 2 O(ж) = 2[Al(OH 2)6]Cl 3(р) основный 6 Na. OH(р) + Al 2 O 3(к) + 3 H 2 O(ж)=2 Na 3[Al(OH)6](р) кислотный • а при сплавлении — с основными и кислотными оксидами. • Al 2 O 3 + Na 2 O = 2 Na. Al. O 2 • Al 2 O 3 + 3 Si. O 2 = Al 2(Si. O 3)3 (Al 2 O 3 3 Si. O 2) 21
 • Сравнительную количественную оценку основнокислотной активности оксидов можно дать на основании значений G соответствующих однотипных реакций. Уменьшение отрицательного значения Gо 298 в реакциях: • свидетельствует об ослаблении в ряду Nа 2 О – Мg. О —Al 2 O 3 их основных свойств, а также об их способности взаимодействовать с водой. 22
• Сравнительную количественную оценку основнокислотной активности оксидов можно дать на основании значений G соответствующих однотипных реакций. Уменьшение отрицательного значения Gо 298 в реакциях: • свидетельствует об ослаблении в ряду Nа 2 О – Мg. О —Al 2 O 3 их основных свойств, а также об их способности взаимодействовать с водой. 22
 • В ряду Р 2 О 5—SO 3—Сl 2 О 7 • наоборот, наблюдается увеличение отрицательного значения Gо 298, что свидетельствует об усилении у оксидов кислотных свойств. 23
• В ряду Р 2 О 5—SO 3—Сl 2 О 7 • наоборот, наблюдается увеличение отрицательного значения Gо 298, что свидетельствует об усилении у оксидов кислотных свойств. 23
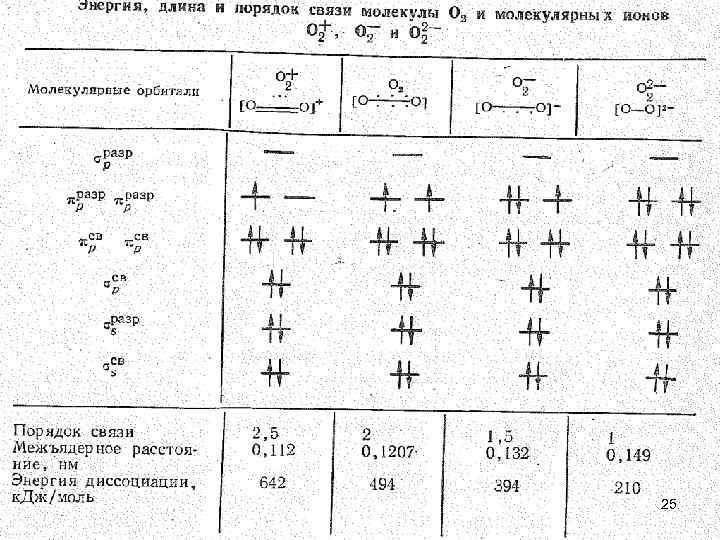
 • Соединения перекисного типа. • Сродство к электрону молекулы O 2 составляет 0, 8 э. В, а ее энергия ионизации 12, 08 э. В. При химических превращениях молекула O 2 может присоединять или терять электроны с образованием молекулярных ионов типа O 22 -, O 2 - и O 2+. • В ряду О 2+ – О 2 — О 2 - — О 22 - расстояние между атомами кислорода увеличивается, а средняя энергия связи уменьшается. 24
• Соединения перекисного типа. • Сродство к электрону молекулы O 2 составляет 0, 8 э. В, а ее энергия ионизации 12, 08 э. В. При химических превращениях молекула O 2 может присоединять или терять электроны с образованием молекулярных ионов типа O 22 -, O 2 - и O 2+. • В ряду О 2+ – О 2 — О 2 - — О 22 - расстояние между атомами кислорода увеличивается, а средняя энергия связи уменьшается. 24
 25
25
 • Присоединение одного электрона к молекуле О 2 вызывает образование надпероксид-иона О 2 - : • Производные радикала О 2 называются надпероксидами; они известны для наиболее активных щелочных металлов (К, Rb, Сs – оранжевые, коричневые). • Для K, Rb, Cs - при сгорании Э + О 2(изб. ) = ЭО 2 26
• Присоединение одного электрона к молекуле О 2 вызывает образование надпероксид-иона О 2 - : • Производные радикала О 2 называются надпероксидами; они известны для наиболее активных щелочных металлов (К, Rb, Сs – оранжевые, коричневые). • Для K, Rb, Cs - при сгорании Э + О 2(изб. ) = ЭО 2 26
 • Надпероксиды образуются при прямом взаимодействии простых веществ: К + O 2 = КO 2. • Непарный электрон иона О 2 - обусловливает парамагнетизм надпероксидов и наличие у них окраски. Надпероксиды — очень сильные окислители. Oни бурно реагируют с водой с выделением перекиси водорода и кислорода. 2 KO 2 + 2 H 2 O = 2 KOH + H 2 O 2 + O 2 2 KO 2 + H 2 SO 4 = K 2 SO 4 + H 2 O 2 + O 2 27
• Надпероксиды образуются при прямом взаимодействии простых веществ: К + O 2 = КO 2. • Непарный электрон иона О 2 - обусловливает парамагнетизм надпероксидов и наличие у них окраски. Надпероксиды — очень сильные окислители. Oни бурно реагируют с водой с выделением перекиси водорода и кислорода. 2 KO 2 + 2 H 2 O = 2 KOH + H 2 O 2 + O 2 2 KO 2 + H 2 SO 4 = K 2 SO 4 + H 2 O 2 + O 2 27
 • Присоединяя два электрона, молекула О 2 превращается в пероксид-ион О 22 -, в котором атомы связаны одной двухэлектронной связью, и поэтому он диамагнитен: • Это также согласуется с отсутствием окраски у пероксидов. Пероксиды образуются при окислении ряда металлов (щелочных, щелочноземельных), например: Ва + О 2 = Ва. О 2 • Для K, Rb, Cs t 2 ЭО 2 = Э 2 О 2 + О 2 28
• Присоединяя два электрона, молекула О 2 превращается в пероксид-ион О 22 -, в котором атомы связаны одной двухэлектронной связью, и поэтому он диамагнитен: • Это также согласуется с отсутствием окраски у пероксидов. Пероксиды образуются при окислении ряда металлов (щелочных, щелочноземельных), например: Ва + О 2 = Ва. О 2 • Для K, Rb, Cs t 2 ЭО 2 = Э 2 О 2 + О 2 28
 • Наибольшее практическое значение имеет пероксид (перекись) водорода Н 2 О 2. • Энергия связи О—О (210 к. Дж/моль) почти в два раза меньше энергии связи О—Н (468 к. Дж/моль). 29
• Наибольшее практическое значение имеет пероксид (перекись) водорода Н 2 О 2. • Энергия связи О—О (210 к. Дж/моль) почти в два раза меньше энергии связи О—Н (468 к. Дж/моль). 29
 • Из-за несимметричного распределения связей Н–О молекула Н 2 О 2 сильно полярна. Между молекулами Н 2 О 2 возникает довольно прочная водородная связь, приводящая к их ассоциации. Поэтому в обычных условиях пероксид водорода — сиропообразная жидкость ( = 1, 44) с довольно высокой температурой кипения (Ткип. 150, 2 °С, Тпл. 0, 41 °С). Она имеет бледноголубую окраску. Пероксид водорода — хороший. ионизирующий растворитель. С водой смешивается в любых отношениях благодаря возникновению новых водородных связей. Из растворов выделяется в виде неустойчивого кристаллогидрата Н 2 О 2 2 Н 2 О (Tпл. 52, 0 °С). В лаборатории обычно используются 3%-ные и 30%-ные растворы Н 2 О 2 (последний называют пергидролем). 30
• Из-за несимметричного распределения связей Н–О молекула Н 2 О 2 сильно полярна. Между молекулами Н 2 О 2 возникает довольно прочная водородная связь, приводящая к их ассоциации. Поэтому в обычных условиях пероксид водорода — сиропообразная жидкость ( = 1, 44) с довольно высокой температурой кипения (Ткип. 150, 2 °С, Тпл. 0, 41 °С). Она имеет бледноголубую окраску. Пероксид водорода — хороший. ионизирующий растворитель. С водой смешивается в любых отношениях благодаря возникновению новых водородных связей. Из растворов выделяется в виде неустойчивого кристаллогидрата Н 2 О 2 2 Н 2 О (Tпл. 52, 0 °С). В лаборатории обычно используются 3%-ные и 30%-ные растворы Н 2 О 2 (последний называют пергидролем). 30
 • В химических реакциях пероксид-радикал может, не изменяясь, переходить в другие соединения, например: Н 2 О 2 + 2 Na. OH = Na 2 O 2 + 2 H 2 O Ba. O 2 + H 2 SO 4 = Ba. SO 4 + H 2 O 2 • Последняя реакция используется для получения перекиси водорода. Электрохимическим окислением H 2 SO 4 и нагреванием надсерной кислоты получают Н 2 О 2 2 HSO 4 - - 2 е = H 2 S 2 O 8 • • H 2 S 2 O 8 + 2 H 2 O = 2 H 2 SO 4 + H 2 O 2 (слабое нагревание) • Чаще, однако, протекают реакции, сопровождающиеся разрушением связи О — О или изменением заряда иона О 22 -. 31
• В химических реакциях пероксид-радикал может, не изменяясь, переходить в другие соединения, например: Н 2 О 2 + 2 Na. OH = Na 2 O 2 + 2 H 2 O Ba. O 2 + H 2 SO 4 = Ba. SO 4 + H 2 O 2 • Последняя реакция используется для получения перекиси водорода. Электрохимическим окислением H 2 SO 4 и нагреванием надсерной кислоты получают Н 2 О 2 2 HSO 4 - - 2 е = H 2 S 2 O 8 • • H 2 S 2 O 8 + 2 H 2 O = 2 H 2 SO 4 + H 2 O 2 (слабое нагревание) • Чаще, однако, протекают реакции, сопровождающиеся разрушением связи О — О или изменением заряда иона О 22 -. 31
 • Окислительные свойства пероксидов выражены сильнее, чем восстановительные. • Так, при действии концентрированных растворов Н 2 О 2 на бумагу, опилки или другие горючие вещества происходит их самовоспламенение. Восстановительные свойства перекись водорода проявляет только по отношению к таким сильным окислителям, как ионы Мn. О 4 -. 2 KI-1 + Na 2 O 2 -1 + 2 H 2 SO 4 = I 20 + Na 2 SO 4 + K 2 SO 4 + H 2 O-2; 2 KMn+7 O 4 + 5 H 2 O 2 -1 + 3 H 2 SO 4 = 2 Mn+2 SO 4 + 5 O 20 + K 2 SO 4 + 8 H 2 O. 32
• Окислительные свойства пероксидов выражены сильнее, чем восстановительные. • Так, при действии концентрированных растворов Н 2 О 2 на бумагу, опилки или другие горючие вещества происходит их самовоспламенение. Восстановительные свойства перекись водорода проявляет только по отношению к таким сильным окислителям, как ионы Мn. О 4 -. 2 KI-1 + Na 2 O 2 -1 + 2 H 2 SO 4 = I 20 + Na 2 SO 4 + K 2 SO 4 + H 2 O-2; 2 KMn+7 O 4 + 5 H 2 O 2 -1 + 3 H 2 SO 4 = 2 Mn+2 SO 4 + 5 O 20 + K 2 SO 4 + 8 H 2 O. 32
 • Для пероксида водорода характерен также распад по типу диспропорционирования: • H 2 O 2 -1 + H 2 O 2 -1 = 2 H 2 O-2 + O 20 • Этот распад ускоряется в присутствии примесей, при освещении, нагревании и может протекать со взрывом. Довольно устойчивы только очень чистая Н 2 О 2 и ее 30— 65%-ные растворы. Пероксид водорода и его растворы обычно хранят в темной посуде и на холоде; для стабилизации добавляют ингибиторы. • Водные растворы пероксида водорода широко используются для отбелки различных материалов, для обеззараживания сточных вод. Пероксид водорода применяют как окислитель ракетного топлива. 33
• Для пероксида водорода характерен также распад по типу диспропорционирования: • H 2 O 2 -1 + H 2 O 2 -1 = 2 H 2 O-2 + O 20 • Этот распад ускоряется в присутствии примесей, при освещении, нагревании и может протекать со взрывом. Довольно устойчивы только очень чистая Н 2 О 2 и ее 30— 65%-ные растворы. Пероксид водорода и его растворы обычно хранят в темной посуде и на холоде; для стабилизации добавляют ингибиторы. • Водные растворы пероксида водорода широко используются для отбелки различных материалов, для обеззараживания сточных вод. Пероксид водорода применяют как окислитель ракетного топлива. 33
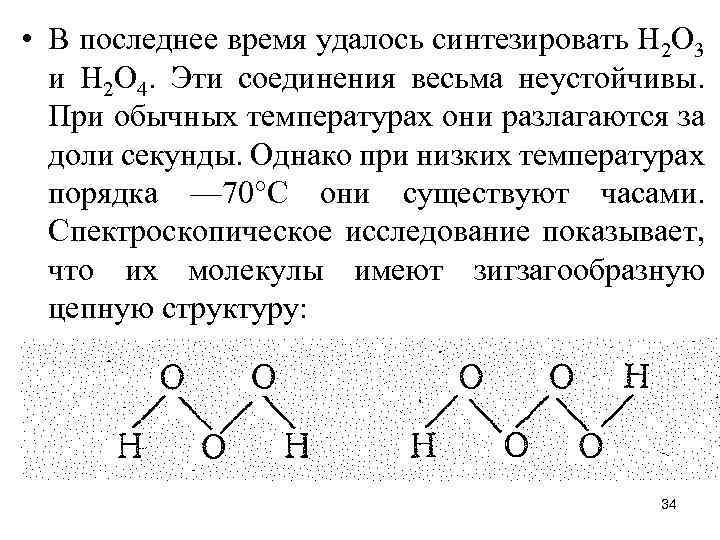 • В последнее время удалось синтезировать Н 2 О 3 и Н 2 О 4. Эти соединения весьма неустойчивы. При обычных температурах они разлагаются за доли секунды. Однако при низких температурах порядка — 70°С они существуют часами. Спектроскопическое исследование показывает, что их молекулы имеют зигзагообразную цепную структуру: 34
• В последнее время удалось синтезировать Н 2 О 3 и Н 2 О 4. Эти соединения весьма неустойчивы. При обычных температурах они разлагаются за доли секунды. Однако при низких температурах порядка — 70°С они существуют часами. Спектроскопическое исследование показывает, что их молекулы имеют зигзагообразную цепную структуру: 34
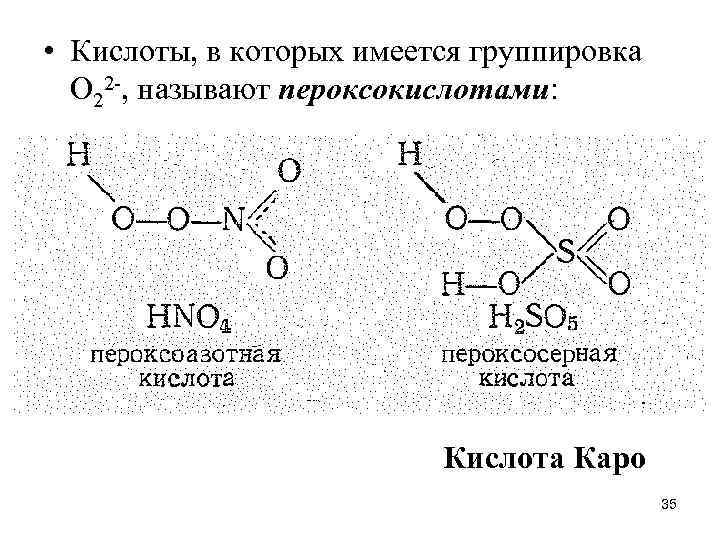 • Кислоты, в которых имеется группировка О 22 -, называют пероксокислотами: Кислота Каро 35
• Кислоты, в которых имеется группировка О 22 -, называют пероксокислотами: Кислота Каро 35
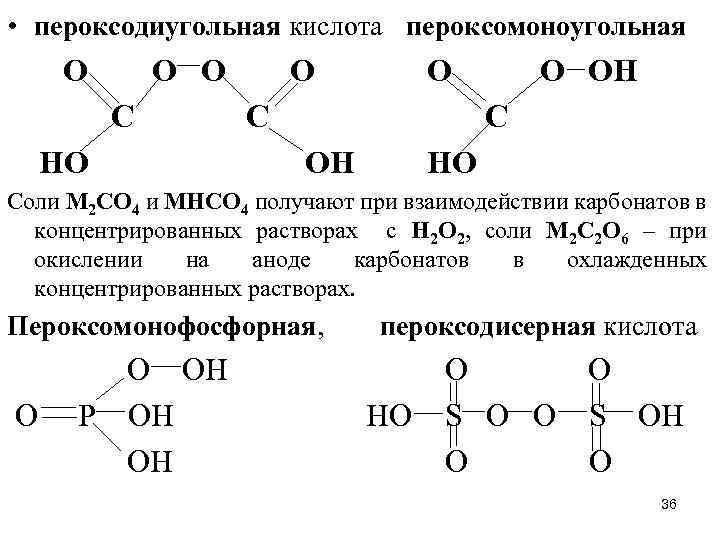 • пероксодиугольная кислота пероксомоноугольная О О О С НО О О С О ОН С ОН НО Соли М 2 СО 4 и МНСО 4 получают при взаимодействии карбонатов в концентрированных растворах с Н 2 О 2, соли М 2 С 2 О 6 – при окислении на аноде карбонатов в охлажденных концентрированных растворах. Пероксомонофосфорная, О О ОН Р ОН OH пероксодисерная кислота О О НО S O O S OH O O 36
• пероксодиугольная кислота пероксомоноугольная О О О С НО О О С О ОН С ОН НО Соли М 2 СО 4 и МНСО 4 получают при взаимодействии карбонатов в концентрированных растворах с Н 2 О 2, соли М 2 С 2 О 6 – при окислении на аноде карбонатов в охлажденных концентрированных растворах. Пероксомонофосфорная, О О ОН Р ОН OH пероксодисерная кислота О О НО S O O S OH O O 36
 • Соединения кислорода (II) и кислорода (I). Можно считать, что электроположительная поляризация атомов кислорода проявляется в соединениях с фтором, а также в ионе О 2+. • Энергия ионизации молекулы О 2 довольно значительная (12, 08 э. В), однако при взаимодействии О 2 с сильнейшим окислителем Рt. F 6 образуется солеподобное вещество О 2+[Рt. F 6]- , в котором роль катиона играет молекулярный ион О 2+ (диоксигенил). [: O O: ] 37
• Соединения кислорода (II) и кислорода (I). Можно считать, что электроположительная поляризация атомов кислорода проявляется в соединениях с фтором, а также в ионе О 2+. • Энергия ионизации молекулы О 2 довольно значительная (12, 08 э. В), однако при взаимодействии О 2 с сильнейшим окислителем Рt. F 6 образуется солеподобное вещество О 2+[Рt. F 6]- , в котором роль катиона играет молекулярный ион О 2+ (диоксигенил). [: O O: ] 37
![O 2 + Pt. F 6 = O 2+[Pt. F 6]восстановитель Гексафтороплатинат (V) диоксигенила O 2 + Pt. F 6 = O 2+[Pt. F 6]восстановитель Гексафтороплатинат (V) диоксигенила](https://present5.com/presentation/3/33311487_173390455.pdf-img/33311487_173390455.pdf-38.jpg) O 2 + Pt. F 6 = O 2+[Pt. F 6]восстановитель Гексафтороплатинат (V) диоксигенила О 2[Рt. F 6] – парамагнитное вещество красного цвета, плавится с разложением при 219 °С. Синтез этого соединения канадским ученым Н. Бартлетом в 1962 г. послужил толчком к синтезу соединений ксенона, энергия ионизации которого близка к таковой молекулы кислорода. 38
O 2 + Pt. F 6 = O 2+[Pt. F 6]восстановитель Гексафтороплатинат (V) диоксигенила О 2[Рt. F 6] – парамагнитное вещество красного цвета, плавится с разложением при 219 °С. Синтез этого соединения канадским ученым Н. Бартлетом в 1962 г. послужил толчком к синтезу соединений ксенона, энергия ионизации которого близка к таковой молекулы кислорода. 38
 Дифторид кислорода OF 2 (получают при быстром пропускании фтора через охлажденный 2% р-р щелочи) 2 F 2 + 2 Na. OH = OF 2 + Na. F + H 2 O - Ядовитый газ бледно-желтого цвета, термически устойчив (200 -250 о. С), сильный окислитель, эффективный фторирующий агент (d. OF=0, 139 нм, FOF = 104 о 16‘). В диоксидифториде O 2 F 2 радикал О 22+ ковалентно связан с атомами фтора. Красная летучая жидкость, образуется при взаимодействии простых веществ в электрическом разряде или под воздействием ионизирующих излучений при температуре -190 о. С. F О О + F 2 = O O (крайне неустойчиво) F полиоксодифториды (O 4 F 2, O 5 F 2, O 6 F 2) 39
Дифторид кислорода OF 2 (получают при быстром пропускании фтора через охлажденный 2% р-р щелочи) 2 F 2 + 2 Na. OH = OF 2 + Na. F + H 2 O - Ядовитый газ бледно-желтого цвета, термически устойчив (200 -250 о. С), сильный окислитель, эффективный фторирующий агент (d. OF=0, 139 нм, FOF = 104 о 16‘). В диоксидифториде O 2 F 2 радикал О 22+ ковалентно связан с атомами фтора. Красная летучая жидкость, образуется при взаимодействии простых веществ в электрическом разряде или под воздействием ионизирующих излучений при температуре -190 о. С. F О О + F 2 = O O (крайне неустойчиво) F полиоксодифториды (O 4 F 2, O 5 F 2, O 6 F 2) 39
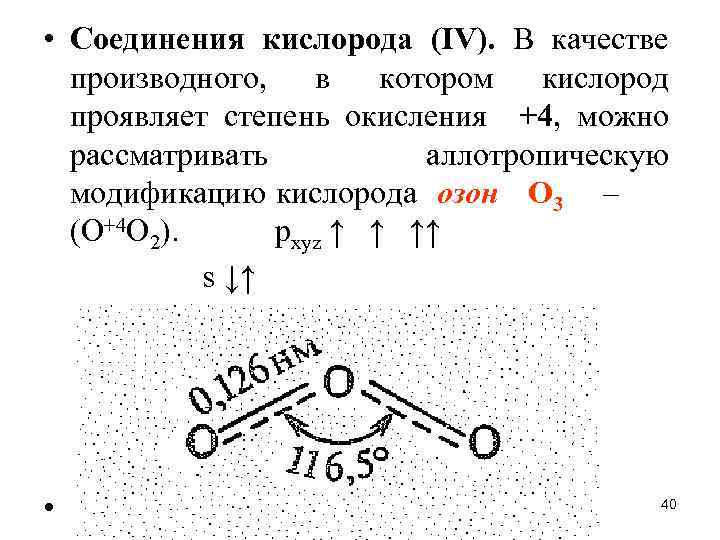 • Соединения кислорода (IV). В качестве производного, в котором кислород проявляет степень окисления +4, можно рассматривать аллотропическую модификацию кислорода озон O 3 – (О+4 O 2). рxyz ↑ ↑ ↑↑ s ↓↑ • ` 40
• Соединения кислорода (IV). В качестве производного, в котором кислород проявляет степень окисления +4, можно рассматривать аллотропическую модификацию кислорода озон O 3 – (О+4 O 2). рxyz ↑ ↑ ↑↑ s ↓↑ • ` 40
 • Центральный атом кислорода молекулы О 3 находится в состоянии sр2 -гибридизации (за счет 2 s-, 2 pх н 2 рy, орбиталей). Две из гибридных sр2 -орбиталей центрального атома участвуют в образовании двух связей О—О (двух молекулярных св. -орбиталей). Третья sр2 -гибридная орбиталь (молекулярная орбиталь) содержит неподеленную электронную пару. 2 рz-орбиталъ центрального атома (расположенная перпендикулярно плоскости расположения атомов) и 2 рz-орбитали крайних атомов участвуют в образовании нелокализованной -связи (молекулярная св. -орбиталь). Таким образом, невозбужденное состояние молекулы О 3 отвечает следующему заполнению молекулярных орбиталей: (2 св. )4( )2. 41
• Центральный атом кислорода молекулы О 3 находится в состоянии sр2 -гибридизации (за счет 2 s-, 2 pх н 2 рy, орбиталей). Две из гибридных sр2 -орбиталей центрального атома участвуют в образовании двух связей О—О (двух молекулярных св. -орбиталей). Третья sр2 -гибридная орбиталь (молекулярная орбиталь) содержит неподеленную электронную пару. 2 рz-орбиталъ центрального атома (расположенная перпендикулярно плоскости расположения атомов) и 2 рz-орбитали крайних атомов участвуют в образовании нелокализованной -связи (молекулярная св. -орбиталь). Таким образом, невозбужденное состояние молекулы О 3 отвечает следующему заполнению молекулярных орбиталей: (2 св. )4( )2. 41
 • Длина связи d. OO (0, 128 нм) является промежуточной между длиной одинарной (0, 149 нм) и двойной связи (0, 1207 нм). Поэтому считают, что в молекуле О 3 порядок связи 1, 5. (Шести электронам, связывающим три атома кислорода, соответствует порядок связи 1, 5). • Озон газ синего цвета с резким раздражающим запахом, очень токсичен. Жидкий озон — темно-синяя жидкость, твердый – темно-фиолетовые кристаллы (Тпл. -192, 7 °С). Поскольку молекула О 3 обладает большей полярностью и поляризуемостью, озон имеет более высокую температуру кипения (-111, 9 °С), чем кислород. Этим же объясняется большая интенсивность окраски озона и лучшая его растворимость в воде. 42
• Длина связи d. OO (0, 128 нм) является промежуточной между длиной одинарной (0, 149 нм) и двойной связи (0, 1207 нм). Поэтому считают, что в молекуле О 3 порядок связи 1, 5. (Шести электронам, связывающим три атома кислорода, соответствует порядок связи 1, 5). • Озон газ синего цвета с резким раздражающим запахом, очень токсичен. Жидкий озон — темно-синяя жидкость, твердый – темно-фиолетовые кристаллы (Тпл. -192, 7 °С). Поскольку молекула О 3 обладает большей полярностью и поляризуемостью, озон имеет более высокую температуру кипения (-111, 9 °С), чем кислород. Этим же объясняется большая интенсивность окраски озона и лучшая его растворимость в воде. 42
 • В естественных условиях озон образуется из атмосферного кислорода при грозовых разрядах, а на высоте 10— 30 км — под действием ультрафиолетовых солнечных лучей. Озон задерживает вредное для жизни ультрафиолетовое излучение Солнца и поглощает инфракрасное излучение Земли, препятствуя ее охлаждению. Следовательно, «озонный пояс» играет большую роль в обеспечении жизни на Земле. • В технике озон получают в озонаторах действием тихого электрического разряда на кислород. 43
• В естественных условиях озон образуется из атмосферного кислорода при грозовых разрядах, а на высоте 10— 30 км — под действием ультрафиолетовых солнечных лучей. Озон задерживает вредное для жизни ультрафиолетовое излучение Солнца и поглощает инфракрасное излучение Земли, препятствуя ее охлаждению. Следовательно, «озонный пояс» играет большую роль в обеспечении жизни на Земле. • В технике озон получают в озонаторах действием тихого электрического разряда на кислород. 43
 • Цепную реакцию образования озона можно представить схемой • • О 2 + h = О 2' + О 2 = О 3 + О О + О 2 = О 3 3 О 2 = 2 О 3 G 0298 = 326 к. Дж/моль Хоть озон и эндотермическое вещество, без катализатора или УФ-облучения разлагается медленно даже при 250 о. С. Жидкий озон и его смеси (70%) взрывоопасны. Более сильный окислитель чем кислород. В обычных условиях окисляет многие малоактивные в-ва (Ag, Hg и др. ) 8 Ag + 2 O 3 = 4 Ag 2 O + O 2 44
• Цепную реакцию образования озона можно представить схемой • • О 2 + h = О 2' + О 2 = О 3 + О О + О 2 = О 3 3 О 2 = 2 О 3 G 0298 = 326 к. Дж/моль Хоть озон и эндотермическое вещество, без катализатора или УФ-облучения разлагается медленно даже при 250 о. С. Жидкий озон и его смеси (70%) взрывоопасны. Более сильный окислитель чем кислород. В обычных условиях окисляет многие малоактивные в-ва (Ag, Hg и др. ) 8 Ag + 2 O 3 = 4 Ag 2 O + O 2 44
 • Сродство к электрону озона около 180 к. Дж/моль, поэтому он может переходить в озонид-ион О 3 -. В частности, при действии озона на щелочные металлы образуются озониды: К + О 3 = КО 3 • Озониды — это соединения состоящие из положительных ионов металла и отрицательных ионов О 3 -. Наличие в ионе О 3 непарного электрона обусловливает парамагнетизм и наличие окраски у озонидов, Обычно они окрашены в красный цвет. • Как сильный окислитель озон используется для очистки питьевой воды, для дезинфекции воздуха, в различных химических синтезах. • Для определения озона можно использовать реакцию 2 I-(р) + O 3(г) + H 2 O(ж) = I 2(тв) + 2 OH-(р) + O 2(г) 45
• Сродство к электрону озона около 180 к. Дж/моль, поэтому он может переходить в озонид-ион О 3 -. В частности, при действии озона на щелочные металлы образуются озониды: К + О 3 = КО 3 • Озониды — это соединения состоящие из положительных ионов металла и отрицательных ионов О 3 -. Наличие в ионе О 3 непарного электрона обусловливает парамагнетизм и наличие окраски у озонидов, Обычно они окрашены в красный цвет. • Как сильный окислитель озон используется для очистки питьевой воды, для дезинфекции воздуха, в различных химических синтезах. • Для определения озона можно использовать реакцию 2 I-(р) + O 3(г) + H 2 O(ж) = I 2(тв) + 2 OH-(р) + O 2(г) 45


