 Т 2. Элементы группы VIIA ФТОР Фтор «F» в невозбужденном состоянии имеет электронную конфигурацию: 1 s 22 p 5. Наличием одного непарного электрона обуславливается сходство фтора с водородом. Однако различие в общем числе валентных электронов и орбиталей предопределяет значительное отличие этих элементов друг от друга. Степень окисления фтора как самого электроотрицательного элемента (4, 0) принимается равной – 1. Максимальная валентность фтора, согласно теории валентных связей, как и других элементов 2 -го периода, равна четырем. 1
Т 2. Элементы группы VIIA ФТОР Фтор «F» в невозбужденном состоянии имеет электронную конфигурацию: 1 s 22 p 5. Наличием одного непарного электрона обуславливается сходство фтора с водородом. Однако различие в общем числе валентных электронов и орбиталей предопределяет значительное отличие этих элементов друг от друга. Степень окисления фтора как самого электроотрицательного элемента (4, 0) принимается равной – 1. Максимальная валентность фтора, согласно теории валентных связей, как и других элементов 2 -го периода, равна четырем. 1
 • Фтор – довольно распространенный элемент. Из минералов фтора наибольшее значение имеют Са. F 2 — плавиковый шпат (флюорит), Nа 3 А 1 F 6 — криолит и Са 5(РО 4)3 F— фторапатит. Фтористые соединения содержатся в организме человека (в основном в зубах и костях). В природе встречается только один изотоп 19 F. Искусственно получены малоустойчивые изотопы (с массовыми числами от 16 до 21). 2
• Фтор – довольно распространенный элемент. Из минералов фтора наибольшее значение имеют Са. F 2 — плавиковый шпат (флюорит), Nа 3 А 1 F 6 — криолит и Са 5(РО 4)3 F— фторапатит. Фтористые соединения содержатся в организме человека (в основном в зубах и костях). В природе встречается только один изотоп 19 F. Искусственно получены малоустойчивые изотопы (с массовыми числами от 16 до 21). 2
 • Простое вещество. Подобно водороду фтор образует двухатомные молекулы F 2, что соответствует следующей электронной конфигурации: • ( sсв)2 ( s разр)2 ( хсв)2 ( y, zсв )4 ( y, zразр)4. • Поскольку на связывающих орбиталях имеется на два электрона больше, чем на разрыхляющих, порядок связи в молекуле F 2 принимается равным 1. 3
• Простое вещество. Подобно водороду фтор образует двухатомные молекулы F 2, что соответствует следующей электронной конфигурации: • ( sсв)2 ( s разр)2 ( хсв)2 ( y, zсв )4 ( y, zразр)4. • Поскольку на связывающих орбиталях имеется на два электрона больше, чем на разрыхляющих, порядок связи в молекуле F 2 принимается равным 1. 3
 • Молекула фтора F 2 имеет относительно небольшую массу и достаточно подвижна, поэтому фтор в обычных условиях — газ (светло-желтого цвета), обладает низкой Тпл. — 223 °С и Ткип. — 187 o. С. • Из-за высокой окислительной активности фтора и большой прочности его соединений фтор получают в свободном состоянии электролизом его расплавленных соединений. Для этих целей обычно используют эвтектическую смесь НF–КF или фторогидрогенаты калия (например K[HF 2] дифторогидрогенат калия). • Фтор и его соединения сильно ядовиты (исключение составляют CF 4, SF 6 - элегаз и некоторые другие вещества). 4
• Молекула фтора F 2 имеет относительно небольшую массу и достаточно подвижна, поэтому фтор в обычных условиях — газ (светло-желтого цвета), обладает низкой Тпл. — 223 °С и Ткип. — 187 o. С. • Из-за высокой окислительной активности фтора и большой прочности его соединений фтор получают в свободном состоянии электролизом его расплавленных соединений. Для этих целей обычно используют эвтектическую смесь НF–КF или фторогидрогенаты калия (например K[HF 2] дифторогидрогенат калия). • Фтор и его соединения сильно ядовиты (исключение составляют CF 4, SF 6 - элегаз и некоторые другие вещества). 4
 • Вследствие высокой химической активности фтор вызывает коррозию почти всех материалов. В качестве материала аппаратуры для получения фтор, его хранения и перевозки используется нержавеющая сталь, медь; никель (и некоторые его сплавы), который устойчив к действию фтора за счет образования защитной пленки Ni. F 2. • В целом проблема эта разрешена, и фтор перевозится в больших количествах в гигантских автоцистернах (обычно в сжиженном виде). 5
• Вследствие высокой химической активности фтор вызывает коррозию почти всех материалов. В качестве материала аппаратуры для получения фтор, его хранения и перевозки используется нержавеющая сталь, медь; никель (и некоторые его сплавы), который устойчив к действию фтора за счет образования защитной пленки Ni. F 2. • В целом проблема эта разрешена, и фтор перевозится в больших количествах в гигантских автоцистернах (обычно в сжиженном виде). 5
 • Широкое применение фтора началось в связи с работами по разделению изотопов урана (в виде 235 UF и 238 UF ) диффузионным методом. 6 6 • UF 4 используется для получения металлического урана. (Фтор также используется в технологии редких элементов Nb, Ta и др. ). В настоящее время фтор широко применяется для синтеза различных хладоагентов и полимерных материалов— фторопластов, отличающихся высокой химической стойкостью. • Жидкий фтор и ряд его соединений применяются в качестве окислителя ракетного топлива. 6
• Широкое применение фтора началось в связи с работами по разделению изотопов урана (в виде 235 UF и 238 UF ) диффузионным методом. 6 6 • UF 4 используется для получения металлического урана. (Фтор также используется в технологии редких элементов Nb, Ta и др. ). В настоящее время фтор широко применяется для синтеза различных хладоагентов и полимерных материалов— фторопластов, отличающихся высокой химической стойкостью. • Жидкий фтор и ряд его соединений применяются в качестве окислителя ракетного топлива. 6
 • Фтор исключительно активен химически, он — сильнейший окислитель. Высокая химическая активность фтора объясняется тем, что его молекула имеет низкую энергию диссоциации (159 к. Дж/моль), в то время как химическая связь в большинстве соединений фтора отличается большой прочностью (порядка 200— 600 к. Дж/моль). (Энергия связи E(H-F) =566, E(Si-F)=582 к. Дж/моль). Кроме того, энергия активации реакций с участием атомов фтора низка (≤ 4 к. Дж/моль). Благодаря малой энергии связи молекулы фтора легко диссоциируют на атомы. • Низкое значение энергии связи молекулы F 2 можно объяснить сильным отталкиванием электронных пар, находящихся на π-орбиталях, обусловленным малой 7 длиной связи F-F.
• Фтор исключительно активен химически, он — сильнейший окислитель. Высокая химическая активность фтора объясняется тем, что его молекула имеет низкую энергию диссоциации (159 к. Дж/моль), в то время как химическая связь в большинстве соединений фтора отличается большой прочностью (порядка 200— 600 к. Дж/моль). (Энергия связи E(H-F) =566, E(Si-F)=582 к. Дж/моль). Кроме того, энергия активации реакций с участием атомов фтора низка (≤ 4 к. Дж/моль). Благодаря малой энергии связи молекулы фтора легко диссоциируют на атомы. • Низкое значение энергии связи молекулы F 2 можно объяснить сильным отталкиванием электронных пар, находящихся на π-орбиталях, обусловленным малой 7 длиной связи F-F.
 • По образному выражению акад. А. Е. Ферсмана, фтор «всесъедающий» . В атмосфере фтора горят такие стойкие вещества, как стекло (в виде ваты), вода: Si. O 2 + 2 F 2 = Si. F 4 + O 2; 2 Н 2 O + 2 F 2 = 4 НF + O 2 (О 3, ОF 2). • В этих реакциях в качестве одного из продуктов горения образуется кислород (!), т. е фтор как окислитель сильнее кислорода. • Pt сгорает во фторе Pt + F 2 = Pt. F 6 (Тпл. = 61, Ткип. = 69 о. С) получается летучее кристаллическое вещество темно-красного цвета. • Относится к числу самых сильных окислителей, является сильнейшим фторирующим реагентом. 8
• По образному выражению акад. А. Е. Ферсмана, фтор «всесъедающий» . В атмосфере фтора горят такие стойкие вещества, как стекло (в виде ваты), вода: Si. O 2 + 2 F 2 = Si. F 4 + O 2; 2 Н 2 O + 2 F 2 = 4 НF + O 2 (О 3, ОF 2). • В этих реакциях в качестве одного из продуктов горения образуется кислород (!), т. е фтор как окислитель сильнее кислорода. • Pt сгорает во фторе Pt + F 2 = Pt. F 6 (Тпл. = 61, Ткип. = 69 о. С) получается летучее кристаллическое вещество темно-красного цвета. • Относится к числу самых сильных окислителей, является сильнейшим фторирующим реагентом. 8
 • Исключительно активно протекает взаимодействие фтора с большинством простых веществ. С серой и фосфором он взаимодействует даже при температуре жидкого воздуха (-190 °С): S + 3 F 2 = SF 6 (г), Нo 298 = -1207 к. Дж/моль; 2 P + 3 F 2 = 2 PF 3 (ж), Нo 298 = -311, 7 к. Дж/моль; 2 Р + 5 F 2 =2 РF 5 (кр), Нo 298 = -3186 к. Дж/моль. Реакции с фтором водородсодержащих веществ (H 2 O, H 2, NH 3, B 2 H 6, Si. H 4, Al. H 3 и др. ) сопровождается образованием HF. 2 NH 3(г) + 3 F 2(г) = 6 HF(г) + N 2(г); Go = — 1604 к. Дж/моль 2 NH 3(г) +6 F 2(г) = 6 HF(г) + 2 NF 3(г); Go = — 1772 к. Дж/моль Первая протекает при высоких Т ( S>0) вторая – при более низких Т ( S<0). 9
• Исключительно активно протекает взаимодействие фтора с большинством простых веществ. С серой и фосфором он взаимодействует даже при температуре жидкого воздуха (-190 °С): S + 3 F 2 = SF 6 (г), Нo 298 = -1207 к. Дж/моль; 2 P + 3 F 2 = 2 PF 3 (ж), Нo 298 = -311, 7 к. Дж/моль; 2 Р + 5 F 2 =2 РF 5 (кр), Нo 298 = -3186 к. Дж/моль. Реакции с фтором водородсодержащих веществ (H 2 O, H 2, NH 3, B 2 H 6, Si. H 4, Al. H 3 и др. ) сопровождается образованием HF. 2 NH 3(г) + 3 F 2(г) = 6 HF(г) + N 2(г); Go = — 1604 к. Дж/моль 2 NH 3(г) +6 F 2(г) = 6 HF(г) + 2 NF 3(г); Go = — 1772 к. Дж/моль Первая протекает при высоких Т ( S>0) вторая – при более низких Т ( S<0). 9
 Фтор окисляет некоторые так называемые инертные газы: (при нормальном Р) Хе + 2 F 2 = Хе. F 4(к), Нo 298 = – 252 к. Дж/моль; Хе + 3 F 2 = Хе. F 6(к) (при повышенном Р = 6 МПа) Хе + F 2 = Хе. F 2(к) (электр. разр. , УФ-излучение) 2 Хе. F 2 = Хе + Хе. F 4; 3 Хе. F 4 = Хе + 2 Хе. F 6 + H 2 O = Хе. OF 4(ж) + 2 HF; Хе. OF 4 +2 H 2 O = Хе. O 3(т) + 4 HF Xe + Pt. F 6 = Xe+[Pt. F 6]-. • Непосредственно фтор не взаимодействует 10 лишь с гелием, неоном и аргоном.
Фтор окисляет некоторые так называемые инертные газы: (при нормальном Р) Хе + 2 F 2 = Хе. F 4(к), Нo 298 = – 252 к. Дж/моль; Хе + 3 F 2 = Хе. F 6(к) (при повышенном Р = 6 МПа) Хе + F 2 = Хе. F 2(к) (электр. разр. , УФ-излучение) 2 Хе. F 2 = Хе + Хе. F 4; 3 Хе. F 4 = Хе + 2 Хе. F 6 + H 2 O = Хе. OF 4(ж) + 2 HF; Хе. OF 4 +2 H 2 O = Хе. O 3(т) + 4 HF Xe + Pt. F 6 = Xe+[Pt. F 6]-. • Непосредственно фтор не взаимодействует 10 лишь с гелием, неоном и аргоном.
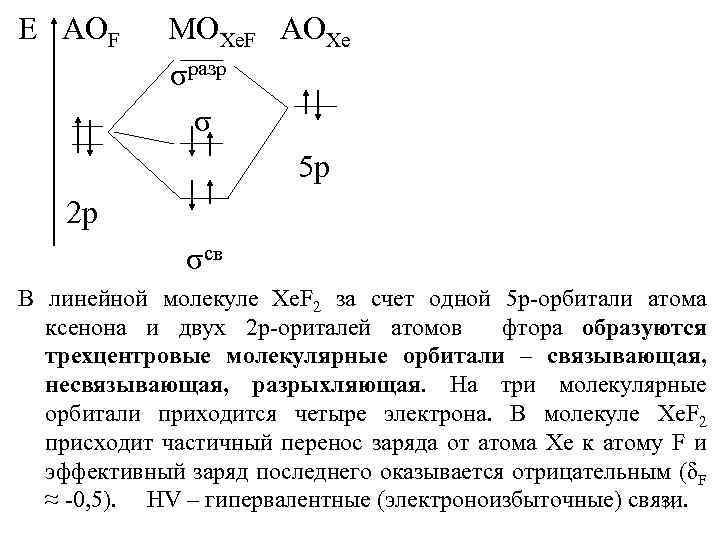 Е АОF MOXe. F AOXe σразр σ 5 p 2 р σсв В линейной молекуле Хе. F 2 за счет одной 5 р-орбитали атома ксенона и двух 2 р-ориталей атомов фтора образуются трехцентровые молекулярные орбитали – связывающая, несвязывающая, разрыхляющая. На три молекулярные орбитали приходится четыре электрона. В молекуле Xe. F 2 присходит частичный перенос заряда от атома Xe к атому F и эффективный заряд последнего оказывается отрицательным (δF ≈ -0, 5). HV – гипервалентные (электроноизбыточные) связи. 11
Е АОF MOXe. F AOXe σразр σ 5 p 2 р σсв В линейной молекуле Хе. F 2 за счет одной 5 р-орбитали атома ксенона и двух 2 р-ориталей атомов фтора образуются трехцентровые молекулярные орбитали – связывающая, несвязывающая, разрыхляющая. На три молекулярные орбитали приходится четыре электрона. В молекуле Xe. F 2 присходит частичный перенос заряда от атома Xe к атому F и эффективный заряд последнего оказывается отрицательным (δF ≈ -0, 5). HV – гипервалентные (электроноизбыточные) связи. 11
 В соответствии с закономерным изменением характера элементов по периодам и группам периодической системы закономерно изменяются и свойства фторидов, например: Химическая природа • • • Na. F, Mg. F 2 основная Al. F 3 амфотерная Al. F 63 Si. F 4, PF 5, SF 6, (Cl. F 5) кислотная Si. F 62 -, PF 6 -, SF 60, (Cl. F 6 -) Известно много прочных комплексов ([BF 4]-, [Be. F 4]2 -, [Si. F 6]2 -, [Al. F 6]3 - и др. ). WF 6>Re. F 6> Os. F 6>Ir. F 6>Pt. F 6 12
В соответствии с закономерным изменением характера элементов по периодам и группам периодической системы закономерно изменяются и свойства фторидов, например: Химическая природа • • • Na. F, Mg. F 2 основная Al. F 3 амфотерная Al. F 63 Si. F 4, PF 5, SF 6, (Cl. F 5) кислотная Si. F 62 -, PF 6 -, SF 60, (Cl. F 6 -) Известно много прочных комплексов ([BF 4]-, [Be. F 4]2 -, [Si. F 6]2 -, [Al. F 6]3 - и др. ). WF 6>Re. F 6> Os. F 6>Ir. F 6>Pt. F 6 12
 • Ионные фториды кристаллические вещества с высокой температурой плавления. Координационное число иона фтора 6 (Nа. F) или 4 (Са. F 2). • Ковалентные фториды газы или жидкости. • Промежуточное положение между ионными и ковалентными фторидами занимают фториды с высокой степенью полярности связи, которые можно назвать ионно-ковалентными соединениями. • К последним, например, можно отнести кристаллические Zn. F 2, Мn. F 2, Со. F 2, Ni. F 2, в которых эффективные заряды электроположительных атомов составляют 1, 56; 1, 63; 1, 46; 1, 40 соответственно. 13
• Ионные фториды кристаллические вещества с высокой температурой плавления. Координационное число иона фтора 6 (Nа. F) или 4 (Са. F 2). • Ковалентные фториды газы или жидкости. • Промежуточное положение между ионными и ковалентными фторидами занимают фториды с высокой степенью полярности связи, которые можно назвать ионно-ковалентными соединениями. • К последним, например, можно отнести кристаллические Zn. F 2, Мn. F 2, Со. F 2, Ni. F 2, в которых эффективные заряды электроположительных атомов составляют 1, 56; 1, 63; 1, 46; 1, 40 соответственно. 13
 • Многие фториды металлов в низких степенях окисления получают действием раствора HF на оксиды, гидроксиды, карбонаты и пр. , например: 3 НF + Аl(ОН)3 = Аl. F 3 + 3 H 2 О • Фториды неметаллов и металлов в высоких степенях окисления получают фторированием простых веществ или низших фторидов, например: F 2 + Cl 2 = 2 Сl. F; Сl. F + F 2 = Сl. F 3; Сl. F 3 + F 2 = Сl. F 5 I 2 + 7 F 2 = 2 IF 7 Стабильность фторидов возрастает с увеличением положительной степени окисления галогенов. Согласно методу МО, трифториды характеризуются неравноценными связями Г-F: одной трехцентровой F-Г-F и одной двухцентровой Г-F. (2 - трехцентровых и 1 -двухцентровых связей 14 соответственно у пентафторида. )
• Многие фториды металлов в низких степенях окисления получают действием раствора HF на оксиды, гидроксиды, карбонаты и пр. , например: 3 НF + Аl(ОН)3 = Аl. F 3 + 3 H 2 О • Фториды неметаллов и металлов в высоких степенях окисления получают фторированием простых веществ или низших фторидов, например: F 2 + Cl 2 = 2 Сl. F; Сl. F + F 2 = Сl. F 3; Сl. F 3 + F 2 = Сl. F 5 I 2 + 7 F 2 = 2 IF 7 Стабильность фторидов возрастает с увеличением положительной степени окисления галогенов. Согласно методу МО, трифториды характеризуются неравноценными связями Г-F: одной трехцентровой F-Г-F и одной двухцентровой Г-F. (2 - трехцентровых и 1 -двухцентровых связей 14 соответственно у пентафторида. )
 • По химической природе ионные фториды являются основными соединениями, а ковалентные фториды — кислотными. Так в реакции 2 Nа. F + Si. F 4 = Nа 2[Si. F 6] основный кислотный гексафторосиликат натрия ионный Nа. F выступает в качестве донора, а ковалентный Si. F 4 — в качестве акцептора электронных пар, носителем которых является фторид-ион F-. 15
• По химической природе ионные фториды являются основными соединениями, а ковалентные фториды — кислотными. Так в реакции 2 Nа. F + Si. F 4 = Nа 2[Si. F 6] основный кислотный гексафторосиликат натрия ионный Nа. F выступает в качестве донора, а ковалентный Si. F 4 — в качестве акцептора электронных пар, носителем которых является фторид-ион F-. 15
 • Основные фториды при гидролизе создают щелочную среду, а кислотные фториды — кислотную Na. F + H 2 O = Na. OH + HF Si. F 4 + 3 Н 2 O = Н 2 Si. О 3 + 4 НF • Амфотерные фториды взаимодействуют как с основными, так и с кислотными фторидами. В последнем случае образуются смешанные фториды, например: 2 КF + Ве. F 2= К 2[Ве. F 4] • (Ве. F 2 как кислотное соединение) Ве. F 2 + Si. F 4 = Be[Si. F 6] • (Ве. F 2 как основное соединение) 16
• Основные фториды при гидролизе создают щелочную среду, а кислотные фториды — кислотную Na. F + H 2 O = Na. OH + HF Si. F 4 + 3 Н 2 O = Н 2 Si. О 3 + 4 НF • Амфотерные фториды взаимодействуют как с основными, так и с кислотными фторидами. В последнем случае образуются смешанные фториды, например: 2 КF + Ве. F 2= К 2[Ве. F 4] • (Ве. F 2 как кислотное соединение) Ве. F 2 + Si. F 4 = Be[Si. F 6] • (Ве. F 2 как основное соединение) 16
 • В неводных растворах PF 5 взаимодействует с основными фторидами KF + PF 5 = KPF 6 • С жидким HF образует НF + PF 5 = HPF 6 – гексафторофосфорная кислота (водный раствор – очень сильная кислота) 17
• В неводных растворах PF 5 взаимодействует с основными фторидами KF + PF 5 = KPF 6 • С жидким HF образует НF + PF 5 = HPF 6 – гексафторофосфорная кислота (водный раствор – очень сильная кислота) 17
 • Комплексные фториды весьма разнообразны. Координационное число по фтору для элементов 2 -го периода равно 4, для элементов других периодов типичное координационное число 6. Кроме того, встречаются комплексные фториды, в которых координационное число комплексообразователя равно 7, 8 и 9, например: К 2[Ве. F 4] К 3[А 1 F 6] К 2[Nb. F 7] К 2[Re. F 9] • Эти же примеры показывают, что во фторокомплексах стабилизируется. высшая степень окисления центральных атомов. • Производные фторокомплексов представляют собой преимущественно ионые соединения либо относятся к смешанным (полимерным) фторидам (например, Ве. Si. F 6). • Соединения с водородом типа НВF 4, НРF 6, Н 2 Si. F 6 в свободном состоянии неустойчивы. Их водные растворы — очень сильные кислоты (типа HCl. O 4). 18
• Комплексные фториды весьма разнообразны. Координационное число по фтору для элементов 2 -го периода равно 4, для элементов других периодов типичное координационное число 6. Кроме того, встречаются комплексные фториды, в которых координационное число комплексообразователя равно 7, 8 и 9, например: К 2[Ве. F 4] К 3[А 1 F 6] К 2[Nb. F 7] К 2[Re. F 9] • Эти же примеры показывают, что во фторокомплексах стабилизируется. высшая степень окисления центральных атомов. • Производные фторокомплексов представляют собой преимущественно ионые соединения либо относятся к смешанным (полимерным) фторидам (например, Ве. Si. F 6). • Соединения с водородом типа НВF 4, НРF 6, Н 2 Si. F 6 в свободном состоянии неустойчивы. Их водные растворы — очень сильные кислоты (типа HCl. O 4). 18
 • Фтор со взрывом взаимодействует с водородом даже при низких температурах и (в отличие от хлора) в темноте с образование фтористого водорода H 2 + F 2 = 2 HF Обычно фтористый водород получают при нагревании действием серной кислоты на флюорит: Ca. F 2 + H 2 SO 4 = Ca. SO 4 + 2 HF 19
• Фтор со взрывом взаимодействует с водородом даже при низких температурах и (в отличие от хлора) в темноте с образование фтористого водорода H 2 + F 2 = 2 HF Обычно фтористый водород получают при нагревании действием серной кислоты на флюорит: Ca. F 2 + H 2 SO 4 = Ca. SO 4 + 2 HF 19
 • Молекула фторида водорода НF сильно полярна и имеет большую склонность к ассоциации за счет водородных связей в зигзагообразные цепи. Поэтому фторид водорода в обычных условиях — бесцветная жидкость (Тпл. -83 °С, Ткип. 19, 5 о. С) с резким запахом, сильно дымящая на воздухе. • Даже в состоянии газа фторид водорода состоит из смеси полимеров Н 2 F 2, Н 3 F 3, Н 4 F 4, Н 5 F 5, Н 6 F 6. Простые молекулы НF существуют лишь при температурах выше 90 °С. Вследствие высокой прочности связи (энергия диссоциации 565 к. Дж/моль) термический распад НF на атомы становится заметным выше 3500 o. C. 20
• Молекула фторида водорода НF сильно полярна и имеет большую склонность к ассоциации за счет водородных связей в зигзагообразные цепи. Поэтому фторид водорода в обычных условиях — бесцветная жидкость (Тпл. -83 °С, Ткип. 19, 5 о. С) с резким запахом, сильно дымящая на воздухе. • Даже в состоянии газа фторид водорода состоит из смеси полимеров Н 2 F 2, Н 3 F 3, Н 4 F 4, Н 5 F 5, Н 6 F 6. Простые молекулы НF существуют лишь при температурах выше 90 °С. Вследствие высокой прочности связи (энергия диссоциации 565 к. Дж/моль) термический распад НF на атомы становится заметным выше 3500 o. C. 20
 • Собственная ионизация жидкого НF незначительна (К = 2, 07 10 -11). Она происходит путем перехода протона (или соответственно иона фтора) от одной молекулы к другой, сопровождающегося превращением водородной связи из межмолекулярной в межатомную и в ковалентную. При этом образуются сольватированные фтороний-ион FH 2+ и фторогидрогенат-ион НF 2 - по схеме Н—F [H—F—H]+ + [F—Н—F]- 21
• Собственная ионизация жидкого НF незначительна (К = 2, 07 10 -11). Она происходит путем перехода протона (или соответственно иона фтора) от одной молекулы к другой, сопровождающегося превращением водородной связи из межмолекулярной в межатомную и в ковалентную. При этом образуются сольватированные фтороний-ион FH 2+ и фторогидрогенат-ион НF 2 - по схеме Н—F [H—F—H]+ + [F—Н—F]- 21
 • Жидкий фторид водорода - сильный ионизирующий растворитель. В нем хорошо растворяются вода, фториды, сульфаты и нитраты s-элементов I группы, несколько хуже аналогичные соединения s-элементов II группы. При этом растворенные вещества, отнимая от молекул НF протоны, увеличивают концентрацию отрицательных ионов (HF 2 -), т. е. ведут себя как основания. Например: КNO 3 + 2 НF К+ + НNO 3 + HF 2 - 22
• Жидкий фторид водорода - сильный ионизирующий растворитель. В нем хорошо растворяются вода, фториды, сульфаты и нитраты s-элементов I группы, несколько хуже аналогичные соединения s-элементов II группы. При этом растворенные вещества, отнимая от молекул НF протоны, увеличивают концентрацию отрицательных ионов (HF 2 -), т. е. ведут себя как основания. Например: КNO 3 + 2 НF К+ + НNO 3 + HF 2 - 22
 • Даже НNО 3 в этих условиях ведет себя как основание: НNО 3 + 2 НF NО 3 Н 2+ + HF 2 • индифферентный в воде этиловый спирт в жидком фториде водорода оказывается таким же сильным основанием, как КОН в воде: С 2 Н 5 ОН + 2 НF С 2 Н 5 OН 2+ + HF 2 - 23
• Даже НNО 3 в этих условиях ведет себя как основание: НNО 3 + 2 НF NО 3 Н 2+ + HF 2 • индифферентный в воде этиловый спирт в жидком фториде водорода оказывается таким же сильным основанием, как КОН в воде: С 2 Н 5 ОН + 2 НF С 2 Н 5 OН 2+ + HF 2 - 23
 • В жидком НF ведут себя как кислоты вещества — акцепторы фторид-ионов, например BF 3, Sb. F 5: BF 3 + 2 НF = FH 2+ + ВF 4 Sb. F 5 + 2 НF = FH 2+ + Sb. F 6 • При растворении кислот увеличивается концентрация положительных фтороний-ионов FH 2+. 24
• В жидком НF ведут себя как кислоты вещества — акцепторы фторид-ионов, например BF 3, Sb. F 5: BF 3 + 2 НF = FH 2+ + ВF 4 Sb. F 5 + 2 НF = FH 2+ + Sb. F 6 • При растворении кислот увеличивается концентрация положительных фтороний-ионов FH 2+. 24
 • Амфотерными соединениями в жидком НF являются, например, фториды алюминия и хрома (III): 3 Nа. F + АIF 3 3 Nа+ + А 1 F 63(АIF 3 как кислотное соединение) Аl. F 3 + 3 ВF 3 А 13+ + 3 ВF 4(АIF 3 как основное соединение) 25
• Амфотерными соединениями в жидком НF являются, например, фториды алюминия и хрома (III): 3 Nа. F + АIF 3 3 Nа+ + А 1 F 63(АIF 3 как кислотное соединение) Аl. F 3 + 3 ВF 3 А 13+ + 3 ВF 4(АIF 3 как основное соединение) 25
 • HF неограниченно растворяется в воде. HF ионизируется с образованием ионов OH 3+ и F-. • Последние взаимодействуя с HF, образуют фторогидрогенат-ионы: 2 HF +Н 2 О = OH 3+ +НF 2 -. • Раствор НF (плавиковая кислота) (фтороводородная = фтористоводородная) является кислотой средней силы (К=6, 2 10 -4). • В растворе содержатся также комплексные ионы Н 2 F 3 -, Н 3 F 4 -, Нn. Fn+1 -. Поэтому при нейтрализации растворов плавиковой кислоты образуются не фториды, а фторогидрогенаты типа К[НF 2]. 26
• HF неограниченно растворяется в воде. HF ионизируется с образованием ионов OH 3+ и F-. • Последние взаимодействуя с HF, образуют фторогидрогенат-ионы: 2 HF +Н 2 О = OH 3+ +НF 2 -. • Раствор НF (плавиковая кислота) (фтороводородная = фтористоводородная) является кислотой средней силы (К=6, 2 10 -4). • В растворе содержатся также комплексные ионы Н 2 F 3 -, Н 3 F 4 -, Нn. Fn+1 -. Поэтому при нейтрализации растворов плавиковой кислоты образуются не фториды, а фторогидрогенаты типа К[НF 2]. 26
![• При нейтрализации HF образуются фторогидрогенаты 2 HF + KOH = K[HF 2] • При нейтрализации HF образуются фторогидрогенаты 2 HF + KOH = K[HF 2]](https://present5.com/presentation/-42637833_141829201/image-27.jpg) • При нейтрализации HF образуются фторогидрогенаты 2 HF + KOH = K[HF 2] + H 2 O КНF 2, КH 2 F 3, КH 3 F 4, КH 4 F 5 Тпл соответственно 239, 62, 66, 72 о. С • Эти соединения, как правило, хорошо кристаллизуются и плавятся без разложения Полимерные гидрогенат-ионы имеют зигзагообразную форму. Они образованы за счет водородной связи. 27
• При нейтрализации HF образуются фторогидрогенаты 2 HF + KOH = K[HF 2] + H 2 O КНF 2, КH 2 F 3, КH 3 F 4, КH 4 F 5 Тпл соответственно 239, 62, 66, 72 о. С • Эти соединения, как правило, хорошо кристаллизуются и плавятся без разложения Полимерные гидрогенат-ионы имеют зигзагообразную форму. Они образованы за счет водородной связи. 27
 • Термическое разложение фторогидрогенатов используется для получения чистого НF и фторида металла: KHF 2 = KF + HF К [Нn. Fn+1] = К [Нn-1 Fn] + НF 28
• Термическое разложение фторогидрогенатов используется для получения чистого НF и фторида металла: KHF 2 = KF + HF К [Нn. Fn+1] = К [Нn-1 Fn] + НF 28
 • Характерная особенность плавиковой кислоты (фтористоводородной = фтороводородной) ее способность взаимодействовать с диоксидом кремния: Si. O 2 (к) + 4 НF (р) = Si. F 4 (г) + 2 Н 2 O (ж) Si. F 4 (г) + 2 НF (р) = H 2 Si. F 6 (р) • Поэтому ее обычно хранят в сосудах из свинца, каучука, полиэтилена или парафина, а не в стеклянной посуде. Она токсична, при попадании на кожу вызывает плохо заживающие болезненные язвы. • Плавиковая кислота применяется для травления стекла, удаления песка с металлического литья, получения фторидов и т. д. Фторид водорода в основном используется в органическом синтезе. 29
• Характерная особенность плавиковой кислоты (фтористоводородной = фтороводородной) ее способность взаимодействовать с диоксидом кремния: Si. O 2 (к) + 4 НF (р) = Si. F 4 (г) + 2 Н 2 O (ж) Si. F 4 (г) + 2 НF (р) = H 2 Si. F 6 (р) • Поэтому ее обычно хранят в сосудах из свинца, каучука, полиэтилена или парафина, а не в стеклянной посуде. Она токсична, при попадании на кожу вызывает плохо заживающие болезненные язвы. • Плавиковая кислота применяется для травления стекла, удаления песка с металлического литья, получения фторидов и т. д. Фторид водорода в основном используется в органическом синтезе. 29
 • В соединениях со фтором у кислорода проявляется электроположительная поляризация атомов. • Простейший представитель такого рода соединений — дифторид кислорода ОF 2: его получают при быстром пропускании фтора через охлажденный 2% -ный раствор щелочи: 2 F 2 + 2 Na. OH = OF 2 + 2 Na. F + H 2 O. • ОF 2 в воде малорастворим и с ней не взаимодействует. Он смешивается (не реагируя) с Н 2, СН 4 или СО. При пропускании через такую смесь искры происходит сильный взрыв. Смеси ОF 2 с Cl 2, Br 2 и I 2 взрываются при комнатной температуре. ОF 2 выделяет остальные галогениды из их кислот и солей: ОF 2 +4 НX (ag) = 2 X 2 + 2 HF + H 2 O. 30
• В соединениях со фтором у кислорода проявляется электроположительная поляризация атомов. • Простейший представитель такого рода соединений — дифторид кислорода ОF 2: его получают при быстром пропускании фтора через охлажденный 2% -ный раствор щелочи: 2 F 2 + 2 Na. OH = OF 2 + 2 Na. F + H 2 O. • ОF 2 в воде малорастворим и с ней не взаимодействует. Он смешивается (не реагируя) с Н 2, СН 4 или СО. При пропускании через такую смесь искры происходит сильный взрыв. Смеси ОF 2 с Cl 2, Br 2 и I 2 взрываются при комнатной температуре. ОF 2 выделяет остальные галогениды из их кислот и солей: ОF 2 +4 НX (ag) = 2 X 2 + 2 HF + H 2 O. 30
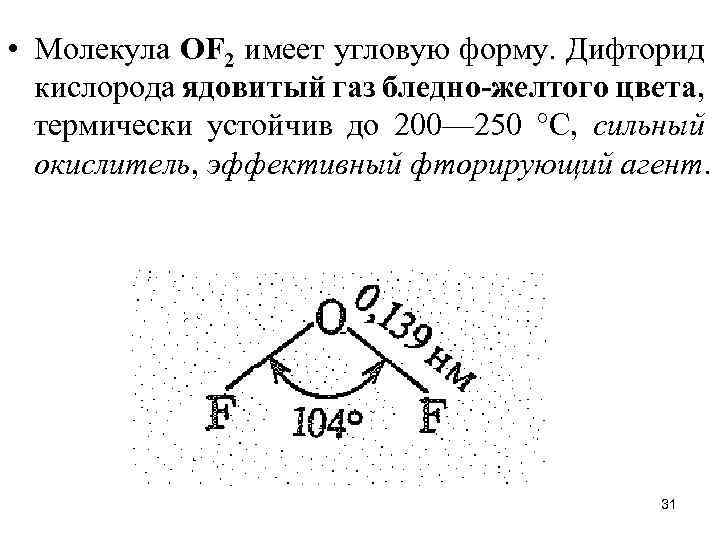 • Молекула ОF 2 имеет угловую форму. Дифторид кислорода ядовитый газ бледно-желтого цвета, термически устойчив до 200— 250 °С, сильный окислитель, эффективный фторирующий агент. 31
• Молекула ОF 2 имеет угловую форму. Дифторид кислорода ядовитый газ бледно-желтого цвета, термически устойчив до 200— 250 °С, сильный окислитель, эффективный фторирующий агент. 31
 ОF 2 довольно легко гидролизуется основаниями, водой – гораздо медленнее: OF 2 + 2 Na. OH = 2 Na. F + O 2 + H 2 O. Но с горячим паром происходит взрыв: ОF 2 + Н 2 О = О 2 + 2 HF. • Молекула О 2 F 2 образуется (в виде красной летучей жидкости) в результате непосредственного взаимодействия простых веществ в электрическом разряде или под действием ионизирующих излучений при температуре жидкого воздуха (-190 °С). (Разлагается при – 57 о. С). Оранжево-желтый газ при н. у. Диамагнитна (все электроны спарены). В диоксидифториде О 2 F 2 радикал О 22+ ковалентно 32 связан с атомами фтора.
ОF 2 довольно легко гидролизуется основаниями, водой – гораздо медленнее: OF 2 + 2 Na. OH = 2 Na. F + O 2 + H 2 O. Но с горячим паром происходит взрыв: ОF 2 + Н 2 О = О 2 + 2 HF. • Молекула О 2 F 2 образуется (в виде красной летучей жидкости) в результате непосредственного взаимодействия простых веществ в электрическом разряде или под действием ионизирующих излучений при температуре жидкого воздуха (-190 °С). (Разлагается при – 57 о. С). Оранжево-желтый газ при н. у. Диамагнитна (все электроны спарены). В диоксидифториде О 2 F 2 радикал О 22+ ковалентно 32 связан с атомами фтора.
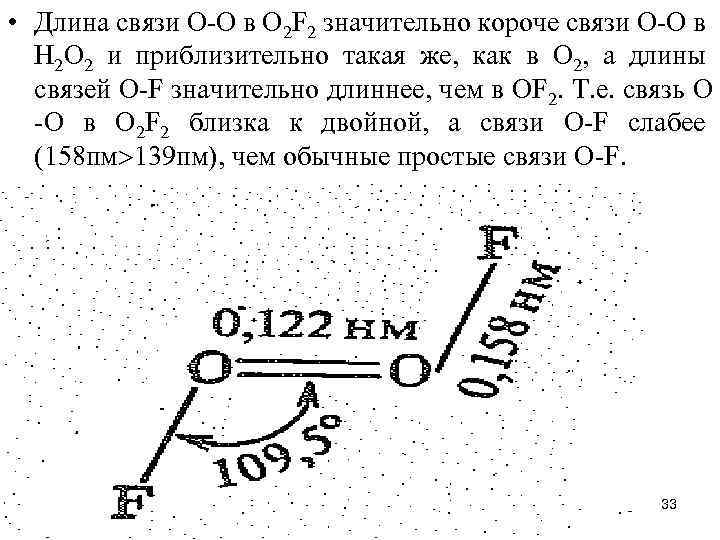 • Длина связи О-О в О 2 F 2 значительно короче связи О-О в Н 2 О 2 и приблизительно такая же, как в О 2, а длины связей О-F значительно длиннее, чем в ОF 2. Т. е. связь О -О в О 2 F 2 близка к двойной, а связи О-F слабее (158 пм 139 пм), чем обычные простые связи О-F. 33
• Длина связи О-О в О 2 F 2 значительно короче связи О-О в Н 2 О 2 и приблизительно такая же, как в О 2, а длины связей О-F значительно длиннее, чем в ОF 2. Т. е. связь О -О в О 2 F 2 близка к двойной, а связи О-F слабее (158 пм 139 пм), чем обычные простые связи О-F. 33
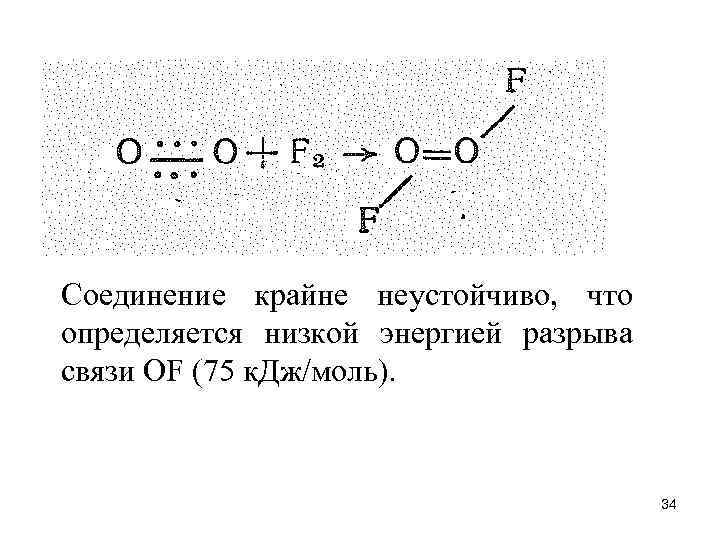 Соединение крайне неустойчиво, что определяется низкой энергией разрыва связи ОF (75 к. Дж/моль). 34
Соединение крайне неустойчиво, что определяется низкой энергией разрыва связи ОF (75 к. Дж/моль). 34
 • Получены также полиоксидифториды типа О 4 F 2, О 5 F 2 и О 6 F 2, существующие лишь при низкой температуре (-190 °С). Предполагают, что их молекулы имеют цепное строение, например F—О—О—F. • Термическая устойчивость полиоксидифторидов уменьшается с увеличением числа атомов в молекуле Оn. F 2 (n = 2 – 6). 35
• Получены также полиоксидифториды типа О 4 F 2, О 5 F 2 и О 6 F 2, существующие лишь при низкой температуре (-190 °С). Предполагают, что их молекулы имеют цепное строение, например F—О—О—F. • Термическая устойчивость полиоксидифторидов уменьшается с увеличением числа атомов в молекуле Оn. F 2 (n = 2 – 6). 35


