L_18_T_10_Elementy_IIA__Be_Mg_Ca.ppt
- Количество слайдов: 52
 Т 10 Л 18 s-ЭЛЕМЕНТЫ IIA ГРУППЫ ПЕРИОДИЧЕСКОЙ СИСТЕМЫ К s-элементам II группы относятся типические элементы — бериллий Ве и магний Мg и элементы подгруппы кальция - кальций Са, стронций Sr, барий Ва, радий Ra. Некоторые константы этих элементов приведены ниже: 1
Т 10 Л 18 s-ЭЛЕМЕНТЫ IIA ГРУППЫ ПЕРИОДИЧЕСКОЙ СИСТЕМЫ К s-элементам II группы относятся типические элементы — бериллий Ве и магний Мg и элементы подгруппы кальция - кальций Са, стронций Sr, барий Ва, радий Ra. Некоторые константы этих элементов приведены ниже: 1
 • В соответствии со строением валентного электронного слоя s-элементы IIА группы проявляют степень окисления +2. • Как и в других главных подгруппах, в ряду рассматриваемых элементов с увеличением порядкового номера энергия ионизации атомов уменьшается, радиусы атомов и ионов увеличиваются, металлические признаки химических элементов усиливаются. 2
• В соответствии со строением валентного электронного слоя s-элементы IIА группы проявляют степень окисления +2. • Как и в других главных подгруппах, в ряду рассматриваемых элементов с увеличением порядкового номера энергия ионизации атомов уменьшается, радиусы атомов и ионов увеличиваются, металлические признаки химических элементов усиливаются. 2
 Бериллий • У бериллия (1 s 22 s 2) по сравнению с бором (1 s 22 р1) в соответствии с увеличением радиуса атома и уменьшением числа валентных электронов неметаллические признаки проявляются слабее, а металлические усиливаются. Бериллий обладает более высокими энергиями ионизации атома (I 1 = 9, 32 э. В, I 2 = 18, 21 э. В), чем остальные s-элементы II группы. В то же время он во многом сходен с алюминием (диагональное сходство в периодической системе) и является типичным амфотерным элементом: в обычных условиях он простых ионов не образует; для него характерны комплексные ионы как катионного, так и анионного типа. Во всех устойчивых соединениях степень окисления бериллия +2. Для Ве (II) наиболее характерно координационное число 4 (sр33 гибридизация валентных орбиталей). (ОЭО 1, 47).
Бериллий • У бериллия (1 s 22 s 2) по сравнению с бором (1 s 22 р1) в соответствии с увеличением радиуса атома и уменьшением числа валентных электронов неметаллические признаки проявляются слабее, а металлические усиливаются. Бериллий обладает более высокими энергиями ионизации атома (I 1 = 9, 32 э. В, I 2 = 18, 21 э. В), чем остальные s-элементы II группы. В то же время он во многом сходен с алюминием (диагональное сходство в периодической системе) и является типичным амфотерным элементом: в обычных условиях он простых ионов не образует; для него характерны комплексные ионы как катионного, так и анионного типа. Во всех устойчивых соединениях степень окисления бериллия +2. Для Ве (II) наиболее характерно координационное число 4 (sр33 гибридизация валентных орбиталей). (ОЭО 1, 47).
 • В земной коре бериллий находится в виде изотопа 9 Ве. Его важнейшие минералы: берилл Ве Аl (Si. O ) , 3 2 3 6 фенакит Ве 2 Si. O 4. Окрашенные примесями прозрачные разновидности берилла (зеленые изумруды, голубые аквамарины и др. ) — драгоценные камни. В настоящее время их получают искусственно. • Содержание в земной коре составляет: Be 6 10 -4 %, Mg 2, 4%, Ca 2, 96%, Sr 4 10 -2 %, Ba 5 10 -2 %. Mg и Ca широко распространены в природе, остальные – мало распространены. В свободном состоянии металлы этой группы не встречаются. Mg и Ca входят в состав многих силикатов и алюмосиликатов. В результате механического разрушения, гидролиза, действия СО 2 соединения Mg и Ca переходят в речную воду, далее в океан. 4
• В земной коре бериллий находится в виде изотопа 9 Ве. Его важнейшие минералы: берилл Ве Аl (Si. O ) , 3 2 3 6 фенакит Ве 2 Si. O 4. Окрашенные примесями прозрачные разновидности берилла (зеленые изумруды, голубые аквамарины и др. ) — драгоценные камни. В настоящее время их получают искусственно. • Содержание в земной коре составляет: Be 6 10 -4 %, Mg 2, 4%, Ca 2, 96%, Sr 4 10 -2 %, Ba 5 10 -2 %. Mg и Ca широко распространены в природе, остальные – мало распространены. В свободном состоянии металлы этой группы не встречаются. Mg и Ca входят в состав многих силикатов и алюмосиликатов. В результате механического разрушения, гидролиза, действия СО 2 соединения Mg и Ca переходят в речную воду, далее в океан. 4
 Простое вещество. Бериллий в виде простого вещества — металл (Tпл. 1284 о. С, Ткип. 2970 °С) серо-стального цвета, имеет плотную гексагональную кристаллическую решетку, довольно тверд и хрупок. На воздухе, как и алюминий, покрывается оксидной пленкой, придающей ему матовый оттенок и обусловливающей пониженную химическую активность. При нагревании бериллий сгорает в кислороде и на воздухе, взаимодействует с серой, азотом. С галогенами реагирует при обычных температурах или при небольшом нагревании. Все эти реакции сопровождаются выделением значительного количества тепла, что определяется большой прочностью кристаллических решеток продуктов взаимодействия: Ве. О, Ве. S, Ве 3 N 2 и др. С водородом в обычных 5 условиях Ве не реагирует.
Простое вещество. Бериллий в виде простого вещества — металл (Tпл. 1284 о. С, Ткип. 2970 °С) серо-стального цвета, имеет плотную гексагональную кристаллическую решетку, довольно тверд и хрупок. На воздухе, как и алюминий, покрывается оксидной пленкой, придающей ему матовый оттенок и обусловливающей пониженную химическую активность. При нагревании бериллий сгорает в кислороде и на воздухе, взаимодействует с серой, азотом. С галогенами реагирует при обычных температурах или при небольшом нагревании. Все эти реакции сопровождаются выделением значительного количества тепла, что определяется большой прочностью кристаллических решеток продуктов взаимодействия: Ве. О, Ве. S, Ве 3 N 2 и др. С водородом в обычных 5 условиях Ве не реагирует.
 • Защитная оксидная пленка препятствует взаимодействию бериллия (Еo 298 = — 1, 85 В) с водой. Но, подобно алюминию, он реагирует с кислотами и щелочами, с выделением водорода, образуя катионные и анионные комплексы: Be + 2 OH 3+ + 2 H 2 O = [Be(OH 2)4]2+ + H 2 Be + 2 OH- + 2 H 2 O = [Be(OH)4]2 - + H 2 • В холодных концентрированных НNO 3 и Н 2 SO 4 бериллий (как и Аl) пассивируется. • Получают электролизом расплава Na. Cl+Be. Cl 2 (350 o. C), • или магнийтермическим способом Mg + Be. F 2 = Mg. F 2 + Be 6
• Защитная оксидная пленка препятствует взаимодействию бериллия (Еo 298 = — 1, 85 В) с водой. Но, подобно алюминию, он реагирует с кислотами и щелочами, с выделением водорода, образуя катионные и анионные комплексы: Be + 2 OH 3+ + 2 H 2 O = [Be(OH 2)4]2+ + H 2 Be + 2 OH- + 2 H 2 O = [Be(OH)4]2 - + H 2 • В холодных концентрированных НNO 3 и Н 2 SO 4 бериллий (как и Аl) пассивируется. • Получают электролизом расплава Na. Cl+Be. Cl 2 (350 o. C), • или магнийтермическим способом Mg + Be. F 2 = Mg. F 2 + Be 6
 • С металлами бериллий образует интерметаллические соединения. Бериллиды ряда d-элементов состава МВе 12 (М=Тi, Nb, Та, Мо), МВе 11 (М = Nb, Та) и другие имеют высокую температуру плавления и не окисляются при нагревании до 1200— 1600 °С. • Бериллий используют в качестве легирующей добавки к сплавам, придающей им повышенную коррозионную стойкость, высокую прочность и твердость. Наиболее ценны сплавы Сu — Ве (бериллиевые бронзы), содержащие до 2, 5% Ве. Сплавы бериллия применяют в самолетостроении, электротехнике и др. 7
• С металлами бериллий образует интерметаллические соединения. Бериллиды ряда d-элементов состава МВе 12 (М=Тi, Nb, Та, Мо), МВе 11 (М = Nb, Та) и другие имеют высокую температуру плавления и не окисляются при нагревании до 1200— 1600 °С. • Бериллий используют в качестве легирующей добавки к сплавам, придающей им повышенную коррозионную стойкость, высокую прочность и твердость. Наиболее ценны сплавы Сu — Ве (бериллиевые бронзы), содержащие до 2, 5% Ве. Сплавы бериллия применяют в самолетостроении, электротехнике и др. 7
 • В атомных реакторах бериллий используется как замедлитель и отражатель нейтронов. • В смеси с препаратами радия бериллий служит источником нейтронов, образующихся при действии на 9 Ве альфа-частиц: 9 Be + 4 He = 12 C + 1 n 4 2 6 0 • Соединения бериллия ядовиты! • Большинство неорганических соединений бериллия (II) в обычных условиях полимерны и являются кристаллическими веществами белого цвета. 8
• В атомных реакторах бериллий используется как замедлитель и отражатель нейтронов. • В смеси с препаратами радия бериллий служит источником нейтронов, образующихся при действии на 9 Ве альфа-частиц: 9 Be + 4 He = 12 C + 1 n 4 2 6 0 • Соединения бериллия ядовиты! • Большинство неорганических соединений бериллия (II) в обычных условиях полимерны и являются кристаллическими веществами белого цвета. 8
 • Оксид Ве. О отличается высокой энергией кристаллической решетки и высокой энергией Гиббса ( Gof = — 582 к. Дж/моль). Он тугоплавок (Тпл. 2530 о. С), теплопроводен; прокаленный (при 400 °С) при низких температурах химически неактивен. Применяют Ве. О в качестве химически стойкого и огнеупорного материала для изготовления тиглей и специальной керамики, а в атомной энергетике — как замедлитель и отражатель нейтронов. • Ве. О входит в состав некоторых стеклообразующих смесей. • Будучи амфотерным, Ве. О взаимодействует при сплавлении и с основными, и с кислотными оксидами: Be. O + Si. O 2 = Be. Si. O 3 основный Be. O + Na 2 O = Na 2 Be. O 2 кислотный • При нагревании Ве. О взаимодействует с кислотами и щелочами: Ве. О + 2 ОН 3+ + Н 2 О = [Be(OH 2)4]2+ основный Be. O + H 2 O + 2 OH- = [Be(OH)4]2— кислотный 9
• Оксид Ве. О отличается высокой энергией кристаллической решетки и высокой энергией Гиббса ( Gof = — 582 к. Дж/моль). Он тугоплавок (Тпл. 2530 о. С), теплопроводен; прокаленный (при 400 °С) при низких температурах химически неактивен. Применяют Ве. О в качестве химически стойкого и огнеупорного материала для изготовления тиглей и специальной керамики, а в атомной энергетике — как замедлитель и отражатель нейтронов. • Ве. О входит в состав некоторых стеклообразующих смесей. • Будучи амфотерным, Ве. О взаимодействует при сплавлении и с основными, и с кислотными оксидами: Be. O + Si. O 2 = Be. Si. O 3 основный Be. O + Na 2 O = Na 2 Be. O 2 кислотный • При нагревании Ве. О взаимодействует с кислотами и щелочами: Ве. О + 2 ОН 3+ + Н 2 О = [Be(OH 2)4]2+ основный Be. O + H 2 O + 2 OH- = [Be(OH)4]2— кислотный 9
 • Гидроксид Ве(ОН)2 имеет полимерное соединение, в воде не растворяется. Получение гидроксида бериллия и его отношение к кислотам и щелочам можно выразить следующей суммарной схемой: • Как показывает схема, в кислых средах (избыток ионов гидроксония ОН 3+) устойчивы аквокомплексы бериллия (II), в щелочных (избыток ионов ОН-) — гидроксобериллат (II)-комплексы. При кристаллизации соединений из кислых водных растворов аквокомплексы переходят в состав кристаллогидратов с четырьмя молекулами воды: Ве. SО 4 4 Н 2 О, Ве. Сl 2 4 Н 2 О, 10 Ве(NО 3)2 4 Н 2 О и др.
• Гидроксид Ве(ОН)2 имеет полимерное соединение, в воде не растворяется. Получение гидроксида бериллия и его отношение к кислотам и щелочам можно выразить следующей суммарной схемой: • Как показывает схема, в кислых средах (избыток ионов гидроксония ОН 3+) устойчивы аквокомплексы бериллия (II), в щелочных (избыток ионов ОН-) — гидроксобериллат (II)-комплексы. При кристаллизации соединений из кислых водных растворов аквокомплексы переходят в состав кристаллогидратов с четырьмя молекулами воды: Ве. SО 4 4 Н 2 О, Ве. Сl 2 4 Н 2 О, 10 Ве(NО 3)2 4 Н 2 О и др.
 • Вследствие относительно высокого поляризующего действия иона Ве 2+ его соли подвергаются заметному гидролизу: • В зависимости от концентрации раствора и типа присутствующих в растворе анионов механизм гидролиза может оказаться существенно различным. В частности, образующиеся при гидролизе гидроксоаквокомплексы [Ве(ОН)(ОН 2)3]+ затем полимеризуются в многоядерные комплексы, например [Ве 3(ОН)3(ОН 2)6]3+ вероятно, следующего строения: 11
• Вследствие относительно высокого поляризующего действия иона Ве 2+ его соли подвергаются заметному гидролизу: • В зависимости от концентрации раствора и типа присутствующих в растворе анионов механизм гидролиза может оказаться существенно различным. В частности, образующиеся при гидролизе гидроксоаквокомплексы [Ве(ОН)(ОН 2)3]+ затем полимеризуются в многоядерные комплексы, например [Ве 3(ОН)3(ОН 2)6]3+ вероятно, следующего строения: 11
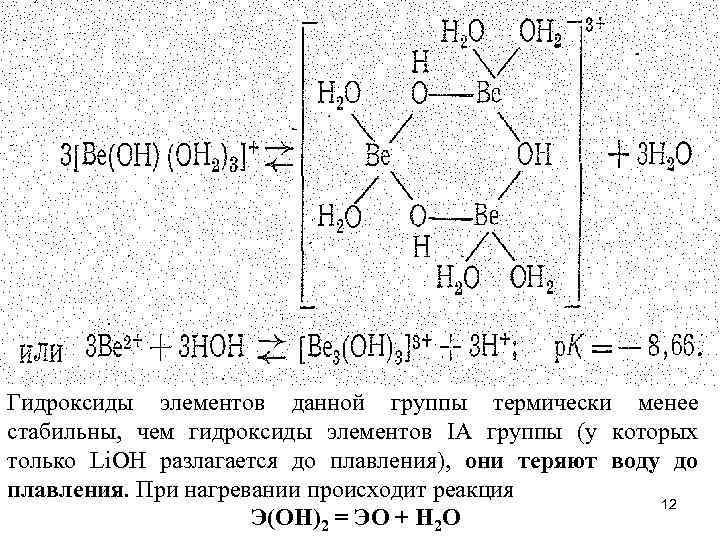 Гидроксиды элементов данной группы термически менее стабильны, чем гидроксиды элементов IA группы (у которых только Li. OH разлагается до плавления), они теряют воду до плавления. При нагревании происходит реакция 12 Э(ОН)2 = ЭО + Н 2 О
Гидроксиды элементов данной группы термически менее стабильны, чем гидроксиды элементов IA группы (у которых только Li. OH разлагается до плавления), они теряют воду до плавления. При нагревании происходит реакция 12 Э(ОН)2 = ЭО + Н 2 О
 • При связывании ионов ОН 3+ (например, анионами СО 32 -, SН-) полимеризация может идти вплоть до образования полимерного гидроксида: Be. S + 2 H 2 O = Be(OH)2 + H 2 S • Гидроксобериллаты в водных растворах существуют лишь при большом избытке щелочи, в противном случае они полностью гидролизуются. Растворимы только бериллаты sэлементов I группы. • Основные свойства гидроксидов увеличиваются от Be(OH)2 к Ba(OH)2. Если Be(OH)2 и Mg(OH)2 слабые основания, 13 Ba(OH)2 – щелочь.
• При связывании ионов ОН 3+ (например, анионами СО 32 -, SН-) полимеризация может идти вплоть до образования полимерного гидроксида: Be. S + 2 H 2 O = Be(OH)2 + H 2 S • Гидроксобериллаты в водных растворах существуют лишь при большом избытке щелочи, в противном случае они полностью гидролизуются. Растворимы только бериллаты sэлементов I группы. • Основные свойства гидроксидов увеличиваются от Be(OH)2 к Ba(OH)2. Если Be(OH)2 и Mg(OH)2 слабые основания, 13 Ba(OH)2 – щелочь.
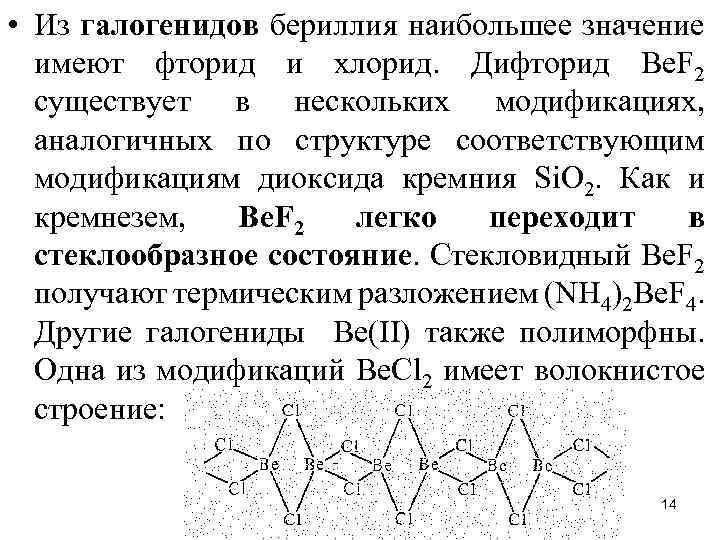 • Из галогенидов бериллия наибольшее значение имеют фторид и хлорид. Дифторид Ве. F 2 существует в нескольких модификациях, аналогичных по структуре соответствующим модификациям диоксида кремния Si. О 2. Как и кремнезем, Ве. F 2 легко переходит в стеклообразное состояние. Стекловидный Ве. F 2 получают термическим разложением (NН 4)2 Ве. F 4. Другие галогениды Ве(II) также полиморфны. Одна из модификаций Ве. Сl 2 имеет волокнистое строение: 14
• Из галогенидов бериллия наибольшее значение имеют фторид и хлорид. Дифторид Ве. F 2 существует в нескольких модификациях, аналогичных по структуре соответствующим модификациям диоксида кремния Si. О 2. Как и кремнезем, Ве. F 2 легко переходит в стеклообразное состояние. Стекловидный Ве. F 2 получают термическим разложением (NН 4)2 Ве. F 4. Другие галогениды Ве(II) также полиморфны. Одна из модификаций Ве. Сl 2 имеет волокнистое строение: 14
 • Амфотерность Ве. Наl 2 наиболее отчетливо проявляется у фторида. Так, при нагревании Bе. F 2 с основными фторидами образуются фторобериллаты, например: 2 КF + Ве. F 2 = К 2[Ве. F 4] • При взаимодействии Bе. F 2 с кислотными фторидами образуются соли бериллия: Ве. F 2 + Si. F 4 = Ве[Si. F 6] 15
• Амфотерность Ве. Наl 2 наиболее отчетливо проявляется у фторида. Так, при нагревании Bе. F 2 с основными фторидами образуются фторобериллаты, например: 2 КF + Ве. F 2 = К 2[Ве. F 4] • При взаимодействии Bе. F 2 с кислотными фторидами образуются соли бериллия: Ве. F 2 + Si. F 4 = Ве[Si. F 6] 15
 • Структурное сходство между Bе. F 2 и Si. O 2 распространяется и на их производные. Полимерные фторобериллаты по структуре аналогичны оксосиликатам, например Nа. Ве. F 3 имеет одинаковое строение с Са. Si. О 3; Nа 2 Ве. F 4 с Са 2 Si. O 4, Nа. Li. Ве. F 4 с Са. Мg. Si. O 4, Li 2 Bе. F 4 с Zn 2 Si. O 4 и т. д. • Полимерные фторобериллаты могут находиться в стеклообразном состоянии. • Другие галогенобериллаты не характерны. 16
• Структурное сходство между Bе. F 2 и Si. O 2 распространяется и на их производные. Полимерные фторобериллаты по структуре аналогичны оксосиликатам, например Nа. Ве. F 3 имеет одинаковое строение с Са. Si. О 3; Nа 2 Ве. F 4 с Са 2 Si. O 4, Nа. Li. Ве. F 4 с Са. Мg. Si. O 4, Li 2 Bе. F 4 с Zn 2 Si. O 4 и т. д. • Полимерные фторобериллаты могут находиться в стеклообразном состоянии. • Другие галогенобериллаты не характерны. 16
 • Присущая бериллию, как амфотерному элементу, склонность образовывать катионные и анионные комплексы проявляется и при расплавлении его соединений. Так, расплавленный Ве. Сl 2 состоит из ионов Ве. Сl+ и Ве. Сl 3 - : Ве. Сl 2 + Ве. Сl 2 Ве. Сl+ + Ве. Сl 3 основный кислотный • Так же ведут себя при расплавлении соединения и других амфотерных элементов, например: 2 Аl. Сl 3 Аl. Сl 2+ + Аl. Сl 42 Та. Сl 5 Та. Сl 4+ +Та. Сl 6 - 17
• Присущая бериллию, как амфотерному элементу, склонность образовывать катионные и анионные комплексы проявляется и при расплавлении его соединений. Так, расплавленный Ве. Сl 2 состоит из ионов Ве. Сl+ и Ве. Сl 3 - : Ве. Сl 2 + Ве. Сl 2 Ве. Сl+ + Ве. Сl 3 основный кислотный • Так же ведут себя при расплавлении соединения и других амфотерных элементов, например: 2 Аl. Сl 3 Аl. Сl 2+ + Аl. Сl 42 Та. Сl 5 Та. Сl 4+ +Та. Сl 6 - 17
 • Нитрид Ве 3 N 2 кристаллическое вещество, получается при нагревании бериллия в атмосфере азота (выше 1000 °С). Бесцветен, очень тверд, тугоплавок (Tпл. 2200 °С). Разлагается водой при нагревании: Ве 3 N 2 + 6 Н 2 O = 3 Ве(ОН)2 + 2 Н 3 N • Гидрид Ве. Н 2 — твердое полимерное вещество, по свойствам подобное Al. H 3. При его разложении водой выделяется водород. Сильный восстановитель. Гидрид бериллия ( Gof = 115, 7 к. Дж/моль) из простых веществ не образуется. Его можно получить взаимодействием Ве. Сl 2 с Li. Н в эфирном растворе: Ве. Сl 2 + 2 Li. Н = Ве. Н 2 + 2 Li. Сl 18
• Нитрид Ве 3 N 2 кристаллическое вещество, получается при нагревании бериллия в атмосфере азота (выше 1000 °С). Бесцветен, очень тверд, тугоплавок (Tпл. 2200 °С). Разлагается водой при нагревании: Ве 3 N 2 + 6 Н 2 O = 3 Ве(ОН)2 + 2 Н 3 N • Гидрид Ве. Н 2 — твердое полимерное вещество, по свойствам подобное Al. H 3. При его разложении водой выделяется водород. Сильный восстановитель. Гидрид бериллия ( Gof = 115, 7 к. Дж/моль) из простых веществ не образуется. Его можно получить взаимодействием Ве. Сl 2 с Li. Н в эфирном растворе: Ве. Сl 2 + 2 Li. Н = Ве. Н 2 + 2 Li. Сl 18
 • Соли бериллия и кислородсодержащих кислот выделяются из растворов обычно в виде кристаллогидратов, которые по структуре и свойствам, естественно, существенно отличаются от безводных производных. Большинство солей бериллия растворимо в воде, нерастворимы Ве. СО 3, Ве(РО 4)2 и некоторые другие. Для бериллия весьма характерны двойные соли — бериллаты со сложными лигандами, например: Nа 2 SО 4 + Ве. SО 4 = Nа 2[Ве(SО 4)2] (NН 4)2 СO 3 + Ве. СО 3 = (NН 4)2[Ве(СО 3)2] • За счет последней реакции нерастворимый в воде Bе. СО 3 растворяется в насыщенных растворах карбонатов sэлементов I группы или аммония. • В разбавленных растворах эти бериллаты разлагаются. 19
• Соли бериллия и кислородсодержащих кислот выделяются из растворов обычно в виде кристаллогидратов, которые по структуре и свойствам, естественно, существенно отличаются от безводных производных. Большинство солей бериллия растворимо в воде, нерастворимы Ве. СО 3, Ве(РО 4)2 и некоторые другие. Для бериллия весьма характерны двойные соли — бериллаты со сложными лигандами, например: Nа 2 SО 4 + Ве. SО 4 = Nа 2[Ве(SО 4)2] (NН 4)2 СO 3 + Ве. СО 3 = (NН 4)2[Ве(СО 3)2] • За счет последней реакции нерастворимый в воде Bе. СО 3 растворяется в насыщенных растворах карбонатов sэлементов I группы или аммония. • В разбавленных растворах эти бериллаты разлагаются. 19
 • Магний заметно отличается от бериллия размерами атома и иона (радиусы ионов Ве 2+ и Mg 2+ соответственно равны 0, 034 и 0, 078 нм, [Li+ – 0, 068]). От своего соседа по периоду — алюминия (0, 057 нм) — магний отличается меньшим числом валентных электронов и относительно большим размером атома. У магния металлические признаки проявляются сильнее, чем у бериллия и алюминия. В частности, для магния менее характерно образование ковалентной связи, чем для бериллия и алюминия, и более характерно образование ионной связи. В этом отношении он ближе к типичным металлическим элементам — элементам подгруппы кальция. 20
• Магний заметно отличается от бериллия размерами атома и иона (радиусы ионов Ве 2+ и Mg 2+ соответственно равны 0, 034 и 0, 078 нм, [Li+ – 0, 068]). От своего соседа по периоду — алюминия (0, 057 нм) — магний отличается меньшим числом валентных электронов и относительно большим размером атома. У магния металлические признаки проявляются сильнее, чем у бериллия и алюминия. В частности, для магния менее характерно образование ковалентной связи, чем для бериллия и алюминия, и более характерно образование ионной связи. В этом отношении он ближе к типичным металлическим элементам — элементам подгруппы кальция. 20
 • Магний — один из наиболее распространенных элементов на Земле. В природе находится в виде трех стабильных изотопов: 24 Mg (78, 6%), 25 Mg 26 Mg (10, 11%) и (11, 29%). Получены искусственные изотопы. Магний входит в состав силикатных минералов (среди них преобладает оливин Мg 2 SО 4, карбонатных минералов — доломита Са. Mg(CO 3)2, магнезита Mg. СО 3. Важное техническое значение имеет минерал карналлит КСl Мg. Сl 2 6 H 2 О, правильнее K[Mg(H 2 O)6]Cl 3. Большое количество магния содержится в морской воде (до 0, 38% Мg. Сl 2) и в воде некоторых озер (до 30% Мg. Сl 2). 21
• Магний — один из наиболее распространенных элементов на Земле. В природе находится в виде трех стабильных изотопов: 24 Mg (78, 6%), 25 Mg 26 Mg (10, 11%) и (11, 29%). Получены искусственные изотопы. Магний входит в состав силикатных минералов (среди них преобладает оливин Мg 2 SО 4, карбонатных минералов — доломита Са. Mg(CO 3)2, магнезита Mg. СО 3. Важное техническое значение имеет минерал карналлит КСl Мg. Сl 2 6 H 2 О, правильнее K[Mg(H 2 O)6]Cl 3. Большое количество магния содержится в морской воде (до 0, 38% Мg. Сl 2) и в воде некоторых озер (до 30% Мg. Сl 2). 21
 • Простое вещество. Магний в виде простого вещества — белый металл (пл. 1, 74 г/см 3, Тпл. 651 °С, Ткип. 1107 °С), на воздухе постепенно окисляется и приобретает матовый оттенок. • Магний мягче и пластичнее бериллия. • Магний активный металл. Легко взаимодействует с галогенами; при нагревании сгорает на воздухе, окисляется серой и азотом. Магний сильный восстановитель. При нагревании восстанавливает даже оксид углерода (IV) 2 Mg + СO 2 = 2 Mg. O + C 22
• Простое вещество. Магний в виде простого вещества — белый металл (пл. 1, 74 г/см 3, Тпл. 651 °С, Ткип. 1107 °С), на воздухе постепенно окисляется и приобретает матовый оттенок. • Магний мягче и пластичнее бериллия. • Магний активный металл. Легко взаимодействует с галогенами; при нагревании сгорает на воздухе, окисляется серой и азотом. Магний сильный восстановитель. При нагревании восстанавливает даже оксид углерода (IV) 2 Mg + СO 2 = 2 Mg. O + C 22
 С соответствующими металлами образует эвтектические смеси, твердые растворы и интерметаллические соединения, которые входят в состав его сплавов. Наиболее важный сплав магния — электрон (3— 10% Аl, 0, 2— 3% Zn, остальное Мg), который благодаря его прочности и малой плотности (1, 8 г/см 3) применяют в ракетной технике и авиастроении. 23
С соответствующими металлами образует эвтектические смеси, твердые растворы и интерметаллические соединения, которые входят в состав его сплавов. Наиболее важный сплав магния — электрон (3— 10% Аl, 0, 2— 3% Zn, остальное Мg), который благодаря его прочности и малой плотности (1, 8 г/см 3) применяют в ракетной технике и авиастроении. 23
 • В ряду напряжений магний расположен перед водородом (Еo 298 = — 2, 36 В). С холодной водой взаимодействует очень медленно, так как образующийся при этом Мg(ОН)2 плохо растворим; при нагревании реакция ускоряется за счет растворения Мg(ОН)2; в кислотах растворяется очень энергично, за исключением кислот (НF, Н 3 РO 4), образующих с ним малорастворимые соединения. Со щелочами магний практически не взаимодействует. • Основную массу производимого магния получают электролизом расплавленного карналлита (КСl Мg. Сl 2) или дихлорида магния, в который для понижения температуры плавления (до 720— 750 °С) добавляют Nа. Сl или другие хлориды. 24
• В ряду напряжений магний расположен перед водородом (Еo 298 = — 2, 36 В). С холодной водой взаимодействует очень медленно, так как образующийся при этом Мg(ОН)2 плохо растворим; при нагревании реакция ускоряется за счет растворения Мg(ОН)2; в кислотах растворяется очень энергично, за исключением кислот (НF, Н 3 РO 4), образующих с ним малорастворимые соединения. Со щелочами магний практически не взаимодействует. • Основную массу производимого магния получают электролизом расплавленного карналлита (КСl Мg. Сl 2) или дихлорида магния, в который для понижения температуры плавления (до 720— 750 °С) добавляют Nа. Сl или другие хлориды. 24
 • Магний получают также металлотермическим и углетермическим методами. При металлотермическом методе восстанавливают в электропечах (при 1200— 1300 °С) в вакууме прокаленный доломит Са. О Мg. О ферросилицием или алюмосилицием: 2(Са. О Мg. О) + Si = Са 2 Si. O 4 + 2 Мg • При углетермическом методе магний получают восстановлением Мg углем в электропечах (при 2100 °С). Для получения чистого магния (99, 999%) технический магний многократно сублимируют в вакууме. С+ Mg. O = CO + Mg Тпл. Zn = 420 о. С, Сd = 321 о. С; Mg = 649 о. С, Са = 839 о. С. 25
• Магний получают также металлотермическим и углетермическим методами. При металлотермическом методе восстанавливают в электропечах (при 1200— 1300 °С) в вакууме прокаленный доломит Са. О Мg. О ферросилицием или алюмосилицием: 2(Са. О Мg. О) + Si = Са 2 Si. O 4 + 2 Мg • При углетермическом методе магний получают восстановлением Мg углем в электропечах (при 2100 °С). Для получения чистого магния (99, 999%) технический магний многократно сублимируют в вакууме. С+ Mg. O = CO + Mg Тпл. Zn = 420 о. С, Сd = 321 о. С; Mg = 649 о. С, Са = 839 о. С. 25
 • Соединения магния (II). Во всех устойчивых соединениях степень окисления магния +2, а координационное число 6. Степень окисления +2 часто проявляется также и в интерметаллических соединениях например Mg 3 Аl 2, Мg 3 Sb 2, Мg 2 Рb. Бинарные соединения Мg (ОЭО 1, 23) в зависимости от природы более электроотрицательного элемента могут быть соединениями от преимущественно металлических до преимущественно ионных. Так, в ряду соединений магния с р-элементами 3 -го периода • происходит постепенное уменьшение металлической и увеличение доли ионной связи. доли 26
• Соединения магния (II). Во всех устойчивых соединениях степень окисления магния +2, а координационное число 6. Степень окисления +2 часто проявляется также и в интерметаллических соединениях например Mg 3 Аl 2, Мg 3 Sb 2, Мg 2 Рb. Бинарные соединения Мg (ОЭО 1, 23) в зависимости от природы более электроотрицательного элемента могут быть соединениями от преимущественно металлических до преимущественно ионных. Так, в ряду соединений магния с р-элементами 3 -го периода • происходит постепенное уменьшение металлической и увеличение доли ионной связи. доли 26
 • По химической природе соединения магния (II) — преимущественно основные. Бромиды и иодиды проявляют восстановительные свойства: ЭI 2 + Cl 2 = ЭCl 2 + I 2 Галогениды Be и Mg сильно гидролизуются. При нагревании образуются оксосоли: ЭГ 2 (р) + Н 2 О = Э(ОН)Г + НГ • Большинство солей-Мg (II) растворимы в воде. Плохо растворимы соли слабых кислот (Мg 3(РО 4)2, Mg. СО 3, Мg. F 2). В водных растворах ионы Мg 2+ находятся в виде бесцветных гексааквокомплексов [Мg(ОН 2)6]2+, которые входят в состав ряда его кристаллогидратов: Мg. Сl 2 6 Н 2 О, Мg(NО 3)2 6 Н 2 О, Мg(Сl. О 4)2 6 Н 2 O, Мg. Si. F 6 6 Н 2 O и др. 27
• По химической природе соединения магния (II) — преимущественно основные. Бромиды и иодиды проявляют восстановительные свойства: ЭI 2 + Cl 2 = ЭCl 2 + I 2 Галогениды Be и Mg сильно гидролизуются. При нагревании образуются оксосоли: ЭГ 2 (р) + Н 2 О = Э(ОН)Г + НГ • Большинство солей-Мg (II) растворимы в воде. Плохо растворимы соли слабых кислот (Мg 3(РО 4)2, Mg. СО 3, Мg. F 2). В водных растворах ионы Мg 2+ находятся в виде бесцветных гексааквокомплексов [Мg(ОН 2)6]2+, которые входят в состав ряда его кристаллогидратов: Мg. Сl 2 6 Н 2 О, Мg(NО 3)2 6 Н 2 О, Мg(Сl. О 4)2 6 Н 2 O, Мg. Si. F 6 6 Н 2 O и др. 27
 • Оксид Мg. О (жженая магнезия) — тугоплавкое (Tпл. 2800 °С) вещество. В технике его получают термическим разложением карбоната: Mg. CO 3 Mg. O + CO 2 • Мелкокристаллический Мg. О химически активен, является основным соединением. Он взаимодействует с водой, поглощает CO 2, легко растворяется в кислотах. Но, сильно прокаленный Мg. О становится очень твердым, теряет химическую активность. • Жженую магнезию применяют в производстве магния, в качестве наполнителя в производстве резины, для очистки нефтепродуктов, в производстве огнеупоров, строительных материалов и др. 28
• Оксид Мg. О (жженая магнезия) — тугоплавкое (Tпл. 2800 °С) вещество. В технике его получают термическим разложением карбоната: Mg. CO 3 Mg. O + CO 2 • Мелкокристаллический Мg. О химически активен, является основным соединением. Он взаимодействует с водой, поглощает CO 2, легко растворяется в кислотах. Но, сильно прокаленный Мg. О становится очень твердым, теряет химическую активность. • Жженую магнезию применяют в производстве магния, в качестве наполнителя в производстве резины, для очистки нефтепродуктов, в производстве огнеупоров, строительных материалов и др. 28
 • Гидроксид Мg(ОН)2 — кристаллическое вещество со слоистой структурой. В воде растворяется незначительно, является основанием средней силы (К 2 = 2, 5 10 -3). В частности, из насыщенных растворов соединений NH 4+ вытесняет аммиак: 2 NН 4 Сl + Мg(ОН)2 = Мg. Сl 2 + 2 Н 3 N + 2 Н 2 O • В химическом анализе добавлением NН 4 Сl пользуются для предотвращения выпадения осадка Мg(ОН)2, когда это нежелательно. Металлический Mg бурно реагирует с водой при добавлении NН 4 Сl с выделением водорода, т. к. NН 4 Сl растворяет защитную пленку Мg(ОН)2 на поверхности металла. • Кроме оксида, широкое применение находит Мg. Сl 2. Его кристаллы образованы октаэдрическими структурными единицами Мg. Сl 6, объединенными в слой. Дихлорид получают хлорированием Мg. О в присутствии угля: Мg. O + Cl 2 + C = Mg. Cl 2 + CO; 29 или обезвоживанием Мg. Сl 2 6 H 2 О, добываемого из морской воды.
• Гидроксид Мg(ОН)2 — кристаллическое вещество со слоистой структурой. В воде растворяется незначительно, является основанием средней силы (К 2 = 2, 5 10 -3). В частности, из насыщенных растворов соединений NH 4+ вытесняет аммиак: 2 NН 4 Сl + Мg(ОН)2 = Мg. Сl 2 + 2 Н 3 N + 2 Н 2 O • В химическом анализе добавлением NН 4 Сl пользуются для предотвращения выпадения осадка Мg(ОН)2, когда это нежелательно. Металлический Mg бурно реагирует с водой при добавлении NН 4 Сl с выделением водорода, т. к. NН 4 Сl растворяет защитную пленку Мg(ОН)2 на поверхности металла. • Кроме оксида, широкое применение находит Мg. Сl 2. Его кристаллы образованы октаэдрическими структурными единицами Мg. Сl 6, объединенными в слой. Дихлорид получают хлорированием Мg. О в присутствии угля: Мg. O + Cl 2 + C = Mg. Cl 2 + CO; 29 или обезвоживанием Мg. Сl 2 6 H 2 О, добываемого из морской воды.
 • Дихлорид в основном применяется для получения магния и в производстве магнезиального цемента. Последний получают смешиванием предварительно прокаленного Мg. О с 30%-ным водным раствором Мg. Сl 2. Вследствие образования полимерных цепей эта смесь постепенно превращается в белую твердую массу, устойчивую по отношению к кислотам и щелочам. • С водородом Мg непосредственно не взаимодействует, но косвенным путем можно получить гидрид состава Мg. Н 2. По сравнению с преимущественно ковалентными гидридами Ве. Н 2 и Аl. Н 3 в Mg. Н 2 более отчетливо проявляется ионная связь. Гидрид магния — нелетучее твердое вещество, более термически устойчивое, чем гидриды бериллия и алюминия. Водой Мg. Н 2 разлагается. Известны также гидридоборат Мg[ВН 4]2 и гидридоалюминат Мg[Аl. Н 4]2 30 магния. Мg. Н 2 + Н 2 О = Мg(ОН)2 + Н 2
• Дихлорид в основном применяется для получения магния и в производстве магнезиального цемента. Последний получают смешиванием предварительно прокаленного Мg. О с 30%-ным водным раствором Мg. Сl 2. Вследствие образования полимерных цепей эта смесь постепенно превращается в белую твердую массу, устойчивую по отношению к кислотам и щелочам. • С водородом Мg непосредственно не взаимодействует, но косвенным путем можно получить гидрид состава Мg. Н 2. По сравнению с преимущественно ковалентными гидридами Ве. Н 2 и Аl. Н 3 в Mg. Н 2 более отчетливо проявляется ионная связь. Гидрид магния — нелетучее твердое вещество, более термически устойчивое, чем гидриды бериллия и алюминия. Водой Мg. Н 2 разлагается. Известны также гидридоборат Мg[ВН 4]2 и гидридоалюминат Мg[Аl. Н 4]2 30 магния. Мg. Н 2 + Н 2 О = Мg(ОН)2 + Н 2
 Подгруппа кальция • Кальций Са, стронций Sr, барий Ва и радий Rа в отличие от ранее рассмотренных элементов имеют относительно большие атомные радиусы и низкие значения потенциалов ионизации. Поэтому в условиях химического взаимодействия кальций и его аналоги легко теряют валентные электроны и образуют простые ионы Э 2+. Поскольку ионы Э 2+ имеют электронную конфигурацию s 2 p 6 и большие размеры (т. е. слабо поляризуют), комплексные ионы с неорганическими лигандами у элементов подгруппы кальция неустойчивы. • В земной коре кальций находится в виде смеси шести, стронций – четырех, барий — семи стабильных изотопов, из которых наиболее распространены 40 Са (96, 97%), 88 Sr (82, 56%) и 138 Ва (71, 66%). Радий 31 устойчивых изотопов не имеет.
Подгруппа кальция • Кальций Са, стронций Sr, барий Ва и радий Rа в отличие от ранее рассмотренных элементов имеют относительно большие атомные радиусы и низкие значения потенциалов ионизации. Поэтому в условиях химического взаимодействия кальций и его аналоги легко теряют валентные электроны и образуют простые ионы Э 2+. Поскольку ионы Э 2+ имеют электронную конфигурацию s 2 p 6 и большие размеры (т. е. слабо поляризуют), комплексные ионы с неорганическими лигандами у элементов подгруппы кальция неустойчивы. • В земной коре кальций находится в виде смеси шести, стронций – четырех, барий — семи стабильных изотопов, из которых наиболее распространены 40 Са (96, 97%), 88 Sr (82, 56%) и 138 Ва (71, 66%). Радий 31 устойчивых изотопов не имеет.
 • Кальций — один из наиболее распространенных элементов на Земле (2, 0 мол. доли, %). Большая его часть содержится в виде силикатов и алюмосиликатов в изверженных горных породах (граниты, гнейсы и др. ). Из других пород наиболее распространены известняк и мел, состоящие в основном из минерала кальцита Са. СО 3. Значительно реже встречается окристаллизованная форм смеси кальцита и доломита — мрамор. Широко распространены ангидрит Са. SO 4 и гипс Са. SО 4 2 Н 2 O (алебастр 2 Са. SО 4 Н 2 O). Важны для промышленности минералы флюорит Са. F 2, апатит 3 Са 3(РО 4)2 Са. Х 2 (F, Сl, ОН) и др. • В качестве продуктов выветривания минералов соединения кальция содержатся в большинстве природных вод и в основном обусловливают их жесткость. • Важнейшие минералы стронция и бария: стронцианит Sr. СО 3, витерит Ва. СО 3, целестин Sr. SО 4, барит (тяжелый шпат) Ва. SО 4. Радий встречается в урановых рудах. 32
• Кальций — один из наиболее распространенных элементов на Земле (2, 0 мол. доли, %). Большая его часть содержится в виде силикатов и алюмосиликатов в изверженных горных породах (граниты, гнейсы и др. ). Из других пород наиболее распространены известняк и мел, состоящие в основном из минерала кальцита Са. СО 3. Значительно реже встречается окристаллизованная форм смеси кальцита и доломита — мрамор. Широко распространены ангидрит Са. SO 4 и гипс Са. SО 4 2 Н 2 O (алебастр 2 Са. SО 4 Н 2 O). Важны для промышленности минералы флюорит Са. F 2, апатит 3 Са 3(РО 4)2 Са. Х 2 (F, Сl, ОН) и др. • В качестве продуктов выветривания минералов соединения кальция содержатся в большинстве природных вод и в основном обусловливают их жесткость. • Важнейшие минералы стронция и бария: стронцианит Sr. СО 3, витерит Ва. СО 3, целестин Sr. SО 4, барит (тяжелый шпат) Ва. SО 4. Радий встречается в урановых рудах. 32
 • Простые вещества. В виде простых веществ кальций и его аналоги — серебристо-белые металлы. На воздухе, правда, они тотчас покрываются желтоватой пленкой продуктов взаимодействия с составными частями воздуха. • Кальций довольно тверд, стронций и барий мягче. Барий в этом отношении напоминает свинец. 33
• Простые вещества. В виде простых веществ кальций и его аналоги — серебристо-белые металлы. На воздухе, правда, они тотчас покрываются желтоватой пленкой продуктов взаимодействия с составными частями воздуха. • Кальций довольно тверд, стронций и барий мягче. Барий в этом отношении напоминает свинец. 33
 • Кальций, стронций и барий энергично взаимодействуют с активными неметаллами уже при обычных условиях. С менее активными (такими, как азот, водород, углерод, кремний и др. ) щелочноземельные металлы реагируют при более или менее сильном нагревании. Реакции сопровождаются выделением большого количества тепла. Активность взаимодействия в ряду Са-Sr-Ва возрастает. При нагревании щелочноземельные металлы взаимодействуют с другими металлами, образуя сплавы, в состав которых входят различные интерметаллические соединения. 34
• Кальций, стронций и барий энергично взаимодействуют с активными неметаллами уже при обычных условиях. С менее активными (такими, как азот, водород, углерод, кремний и др. ) щелочноземельные металлы реагируют при более или менее сильном нагревании. Реакции сопровождаются выделением большого количества тепла. Активность взаимодействия в ряду Са-Sr-Ва возрастает. При нагревании щелочноземельные металлы взаимодействуют с другими металлами, образуя сплавы, в состав которых входят различные интерметаллические соединения. 34
 • В ряду напряжений кальций и его аналоги располагаются далеко впереди водорода. Взаимодействие с водой, даже на холоду, сопровождается растворением, поскольку образуются при этом более или менее растворимые гидроксиды. Активность взаимодействия с водой в ряду Са —Sr—Ва заметно возрастает. • Кальций и стронций получают электролизом их расплавленных хлоридов. • Барий высокой чистоты получают алюминотермическим методом из Ва. О. • Вследствие высокой химической активности щелочноземельные металлы хранят под керосином, в запаянных сосудах (кальций обычно в плотно 35 закрывающихся металлических банках).
• В ряду напряжений кальций и его аналоги располагаются далеко впереди водорода. Взаимодействие с водой, даже на холоду, сопровождается растворением, поскольку образуются при этом более или менее растворимые гидроксиды. Активность взаимодействия с водой в ряду Са —Sr—Ва заметно возрастает. • Кальций и стронций получают электролизом их расплавленных хлоридов. • Барий высокой чистоты получают алюминотермическим методом из Ва. О. • Вследствие высокой химической активности щелочноземельные металлы хранят под керосином, в запаянных сосудах (кальций обычно в плотно 35 закрывающихся металлических банках).
 • Соединения кальция (II), стронция (II), бария (II). Неорганические соединения кальция и его аналогов представляют собой кристаллические вещества, в большинстве с высокими температурами плавления. • Оксиды ЭО получают в лаборатории термическим разложением соответствующих карбонатов или нитратов: Са. СО 3 Са. О + СО 2 2 Ва(NO 3)2 = 2 Ва. О + 4 NO 2 + O 2 в технике — термическим разложением природных карбонатов. Оксиды энергично взаимодействуют с водой, образуя более или менее растворимые основания Э(ОН)2 и выделяя большое количество тепла. Энтальпия гидратации Нгидр в ряду Са. О—Sr. О— Ва. О возрастает. Са. О + Н 2 О = Са(ОН)2 36
• Соединения кальция (II), стронция (II), бария (II). Неорганические соединения кальция и его аналогов представляют собой кристаллические вещества, в большинстве с высокими температурами плавления. • Оксиды ЭО получают в лаборатории термическим разложением соответствующих карбонатов или нитратов: Са. СО 3 Са. О + СО 2 2 Ва(NO 3)2 = 2 Ва. О + 4 NO 2 + O 2 в технике — термическим разложением природных карбонатов. Оксиды энергично взаимодействуют с водой, образуя более или менее растворимые основания Э(ОН)2 и выделяя большое количество тепла. Энтальпия гидратации Нгидр в ряду Са. О—Sr. О— Ва. О возрастает. Са. О + Н 2 О = Са(ОН)2 36
 • Гидроксиды Э(ОН)2 — сильные основания, по силе уступающие лишь гидроксидам s-элементов I группы. В ряду Са(ОН)2—Sr(ОН)2—Ва(ОН)2 усиливается основный характер гидроксидов. В этом же направлении усиливаются растворимость и термическая устойчивость. • Раствор Ва(ОН)2 (баритовая вода) — лабораторный реактив для открытия СО 2. • Са(ОН)2 (известковое молоко, гашеная известь) применяется в качестве дешевого растворимого основания. 37
• Гидроксиды Э(ОН)2 — сильные основания, по силе уступающие лишь гидроксидам s-элементов I группы. В ряду Са(ОН)2—Sr(ОН)2—Ва(ОН)2 усиливается основный характер гидроксидов. В этом же направлении усиливаются растворимость и термическая устойчивость. • Раствор Ва(ОН)2 (баритовая вода) — лабораторный реактив для открытия СО 2. • Са(ОН)2 (известковое молоко, гашеная известь) применяется в качестве дешевого растворимого основания. 37
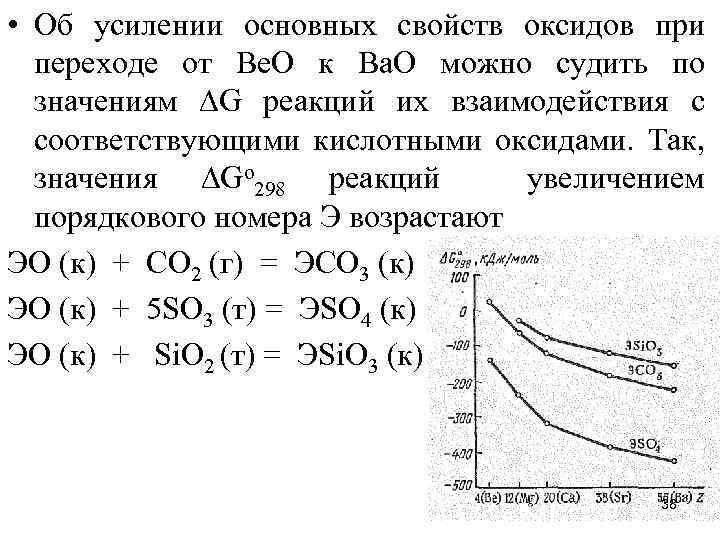 • Об усилении основных свойств оксидов при переходе от Ве. О к Ва. О можно судить по значениям G реакций их взаимодействия с соответствующими кислотными оксидами. Так, значения Go 298 реакций увеличением порядкового номера Э возрастают ЭО (к) + СО 2 (г) = ЭСО 3 (к) ЭО (к) + 5 SО 3 (т) = ЭSO 4 (к) ЭО (к) + Si. O 2 (т) = ЭSi. O 3 (к) 38
• Об усилении основных свойств оксидов при переходе от Ве. О к Ва. О можно судить по значениям G реакций их взаимодействия с соответствующими кислотными оксидами. Так, значения Go 298 реакций увеличением порядкового номера Э возрастают ЭО (к) + СО 2 (г) = ЭСО 3 (к) ЭО (к) + 5 SО 3 (т) = ЭSO 4 (к) ЭО (к) + Si. O 2 (т) = ЭSi. O 3 (к) 38
 • Аналогично можно показать усиление основных свойств в ряду Са(ОН)2—Sr(ОН)2—Ва(ОН)2 по значениям Go 298 образования ЭСО 3 в реакции Э(ОH)2 (к) + СО 2 (г)=ЭСО 3 (к) + Н 2 O (ж), Об усилении основных свойств однотипных соединений в ряду Са (II)— Sr (II) — Ва (II) свидетельствует также увеличение устойчивости солей с одинаковым сложным анионом. По мере усиления основных признаков в ряду Са. F 2 — Sr. F 2 — Ва. F 2 устойчивость в ряду Са. Ве. F 4 — Sr. Be. F 4 — Ва. Ве. F 4 заметно возрастает: фторобериллат бария плавится без разложения (при 1080 o. С), а фторобериллат кальция при нагревании (до 890 o. С) разлагается на Са. F 2 и Ве. F 2. 39
• Аналогично можно показать усиление основных свойств в ряду Са(ОН)2—Sr(ОН)2—Ва(ОН)2 по значениям Go 298 образования ЭСО 3 в реакции Э(ОH)2 (к) + СО 2 (г)=ЭСО 3 (к) + Н 2 O (ж), Об усилении основных свойств однотипных соединений в ряду Са (II)— Sr (II) — Ва (II) свидетельствует также увеличение устойчивости солей с одинаковым сложным анионом. По мере усиления основных признаков в ряду Са. F 2 — Sr. F 2 — Ва. F 2 устойчивость в ряду Са. Ве. F 4 — Sr. Be. F 4 — Ва. Ве. F 4 заметно возрастает: фторобериллат бария плавится без разложения (при 1080 o. С), а фторобериллат кальция при нагревании (до 890 o. С) разлагается на Са. F 2 и Ве. F 2. 39
 • Соли и солеподобные соединения кальция и его аналогов гидролизу либо не подвергаются (ЭНаl 2, Э(NО 3)2, ЭSi. F 6 и др. ), либо дают щелочную среду: ЭН 2 + 2 Н 2 O = Э(ОН)2 + 2 Н 2 ; Э 3 N 2 + 6 Н 2 O = 3 Э(ОН)2 + 2 Н 3 N. • В качестве производных катионных комплексов Са (II) и его аналогов можно рассматривать их некоторые кристаллогидраты. Например: Са. Сl 2 6 Н 2 O, ([Са(ОН 2)6]Сl 2). Склонностью к образованию кристаллогидратов объясняется гигроскопичность соединений. • Из-за высокой гигроскопичности Са. Сl 2 применяется в качестве обезвоживающего 40 средства.
• Соли и солеподобные соединения кальция и его аналогов гидролизу либо не подвергаются (ЭНаl 2, Э(NО 3)2, ЭSi. F 6 и др. ), либо дают щелочную среду: ЭН 2 + 2 Н 2 O = Э(ОН)2 + 2 Н 2 ; Э 3 N 2 + 6 Н 2 O = 3 Э(ОН)2 + 2 Н 3 N. • В качестве производных катионных комплексов Са (II) и его аналогов можно рассматривать их некоторые кристаллогидраты. Например: Са. Сl 2 6 Н 2 O, ([Са(ОН 2)6]Сl 2). Склонностью к образованию кристаллогидратов объясняется гигроскопичность соединений. • Из-за высокой гигроскопичности Са. Сl 2 применяется в качестве обезвоживающего 40 средства.
 • Безводные хлориды, бромиды и иодиды склонны также к присоединению H 3 N с образованием аммиакатов состава ЭНаl 2 8 Н 3 N - ( [Са(NH 3)8]I 2 ). В ряду Са—Sr—Ва устойчивость аммиакатов несколько падает. • Высокая активность Са и его аналогов проявляется также в их способности. образовывать многочисленные перекисные соединения, например пероксиды ЭO 2, надпероксиды Э(O 2)2, персульфиды ЭSn (n = 2— 5), перкарбиды ЭС 2. В ряду Са(II)—Sr(II)—Ва(II) устойчивость этих соединений возрастает. 41 ЭS + 2 Н 2 О = Э(ОН)2 + Н 2 S
• Безводные хлориды, бромиды и иодиды склонны также к присоединению H 3 N с образованием аммиакатов состава ЭНаl 2 8 Н 3 N - ( [Са(NH 3)8]I 2 ). В ряду Са—Sr—Ва устойчивость аммиакатов несколько падает. • Высокая активность Са и его аналогов проявляется также в их способности. образовывать многочисленные перекисные соединения, например пероксиды ЭO 2, надпероксиды Э(O 2)2, персульфиды ЭSn (n = 2— 5), перкарбиды ЭС 2. В ряду Са(II)—Sr(II)—Ва(II) устойчивость этих соединений возрастает. 41 ЭS + 2 Н 2 О = Э(ОН)2 + Н 2 S
 Ca. O + 3 C = Ca. C 2 +CO; Ca. C 2 + H 2 O = Ca(OH)2+ C 2 H 2; Be 2 C + 4 H 2 O = 2 Be(OH)2 + CH 4, Mg 2 C 3 + 2 H 2 O = 2 Mg(OH)2 + CH 3–C CH. • При нагревании Ва. О в присутствии кислорода образуется пероксид бария: Ва. О (кр) + ½ О 2 (г) = Ва. О 2 (кр) При сравнительно невысоких температурах (до 600 о. С) она протекает вправо, при более высоких температурах (~800 о. С) она интенсивно идет влево. • Пероксиды металлов IIA группы получают действуя конц. раствором Н 2 О 2 на гидроксиды. Стабильность ЭО 2 уменьшается от Ва. О 2 к Mg. O 2 (Ве. О 2 неизвестен). • В воде ЭО 2 малорастворимы, подвергаются сильному гидролизу и разлагаются даже Н 2 СО 3, образуя соль металла и Н 2 О 2. Ва. О 2 + Н 2 SO 4 = Ва. SO 4 + Н 2 О 2. 42
Ca. O + 3 C = Ca. C 2 +CO; Ca. C 2 + H 2 O = Ca(OH)2+ C 2 H 2; Be 2 C + 4 H 2 O = 2 Be(OH)2 + CH 4, Mg 2 C 3 + 2 H 2 O = 2 Mg(OH)2 + CH 3–C CH. • При нагревании Ва. О в присутствии кислорода образуется пероксид бария: Ва. О (кр) + ½ О 2 (г) = Ва. О 2 (кр) При сравнительно невысоких температурах (до 600 о. С) она протекает вправо, при более высоких температурах (~800 о. С) она интенсивно идет влево. • Пероксиды металлов IIA группы получают действуя конц. раствором Н 2 О 2 на гидроксиды. Стабильность ЭО 2 уменьшается от Ва. О 2 к Mg. O 2 (Ве. О 2 неизвестен). • В воде ЭО 2 малорастворимы, подвергаются сильному гидролизу и разлагаются даже Н 2 СО 3, образуя соль металла и Н 2 О 2. Ва. О 2 + Н 2 SO 4 = Ва. SO 4 + Н 2 О 2. 42
 • Вяжущие материалы. Природные соединения кальция широко применяются в производстве вяжущих материалов. Последние представляют собой порошкообразные вещества, образующие при смешении с водой пластичную массу, затвердевающую в твердое прочное тело. Вяжущие материалы используются в строительных растворах (для скрепления камней, кирпичей, отдельных элементов сооружений), для изготовления бетона, строительных деталей и конструкций. К вяжущим веществам относятся цементы, гипсовые материалы, известь и др. 43
• Вяжущие материалы. Природные соединения кальция широко применяются в производстве вяжущих материалов. Последние представляют собой порошкообразные вещества, образующие при смешении с водой пластичную массу, затвердевающую в твердое прочное тело. Вяжущие материалы используются в строительных растворах (для скрепления камней, кирпичей, отдельных элементов сооружений), для изготовления бетона, строительных деталей и конструкций. К вяжущим веществам относятся цементы, гипсовые материалы, известь и др. 43
 • По химическому составу цементы представляют собой главным образом силикаты и алюминаты кальция, т. е. в их состав входят Si и Аl – химические элементы, особо склонные к образованию гетероцепных полимеров (в основе которых лежат связи Si—О—Si и Аl—О—Аl, Si —О—Аl ). В зависимости от относительного содержания силикатов и алюминатов различают силикатный цемент (портландцемент) и алюминатный (глиноземистый). 44
• По химическому составу цементы представляют собой главным образом силикаты и алюминаты кальция, т. е. в их состав входят Si и Аl – химические элементы, особо склонные к образованию гетероцепных полимеров (в основе которых лежат связи Si—О—Si и Аl—О—Аl, Si —О—Аl ). В зависимости от относительного содержания силикатов и алюминатов различают силикатный цемент (портландцемент) и алюминатный (глиноземистый). 44
 • Силикатные цементы синтезируют обжигом (при 1400— 1600 °С) до спекания тонкоизмельченной смеси известняка и богатой Si. O 2 глины. При этом частично разрушаются связи Si—О—Si и Аl —О—Аl, образуются относительно простые по структуре силикаты и алюминаты кальция и выделяется СО 2. Тонко измельченный цементный клинкер, будучи замешан с водой в тестообразную массу, постепенно твердеет. Этот переход (схватывание цемента) обусловливается сложными процессами гидратации и поликонденсации составных частей клинкера, приводящими к образованию высокомолекулярных силикатов и алюминатов кальция. 45
• Силикатные цементы синтезируют обжигом (при 1400— 1600 °С) до спекания тонкоизмельченной смеси известняка и богатой Si. O 2 глины. При этом частично разрушаются связи Si—О—Si и Аl —О—Аl, образуются относительно простые по структуре силикаты и алюминаты кальция и выделяется СО 2. Тонко измельченный цементный клинкер, будучи замешан с водой в тестообразную массу, постепенно твердеет. Этот переход (схватывание цемента) обусловливается сложными процессами гидратации и поликонденсации составных частей клинкера, приводящими к образованию высокомолекулярных силикатов и алюминатов кальция. 45
 • Гипсовые материалы — это прежде всего жженый гипс, или алебастр, — гидрат состава 2 Са. SО 4 Н 2 О. Его получают обжигом гипса при 150— 180 °С. При замешивании теста из порошка 2 Са. SО 4 Н 2 O с водой происходит присоединение воды, сопровождающееся отвердеванием всей массы вследствие закристаллизовывания 2[Са. SO 4 0, 5 Н 2 O] + 3 Н 2 O = 2[Са. SO 4 2 Н 2 O] • На этом основано применение гипса при изготовлении строительных перегородочных плит и панелей, слепков с различных предметов, а также в виде известково-гипсовых растворов 46 для штукатурных работ и т. д.
• Гипсовые материалы — это прежде всего жженый гипс, или алебастр, — гидрат состава 2 Са. SО 4 Н 2 О. Его получают обжигом гипса при 150— 180 °С. При замешивании теста из порошка 2 Са. SО 4 Н 2 O с водой происходит присоединение воды, сопровождающееся отвердеванием всей массы вследствие закристаллизовывания 2[Са. SO 4 0, 5 Н 2 O] + 3 Н 2 O = 2[Са. SO 4 2 Н 2 O] • На этом основано применение гипса при изготовлении строительных перегородочных плит и панелей, слепков с различных предметов, а также в виде известково-гипсовых растворов 46 для штукатурных работ и т. д.
 • В качестве вяжущего материала служит также смесь гашеной извести с песком и водой (известковый раствор). Известковый раствор затвердевает за счет перехода Са(ОН)2 при поглощении СО 2 воздуха в кристаллический Са. СО 3: Са(ОН)2 + СО 2 = Са. СО 3 + Н 2 О • Одновременно образуются силикаты кальция (за счет Si. O 2 песка). • Са. СО 3 + СО 2 + Н 2 О = Са(HСО 3)2 • ЭСО 3 (t)= ЭО + СО 2 • ЭСО 3 + С (t) = ЭО + 2 СО 47
• В качестве вяжущего материала служит также смесь гашеной извести с песком и водой (известковый раствор). Известковый раствор затвердевает за счет перехода Са(ОН)2 при поглощении СО 2 воздуха в кристаллический Са. СО 3: Са(ОН)2 + СО 2 = Са. СО 3 + Н 2 О • Одновременно образуются силикаты кальция (за счет Si. O 2 песка). • Са. СО 3 + СО 2 + Н 2 О = Са(HСО 3)2 • ЭСО 3 (t)= ЭО + СО 2 • ЭСО 3 + С (t) = ЭО + 2 СО 47
 • Жесткость воды. Как уже говорилось выше, наличие в природной воде солей кальция и магния обусловливает ее жесткость. Различают временную и постоянную жесткость воды. Временную жесткость придают воде гидрокарбонаты, постоянную — сульфаты и хлориды Са (II) и Мg (II). • Жесткость воды устраняют физическими и химическими методами. Временная жесткость устраняется кипячением воды. При этом гидрокарбонаты переходят в нерастворимые карбонаты: t Са(НСО 3)2 = Са. СО 3 + СО 2 + Н 2 О 48
• Жесткость воды. Как уже говорилось выше, наличие в природной воде солей кальция и магния обусловливает ее жесткость. Различают временную и постоянную жесткость воды. Временную жесткость придают воде гидрокарбонаты, постоянную — сульфаты и хлориды Са (II) и Мg (II). • Жесткость воды устраняют физическими и химическими методами. Временная жесткость устраняется кипячением воды. При этом гидрокарбонаты переходят в нерастворимые карбонаты: t Са(НСО 3)2 = Са. СО 3 + СО 2 + Н 2 О 48
 • Химическое умягчение основано на введении в воду реагентов, обогащающих ее анионами СО 32 - и ОН-, в результате чего образуются малорастворимые Са. СО 3 и Mg(OН)2. Для этого природную воду обрабатывают гашеной известью или содой: Са. SO 4 (р) + Nа 2 СО 3 (р) = Са. СО 3 (т) + Nа 2 SО 4 (р) Са(НСО 3) (р) + Са(ОН)2 (р) = 2 Са. СО 3 (т) +2 Н 2 O(ж) Мg. SО 4 (р) + Са(ОН)2 (р) = Мg(ОН)2 (т) + Са. SO 4(р) • Для удаления ионов Са 2+ и Мg 2+ можно применять также фосфаты натрия, буру, поташ и др. 49
• Химическое умягчение основано на введении в воду реагентов, обогащающих ее анионами СО 32 - и ОН-, в результате чего образуются малорастворимые Са. СО 3 и Mg(OН)2. Для этого природную воду обрабатывают гашеной известью или содой: Са. SO 4 (р) + Nа 2 СО 3 (р) = Са. СО 3 (т) + Nа 2 SО 4 (р) Са(НСО 3) (р) + Са(ОН)2 (р) = 2 Са. СО 3 (т) +2 Н 2 O(ж) Мg. SО 4 (р) + Са(ОН)2 (р) = Мg(ОН)2 (т) + Са. SO 4(р) • Для удаления ионов Са 2+ и Мg 2+ можно применять также фосфаты натрия, буру, поташ и др. 49
 • Широкое распространение в технике получил метод устранения жесткости воды путем ионного обмена. В этом методе используется способность некоторых природных и искусственных высокомолекулярных соединений — ионитов — обменивать входящие в их состав радикалы на ионы, находящиеся в растворе. • По характеру обмениваемых ионов среди ионитов различают катиониты и аниониты. Катионитами являются алюмосиликаты типа цеолитов, например Nа 2[Аl 2 Si 2 О 8] n. Н 2 О, искусственно приготовленные гидратированные алюмосиликаты пермутиты, ряд силикатов и др. Происходящий между алюмосиликатом и жесткой водой обмен нонами можно схематически представить следующими уравнениями реакций: Nа 2 R + Са(НСО 3)2 Са. R + 2 Nа. НСО 3 Nа. R + Са. SO 4 Са. R + Nа 2 SО 4 • где R — сложный алюмосиликатный анион 50 [Аl 2 Si 2 O 8 n. Н 2 О]2 -.
• Широкое распространение в технике получил метод устранения жесткости воды путем ионного обмена. В этом методе используется способность некоторых природных и искусственных высокомолекулярных соединений — ионитов — обменивать входящие в их состав радикалы на ионы, находящиеся в растворе. • По характеру обмениваемых ионов среди ионитов различают катиониты и аниониты. Катионитами являются алюмосиликаты типа цеолитов, например Nа 2[Аl 2 Si 2 О 8] n. Н 2 О, искусственно приготовленные гидратированные алюмосиликаты пермутиты, ряд силикатов и др. Происходящий между алюмосиликатом и жесткой водой обмен нонами можно схематически представить следующими уравнениями реакций: Nа 2 R + Са(НСО 3)2 Са. R + 2 Nа. НСО 3 Nа. R + Са. SO 4 Са. R + Nа 2 SО 4 • где R — сложный алюмосиликатный анион 50 [Аl 2 Si 2 O 8 n. Н 2 О]2 -.
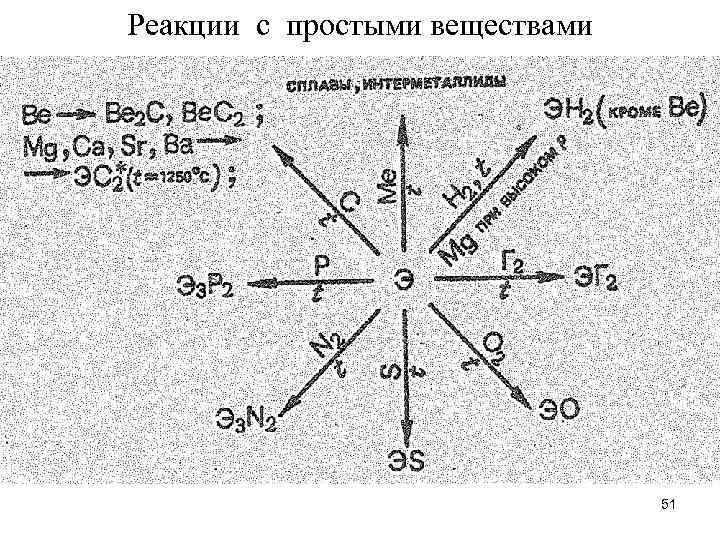 Реакции с простыми веществами 51
Реакции с простыми веществами 51
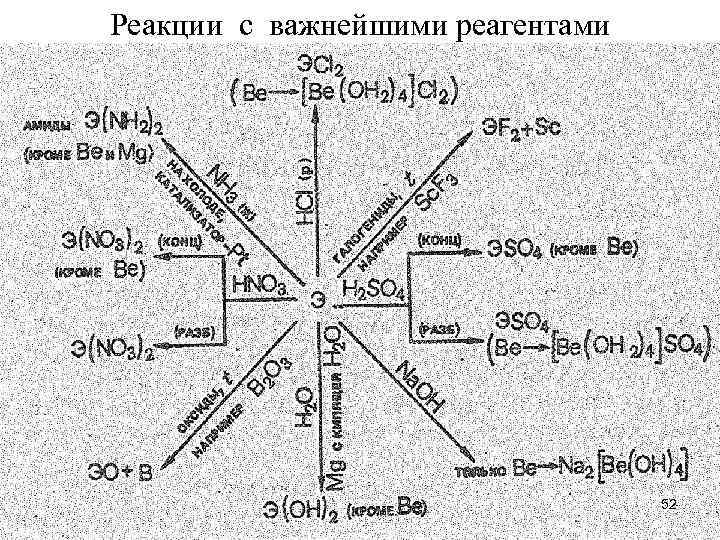 Реакции с важнейшими реагентами 52
Реакции с важнейшими реагентами 52


