03 Фазовые переходы.ppt
- Количество слайдов: 25
 Свойства пластовых флюидов Фазовые равновесия • Гомогенные системы • Гетерогенные системы Ф - число фаз – количество сосуществующих равновесных агрегатных состояний. Может быть только 1 газовая фаза и много жидких и твердых. К - компоненты - соединения, которые определяют состав фаз С – число термодинамической степени свободы – наименьшее число параметров состояния (давление, температура и концентрации веществ в различных фазах), которое полностью описать состояние системы при постоянстве числа фаз. Если К =1, необходимо знать 2 параметра P и T. Если К= 2, надо знать еще 1 концентрацию. Если К больше 2, надо знать К-1 концентраций. Итого необходимое число параметров для определения состояния системы равно Ф(К-1) +2 1
Свойства пластовых флюидов Фазовые равновесия • Гомогенные системы • Гетерогенные системы Ф - число фаз – количество сосуществующих равновесных агрегатных состояний. Может быть только 1 газовая фаза и много жидких и твердых. К - компоненты - соединения, которые определяют состав фаз С – число термодинамической степени свободы – наименьшее число параметров состояния (давление, температура и концентрации веществ в различных фазах), которое полностью описать состояние системы при постоянстве числа фаз. Если К =1, необходимо знать 2 параметра P и T. Если К= 2, надо знать еще 1 концентрацию. Если К больше 2, надо знать К-1 концентраций. Итого необходимое число параметров для определения состояния системы равно Ф(К-1) +2 1
 При равновесии в системе во всех фазах имеем: µ(1)I = µ(1)II = µ (1)III =. . . = µ (1)Ф, µ(2)I = µ (2)III =. . . = µ (2)Ф, . . . µ(K)I = µ (K)III =. . . = µ (K)Ф (внизу номер фазы, а верху номер компонента). Тогда концентрации одного компонента в одной фазе связаны константами равновесия и достаточно знать 1 концентрацию. Значит параметр в количестве К(Ф - 1) становится лишним. Поэтому в многокомпонентной равновесной системе: С = Ф(К - 1) + 2 - К(Ф - 1) =2 + К – Ф Правило фаз Гиббса (закон равновесия фаз). С = 2+К – Ф
При равновесии в системе во всех фазах имеем: µ(1)I = µ(1)II = µ (1)III =. . . = µ (1)Ф, µ(2)I = µ (2)III =. . . = µ (2)Ф, . . . µ(K)I = µ (K)III =. . . = µ (K)Ф (внизу номер фазы, а верху номер компонента). Тогда концентрации одного компонента в одной фазе связаны константами равновесия и достаточно знать 1 концентрацию. Значит параметр в количестве К(Ф - 1) становится лишним. Поэтому в многокомпонентной равновесной системе: С = Ф(К - 1) + 2 - К(Ф - 1) =2 + К – Ф Правило фаз Гиббса (закон равновесия фаз). С = 2+К – Ф
 Системы делят Ø по числу компонентов (одно-, двухкомпонентные и т. д. ), Ø по числу фаз (одно-, двухфазные и т. д. ) и Ø по числу степеней свободы (инвариантные, моно-, дивариантные и т. д. ). Минимальное число степеней свободы 0. Тогда Ф = К + 2, т. е. максимальное количество фаз, которые может находиться в равновесии, равно К+2. В однокомпонентной системе (в чистом веществе) С = 3. В двухкомпонентной системе С = 4 и т. д. 3
Системы делят Ø по числу компонентов (одно-, двухкомпонентные и т. д. ), Ø по числу фаз (одно-, двухфазные и т. д. ) и Ø по числу степеней свободы (инвариантные, моно-, дивариантные и т. д. ). Минимальное число степеней свободы 0. Тогда Ф = К + 2, т. е. максимальное количество фаз, которые может находиться в равновесии, равно К+2. В однокомпонентной системе (в чистом веществе) С = 3. В двухкомпонентной системе С = 4 и т. д. 3
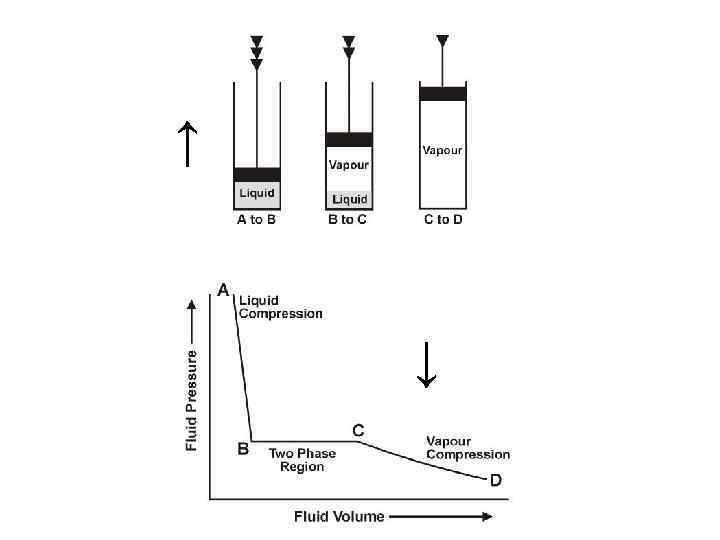
 Фазы могут быть твердыми, жидкими и газообразными. Газовые фазы всегда растворимы друг в друге и могут иметь только 1 фазу. Жидкие фазы в условиях гидролитосферы образуют 2 фазы: • растворы полярных соединений (электорлитов) и • растворы неполярных соединений. Первые хорошо растворяются в H 2 O и образуют широко распространенные водные растворы. Вторые хорошо растворяются только друг в друге и образуют менее растворенные гидрофобные растворы. Твердые фазы (минералы) имеют неограниченное число и в совокупности образуют породу. Поэтому в условиях низких температур встречаются только две естественные жидкие фазы Все эти фазы называют флюидами. Флюиды включают два жидких раствора: подземная вода и нефть – битумы и один газовый. – Газовые растворы - фаза, которая меняет объем и может быть сконденсирована понижением температуры при постоянном давлении. – Жидкий раствор - фаза, которая меняет форму и может быть переведена в пар понижением давления при постоянной температуре.
Фазы могут быть твердыми, жидкими и газообразными. Газовые фазы всегда растворимы друг в друге и могут иметь только 1 фазу. Жидкие фазы в условиях гидролитосферы образуют 2 фазы: • растворы полярных соединений (электорлитов) и • растворы неполярных соединений. Первые хорошо растворяются в H 2 O и образуют широко распространенные водные растворы. Вторые хорошо растворяются только друг в друге и образуют менее растворенные гидрофобные растворы. Твердые фазы (минералы) имеют неограниченное число и в совокупности образуют породу. Поэтому в условиях низких температур встречаются только две естественные жидкие фазы Все эти фазы называют флюидами. Флюиды включают два жидких раствора: подземная вода и нефть – битумы и один газовый. – Газовые растворы - фаза, которая меняет объем и может быть сконденсирована понижением температуры при постоянном давлении. – Жидкий раствор - фаза, которая меняет форму и может быть переведена в пар понижением давления при постоянной температуре.
 ↑ ↓
↑ ↓

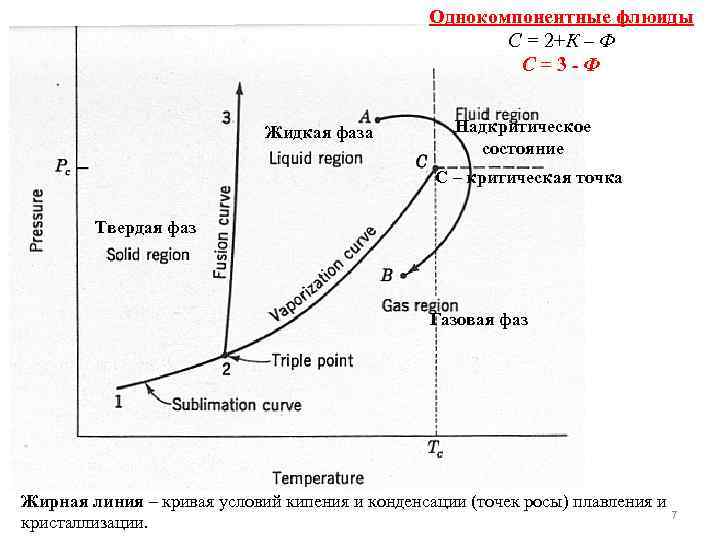 Однокомпонентные флюиды С = 2+К – Ф С=3 -Ф Жидкая фаза Надкритическое состояние C – критическая точка Твердая фаз Газовая фаз Жирная линия – кривая условий кипения и конденсации (точек росы) плавления и 7 кристаллизации.
Однокомпонентные флюиды С = 2+К – Ф С=3 -Ф Жидкая фаза Надкритическое состояние C – критическая точка Твердая фаз Газовая фаз Жирная линия – кривая условий кипения и конденсации (точек росы) плавления и 7 кристаллизации.
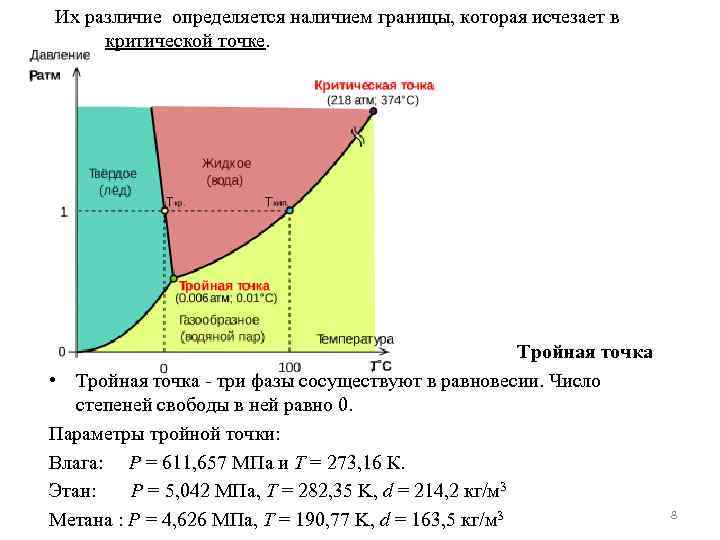 Их различие определяется наличием границы, которая исчезает в критической точке. Тройная точка • Тройная точка - три фазы сосуществуют в равновесии. Число степеней свободы в ней равно 0. Параметры тройной точки: Влага: Р = 611, 657 МПа и Т = 273, 16 К. Этан: P = 5, 042 МПа, T = 282, 35 K, d = 214, 2 кг/м 3 Метана : P = 4, 626 МПа, T = 190, 77 K, d = 163, 5 кг/м 3 8
Их различие определяется наличием границы, которая исчезает в критической точке. Тройная точка • Тройная точка - три фазы сосуществуют в равновесии. Число степеней свободы в ней равно 0. Параметры тройной точки: Влага: Р = 611, 657 МПа и Т = 273, 16 К. Этан: P = 5, 042 МПа, T = 282, 35 K, d = 214, 2 кг/м 3 Метана : P = 4, 626 МПа, T = 190, 77 K, d = 163, 5 кг/м 3 8
 Критическая точка • Критическая точка: максимальное давление и температура, при которых чистое вещество может иметь равновесие между разделенными паром и жидкостью. Выше Pc и Tc различие между паром и жидкостью, а также граница между ними отсутствуют. Влага H 2 O: Tкр=647, 3 К, Pкр =22, 048 МПа. Этан C 2 H 6: Tкр=305, 36 К, Pкр =4, 873 МПа. • К критической точке мениск между фазами постепенно исчезает. • Если двигаться вокруг критической точки, можно перейти от газового состояния в жидкое минуя границу между ними. 9
Критическая точка • Критическая точка: максимальное давление и температура, при которых чистое вещество может иметь равновесие между разделенными паром и жидкостью. Выше Pc и Tc различие между паром и жидкостью, а также граница между ними отсутствуют. Влага H 2 O: Tкр=647, 3 К, Pкр =22, 048 МПа. Этан C 2 H 6: Tкр=305, 36 К, Pкр =4, 873 МПа. • К критической точке мениск между фазами постепенно исчезает. • Если двигаться вокруг критической точки, можно перейти от газового состояния в жидкое минуя границу между ними. 9
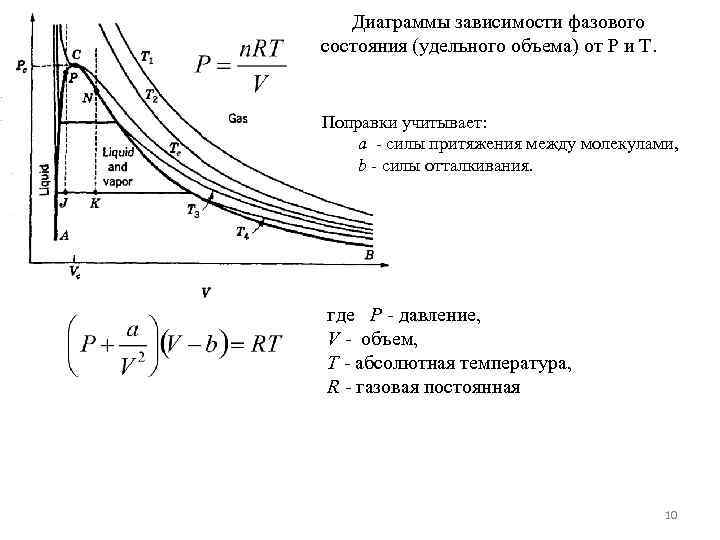 Диаграммы зависимости фазового состояния (удельного объема) от P и T. Поправки учитывает: a - силы притяжения между молекулами, b - силы отталкивания. где P - давление, V - объем, T - абсолютная температура, R - газовая постоянная 10
Диаграммы зависимости фазового состояния (удельного объема) от P и T. Поправки учитывает: a - силы притяжения между молекулами, b - силы отталкивания. где P - давление, V - объем, T - абсолютная температура, R - газовая постоянная 10
 Критический удельный объем в точке С: C 2 H 6 147, 05 см 3/моль, H 2 O 56, 01 см 3/моль 11
Критический удельный объем в точке С: C 2 H 6 147, 05 см 3/моль, H 2 O 56, 01 см 3/моль 11
 Бинарные системы включают два компонента.
Бинарные системы включают два компонента.
 Зависимость критического давления от температуры для двойных смесей метана и нормальных парафиновых углеводородов.
Зависимость критического давления от температуры для двойных смесей метана и нормальных парафиновых углеводородов.
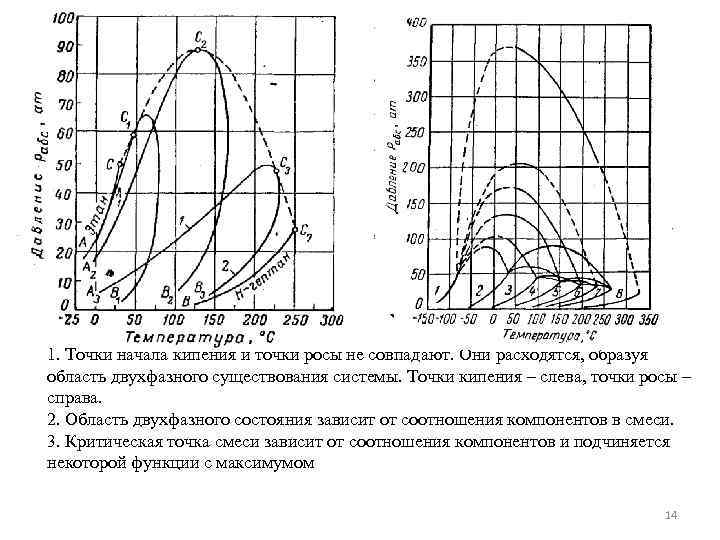 1. Точки начала кипения и точки росы не совпадают. Они расходятся, образуя область двухфазного существования системы. Точки кипения – слева, точки росы – справа. 2. Область двухфазного состояния зависит от соотношения компонентов в смеси. 3. Критическая точка смеси зависит от соотношения компонентов и подчиняется некоторой функции с максимумом 14
1. Точки начала кипения и точки росы не совпадают. Они расходятся, образуя область двухфазного существования системы. Точки кипения – слева, точки росы – справа. 2. Область двухфазного состояния зависит от соотношения компонентов в смеси. 3. Критическая точка смеси зависит от соотношения компонентов и подчиняется некоторой функции с максимумом 14
 15
15
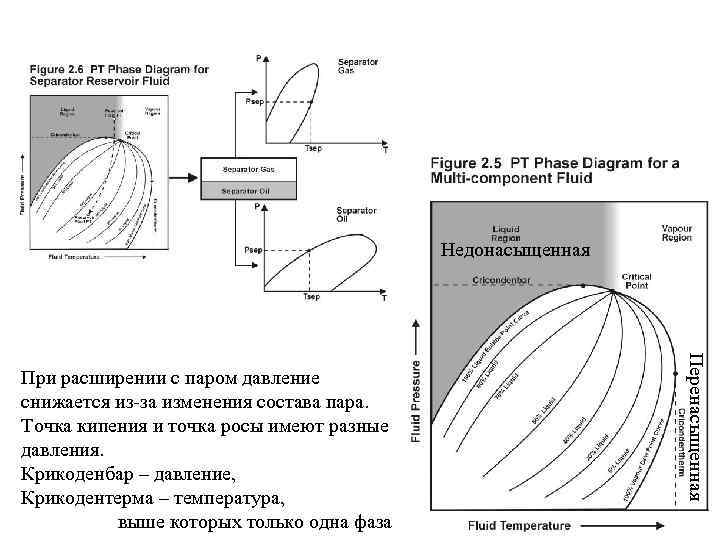 Недонасыщенная Перенасыщенная При расширении с паром давление снижается из-за изменения состава пара. Точка кипения и точка росы имеют разные давления. Крикоденбар – давление, Крикодентерма – температура, выше которых только одна фаза
Недонасыщенная Перенасыщенная При расширении с паром давление снижается из-за изменения состава пара. Точка кипения и точка росы имеют разные давления. Крикоденбар – давление, Крикодентерма – температура, выше которых только одна фаза
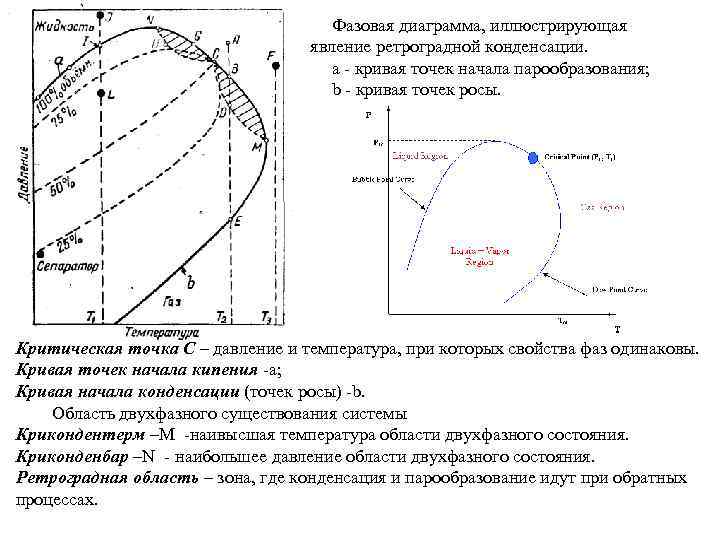 Фазовая диаграмма, иллюстрирующая явление ретроградной конденсации. а - кривая точек начала парообразования; b - кривая точек росы. Критическая точка C – давление и температура, при которых свойства фаз одинаковы. Кривая точек начала кипения -а; Кривая начала конденсации (точек росы) -b. Область двухфазного существования системы Крикондентерм –M -наивысшая температура области двухфазного состояния. Криконденбар –N - наибольшее давление области двухфазного состояния. Ретроградная область – зона, где конденсация и парообразование идут при обратных процессах.
Фазовая диаграмма, иллюстрирующая явление ретроградной конденсации. а - кривая точек начала парообразования; b - кривая точек росы. Критическая точка C – давление и температура, при которых свойства фаз одинаковы. Кривая точек начала кипения -а; Кривая начала конденсации (точек росы) -b. Область двухфазного существования системы Крикондентерм –M -наивысшая температура области двухфазного состояния. Криконденбар –N - наибольшее давление области двухфазного состояния. Ретроградная область – зона, где конденсация и парообразование идут при обратных процессах.
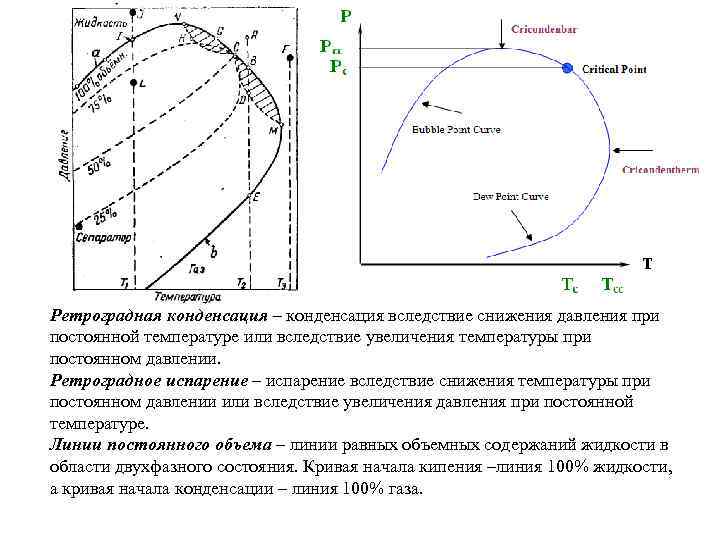 Ретроградная конденсация – конденсация вследствие снижения давления при постоянной температуре или вследствие увеличения температуры при постоянном давлении. Ретроградное испарение – испарение вследствие снижения температуры при постоянном давлении или вследствие увеличения давления при постоянной температуре. Линии постоянного объема – линии равных объемных содержаний жидкости в области двухфазного состояния. Кривая начала кипения –линия 100% жидкости, а кривая начала конденсации – линия 100% газа.
Ретроградная конденсация – конденсация вследствие снижения давления при постоянной температуре или вследствие увеличения температуры при постоянном давлении. Ретроградное испарение – испарение вследствие снижения температуры при постоянном давлении или вследствие увеличения давления при постоянной температуре. Линии постоянного объема – линии равных объемных содержаний жидкости в области двухфазного состояния. Кривая начала кипения –линия 100% жидкости, а кривая начала конденсации – линия 100% газа.
 Все многокомпонентные системы делят на газовые и нефтяные. Газовые делят на сухие, жирные и конденсатные (ретроградные). Сухой газ состоит из метана и незначительного содержания более тяжелых газовых углеводородов. Условия конденсации этих газов далеки от пластовых и нормальных (сепарации) условий. Поэтому конденсат углеводородов не образуется. Сухой газ
Все многокомпонентные системы делят на газовые и нефтяные. Газовые делят на сухие, жирные и конденсатные (ретроградные). Сухой газ состоит из метана и незначительного содержания более тяжелых газовых углеводородов. Условия конденсации этих газов далеки от пластовых и нормальных (сепарации) условий. Поэтому конденсат углеводородов не образуется. Сухой газ
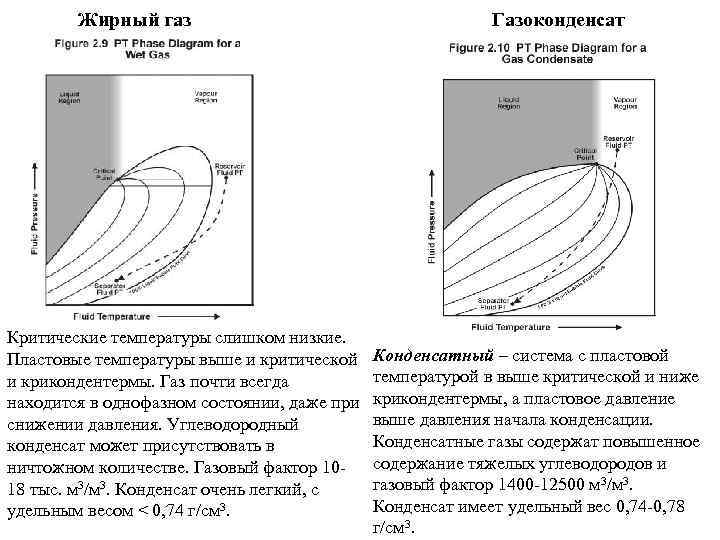 Жирный газ Критические температуры слишком низкие. Пластовые температуры выше и критической и крикондентермы. Газ почти всегда находится в однофазном состоянии, даже при снижении давления. Углеводородный конденсат может присутствовать в ничтожном количестве. Газовый фактор 1018 тыс. м 3/м 3. Конденсат очень легкий, с удельным весом < 0, 74 г/см 3. Газоконденсат Конденсатный – система с пластовой температурой в выше критической и ниже крикондентермы, а пластовое давление выше давления начала конденсации. Конденсатные газы содержат повышенное содержание тяжелых углеводородов и газовый фактор 1400 -12500 м 3/м 3. Конденсат имеет удельный вес 0, 74 -0, 78 г/см 3.
Жирный газ Критические температуры слишком низкие. Пластовые температуры выше и критической и крикондентермы. Газ почти всегда находится в однофазном состоянии, даже при снижении давления. Углеводородный конденсат может присутствовать в ничтожном количестве. Газовый фактор 1018 тыс. м 3/м 3. Конденсат очень легкий, с удельным весом < 0, 74 г/см 3. Газоконденсат Конденсатный – система с пластовой температурой в выше критической и ниже крикондентермы, а пластовое давление выше давления начала конденсации. Конденсатные газы содержат повышенное содержание тяжелых углеводородов и газовый фактор 1400 -12500 м 3/м 3. Конденсат имеет удельный вес 0, 74 -0, 78 г/см 3.
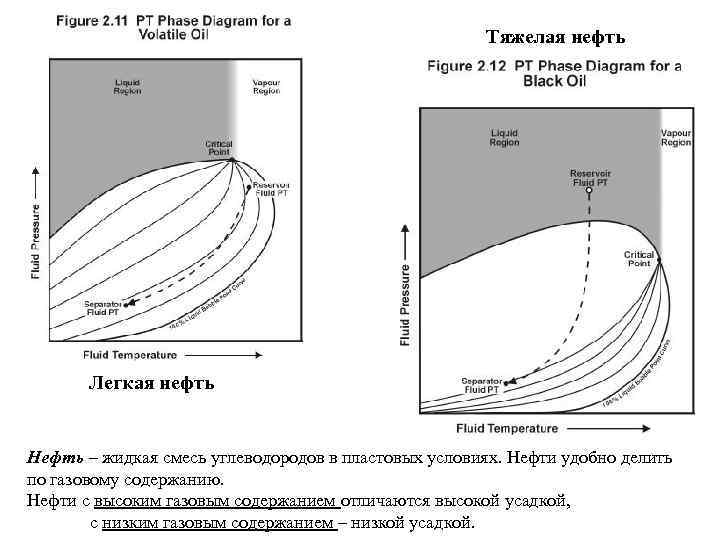 Тяжелая нефть Легкая нефть Нефть – жидкая смесь углеводородов в пластовых условиях. Нефти удобно делить по газовому содержанию. Нефти с высоким газовым содержанием отличаются высокой усадкой, с низким газовым содержанием – низкой усадкой.
Тяжелая нефть Легкая нефть Нефть – жидкая смесь углеводородов в пластовых условиях. Нефти удобно делить по газовому содержанию. Нефти с высоким газовым содержанием отличаются высокой усадкой, с низким газовым содержанием – низкой усадкой.
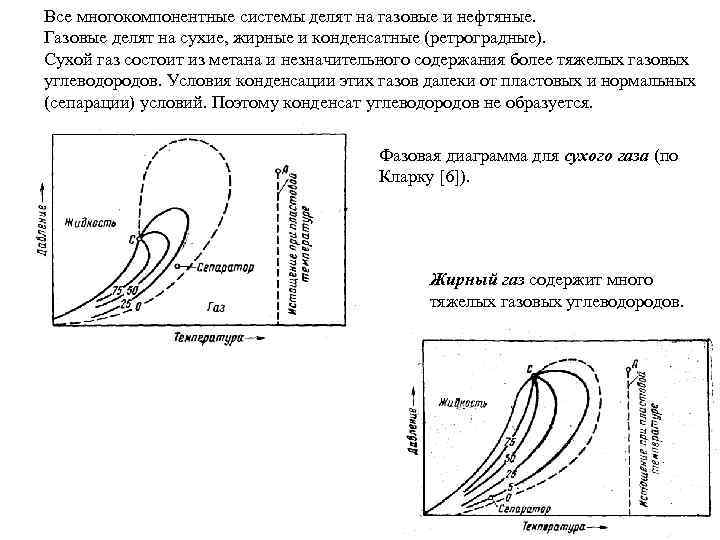 Все многокомпонентные системы делят на газовые и нефтяные. Газовые делят на сухие, жирные и конденсатные (ретроградные). Сухой газ состоит из метана и незначительного содержания более тяжелых газовых углеводородов. Условия конденсации этих газов далеки от пластовых и нормальных (сепарации) условий. Поэтому конденсат углеводородов не образуется. Фазовая диаграмма для сухого газа (по Кларку [6]). Жирный газ содержит много тяжелых газовых углеводородов.
Все многокомпонентные системы делят на газовые и нефтяные. Газовые делят на сухие, жирные и конденсатные (ретроградные). Сухой газ состоит из метана и незначительного содержания более тяжелых газовых углеводородов. Условия конденсации этих газов далеки от пластовых и нормальных (сепарации) условий. Поэтому конденсат углеводородов не образуется. Фазовая диаграмма для сухого газа (по Кларку [6]). Жирный газ содержит много тяжелых газовых углеводородов.
![Фазовая диаграмма для смеси природного газа с природным газолином (по Кацу и Курату [5]). Фазовая диаграмма для смеси природного газа с природным газолином (по Кацу и Курату [5]).](https://present5.com/presentation/184980035_144560122/image-23.jpg) Фазовая диаграмма для смеси природного газа с природным газолином (по Кацу и Курату [5]).
Фазовая диаграмма для смеси природного газа с природным газолином (по Кацу и Курату [5]).
![Фазовая диаграмма для нефти с высокой усадкой (по Кларку [6]). Фазовая диаграмма для нефти Фазовая диаграмма для нефти с высокой усадкой (по Кларку [6]). Фазовая диаграмма для нефти](https://present5.com/presentation/184980035_144560122/image-24.jpg) Фазовая диаграмма для нефти с высокой усадкой (по Кларку [6]). Фазовая диаграмма для нефти с низкой усадкой (по Кларку [6]).
Фазовая диаграмма для нефти с высокой усадкой (по Кларку [6]). Фазовая диаграмма для нефти с низкой усадкой (по Кларку [6]).
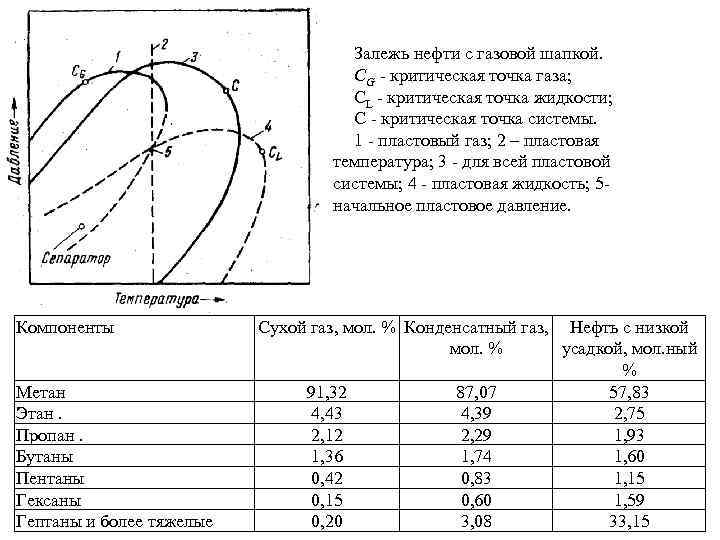 Залежь нефти с газовой шапкой. СG - критическая точка газа; СL - критическая точка жидкости; С - критическая точка системы. 1 - пластовый газ; 2 – пластовая температура; 3 - для всей пластовой системы; 4 - пластовая жидкость; 5 начальное пластовое давление. Компоненты Метан Этан. Пропан. Бутаны Пентаны Гексаны Гептаны и более тяжелые Сухой газ, мол. % Конденсатный газ, Нефть с низкой мол. % усадкой, мол. ный % 91, 32 87, 07 57, 83 4, 43 4, 39 2, 75 2, 12 2, 29 1, 93 1, 36 1, 74 1, 60 0, 42 0, 83 1, 15 0, 60 1, 59 0, 20 3, 08 33, 15
Залежь нефти с газовой шапкой. СG - критическая точка газа; СL - критическая точка жидкости; С - критическая точка системы. 1 - пластовый газ; 2 – пластовая температура; 3 - для всей пластовой системы; 4 - пластовая жидкость; 5 начальное пластовое давление. Компоненты Метан Этан. Пропан. Бутаны Пентаны Гексаны Гептаны и более тяжелые Сухой газ, мол. % Конденсатный газ, Нефть с низкой мол. % усадкой, мол. ный % 91, 32 87, 07 57, 83 4, 43 4, 39 2, 75 2, 12 2, 29 1, 93 1, 36 1, 74 1, 60 0, 42 0, 83 1, 15 0, 60 1, 59 0, 20 3, 08 33, 15


