III группа 2012.pptx
- Количество слайдов: 53
 Свойства элементов III группы Латаноиды и актиноиды
Свойства элементов III группы Латаноиды и актиноиды
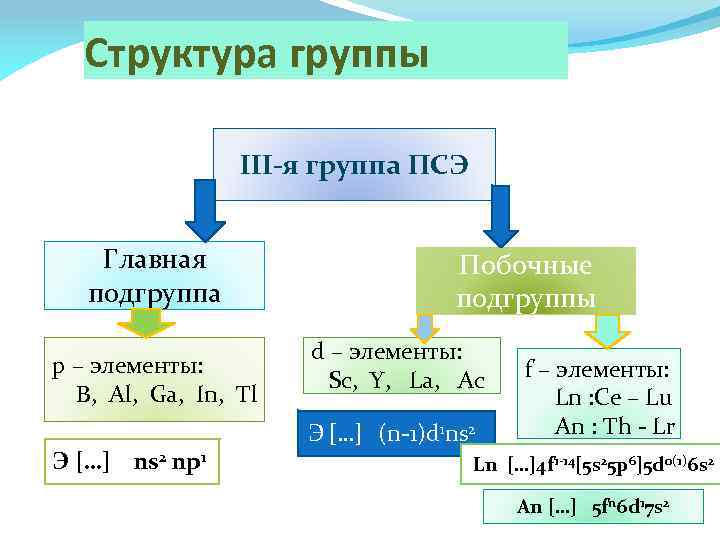 Структура группы III-я группа ПСЭ Главная подгруппа Побочные подгруппы d – элементы: Sc, Y, La, Ac p – элементы: B, Al, Ga, In, Tl Э […] ns 2 np 1 Э […] (n-1)d 1 ns 2 f – элементы: Ln : Ce – Lu An : Th - Lr Ln […]4 f 1 -14[5 s 25 p 6]5 d 0(1)6 s 2 An […] 5 fn 6 d 17 s 2
Структура группы III-я группа ПСЭ Главная подгруппа Побочные подгруппы d – элементы: Sc, Y, La, Ac p – элементы: B, Al, Ga, In, Tl Э […] ns 2 np 1 Э […] (n-1)d 1 ns 2 f – элементы: Ln : Ce – Lu An : Th - Lr Ln […]4 f 1 -14[5 s 25 p 6]5 d 0(1)6 s 2 An […] 5 fn 6 d 17 s 2
 Свойства элементов III группы Общие свойства: § Все элементы имеют общую валентность III и общий состав химических соединений. Элементы характеризуются металлическими свойствами , за исключением бора. § Для оксидов Э 2 О 3 и гидроксидов Э(ОН)3 характерны основные свойства , кроме Al, Ga, Sc. Элементы имеют подобные растворимые и нерастворимые соединения.
Свойства элементов III группы Общие свойства: § Все элементы имеют общую валентность III и общий состав химических соединений. Элементы характеризуются металлическими свойствами , за исключением бора. § Для оксидов Э 2 О 3 и гидроксидов Э(ОН)3 характерны основные свойства , кроме Al, Ga, Sc. Элементы имеют подобные растворимые и нерастворимые соединения.
 различные свойства Элементы главной подгруппы имеют иное электронное строение. Являются p-элементами (менее активные металлы). d- и f- элементы имеют на внешнем уровне ns- два электрона, поэтому являются типичными металлами Различие в свойствах элементов побочных подгрупп определяется электронным строением предшествующих электронных слоев.
различные свойства Элементы главной подгруппы имеют иное электронное строение. Являются p-элементами (менее активные металлы). d- и f- элементы имеют на внешнем уровне ns- два электрона, поэтому являются типичными металлами Различие в свойствах элементов побочных подгрупп определяется электронным строением предшествующих электронных слоев.
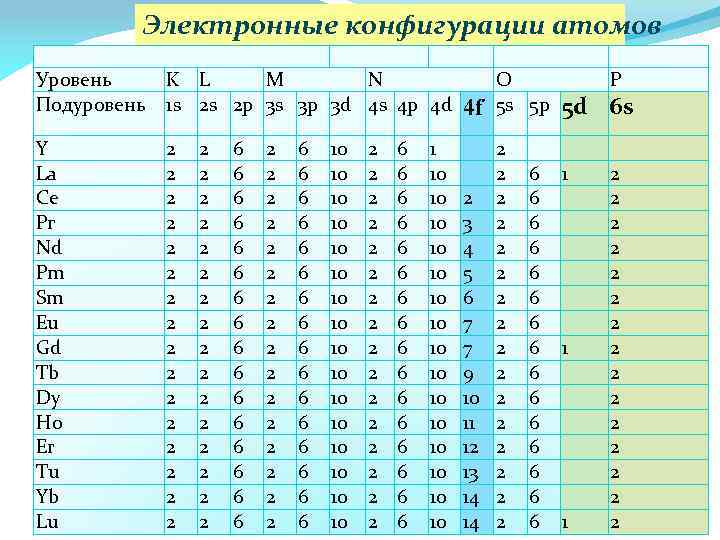 Электронные конфигурации атомов Уровень Подуровень K L M N 1 s 2 s 2 p 3 s 3 p 3 d 4 s 4 p 4 d Y La Се Рг Nd Pm Sm Eu Gd Tb Dy Ho Er Tu Yb Lu 2 2 2 2 2 2 2 2 6 6 6 6 2 2 2 2 6 6 6 6 10 10 10 10 2 2 2 2 6 6 6 6 1 10 10 10 10 4 f O 5 s 5 p 2 3 4 5 6 7 7 9 10 11 12 13 14 14 2 2 2 2 6 6 6 6 P 5 d 6 s 1 1 1 2 2 2 2
Электронные конфигурации атомов Уровень Подуровень K L M N 1 s 2 s 2 p 3 s 3 p 3 d 4 s 4 p 4 d Y La Се Рг Nd Pm Sm Eu Gd Tb Dy Ho Er Tu Yb Lu 2 2 2 2 2 2 2 2 6 6 6 6 2 2 2 2 6 6 6 6 10 10 10 10 2 2 2 2 6 6 6 6 1 10 10 10 10 4 f O 5 s 5 p 2 3 4 5 6 7 7 9 10 11 12 13 14 14 2 2 2 2 6 6 6 6 P 5 d 6 s 1 1 1 2 2 2 2
 Лантаноиды Цериевая подгруппа Иттриевая подгруппа (легкие лантаноиды) (тяжелые лантаноиды) Се-Eu Gd-Lu
Лантаноиды Цериевая подгруппа Иттриевая подгруппа (легкие лантаноиды) (тяжелые лантаноиды) Се-Eu Gd-Lu
 Характеристика РЗЭ Лантаноиды – элементы, следующие за лантаном и имеющие сходные с ним свойства. Лантаноиды относятся к f-элементам и имеют общее электронное строение: Ln […]4 f 1 -14[5 s 25 p 6 ]5 d 0(1) 6 s 2 Лантан, гадолиний и лютеций склонны проявлять только валентность равную III Церий, празеодим, тербий могут проявлять как валентность III, так и валентность IV Самарий, Европий, иттербий могут проявлять валентность II Радиусы атомов и ионов РЗЭ уменьшаются от La к Lu - эффект «лантаноидного сжатия»
Характеристика РЗЭ Лантаноиды – элементы, следующие за лантаном и имеющие сходные с ним свойства. Лантаноиды относятся к f-элементам и имеют общее электронное строение: Ln […]4 f 1 -14[5 s 25 p 6 ]5 d 0(1) 6 s 2 Лантан, гадолиний и лютеций склонны проявлять только валентность равную III Церий, празеодим, тербий могут проявлять как валентность III, так и валентность IV Самарий, Европий, иттербий могут проявлять валентность II Радиусы атомов и ионов РЗЭ уменьшаются от La к Lu - эффект «лантаноидного сжатия»
 РЗЭ реагируют с водой (при нагревании – быстро). 2 РЗЭ 0+6 H+2 O 2 РЗЭ+3(OH)3+3 H 02 РЗЭ 0 -3 е РЗЭ+3 2 H+ +2 е H 02 Замещаются металлами: 2 РЗЭ+3 Cl 3+3 Ca 0 t 2 РЗЭ 0+3 Ca+2 Cl 2 РЗЭ+3+3 е РЗЭ 0 Ca 0 -2 е Ca+2
РЗЭ реагируют с водой (при нагревании – быстро). 2 РЗЭ 0+6 H+2 O 2 РЗЭ+3(OH)3+3 H 02 РЗЭ 0 -3 е РЗЭ+3 2 H+ +2 е H 02 Замещаются металлами: 2 РЗЭ+3 Cl 3+3 Ca 0 t 2 РЗЭ 0+3 Ca+2 Cl 2 РЗЭ+3+3 е РЗЭ 0 Ca 0 -2 е Ca+2
 Основные химические свойства РЗЭ На воздухе легкие Ln окисляются при комнатной t, Остальные - при t = 180 -200 °С: 4 Ln 0+3 O 20 t 2 Ln 2+3 O 3 -2 Ln 0 -3 е Ln+3 O 02+4 е 2 O-2 Се и богатые Се сплавы пирофорны. Се 0+О 20 Се+4 О 2 -2 Се 0 - 4 е Се+4 O 02+ 4 е 2 O-2 С галогенами взаимодействуют при невысокой температуре 2 РЗЭ+3 Cl 2 t 2 РЗЭCl 3 РЗЭ 0 -3 е РЗЭ+3 Cl 02+2 е 2 Cl- интенсивность взаимодействия уменьшается от фтора к йоду.
Основные химические свойства РЗЭ На воздухе легкие Ln окисляются при комнатной t, Остальные - при t = 180 -200 °С: 4 Ln 0+3 O 20 t 2 Ln 2+3 O 3 -2 Ln 0 -3 е Ln+3 O 02+4 е 2 O-2 Се и богатые Се сплавы пирофорны. Се 0+О 20 Се+4 О 2 -2 Се 0 - 4 е Се+4 O 02+ 4 е 2 O-2 С галогенами взаимодействуют при невысокой температуре 2 РЗЭ+3 Cl 2 t 2 РЗЭCl 3 РЗЭ 0 -3 е РЗЭ+3 Cl 02+2 е 2 Cl- интенсивность взаимодействия уменьшается от фтора к йоду.
 РЗЭ реагируют с кислотами 2 РЗЭ+3 H 2 SO 4 РЗЭ 2(SO 4)3+3 H 2 РЗЭ 0 -3 е РЗЭ+3 2 2 H+ +2 е H 02 3 8 РЗЭ 0+30 HN+5 O 3 3 N-3 H 4 NO 3+8 РЗЭ(NO 3)3+9 H 2 O РЗЭ 0 -3 е РЗЭ+3 N+5+8 е N-3 Реагируют с солями: РЗЭ 2(SO 4)3 +3 Na 2 CO 3 РЗЭ 2(CO 3)3 +3 Na 2 SO 4 РЗЭ+3+3 NH 4 F РЗЭ F 3 +3 NH 4+ Щелочи на них не действуют даже при нагревании. РЗЭ+Na. OH t не идет
РЗЭ реагируют с кислотами 2 РЗЭ+3 H 2 SO 4 РЗЭ 2(SO 4)3+3 H 2 РЗЭ 0 -3 е РЗЭ+3 2 2 H+ +2 е H 02 3 8 РЗЭ 0+30 HN+5 O 3 3 N-3 H 4 NO 3+8 РЗЭ(NO 3)3+9 H 2 O РЗЭ 0 -3 е РЗЭ+3 N+5+8 е N-3 Реагируют с солями: РЗЭ 2(SO 4)3 +3 Na 2 CO 3 РЗЭ 2(CO 3)3 +3 Na 2 SO 4 РЗЭ+3+3 NH 4 F РЗЭ F 3 +3 NH 4+ Щелочи на них не действуют даже при нагревании. РЗЭ+Na. OH t не идет

 CВОЙСТВА ЦЕРИЯ Электронная конфигурация атома церия 2 2 6 0 2 58 Се [ ] 4 f [5 s 5 p ]5 d 6 s Церий активный металл. Церий взаимодействует при нагревании с большинством неметаллов (O 2, H 2, N 2, Cl 2, C, S, P и т. д. ) с образованием соответствующих бинарных соединений. 2 Ce + N 2 2 Ce. N Бурно взаимодействует с кислородом Ce + O 2 → Ce. O 2
CВОЙСТВА ЦЕРИЯ Электронная конфигурация атома церия 2 2 6 0 2 58 Се [ ] 4 f [5 s 5 p ]5 d 6 s Церий активный металл. Церий взаимодействует при нагревании с большинством неметаллов (O 2, H 2, N 2, Cl 2, C, S, P и т. д. ) с образованием соответствующих бинарных соединений. 2 Ce + N 2 2 Ce. N Бурно взаимодействует с кислородом Ce + O 2 → Ce. O 2
 ХИМ. СВОЙСТВА ЦЕРИЯ Реагирует с водой с выделением Н 2. В ряду активности Церий и др. лантаноиды можно расположить между Са и Mg. Се +3 Н 2 О Ce (OН)3+3 H 2 Карбонаты церия горят на воздухе Ce+32(CO 3)3 + O 02 t Ce+4 O 2 + 6 CO 2. Се+3 -е Се+4 4 восстановитель Eвос=1. 61 В; O 02 +4 е 2 O-2 1 окислитель Еок=1. 23 В; E = Eок-Eвос =-0. 38 Ce+32(C 2 O 4)3 + O 02 t 2 Ce+4 O 2 + 6 CO 2
ХИМ. СВОЙСТВА ЦЕРИЯ Реагирует с водой с выделением Н 2. В ряду активности Церий и др. лантаноиды можно расположить между Са и Mg. Се +3 Н 2 О Ce (OН)3+3 H 2 Карбонаты церия горят на воздухе Ce+32(CO 3)3 + O 02 t Ce+4 O 2 + 6 CO 2. Се+3 -е Се+4 4 восстановитель Eвос=1. 61 В; O 02 +4 е 2 O-2 1 окислитель Еок=1. 23 В; E = Eок-Eвос =-0. 38 Ce+32(C 2 O 4)3 + O 02 t 2 Ce+4 O 2 + 6 CO 2
 Свойства соединений церия Ce 3+ Кислотно-основные свойства Ce(OH)3 Гидроксид в водных растворах проявляет основной характер. Ce(NO 3)3+3 Na. OH Ce(OH)3 (бел. )+3 Na. NO 3; 2 Ce(OH)3 +3 H 2 SO 4 Ce 2(SO 4)3 + 3 H 2 O Ce(OH)3 +Na. OH ;
Свойства соединений церия Ce 3+ Кислотно-основные свойства Ce(OH)3 Гидроксид в водных растворах проявляет основной характер. Ce(NO 3)3+3 Na. OH Ce(OH)3 (бел. )+3 Na. NO 3; 2 Ce(OH)3 +3 H 2 SO 4 Ce 2(SO 4)3 + 3 H 2 O Ce(OH)3 +Na. OH ;
 Получение малорастворимых солей церия(III) 2 Ce(NO 3)3+3(NH 4)C 2 O 4 Ce 2(C 2 O 4)3 (бел)+6 NH 4 NO 3 2 Ce(NO 3)3+3 Na 2 CO 3 Ce 2(CO 3)3 (бел)+6 Na. NO 3 Ce(NO 3)3+Na 3 PO 4 Ce. PO 4 (бел)+3 Na. NO 3 Ce(NO 3)3+3 Na. F Ce. F 3 (бел)+3 Na. NO 3
Получение малорастворимых солей церия(III) 2 Ce(NO 3)3+3(NH 4)C 2 O 4 Ce 2(C 2 O 4)3 (бел)+6 NH 4 NO 3 2 Ce(NO 3)3+3 Na 2 CO 3 Ce 2(CO 3)3 (бел)+6 Na. NO 3 Ce(NO 3)3+Na 3 PO 4 Ce. PO 4 (бел)+3 Na. NO 3 Ce(NO 3)3+3 Na. F Ce. F 3 (бел)+3 Na. NO 3
 Окислтельно-восстановительные свойства Ce 3+ + окислитель Ce 4+ 3 Ce+3(OH)3 + KMn+7 O 4 + 2 H 2 O 3 Ce+4(OH)4 + Mn+4 O 2 + KOH Се+3 -е Се+4 3 Eвос=1. 61 В; Mn+7+3 е Mn+4 1 Еок=0. 6 В; E = Eок-Eвос =1, 01 В. 2 Ce (NO 3)3+Na. Bi+5 O 3 +6 HNO 3 2 Ce(NO 3)4(ж. )+Bi+3(NO 3)3+Na. NO 3+3 H 2 O(p. H<7) Bi+5+2 e Bi+3 Ce+3 -e Ce+4 1 2 Eок=1. 86 В Eвос=1. 61 В E = Eок-Eвос = 0, 25 В.
Окислтельно-восстановительные свойства Ce 3+ + окислитель Ce 4+ 3 Ce+3(OH)3 + KMn+7 O 4 + 2 H 2 O 3 Ce+4(OH)4 + Mn+4 O 2 + KOH Се+3 -е Се+4 3 Eвос=1. 61 В; Mn+7+3 е Mn+4 1 Еок=0. 6 В; E = Eок-Eвос =1, 01 В. 2 Ce (NO 3)3+Na. Bi+5 O 3 +6 HNO 3 2 Ce(NO 3)4(ж. )+Bi+3(NO 3)3+Na. NO 3+3 H 2 O(p. H<7) Bi+5+2 e Bi+3 Ce+3 -e Ce+4 1 2 Eок=1. 86 В Eвос=1. 61 В E = Eок-Eвос = 0, 25 В.
 Свойства Ce 4+. • Кислотно - основные: Ce(SO 4)2(жёлт. )+4 Na. OH Ce(OH)4(бел. ) +2 Na 2 SO 4 Слабые амфотерные свойства Ce(OH)4 проявляет только при высоких температурах( при спекании с щелочью): • Ce(OH)4 +Na. OH водный р-р • Ce(OH)4 + 2 Na. OН(тв) t Na 2 Ce. O 3 + 3 H 2 O • Ce(OH)4 +2 H 2 SO 4 Ce(SO 4)2 + 4 H 2 O
Свойства Ce 4+. • Кислотно - основные: Ce(SO 4)2(жёлт. )+4 Na. OH Ce(OH)4(бел. ) +2 Na 2 SO 4 Слабые амфотерные свойства Ce(OH)4 проявляет только при высоких температурах( при спекании с щелочью): • Ce(OH)4 +Na. OH водный р-р • Ce(OH)4 + 2 Na. OН(тв) t Na 2 Ce. O 3 + 3 H 2 O • Ce(OH)4 +2 H 2 SO 4 Ce(SO 4)2 + 4 H 2 O
 Окислительно-восстановительные свойства. Ce(IV) 2 Ce(SO 4)2+2 KI I 2+K 2 SO 4+Ce 2(SO 4)3 (p. H<7) Ce+4+e Ce+3 окислитель Eок=1. 61 В; 2 I--2 e I 2 восстановитель Eвост=-0. 54 В; Ер=Еок-Евост=1. 07 В; 2 Ce(SO 4)2+H 2 O 2 Ce 2(SO 4)3+O 2 +H 2 SO 4 Ce+4+e Ce+3 окислитель Еок=1. 61 В; 2 O 2 -2 -2 e O 20 восстановитель Евост=1. 23 В; 1 Ер=Еок-Евост=0. 38 В. 2 1
Окислительно-восстановительные свойства. Ce(IV) 2 Ce(SO 4)2+2 KI I 2+K 2 SO 4+Ce 2(SO 4)3 (p. H<7) Ce+4+e Ce+3 окислитель Eок=1. 61 В; 2 I--2 e I 2 восстановитель Eвост=-0. 54 В; Ер=Еок-Евост=1. 07 В; 2 Ce(SO 4)2+H 2 O 2 Ce 2(SO 4)3+O 2 +H 2 SO 4 Ce+4+e Ce+3 окислитель Еок=1. 61 В; 2 O 2 -2 -2 e O 20 восстановитель Евост=1. 23 В; 1 Ер=Еок-Евост=0. 38 В. 2 1
 Ионы Ce 4+ - сильные окислители в кислых средах 2 Ce+4(OH)4+8 HCl-1 2 Ce+3 Cl 3+Cl 2 +8 H 2 O Ce+4+e Ce+3 2 ок-ль Еок=1. 61 В; 2 Cl-1 -2 e Cl 20 1 в-ль Евост=1. 36 В; Ер=Еок-Евост=0, 25 В; 2 Ce(SO 4)2+2 KI I 2+K 2 SO 4+Ce 2(SO 4)3 Ce+3 Cl 4 Ce+3 Br 4 Ce+3 I 4 (p. H<7)
Ионы Ce 4+ - сильные окислители в кислых средах 2 Ce+4(OH)4+8 HCl-1 2 Ce+3 Cl 3+Cl 2 +8 H 2 O Ce+4+e Ce+3 2 ок-ль Еок=1. 61 В; 2 Cl-1 -2 e Cl 20 1 в-ль Евост=1. 36 В; Ер=Еок-Евост=0, 25 В; 2 Ce(SO 4)2+2 KI I 2+K 2 SO 4+Ce 2(SO 4)3 Ce+3 Cl 4 Ce+3 Br 4 Ce+3 I 4 (p. H<7)
 Отделение Ce от других РЗЭ В основе — способность церия проявлять степень окисления +4. Ce 2(C 2 O 4)3 + (NH 4)C 2 O 4 не идёт. Ce(C 2 O 4)2 + 2(NH 4)2 C 2 O 4 (NH 4)4[Ce(C 2 O 4)4] Ce(OH)3 + 3 HCl Ce. Cl 3 + 3 H 2 O. РЗЭ(OH)3 + 3 HCl РЗЭCl 3 + 3 H 2 O (p. H = 6, 5) 2 H 2 O+Ce. Cl 3+KMn. O 4+8 Na. OH Ce(OH)4 +Mn. O 2 +KCl+8 Na. Cl
Отделение Ce от других РЗЭ В основе — способность церия проявлять степень окисления +4. Ce 2(C 2 O 4)3 + (NH 4)C 2 O 4 не идёт. Ce(C 2 O 4)2 + 2(NH 4)2 C 2 O 4 (NH 4)4[Ce(C 2 O 4)4] Ce(OH)3 + 3 HCl Ce. Cl 3 + 3 H 2 O. РЗЭ(OH)3 + 3 HCl РЗЭCl 3 + 3 H 2 O (p. H = 6, 5) 2 H 2 O+Ce. Cl 3+KMn. O 4+8 Na. OH Ce(OH)4 +Mn. O 2 +KCl+8 Na. Cl
 Качественные реакции на ионы церия. • Ce(NO 3)3+3 NH 4 OH Ce(OH)3 (бел. )+3 NH 4 NO 3 2 Ce(OH)3+H 2 O 2 2 Ce(OH)4 (желт. ) (p. H > 7); Се+3 -е Се+4 восстановитель Eвос=1. 61 В; O 2 -2 + 2 e 2 O-2 окислитель Еок=1. 77 В; Ер=Еок-Евост=0. 16 В. • Ce(OH)4 +H 2 O 2 Ce(OH)3(OOH) (оранж. )+H 2 O (p. H > 7)
Качественные реакции на ионы церия. • Ce(NO 3)3+3 NH 4 OH Ce(OH)3 (бел. )+3 NH 4 NO 3 2 Ce(OH)3+H 2 O 2 2 Ce(OH)4 (желт. ) (p. H > 7); Се+3 -е Се+4 восстановитель Eвос=1. 61 В; O 2 -2 + 2 e 2 O-2 окислитель Еок=1. 77 В; Ер=Еок-Евост=0. 16 В. • Ce(OH)4 +H 2 O 2 Ce(OH)3(OOH) (оранж. )+H 2 O (p. H > 7)
 Отделение Eu от других РЗЭ. связано с способностью образовывать труднорастворимый сульфат 2 Eu. Cl 3+Zn+2 H 2 SO 4 2 Eu. SO 4 +Zn. Cl 3+4 HCl Eu 3+ +e Eu 2+окислитель Еок=-0. 55 В; 2 • Zn 0 -2 e Zn 2+восстановитель Евост. =-0. 762 В; 1 Ер=Еок-Евост=0. 212 В; Eu 2(SO 4)3+Zn 2 Eu. SO 4 +Zn SO 4 РЗЭ 2(SO 4)3+Zn Eu. C 2+ 2 H 2 O Eu(OH)2 +C 2 H 2(ацетилен) • РЗЭ+Zn отделение скандия от РЗЭ +3 + Sc +3 NH 4 F Sc. F 3 +3 NH 4 РЗЭ+3+3 NH 4 F РЗЭ F 3 +3 NH 4+ Sc. F 3+3 NH 4 F (NH 4)3[Sc. F 6] РЗЭ F 3 + NH 4 F
Отделение Eu от других РЗЭ. связано с способностью образовывать труднорастворимый сульфат 2 Eu. Cl 3+Zn+2 H 2 SO 4 2 Eu. SO 4 +Zn. Cl 3+4 HCl Eu 3+ +e Eu 2+окислитель Еок=-0. 55 В; 2 • Zn 0 -2 e Zn 2+восстановитель Евост. =-0. 762 В; 1 Ер=Еок-Евост=0. 212 В; Eu 2(SO 4)3+Zn 2 Eu. SO 4 +Zn SO 4 РЗЭ 2(SO 4)3+Zn Eu. C 2+ 2 H 2 O Eu(OH)2 +C 2 H 2(ацетилен) • РЗЭ+Zn отделение скандия от РЗЭ +3 + Sc +3 NH 4 F Sc. F 3 +3 NH 4 РЗЭ+3+3 NH 4 F РЗЭ F 3 +3 NH 4+ Sc. F 3+3 NH 4 F (NH 4)3[Sc. F 6] РЗЭ F 3 + NH 4 F
 актиноиды
актиноиды
 электронное строение Аn 5 f k 6 d m 7 s 2, где k изменяется от 2 до 14, а m равно 0 или 1 Различие в энергиях 5 f- и 6 d-орбиталей меньше, чем 4 f- и 5 d-орбиталей Поэтому легкие актиноиды характеризуются большим разнообразием степеней окисления, и более склонны к образованию комплексных соединений, чем лантаноиды.
электронное строение Аn 5 f k 6 d m 7 s 2, где k изменяется от 2 до 14, а m равно 0 или 1 Различие в энергиях 5 f- и 6 d-орбиталей меньше, чем 4 f- и 5 d-орбиталей Поэтому легкие актиноиды характеризуются большим разнообразием степеней окисления, и более склонны к образованию комплексных соединений, чем лантаноиды.
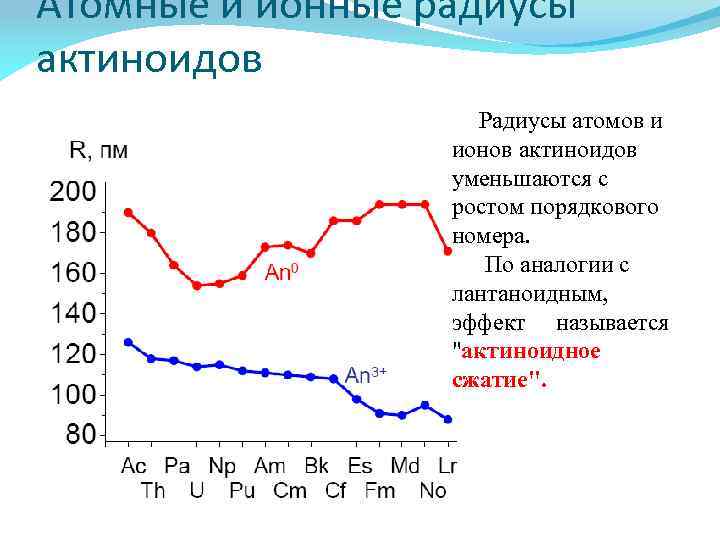 Атомные и ионные радиусы актиноидов Радиусы атомов и ионов актиноидов уменьшаются с ростом порядкового номера. По аналогии с лантаноидным, эффект называется "актиноидное сжатие".
Атомные и ионные радиусы актиноидов Радиусы атомов и ионов актиноидов уменьшаются с ростом порядкового номера. По аналогии с лантаноидным, эффект называется "актиноидное сжатие".
 Химические свойства актиноидов Обладают большой склонностью к комплексообразованию, особенно с кислородсодержащими лигандами ; В ряду легких актиноидов (от актиния до америция) свойства элементов сильно различаются В ряду тяжелых актиноидов (от кюрия до лоуренсия) они в значительной степени аналогичны и похожи на свойства лантаноидов;
Химические свойства актиноидов Обладают большой склонностью к комплексообразованию, особенно с кислородсодержащими лигандами ; В ряду легких актиноидов (от актиния до америция) свойства элементов сильно различаются В ряду тяжелых актиноидов (от кюрия до лоуренсия) они в значительной степени аналогичны и похожи на свойства лантаноидов;
 Свойства тория Электронная формула 6 d 2 7 s 2 Природный торий содержит практически один изотоп 232 Th, период полураспада равен 1, 4· 1010 лет Основная степень окисления +4
Свойства тория Электронная формула 6 d 2 7 s 2 Природный торий содержит практически один изотоп 232 Th, период полураспада равен 1, 4· 1010 лет Основная степень окисления +4
 Свойства тория Торий — активный металл, по реакционной способности близкий к лантаноидам, но отличается от них степенью окисления При нагревании торий реагирует со многими неметаллами: O 2 , Н 2, С, Cl 2, Br 2, S, N 2
Свойства тория Торий — активный металл, по реакционной способности близкий к лантаноидам, но отличается от них степенью окисления При нагревании торий реагирует со многими неметаллами: O 2 , Н 2, С, Cl 2, Br 2, S, N 2
 Торий взаимодействует с азотом при 800 °C с образованием нитрида тория Th. N(t 2500 °С) , 2 Th + N 2 2 Th. N Взаимодействия тория с углеродом Th + C Th + 2 C Th. C 2 карбиды разлагаются водой с образованием углеводородов. Th. C + 4 H 2 O Th(OH)4 + CH 4↑ Th. C 2 + 4 H 2 O Th(OH)4 + C 2 H 4↑
Торий взаимодействует с азотом при 800 °C с образованием нитрида тория Th. N(t 2500 °С) , 2 Th + N 2 2 Th. N Взаимодействия тория с углеродом Th + C Th + 2 C Th. C 2 карбиды разлагаются водой с образованием углеводородов. Th. C + 4 H 2 O Th(OH)4 + CH 4↑ Th. C 2 + 4 H 2 O Th(OH)4 + C 2 H 4↑
 Взаимодействие тория с водой и кислотами Торий - активный восстановитель (Е о = -1, 9 В) Торий вытесняет водород из кипящей воды Th + 4 H 2 O Th(OH)4 + 2 H 2↑ медленно растворяется в разбавленных фтороводородной, азотной или серной кислотах Th +2 H 2 SO 4(разб) Th + 4 HF(разб) Th (SO 4)2 + 2 H 2↑ Th. F 4 + 2 H 2↑
Взаимодействие тория с водой и кислотами Торий - активный восстановитель (Е о = -1, 9 В) Торий вытесняет водород из кипящей воды Th + 4 H 2 O Th(OH)4 + 2 H 2↑ медленно растворяется в разбавленных фтороводородной, азотной или серной кислотах Th +2 H 2 SO 4(разб) Th + 4 HF(разб) Th (SO 4)2 + 2 H 2↑ Th. F 4 + 2 H 2↑
 Соединения тория (IV) Th(OH)4 - имеет основной характер Th (SO 4)2 + 4 NH 4 OH → Th (OH)4↓ +2(NH 4)2 SO 4 Th (OH)4↓ Th. O 2 + 2 H 2 O Th (OH)4↓ + 4 HCl(разб) Th. Cl 4 + 2 H 2 O Th (OH)4↓ + CO 2 → Th OCO 3↓ + H 2 O к растворимым в воде соединениям относятся нитраты, хлориды и сульфаты тория (IV) Гидролиз солей Th(NO 3)4 + H 2 O Th. O(NO 3)2 + 2 HNO 3 Th(NO 3)4 + 2 Na 2 CO 3 + H 2 O Th. O CO 3 + H 2 CO 3 + 4 Na. NO 3
Соединения тория (IV) Th(OH)4 - имеет основной характер Th (SO 4)2 + 4 NH 4 OH → Th (OH)4↓ +2(NH 4)2 SO 4 Th (OH)4↓ Th. O 2 + 2 H 2 O Th (OH)4↓ + 4 HCl(разб) Th. Cl 4 + 2 H 2 O Th (OH)4↓ + CO 2 → Th OCO 3↓ + H 2 O к растворимым в воде соединениям относятся нитраты, хлориды и сульфаты тория (IV) Гидролиз солей Th(NO 3)4 + H 2 O Th. O(NO 3)2 + 2 HNO 3 Th(NO 3)4 + 2 Na 2 CO 3 + H 2 O Th. O CO 3 + H 2 CO 3 + 4 Na. NO 3
 комплексообразование В водных растворах торий образует комплексные соединения с КЧ=6, 8 и реже 10 или 12. Комплексообразование используют для растворения труднорастворимых соединений тория (карбонатов, оксалатов). Th. OCO 3↓ + 3 Na 2 CO 3 + H 2 O → Na 4[Th(CO 3)4] + 2 Na. OH Th(C 2 O 4)2 ↓ + 2(NH 4)2 C 2 O 4 → (NH 4)4[Th(C 2 O 4)4]
комплексообразование В водных растворах торий образует комплексные соединения с КЧ=6, 8 и реже 10 или 12. Комплексообразование используют для растворения труднорастворимых соединений тория (карбонатов, оксалатов). Th. OCO 3↓ + 3 Na 2 CO 3 + H 2 O → Na 4[Th(CO 3)4] + 2 Na. OH Th(C 2 O 4)2 ↓ + 2(NH 4)2 C 2 O 4 → (NH 4)4[Th(C 2 O 4)4]
 Получение тория минерал монацит вскрывают сернокислотным или щелочным способом Th 3(PO 4)4+12 Na. OH → 3 Th(OH)4↓+4 Na 3 PO 4 оксид тория Th. O 2 подвергают металлотермическому восстановлению кальцием в атмосфере инертного газа: Th. O 2+2 Ca Th + 2 Ca. O электролиз расплава галогенида тория Th. F 4 или Th. Cl 4.
Получение тория минерал монацит вскрывают сернокислотным или щелочным способом Th 3(PO 4)4+12 Na. OH → 3 Th(OH)4↓+4 Na 3 PO 4 оксид тория Th. O 2 подвергают металлотермическому восстановлению кальцием в атмосфере инертного газа: Th. O 2+2 Ca Th + 2 Ca. O электролиз расплава галогенида тория Th. F 4 или Th. Cl 4.
 Уран и его свойства
Уран и его свойства
 Уран — самый тяжелый из встречающихся в природе элементов Его содержание в земной коре составляет 3· 10 -4 % по массе Он имеет три изотопа: 99, 28% природного урана составляет изотоп 238 U, период полураспада которого равен 4, 5· 109 лет; 0, 715 % – изотоп 235 U с периодом полураспада 7, 1· 108 лет; 0, 005 % – изотоп 234 U с периодом полураспада 2, 47· 105 лет. Изотоп 233 U получен в результате ядерных реакций.
Уран — самый тяжелый из встречающихся в природе элементов Его содержание в земной коре составляет 3· 10 -4 % по массе Он имеет три изотопа: 99, 28% природного урана составляет изотоп 238 U, период полураспада которого равен 4, 5· 109 лет; 0, 715 % – изотоп 235 U с периодом полураспада 7, 1· 108 лет; 0, 005 % – изотоп 234 U с периодом полураспада 2, 47· 105 лет. Изотоп 233 U получен в результате ядерных реакций.
 Электронное строение и СО урана U 5 f 36 d 17 s 2 степени окисления от +3 , +4, +5, +6, наиболее устойчивыми среди них являются степени окисления +4 и +6 в степени окисления +6 – амфотерные свойства; Его температура плавления равна 1132 °C Он химически активен и реагирует со многими элементами периодической системы.
Электронное строение и СО урана U 5 f 36 d 17 s 2 степени окисления от +3 , +4, +5, +6, наиболее устойчивыми среди них являются степени окисления +4 и +6 в степени окисления +6 – амфотерные свойства; Его температура плавления равна 1132 °C Он химически активен и реагирует со многими элементами периодической системы.
 Свойства урана Уран имеет очень высокое сродство к кислороду U + O 2 UO 2 UO 3 U 3 O 8 ) 2 U + N 2 2 UN U + C UC U + 2 C UC 2 UC + 4 H 2 O U(OH)4 + CH 4↑ UC 2 + 4 H 2 O U(OH)4 + C 2 H 4↑ U + 3 F 2 UF 6 U + 3 Cl 2 UCl 6
Свойства урана Уран имеет очень высокое сродство к кислороду U + O 2 UO 2 UO 3 U 3 O 8 ) 2 U + N 2 2 UN U + C UC U + 2 C UC 2 UC + 4 H 2 O U(OH)4 + CH 4↑ UC 2 + 4 H 2 O U(OH)4 + C 2 H 4↑ U + 3 F 2 UF 6 U + 3 Cl 2 UCl 6
 Свойства U(IV) Безводный тетрафторид получают из диоксида урана UO 2+4 HF UF 4↓+2 H 2 O восстановлением гексафторида урана различными восстановителями, например, водородом UF 6+H 2 UF 4↓+2 HF
Свойства U(IV) Безводный тетрафторид получают из диоксида урана UO 2+4 HF UF 4↓+2 H 2 O восстановлением гексафторида урана различными восстановителями, например, водородом UF 6+H 2 UF 4↓+2 HF
 Свойства U(IV) -аналог Th 4+ характерны: основные свойства Гидролиз U (NO 3)4 + H 2 O UOH(NO 3)3 + HNO 3 Комплексообразование ОВР
Свойства U(IV) -аналог Th 4+ характерны: основные свойства Гидролиз U (NO 3)4 + H 2 O UOH(NO 3)3 + HNO 3 Комплексообразование ОВР
 Под действием окислителей уран (IV) переходит в уран (VI) U(SO 4)2 + 2 Ce(SO 4)2 + 2 H 2 O → UO 2 SO 4 + Ce 2(SO 4)3 + 2 H 2 SO 4 2 U(SO 4)2 + 2 KMn. O 4 + 2 H 2 O → 5 UO 2 SO 4 + 2 Mn. SO 4 + KHSO 4 + H 2 SO 4 Под действием восстановителей уран (IV) переходит в уран (I I I) 2 U(SO 4)2 + Zn + → U 2(SO 4)3 + Zn. SO 4
Под действием окислителей уран (IV) переходит в уран (VI) U(SO 4)2 + 2 Ce(SO 4)2 + 2 H 2 O → UO 2 SO 4 + Ce 2(SO 4)3 + 2 H 2 SO 4 2 U(SO 4)2 + 2 KMn. O 4 + 2 H 2 O → 5 UO 2 SO 4 + 2 Mn. SO 4 + KHSO 4 + H 2 SO 4 Под действием восстановителей уран (IV) переходит в уран (I I I) 2 U(SO 4)2 + Zn + → U 2(SO 4)3 + Zn. SO 4
 Свойства U(VI) Гидролиз солей: UCl 6 + 2 H 2 O → UO 2 Cl 2 + 4 HCl Амфотерность: при растворении в кислотах образуются соли диоксоурана UO 2(OH)2 + H 2 SO 4 → UO 2 SO 4 + 2 H 2 O при растворении в концентрированных щелочах – уранаты UO 2(OH)2 +2 Na. OH → Na 2 UO 4 + 2 H 2 O или диуранаты 2 UO 2(OH)2 +2 Na. OH → Na 2 U 2 O 7 + 3 H 2 O
Свойства U(VI) Гидролиз солей: UCl 6 + 2 H 2 O → UO 2 Cl 2 + 4 HCl Амфотерность: при растворении в кислотах образуются соли диоксоурана UO 2(OH)2 + H 2 SO 4 → UO 2 SO 4 + 2 H 2 O при растворении в концентрированных щелочах – уранаты UO 2(OH)2 +2 Na. OH → Na 2 UO 4 + 2 H 2 O или диуранаты 2 UO 2(OH)2 +2 Na. OH → Na 2 U 2 O 7 + 3 H 2 O
 комплексообразование Трикарбонатный комплекс катиона диоксоурана хорошо растворим UO 2 SO 4 + 3 Na 2 CO 3 → Na 4[UO 2(CO 3)3] + Na 2 SO 4 (NH 4)2 U 2 O 7↓ + 6(NH 4)2 CO 3 + 3 H 2 O → 2(NH 4)4[UO 2(CO 3)3] + 6 Na. OH В карбонатных комплексах иона диоксоурана два координационных места заняты атомами кислорода
комплексообразование Трикарбонатный комплекс катиона диоксоурана хорошо растворим UO 2 SO 4 + 3 Na 2 CO 3 → Na 4[UO 2(CO 3)3] + Na 2 SO 4 (NH 4)2 U 2 O 7↓ + 6(NH 4)2 CO 3 + 3 H 2 O → 2(NH 4)4[UO 2(CO 3)3] + 6 Na. OH В карбонатных комплексах иона диоксоурана два координационных места заняты атомами кислорода
 Окислительно-восстановительные свойства U 6+ окислитель восстановление шестивалентного урана проводят электрохимически или с использованием таких металлов, как железо или цинк: UO 2 SO 4 + Zn + 2 H 2 SO 4 → U(SO 4)2 + Zn. SO 4 + 2 H 2 O
Окислительно-восстановительные свойства U 6+ окислитель восстановление шестивалентного урана проводят электрохимически или с использованием таких металлов, как железо или цинк: UO 2 SO 4 + Zn + 2 H 2 SO 4 → U(SO 4)2 + Zn. SO 4 + 2 H 2 O
 Получение и очистка урана Металлический уран получают восстановлением тетрафторида урана UF 4 кальцием или магнием в инертной атмосфере: UF 4+2 Ca U + 2 Ca. F 2
Получение и очистка урана Металлический уран получают восстановлением тетрафторида урана UF 4 кальцием или магнием в инертной атмосфере: UF 4+2 Ca U + 2 Ca. F 2
 Получение урана Для урана известно около 200 минералов промышленное значение имеет минерал настуран (урановая смолка) U 3 O 8 урановую смоляную руду, обрабатывают минеральными кислотами, например азотной или серной кислотой, в присутствии Mn. O 2, для окисления урана(IV): U 3 O 8 + Mn. O 2 + 4 H 2 SO 4 → Mn. SO 4 + 3 UO 2 SO 4 + 4 H 2 O
Получение урана Для урана известно около 200 минералов промышленное значение имеет минерал настуран (урановая смолка) U 3 O 8 урановую смоляную руду, обрабатывают минеральными кислотами, например азотной или серной кислотой, в присутствии Mn. O 2, для окисления урана(IV): U 3 O 8 + Mn. O 2 + 4 H 2 SO 4 → Mn. SO 4 + 3 UO 2 SO 4 + 4 H 2 O
 Методы разделения
Методы разделения
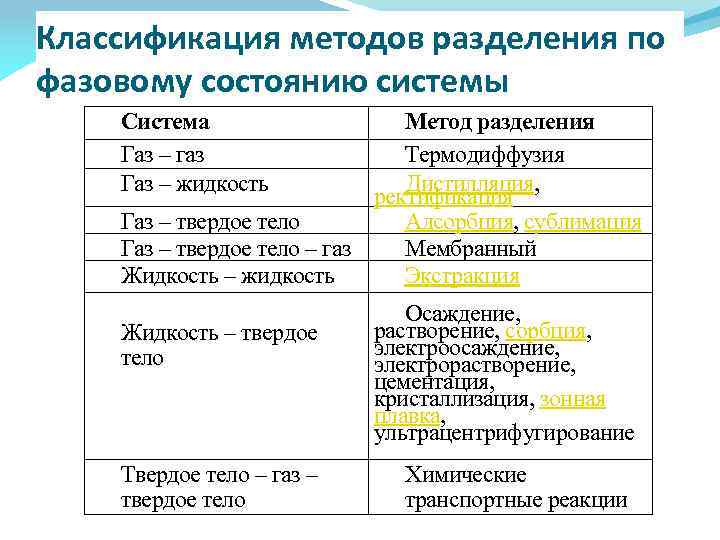 Классификация методов разделения по фазовому состоянию системы Система Газ – газ Газ – жидкость Метод разделения Термодиффузия Дистилляция, ректификация Газ – твердое тело Адсорбция, сублимация Газ – твердое тело – газ Мембранный Жидкость – жидкость Экстракция Жидкость – твердое тело Твердое тело – газ – твердое тело Осаждение, растворение, сорбция, электроосаждение, электрорастворение, цементация, кристаллизация, зонная плавка, ультрацентрифугирование Химические транспортные реакции
Классификация методов разделения по фазовому состоянию системы Система Газ – газ Газ – жидкость Метод разделения Термодиффузия Дистилляция, ректификация Газ – твердое тело Адсорбция, сублимация Газ – твердое тело – газ Мембранный Жидкость – жидкость Экстракция Жидкость – твердое тело Твердое тело – газ – твердое тело Осаждение, растворение, сорбция, электроосаждение, электрорастворение, цементация, кристаллизация, зонная плавка, ультрацентрифугирование Химические транспортные реакции
 Характеристики процесса разделения 1. Коэффициент распределения Di = Ci/Ci При значениях D>1 вещество можно сконцентрировать в извлекающей фазе 2. Коэффициент разделения Разделение веществ возможно при β>1 Di- коэфф. распределения основного в-ва Dj- коэфф. распределения примеси Чем больше β отличается от единицы, тем более избирателен (селективен) метод разделения.
Характеристики процесса разделения 1. Коэффициент распределения Di = Ci/Ci При значениях D>1 вещество можно сконцентрировать в извлекающей фазе 2. Коэффициент разделения Разделение веществ возможно при β>1 Di- коэфф. распределения основного в-ва Dj- коэфф. распределения примеси Чем больше β отличается от единицы, тем более избирателен (селективен) метод разделения.
 Методы разделения химические методы физико-химические методы осаждение, растворение, цементация, физические методы термодиффузию, кристаллизацию, зонная плавка, ультрацентрифугирование сорбция, экстракция, электроосаждение, электрорастворение, транспортные реакции,
Методы разделения химические методы физико-химические методы осаждение, растворение, цементация, физические методы термодиффузию, кристаллизацию, зонная плавка, ультрацентрифугирование сорбция, экстракция, электроосаждение, электрорастворение, транспортные реакции,
 химические методы В их основе лежит применение специфических реагентов, которые по-разному взаимодействуют с основным и примесными компонентами, позволяя перевести один из них в газовую или твердую фазы. В качестве специфических реагентов могут служить минеральные кислоты, щелочи, окислители, комплексообразователи
химические методы В их основе лежит применение специфических реагентов, которые по-разному взаимодействуют с основным и примесными компонентами, позволяя перевести один из них в газовую или твердую фазы. В качестве специфических реагентов могут служить минеральные кислоты, щелочи, окислители, комплексообразователи
 Осаждение Основан на различной растворимости компонентов растворов. Для отделения от примесей используют селективные осадители и промывку полученных осадков на фильтре. Ag++Cl- = Ag. Cl↓, Ba 2++SO 42 - = Ba. SO 4↓ Коэффициент разделения для процессов осаждения β = ПРi/ПРj отделение скандия от РЗЭ и тория Sc. F 3+3 NH 4 F = (NH 4)3[Sc. F 6] растворим
Осаждение Основан на различной растворимости компонентов растворов. Для отделения от примесей используют селективные осадители и промывку полученных осадков на фильтре. Ag++Cl- = Ag. Cl↓, Ba 2++SO 42 - = Ba. SO 4↓ Коэффициент разделения для процессов осаждения β = ПРi/ПРj отделение скандия от РЗЭ и тория Sc. F 3+3 NH 4 F = (NH 4)3[Sc. F 6] растворим
 цементация в качестве осадителей могут применяться чистые металлы, которые вытесняют из растворов более электроположительные металлы. например, получение меди из ее разбавленных р-ров: Cu. SO 4+Fe = Cu↓+Fe. SO 4 также очищают сульфатные цинковые растворы от примеси меди и кадмия : Cu. SO 4+Zn = Cu↓+Zn. SO 4 Cd. SO 4+Zn = Cd↓+Zn. SO 4
цементация в качестве осадителей могут применяться чистые металлы, которые вытесняют из растворов более электроположительные металлы. например, получение меди из ее разбавленных р-ров: Cu. SO 4+Fe = Cu↓+Fe. SO 4 также очищают сульфатные цинковые растворы от примеси меди и кадмия : Cu. SO 4+Zn = Cu↓+Zn. SO 4 Cd. SO 4+Zn = Cd↓+Zn. SO 4
 ОВР применяют для выделения из смеси тех элементов, которые могут существовать в растворах в различных степенях окисления выделение ионов марганца из сульфатных р-ров 3 Mn. SO 4+2 KMn. O 4+2 H 2 O = 5 Mn. O 2↓+K 2 SO+4 4+2 H 2 SO 4 +7 Mn +3 e = Mn Mn+2 -2 e = Mn+4 2 3 Отделение европия от сульфатов трехвалентных РЗЭ 2 Eu. Cl 3+Zn+2 H 2 SO 4 = 2 Eu. SO 4↓+Zn. Cl 2+4 HCl
ОВР применяют для выделения из смеси тех элементов, которые могут существовать в растворах в различных степенях окисления выделение ионов марганца из сульфатных р-ров 3 Mn. SO 4+2 KMn. O 4+2 H 2 O = 5 Mn. O 2↓+K 2 SO+4 4+2 H 2 SO 4 +7 Mn +3 e = Mn Mn+2 -2 e = Mn+4 2 3 Отделение европия от сульфатов трехвалентных РЗЭ 2 Eu. Cl 3+Zn+2 H 2 SO 4 = 2 Eu. SO 4↓+Zn. Cl 2+4 HCl


