Периодический закон.ppt
- Количество слайдов: 48


Свойства элементов, а также свойства образованных ими простых и сложных веществ находятся в периодической зависимости от атомной массы. Дмитрий Иванович открыл фундаментальный закон химии. В его время (середина XIX века) было известно 63 сорта атомов – химических элементов. И другие ученые пытались их систематизировать, но почему же русскому химику «улыбнулась удача? » Самой первой попыткой систематизировать сорта атомов наверняка была попытка разделить их на металлы и неметаллы.

Металлы Серебро Ag Натрий Na Платина Pt Марганец Mn Золото Au Медь Сu По своим физическим свойствам металлы довольно однообразны : имеют блеск, ковкие , пластичные, прекрасно проводят ток и тепло, большинство серебристо – серые.

Неметаллы Сера S Фосфор (разный) Р Йод I 2 Хлор Cl 2 Кислород О 2 В отличие от металлов, неметаллы более разнообразны : у них разное агрегатное состояние при н. у. , разный цвет; теплопроводность меньше чем у металлов; по отношению к току не. Ме изоляторы или полупроводники.

Но этой систематизации явно не хватало, слишком она примитивная. Тогда Менделеев задумался и решил разложить карточки с выписанными свойствами элементов просто в ряд по мере возрастания атомной массы: И как же быть –то ? И он заметил, что через каждые 7 элементов физические и химические свойства веществ повторяются!

Литий Li Натрий Na Литий и натрий – очень мягкие, серебристые, чрезвычайно активные металлы, мощные восстановители. Оксиды и гидроксиды – с основными свойствами. Углерод (графит) и кремний – серые с металлическим блеском вещества полупроводники, слабые окислители и сильные восстановители. Оксиды и гидроксиды с кислотными Кремний Si свойствами. Алмаз С Графит С У алмаза (разновидности углерода) и у кремния одинаковая кристаллическая решетка ( тетраэдр)

Следующий важный вывод сделал Менделеев: начиная с лития, падают металлические свойства, а также восстановительные свойства элементов, а неметаллические свойства , а также окислительные , наоборот, возрастают. Когда в конце XIX века открыли благородные газы, ученый интуитивно правильно поместил их вслед за активными неметаллами-галогенами (фтором, хлором, бромом, йодом). Таким образом, Менделеев открыл повторяемость элементов через каждые 8 штук (другие ученые называли это «закон октав» ). Эту «химическую октаву» Дмитрий Иванович назвал «периодом» . Период должен был начинаться активным щелочным металлом, а завершаться инертным благородным газом. Менделеев не был педантом, он понимал, что все тайны атома еще не изучены, следовательно из его Калий К Аргон Ar закона могут быть Ar=39 Ar=40 исключения

Он совершенно справедливо поставил более тяжелый атом аргона перед более легким атомом калия, потому что благородный газ аргон по сути должен был завершать 3 период, а щелочной металл калий – открывать период четвертый. После того как внутреннее строение атома было разгадано (создана планетарная модель), правильный поступок Менделеева да и вообще Периодический закон блестяще подтвердились. Свойства элементов, а также свойства образованных ими простых и сложных веществ находятся в периодической зависимости от заряда ядра атома. Ребята, вам к Периодическому законы важная ссылка на работу «Строение атома»

Порядковый номер атома в Периодической системе элементов Кратко напомню, что главная частица в атомном ядре протон, он определяет сорт атома и равен порядковому номеру элемента в Периодической системе. Изотопы кислорода Пара изобаров Еще напоминание: существование таких разновидностей атомного ядра как изотопы и изобары (См. «Строение атома» ) доказывает, что нельзя атомную массу считать признаком элемента. Пара изотопов
Это графическое подтверждение Периодического закона. В настоящее время внутри нее нет «белых пятен» , т. е. все элементы открыты в природе или искусственно созданы людьми. Но она все пополняется и пополняется с конца, так как физики-ядерщики создают новые элементы в ходе ядерных реакций. Трудность ядерного синтеза в том, что тяжелые нуклиды радиоактивны и живут порой очень-очень мало.

Современные разновидности таблиц Менделеева После триумфа Периодического закона на полном серьезе было создано столько разновидностей и интерпретаций таблицы элементов, что люди откровенно путались. Поэтому международный съезд химиков ИЮПАК (союз аналитической и прикладной химии) постановил признать официальными только 3 вида таблиц Менделеева. А вот это все «от лукавого»
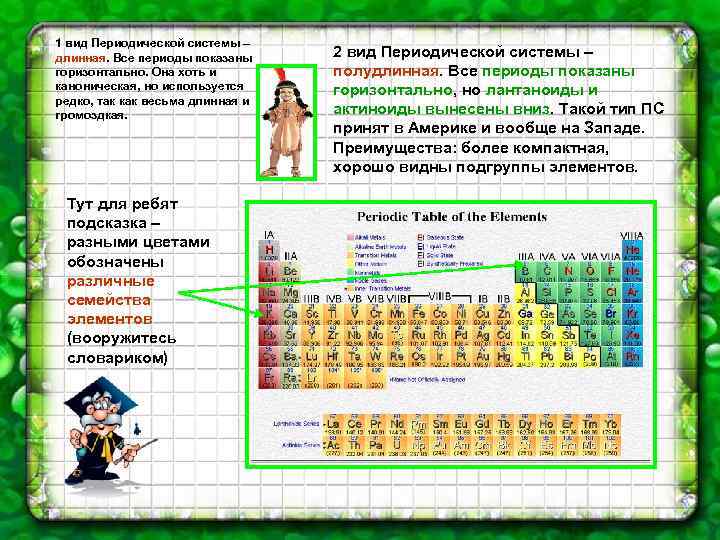
1 вид Периодической системы – длинная. Все периоды показаны горизонтально. Она хоть и каноническая, но используется редко, так как весьма длинная и громоздкая. Тут для ребят подсказка – разными цветами обозначены различные семейства элементов (вооружитесь словариком) 2 вид Периодической системы – полудлинная. Все периоды показаны горизонтально, но лантаноиды и актиноиды вынесены вниз. Такой тип ПС принят в Америке и вообще на Западе. Преимущества: более компактная, хорошо видны подгруппы элементов.

На этой таблице показаны также семейства элементов; буквой «А» обозначены элементы главных подгрупп, а буквой «В» элементы побочных подгрупп. Здесь же изображены разным цветом также семейства элементов, а также основная область применения Можете щелкнуть мышкой и увеличить изображение.

А эта таблица (вполне официальная) вызовет интерес у ребят начальной школы, она красочная, и на ней также показаны основные области применения элементов. (Увеличьте ее и порассматривайте хорошенько).
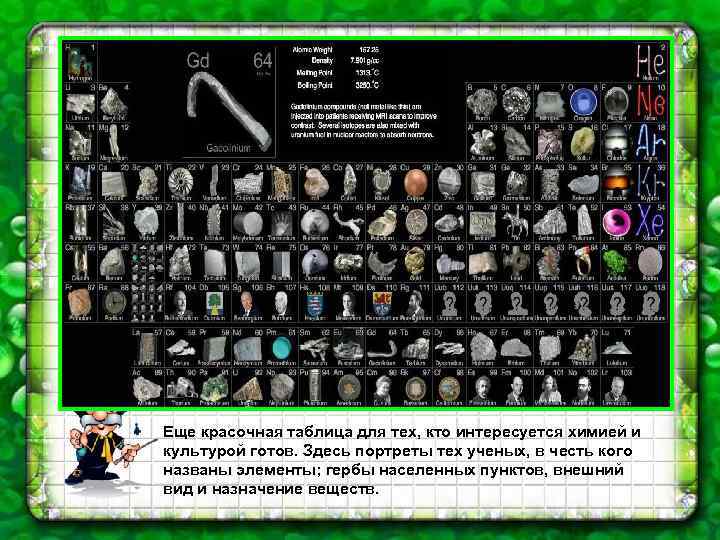
Еще красочная таблица для тех, кто интересуется химией и культурой готов. Здесь портреты тех ученых, в честь кого названы элементы; гербы населенных пунктов, внешний вид и назначение веществ.

Периодическая система – источник вдохновения не только для ученых, но и для дизайнеров!

И , наконец, 3 канонический вариант ПС, принятый в России – краткая форма. Большие периоды сложены «пополам» , лантаноиды и актиноиды внизу. Видны группы элементов и их единство (это не показано в «западном» варианте ПС). Вообще при такой форме проще увязать строение атома и положение элемента в ПС. При таком дизайне показаны электронные семейства атомов (s-, p-, d-, fэлементы. )
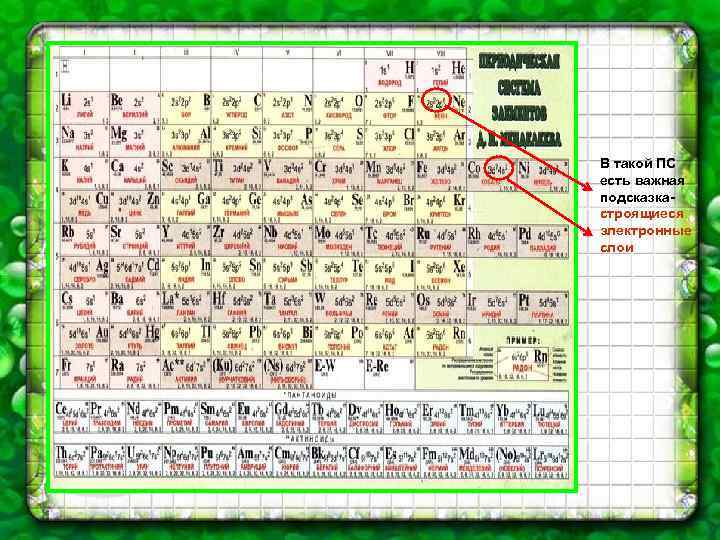
В такой ПС есть важная подсказкастроящиеся электронные слои

И такая ПС совершенно необходима , важная цветовая информация показана внизу таблицы (только тут нет fэлементов). Вообще при изучении химии можно и нужно иметь под рукой ПС разных дизайнов и несущих разную полезную информацию!

Алкогольные элементы Таблица десертов Шутка: пародии на таблицу Менделеева Таблица овощей Криминальные элементы

Строение таблицы Менделеева (короткий вариант) Давайте для начала рассмотрим важную информацию, которая есть в «клеточке-ячейке» , предназначенной для каждого отдельного сорта атома. Порядковый № Символ элемента Национальное название элемента (Именно он определяет заряд ядра и сорт атома) Атомная масса (при расчетах она округляется до целого числа) Строящиеся электронные слои

Ребята порой путаются в таком вопросе: где элементы главных и побочных подгрупп и как их различить в т. М. ? Помогут здесь символическая окраска «клеточки элемента» и расположение в ней символа элемента. Прежде всего, у элементов главных подгрупп символы в клеточках чаще всего расположены слева; окраска ячеек соответствует электронным семействам s- и р-элементов. Тут показан участок Т. М. Неметаллы и металлоиды показаны соответственно зеленым и фиолетовым цветом. Они всегда главным подгруппам.

А у элементов побочных подгрупп символы в клеточках чаще всего расположены справа; окраска ячеек соответствует электронным семействам d- и f-элементов. Еще важное правило : элементами главных подгрупп могут быть металлы и неметаллы, а элементами побочных подгрупп – только металлы.

Период – горизонтальный ряд в т. М. , который начинается активным щелочным металлом и завершается благородным газом. Всего в ПС 7 периодов: 3 малых и 4 больших. Они включают в себя разные электронные семейства. 1 период – 2 s-элемента; 2 и 3 периоды – всего по 8 элементов, в них s- и рэлементы. У всех этих атомов строится внешний электронный слой все они главным подгруппам. В 4 и 5 периодах по 18 элементов, есть s- и рэлементы, добавляются d-элементы (вставные декады) В 6 периоде 32 элемента, есть s, p-, d-элементы + лантаноиды

7 период неполный, он включает в себя много сильно радиоактивных элементов, созданных физиками, есть s-, d-, fэлементы (актиноиды) , р-элементы еще не синтезированы (но все впереди!) Группа – вертикальный столбец в т. М. , который объединяет элементы с одинаковым числом валентных электронов. Всего таких групп 8 штук.

Вот посмотрим, например, на представителей 6 и 7 групп. В их состав входят р-элементы (они главной подгруппам, символы слева) и dэлементы, вставные декады (они побочным подгруппам, символы справа) 3 группа – совершенно особенная, очень большая. В нее входят рэлементы ( главной подгруппе), dэлементы ( 1 -й побочной подгруппе) и f-элементы лантаноиды и актиноиды ( 2 -й побочной подгруппе).

В «западных» ПС элементы одной группы пространственно разделены, тут другая подсказка: римской цифрой обозначен № группы, а буквами «А» и «В» соответственно главная и побочная подгруппы. Кстати, в таких Т. М. положение элементов в клеточках часто одинаковое из-за того, что главная и побочная подгруппы разделены в пространстве. Мы же будем работать с «русской» версией Т. М. и должны уметь понимать сходство и различие в свойствах атомов и веществ, объединенных в состав одной группы.

Сравним для начала представителей 7 группы: фтор, хлор и марганец. Фтор хлор марганец Фтор и хлор похожи между собой: простые вещества образуют двухатомные молекулы, это ядовитые чрезвычайно химически активные газы, мощные окислители. Температура плавления у них низкая, твердые хлор и фтор хрупкие вещества, изоляторы. Марганец же – типичный металл , ковкий, пластичный, проводник, температура плавления высокая. Решетка металлическая, проявляет лишь восстановительные свойства. Что же у него-то общего с хлором и фтором?

Разгадка сходства этих элементов кроется в строении их атомов : у них у всех общее число валентных электронов, но расположены они в атомах по-разному, отсюда и различие! Фтор и хлор р- элементы у них строятся внешний s- и р-подуровни; у них по 7ē на внешнем слое (Красный цвет квантовых ячеек). Марганец же d-элемент валентные ē на внешнем 4 s- и предвнешнем 3 dподуровне. Но их тоже 7 штук!

Забегая вперед скажу, что фтор не может распаривать свои внешние электроны и образовывать катионы, а хлор может распарить все свои валентные электроны и образовывать соединения с валентностью =VII (хлорный ангидрид, хлорную кислоту и ее соли). Марганец тоже имеет семивалентные соединения (соответственно марганцовый ангидрид, марганцовую кислоту и ее соли). Правило: № периода говорит о числе электронных слоев в атоме, № группы говорит о числе валентных электронов в атомах , а также максимальной валентности элемента и значении степени окисления (исключения: валентность и СТОК < № группы: фтор, кислород, азот (у него максимальная валентность =IV), железо (max СТОК=+6), кобальт (max СТОК=+3); max СТОК>№ группы: медь (max СТОК=+2), золото (max СТОК=+3). Теперь вот о чем: когда вы будете сравнивать свойства элементов по группе, то сравнивайте только представителей одной и той же подгруппы; а то уж больно велика разница в строении и свойствах элементов разных подгрупп!
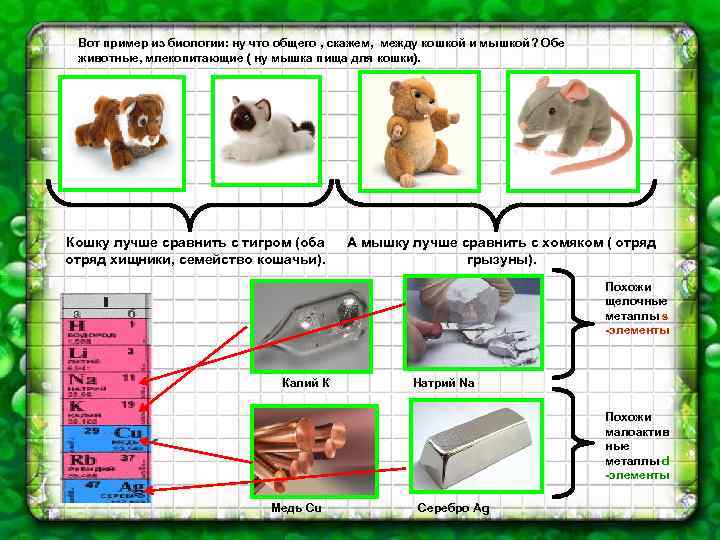
Вот пример из биологии: ну что общего , скажем, между кошкой и мышкой? Обе животные, млекопитающие ( ну мышка пища для кошки). Кошку лучше сравнить с тигром (оба отряд хищники, семейство кошачьи). А мышку лучше сравнить с хомяком ( отряд грызуны). Похожи щелочные металлы s -элементы Калий К Натрий Na Похожи малоактив ные металлы d -элементы Медь Сu Серебро Ag
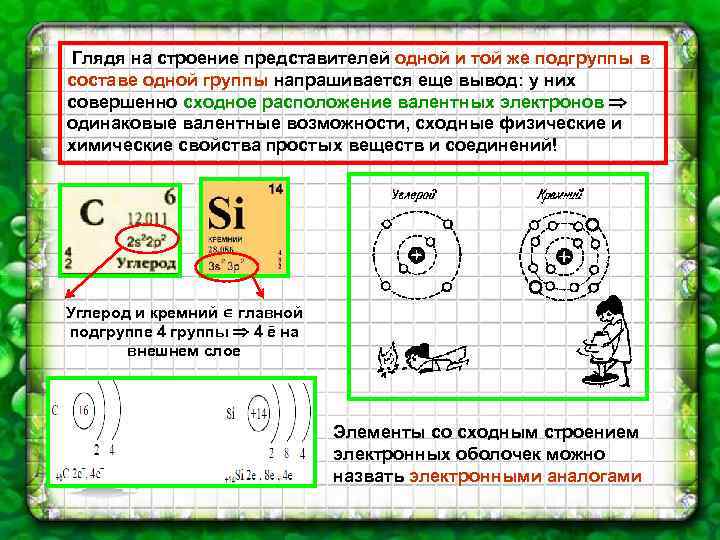
Глядя на строение представителей одной и той же подгруппы в составе одной группы напрашивается еще вывод: у них совершенно сходное расположение валентных электронов одинаковые валентные возможности, сходные физические и химические свойства простых веществ и соединений! Углерод и кремний главной подгруппе 4 группы 4 ē на внешнем слое Элементы со сходным строением электронных оболочек можно назвать электронными аналогами

У элементов одного и того же периода тоже есть сходство в строении атомов : у них одинаковое число электронных слоев и одинаковый набор орбиталей (на модели – квантовых ячеек). Представители II периода

Первичная периодичность – закономерное изменение свойств атомов, простых и сложных веществ по периодам и по подгруппам в составе одной группы. Будем рассматривать следующие изменения у химических элементов: радиус атома (r), электроотрицательность (ЭО), металлические св-ва (способность отдавать внешние ē), восстановительные св-ва (Red св-ва), неметаллические св-ва (способность принимать ē), окислительные св-ва (Ох св-ва). У сложных веществ сравним кислотноосновный характер оксидов и гидроксидов Рассмотрим 3 период как наиболее типичный.

Изменение свойств по периоду Но для начала поглядим на элементы I и II периодов, чтобы сделать выводы о том, как же меняются радиусы атомов. У элементов II периода добавляется новый ē-слой, кажется, что радиусы атомов одного и того же периода должны быть одинаковые. Но на самом деле растет заряд ядра , увеличивается атомная масса, а также растет число ē на внешнем слое. И эти электроны все сильнее и сильнее притягиваются ядром r атома (вплоть до элемента 7 группы). У благородного газа идет стабилизация ē оболочки r несколько.
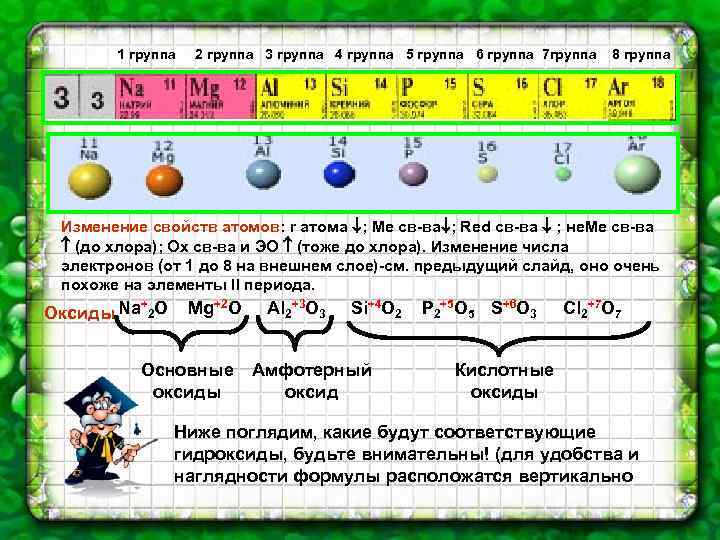
1 группа 2 группа 3 группа 4 группа 5 группа 6 группа 7 группа 8 группа Изменение свойств атомов: r атома ; Ме св-ва ; Red св-ва ; не. Ме св-ва (до хлора); Ох св-ва и ЭО (тоже до хлора). Изменение числа электронов (от 1 до 8 на внешнем слое)-см. предыдущий слайд, оно очень похоже на элементы II периода. + Оксиды Na 2 O Mg+2 O Al 2+3 O 3 Si+4 O 2 Основные Амфотерный оксиды оксид P 2+5 O 5 S+6 O 3 Cl 2+7 O 7 Кислотные оксиды Ниже поглядим, какие будут соответствующие гидроксиды, будьте внимательны! (для удобства и наглядности формулы расположатся вертикально
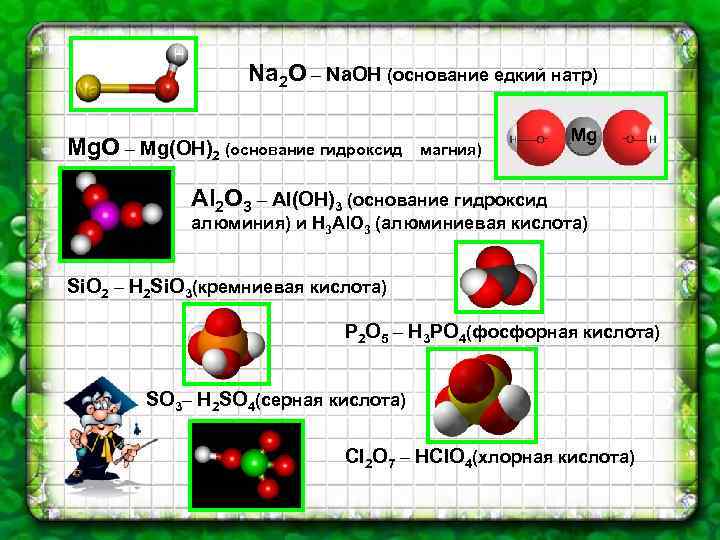
Na 2 O – Na. OH (основание едкий натр) Mg. O – Mg(OH)2 (основание гидроксид магния) Mg Al 2 O 3 – Al(OH)3 (основание гидроксид алюминия) и Н 3 Al. O 3 (алюминиевая кислота) Si. O 2 – H 2 Si. O 3(кремниевая кислота) P 2 O 5 – H 3 PO 4(фосфорная кислота) SO 3– H 2 SO 4(серная кислота) Сl 2 O 7 – HCl. O 4(хлорная кислота)

Вывод: при движении по периоду свойства оксидов и гидроксидов меняются так: основные свойства ослабевают, потом идет(ут) амфотерное(ые) соединение(я), далее возрастают кислотные свойства вплоть до галогена (элемента главной подгруппы 7 группы). Но у тяжелых благородных газов (ксенона и радона), замыкающих 5 и 6 периоды, есть уже сложные соединения, они тоже кислотные, но более слабые, чем соединения галогенов. У элементов больших периодов не такое резкое изменение атомных радиусов, да и вообще свойств атомов и их соединений. У элементов вставных декад строится предвнешний d-подуровень, поэтому радиусы d -элементов почти одинаковые. Более резко меняются свва р-элементов (как и в малых периодах).

Изменения свойств по группам ( в составе главной подгруппы). Рассмотрим для примера главную подгруппу 5 группы (азот, фосфор, мышьяк, сурьму и висмут). Свойства элементов меняются с № так: r , Ме св-ва ; Red св-ва ; не. Ме св -ва ; Ох св-ва ; ЭО. А число валентных ē cоnst. , оно = № группы (здесь =5). Изменение св-в соединений с № : ослабление кислотных св-в и усиление основных.

Азот - бесцветный газ, изолятор; у соединений кислотные св-ва Мышьяк – твердый серый, полупроводник; у соединений кислотные св-ва Фосфор – разные твердые аллотропные модификации, изолятор (но черный «Р» полупроводник); у соединений кислотные св-ва Cурьма – серый металл, проводник; у соединений амфотерные св-ва

Висмут - своеобразный металл с голубоватым отливом, проводник; у соединений амфотерные и основные св-ва Подгруппа азота выбрана не случайно : велико разнообразие ее представителей. Вы убедились, что они разные по внешнему виду простых веществ и свойствам соединений, но у них у всех одинаковое строение внешней электронной оболочки ns 2 np 3.

Вторичная периодичность. Это явление немонотонного изменения свойств атома или его соединений в периоде или в группе. Короче, есть элементы, которые можно назвать «белыми воронами» , у них есть особенности строения. 1 -й пример: рассмотрим изменение такой величины как энергия ионизации во II и III периодах. Энергия ионизации – та энергия, которую надо затратить на то, чтобы оторвать от атома 1 электрон. На рисунке видно, что в периоде Еион. от щелочного металла к инертному газу. Но у элементов главной подгруппы 2 группы (Be и Mg) и эл-тов главной подгруппы 5 группы (N и P) она несколько выше, чем у соседей. Почему?

Ответ следует искать в строении электронных оболочек данных атомов. Дело в том, что если у элемента есть полностью или наполовину заполненные подуровни, то его электронная оболочка обладает меньшей энергией более прочная. У бериллия (и у магния полностью заполнен внешний s-подуровень У азота и фосфора наполовину заполнен внешний рподуровень такие конфигурации прочные, поэтому на отрыв ē надо затратить энергии побольше, чем у соседних атомов.

Вот пример вторичной периодичности у галогенов (гл. Подгр. 7 группы) Самый элекроотрицательный из элементов никогда не бывает анионом; нет возбужденного атома валентность const=I; СТОК=0 или -1 Соединения брома со СТОК=+7 получили довольно поздно, в 1967 году. Br 1 s 22 p 63 s 23 p 63 d 104 s 24 p 5 Исходя из электронного паспорта брома, мы видим, что его валентные ē-ны находятся на орбиталях 4 s и 4 р-подуровней. У Br*** они распариваются на 4 dподуровень. Но чтобы произошло распаривание ē-нов и вступление их в химическую связь, надо этим ē-нам в момент химического взаимодействия «быть дома» ( то есть находиться на своих орбиталях. А это не всегда имеет место и вот почему. ē-ны стремятся из-за своего «-» заряда быть ближе к атомному ядру. Из-за своей вещественно - волновой двойственности они «могут это делать. » У атома брома 3 -й предвнешний ē-слой полностью заполнен. Заполнен 3 d -подуровень. И вот под этот 3 d 10 -экран и проникают стремящиеся быть ближе к ядру валентные ē-ны брома. Чтобы их «вытащить» из-под 3 d 10 экрана и «вернуть» на орбитали, применяют жесткие условия протекания реакции (нагрев, давление, активные реагенты, селективные катализаторы). Особенно тяжело «возвращается на орбитали» 4 s-пара валентных ē-нов отсюда и затруднительно было получить соединения Br+7. Здесь на примере брома был образно описан эффект проникновения валентных ē-нов атома под предвнешний d 10 -экран.

Дмитрий Иванович не только открыл фундаментальный закон, но и создал его подтверждение – Периодическую систему элементов. И благодаря этой системе можно было с очень большой долей вероятности описать свойства не только уже известных атомов и веществ, но и еще не найденных Вот первоначальная ПС на доме, где жил и работал ученый в Петербурге у метро «Технологический институт» . Как вы думаете, сильно ли она отличается от нынешней?
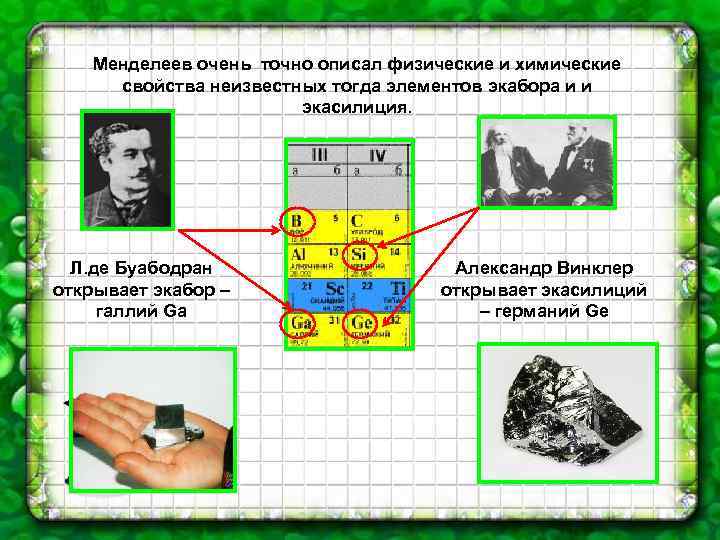
Менделеев очень точно описал физические и химические свойства неизвестных тогда элементов экабора и и экасилиция. Л. де Буабодран открывает экабор – галлий Ga Александр Винклер открывает экасилиций – германий Ge

В 1976 году команда американских физиков-ядерщиков во главе с Гленом Сиборгом синтезировала 101 элемент. Решено было назвать его в честь Менделеева. Это был разгар «холодной войны» между СССР и США, поэтому желание назвать элемент в честь русского было довольно смелым поступком. Советские ученые не остались в долгу и назвали открытый ими в Дубне 106 элемент сиборгием.

Периодический закон.ppt