06_Радикалы - ведение [Автосохраненный].pptx
- Количество слайдов: 27

Свободные радикалы и болезни Ю. А. Владимиров Медико-биологический факультет РГМУ Факультет Фундаментальной Медицины МГУ

Свободные радикалы и старение организма Ранние публикации Hаrman D. (1955): Aging: a theory based on free radical and radiation chemistry. Univ. Cal. Rad. Lab. Rep. , No 3078, July 14. Harman D. (1956): Aging: a theory based on free radical and radiation chemistry. J. Gerontol. 11: 298 - 300. Harman D. (1957): Atherosclerosis: Hypothesis concerning the initiating steps in pathogenesis. J. Gerontol. 12: 199 - 202.

Доказательства участия свободных радикалов в процессе старения: • Данные о происхождении и эволюции жизни. • Результаты изучения действия радиации на организмы. • Опыты по увеличению продолжительности жизни при кормлении диетой, содержащей антиоксиданты. • Возможность объяснить основные проявления старения организма с позиций свободно-радикальной теории. • Возрастание числа публикаций о роли радиклов в патогенезе многих заболеваний. • D. Harman. Free radicals in aging. Mol. Cell Biochem. 84 (2): 155 -161, 1988.

Сборник обзоров о роли свободных радикалов в развитии болезней человека • Volume 8 • Modern Aging Research Free Radicals, Aging, and Degenerative Diseases • Editors: John E. Johnson Jr. Roy Walford Denham Harman Jame Miquel Allan R. Liss, Inc. , New York Темы обзоров • Свободно-радикальная теория старения • Процессы с участием свободных радикалов • Свободные радикалы, рак и старение • Свободные радикалы и болезнь Баттона • Радикалы и повреждение ДНК при аутоиммунных заболеваниях • Антиоксиданты и иммунный ответ • Роль ловушек свободных радикалов в радиационной защите ДНК • и другие (1986 год, 588 стр. )
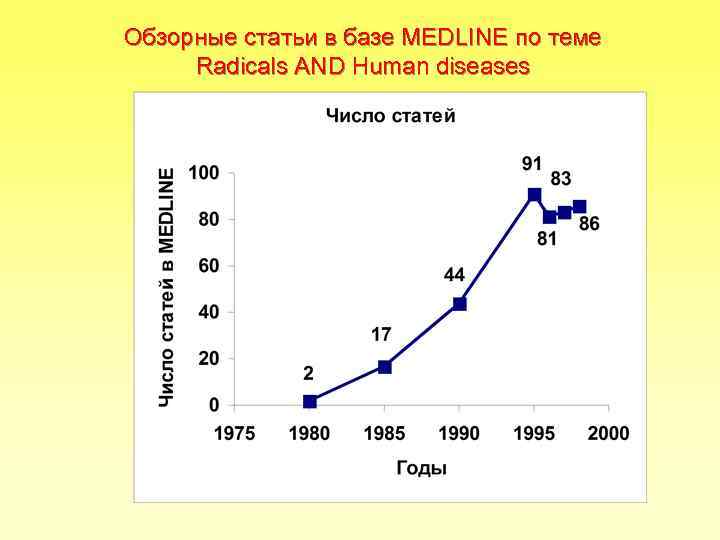
Обзорные статьи в базе MEDLINE по темe Radicals AND Human diseases

Обзорные статьи в базе MEDLINE по темe Radicals AND *** за 1996 -1999 гг ***
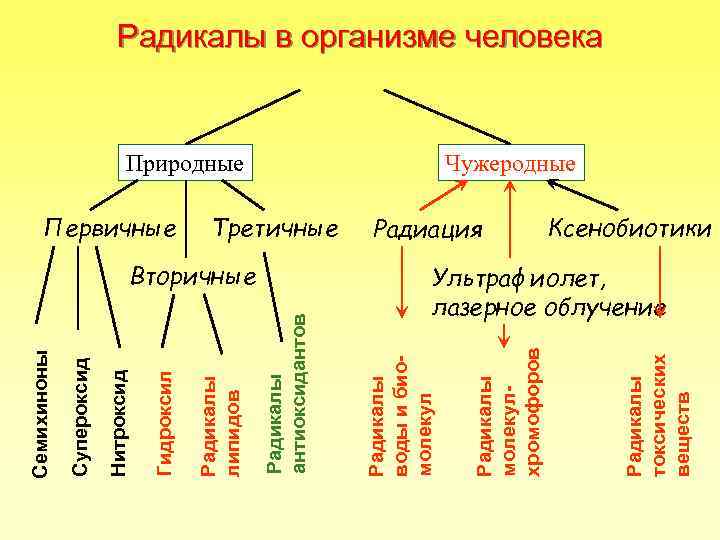
Вторичные Радиация Радикалы токсических веществ Природные Радикалы молекулхромофоров Третичные Радикалы воды и биомолекул Радикалы антиоксидантов Первичные Радикалы липидов Гидроксил Нитроксид Супероксид Семихиноны Радикалы в организме человека Чужеродные Ксенобиотики Ультрафиолет, лазерное облучение

Radicals and reactive molecular species Vladimirov, Y. A. , Free radicals in cell life: two sides of the same coin, in Oxidative Stress at molecular, Cellular and Organ Levels, P. Johnson and A. A. Boldyrev, Editors. 2002, Research Signpost: Fort P. O. Trivandrum. p. 13 -43. dases roxi NEW dical – Ra ide pe s ins
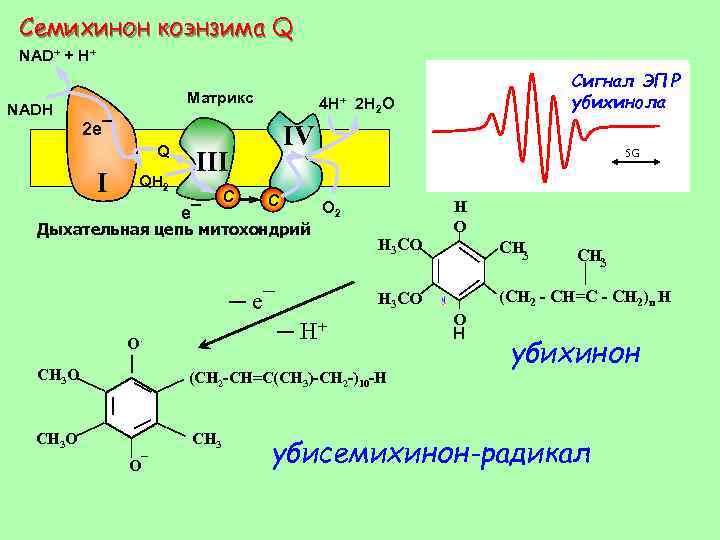
Семихинон коэнзима Q NAD+ + H+ Матрикс NADH 2 e¯ Q I QH 2 4 H+ 2 H 2 O IV II III e¯ C C 5 G O 2 Дыхательная цепь митохондрий ─ e¯ H 3 CO ─ H+ O· CH 3 O (CH 2 -CH=C(CH 3)-CH 2 -)10 -H CH 3 O CH 3 O¯ Сигнал ЭПР убихинола H O CH 3 (CH 2 - CH=C - CH 2)n H O H убихинон убисемихинон-радикал
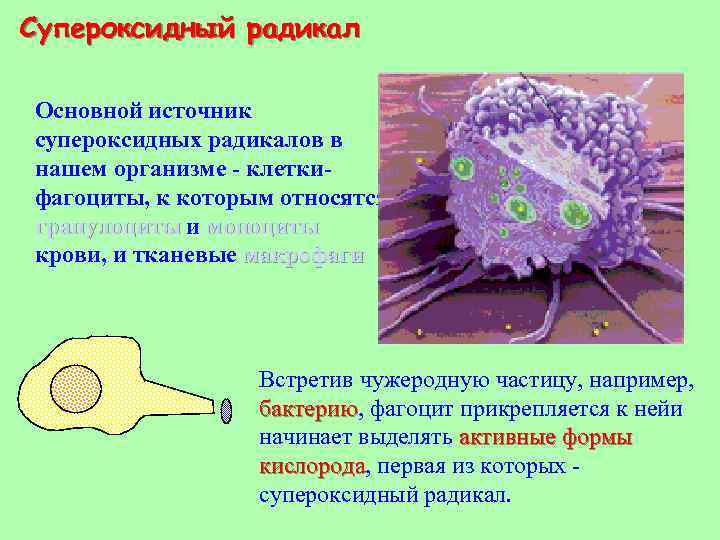
Супероксидный радикал Основной источник супероксидных радикалов в нашем организме - клеткифагоциты, к которым относятся гранулоциты и моноциты крови, и тканевые макрофаги Встретив чужеродную частицу, например, бактерию, фагоцит прикрепляется к нейи бактерию начинает выделять активные формы кислорода, первая из которых кислорода супероксидный радикал.

Рис. 5. Активации фагоцита внешним сти мулом: а—схематическое изображение клетки фагоцита; 1 — захват клеткой чужеродной частицы (фагоцитоз); 2 — активация клетки химическим веществом, напри мер хемоатрактантом; б—участок клеточной мем браны; НАДФН, образующийся при пентозофосфатном пути окисления глюкозы (гексозомонофосфатньй шунт), окисляется ферментным комплексом цитоплазматической мембраны с образованием супероксидных радикалов, в присутствии акцептора люминола наблюдается интенсивная хемилюминесценция
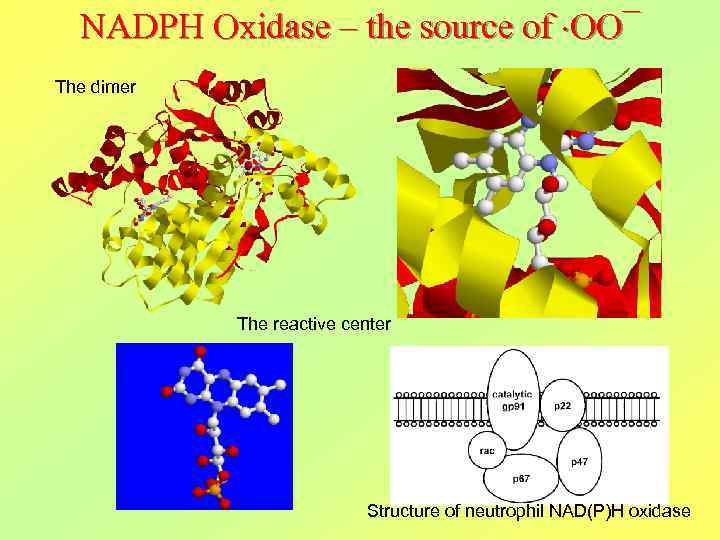
NADPH Oxidase – the source of OO¯ The dimer The reactive center Structure of neutrophil NAD(P)H oxidase
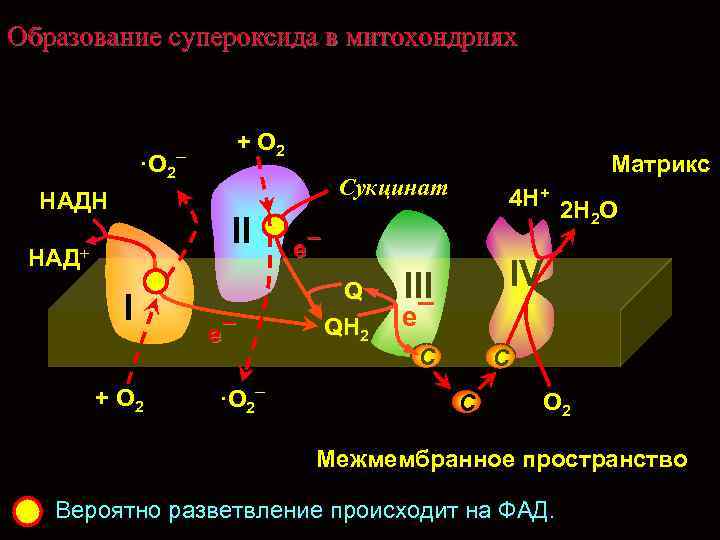
Образование супероксида в митохондриях + O 2 ·O 2¯ НАДН Сукцинат II НАД+ I + O 2 Матрикс e¯ ·O 2¯ 4 H+ 2 H O 2 e¯ Q QH 2 IV III e¯ C C C O 2 Межмембранное пространство Вероятно разветвление происходит на ФАД.
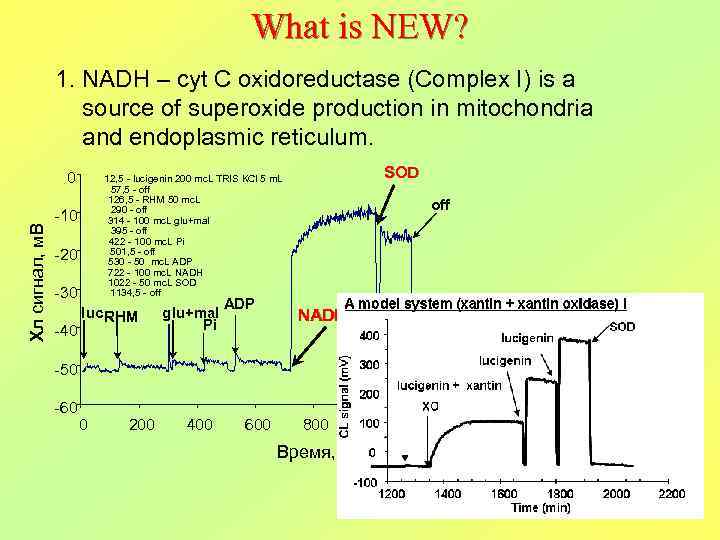
What is NEW? 1. NADH – cyt C oxidoreductase (Complex I) is a source of superoxide production in mitochondria and endoplasmic reticulum. Хл сигнал, м. В 0 10 20 30 40 SOD 12, 5 lucigenin 200 mc. L TRIS KCl 5 m. L 57, 5 off 126, 5 RHM 50 mc. L 290 off 314 100 mc. L glu+mal 395 off 422 100 mc. L Pi 501, 5 off 530 50 mc. L ADP 722 100 mc. L NADH 1022 50 mc. L SOD 1134, 5 off luc RHM glu+mal Pi ADP off NADH 50 60 0 200 400 600 800 Время, с 1000 1200 1400
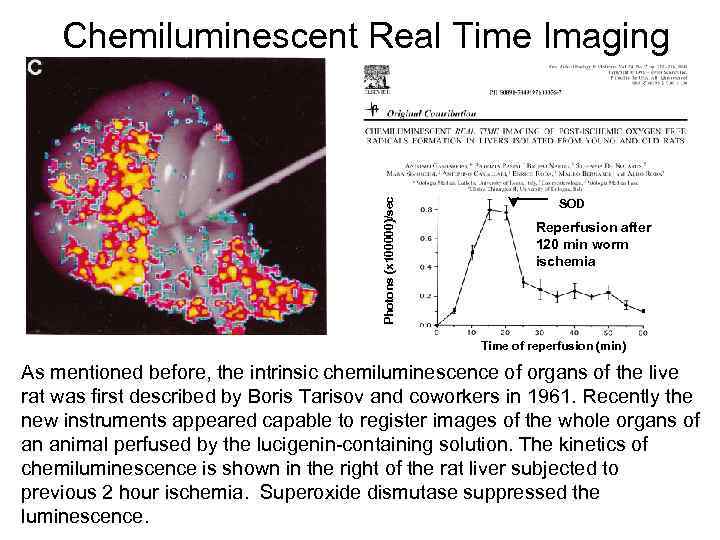
Photons (x 100000)/sec Chemiluminescent Real Time Imaging SOD Reperfusion after 120 min worm ischemia Time of reperfusion (min) As mentioned before, the intrinsic chemiluminescence of organs of the live rat was first described by Boris Tarisov and coworkers in 1961. Recently the new instruments appeared capable to register images of the whole organs of an animal perfused by the lucigenin containing solution. The kinetics of chemiluminescence is shown in the right of the rat liver subjected to previous 2 hour ischemia. Superoxide dismutase suppressed the luminescence.

Приборы и материалы Хемилюминометр, оснащенный перистальтическим насосом, который обеспечивает постоянную и контролируемую аэрацию Хемилюминометр Smart. Lum 5773 Перистальтический насос Аэрация образца (2, 5 об/мин) Система 1. Физраствор или раствор Хенкса (р. Н 7, 4) 2. Люцигенин (60 мк. М) 3. Исследуемый образец ткани печени крысы
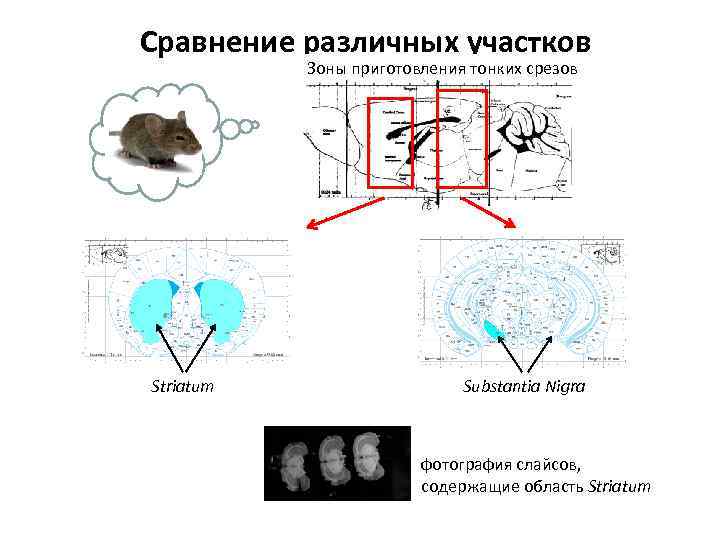
Сравнение различных участков Зоны приготовления тонких срезов мозга Striatum Substantia Nigra фотография слайсов, содержащие область Striatum
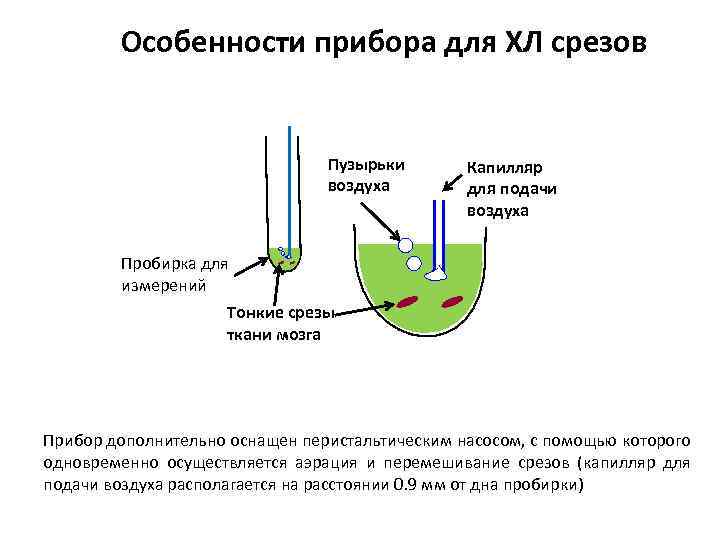
Особенности прибора для ХЛ срезов Пузырьки воздуха Капилляр для подачи воздуха Пробирка для измерений Тонкие срезы ткани мозга Прибор дополнительно оснащен перистальтическим насосом, с помощью которого одновременно осуществляется аэрация и перемешивание срезов (капилляр для подачи воздуха располагается на расстоянии 0. 9 мм от дна пробирки)
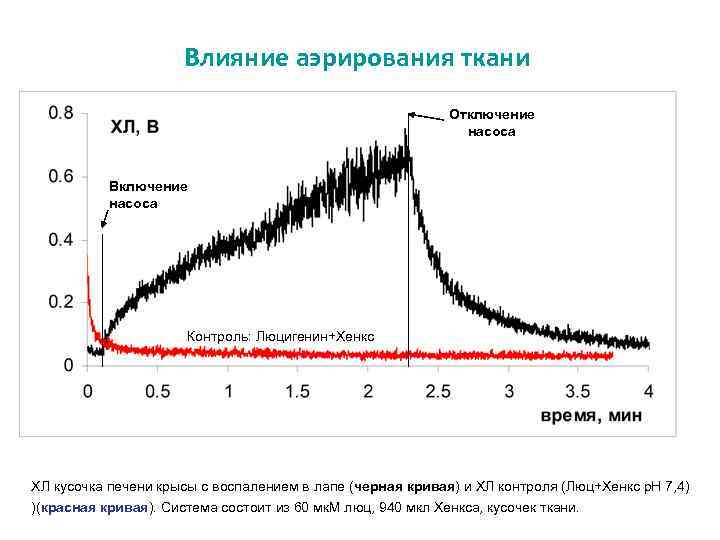
Влияние аэрирования ткани Отключение насоса Включение насоса Контроль: Люцигенин+Хенкс ХЛ кусочка печени крысы с воспалением в лапе (черная кривая) и ХЛ контроля (Люц+Хенкс р. Н 7, 4) )(красная кривая). Система состоит из 60 мк. М люц, 940 мкл Хенкса, кусочек ткани.

Лекции Физико химические основы патологии клетки Активные формы кислорода Ю. А Владимиров Москва 2002

Что относят к активным формам кислорода? 1. 1 O 2 Синглетный кислород 2. ▪O 2─ Супероксидный радикал 3. H 2 O 2 Пероксид водорода 4. ▪OH Гидроксильный радикал 5. Cl. O─ Гипохлорит (активная форма хлора) 6. ONOO─ Пероксинитрит (активная форма азота) 7. Радикалы липидов (активная форма липидов) 1. L▪ Алкил 2. LO▪ Алкоксил 3. LOO ▪ Диоксил (пероксил)
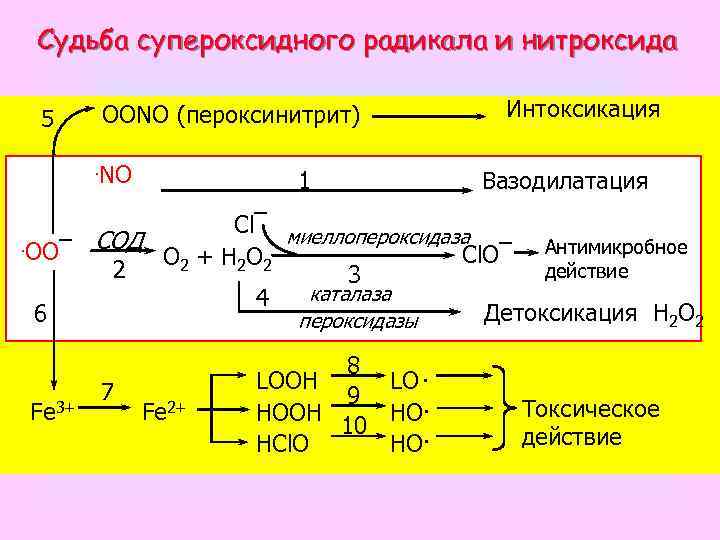
Судьба супероксидного радикала и нитроксида 5 OONO (пероксинитрит). NO 1 Интоксикация Вазодилатация Cl¯ миеллопероксидаза. OO¯ СОД Cl. O¯ Антимикробное O 2 + H 2 O 2 действие 2 3 каталаза 4 Детоксикация H 2 O 2 6 пероксидазы Fe 3+ 7 Fe 2+ 8 LOOH LO. 9 HOOH HO. 10 HCl. O HO. Токсическое действие

Метаболизм супероксидного радикала и пероксида водорода в водной среде NADPH – оксидаза: O 2 + e¯ ·O 2¯ (супероксид) Супероксиддисмутаза (СОД): ·O 2¯ + 2 H+ O 2 + H 2 O 2 (пероксид водорода) Глутатионпероксидаза: 2 H 2 O 2 + 2 GSH 2 H 2 O + O 2 + GSSG Каталаза: 2 H 2 O 2 2 H 2 O + O 2 Миелопероксидаза: H 2 O 2 + Cl¯ H 2 O + Cl. O¯ (гипохлорит) Cl. O Реакция Фентона: H 2 O 2 + Fe 2+ Fe 3+ + HO¯ + ·OH (гидроксил-радикал) HO Реакция Осипова: H 2 O 2 + Fe 2+ Fe 3+ + HO¯ + ·OH HO
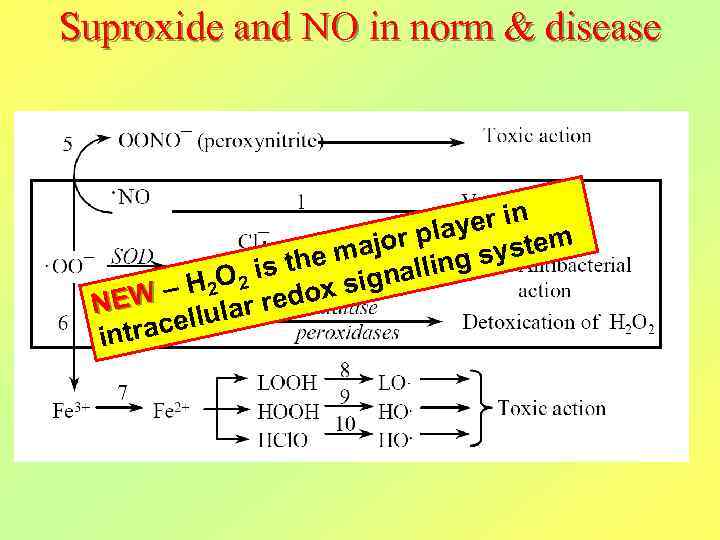
Suproxide and NO in norm & disease yer in or pla system e maj lling is th H 2 O 2 dox signa EW – N lar re u racell int
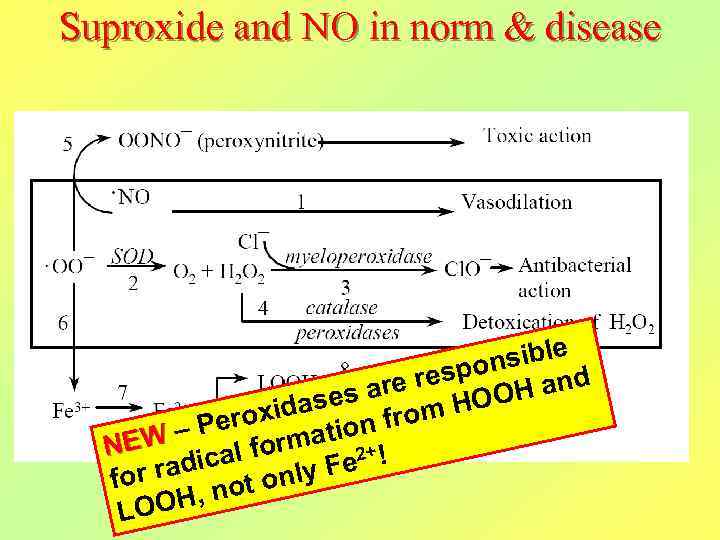
Suproxide and NO in norm & disease nsible espo and are r ases rom HOOH d eroxi ation f W – P l form NE 2+ ! ica e or rad ot only F f OH, n LO
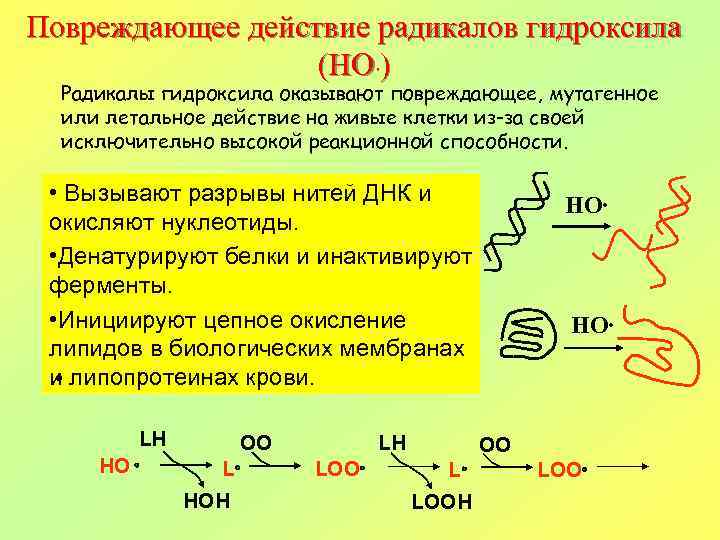
Повреждающее действие радикалов гидроксила (HO. ) Радикалы гидроксила оказывают повреждающее, мутагенное или летальное действие на живые клетки из-за своей исключительно высокой реакционной способности. • Вызывают разрывы нитей ДНК и окисляют нуклеотиды. • Денатурируют белки и инактивируют ферменты. • Инициируют цепное окисление липидов в биологических мембранах и липопротеинах крови. • LH HO OO L HOH LH LOO HO. OO L LOOH LOO

Вопросы к зачету 1. Что такое активные формы кислорода? 2. Образование супероксидного радикала клетками- фагоцитами. 3. Место и условия образования супероксидного радикала в дыхательной цепи митохондрий. 4. Основные реакции метаболизма супероксида в норме. 5. Основные реакции метаболизма супероксида в патологии. Роль ионов железа. 6. Мишени повреждающего действия гидроксил-радикала.
06_Радикалы - ведение [Автосохраненный].pptx