08 Биоэнергетика.ppt
- Количество слайдов: 20
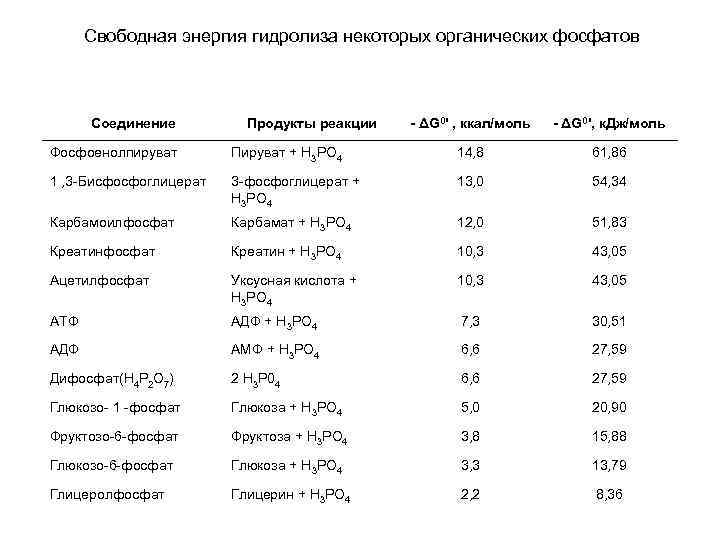
Свободная энергия гидролиза некоторых органических фосфатов Соединение Продукты реакции - ΔG 0' , ккал/моль - ΔG 0', к. Дж/моль Фосфоенолпируват Пируват + Н 3 РО 4 14, 8 61, 86 1 , 3 -Бисфосфоглицерат 3 -фосфоглицерат + Н 3 РО 4 13, 0 54, 34 Карбамоилфосфат Карбамат + Н 3 РО 4 12, 0 51, 83 Креатинфосфат Креатин + Н 3 РО 4 10, 3 43, 05 Ацетилфосфат Уксусная кислота + Н 3 РО 4 10, 3 43, 05 АТФ АДФ + Н 3 РО 4 7, 3 30, 51 АДФ АМФ + Н 3 РО 4 6, 6 27, 59 Дифосфат(Н 4 Р 2 О 7) 2 Н 3 Р 04 6, 6 27, 59 Глюкозо- 1 -фосфат Глюкоза + Н 3 РО 4 5, 0 20, 90 Фруктозо-6 -фосфат Фруктоза + Н 3 РО 4 3, 8 15, 88 Глюкозо-6 -фосфат Глюкоза + Н 3 РО 4 3, 3 13, 79 Глицеролфосфат Глицерин + Н 3 РО 4 2, 2 8, 36
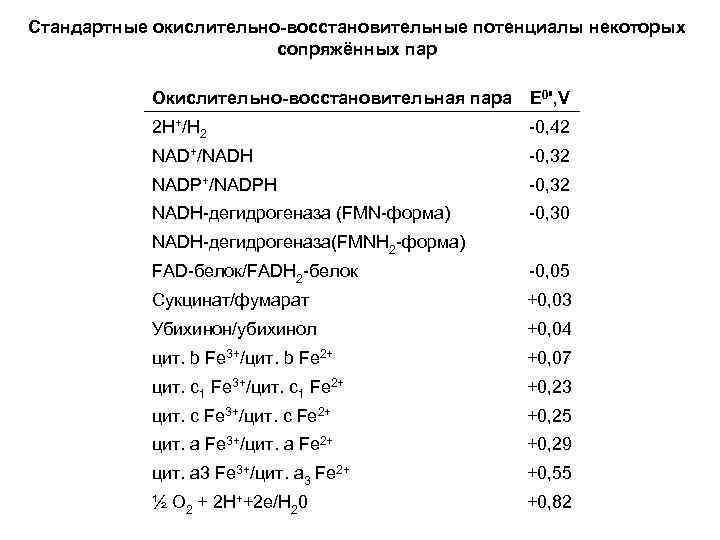
Стандартные окислительно-восстановительные потенциалы некоторых сопряжённых пар Окислительно-восстановительная пара E 0', V 2 Н+/Н 2 -0, 42 NAD+/NADH -0, 32 NADP+/NADPH -0, 32 NADH-дегидрогеназа (FMN-форма) -0, 30 NАDН-дегидрогеназа(FМNН 2 -форма) FАD-белок/FАDН 2 -белок -0, 05 Сукцинат/фумарат +0, 03 Убихинон/убихинол +0, 04 цит. b Fе 3+/цит. b Fe 2+ +0, 07 цит. c 1 Fе 3+/цит. c 1 Fe 2+ +0, 23 цит. с Fе 3+/цит. с Fе 2+ +0, 25 цит. а Fе 3+/цит. а Fе 2+ +0, 29 цит. a 3 Fе 3+/цит. а 3 Fе 2+ +0, 55 ½ O 2 + 2 Н++2 е/Н 20 +0, 82
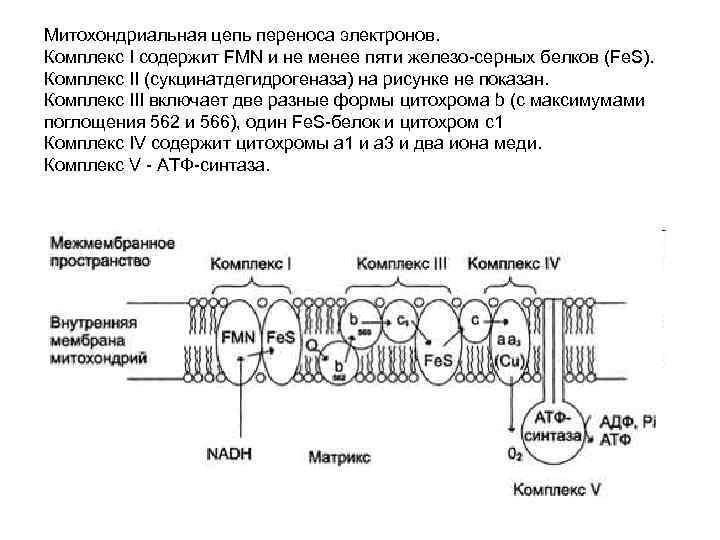
Митохондриальная цепь переноса электронов. Комплекс I содержит FMN и не менее пяти железо-серных белков (Fe. S). Комплекс II (сукцинатдегидрогеназа) на рисунке не показан. Комплекс III включает две разные формы цитохрома b (с максимумами поглощения 562 и 566), один Fe. S-белок и цитохром с1 Комплекс IV содержит цитохромы a 1 и а 3 и два иона меди. Комплекс V - АТФ-синтаза.
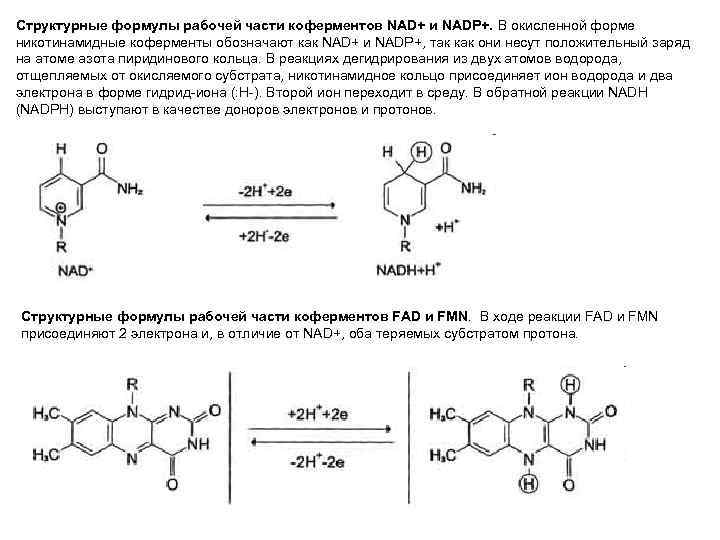
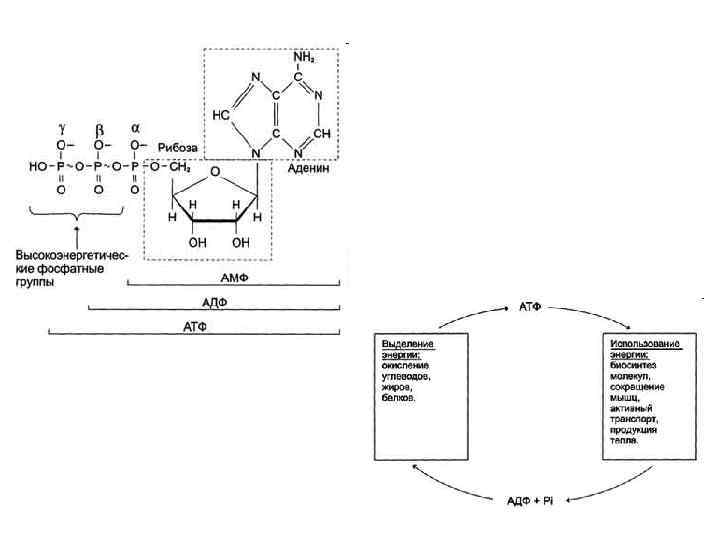
Структурные формулы рабочей части коферментов NAD+ и NADP+. В окисленной форме никотинамидные коферменты обозначают как NAD+ и NADP+, так как они несут положительный заряд на атоме азота пиридинового кольца. В реакциях дегидрирования из двух атомов водорода, отщепляемых от окисляемого субстрата, никотинамидное кольцо присоединяет ион водорода и два электрона в форме гидрид-иона (: Н-). Второй ион переходит в среду. В обратной реакции NADH (NADPH) выступают в качестве доноров электронов и протонов. Структурные формулы рабочей части коферментов FAD и FMN. В ходе реакции FAD и FMN присоединяют 2 электрона и, в отличие от NAD+, оба теряемых субстратом протона.
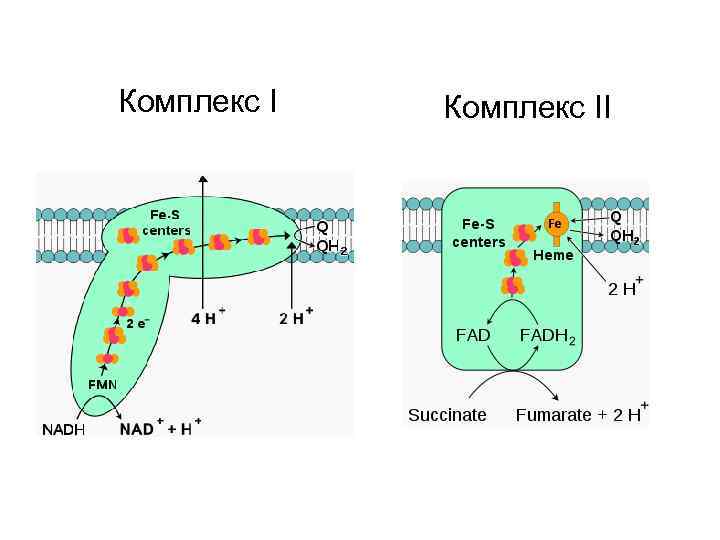
Комплекс II
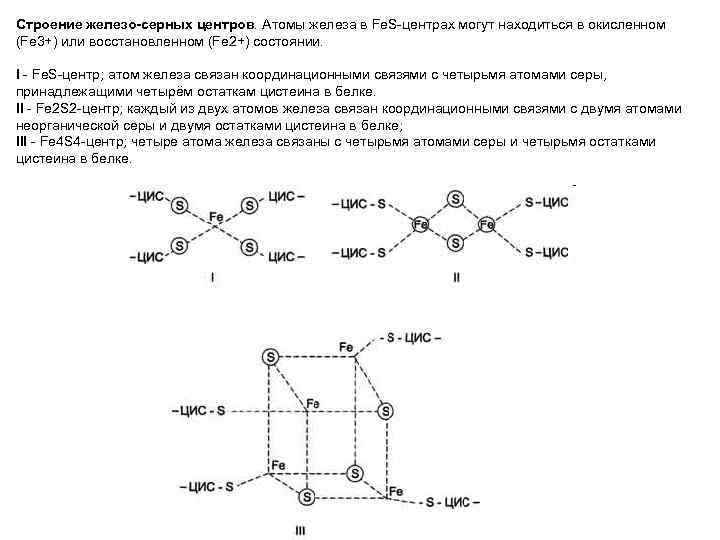
Строение железо-серных центров. Атомы железа в Fe. S-центрах могут находиться в окисленном (Fe 3+) или восстановленном (Fe 2+) состоянии. I - Fe. S-центр; атом железа связан координационными связями с четырьмя атомами серы, принадлежащими четырём остаткам цистеина в белке. II - Fе 2 S 2 -центр; каждый из двух атомов железа связан координационными связями с двумя атомами неорганической серы и двумя остатками цистеина в белке; III - Fe 4 S 4 -центр; четыре атома железа связаны с четырьмя атомами серы и четырьмя остатками цистеина в белке.
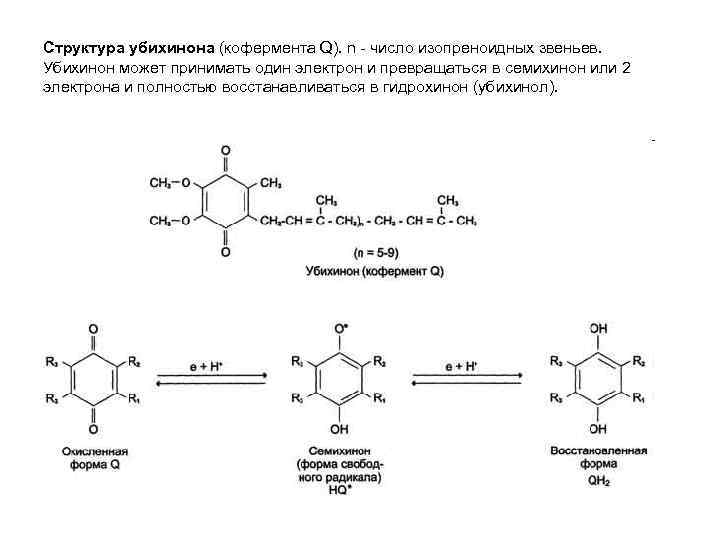
Структура убихинона (кофермента Q). n - число изопреноидных звеньев. Убихинон может принимать один электрон и превращаться в семихинон или 2 электрона и полностью восстанавливаться в гидрохинон (убихинол).
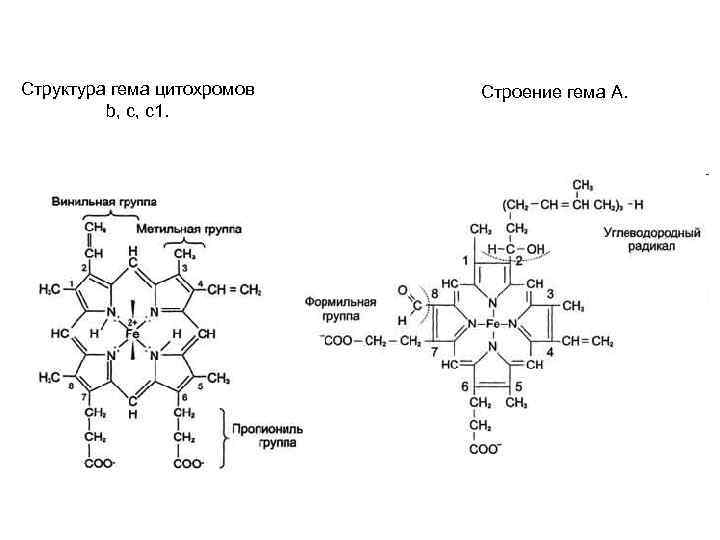
Структура гема цитохромов b, с, с1. Строение гема А.
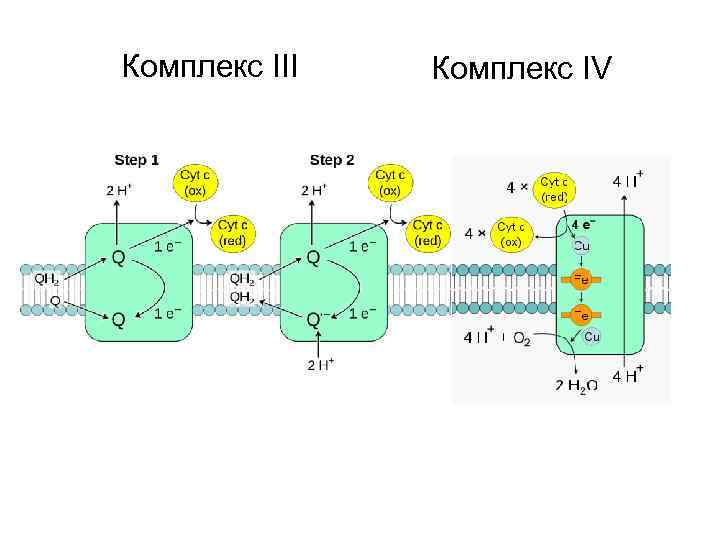
Комплекс III Комплекс IV

Компоненты митохондриальной цепи переноса электронов Название компонента Простетическая группа Донор e Акцептор е NADH-дегидрогеназа, комплекс I FMN, Fe. S NADH Ko. Q Коэнзим Q, убихинон NADH Комплекс III (bc 1) р. Н 2 -дегидрогеназа, комплекс III Fe. S, гем b 1 (562), гемb 2(566), гемм с1 QH 2 Цитохром с Гем с Комплекс III Комплекс IV Цитохромоксидаза, комплекс IV Гем А Сu 2+ Цитохром с O 2 Сукцинатдегидрогеназа, комплекс II FAD, Fe. S Сукцинат Ko. Q
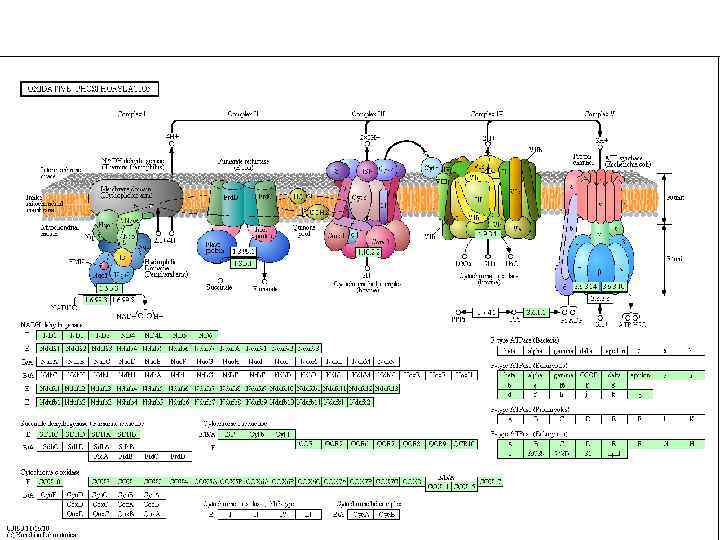
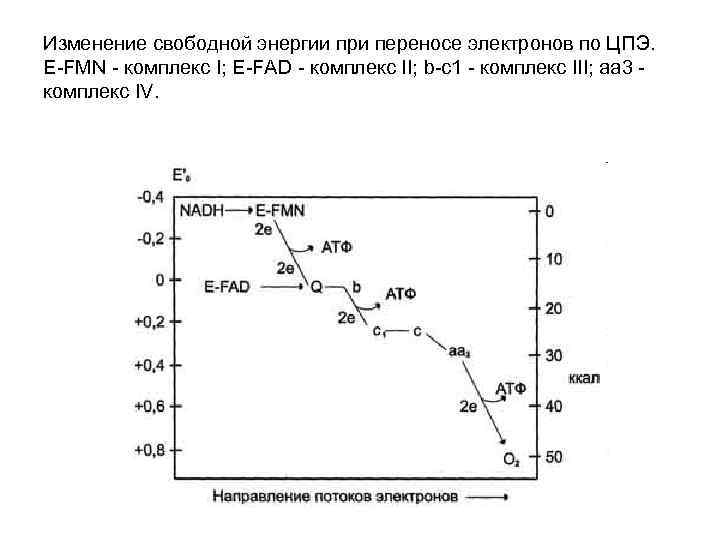
Изменение свободной энергии при переносе электронов по ЦПЭ. E-FMN - комплекс I; E-FAD - комплекс II; b-с1 - комплекс III; aa 3 - комплекс IV.
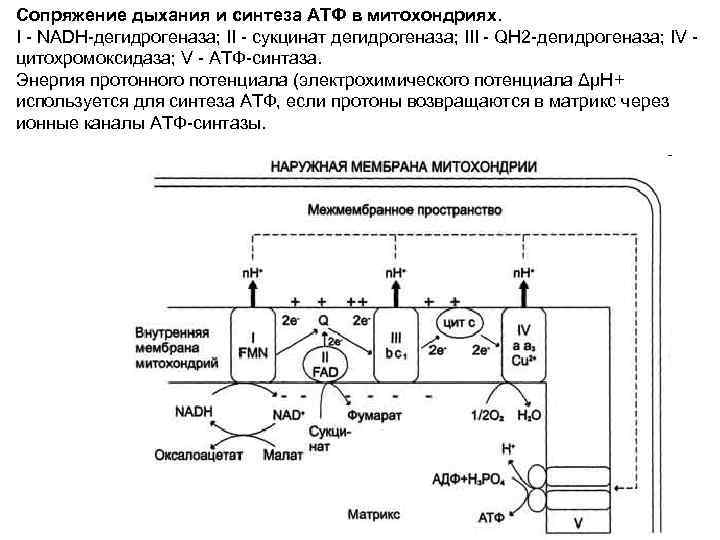
Сопряжение дыхания и синтеза АТФ в митохондриях. I - NADH-дегидрогеназа; II - сукцинат дегидрогеназа; III - QН 2 -дегидрогеназа; IV - цитохромоксидаза; V - АТФ-синтаза. Энергия протонного потенциала (электрохимического потенциала ΔμН+ используется для синтеза АТФ, если протоны возвращаются в матрикс через ионные каналы АТФ-синтазы.
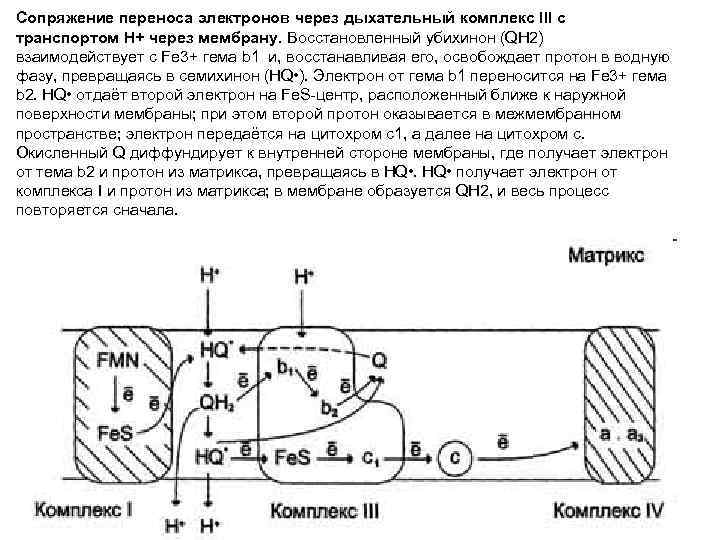
Сопряжение переноса электронов через дыхательный комплекс III с транспортом Н+ через мембрану. Восстановленный убихинон (QH 2) взаимодействует с Fе 3+ гема b 1 и, восстанавливая его, освобождает протон в водную фазу, превращаясь в семихинон (НQ • ). Электрон от гема b 1 переносится на Fe 3+ гема b 2. HQ • отдаёт второй электрон на Fe. S-центр, расположенный ближе к наружной поверхности мембраны; при этом второй протон оказывается в межмембранном пространстве; электрон передаётся на цитохром с1, а далее на цитохром с. Окисленный Q диффундирует к внутренней стороне мембраны, где получает электрон от тема b 2 и протон из матрикса, превращаясь в НQ • получает электрон от комплекса I и протон из матрикса; в мембране образуется QН 2, и весь процесс повторяется сначала.
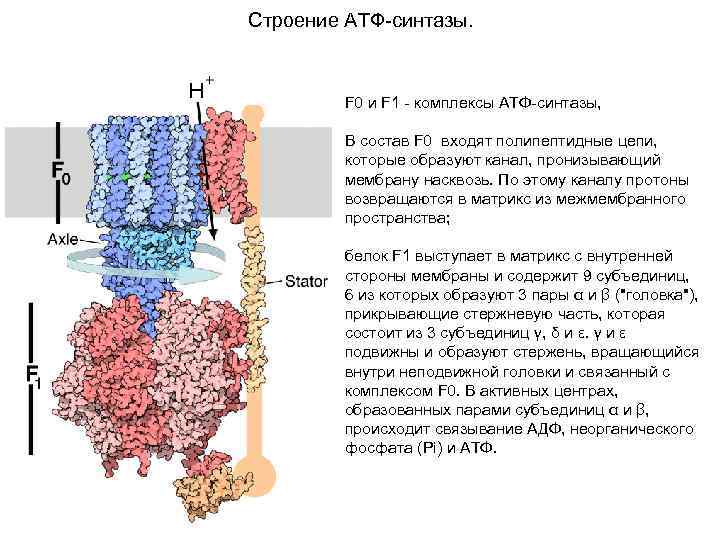
Строение АТФ-синтазы. F 0 и F 1 - комплексы АТФ-синтазы, В состав F 0 входят полипептидные цепи, которые образуют канал, пронизывающий мембрану насквозь. По этому каналу протоны возвращаются в матрикс из межмембранного пространства; белок F 1 выступает в матрикс с внутренней стороны мембраны и содержит 9 субъединиц, 6 из которых образуют 3 пары α и β ("головка"), прикрывающие стержневую часть, которая состоит из 3 субъединиц γ, δ и ε. γ и ε подвижны и образуют стержень, вращающийся внутри неподвижной головки и связанный с комплексом F 0. В активных центрах, образованных парами субъединиц α и β, происходит связывание АДФ, неорганического фосфата (Рi) и АТФ.
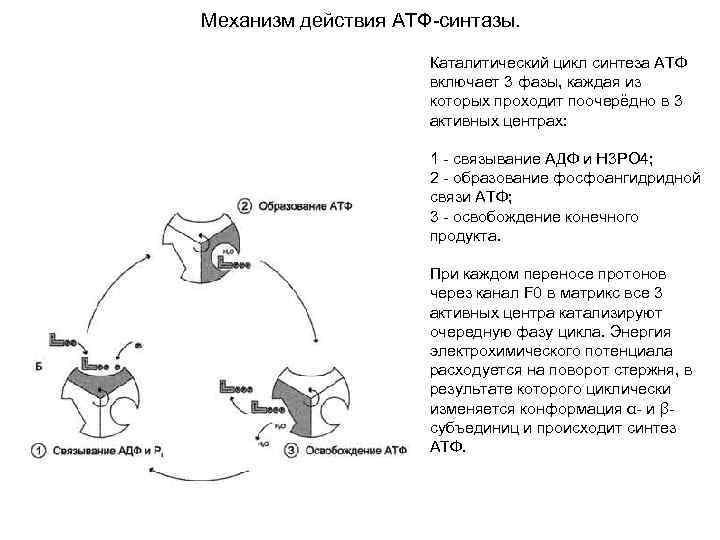
Механизм действия АТФ-синтазы. Каталитический цикл синтеза АТФ включает 3 фазы, каждая из которых проходит поочерёдно в 3 активных центрах: 1 - связывание АДФ и Н 3 РО 4; 2 - образование фосфоангидридной связи АТФ; 3 - освобождение конечного продукта. При каждом переносе протонов через канал F 0 в матрикс все 3 активных центра катализируют очередную фазу цикла. Энергия электрохимического потенциала расходуется на поворот стержня, в результате которого циклически изменяется конформация α- и βсубъединиц и происходит синтез АТФ.
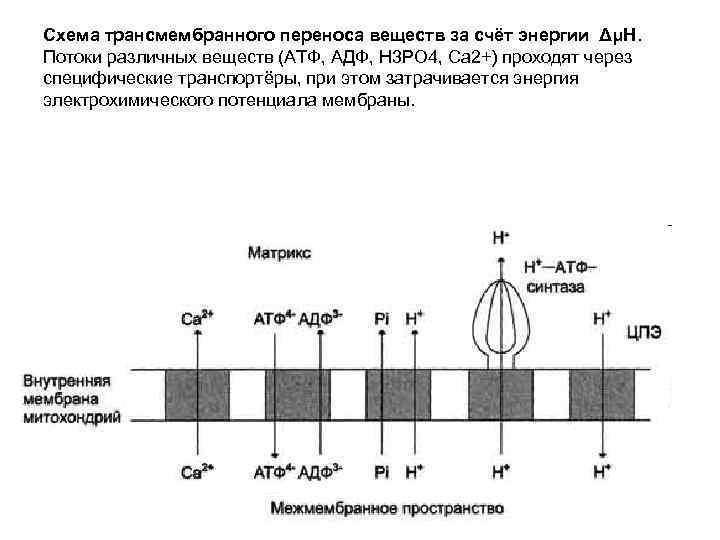
Схема трансмембранного переноса веществ за счёт энергии ΔμН. Потоки различных веществ (АТФ, АДФ, Н 3 РО 4, Са 2+) проходят через специфические транспортёры, при этом затрачивается энергия электрохимического потенциала мембраны.
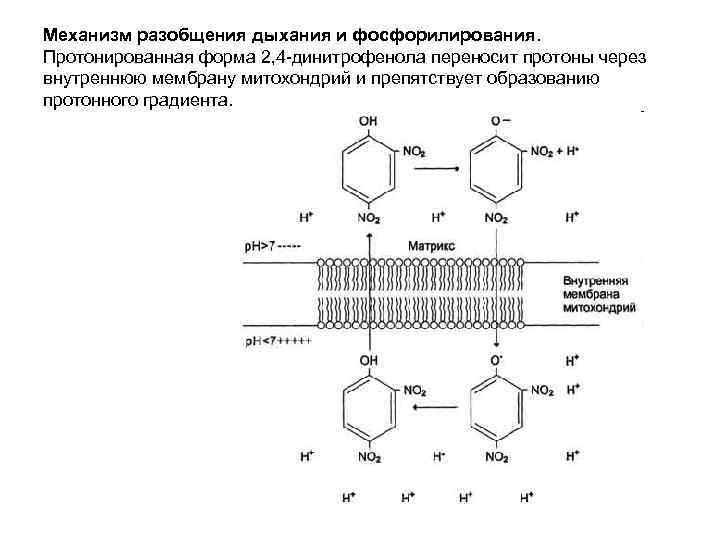
Механизм разобщения дыхания и фосфорилирования. Протонированная форма 2, 4 -динитрофенола переносит протоны через внутреннюю мембрану митохондрий и препятствует образованию протонного градиента.
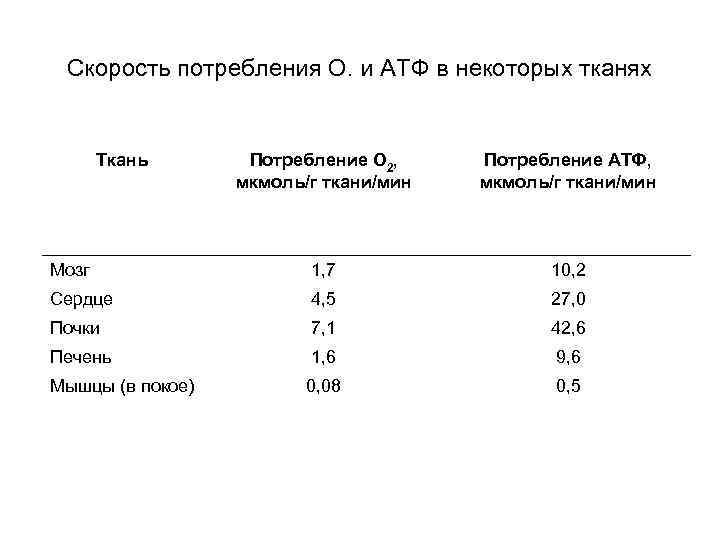
Скорость потребления О. и АТФ в некоторых тканях Ткань Потребление О 2, мкмоль/г ткани/мин Потребление АТФ, мкмоль/г ткани/мин Мозг 1, 7 10, 2 Сердце 4, 5 27, 0 Почки 7, 1 42, 6 Печень 1, 6 9, 6 Мышцы (в покое) 0, 08 0, 5
08 Биоэнергетика.ppt